Перед Вами номер Российского кардиологического журнала, который посвящен вопросам диагностики и ведения пациентов с атеросклерозом и нарушениями липидного обмена.
ОРИГИНАЛЬНЫЕ СТАТЬИ
Цель. Изучить распространенность инфаркта миокарда (ИМ) в популяции российских регионов и вклад в сердечно-сосудистые события.
Материал и методы. Материалом для анализа были представительные выборки из населения в возрасте 35-64 лет из 11 регионов Российской Федерации, обследованные в рамках многоцентрового исследования “Эпидемиология сердечно-сосудистых заболеваний и их факторов риска в различных регионах Российской Федерации”. Отклик составил ~80%. В исследовании использовалась систематическая стратифицированная многоступенчатая случайная выборка, сформированная по территориальному принципу на базе лечебно-профилактических учреждений. При проведении исследования информацию о наличии перенесенного ИМ получали опросным методом по стандартному вопроснику, выполнялась антропометрия и измерение артериального давления (АД) и частоты сердечных сокращений (ЧСС) автоматическим тонометром, регистрировалась электрокардиограмма (ЭКГ) в покое с последующим кодированием Миннесотским кодом. В качестве ЭКГ изменений ишемического типа считались мажорные и минорные зубцы QQS и сегменты STT. Биохимические параметры определялись на автоанализаторе Arkhitect 000. Медиана проспективного наблюдения составила 6,21 [5,25; 6,75] лет. Анализировалась комбинированная сердечно-сосудистая конечная точка (ККТ), включающая смерть от сердечно-сосудистых заболеваний и нефатальный ИМ. За период наблюдения выявлено 363 случая смерти от всех причин, из них 134 — от сердечно-сосудистых заболеваний; 196 случаев ККТ. Статистический анализ проведен в среде R 3.6.1.
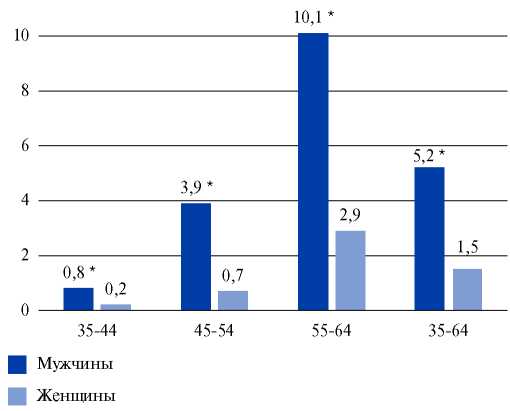
Результаты. Распространенность ИМ среди населения российских регионов составила 2,9%; 5,2% среди мужчин и 1,5% среди женщин, увеличиваясь с возрастом. Мужчины с ИМ в анамнезе чаще принимали статины и бета-блокаторы, чем женщины: 39,0% vs 25,6% и 29,3% vs 27,1%, соответственно. Наличие ИМ, впервые выявленного в период наблюдения, ассоциировалось с основными факторами риска (ФР): курением, повышенными АД, ЧСС, триглицеридами и глюкозой. Для лиц с ИМ в анамнезе статистически значимая связь была выявлена только с курением. Множественное сравнение вклада ФР, ЭКГ изменений и ИМ в анамнезе показало, что включение в анализ ишемических изменений ЭКГ достоверно повышает риск сердечно-сосудистых событий у лиц без ИМ в анамнезе по сравнению с лицами без ИМ и без изменений ЭКГ. Высокий риск возникновения ККТ отмечен у лиц с ИМ в анамнезе: относительный риск (RR) — 4,73 (доверительный интервал (ДИ) 2,92-7,65); добавление ЭКГ признаков ишемии увеличило RR до 5,75 (ДИ 3,76-8,8).
Заключение. RR возникновения ККТ у больных с ИМ в анамнезе без или с изменениями ЭКГ ишемического типа в 4,73 и 5,75 раз выше, чем у лиц без ИМ и ЭКГ-изменений. Выявленные при этом ФР не могут объяснить такое увеличение ККТ. Очевидно, что лица с перенесенным ИМ нуждаются в реабилитации. Наличие ФР у лиц с впервые выявленным ИМ указывает на недостаточную первичную профилактику, что позволяет предполагать, что усиление профилактической работы по устранению традиционных ФР у больных с впервые выявленным ИМ будет способствовать снижению риска повторного ИМ или сердечно-сосудистой смертности.
Цель. Оценить вклад субклинического атеросклероза в стратификацию больных с риском сердечно-сосудистых осложнений (ССО) по SCORE <5% по данным 10-летнего наблюдения.
Материал и методы. В исследование было включено 379 больных с риском ССО по SCORE <5% (82 м/297 ж). В 2009г всем больным проводилось клиническое обследование, ультразвуковое исследование сонных артерий (СА) с определением количества атеросклеротических бляшек (АСБ) в СА, суммарного стеноза СА, толщины комплекса интима-медиа (ТИМ) общей СА (ОСА). Количество АСБ определяли как суммарное количество всех бляшек в 6 сегментах — на протяжении обеих ОСА, обеих бифуркаций ОСА и обеих внутренних СА. Суммарный стеноз рассчитывали как сумму стенозов в 6 сегментах СА в %. В 2019г был проведен телефонный опрос больных, с заполнением опросника, отражающего ССО за прошедшее время: смерть от любых причин, смерть от сердечно-сосудистых заболеваний (ССЗ), острые инфаркты миокарда (ОИМ), острые нарушения мозгового кровообращения (ОНМК), случаи реваскуляризации миокарда, госпитализации по ССЗ, комбинированная конечная точка.
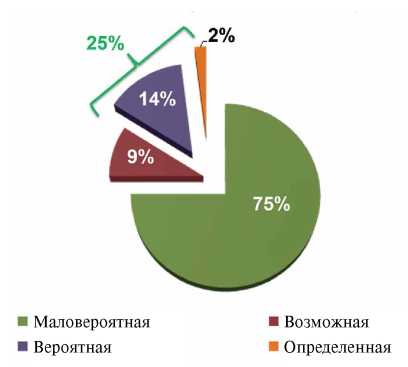
Результаты. Возраст больных исходно составлял от 35 до 67 лет (51,1±7,5 лет). АСБ от 20% до 50% были выявлены у 303 человек (79,94%). За истекшие 10 лет произошло 5 случаев сердечно-сосудистой смерти (1,3%), 7 ОИМ (1,8%), 5 случаев нестабильной стенокардии (1,3%), 12 случаев реваскуляризации миокарда (3,2%), 15 ОНМК (4,0%), 51 госпитализация по ССЗ (13,5%). Доля больных, у которых были зарегистрированы конечные точки (ССО+), составила 22,4% (85 человек). Группы больных ССО+ и не перенесших ССО отличались по уровню систолического артериального давления (АД) и триглицеридов крови, не различались по уровню диастолического АД, показателям липидного профиля, глюкозы, частоты сердечных сокращений, статусу курения, полу, возрасту. В группе ССО+ были выше ТИМ ОСА 0,65 (0,64;0,70) мм vs 0,62 (0,62;0,66) мм, р<0,05, суммарный стеноз СА 102,5 (88,1;120,8)% vs 80 (72,5;88,1)%, р=0,01, и количество АСБ в СА 4,0 (2,8;3,9) vs 3,0 (2,6;3,1), р=0,01, соответственно. Суммарный стеноз СА показал себя независимым предиктором развития ССО при введении поправки на пол, возраст, систолическое АД и диастолическое АД (β=0,149; p<0,05), но не на показатели липидного профиля. В результате ROC-анализа была получена “отрезная точка” для суммарного стеноза СА, составившая 82,5% (AUC=0,598, 95% доверительный интервал 0,5243-0,673, p<0,05).
Заключение. Суммарный стеноз СА показал себя независимым предиктором развития ССО у больных с риском по SCORE <5%.
Цель. Оценить частоту семейной гиперхолестеринемии (СГХС) и гиперлипопротеидемии(а) (гиперЛп(а)) у больных с ранней манифестацией острого коронарного синдрома (ОКС).
Материал и методы. В исследование включено 120 пациентов с развитием ОКС до 60 лет (средний возраст 53±7 лет, 104 (87%) мужчины) и 44 человека из группы сравнения без атеросклеротических сердечно-сосудистых заболеваний и дислипидемии (средний возраст 48±11 лет, 19 (43%) мужчин). Всем больным с ОКС выполнена коронарная ангиография. Показатели липидного профиля и липопротеид(а) (Лп(а)) определяли у всех пациентов.
Результаты. Частота гиперЛп(а) у пациентов с преждевременной манифестацией ОКС составила 41% (n=49), потенциальной СГХС — 25% (n=30), сочетания СГХС и гиперЛп(а) — 13% (n=15). В группе сравнения повышенная концентрация Лп(а) выявлена у 14% (n=6). Согласно анализу кривых операционных характеристик, уровень Лп(а) ≥30 мг/дл обладал максимальной значимостью для оценки вероятности наличия ОКС с чувствительностью 40% и специфичностью 86% (площадь под кривой 0,6; 95% доверительный интервал (ДИ): 0,5-0,7, p<0,05), а уровень Лп(а) ≥15 мг/дл ассоциировался с поражением двух и более коронарных артерий с чувствительностью 67% и специфичностью 65% (площадь под кривой 0,7; 95% ДИ: 0,6-0,7, p<0,01). При логистическом регрессионном анализе возраст (отношение шансов (ОШ) 1,1; 95% ДИ: 1,0-1,2, <0,05), курение (ОШ 7,5; 95% ДИ: 2,5-22,0, р<0,001) и уровень Лп(а) ≥30 мг/дл (ОШ 6,7; 95% ДИ: 1,1-39,7, р<0,05) независимо связаны с ранним развитием ОКС. Только уровень Лп(а) ≥15 мг/дл ассоциировался с многососудистым поражением коронарных артерий у этих пациентов (ОШ 3,8; 95% ДИ: 1,52-9,74, р<0,01).
Заключение. Каждый четвертый пациент с ранней манифестацией ОКС имеет СГХС, почти каждый второй — гиперЛп(а), и каждый восьмой — сочетание СГХС и гиперЛп(а). ГиперЛп(а) ассоциирована с развитием ОКС до 60 лет и с наличием у этих больных многососудистого поражения коронарных артерий.
Цель. Оценить у пациентов с очень высоким сердечно-сосудистым риском (ССР) эффективность и безопасность применения комбинированной липидснижающей терапии в составе с ингибитором PCSK9 на протяжении 6 мес. наблюдения.
Материал и методы. В проспективное открытое одноцентровое поисковое научное исследование с активным лечением включено 5 амбулаторных пациентов очень высокого ССР, имевших в 80% анамнез ишемической болезни сердца, 20% — заболевания периферических артерий, 60% — постинфарктный кардиосклероз. Главным критерием включения являлось недостижение целевых значений холестерина липопротеинов низкой плотности (ХС ЛНП) <1,4 ммоль/л на фоне высокоинтенсивной монотерапии статинами в максимально переносимых дозах или комбинированной терапии с эзетимибом. На регулярной основе все включенные пациенты принимали аторвастатин 40-80 мг/сут. или розувастатин 20-40 мг/сут., или питавастатин 2-4 мг/сут., 2 пациента получали статин в комбинации с эзетимибом 10 мг/сут. Наблюдение за пациентами осуществлялось на протяжении 6 мес.: каждые 2 нед. под контролем липидограммы выполнялись подкожные инъекции алирокумаба в дозе 150 мг/мл. Дополнительно оценивались клинические и лабораторные показатели безопасности терапии.
Результаты. Через 6 мес. на фоне применения комбинированной липидснижающей терапии с применением алирокумаба достигнуто снижение медиан ХС ЛНП с 4,3 (4,11-4,67) до 1,27 (1,06-1,47) (р=0,001) ммоль/л, общего холестерина с 6,1 (6-7) до 3,7 (3,5-3,9) (р=0,018) ммоль/л, индекса атерогенности с 3,2 (3-3,26) до 0,8% (0,8-1,5) (р=0,001). Достоверного снижения медианы триглицеридов и прироста медианы холестерина липопротеинов высокой плотности продемонстрировано не было. Применение липидснижающей терапии ингибитором PCSK9 у пациентов очень высокого риска в течение 6 мес. происходило без развития нежелательных явлений и позволило достигнуть максимального снижения ХС ЛНП в среднем на 75,4% уже к 4 мес. лечения в реальной клинической практике.
Заключение. Комбинированная липидснижающая терапия с применением алирокумаба 150 мг подкожно раз в 2 нед. в течение 6 мес. у пациентов очень высокого риска позволяет у большинства пациентов достигать целевых значений ХС ЛНП.
Цель. Изучить прогностическую значимость шкалы ABS в отношении развития крупных неблагоприятных сердечно-сосудистых событий у пациентов различного сердечно-сосудистого риска (ССР) в возрасте от 40 до 64 лет.
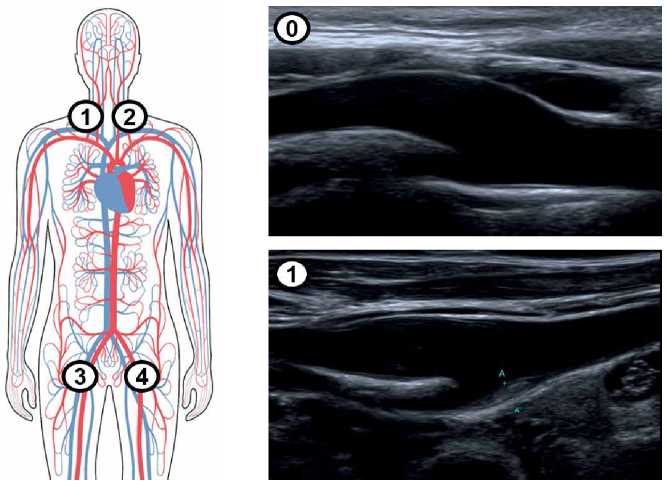
Материал и методы. В исследование включали мужчин и женщин в возрасте от 40 до 64 лет. Всем пациентам проводили дуплексное сканирование артерий каротидного бассейна и артерий нижних конечностей. Суммарный балл по шкале ABS рассчитывали по результатам оценки наличия атеросклеротической бляшки в бифуркациях общей сонной артерии и общей бедренной артерии с обеих сторон. Комбинированной конечной точкой являлась смерть от кардиоваскулярных причин, нефатальный инфаркт миокарда, нефатальный инсульт, коронарная реваскуляризация или реваскуляризация периферических артерий.
Результаты. В исследование были включены 232 пациента, удовлетворявших критериям включения, медиана возраста составляла 55,0 лет. Очень высокий ССР был установлен у 94 (40,5%) пациентов, высокий CCР был зарегистрирован у 48 (20,7%) пациентов, низкий и промежуточный ССР был установлен у 90 (38,8%) пациентов. Длительность периода наблюдения составляла 23,6 (15,5; 51,2) мес., что обеспечивало 632,6 пациенто-лет наблюдения. События, составляющие комбинированную конечную точку, произошли у 28 (12,1%) пациентов. Увеличение кумулятивного риска неблагоприятных сердечно-сосудистых событий наблюдалось при значениях ABS ≥2, с существенным возрастанием относительного риска (RR) при значениях ABS ≥3. По данным регрессионного анализа Кокса наличие ABS ≥3 было связано с увеличением RR развития неблагоприятных сердечно-сосудистых событий в 3,71 раза (95% доверительный интервал (ДИ) 1,18-11,6; p=0,025) после поправки на пол, возраст, исходный ССР, ожирение, курение, гипертоническую болезнь, ишемическую болезнь сердца, реваскуляризацию миокарда в анамнезе, сахарный диабет 2 типа, лекарственную терапию, а также уровни холестерина не-липопротеидов высокой плотности, высокочувствительного С-реактивного белка, скорости клубочковой фильтрации.
Заключение. У пациентов различного ССР в возрасте 40-64 лет балл по ультразвуковой шкале ABS ≥3 ассоциировался с увеличением RR развития неблагоприятных сердечно-сосудистых событий в 3,71 раза (95% ДИ 1,18-11,6; p=0,025) после поправки на потенциальные вмешивающиеся факторы, в т.ч. пол, возраст, исходный ССР, ишемическую болезнь сердца и сахарный диабет 2 типа.
Цель. Сравнить частоту прогрессирования коронарного атеросклероза у пациентов, перенесших коронарное стентирование (КС), при очном и дистанционном наблюдении кардиологом по данным годового исследования.
Материал и методы. В исследование включено 279 пациентов 61,5±9,5 лет со стабильной стенокардией напряжения 2 функционального класса и выше, либо безболевой ишемией миокарда, которым было проведено КС. Было сформировано 3 группы: группа 1 (n=96) — непосредственное наблюдение кардиолога перед КС, через 1, 3, 6 и 12 мес. после него. Группа 2 (n=95) — дистанционное наблюдение: пациенты находились под непосредственным контролем терапевта по месту жительства с привлечением кардиолога по дистанционным каналам связи (электронная почта, телефон, Skype) через 1, 3, 6 и 12 мес. Группа 3 (n=88) — наблюдение терапевтом по месту жительства, контакт с координатором исследования осуществлялся перед КС и по истечении 12 мес. после вмешательства. По истечении 12 мес. после КС всем пациентам была проведена проба на стресс-индуцированную ишемию миокарда. При положительном либо сомнительном результате пробы проводилась коронароангиография (КАГ).
Результаты. Стресс-индуцированная ишемия миокарда в ходе инструментального обследования через 12 мес. после КС была верифицирована у 58 пациентов (21%): 19 пациентов (19,8%) группы 1, 9 пациентов (9,5%) группы 2 и 30 пациентов (34,1%) группы 3, р<0,05. Контрольная КАГ была проведена 96 пациентам (34,4% от общего числа больных). У 8 (2,9%) пациентов выявлен рестеноз, у 38 (13,6%) — прогрессирование коронарного атеросклероза и у 4 (1,4%) — сочетание вышеперечисленного. Прогрессирование коронарного атеросклероза достоверно чаще отмечалось в группе 3: 10,4%, 9,5% и 21,6% в группах 1, 2 и 3, соответственно (p<0,05). По частоте развития рестеноза стента группы были сопоставимы: 2,1%, 3,2% и 3,5% в группах 1, 2 и 3, соответственно.
Заключение. Прогрессирование коронарного атеросклероза было основной причиной повторных реваскуляризаций через 12 мес. после индексного КС. Очное и дистанционное наблюдение кардиолога ассоциировано с меньшей частотой прогрессирования коронарного атеросклероза и повторной КАГ на протяжении 12 мес. наблюдения после КС.
Цель. Оценить взаимосвязь между ранней манифестацией ишемической болезни сердца (ИБС) с различными показателями липидного спектра.
Материал и методы. В продольное исследование с ретроспективным сбором данных были включены 166 мужчин в возрасте 57±9 лет с ИБС, которая дебютировала до 55 лет. Контрольную группу составили 62 мужчины (60±8 лет), не имевшие ИБС и стенозирующего атеросклероза в коронарном и периферических бассейнах. Для всех больных группы исследования были собраны данные о показателях липидного спектра: общий холестерин (ОХС), холестерин липопротеидов низкой плотности (ХС ЛНП), холестерин липопротеидов высокой плотности (ХС ЛВП), холестерин, не связанный с липопротеидами высокой плотности (ХС неЛВП), и концентрация липопротеида(а) (Лп(а)) на момент манифестации ИБС; пациентам контрольной группы — на первом визите в Институт клинической кардиологии им. А.Л. Мясникова. Соответствующие показатели были измерены в плазме крови в момент включения в исследование у всех пациентов. Дополнительно был рассчитан уровень корригированного ХС ЛНП (ХС ЛНПкорр), учитывающего холестерин, входящий в состав частицы Лп(а). Диагноз гиперхолестеринемии выставлялся при исходно выявленном уровне ОХС >5 ммоль/л и/или ХС ЛНП >3,0 ммоль/л и/или холестерина, ХС неЛВП >3,8 ммоль/л, гиперлипопротеидемии(а) (гиперЛп(а)) — при уровне Лп(а) >30 мг/дл.
Результаты. Нарушения липидного обмена достоверно чаще встречались в группе пациентов с ранней ИБС по сравнению с контрольной группой. Концентрация Лп(а) ≥30 мг/дл наряду с повышенными уровнями ХС неЛВП или ХС ЛНПкорр ассоциировались с ранним развитием ИБС вне зависимости от наследственности и курения в общей когорте обследованных мужчин. Анализ кривых выживаемости Каплана-Мейера продемонстрировал, что любые формы нарушения липидного обмена ассоциировались с увеличением риска развития ранней ИБС. Кроме того, пациенты с изолированно повышенной концентрацией Лп(а) доживали до манифестации ИБС на 8 лет раньше — 47 vs 55 лет, р<0,02. Вероятность ранней ИБС была максимальной при сочетании повышенного уровня ХС неЛВП и гиперЛп(а) — коэффициент рисков 2,91 (95% ДИ 1,96-4,33), р<0,0001.
Заключение. ГиперЛп(а) является независимым фактором раннего развития ИБС даже на фоне нормолипидемии, что подтверждает необходимость рутинного измерения Лп(а) в клинической практике.
Цель. Исследовать окислительно-антиоксидантный профиль крови у молодых людей с ранней ишемической болезнью сердца (ИБС) на фоне абдоминального ожирения (АО).
Материал и методы. В исследование было включено 169 человек. Основную группу составили 47 с диагнозом ранняя (до 45 лет) ИБС (по эпидемиологическим критериям “Определенная ИБС”), из них 22 человека с АО и 25 человек без АО. В контрольную группу было включено 122 без ИБС, сопоставимых с основной группой по полу, возрасту и индексу массы тела. Среди них с АО 67 человек и без АО 55 человек. У всех обследованных в крови определяли содержание общего холестерина (ХС), триглицеридов, ХС липопротеинов высокой плотности (ЛВП), МДА-модифицированных окисленных липопротеинов низкой плотности (ЛНП), супероксиддисмутазы (СОД), глутатион-пероксидазы 1 и общей антиоксидантной способности (ОАС) крови. Статистическая обработка результатов проводилась в программе SPSS 13.0.
Результаты. ОАС крови была ниже в 2,3 раза у лиц с ИБС, чем в группе лиц без ИБС, и составила 1,58 ммоль тролокса. Уровень в крови СОД в группе лиц с ИБС был в 1,16 раза выше, чем в группе лиц без ИБС. Относительный шанс наличия ранней ИБС был связан со снижением ОАС (В=-2,855; Exp(B)=0,058; 95% доверительный интервал (ДИ) 0,008-0,392; р=0,004) и с повышенным уровнем СОД (В=0,105; Exp(B)=1,076; 95% ДИ 1,031-1,196; р=0,006), независимо от пола, возраста, факторов риска.
Заключение. Таким образом, из изученных нами окислительно-антиоксидантных показателей только повышенный уровень СОД и сниженная ОАС крови могут являться потенциальными биомаркерами для выявления ранней ИБС у людей до 45 лет.
Цель. Проанализировать связь показателей липидного спектра крови, включая уровень липопротеида(а) (Лп(а)), субпопуляционного состава циркулирующих CD4+ Т-лимфоцитов с ранним развитием ишемической болезни сердца (ИБС).
Материал и методы. В ретроспективное одномоментное исследование было включено 76 мужчин в возрасте от 40 до 79 лет. Пациенты были разделены на группы: ИБС (58 [54;64] лет, n=56) с манифестацией заболевания до 55 лет и контрольную (62 [57;66] лет, n=20) без ИБС и стенозирующего атеросклероза коронарных и периферических артерий. Статины принимали 51 (91%) и 9 (45%) пациентов в основной и контрольной группе, соответственно. В образцах сыворотки и плазмы были определены показатели липидного спектра и концентрация (Лп(а)). Фенотипирование клеток проводили методом прямой иммунофлуоресценции в культуре мононуклеарных лейкоцитов, выделенных из крови; для определения цитокинов клетки активировали in vitro в присутствии блокатора внутриклеточного транспорта секреторных белков. Флуоресценцию клеток определяли с помощью цитофлуориметрии в потоке.
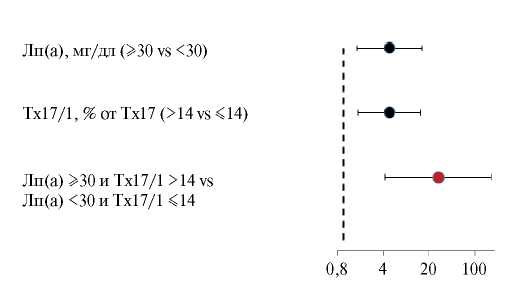
Результаты. Пациенты обеих групп были сопоставимы по возрасту, индексу массы тела, частоте артериальной гипертензии и сахарного диабета. Концентрация Лп(а) в крови была выше в группе с ИБС по сравнению с контрольной (49 [10;102] мг/дл vs 12 [4,3;32] мг/дл, p<0,05). Содержание интерферон γ-продуцирующих Т-хелперов 17 (Тх17/1) также было выше в группе ИБС (19 [15;24]% vs 13 [11;22]% от Тх17, p=0,05). Согласно данным логистического регрессионного анализа повышенная концентрация Лп(а) (≥30 мг/дл) и относительное количество Тх17/1 (>14% от Тх17) независимо друг от друга, уровня холестерина атерогенных липопротеидов, классических факторов риска и приема статинов ассоциировались с преждевременным развитием ИБС в общей группе пациентов с отношением шансов (ОШ) 4,6 (95% доверительный интервал (ДИ) 1,1-20,2) и 10,9 (2,1-56,7), р<0,05, соответственно. Сочетание концентрации Лп(а) >30 мг/дл и Тх17/1 >14% многократно увеличивало шансы ранней манифестации ИБС (ОШ 28,0, 95% ДИ 4,31-181,75, р=0,0005).
Заключение. Впервые показано, что повышенная концентрация Лп(а) на фоне увеличенного содержания Тх17/1 связана с преждевременным развитием стенозирующего атеросклероза коронарных артерий и ранней манифестацией ИБС у мужчин.
Цель. Оценить предиктивный потенциал электрокардиографических (ЭКГ), эхокардиографических (ЭхоКГ) и липидных показателей для прогнозирования обструктивного поражения коронарных артерий (ОПКА) у больных с острым коронарным синдромом без подъема сегмента ST (ОКСбпST) до проведения инвазивной коронароангиографии (КАГ).
Материал и методы. В проспективное обсервационное когортное исследование было включено 525 пациентов с ОКСбпST с медианой возраста 62 года, которым выполнялась инвазивная КАГ. Было выделено 2 группы, первую из которых составил 351 (67%) больной с ОПКА (стеноз 50%), а вторую — 174 (33%) без ОПКА (<50%). Клинико-функциональный статус больных до проведения КАГ оценивали по 40 показателям. Для обработки и анализа данных использовали методы Манна-Уитни, Фишера, хи-квадрат, однофакторную логистическую регрессию (ЛР), а для разработки прогностических моделей — многофакторную ЛР (МЛР), стохастический градиентный бустинг (XGBoost) и искусственные нейронные сети (ИНС). Качество моделей оценивали по 4 метрикам: площадь под ROC-кривой (AUC), чувствительность (Se), специфичность (Sp) и точность (Ac).
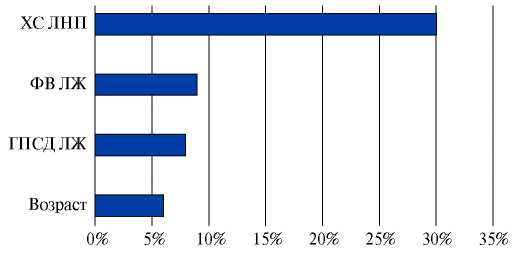
Результаты. Комплексный анализ показателей ЭКГ, ЭхоКГ и липидного спектра позволил выделить факторы, линейно и нелинейно связанные с ОПКА. Методами ЛР были определены их весовые коэффициенты и пороговые значения с наибольшим предиктивным потенциалом. Метрики качества лучшего прогностического алгоритма на основе МЛР составили по AUC — 0,81, Sp и Ac — 0,74, Se — 0,75. Предикторами данной модели были 4 показателя в категориальной форме (фракция выброса левого желудочка (ЛЖ) 42-60%, глобальная продольная систолическая деформация ЛЖ <19%, холестерин липопротеидов низкой плотности >3,5 ммоль/л, возраст >55 лет у мужчин и >65 лет — у женщин).
Заключение. Прогностическая модель, разработанная на основе МЛР, позволяет с высокой точностью верифицировать ОПКА у больных с ОКСбпST до проведения инвазивной КАГ. Модели на основе XGBoost и ИНС обладали меньшей предсказательной ценностью.
Цель. Оценить изменение активности эргорефлекса (ЭРф) у больных с хронической сердечной недостаточностью (ХСН) на фоне сниженной систолической функции левого желудочка в исследовании эффективности курса физических тренировок (ФТ), режим которых рассчитывали по оригинальной методике, по сравнению с ФТ, режим которых рассчитывали традиционно.
Материал и методы. Одноцентровое открытое исследование 297 пациентов с ХСН III функционального класса (ФК). Больных распределяли в две группы: основную (ОГ), пациентам которой интенсивность ФТ рассчитывали на основании определения лактатного порога (ЛП); и группу сравнения (ГС), пациентам которой расчет интенсивности нагрузки осуществляли согласно существующим рекомендациям, на основании 60% VO2peak. Выполнен анализ 1) активности ЭРф, 2) связи ЭРф с толерантностью к физической нагрузке (ТФН), рутинными маркерами системного воспаления, клиническими проявлениями ХСН, 3) ТФН на основании оценки поглощения кислорода на пике ФН (VO2peak).
Результаты. Увеличение скорости ходьбы на уровне ЛП после 3 мес. ФТ зарегистрировано у 94% (210 человек) ОГ. В ГС через 3 мес. режим ФТ пересчитывали по 60% VO2peak, увеличение скорости ходьбы на этом уровне после 3 мес. ФТ зарегистрировано у 70% больных ГС (35 человек). Выраженность ХСН уменьшилась в обеих группах, но динамика была более явной в ОГ, где II ФК достигли 75% пациентов (в ГС — 44%, р=0,003). В ОГ в большей степени, чем в ГС, увеличилась ТФН. Активность ЭРф (по ΔVE) снизилась на ≥15% у 230 (97%) больных ОГ и у 31 (63%) больного ГС. После завершения периода ФТ, когда у части пациентов ФК ХСН снизился до II (NYHA), была выявлена прямая ассоциация величины ЭРф (по ΔVE) с большей выраженностью ХСН (r=-0,57, p=0,01) и связи между снижением активности ЭРф (по ΔVE), повышением показателей VO2ЛП (r=-0,55, p=0,001), VO2peak (r=0,49, p=0,001), снижением содержания моноцитов (r=0,63, p=0,01).
Заключение. У пациентов с ХСН III ФК, находящихся в стабильном состоянии и получающих максимально возможную болезнь-модифицирующую терапию, активность ЭРф повышена и связана с ФК, ТФН, активностью системного воспаления. В ходе физической реабилитации уменьшение активности ЭРф сопровождается снижением ФК, повышением ТФН, более выраженным на фоне персонифицированных аэробных тренировок, режим которых рассчитывали с помощью определения ЛП.
Цель. Выполнить перевод, кросс-культурную адаптацию и валидацию психометрических показателей русскоязычной версии опросника уровня знаний об ишемической болезни сердца (ИБС) The second version of “the Coronary Artery Disease Education Questionnaire” (CADE-Q II) у пациентов с хроническими коронарными синдромами (ХКС)
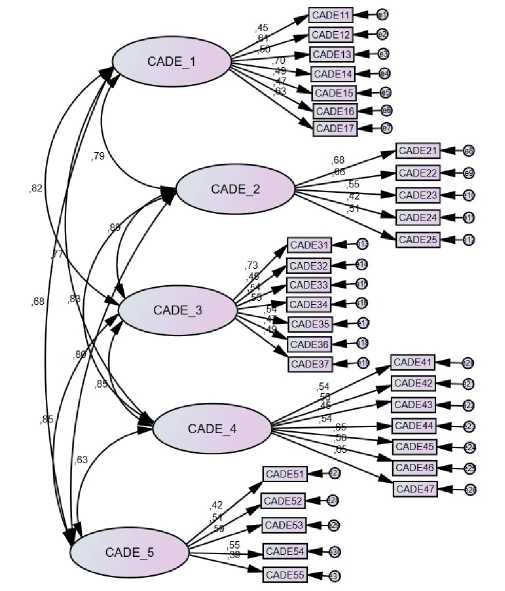
Материал и методы. Независимый и обратный переводы опросника CADE-Q II были выполнены двуязычными медицинскими работниками и сертифицированными переводчиками соответственно. Эксперты провели совещание по рассмотрению культурной значимости пунктов опросника для российских пациентов. Затем, окончательная версия была проверена на группе пациентов. Так, 303 пациента со стабильной ИБС, проходивших амбулаторное лечение в кардиологическом отделении в период с апреля по ноябрь 2021 года, были оценены с помощью CADE-Q II. Проводилась оценка следующих психометрических показателей: подтверждающий факторный анализ, внутренняя согласованность (оцененная с помощью коэффициента надёжности Кронбаха), ретестовая надежность и критериальная валидность.
Результаты. После окончания перевода, редакции и культурной адаптации, 30 пациентам потребовалось 30 минут, чтобы заполнить CADE-Q II во время пилотного теста. Анкета была понятна всем участникам опроса. Факторный анализ (критерий Кайзера-Мейера-Олкина =0,692, критерий сферичности Бартлетта <0,05) выявил четыре фактора, все из которых внутренне непротиворечивы и соответствуют исходной версии опросника. Показатели коэффициента надёжности Кронбаха варьировались от 0,61 до 0,88, а ретестовая надежность составляла 0,81. Достоверность критерия была подтверждена значительными различиями в сумме баллов CADE-Q II в зависимости от уровня образования участников и корреляцией между баллами CADE-Q II и опросником способности к самопомощи The Self Care of Coronary Heart Disease Inventory (r=0,251, p<0,05).
Заключение. Русскоязычная версия CADE-Q II показала достаточную надежность для оценки уровня знаний о заболеваниях у пациентов с ХКС в России.
Цель. Поиск ранних предикторов формирования патологического постинфарктного ремоделирования у больных, перенесших инфаркт миокарда с подъемом сегмента ST (ИМпST), с помощью метода speckle tracking эхокардиографии (STE).
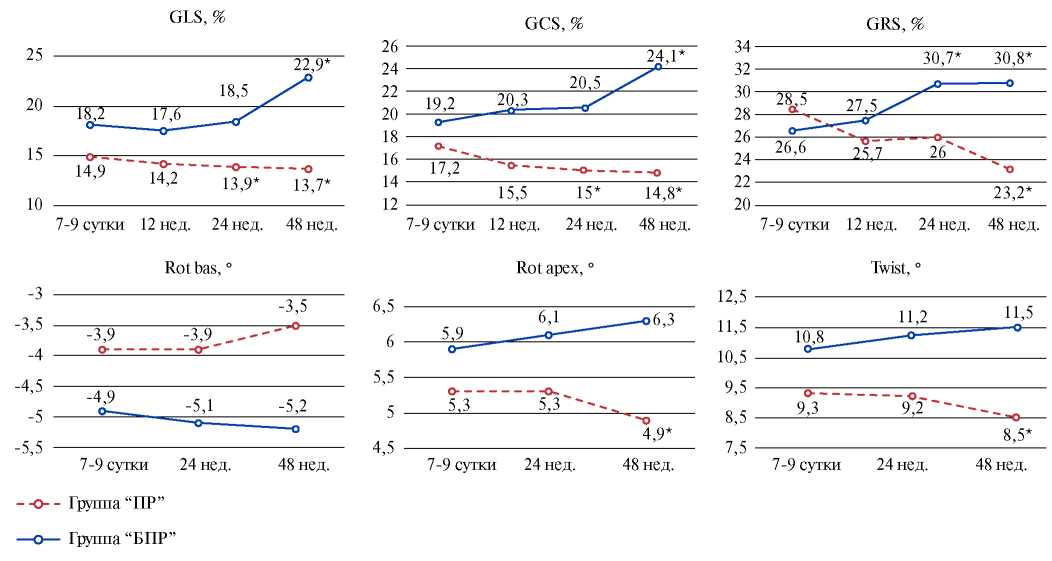
Материал и методы. В исследовании включено 114 больных ИМпST в возрасте 52 (44; 58) года. Проводилась двумерная эхокардиография c анализом стандартных параметров и STE с анализом деформационных и ротационных характеристик миокарда; определение концентрации мозгового натрийуретического пептида, уровень тропонина-I. В качестве конечной точки оценивали развитие патологического постинфарктного ремоделирования в течение 12 мес. наблюдения. В зависимости от исхода выделены 2 группы: с развитием патологического ремоделирования (ПР) — 45 (39,5%), без ПР (БПР) — 69 (60,5%).
Результаты. Раннее ремоделирование выявлено у 24 (53,3%) человек, среднесрочное — у 15 (33,4%) и у 6 (13,3%) — позднее ремоделирование. В группе “ПР” хроническая сердечная недостаточность (ХСН) наблюдалась у 100% больных, а в группе “БПР” 23 (33,3%) пациента не имели признаков ХСН.
Было установлено, что в раннем периоде инфаркта миокарда каждый из таких показателей, как глобальная продольная деформация (GLS) <11,7%, глобальная циркулярная деформация (GCS) <12,4% и снижение до 7,8o скручивания (Twist), c высокой чувствительностью и специфичностью прогнозирует развитие постинфарктной патологической дилатации. Была создана многофакторная логистическая регрессионная модель формирования ПР у больных ИМпST, в которую вошли GLS, глобальная радиальная деформация (GRS), индекс конечно-диастолического объема (иКДО), определенные на 7-9-е сут. ИМпST.
Заключение. GLS, GSC, Twist ЛЖ являются независимыми высокочувствительными и специфичными предикторами ПР. Установлены ранние предикторы постинфарктной патологической дилатации: сниженная GLS в сочетании с более высокой GRS и иКДО ЛЖ.
ОБЗОР ЛИТЕРАТУРЫ
Современные визуализирующие методики занимают важное место в диагностике, выборе метода лечения и прогнозе пациентов с ишемической болезнью сердца. Гибридная визуализация представляет собой комбинацию двух наборов диагностических данных, которые дополняют и увеличивают информативность друг друга путём сопоставления анатомических и функциональных характеристик. Как правило, гибридная визуализация является синергетической, т.е. более мощной, чем простая сумма ее частей, поскольку добавление новой информации приводит к повышению чувствительности и специфичности каждой из модальностей по отдельности.
В обзоре приводятся краткие сведения о диагностической эффективности перфузионной сцинтиграфии миокарда (ПСМ), рентгеновской компьютернотомографической (КТ) коронарографии в сравнении с инвазивной коронарографией и фракционным резервом кровотока. Детально характеризуется диагностическая и прогностическая значимость оценки кальциевого индекса совместно с ПСМ, а также КТ-коронарографии, совмещенной с ПСМ в диагностике, стратификации риска и прогнозе пациентов с ИБС. Отдельный раздел посвящен значению гибридной визуализации в принятии решений о реваскуляризации миокарда.
ИНФОРМАЦИЯ
С 21 по 25 мая 2022г в г. Милане (Италия) в гибридном формате прошел 90-й конгресс Европейского общества атеросклероза (EAS).
ISSN 2618-7620 (Online)