Перейти к:
Инфаркт миокарда в популяции некоторых регионов России и его прогностическое значение
https://doi.org/10.15829/1560-4071-2022-4952
Аннотация
Цель. Изучить распространенность инфаркта миокарда (ИМ) в популяции российских регионов и вклад в сердечно-сосудистые события.
Материал и методы. Материалом для анализа были представительные выборки из населения в возрасте 35-64 лет из 11 регионов Российской Федерации, обследованные в рамках многоцентрового исследования “Эпидемиология сердечно-сосудистых заболеваний и их факторов риска в различных регионах Российской Федерации”. Отклик составил ~80%. В исследовании использовалась систематическая стратифицированная многоступенчатая случайная выборка, сформированная по территориальному принципу на базе лечебно-профилактических учреждений. При проведении исследования информацию о наличии перенесенного ИМ получали опросным методом по стандартному вопроснику, выполнялась антропометрия и измерение артериального давления (АД) и частоты сердечных сокращений (ЧСС) автоматическим тонометром, регистрировалась электрокардиограмма (ЭКГ) в покое с последующим кодированием Миннесотским кодом. В качестве ЭКГ изменений ишемического типа считались мажорные и минорные зубцы QQS и сегменты STT. Биохимические параметры определялись на автоанализаторе Arkhitect 000. Медиана проспективного наблюдения составила 6,21 [5,25; 6,75] лет. Анализировалась комбинированная сердечно-сосудистая конечная точка (ККТ), включающая смерть от сердечно-сосудистых заболеваний и нефатальный ИМ. За период наблюдения выявлено 363 случая смерти от всех причин, из них 134 — от сердечно-сосудистых заболеваний; 196 случаев ККТ. Статистический анализ проведен в среде R 3.6.1.
Результаты. Распространенность ИМ среди населения российских регионов составила 2,9%; 5,2% среди мужчин и 1,5% среди женщин, увеличиваясь с возрастом. Мужчины с ИМ в анамнезе чаще принимали статины и бета-блокаторы, чем женщины: 39,0% vs 25,6% и 29,3% vs 27,1%, соответственно. Наличие ИМ, впервые выявленного в период наблюдения, ассоциировалось с основными факторами риска (ФР): курением, повышенными АД, ЧСС, триглицеридами и глюкозой. Для лиц с ИМ в анамнезе статистически значимая связь была выявлена только с курением. Множественное сравнение вклада ФР, ЭКГ изменений и ИМ в анамнезе показало, что включение в анализ ишемических изменений ЭКГ достоверно повышает риск сердечно-сосудистых событий у лиц без ИМ в анамнезе по сравнению с лицами без ИМ и без изменений ЭКГ. Высокий риск возникновения ККТ отмечен у лиц с ИМ в анамнезе: относительный риск (RR) — 4,73 (доверительный интервал (ДИ) 2,92-7,65); добавление ЭКГ признаков ишемии увеличило RR до 5,75 (ДИ 3,76-8,8).
Заключение. RR возникновения ККТ у больных с ИМ в анамнезе без или с изменениями ЭКГ ишемического типа в 4,73 и 5,75 раз выше, чем у лиц без ИМ и ЭКГ-изменений. Выявленные при этом ФР не могут объяснить такое увеличение ККТ. Очевидно, что лица с перенесенным ИМ нуждаются в реабилитации. Наличие ФР у лиц с впервые выявленным ИМ указывает на недостаточную первичную профилактику, что позволяет предполагать, что усиление профилактической работы по устранению традиционных ФР у больных с впервые выявленным ИМ будет способствовать снижению риска повторного ИМ или сердечно-сосудистой смертности.
Ключевые слова
Для цитирования:
Шальнова С.А., Драпкина О.М., Куценко В.А., Капустина А.В., Муромцева Г.А., Яровая Е.Б., Баланова Ю.А., Евстифеева С.Е., Имаева А.Э., Шляхто Е.В., Бойцов С.А., Астахова З.Т., Барбараш О.Л., Белова О.A., Гринштейн Ю.И., Ефанов А.Ю., Калачикова О.Н., Кулакова Н.В., Недогода С.В., Ротарь О.П., Трубачева И.А., Черных от имени участников исследования ЭССЕ-РФ Т.М. Инфаркт миокарда в популяции некоторых регионов России и его прогностическое значение. Российский кардиологический журнал. 2022;27(6):4952. https://doi.org/10.15829/1560-4071-2022-4952
For citation:
Shalnova S.A., Drapkina O.M., Kutsenko V.A., Kapustina A.V., Muromtseva G.A., Yarovaya E.B., Balanova Yu.A., Evstifeeva S.E., Imaeva A.E., Shlyakhto E.V., Boytsov S.A., Astakhova Z.T., Barbarash O.L., Belova O.A., Grinshtein Yu.I., Efanov A.Yu., Kalachikova O.N., Kulakova N.V., Nedogoda S.V., Rotar O.P., Trubacheva I.A., Chernykh on behalf of the ESSE-RF study participants. T.M. Myocardial infarction in the population of some Russian regions and its prognostic value. Russian Journal of Cardiology. 2022;27(6):4952. (In Russ.) https://doi.org/10.15829/1560-4071-2022-4952
Ишемическая болезнь сердца (ИБС) является основной причиной смертности и инвалидности в структуре осложнений сердечно-сосудистых заболеваний (ССЗ) во всем мире и представляет собой глобальную проблему общественного здоровья [1-3]. Несмотря на то, что смертность от этого заболевания в последние десятилетия снижалась, приводя к увеличению продолжительности жизни, этот же процесс привел к росту заболеваемости и коморбидных состояний. Иначе говоря, бремя ИБС увеличивается параллельно росту продолжительности жизни [4].
По данным исследования Global Burden (2020) было отмечено, что ИБС страдают ~126 млн человек во всем мире (1655 на 100 тыс.), что составляет 1,72% населения планеты. В Европе показатели распространенности ИБС и инвалидизации от нее составили 3547 на 100 тыс. и 3771 на 100 тыс. населения, соответственно, в США — 2929 на 100 тыс. и 2470 на 100 тыс., соответственно. Аналогичные российские показатели, к сожалению, существенно выше и составляют 4198 на 100 тыс. и 6758 на 100 тыс., соответственно. Особо обращает на себя внимание большое количество лет, потерянных из-за инвалидизации [4]. Прогнозы показывают, что к 2030г распространенность ИБС может увеличиться до 1845 случаев и более на 100 тыс., с верхней доверительной оценкой 1917 случаев на 100 тыс. Heidenreich P, et al. (2011) продемонстрировали, что рост распространенности ИБС приведет к существенному росту стоимости заболевания и к увеличению финансового бремени [5]. Таким образом, вопрос выявления лиц с ССЗ, изучения частоты заболевания и его исходов становится все более актуальным и важным.
Одним из наиболее серьезных осложнений ИБС является инфаркт миокарда (ИМ), который возникает чаще всего вследствие атеротромботической окклюзии сосудов сердца. Поскольку атеросклероз протекает в основном бессимптомно, ИМ может быть как следствием хронического течения атеросклероза, так и первым проявлением заболевания. Greenlee RT, et al. (2002) в работе, посвященной изучению ИМ в популяции, показали, что ~20% случаев этого заболевания составляет впервые выявленный ИМ [6]. ИМ обычно возникает внезапно, его симптомы хорошо известны, разработаны диагностические критерии [7] и рекомендации по лечению различных форм ИМ. В этих условиях изучение факторов, способствующих развитию ИМ, в т.ч. повторного, является ключевой проблемой профилактики ССЗ. Например, мужской пол является доказанным известным фактором риска (ФР), и, по данным Khan MA, et al. (2020), распространенность ИБС была выше у мужчин по сравнению с женщинами (1786 vs 1522 случаев на 100 тыс.) [4]. Эта разница присутствует во всех возрастных группах. В большинстве исследований показан рост распространенности и заболеваемости с увеличением возраста и ассоциации с ФР и сопутствующей патологией [8-10]. Вместе с тем прогноз зависит не только от тяжести заболевания и состояния организма пациента, но и от системы оказания медицинской кардиологической помощи, которая может существенно различаться между странами и регионами [10]. Распространенность ИМ, факторы, влияющие на его возникновение и прогноз, интересуют исследователей со времен Фремингема [11][12].
Целью нашего исследования было изучение распространенности ИМ и его ассоциаций с ФР, а также среднесрочный прогноз комбинированной конечной точки (фатальных и нефатальных сердечно-сосудистых событий) у лиц с ИМ в анамнезе в популяции трудоспособного возраста некоторых регионов России.
Материал и методы
Материалом многоцентрового исследования “Эпидемиология сердечно-сосудистых заболеваний и их факторов риска в различных регионах Российской Федерации” (2012-2014гг) были представительныевыборки из неорганизованного мужского и женского населения в возрасте от 35-64 лет из 11 регионов Российской Федерации. Исследование было выполнено в соответствии со стандартами надлежащей клинической практики (Good Clinical Practice) и принципами Хельсинкской декларации. Исследование было одобрено Независимыми Этическими Комитетами ФГБУ “НМИЦ ТПМ” Минздрава России, ФГБУ “НМИЦ Кардиологии” Минздрава России и ФГБУ “НМИЦ им. В.А. Алмазова” Минздрава России и центров-соисполнителей. Все обследованные лица подписали добровольное информированное согласие на участие в нем. Отклик на обследование в целом составил ~80%.
В исследовании использовалась систематическая стратифицированная многоступенчатая случайная выборка, сформированная по территориальному принципу на базе лечебно-профилактических учреждений по методу Kish L [13].
Обследуемые опрашивались по стандартному вопроснику, разработанному на основе адаптированных международных методик. Вопросник, построенный по модульному типу, содержит: социально-демографические данные; данные о статусе курения и потребления алкоголя; отношение к здоровью; анамнез заболеваний. Диагноз перенесенного ИМ ставился при положительном ответе на вопрос: “Говорил ли Вам когда-нибудь врач, что у Вас имеются/имелись следующие болезни: ИМ?”
Измерение артериального давления (АД) проводили с использованием автоматического измерителя давления “M3 Expert” фирмы “OMRON” (Япония) на правой руке двукратно с интервалом 5 мин в положении сидя. В анализ включали среднее значение из 2 измерений. За артериальную гипертонию принимали уровень АД 140/90 мм рт.ст. и более или прием антигипертензивной терапии.
Анализировались следующие ФР ССЗ: общий холестерин (ОХС) ≥5 ммоль/л; холестерин липопротеинов низкой плотности (ХС ЛНП) >3,0 ммоль/л; холестерин липопротеинов высокой плотности (ХС ЛВП) <1,0 ммоль/л, <1,2 ммоль/л у женщин; триглицериды (ТГ) >1,7 ммоль/л; глюкоза плазмы натощак 5,6- 6,9 ммоль/л; ожирение (индекс массы тела ≥30 кг/м2); абдоминальное ожирение (окружность талии (ОТ) ≥102 см у мужчин и ≥88 см у женщин).
Регистрация 12 отведений электрокардиограммы (ЭКГ) в покое выполнялась после 5-минутного отдыха на компьютерном ЭКГ-комплексе PADSY (фирмы МедСет Медицинтехник ГмбХ, Гамбург, Германия) в положении лежа на спине. ЭКГ из регионов пересылались в электронном виде по интернет-каналу в Единую федеральную базу данных, находящуюся на территории ФГБУ “НМИЦ ТПМ” Минздрава России. Анализ ЭКГ и кодирование по Миннесотскому коду (МК) осуществляли двумя специалистами НМИЦ ТПМ с привлечением третьего в случае несогласия. Классификация ЭКГ-показателей проводилась по категориям МК “Мажорные и минорные изменения” [14]. Из Мажорных изменений выделяли зубцы QQS (МК 1-1, 1-2), (МК 1-3 плюс МК 4-1, 4-2, 5-1, 5-2) и изменения STT (МК 4-1, 4-2, 5-1, 5-2, без МК 3-1, 3-3, т.е. исключая вторичные изменения STT вследствие гипертрофии левого желудочка). Дополнительно выделяли так называемые минорные изменения на ЭКГ QQS (МК 1-3 без МК 4-1, 4-2, 5-1, 5-2) и изменения STT (МК 4-3, 4-4, 5-3, 5-4). Для анализа ЭКГ были сформированы в 4 группы в зависимости от наличия ИМ и сопутствующих изменений на ЭКГ: лица без ИМ в анамнезе и ЭКГ изменений (1), лица без ИМ, но с изменениями на ЭКГ (2); 3-я группа — лица с ИМ в анамнезе, но без ЭКГ изменений; и 4-я группа — те, кто имел и ИМ, и ЭКГ изменения.
Подробный протокол исследования ЭССЕ-РФ описан ранее [15]. Всего было обследовано 17345 человек. Два центра были исключены по причине отсутствия ЭКГ. В общий анализ включено 13446, в т.ч. 4948 мужчин и 8498 женщин. Кодирование и анализ ЭКГ проводили на выборке из 10941 человека, на которых была полная информация по всем анализируемым показателям.
В проспективном когортном наблюдении конечные точки (КТ) собирались один раз в два года с помощью прямого и непрямого контакта. В первую очередь устанавливали жизненный статус участника, затем причины смерти и несмертельные случаи ССЗ. Данные по смертности получены из регионального регистра с закодированными причинами смерти по МКБ-10. Заболеваемость проверялась и уточнялась по историям болезни и в Фонде обязательного медицинского страхования.
Период проспективного наблюдения составил 6,21 [ 5,25; 6,75] лет. Всего включено в анализ 363 случая смерти от всех причин, из них от ССЗ — 134. При анализе в качестве КТ использовали показатель смертности от ССЗ плюс нефатальный ИМ (комбинированная сердечно-сосудистая КТ, ККТ), которая составила 196 случаев или 2,9% наблюдаемой когорты.
Статистический анализ данных. Статистический анализ проведен в среде R 3.6.1. Для оценки отклонения распределения от нормального использован коэффициент непараметрической асимметрии Пирсона. Он вычисляется как разность между средним и медианой, нормированная на стандартное отклонение. Если параметр был унимодальным и имел непараметрическую асимметрию <0,2, то для него приведены среднее и стандартное отклонение (M±sd). Если хотя бы одно из условий нарушено, то для параметра приведены медиана и интерквартильный размах (Me [Q25; Q75]). Качественные показатели описаны относительными частотами в процентах.
Оценка различий между двумя независимыми выборками для непрерывных параметров проводилась с использованием критерия Манна-Уитни, для дискретных — точного критерия Фишера. Кривые выживаемости построены методом Каплана-Мейера. Сравнение кривых выживаемости проводилось лог-ранговым критерием с поправкой Холма для множественных сравнений. Оценка вклада ФР в смертность проводилась с использованием как однофакторных, так и многофакторных моделей пропорциональных рисков Кокса. При проверке всех статистических гипотез уровень значимости принят равным 0,05.
Проспективная часть исследования выполнена в рамках государственного задания ФГБУ “Национальный медицинский исследовательский центр терапии и профилактической медицины” Минздрава России № AAAA-A17 117070760036-6 “Эпидемиология сердечно-сосудистых заболеваний и их факторов риска в различных регионах Российской Федерации (ЭССЕ-РФ-проспективное). Развитие системы динамического наблюдения за эпидемиологической ситуацией, связанной с сердечно-сосудистыми заболеваниями и их факторами риска, в регионах Российской Федерации (ЭССЕ-РФ-2)”.
Результаты
Как и ожидалось, распространенность ИМ среди населения 35-64 лет выше у мужчин по сравнению с женщинами и увеличивается с возрастом у лиц обоего пола: от 0,8% до 10,1% у мужчин и от 0,2% до 2,9% у женщин, составив в среднем 5,2% и 1,5%, соответственно (рис. 1).
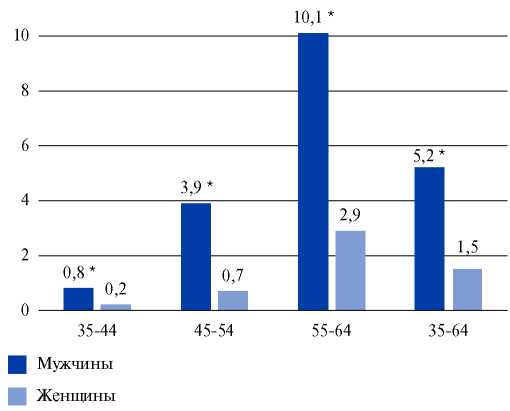
Рис. 1. Распространенность ИМ в исследовании ЭССЕ-РФ в зависимости от пола и возраста (%).
Примечание: * — p <0,05 (анализ с использованием точного двустороннего критерия Фишера).
В таблице 1 представлены ФР в зависимости от наличия и отсутствия ИМ в анамнезе на момент обследования. Женщины с ИМ в анамнезе были значимо старше мужчин с ИМ (58,8±5,3 vs 56,4±5,7 лет, p<0,05). Ассоциаций ИМ с уровнем образования не выявлено независимо от пола.
Таблица 1
Ассоциации ФР и ИМ у мужчин и женщин

Примечание: для показателей в таблице значения представлены в виде M±sd или n (%), или Me [Q25; Q75]. * — статистически значимые различия между группами “с ИМ” и “без ИМ” при поправке на возраст и регион с помощью логистической регрессии. Для показателя “возраст” поправка на возраст не проводилась.
Сокращения: АГ — артериальная гипертония, ДАД — диастолическое артериальное давление, ИМ — инфаркт миокарда, ИМТ — индекс массы тела, КТ — конечная точка, комбинированная КТ — нефатальный инфаркт миокарда или ССЗ-смерть, ОТ — окружность талии, ОХС — общий холестерин, САД — систолическое артериальное давление, СКФ — скорость клубочковой фильтрации, ССЗ — сердечно-сосудистые заболевания, ТГ — триглицериды, ХС ЛВП — холестерин липопротеинов высокой плотности, ХС ЛНП — холестерин липопротеинов низкой плотности, ЧСС — частота сердечных сокращений.
ИМ преимущественно выявлялся у мужчин с низким и средним доходом. Мужчины с ИМ в анамнезе чаще имели низкий образовательный ценз, более высокий уровень диастолического АД, значительно более низкий уровень ХС ЛВП, ХС ЛНП и ОХС, последние, возможно, за счет приема статинов. У женщин с ИМ относительно женщин без ИМ уровень ХС ЛВП и ОХС был выше. Следует отметить и у мужчин, и у женщин значимые ассоциации с более низким уровнем скорости клубочковой фильтрации и большей ОТ. Частота сердечных сокращений (ЧСС) у мужчин с ИМ была ниже, у женщин с ИМ выше, чем у лиц без ИМ.
За период наблюдения у лиц без ИМ в анамнезе первый ИМ развился у 106 (2,3%) мужчин и всего у 74 (0,9%) женщин, а в группе с ИМ в анамнезе новый ИМ или, скорее, повторный развился у 25 (9,7%) мужчин и 9 (7%) женщин, различия статистически значимы в обоих случаях. Независимо от пола все КТ выявляются достоверно чаще у лиц с ИМ в анамнезе.
Женщины, как известно, чаще принимают лекарственные препараты, чем мужчины. В нашем исследовании женщины по сравнению с мужчинами также чаще принимали все препараты, за исключением бета-адреноблокаторов и статинов, в приеме которых лидируют мужчины с перенесенным ИМ в анамнезе (табл. 2).
Таблица 2
Прием препаратов в зависимости от наличия ИМ в анамнезе
Примечание: * — статистически значимые различия между группами “с ИМ” и “без ИМ” при поправке на возраст и регион.
Сокращения: БРА — блокаторы рецепторов к ангиотензину II, иАПФ — ингибиторы ангиотензинпревращающего фермента, ИМ — инфаркт миокарда.
Следует, однако, отметить, что лекарственные препараты принимали лишь 10-39% больных с ИМ, что явно не соответствует рекомендациям. Так, статины принимали лишь 39,0% мужчин и 25,6% женщин с ИМ в анамнезе, бета блокаторы — 29,3% и 27,1% больных, соответственно. Самыми популярными препаратами, особенно, у женщин, была группа блокаторов ренин-ангиотензин-альдостероновой системы. Антиагреганты не учитывались в исследовании и не вошли в анализ.
На рисунке 2 представлено сравнение рисков изучаемых показателей для ККТ у лиц с ИМ в анамнезе и без него (по данным однофакторного анализа). Достоверные ассоциации между возникновением ИМ и ФР выявлены только при отсутствии ИМ в анамнезе: среди лиц мужского пола, в пожилом возрасте, у курящих, при повышенном уровне АД и ЧСС ≥80 уд./мин, повышенном уровне ТГ и глюкозы. Высокий уровень образования также снижает риск ККТ при отсутствии ИМ в анамнезе.
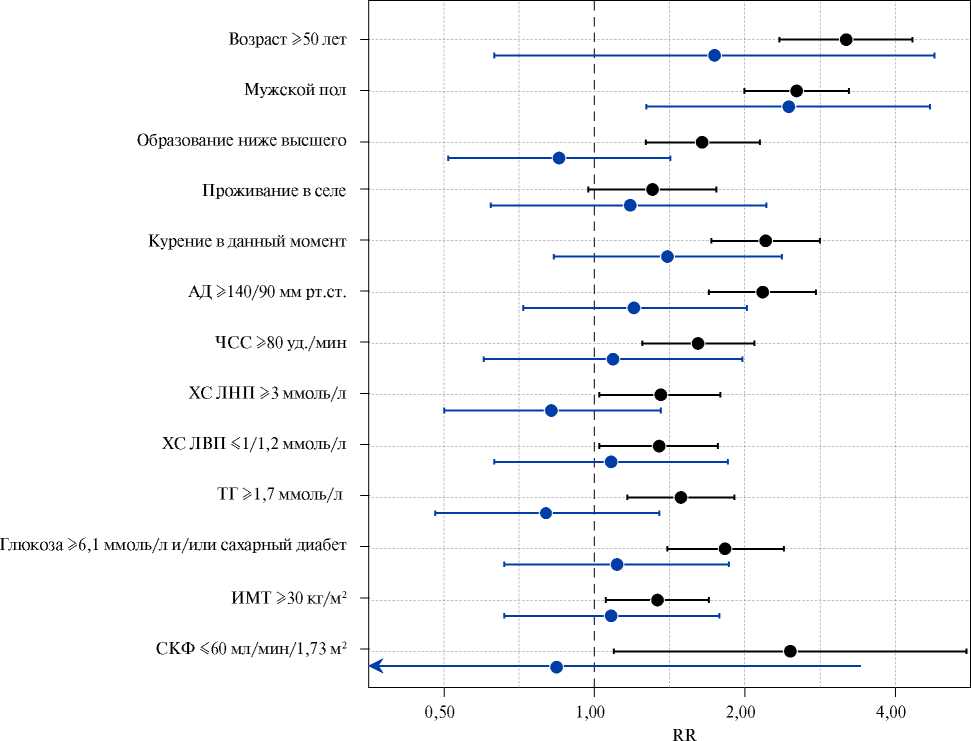
Рис. 2. Однофакторные модели для социально-демографических параметров и основных биомаркеров.
Примечание: синий — выборка участников с инфарктом миокарда, черный — без инфаркта миокарда. Цветное изображение доступно в электронной версии журнала.
Сокращения: АД — артериального давления, ИМТ — индекс массы тела, СКФ — скорость клубочковой фильтрации, ТГ — триглицериды, ХС ЛВП — холестерин липопротеинов высокой плотности, ХС ЛНП — холестерин липопротеинов низкой плотности, ЧСС — частота сердечных сокращений, RR — относительный риск.
Следует отметить, что для лиц с перенесенным ИМ влияние большинства ФР на ККТ, за исключением мужского пола, было существенно ниже и статистически незначимо. В этой выборке пациентов мы оценили частоту и прогностическое значение изменений ишемического типа на ЭКГ. Группа, не имевшая при обследовании ИМ и ЭКГ изменений, состояла из 9155 человек (83,7%), а без ИМ, но с признаками ЭКГ изменений (13,6%) — 1492 человек. Лица с ИМ в анамнезе, но без изменений на ЭКГ составили 153 человека (1,4%); те, кто имел ИМ и изменения на ЭКГ — 141 человек (1,3%).
Изменения зубцов QQS выявлялись чаще у мужчин, чем у женщин (7,2% vs 4,4%), тогда как снижение сегмента STT было более характерно для женщин (11,9% vs 9,0%), при наличии любого из указанных ЭКГ-изменений достоверной разницы не обнаружено (14,4% и 15,3%, p=0,21). Среди больных с ИМ 48% имели ишемические изменения на ЭКГ, среди лиц без ИМ лишь у 14% зарегистрированы аналогичные ЭКГ-изменения.
На рисунке 3 можно видеть выживаемость в четырех анализируемых группах.
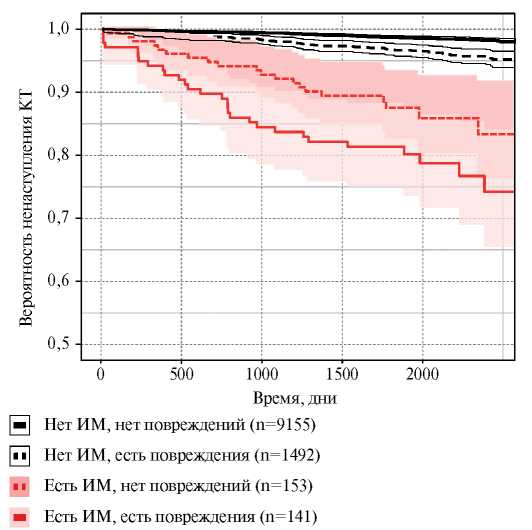
Рис. 3. Кривые Каплана-Мейера в зависимости от наличия/отсутствия ИМ и/ или изменений на ЭКГ при обследовании.
Примечание: цветное изображение доступно в электронной версии журнала.
Сокращения: ИМ — инфаркт миокарда, КТ — конечные точки.
На рисунке 3 все кривые Каплана-Мейера различаются значимо, за исключением групп “есть ИМ, нет нарушений” и “есть ИМ, есть нарушения на ЭКГ” (р=0,059), демонстрируя существенные потери выживаемости у тех, кто перенес ИМ. 6,5-летние вероятности ненаступления комбинированной КТ в группах составили 98,2%, 95,5%, 83,2% и 76,6% для групп “нет ИМ и повреждений”, “нет ИМ, есть повреждения”, “есть ИМ, нет повреждений”, “есть ИМ, есть повреждения”, соответственно. В пересчете на годовую смертность (без поправки на пол и возраст) это эквивалентно вероятности наступления КТ в год, равной примерно 0,3%, 0,7%, 2,8% и 4%, соответственно. Вероятности наступления КТ составили примерно 0,8% в год для мужчин и 0,2% в год для женщин.
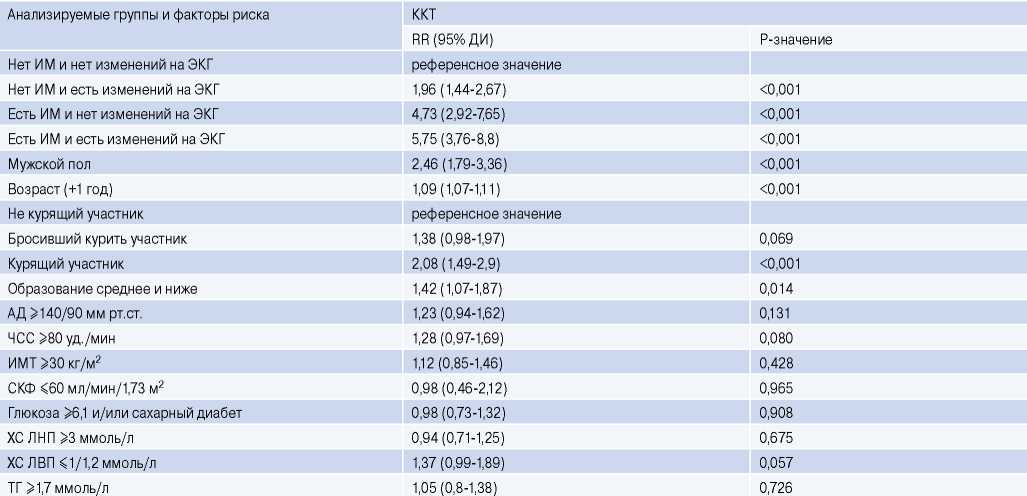
Вклад факторов в возникновение сердечно-сосудистых событий (ККТ), по данным многофакторной модели Кокса для обоих полов при коррекции на множественные ФР, представлен в таблице 3.
Таблица 3
Вклад факторов в возникновение сердечно-сосудистых событий (ККТ) (по данным многофакторной модели Кокса для обоих полов при коррекции на множественные ФР)
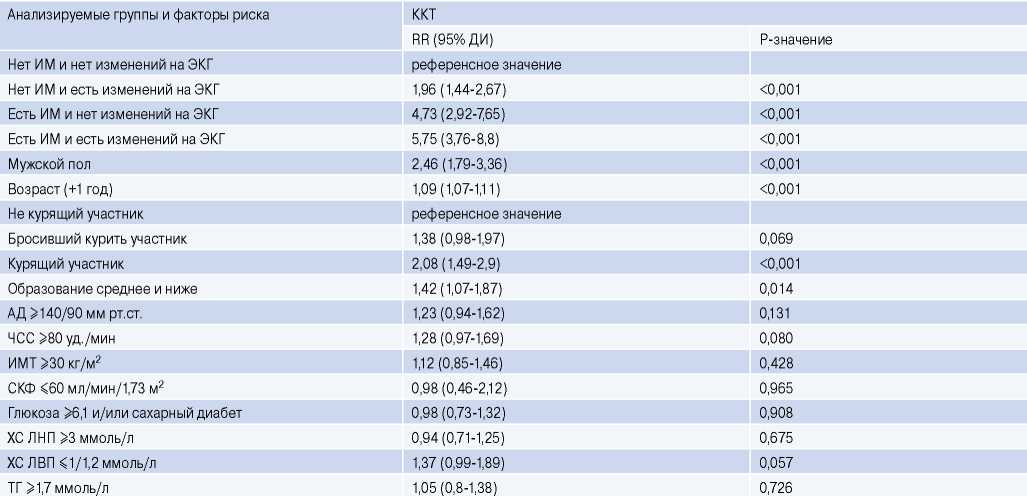
Примечание: если показатель принимал два значения, то за референсное принимали противоположное, не указанное в таблице значение. В многофакторную модель не включен ОХС в силу того, что в нее включены все его липидные фракции.
Сокращения: АД — артериальное давление, ДИ — доверительный интервал, ИМ — инфаркт миокарда, ИМТ — индекс массы тела, ККТ — комбинированная сердечно-сосудистая конечная точка, ОХС — общий холестерин, СКФ — скорость клубочковой фильтрации, ТГ — триглицериды, ЧСС — частота сердечных сокращений, ХС ЛВП — холестерин липопротеинов высокой плотности, ХС ЛНП — холестерин липопротеинов низкой плотности, ЭКГ — электрокардиограмма, RR — относительный риск.
Изменения ЭКГ, представленные зубцами QQS и/или депрессией сегмента STT, в многофакторном анализе имеют несколько меньший по значимости вклад в ККТ (1,96), но близкий к значениям риска мужского пола (2,46) и курения (2,08). Значимыми остались также возраст, низкий уровень образования, а также на уровне тенденции сниженный ХС ЛВП и ЧСС ≥80 уд./мин. Все остальные ФР статистически незначимы.
Обсуждение
Заболеваемость ССЗ в России в последние 3 года неустойчива, что объяснимо: пандемия ковид-19 вмешивается и в статистику ССЗ. Так, в 2019г по официальным данным среди трудоспособного населения число случаев ИМ составило 164709, повторного инфаркта — 20814. Коэффициент заболеваемости ИМ на 100 тыс. населения составил 141,4 и 19,6, соответственно. Это существенно выше, чем в 2018г, когда коэффициент смертности в этой же возрастной группе был 138,2 и 21,2 на 100 тыс., соответственно. Вместе с тем в 2020г зарегистрировано всего 154457 случаев первичного ИМ и 21041 случай повторного [16]. Снижение частоты ИМ относительно 2018 и 2019гг, скорее всего, объясняется ситуацией, связанной с посещением или, точнее, “не посещением” врача из-за боязни заразиться в поликлинике вирусной инфекцией.
Распространенность ИМ среди лиц в возрасте 35-64 года, по данным нашего исследования (2012- 2013гг), составила 5,2% у мужчин и 1,5% у женщин возраста 35-64 года. Как и ожидалось, отмечено увеличение частоты ИМ с возрастом у лиц обоего пола. Об этом же свидетельствуют данные NHANES: распространенность ИМ в США составляла в 2018г 3,1%, в т.ч. у мужчин 4,6%, у женщин — 2,1%. С возрастом этот показатель увеличивается от 0,4% в возрасте 35-44 лет до 15,8% в 80+ лет у мужчин и до 8,7% у женщин [1]. Piwonska A, et al. (2019) также обнаружили увеличение ИМ с возрастом в большой выборке 20 лет и старше. Диагноз выставлялся на основе МК ЭКГ. Однако в исследовании отмечается довольно высокая частота зубцов Q-QS в молодой части когорты [9]. В целом, рост частоты ИМ с возрастом показан у лиц обоего пола в большинстве популяционных исследований [17-19].
Литературные данные свидетельствуют о разнообразии критериев ИМ, подходах к анализу, объеме выборок и количества переменных. Это обстоятельство, с одной стороны, заставляет искать возможности для сравнения данных, с другой, создает возможность более глубокого подхода к анализу.
Надо отметить, что во многих публикациях по эпидемиологии в целях стандартизации результата за ИМ принимают ЭКГ-изменения ишемического типа, оцененные по критериям МК [9][17-21]. В нашем исследовании ИМ диагностировали при положительном ответе на вопрос: “Говорил ли Вам врач, что у Вас ИМ?”. Этот простой рутинный вопрос использует, в частности, Американская ассоциация сердца для оценки заболеваемости ИМ при сборе статистических данных о ССЗ [1]. Изменения на ЭКГ мы рассматривали в качестве свидетельства изменений миокарда, которые могут ухудшать прогноз. Лица с ИМ в анамнезе почти в половине случаев (48,0%) имели изменения миокарда, у лиц без ИМ изменения на ЭКГ встречались в 3 раза реже (14,0%). Можно предположить, что те обследуемые, которые не сообщали об ИМ, но на ЭКГ у них регистрировались признаки повреждения миокарда, могли иметь безболевую форму ИМ, встречающуюся, например, при сахарном диабете, ожирении и других состояниях [22]. Анализ выживаемости в зависимости от наличия ИМ и изменений на ЭКГ показал, что среди тех, кто не имел ИМ, выявлены наименьшие потери продолжительности жизни. Тогда как нижние кривые на рисунке 3, представляющие группы с ИМ независимо от наличия или отсутствия изменений ишемического типа на ЭКГ, демонстрируют 20% и 30% потерь вследствие возникновения ККТ, соответственно.
Примечательно, что первичный ИМ ассоциируется с различными ФР: пол, возраст, низкий образовательный статус, повышенные уровни АД, глюкозы, повышенная ЧСС, тогда как у лиц с ИМ в анамнезе ассоциаций с ФР не выявлено, кроме ЧСС и курения. Таким образом, влияние ФР у лиц с впервые развившимся ИМ выше, чем у лиц с повторными его эпизодами. Другими словами, первичный ИМ может быть предотвращен, уменьшив бремя ФР у лиц без ИМ. При повторном ИМ на первый план выходят, видимо, другие механизмы. На это указывает результат, полученный в настоящем исследовании: наличие ИМ в анамнезе существенно увеличивает риск возникновения ККТ, независимо даже от наличия изменений ишемического генеза на ЭКГ. Сам по себе ИМ в анамнезе увеличивает риск сердечно-сосудистых событий почти в 5 раз (относительный риск (RR) 4,73), а при добавлении ЭКГ изменений, подтверждающих поражение миокарда, — почти в 6 раз (RR 5,75) (табл. 3). Наличие на ЭКГ QQS или STTизменений ишемического типа у лиц без подтвержденного ИМ (со слов опрашиваемых) увеличивает риск ККТ в 1,96 раза. Это может указывать на собственный вклад в ККТ изменений миокарда предположительно вследствие перенесенного безболевого ИМ или иных форм ИБС.
Данное предположение подтверждается результатами литовских исследователей, показавших, что ишемические изменения и возможный ИМ были связаны с 2,5-кратным и 4,4-кратным повышением риска смерти от ССЗ у мужчин и 1,51-кратным и 2,56-кратным повышением риска смерти от ССЗ у женщин по сравнению с лицами без или с незначительными аномалиями ЭКГ [23]. Добавление изменений на ЭКГ к традиционным ФР ССЗ несколько улучшило показатели регрессионных моделей Кокса, позволив сделать вывод о наличии связи изменений ЭКГ с повышенным риском смертности от ССЗ. Однако авторы отмечают, что такая добавка лишь незначительно улучшала прогноз смертности от ССЗ помимо традиционных ФР.
В нашем исследовании наблюдается более существенное увеличение риска ККТ у лиц с ИМ в анамнезе в зависимости от сопутствующих изменений на ЭКГ. Повышенное влияние, собственно, ИМ на ККТ свидетельствует, по видимому, о недостаточной активности вторичной профилактики больных ИМ в стране в последние годы. Данные Хабаровского регистра, показавшего высокий уровень смертности больных после выписки из стационара [24], служат дополнительным свидетельством данного предположения.
Прием бета-адреноблокаторов составлял 73,8%, по данным Хабаровского регистра лиц, перенесших ИМ, vs 29,3% у мужчин и 27,1% у женщин в нашем исследовании. Хабаровский регистр показал, что далеко не все лица, перенесшие ИМ, принимают необходимые препараты [24]. Однако эти частоты в 2, а то и в 3 раза выше популяционных данных, полученных в нашем исследовании. Регистр Профиль также продемонстрировал недостаточную частоту приема рекомендованных лекарственных препаратов во вторичной профилактике после референсного острого ИМ, особенно в отношении статинов и двойной антитромбоцитарной терапии [25]. В регистрах ИМ часто отмечают недостаточное употребление рекомендованных лекарственных средств — это, пожалуй, общее для всех регистров.
В крупном бразильском исследовании, включавшем 15 тыс. человек обоего пола в возрасте 35-64 лет, QQS зарегистрированы у 3,3% мужчин и 1,3% у женщин, что практически совпадает с нашими данными. Кроме того, по заключению бразильских авторов на связь с ККТ влияло множество ФР. Хотя аналогичные ассоциации в нашей выборке выявлены только при первичном ИМ, в бразильской выборке риск не достигал двух, что существенно ниже, чем в нашей [1]. Это позволяет сделать вывод о недостаточной первичной профилактике ИМ в нашей стране. Об этом же пишут и авторы публикации, посвященной данным регистра ПРОФИЛЬ-ИМ: “Большинство больных, перенесших острый ИМ, уже имели ССЗ атеросклеротического генеза, либо набор традиционных ФР ИБС, т.е. развитие острого ИМ у них было вполне предсказуемым. Значительная часть этих больных до развития ИМ не была охвачена системой первичной и вторичной профилактики ИБС” [24].
Многофакторный анализ, проведенный в нашем исследовании, позволяет предположить, что среди показателей, оказывающих влияние на развитие ККТ, первое место занимает наличие ИМ в анамнезе. Риск появления ККТ несколько усиливается при добавлении в модель изменений на ЭКГ ишемического генеза, курения, пожилого возраста и пониженного уровня ХС ЛВП. В других исследованиях показана более плотная связь ИМ с ФР, что дает перспективы вторичной профилактике, предупреждающей развитие его повторных эпизодов и сердечно-сосудистой смертности [17][18]. В нашем случае влияние модифицируемых ФР не столь значительно, за исключением курения, и даже повреждения миокарда, подтвержденные изменениями на ЭКГ, не являются критическими. В этом смысле, результаты проведенного многофакторного анализа согласуются с анализом кривых выживаемости Каплана-Мейера: потери выживаемости выявлены только в группах с ИМ и ИМ, сопровождающимся изменениями на ЭКГ.
Проблемы профилактики и лечения ИМ в общем одинаковы для всех стран. Среди этих проблем: недостаточные первичная профилактика или предупредительная работа с населением о ФР, недостаточная приверженность здоровому образу жизни и терапии у больных. Полученные результаты наводят на мысль и о недостаточности вторичной профилактики больных ИМ.
Ограничения исследования. Спектр лекарственных препаратов представлен не в надлежащем объеме, что не позволило оценить их влияние на ККТ.
Заключение
Следует подчеркнуть, что эпидемиология ССЗ вовсе не так уж далека “от народа”, как кажется иному врачу. Эпидемиологический подход позволяет выяснить неблагоприятные события в процессе медицинской деятельности и формулирует вопрос, ответ на который должен способствовать улучшению клинической практики.
Риск ККТ, включающий смерть от ССЗ и/или нефатальные ИМ, у россиян с ИМ в анамнезе, по нашим данным, существенно выше, чем в других странах, несмотря на более широкие критерии ИМ. Пока у пациента нет ИМ, состояние его здоровья определяют в основном поведенческие и биологические ФР. Следовательно, их своевременная коррекция средствами первичной профилактики может сохранить здоровье человека. Однако после возникновения ИМ приоритет оказывается у иных факторов воздействия, которые резко уменьшают шансы больного на жизнь. Для предотвращения повторного ИМ требуется применение иных методов, а именно, безотлагательной кардиореабилитации и вторичной профилактики. Как показали результаты данного исследования, потребность популяции в этих методах воздействия сохраняется высокой.
Благодарности. Авторы настоящего исследования выражают глубокую благодарность всем исполнителям в регионах за сбор материала для данной работы.
Отношения и деятельность: все авторы заявляют об отсутствии потенциального конфликта интересов, требующего раскрытия в данной статье.
Список литературы
1. Virani SS, Alonso A, Aparicio HJ, et al. Heart Disease and Stroke Statistics — 2021 Update: A Report From the American Heart Association. Circulation. 2021;143(8):e254-e743. doi:10.1161/CIR.0000000000000950.
2. Hashim MJ. Principles of family medicine and general practice-defining the five core values of the specialty. J Prim Health Care. 2016;8:283-7. doi:10.1071/HC16006.
3. Nowbar AN, Gitto M, Howard JP, et al. Mortality from ischemic heart disease: analysis of data from the World Health Organization and coronary artery disease risk factors from NCD Risk Factor Collaboration. Circ Cardiovasc Qual Outcomes. 2019;12:005375. doi:10.1161/CIRCOUTCOMES.118.005375.
4. Khan MA, Hashim MJ, Mustafa H, et al. Global Epidemiology of Ischemic Heart Disease: Results from the Global Burden of Disease Study. Cureus. 2020;12(7):e9349. doi:10.7759/cureus.9349.
5. Heidenreich PA, Trogdon JG, Khavjou OA, et al. Forecasting the Future of Cardiovascular Disease in the United States: A Policy Statement From the American Heart Association. Circulation. 2011;123(8):933-44. doi:10.1161/CIR.0b013e31820a55f5.
6. Greenlee RT, Naleway AL, Vidaillet H. Incidence of myocardial infarction in a general population: the Marshfield Epidemiologic Study Area. WMJ. 2002;101(7):46-52.
7. Thygesen K, Alpert JS, Jaffe AS, et al. ESC Scientific Document Group. Fourth universal definition of myocardial infarction (2018). Eur Heart J. 2019;40:237-69. doi:10.1093/eurheartj/ehy462.
8. Акимова Е.В., Гафаров В.В., Трубачева И.А. и др. Ишемическая болезнь сердца в Сибири: межпопуляционные различия. Сибирский медицинский журнал. 2011;26(3),1:153-7.
9. Piwońska A, Piwoński J, Szcześniewska D, et al. Population prevalence of electrocardiographic abnormalities: results of the Polish WAWKARD study. Kardiol Pol. 2019;77(9):859-67. doi:10.33963/KP.14911.
10. Прохода В.А. Оценка национальной системы здравоохранения жителями России и других европейских стран. Политика и Общество. 2018;10:65-77. doi:10.7256/2454-0684.2018.10.27654.
11. Dawber TR, Meadors GF, Moore Jr FE. Epidemiological approaches to heart disease: the Framingham Study. Am J Pub Health. 1951;41:279-86. doi:10.2105/ajph.41.3.279.
12. Kannel WB. Some lessons in cardiovascular epidemiology from Framingham. Am J Cardiol. 1976;37(2):269-82. doi:10.1016/0002-9149(76)90323-4.
13. Kish L. A procedure for objective respondent within households in phone surveys. J. Am. Statistical association. 1949;247:380-7.
14. Prineas RJ, Crow RS, Zhang ZM. The Minnesota Code Manual of Electrocardiographic Findings (Including Measurement and Comparison with the Novacode: Standards and Procedures for Measurement in Epidemiologic and Clinical Trials). 2nd. Springer; London. 2009:277-324. ISBN 978-1-84882-777-6. e-ISBN 978-1-84882-778-3. doi:10.1007/978-1-84882-778-3.
15. Бойцов С. А., Чазов Е. И., Шляхто Е. В. и др. Научно-организационный комитет проекта ЭССЕ-РФ. Эпидемиология сердечно-сосудистых заболеваний в различных регионах России (ЭССЕ-РФ), обоснование и дизайн исследования. Профилактическая Медицина. 2013;16(6):25-34.
16. Котова Е.Г., Кобякова О.С., Стародубов В.И. и др. Заболеваемость взрослого населения России в 2020 году с диагнозом, установленным впервые в жизни: статистические материалы. М.: ЦНИИОИЗ Минздрава России, 2021;164 с. ISBN 978-5-94116-040-2.
17. Denes P, Daniel B, Garside DB, et al. Major and Minor Electrocardiographic Abnormalities and their Association with Underlying Cardiovascular Disease and Risk Factors in Hispanics/Latinos (From the Hispanic Community Health Study/ Study of Latinos [HCHS/SOL]). Am J Cardiol. 2013;112(10):1667-75. doi:10.1016/j.amjcard.2013.08.004.
18. Pinto-Filho MM, Brant LCC, Foppa M, et al. Major Electrocardiographic Abnormalities According to the Minnesota Coding System Among Brazilian Adults (from the ELSA-Brasil Cohort Study). Am J Cardiol. 2017;119:2081e2087. doi:10.1016/j.amjcard.2017.03.043.
19. Silva M, Palhares D, Ribeiro L, et al. Prevalence of major and minor electrocardiographic abnormalities in one million primary care Latinos. J Electrocardiol. 2021;64:36-41. doi:10.1016/j.jelectrocard.2020.11.013.
20. Jayaraj JC, Davatyan K, Subramanian S, et al. Epidemiology of Myocardial Infarction. In. Pamukçu B. (ed.), Myocardial Infarction, IntechOpen, London 2018. doi:10.5772/intechopen.74768.
21. Hinton W, McGovern A, Coyle R, et al. Incidence and prevalence of cardiovascular disease in English primary care: a cross-sectional and follow-up study of the Royal College of General Practitioners (RCGP) Research and Surveillance Centre (RSC). BMJ Open. 2018;8:e020282. doi:10.1136/bmjopen-2017-020282.
22. Аметов А. С., Орлов В. А., Жестовский С. С. Особенности безболевой ишемии миокарда у больных инсулиннезависимым сахарным диабетом. Опыт применения персантина. Проблемы Эндокринологии. 1997;43(4):9-12. doi:10.14341/probl19974349-12.
23. Tamosiunas A, Petkeviciene J, Radisauskas R, et al. Trends in electrocardiographic abnormalities and risk of cardiovascular mortality in Lithuania, 1986–2015. BMC Cardiovascular Disorders. 2019;19:30. doi:10.1186/s12872-019-1009-3.
24. Давидович И. М., Малай Л. Н., Кутишенко Н.П. Отдаленные результаты и приверженность терапии у пациентов после острого инфаркта миокарда: данные регистра (Хабаровск). Клиницист. 2016/2017; 10/11(4):36-44. doi:10.17650/1818-8338-2016-10-4-36-44.
25. Марцевич С.Ю., Кутишенко Н.П., Сичинава Д. П. и др. Проспективный амбулаторный регистр больных, перенесших острый инфаркт миокарда (ПРОФИЛЬ-ИМ): дизайн исследования и первые результаты. Кардиоваскулярная терапия и профилактика. 2018;17(1):81-6. doi:10.15829/1728-8800-2018-1-81-86.
Об авторах
С. А. ШальноваРоссия
Шальнова Светлана Анатольевна — доктор медицинских наук, профессор, руководитель отдела эпидемиологии хронических неинфекционных заболеваний.
Москва.
Конфликт интересов:
Нет
О. М. Драпкина
Россия
Драпкина Оксана Михайловна — доктор медицинских наук, профессор, академик РАН, директор.
Москва.
Конфликт интересов:
Нет
В. А. Куценко
Россия
Куценко Владимир Александрович — младший научный сотрудник, лаборатория биостатистики, отдел эпидемиологии хронических неинфекционных заболеваний НМИЦ ТПМ МЗ РФ; аспирант, кафедра теории вероятностей, отделение математики, механико-математический факультет МГУ им. М.В. Ломоносова.
Москва.
Конфликт интересов:
Нет
А. В. Капустина
Россия
Капустина Анна Владимировна — старший научный сотрудник, отдел эпидемиологии хронических неинфекционных заболеваний.
Москва.
Конфликт интересов:
Нет
Г. А. Муромцева
Россия
Муромцева Галина Аркадьевна — кандидат биологических наук, ведущий научный сотрудник, отдел эпидемиологии хронических неинфекционных заболеваний.
Москва.
Конфликт интересов:
Нет
Е. Б. Яровая
Россия
Яровая Елена Борисовна — доктор физико-математических наук, профессор, руководитель лаборатории биостатистики, отдел эпидемиологии хронических неинфекционных заболеваний НМИЦ ТПМ МЗ РФ; доцент, кафедра теории вероятностей, Отделение математики, Механико-математический факультет МГУ им. М.В. Ломоносова.
Москва.
Конфликт интересов:
Нет
Ю. А. Баланова
Россия
Баланова Юлия Андреевна — кандидат медицинских наук, ведущий научный сотрудник, отдел эпидемиологии хронических неинфекционных заболеваний.
Москва.
Конфликт интересов:
Нет
С. Е. Евстифеева
Россия
Евстифеева Светлана Евгеньевна — кандидат медицинских наук, старший научный сотрудник, отдел эпидемиологии хронических неинфекционных заболеваний.
Москва.
Конфликт интересов:
Нет
А. Э. Имаева
Россия
Имаева Асия Эмверовна — кандидат медицинских наук, старший научный сотрудник, отдел эпидемиологии хронических неинфекционных заболеваний.
Москва.
Конфликт интересов:
Нет
Е. В. Шляхто
Россия
Шляхто Евгений Владимирович — доктор медицинских наук, профессор, академик РАН, генеральный директор.
Санкт-Петербург.
Конфликт интересов:
Нет
С. А. Бойцов
Россия
Бойцов Сергей Анатольевич — доктор медицинских наук, профессор, академик РАН, генеральный директор.
Москва.
Конфликт интересов:
Нет
З. Т. Астахова
Россия
Доктор медицинских наук, профессор, заведующая кафедрой внутренних болезней № 4.
Владикавказ.
Конфликт интересов:
Нет
О. Л. Барбараш
Россия
Доктор медицинских наук, профессор, член-корреспондент РАН, директор.
Кемерово.
Конфликт интересов:
Нет
О. A. Белова
Россия
Главный врач.
Иваново.
Конфликт интересов:
Нет
Ю. И. Гринштейн
Россия
Доктор медицинских наук, профессор, заведующий кафедрой терапии, Институт последипломного образования.
Красноярск.
Конфликт интересов:
Нет
А. Ю. Ефанов
Россия
Доктор медицинских наук, руководитель Центра международного образования, доцент кафедры кардиологии, кардиохирургии с курсом СМП.
Тюмень.
Конфликт интересов:
Нет
О. Н. Калачикова
Россия
Кандидат экономических наук, заместитель директора по научной работе, заведующая отделом исследования уровня и образа жизни населения.
Вологда.
Конфликт интересов:
Нет
Н. В. Кулакова
Россия
Кандидат медицинских наук, доцент института терапии и инструментальной диагностики.
Владивосток.
Конфликт интересов:
Нет
С. В. Недогода
Россия
Доктор медицинских наук, профессор, заведующий кафедрой терапии и эндокринологии факультета усовершенствования врачей.
Волгоград.
Конфликт интересов:
Нет
О. П. Ротарь
Россия
Доктор медицинских наук, главный научный сотрудник, НИЛ эпидемиологии неинфекционных заболеваний.
Санкт-Петербург.
Конфликт интересов:
Нет
И. А. Трубачева
Россия
Доктор медицинских наук, руководитель отделения популяционной кардиологии, заместитель директора по научно-организационной работе, НИИ кардиологии.
Томск.
Конфликт интересов:
Нет
Т. М. Черных от имени участников исследования ЭССЕ-РФ
Россия
Доктор медицинских наук, профессор, заведующий кафедрой госпитальной терапии и эндокринологии.
Воронеж.
Конфликт интересов:
Нет
Дополнительные файлы
Рецензия
Для цитирования:
Шальнова С.А., Драпкина О.М., Куценко В.А., Капустина А.В., Муромцева Г.А., Яровая Е.Б., Баланова Ю.А., Евстифеева С.Е., Имаева А.Э., Шляхто Е.В., Бойцов С.А., Астахова З.Т., Барбараш О.Л., Белова О.A., Гринштейн Ю.И., Ефанов А.Ю., Калачикова О.Н., Кулакова Н.В., Недогода С.В., Ротарь О.П., Трубачева И.А., Черных от имени участников исследования ЭССЕ-РФ Т.М. Инфаркт миокарда в популяции некоторых регионов России и его прогностическое значение. Российский кардиологический журнал. 2022;27(6):4952. https://doi.org/10.15829/1560-4071-2022-4952
For citation:
Shalnova S.A., Drapkina O.M., Kutsenko V.A., Kapustina A.V., Muromtseva G.A., Yarovaya E.B., Balanova Yu.A., Evstifeeva S.E., Imaeva A.E., Shlyakhto E.V., Boytsov S.A., Astakhova Z.T., Barbarash O.L., Belova O.A., Grinshtein Yu.I., Efanov A.Yu., Kalachikova O.N., Kulakova N.V., Nedogoda S.V., Rotar O.P., Trubacheva I.A., Chernykh on behalf of the ESSE-RF study participants. T.M. Myocardial infarction in the population of some Russian regions and its prognostic value. Russian Journal of Cardiology. 2022;27(6):4952. (In Russ.) https://doi.org/10.15829/1560-4071-2022-4952

















































