Перейти к:
Интенсификация липидснижающей терапии у пациентов очень высокого риска: возможности комбинации с ингибиторами PCSK9
https://doi.org/10.15829/1560-4071-2022-5030
Аннотация
Цель. Оценить у пациентов с очень высоким сердечно-сосудистым риском (ССР) эффективность и безопасность применения комбинированной липидснижающей терапии в составе с ингибитором PCSK9 на протяжении 6 мес. наблюдения.
Материал и методы. В проспективное открытое одноцентровое поисковое научное исследование с активным лечением включено 5 амбулаторных пациентов очень высокого ССР, имевших в 80% анамнез ишемической болезни сердца, 20% — заболевания периферических артерий, 60% — постинфарктный кардиосклероз. Главным критерием включения являлось недостижение целевых значений холестерина липопротеинов низкой плотности (ХС ЛНП) <1,4 ммоль/л на фоне высокоинтенсивной монотерапии статинами в максимально переносимых дозах или комбинированной терапии с эзетимибом. На регулярной основе все включенные пациенты принимали аторвастатин 40-80 мг/сут. или розувастатин 20-40 мг/сут., или питавастатин 2-4 мг/сут., 2 пациента получали статин в комбинации с эзетимибом 10 мг/сут. Наблюдение за пациентами осуществлялось на протяжении 6 мес.: каждые 2 нед. под контролем липидограммы выполнялись подкожные инъекции алирокумаба в дозе 150 мг/мл. Дополнительно оценивались клинические и лабораторные показатели безопасности терапии.
Результаты. Через 6 мес. на фоне применения комбинированной липидснижающей терапии с применением алирокумаба достигнуто снижение медиан ХС ЛНП с 4,3 (4,11-4,67) до 1,27 (1,06-1,47) (р=0,001) ммоль/л, общего холестерина с 6,1 (6-7) до 3,7 (3,5-3,9) (р=0,018) ммоль/л, индекса атерогенности с 3,2 (3-3,26) до 0,8% (0,8-1,5) (р=0,001). Достоверного снижения медианы триглицеридов и прироста медианы холестерина липопротеинов высокой плотности продемонстрировано не было. Применение липидснижающей терапии ингибитором PCSK9 у пациентов очень высокого риска в течение 6 мес. происходило без развития нежелательных явлений и позволило достигнуть максимального снижения ХС ЛНП в среднем на 75,4% уже к 4 мес. лечения в реальной клинической практике.
Заключение. Комбинированная липидснижающая терапия с применением алирокумаба 150 мг подкожно раз в 2 нед. в течение 6 мес. у пациентов очень высокого риска позволяет у большинства пациентов достигать целевых значений ХС ЛНП.
Ключевые слова
Для цитирования:
Седых Д.Ю., Кашталап В.В., Хрячкова О.Н., Петрова Т.С., Барбараш О.Л. Интенсификация липидснижающей терапии у пациентов очень высокого риска: возможности комбинации с ингибиторами PCSK9. Российский кардиологический журнал. 2022;27(6):5030. https://doi.org/10.15829/1560-4071-2022-5030
For citation:
Sedykh D.Yu., Kashtalap V.V., Khryachkova O.N., Petrova T.S., Barbarash O.L. Intensification of lipid-lowering therapy in very high-risk patients: potential of combination with PCSK9 inhibitors. Russian Journal of Cardiology. 2022;27(6):5030. (In Russ.) https://doi.org/10.15829/1560-4071-2022-5030
Контроль уровня атерогенных фракций липидов крови является одной из наиболее эффективных стратегий первичной и вторичной профилактики сердечно-сосудистых заболеваний, ассоциированных с атеросклерозом [1]. В качестве ключевой цели липидснижающей терапии рассматривается снижение до целевых значений показателя холестерина липопротеинов низкой плотности (ХС ЛНП), который является основным маркером кардиоваскулярного риска и ключевым фактором развития и прогрессирования атеросклеротических сердечно-сосудистых заболеваний [1][2]. Статины в максимально переносимых дозах остаются препаратами выбора для коррекции уровней атерогенных фракций липидов, однако достижение целевых показателей в реальной клинической практике составляет от 12 до 35%, в особенности среди пациентов с очень высоким и экстремальным сердечно-сосудистым риском (ССР) [3, 4]. Согласно рекомендациям Европейского общества кардиологов целевым уровнем ХС ЛНП для данной группы является показатель <1,4 ммоль/л и его снижение на 50% от исходного значения, однако на высокоинтенсивной монотерапии статинами только 32% пациентов достигают требуемого диапазона [1][5][6]. Такие результаты могут объясняться в т.ч. и инертностью врачей в отношении интенсификации липидснижающей терапии путем добавления второго компонента (прежде всего эзетимиба 10 мг/сут. — ингибитора абсорбции холестерина в кишечнике), недостаточной приверженностью самих пациентов к лечению, частым наличием не диагностированной генетически обусловленной семейной гиперхолестеринемии или ложной или истинной непереносимости статинов, требующих осторожности при выборе высокоинтенсивной статинотерапии [6].
В связи с этим крайне актуальным является внедрение в реальную клиническую практику эффективных медикаментозных технологий интенсификации липидснижающей терапии, обеспечивающих высокую приверженность пациентов к назначенному лечению. Перспективным в этом отношении является использование моноклональных антител к ферменту пропротеиновой конвертазе субтилизин-кексин типа 9 (PCSK9) [7]. Фармакологические эффекты данной группы лекарственных препаратов обусловлены ингибированием белка PCSK9, основная функция которого заключается в мобилизации клеточных рецепторов к ХС ЛНП, способствуя тем самым снижению этой атерогенной фракции липидов, а также дополнительно приводя к уменьшению уровней аполипопротеина В, холестерина липопротеинов не высокой плотности, триглицеридов (ТГ), липопротеина (а) [8][9].
Согласно действующим клиническим рекомендациям, инициация терапии ингибиторами PCSK9 является целесообразной при неэффективности двойной схемы липидснижающей терапии (высокоинтенсивный статин в максимально переносимой дозе + эзетимиб) в течение 4-6 нед. приема, а также при исходно тяжелых нарушениях липидного обмена и очень высоком ССР (ХС ЛНП >4,9 ммоль/л) [1]. Такая “тройная” терапия позволяет снизить исходный уровень ХС ЛНП на 85%, однако нерешенные вопросы с оплатой дорогостоящей медикаментозной терапии, наряду с опасениями врачей о безопасности и эффективности длительной высокоинтенсивной комбинированной липидснижающей терапии, ограничивают ее более широкое использование [10]. Ингибиторы PCSK9 обладают исходно высокой селективностью в отношении мишени для лекарственного воздействия, являются полностью человеческими моноклональными антителами. Эффективность и безопасность применения ингибиторов PCSK9 доказана в рандомизированных клинических исследованиях [11-14]. Для выполнения поискового научного исследования (ПНИ) в реальной клинической практике выбран алирокумаб.
Цель исследования — на протяжении 6 мес. наблюдения оценить у пациентов с очень высоким ССР эффективность и безопасность применения комбинированной липидснижающей терапии с ингибитором PCSK9 в составе.
Материал и методы
Настоящее исследование было выполнено в соответствии с Хельсинкской декларацией Всемирной медицинской ассоциации “Этические принципы проведения научных медицинских исследований с участием человека”.
Финансирование программы ПНИ осуществлялось Министерством науки и высшего образования Российской Федерации. Протокол ПНИ был разработан научными сотрудниками учреждения и одобрен Локальным этическим комитетом учреждения.
Критериями включения пациентов в работу были: 1) наличие подписанного информированного добровольного согласия для участия в ПНИ; 2) возраст пациента старше 18 лет; 3) документированные тяжелые нарушения липидного обмена (ХС ЛНП >3,5 ммоль/л) на фоне длительной (более года) высокоинтенсивной статинотерапии (аторвастатин 40- 80 мг/сут., розувастатин 20-40 мг/сут. или их комбинация с эзетимибом 10 мг/сут., ранее не лечившиеся ингибиторами PCSK9); 5) наличие у пациента очень высокого ССР; 6) отсутствие индивидуальной непереносимости и/или противопоказаний к применению ингибиторов PCSK9.
В исследование не включались пациенты: 1) не подписавшие информированное добровольное согласие для участия в ПНИ; 2) пациенты с “низкой” ожидаемой продолжительностью жизни (до 1 года) ввиду наличия тяжелой сопутствующей соматической патологии без возможности компенсации.
Исследование проспективное, с активным лечением, одноцентровое, разослепленное, без группы плацебо. Всего в рамках исследования были включены 5 пациентов. Все пациенты характеризовались большой частотой факторов риска и очень высоким ССР (табл. 1).
Таблица 1
Исходная клинико-анамнестическая характеристика пациентов (n=5)
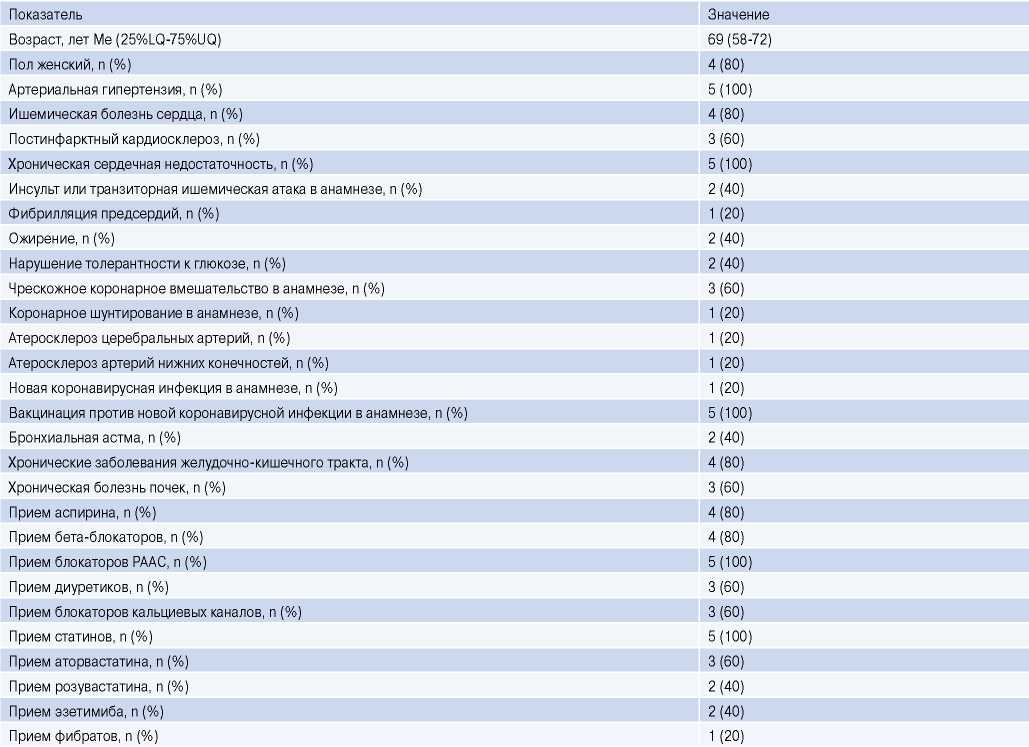
Сокращение: РААС — ренин-ангиотензин-альдостероновая система.
Дизайн исследования подразумевал выполнение подкожных инъекций препарата алирокумаб в дозе 150 мг/мл 2 раза в мес. на протяжении полугода. На каждом визите врачом-исследователем акцентировалось внимание пациента на основных аспектах немедикаментозной коррекции дислипидемий и необходимости приверженности лечению. На визите включения до введения препарата оценивались клинико-анамнестические характеристики пациентов, забирались образцы крови для выполнения развернутой липидограммы (общего холестерина (ОХС), ХС ЛНП, липопротеинов высокой плотности (ХС ЛВП), ТГ, индекса атерогенности (ИА)), после чего препарат вводился пациентам. На последующих визитах с временным интервалом через 2 нед. в течение 6 мес. до проведения инъекции пациенту выполнялась динамическая оценка нежелательных явлений (клинические проявления и лабораторные изменения профиля безопасности (ферментов цитолиза, креатинкиназы и креатинина) по медицинской документации) и повторный забор липидограммы.
Статистическая обработка всех данных, получаемых в исследовании, производилась с помощью программы STATISTICA версии 10.0 компании StatSoft Inc (США). При создании первичной базы данных применялась программа Microsoft Office Excel 2007 (США). Характер распределения выборки проверялся с помощью критерия Шапиро-Уилка. Качественные признаки в исследовании представлены в виде абсолютных (n) и относительных частот (%), для количественных признаков указывались медианы значений (Ме) и нижняя и верхняя квартили (25%-75%). Достоверность различий между количественными признаками определялась с помощью критерия Манна-Уитни. Уровнем критической значимости (р) считали значения <0,05.
Результаты
Исходные значения липидограммы крови, а также ее динамика через 2 нед. и после инъекции алирокумаба представлены в таблице 2. Развития нежелательных явлений на фоне терапии за период 6 мес. не зарегистрировано.
Таблица 2
Динамика липидограммы у пациентов исследования (n=5)
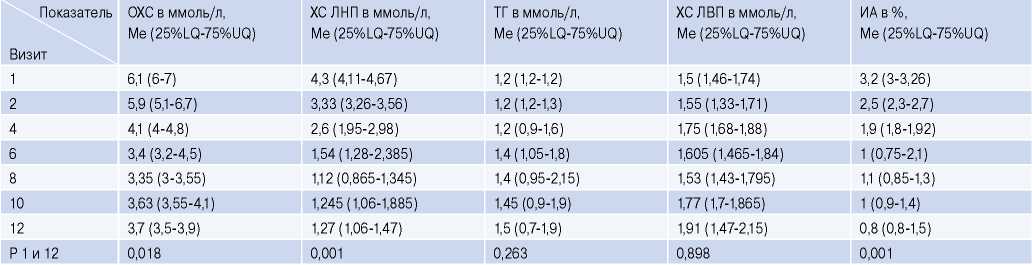
Сокращения: ИА — индекс атерогенности, ОХС — общий холестерин, ХС ЛНП — холестерин липопротеинов низкой плотности, ХС ЛВП — холестерин липопротеинов высокой плотности, ТГ — триглицериды, Р — достоверность различий.
В ходе проведения ПНИ продемонстрировано достоверное снижение ОХС, ХС ЛНП, ИА без статистически значимых изменений уровней ТГ и ХС ЛВП. Максимально низкие уровни ОХС, ХС ЛНП, ИА были достигнуты к 4 мес. (8 визиту) комбинированной терапии. Максимальное снижение ХС ЛНП составило в среднем на 75,4%, снижение ОХС — на 44,6%, ИА — на 69%.
Таким образом, снижение уровня ХС ЛНП составило 75,4% от исходного уровня на фоне терапии статинами или их комбинации с эзетимибом. В соответствии с актуальными рекомендациями всем пациентам удалось достичь целевого уровня ХС ЛНП (<1,4 ммоль/л). Результаты подтверждают высокую эффективность введения алирокумаба на протяжении 6 мес., помимо приема высокоинтенсивной терапии статинами или двойной их комбинации с эзетимибом. Следует также сказать, что среди участников на протяжении всего периода исследования не отмечались лабораторные изменения профиля безопасности (превышение 3 верхних границ норм аспартатаминотрансферазы и аланинаминотрансферазы, 10 верхних границ норм креатинкиназы, нарастания уровня креатинина), а также не регистрировались местные кожные реакции и новые случаи развития сахарного диабета. Все участники исследования в последующем были направлены на консультацию в региональный липидный центр, где им определены показания для продолжения приема алирокумаба, оформлены документы для адресной помощи по поводу тяжелого течения основного заболевания по жизненным показаниям, 2 пациента получили квоту для дальнейшей терапии ингибиторами PCSK9.
Обсуждение
В настоящей работе, несмотря на длительный прием пациентами высоких доз статинов или их комбинации с эзетимибом, не было достигнуто целевых значений ХС ЛНП. Включение участников очень высокого ССР в наше исследование позволило уже через 4 мес. превысить средний порог снижения ХС ЛНП, составляющий 62,7% в многоцентровом исследовании ODYSSEY [12]. Результаты аналогичные полученным нами продемонстрированы авторами исследования по оценке эффективности комбинированной липидснижающей терапии с алирокумабом в составе в течение 3 мес. [13]. Опубликованы работы, в которых было показано, что терапия алирокумабом предотвращает развитие острого коронарного синдрома, а также новых случаев острого нарушения мозгового кровообращения и транзиторных ишемических атак при исходно высоком уровне ХС ЛНП; в нашем исследовании у пациентов не было острых событий за период лечения, несмотря на очень высокий ССР у пациентов [10][14][15]. При этом все пациенты нашего исследования достигли целевого уровня ХС ЛНП, тогда как в другом исследовании со схожим дизайном частота “достигших” целевых значений ХС ЛНП составила 77,8% [10].
Следует отметить, что в настоящее время не получено доказательств эффективности и безопасности изолированного или комбинированного со статинами назначения ингибиторов PCSK9 в случаях умеренного и низкого ССР у пациентов, что связано с критериями отбора имеющихся исследований и требует дальнейшего изучения [16]. Анализ результатов 14 исследований выявил высокую безопасность комбинированной терапии с применением алирокумаба независимо от наличия или отсутствия у пациентов коморбидных состояний [11][12][14]. Пролонгированная 78-нед. терапия алирокумабом в исследовании ODYSSEY LONG TERM не сопровождалась увеличением частоты нежелательных явлений [17]. Эти данные полностью сопоставимы результатам, представленным в нашем исследовании. В другом исследовании — ODYSSEY APPRISE у пациентов с семейной гиперхолестеринемией, продолжительность применения алирокумаба составила 72,4 нед. Были выявлены только неспецифические нежелательные явления (назофарингит (7,8%), миалгия (7,1%) и головная боль (6,2%)) [18]. Метаанализ 30 рандомизированных исследований с участием 59026 пациентов, в которых алирокумаб или эволокумаб сравнивали с плацебо на фоне назначения таблетированной липидснижающей терапии, не выявил различий в отношении частоты прекращения лечения, системных аллергических реакций, значимых нейрокогнитивных нарушений, офтальмологических явлений, а также новых проявлений или ухудшения течения ранее существовавшего сахарного диабета [19].
Дальнейшая разработка технологий лекарственного снижения PCSK9, с меньшей частотой введения, более эффективных в отношении снижения ХС ЛНП и доступных по фармакоэкономическим показателям, чем использование моноклональных антител, является актуальной задачей современной медицинской науки и фарминдустрии для повышения доступности среди лиц, нуждающихся в коррекции тяжелых проявлений дислипидемии [20-22].
Заключение
Комбинированная липидснижающая терапия с применением алирокумаба 150 мг подкожно раз в 2 нед. в течение 6 мес. у пациентов очень высокого риска позволяет у большинства пациентов достигать целевых значений ХС ЛНП. Изученная “тройная” комбинация липидснижающих препаратов может быть рекомендована для внедрения в реальную клиническую практику медицинских учреждений, оказывающих стационарную и амбулаторную помощь пациентам очень высокого ССР с отсутствием достижения рекомендуемых параметров липидограммы на фоне стандартной таблетированной холестеринснижающей терапии.
Отношения и деятельность: все авторы заявляют об отсутствии потенциального конфликта интересов, требующего раскрытия в данной статье.
Список литературы
1. Диагностика и коррекция нарушений липидного обмена с целью профилактики и лечения атеросклероза. Российские рекомендации, VII пересмотр. Атеросклероз и дислипидемии. 2020;1(38):7-41. doi:10.34687/2219-8202.JAD.2020.01.0002.
2. Chapman MJ, Stock JK, Ginsberg HN. PCSK9 inhibitors and cardiovascular disease: heralding a new therapeutic era. Curr. Opin. Lipidol. 2015;26:511-20. doi:10.1097/MOL.0000000000000239.
3. Оганов Р. Г., Кухарчук В. В., Арутюнов Г. П. и др. Сохраняющиеся нарушения показателей липидного спектра у пациентов с дислипидемией, получающих статины, в реальной клинической практике в Российской Федерации (российская часть исследования DYSIS). Кардиоваскулярная терапия и профилактика. 2012;11(4):70-8. doi:10.15829/1728-8800-2012-4-70-78.
4. Stock JK. DA VINCI study: Change in approach to cholesterol management will be needed to reduce the implementation gap between guidelines and clinical practice in Europe. Atherosclerosis. 2020;314:74-6. doi:10.1016/j.atherosclerosis.2020.09.023.
5. Mach F, Baigent C, Catapano AL, et al. ESC Scientific Document Group. 2019 ESC/EAS Guidelines for the management of dyslipidaemias: lipid modification to reduce cardiovascular risk. Eur Heart J. 2020;41(1):111-88. doi:10.1093/eurheartj/ehz455.
6. De Backer G, Jankowski P, Kotseva K, et al. Management of dyslipidaemia in patients with coronary heart disease: Results from the ESC-EORP EUROASPIRE V survey in 27 countries. Atherosclerosis. 2019;285:135-46. doi:10.1016/j.atherosclerosis.2019.03.014.
7. Agabiti R, Salvetti M. Management of Hypercholesterolemia, Appropriateness of Therapeutic Approaches and New Drugs in Patients with High Cardiovascular Risk. High Blood Press Cardiovasc Prev. 2016;23(3):217-30. doi:10.1007/s40292-016-0155-2.
8. Roth EM, Davidson MH. PCSK9 inhibitors: mechanism of action, efficacy, and safety. Rev Cardiovasc Med. 2018;19(S1):S31-46.
9. Steg PG, Szarek M, Bhatt DL, et al. Effect of alirocumab on mortality after acute coronary syndromes. Circulation. 2019;140(2):103-12. doi:10.1161/CIRCULATIONAHA.118.038840.
10. Корнева В. А., Кузнецова Т. Ю., Скопец И. С. и др. Опыт применения ингибитора PCSK9 алирокумаба у пациентов экстремально высокого сердечно-сосудистого риска. Кардиология. 2020;60(8):71-7. doi:10.18087/cardio.2020.8.n1046.
11. Blom DJ, Harada-Shiba M, Rubba P, et al. Efficacy and Safety of Alirocumab in Adults With Homozygous Familial Hypercholesterolemia: The ODYSSEY HoFH Trial. J Am Coll Cardiol. 2020;76(2):131-42. doi:10.1016/j.jacc.2020.05.027.
12. Schwartz GG, Steg PG, Szarek M, et al. Alirocumab and cardiovascular outcomes after acute coronary syndrome. N Engl J Med. 2018;379:2097-107. doi:10.1056/NEJMoa1801174.
13. Steffens D, Bramlage P, Müller J, et al. Intensified lipid-lowering treatment with alirocumab in patients with coronary heart disease. Open Heart. 2021;8(1):e001572. doi:10.1136/openhrt-2021-001572.
14. Leiter LA, Tinahones FJ, Karalis DG, et al. Alirocumab safety in people with and without diabetes mellitus: pooled data from 14 ODYSSEY trials. Diabet Med. 2018;35(12):1742-51. doi:10.1111/dme.13817.
15. Della PG, Bozzetto L, Annuzzi G, et al. Alirocumab for the treatment of hypercholesterolaemia. Expert Rev Clin Pharmacol. 2017;10(6):571-82. doi:10.1080/17512433.2017.1318063.
16. Schmidt AF, Carter JL, Pearce LS, et al. PCSK9 monoclonal antibodies for the primary and secondary prevention of cardiovascular disease. Cochrane Database Syst Rev. 2020;10(10):CD011748. doi:10.1002/14651858.CD011748.pub3.
17. Tomlinson B, Hu M, Zhang Y, et al. Alirocumab for the treatment of hypercholesterolemia. Expert Opin Biol Ther. 2017;17(5):633-43. doi:10.1080/14712598.2017.1305354.
18. Gaudet D, López-Sendón JL, Averna M, et al. Safety and efficacy of alirocumab in a real-life setting: the ODYSSEY APPRISE study. Eur J Prev Cardiol. 2022;28(17):1864-72. doi:10.1093/eurjpc/zwaa097.
19. Guedeney P, Sorrentino S, Giustino G, et al. Indirect comparison of the efficacy and safety of alirocumab and evolocumab: a systematic review and network meta-analysis. European Heart Journal — Cardiovascular Pharmacotherapy. 2021;7(3):225-35. doi:10.1093/ehjcvp/pvaa024.
20. Preiss D, Mafham M. PCSK9 inhibition: the dawn of a new age in cholesterol lowering? Diabetologia. 2017;60(3):381-9. doi:10.1007/s00125-016-4178-y.
21. Чаулин А. М. Новые группы гиполипидемических препаратов, основанные на ингибировании пропротеиновой конвертазы субтилизин-кексинового типа 9 (PCSK9). Часть 1. Клиническая медицина. 2020;98(11-12):739-44. doi:10.30629/0023-2149-2020-98-11-12-739-744.
22. Федорова Н. В., Седых Д. Ю., Кашталап В. В. и др. Интенсификация липидснижающей терапии у пациентов с острым коронарным синдромом на госпитальном этапе (клиническое наблюдение). Комплексные проблемы сердечно-сосудистых заболеваний. 2019;8(4S):121-9. doi:10.17802/2306-1278-2019-8-4S-121-129.
Об авторах
Д. Ю. СедыхРоссия
Седых Дарья Юрьевна — кандидат медицинских наук, научный сотрудник лаборатории патологии кровообращения отдела клинической кардиологии.
Кемерово.
Конфликт интересов:
Нет
В. В. Кашталап
Россия
Кашталап Василий Васильевич — доктор медицинских наук, доцент, заведующий отделом клинической кардиологии.
Кемерово.
Конфликт интересов:
Нет
О. Н. Хрячкова
Россия
Хрячкова Оксана Николаевна — кандидат биологических наук, младший научный сотрудник лаборатории геномной медицины отдела экспериментальной медицины.
Кемерово.
Конфликт интересов:
Нет
Т. С. Петрова
Россия
Петрова Татьяна Сергеевна — аспирант.
Кемерово.
Конфликт интересов:
Нет
О. Л. Барбараш
Россия
Барбараш Ольга Леонидовна — доктор медицинских наук, профессор, член-корреспондент Российской академии наук, директор.
Кемерово.
Конфликт интересов:
Нет
Дополнительные файлы
Рецензия
Для цитирования:
Седых Д.Ю., Кашталап В.В., Хрячкова О.Н., Петрова Т.С., Барбараш О.Л. Интенсификация липидснижающей терапии у пациентов очень высокого риска: возможности комбинации с ингибиторами PCSK9. Российский кардиологический журнал. 2022;27(6):5030. https://doi.org/10.15829/1560-4071-2022-5030
For citation:
Sedykh D.Yu., Kashtalap V.V., Khryachkova O.N., Petrova T.S., Barbarash O.L. Intensification of lipid-lowering therapy in very high-risk patients: potential of combination with PCSK9 inhibitors. Russian Journal of Cardiology. 2022;27(6):5030. (In Russ.) https://doi.org/10.15829/1560-4071-2022-5030

















































