МИОКАРДИТ, ЭНДОКАРДИТ И КАРДИОМИОПАТИИ
- У трети пациентов с синдромом первичной гипертрофии миокарда диагностирован сопутствующий миокардит.
- Частота сопутствующего миокардита максимальна при AL-амилоидозе (50%) и гипертрофической кардиомиопатии в сочетании с некомпактным миокардом левого желудочка (40%).
- Наличие сопутствующего миокардита приводит к прогрессированию сердечной недостаточности, усугублению желудочковых нарушений ритма и увеличению риска внезапной сердечной смерти.
- Назначение иммуносупрессивной терапии миокардита позволяет стабилизировать состояние пациентов с синдромом первичной гипертрофии миокарда.
Цель. Оценить частоту миокардита у пациентов с синдромом первичной гипертрофии миокарда и изучить его вклад в течение заболевания.
Материал и методы. В исследование вошли 100 пациентов с первичной гипертрофией миокарда левого желудочка, 52 мужчины и 48 женщин, средний возраст 51,5±15,7 лет, срок наблюдения 10,4 [2,1; 36,1] мес. Всем пациентам выполнены: электрокардиография, суточное мониторирование электрокардиограммы, эхокардиография, а также ДНК-диагностика (n=96), морфологическое исследование миокарда (n=29), магнитно-резонансная томография сердца (n=31), мультиспиральная компьютерная томография сердца (n=26), определение титров антикардиальных антител (n=43), количественное определение свободных лёгких цепей иммуноглобулинов в сыворотке крови и в моче методом иммунофиксации (n=10); сцинтиграфия миокарда с 99mTcпирофосфатом (n=5); биопсия слизистой прямой кишки и/или подкожной жировой клетчатки на амилоид (n=9).
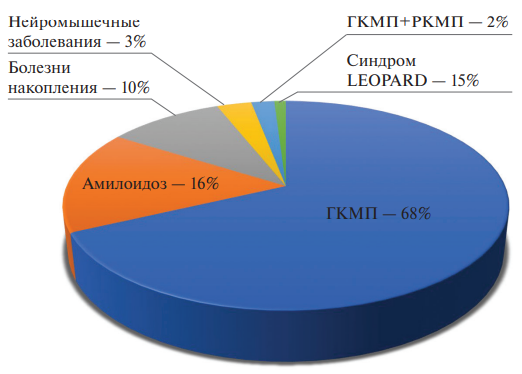
Результаты. У 68% была диагностирована истинная (саркомерная) гипертрофическая кардиомиопатия (ГКМП), у 16% — амилоидоз с поражением сердца, у 10% — болезни накопления, у 3% — нейромышечные заболевания, у 2% гипертрофия миокарда сочеталась с выраженной рестрикцией (смешанный фенотип), а у 1% — синдром LEOPARD. Сопутствующий миокардит диагностирован у 30% больных. При ГКМП миокардит выявлен в 31% случаев, у этих пациентов были достоверно выше функциональный класс сердечной недостаточности (хроническая сердечная недостаточность, 3 [2; 3] vs 2 [1; 3], p=0,026) и смертность (33,3% vs 6,4%, р=0,01). При амилоидозе частота миокардита составила 31,3%, у этих пациентов достоверно чаще наблюдалась желудочковая тахикардия: 80,0% vs 18,2%, р=0,036. Частота сопутствующего миокардита в подгруппе болезней накопления составила 30%: у 2 пациентов с болезнью Фабри и у 1 пациентки с болезнью Данона. Из трех пациентов с нейромышечными заболеваниями миокардит был диагностирован у 1, а в подгруппах с рестриктивным фенотипом и синдромом LEOPARD случаев миокардита зафиксировано не было. Лечение миокардита позволяло стабилизировать состояние пациентов.
Заключение. Наличие сопутствующего миокардита приводило к прогрессированию сердечной недостаточности, усугублению желудочковых нарушений ритма и как следствие увеличению риска внезапной сердечной-смерти, а также повышало вероятность летального исхода. Необходимо активно диагностировать и лечить миокардит у пациентов с синдромом первичной гипертрофии миокарда и в состоянии декомпенсации.
- Значительная вариабельность показателей смертности от алкогольной кардиомиопатии (код I42.6) может быть обусловлена дискуссионными вопросами диагностики и определения первоначальной причины смерти.
- В статье представлены фактические данные и проблемы их интерпретации.
- Предлагается создать междисциплинарный консенсус по вопросам заполнения медицинских свидетельств о смерти.
Алкогольная кардиомиопатия (АКМП) считается самостоятельным заболеванием, диагностика которого основана в большой степени на анамнезе злоупотребления алкоголем и исключении других причин кардиомиопатии.
Цель. Обсудить учет и корректность анализа смертности от АКМП, в т.ч. оценить вариабельность и динамику региональных стандартизованных коэффициентов смертности (СКС) за 2013-2021гг; провести анализ медицинских свидетельств о смерти (МСС) и обсудить критерии указания АКМП в качестве первоначальной причины смерти (ППС).
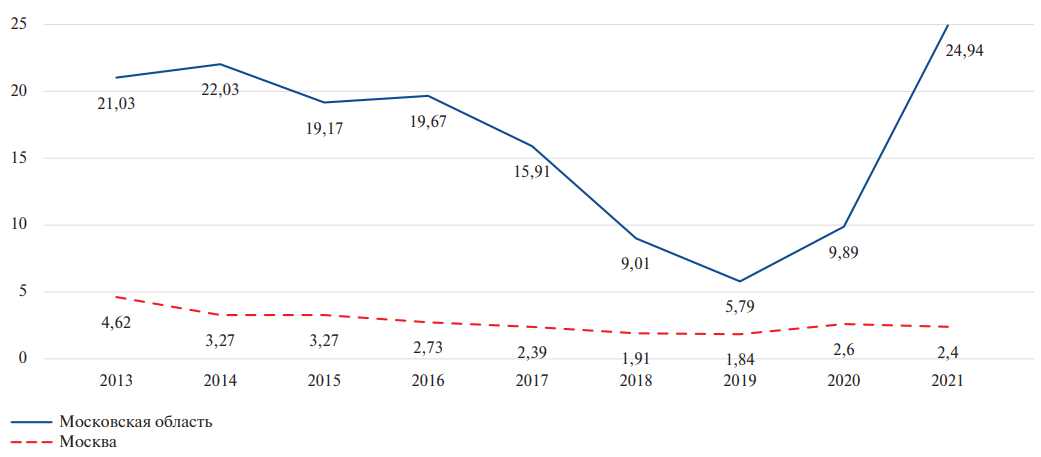
Материал и методы. Данные Росстата о среднегодовой численности населения и числе умерших от АКМП (I42.6) в 2013-2021гг по регионам. СКС рассчитывались с помощью программного обеспечения. Для анализа МСС использованы обезличенные данные Главного управления ЗАГС Московской области (всего 3538 МСС).
Результаты. В 2013г среднерегиональный СКС от АКМП составил 14,0±13,9 на 100 тыс. населения, в 2021г — 13,2±13,6. Единственный регион, в котором ежегодно отмечалось снижение СКС — Тюменская область. Нулевые значения зарегистрированы в республиках Ингушетия и Чечня. В остальных регионах отмечена "волнообразная" динамика — снижение или увеличение СКС. Коэффициент вариации СКС был минимальным в 2016г — 73% и максимальным в 2021г — 103%. Вклад в смертность варьировал от 0 до 6%. В качестве непосредственной причины смерти в 93,3% МСС указаны коды группы сердечной недостаточности (I50). Часть II МСС была заполнена в 39,1%; наиболее частой причиной, способствующей смерти, указаны коды группы F10 (психические расстройства, вызванные употреблением алкоголя) и коды группы К70 (алкогольная болезнь печени). В литературе и рекомендациях нет четких критериев АКМП как ППС, а указание кодов, связанных с алкоголем в части II МСС противоречит правилам Международной классификации болезней 10-го пересмотра.
Заключение. Значительная региональная вариабельность СКС от АКМП может быть обусловлена проблемами определения ППС, и несмотря на небольшой вклад АКМП в смертность от всех причин, необходим консенсус специалистов по критериям диагностики и заполнения МСС.
- Не подтверждено развитие коронавирус-ассоциированного миокардита ни у одного пациента в постостром периоде коронавирусной инфекции. Кардиальные симптомы постковидного синдрома могут быть следствием ремоделирования миокарда.
- При иммуногистохимическом исследовании экспрессия spike protein SARS-CoV-2 отмечена на клетках воспалительного инфильтрата в ткани миокарда и на эндотелии единичных сосудов, но не подтверждена с помощью полимеразной цепной реакции.
- По данным эндомиокардиальной биопсии морфологические проявления постковидного синдрома связаны с увеличением количества CD68+-макрофагов в миокарде. Увеличение M2-макрофагов может указывать на репарацию миокарда после повреждения ткани в остром периоде коронавирусной инфекции.
Цель. Охарактеризовать клинические проявления и морфологические изменения в миокарде у пациентов с сердечно-сосудистыми осложнениями постковидного синдрома.
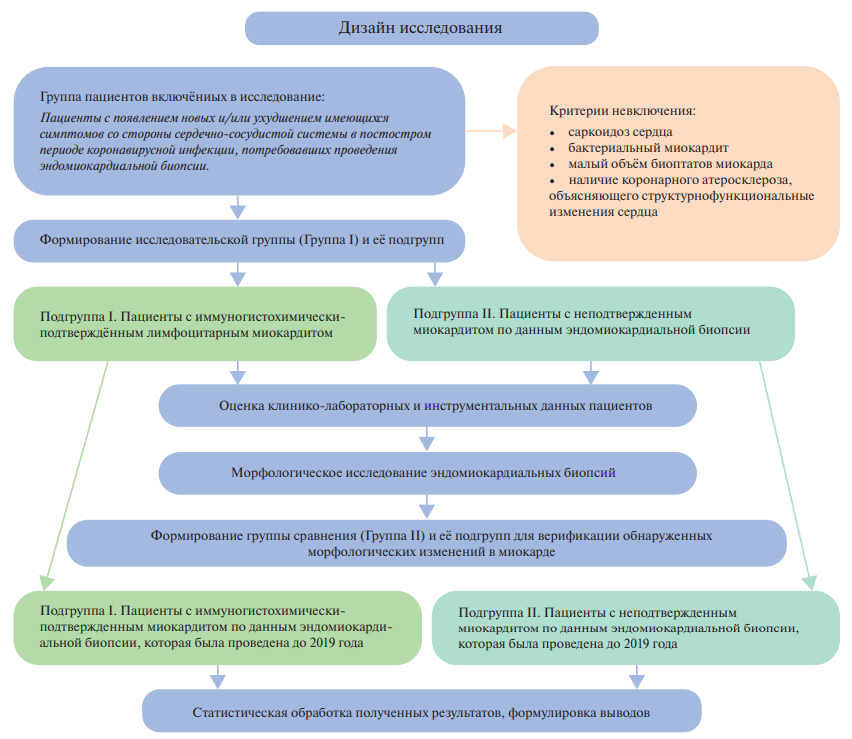
Материал и методы. 38 пациентам (I группа) с кардиальными симптомами в постковидном периоде выполнена эндомиокардиальная биопсия (ЭМБ). Больных из I группы разделили на 2 подгруппы в зависимости от наличия или отсутствия морфологически подтвержденного миокардита. Для морфологического сравнения сформирована II группа (41 пациент с выполненной ЭМБ до 2019г, не переносивший COVID-19). II группа также разделена на две подгруппы с и без морфологически подтвержденного миокардита. Помимо анализа клинических, лабораторных и инструментальных данных, проведено гистологическое и иммуногистохимическое исследование ткани миокарда с антителами к CD3, CD68, CD16, HLA-DR, MНC1, C1q, VP1 энтеровируса, spike protein SARS-CoV-2, АПФ2, Ang1, фактору Виллебранда, VEGF и ПЦР-исследование ткани миокарда после обратной транскрипции. Дополнительно выполнялось иммунофлюоресцентное исследование ткани миокарда с использованием коктейлей антител spike protein SARS-CoV-2/ CD16, spike protein SARS-CoV-2/CD68, CD80/CD163. Статистическая обработка выполнялась с использованием библиотек NumPy, SciPy, Pandas и Matplotlib на языке программирования Python.
Результаты. Среди пациентов I группы 65% имели морфологически доказанный лимфоцитарный миокардит (1 подгруппа, n=29). 35% пациентов не имели признаков воспалительных изменений в миокарде (2 подгруппа, n=9). Группа сравнения (II группа) включала 33 пациента с миокардитом (80%) и 8 пациентов (20%) без него. Отмечена выраженная экспрессия CD68+-макрофагов в ткани миокарда у пациентов с постковидным синдромом в сравнении со II группой как имеющих морфологические критерии миокардита (p=0,014), так и без них (p=0,007), преимущественно за счёт M2 макрофагов. Более выраженная экспрессия CD68+-макрофагов наблюдалась при выполнении ЭМБ на более ранних сроках. В случае выявления в I группе spike protein SARS-CoV-2 на эндотелии и воспалительном инфильтрате иммуногистохимическим методом выполнялась ПЦР ткани миокарда на SARS-CoV-2 (n=5), которая не выявила вирусных частиц SARS-CoV-2 ни в одном из анализируемых образцов.
Заключение. Кардиальные симптомы постковидного синдрома обусловлены ремоделированием миокарда, в т.ч. и у пациентов без морфологически подтвержденного миокардита. Не доказано прямое участие SARS-CoV-2 в развитии миокардита в постостром периоде COVID-19.
- Фибрилляция предсердий (ФП) как одна из наиболее частых устойчивых предсердных тахиаритмий в популяции продемонстрировала относительно низкую распространенность у пациентов с дилатационной кардиомиопатией (ДКМП) в долгосрочном периоде наблюдения по сравнению с частотой желудочковых тахиаритмий (27,8% vs 60,4%; р=0,0001).
- Среди факторов риска в структуре негативного ремоделирования сердца у пациентов с ДКМП определены независимые предикторы ФП: атриальная дромотропная дисфункция (межпредсердная блокада), сократительная дисфункция правого желудочка (снижение TAPSE) и повышенная частота сердечных сокращений на фоне терапии.
- Развитие устойчивых форм ФП у пациентов с ДКМП ассоциировано с 4-кратным повышением риска сердечно-сосудистой смерти, вероятность летального исхода в 6-летнем периоде составляет 80%.
Цель. Изучение эпидемиологического профиля фибрилляции предсердий (ФП) с долгосрочной оценкой прогностической значимости ФП как фактора риска неблагоприятных клинических исходов у пациентов с дилатационной кардиомиопатией (ДКМП).
Материал и методы. В исследование включили 270 пациентов с ДКМП (206/76,3% мужчин, возраст 47 [37; 56] лет, фракция выброса левого желудочка (ЛЖ) 29 [21; 35]%). Период наблюдения составил 6 лет (Ме 76 [57; 119] мес.). Для оценки влияния ФП на прогноз ДКМП проведены процедуры Каплан-Мейера и Кокс-регрессионный анализ клинических исходов, включающих сердечно-сосудистую смерть, трансплантацию сердца, имплантацию вспомогательного желудочкового устройства.
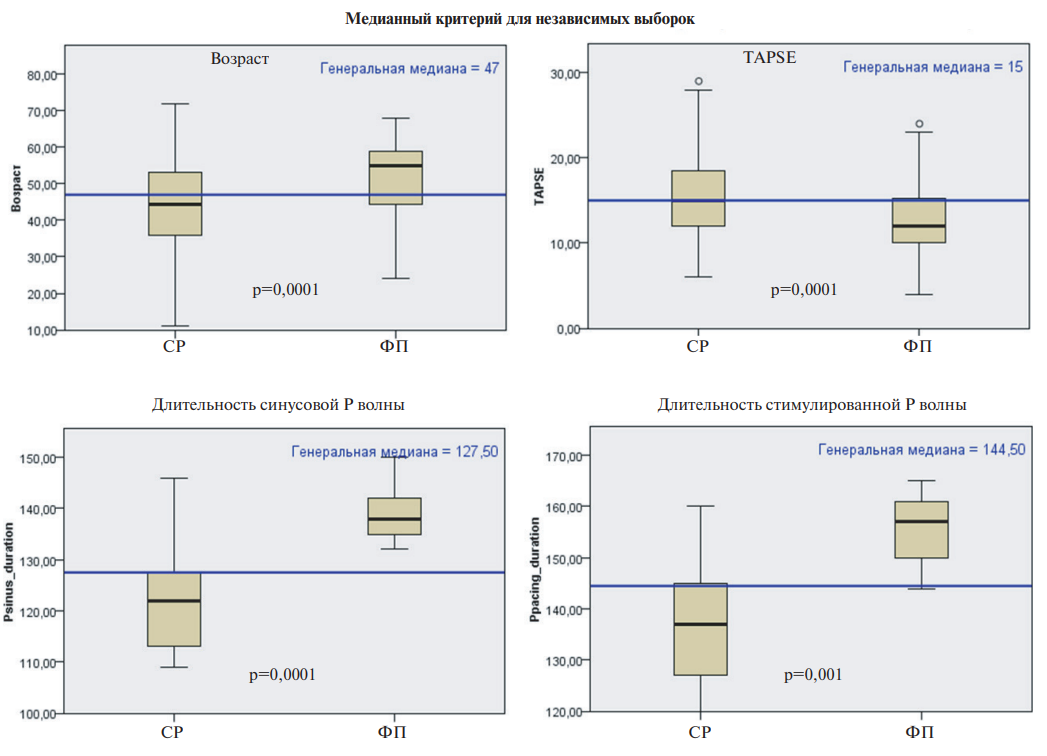
Результаты. Из 270 пациентов с ДКМП у 10 (3,7%) лиц выявлена пароксизмальная ФП (исходно 5/1,85% и в течение первого года наблюдения 5/1,85%), через 5 лет ещё у 65 (24,1%) лиц наблюдалась ФП (пароксизмальная, персистирующая или перманентная). Желудочковые тахиаритмии зарегистрированы у 163 (60,4%). По сравнению с пациентами, сохранившими синусовый ритм, пациенты с ФП были старше (51,4±10 vs 43,6±13 лет, p=0,001), имели более низкую толерантность к нагрузке (тест 6-минутной ходьбы: 379±45 vs 445±43 м; р=0,0002) и более высокий функциональный класс сердечной недостаточности (функциональный класс IIIIV по NYHA: 38/50,7% vs 52/26,7%; χ2=13,6; p=0,0003); у пациентов с ФП наблюдались исходно более выраженные проявления сократительной дисфункции правого желудочка (TAPSE: 13,1±3,4 vs 15,5±4,6 мм; р=0,0001) и диастолической дисфункции ЛЖ (E/A: 2,9±1,5 vs 2,1±1,3; p=0,006; E/e' 15,6±6,9 vs 11,8±7,2; p=0,019), более расширенное левое предсердие (индексированный объем левого предсердия: 63,3±19 vs 50±18,7 мл/ м2; р=0,006). В период 6-летней медианы наблюдения ФП наблюдалась у 75 пациентов (0,46 новых случаев/100 пациентов/год). В результате Кокс-регрессионного анализа, ФП как фактор, зависящий от времени, определен в качестве независимого предиктора летального исхода от всех сердечно-сосудистых причин (отношение рисков 3,99; 95% доверительный интервал: 1,67-8,59; p=0,0001).
Заключение. Таким образом, ФП как одна из наиболее частых устойчивых предсердных тахиаритмий в популяции продемонстрировала более низкую распространенность (27,8%) в когорте ДКМП по сравнению с желудочковыми тахиаритмиями (60,4%), однако высокую прогностическую значимость негативного влияния на риск летальных исходов. Развитие ФП у пациентов с ДКМП ассоциировано с 4-кратным повышением риска сердечнососудистой смерти в 6-летнем периоде.
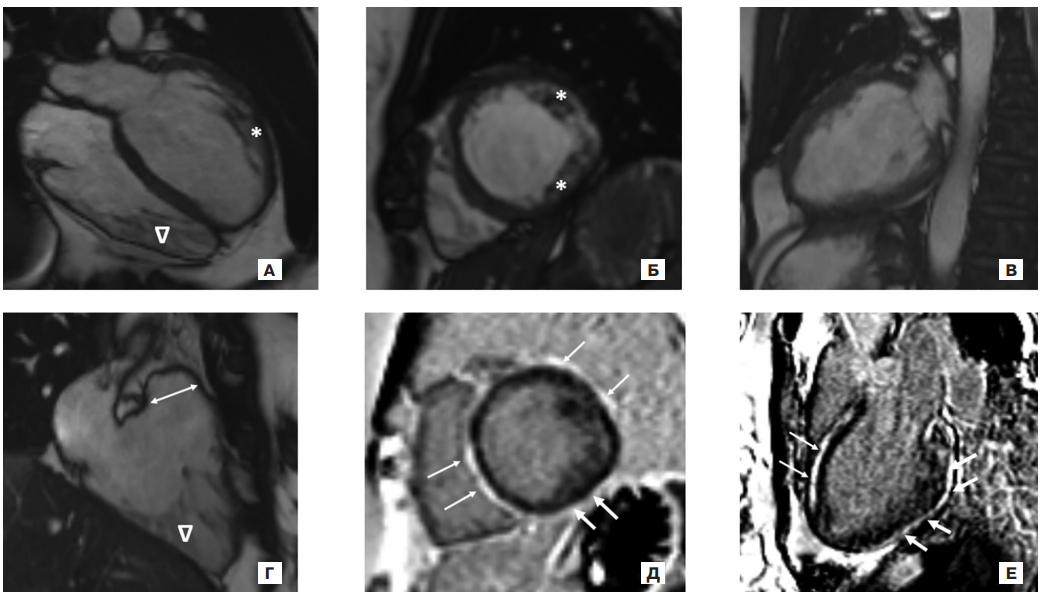
- Картина амилоидоза сердца во многом сходна с проявлениями гипертрофической кардиомиопатии.
- Симметричность утолщения стенки левого желудочка, зернистый и блестящий вид миокарда и утолщение створок клапанов сердца являются лучшими кардиальными предикторами амилоидоза сердца.
- Возраст старше 63 лет, снижение скорости клубочковой фильтрации и протеинурия являются лучшими внекардиальными предикторами амилоидоза сердца.
Цель. Определить особенности, помогающие дифференциальной диагностике этих двух состояний, путем анализа клинических, электро-, эхокардиографических и лабораторных данных у пациентов с системным амилоидозом и гипертрофической кардиомиопатией (ГКМП).
Материал и методы. Обследовали 38 больных с амилоидозом сердца и 80 больных ГКМП.
Результаты. Было обнаружено, что симметричность утолщения стенки левого желудочка (ЛЖ), зернистый и блестящий вид миокарда и утолщение створок клапанов сердца являются лучшими кардиальным предикторами, а возраст выше 63 лет, снижение скорости клубочковой фильтрации и протеинурия являются лучшими внекардиальными предикторами амилоидоза сердца, тогда как низкий вольтаж комплексов QRS и перикардиальный выпот имели меньшее клиническое значение. Переднесистолическое движение передней створки митрального клапана, асимметричное утолщение стенки ЛЖ и электрокардиографические признаки гипертрофии ЛЖ с высокой вероятностью свидетельствовали о ГКМП.
Заключение. Таким образом, стандартные неинвазивные методы могут быть полезны для выявления инфильтративного процесса в миокарде и дифференциальной диагностики амилоидоза сердца и ГКМП.
- Десмоплакиновая кардиомиопатия (КМП) — уникальная форма КМП, характеризующаяся преимущественным поражением левого желудочка с обширным субэпикардиальным фиброзом, жизнеугрожающими желудочковыми аритмиями и эпизодами воспалительного повреждения миокарда. Однако, учитывая недавнее выделение десмоплакиновой КМП в отдельную нозологическую единицу, вопросы ведения таких пациентов, в т.ч. профилактика внезапной сердечной смерти (ВСС), остаются неоднозначными.
- В статье представлен клинический случай семьи с десмоплакиновой КМП, а также обзор современных литературных данных об этом заболевании.
- Подчеркнута необходимость применения генотип-специфического подхода к диагностике, выбору тактики ведения и профилактике ВСС у пациентов с десмоплакиновой КМП.
Наследственные кардиомиопатии (КМП) — это группа гетерогенных заболеваний, характеризующихся патологией сердечной мышцы, не обусловленной ишемической болезнью сердца, гипертензией, клапанными и врожденными пороками. Благодаря развитию методов визуализации и молекулярногенетической диагностики стало понятно, что для многих КМП характерен фенотипический и генотипический "перекрест". И хотя генетическая составляющая не всегда определяет конкретный фенотип заболевания, в настоящее время доказано, что генетическое тестирование играет существенную роль в стратификации риска, определении прогноза и тактики ведения пациентов, а также проведении семейного скрининга. Принимая во внимание высокую диагностическую и прогностическую значимость генотипа, в последние годы были предложены новые стратегии классификации КМП, основанные на генотипе, а не на фенотипе. Одним из примеров такого генотип-специфического подхода является выделение десмоплакиновой КМП как отдельной самостоятельной нозологической единицы. В статье представлен клинический случай семьи, в трех поколениях которой выявлен патогенный вариант гена DSP (p.Gln948LysfsTer29), приводящий к развитию специфического фенотипа КМП. Проведено комплексное обследование, продемонстрирована стадийность естественного течения заболевания, а также предложена тактика ведения пациентов с десмоплакиновой КМП.
- Вторичный инфекционный (ИЭ) эндокардит чаще встречается на фоне наличия бикуспидального аортального клапана.
- Среди пациентов с ИЭ нативных клапанов по данным гистологического исследования часто встречаются слабоактивные формы.
- Пациенты с ИЭ протезов клапанов сердца имеют более высокую патоморфологическую активность.
Цель. Оценка данных клинико-патоморфологического исследования у пациентов с инфекционным эндокардитом (ИЭ) нативных и протезированных клапанов сердца.
Материал и методы. Проведено ретроспективное когортное исследование 354 пациентов, у которых при патоморфологическом анализе операционного материала тканей нативных клапанов и протезов клапанов сердца выявлялись признаки ИЭ. Пациенты были разделены на две группы: в первую группу были включены пациенты с ИЭ нативного клапана (n=328), во вторую — пациенты с протезным ИЭ (n=26).
Результаты. Среди пациентов с ИЭ нативного клапана наиболее часто регистрировался ИЭ аортального клапана (АК) — 67,6%, реже отмечалось поражение митрального клапана (МК) — 20,7%. В группе пациентов с протезным ИЭ также преобладал ИЭ протеза АК — 57,7% и также реже отмечался ИЭ протеза МК — 26,9%. У большинства пациентов первой группы выявлялся вторичный ИЭ — 68,9%, преобладало развитие ИЭ на фоне наличия бикуспидального АК (БАК) — 40,7%, немного реже встречалось развитие ИЭ на фоне дегенеративного порока АК — 31,4%, самым редким предшествующим ИЭ структурным заболеванием было ревматическое поражение клапана — 6,7%. В группе пациентов с ИЭ нативного клапана наиболее часто выявлялся слабоактивный ИЭ — в 38,4%, у 7,1% выявлялись признаки ремиссии процесса. В группе пациентов с протезным ИЭ чаще, чем в группе пациентов с ИЭ нативного клапана выявлялся ИЭ с умеренной активностью (42,3% vs 26,8%, p=0,042). В группе пациентов с протезным ИЭ несколько чаще встречалось наличие колоний микроорганизмов и нейтрофильной инфильтрации в гистологическом материале, при этом у пациентов с ИЭ нативного клапана отмечалась тенденция к более высокому проценту встречаемости некрозов в исследуемом материале (42,4% vs 38,5%, p>0,05).
Заключение. Результаты данной работы подтверждают изменение эпидемиологических характеристик пациентов с ИЭ. Отмечена высокая частота слабоактивных форм ИЭ по данным патоморфологического исследования у пациентов с ИЭ нативных клапанов, что требует разработки индивидуального подхода к назначению антибактериальной терапии в зависимости от патоморфологической активности ИЭ.
МАРКЕРЫ ДИАГНОСТИКИ И ФАКТОРЫ РИСКА
Что известно о предмете исследования?
- Апоптоз считается одним из морфологических признаков, характерных для различных типов регулируемой гибели клеток.
- Апоптоз кардиомиоцитов является ведущим процессом в развитии ишемии.
- В результате воздействия триггерных факторов во всех клетках атеромы обнаруживаются морфологические признаки апоптоза, что впоследствии может приводить к нестабильности атеросклеротической бляшки с увеличением риска тромбообразования и разрыва.
Что добавляют?
- Изучение связи маркеров апоптоза Bax, Bcl-2, Bcl-2/Bax, p53, TRAIL с выраженностью атеросклеротического поражения коронарных артерий и клинико-инструментальными характеристиками демонстрирует преобладание процессов апоптоза у пациентов с ишемической болезнью сердца и может создать перспективы в создании новых лечебно диагностических стратегий.
Цель. Определение маркеров апоптоза в сыворотке крови в зависимости от выраженности атеросклеротического поражения коронарных артерий (КА); изучение связи с клинико-инструментальными характеристиками пациентов с ишемической болезнью сердца (ИБС).
Материал и методы. В исследование включены 176 человек (105 мужчин и 71 женщина), из них 150 — пациенты с установленным диагнозом ИБС, 26 — здоровые добровольцы (группа контроля). Больные были разделены на следующие группы: 1 группа — с атеросклеротическим поражением КА без явных стенотических сужений (17 человек); 2 группа — с гемодинамически невыраженным ("стенозы <50%") атеросклерозом КА (21 человек); 3 группа — с гемодинамически значимым ("стенозы >50%") атеросклеротическим поражением КА (112 человек). Группа 4 была представлена здоровыми добровольцами (26 человек). Пациентам была выполнена коронароангиография с использованием шкалы SYNTAX; эхокардиографическое исследование; дуплексное ультразвуковое сканирование внечерепных отделов брахиоцефальных артерий. У всех испытуемых проведено исследование уровня маркеров апоптоза Bcl-2, Bax, Bcl-2/Bax, TRAIL и p53 в сыворотке крови. Статистическую обработку полученных результатов осуществляли с использованием программного обеспечения "Statistica 10.0"; достоверными считали различия при р<0,05.
Результаты. Отмечена сильная корреляционная связь очень высокой значимости между показателями Bcl-2 (r=-0,84; p<0,001), Bax (r=0,83; p<0,001), Bcl-2/Bax (r=-0,86; p<0,001), p53 (r=0,80; p<0,001), TRAIL (r=-0,78; p<0,001) и выраженностью атеросклеротического поражения КА. Выявлена корреляционная связь разной силы и значимости между значениями данных маркеров апоптоза — и рядом клинико-инструментальных характеристик пациентов. Также необходимо отметить достоверность различий (p<0,001) показателей Bcl-2, Bax, Bcl2/Bax, p53 и TRAIL между группами пациентов с мультифокальным атеросклерозом, рестенозами после ранее проведенной реваскуляризации и наличием инфаркта миокарда в анамнезе в сравнении с пациентами без данных признаков.
Заключение. Выявленные нами корреляционные связи между лабораторными признаками апоптоза и поражением КА, клинико-инструментальными характеристиками пациентов, а также обнаруженная достоверность различий между группами с мультифокальным атеросклерозом, рестенозами КА и инфарктом миокарда в анамнезе, позволяют рассматривать данные биомаркеры как показатели выраженности атеросклеротических процессов, а также могут лечь в основу формирования новых лечебно-диагностических стратегий.
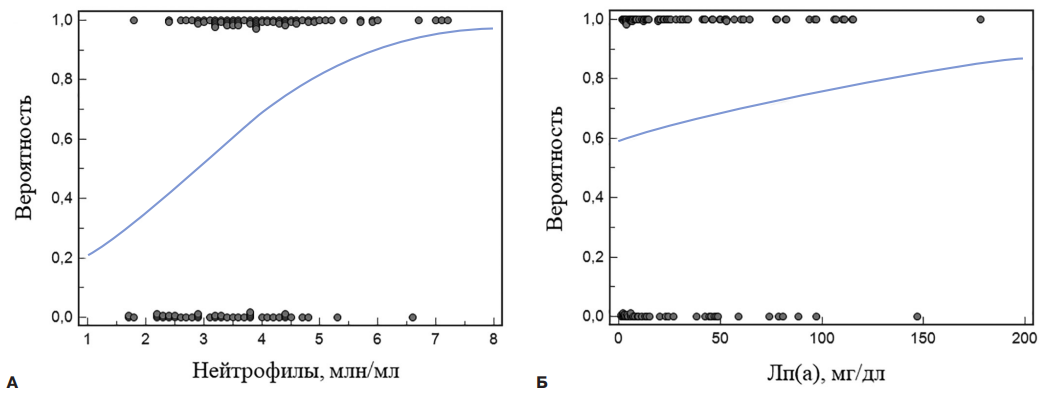
- Сочетание высоких значений количества нейтрофилов и уровня липопротеида (а) повышает шансы развития диффузного атеросклероза коронарных артерий у пациентов старше 60 лет.
- Липопротеид (а) способен вызывать активацию нейтрофилов в "цельной крови", а также образование нейтрофильных внеклеточных ловушек в первичной культуре клеток.
Цель. Оценить уровень липопротеида (а) (Лп(а)) и другие параметры липидного спектра, состав лейкоцитов крови у больных с очаговым и диффузным атеросклерозом коронарных артерий, перенесших операцию аортокоронарного шунтирования (АКШ), изучить влияние Лп(а) на активацию лейкоцитов in vitro.
Материал и методы. Включено 120 пациентов мужского пола, средний возраст 67±5 лет, с многососудистым поражением коронарных артерий, которым была выполнена плановая операция АКШ. Согласно типу поражения коронарных артерий пациенты были разделены на группы диффузного (n=77) и очагового (n=43) атеросклероза. В образцах периферической крови определяли содержание основных фракций липопротеидов, включая Лп(а). В цельной крови и в первичной культуре клеток оценивали активацию нейтрофильных гранулоцитов при внесении Лп(а).
Результаты. У пациентов с диффузным стенозированием коронарных артерий отмечалась тенденция к более высокому уровню Лп(а), изменений в других показателях липидного спектра не выявлено. В данной группе пациентов отмечено увеличение абсолютного количества лейкоцитов за счет нейтрофильных гранулоцитов. Абсолютное количество нейтрофилов >2,9 млн/мл ассоциировалось с диффузным поражением (AUC 0,69 (95% доверительный интервал (ДИ): 0,60-0,77), р=0,0002, чувствительность 85%, специфичность 42%). У пациентов с уровнем Лп(а) ³30 мг/дл диагностическая значимость количества нейтрофилов >2,9 млн/мл в отношении диффузного стенозирования была выше (AUC 0,74 (95% ДИ: 0,60-0,86), р=0,005, чувствительность 90%, специфичность 48%). По данным логистического регрессионного анализа с введением в модель количества нейтрофилов и традиционных факторов риска (возраст, индекс массы тела, наличие артериальной гипертензии и курения), только количество нейтрофилов выше порогового уровня оставалось независимым фактором диффузного стенозирования коронарного русла. Лп(а) способен вызывать активацию нейтрофилов, детектируемую по увеличению экспозиции CD66b клетками в цельной крови, а также образованию нейтрофильных внеклеточных ловушек в первичной культуре клеток.
Заключение. Нейтрофильные гранулоциты могут участвовать в формировании диффузных атеросклеротических поражений коронарного русла. Одним из активаторов нейтрофилов может быть Лп(а). Сочетание высоких значений количества нейтрофилов и уровня Лп(а) в крови повышает шансы развития диффузного атеросклероза коронарных артерий.
Что уже известно о предмете исследования?
- Антропометрия является методом, широко используемом в спорте для оценки физических
характеристик и отбора спортсменов, что может улучшить их спортивные результаты.
Что нового?
- Показано, что антропометрические особенности являются важными составляющими и критериями оценки функционального состояния
сердечно-сосудистой системы у квалифицированных спортсменов. - Установленные корреляционным анализом взаимосвязи характерных антропометрических
параметров и показателей кардиогемодинамики определяются видом спорта, продолжительностью подготовки и направленностью тренировочного процесса.
Возможный вклад в клиническую практику
- Необходим динамический контроль антропометрических данных и показателей кардиогемодинамики в процессе подготовки квалифицированных спортсменов и в прогнозировании спортивных результатов.
Цель. Оценить антропометрические особенности и функциональное состояние сердечно-сосудистой системы у квалифицированных спортсменов разных видов спорта.
Материал и методы. Обследовано 136 спортсменов, мужчины. Квалифицированные спортсмены — 116 чел. (возраст 22,07±4,10 года, спортивный стаж 9,56±3,08 года) разделены на группы: I (n=30) спортивная борьба, дзюдо, II (n=27) лыжные гонки, биатлон, III (n=33) пауэрлифтинг, IV (n=26) волейбол. Контрольная (n=20), подготовка <3 лет. Методы: антропометрия с оценкой длины и массы тела, окружности грудной клетки, площади поверхности тела (S тела), индексов массы тела (ИМТ), Пинье, Эрисмана, кистевой и становой динамометрии; эхокардиография (ЭхоКГ); велоэргометрия с оценкой физической работоспособности (PWC170) и максимального потребления кислорода (МПК). Взаимосвязь признаков оценивали при помощи коэффициента ранговой корреляции Спирмена (rs). Порог значимости p<0,05.
Результаты. Квалифицированные спортсмены по данным ЭхоКГ имели значимые различия морфоструктурных показателей. II группа характеризовалась увеличением объемных размеров левого желудочка (ЛЖ) и выявленными корреляциями ИМТ и S тела с конечно-диастолическим размером (r=0,602), конечно-диастолическим объемом (r=0,591), конечно-систолическим объемом (КСО) (r=0,429), ударным объемом (r=0,597), PWC170 (r=0,550). I и III группы характеризовались увеличением толщины задней стенки ЛЖ (ТЗСЛЖ) и межжелудочковой перегородки (ТМЖП). В I группе отмечены взаимосвязи S тела с ТЗСЛЖ (r=0,413); индекса Пинье с МПК (r=0,623); PWC170 с индексом Эрисмана (r=0,573), силой правой (r=0,610) и левой кисти (r=0,515), мышц спины (r=0,445). III группа отличалась наиболее высокими показателями ИМТ и S тела, при этом выявлены взаимосвязи с ТЗСЛЖ (r=0,426), ТМЖП (r=0,409), массой миокарда ЛЖ (ММЛЖ) (r=0,453), силой мышц спины (r=0,464); индекс Эрисмана коррелировал с индексом ММЛЖ (r=0,359). В IV группе параметры роста, массы тела и S тела взаимосвязаны с ММЛЖ (r=0,731), ТЗСЛЖ (r=0,523), ТМЖП (r=0,399), КСО (r=0,504), конечно-систолическим размером (r=0,467), силой правой кисти (r=0,583).
Заключение. Установленные корреляционным анализом взаимосвязи показали, что антропометрические особенности являются важными составляющими и критериями оценки функционального состояния кардиогемодинамики квалифицированных спортсменов в зависимости от вида спорта, направленности физических нагрузок, продолжительности подготовки, что необходимо учитывать при достижении спортивных результатов.
- Уровни катестатина имели обратную взаимосвязь с тяжестью сердечной недостаточности с сохраненной фракцией выброса (СНсФВ).
- Значения катестатина обратно коррелировали с параметрами ремоделирования левого желудочка, а также с уровнем N-концевого промозгового натрийуретического пептида и высокочувствительного С-реактивного белка.
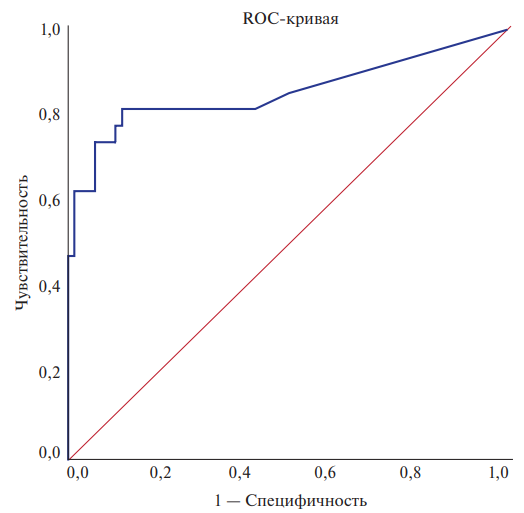
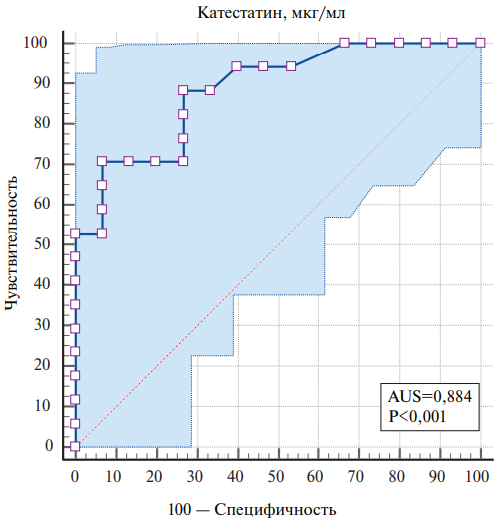
- Снижение уровней катестатина ≤132,83 мкг/мл (AUC=0,884; чувствительность 70,59%; специфичность 93,33%; p<0,001) было ассоциировано с наличием СНсФВ у пациентов с необструктивным поражением коронарных артерий.
Цель. Оценка у пациентов с неокклюзирующим коронарным атеросклерозом 1) патофизиологического значения и диагностической эффективности использования катестатина в отношении выявления сердечной недостаточности с сохраненной фракцией выброса (СНсФВ), 2) взаимосвязи уровней данного биомаркера с параметрами вариабельности ритма сердца (ВРС) и выраженностью диастолической дисфункции.
Материал и методы. В исследование было включено 83 пациента (44 мужчины, средний возраст 62,0 [57,0; 68,5] года) с необструктивным поражением коронарных артерий и сохраненной фракцией выброса левого желудочка (ЛЖ) (63 [60; 64]%). Эхокардиографию выполняли по стандартному протоколу. ВСР оценивали с помощью суточного мониторирования электрокардиограммы. Уровни биомаркеров в сыворотке определяли с помощью иммуноферментного анализа.
Результаты. Пациенты были разделены на группы в зависимости от наличия СНсФВ: в группу 1 (n=63) вошли больные с впервые выявленной СНсФВ, а в группу 2 — пациенты без сердечной недостаточности (n=20). Сывороточные концентрации катестатина были ниже на 43,1% (p<0,001) у больных с СНсФВ, чем у пациентов без нее. Катестатин имел отрицательную корреляционную связь с уровнями N-концевого промозгового натрийуретического пептида и С-реактивного белка. Более того, сывороточные значения катестатина обратно коррелировали с параметрами ремоделирования ЛЖ, тогда как со значениями ВРС взаимосвязи обнаружено не было. По данным ROC-анализа значения катестатина £132,83 мкг/мл (AUC=0,884; p<0,001) были определены как пороговые значения, связанные с наличием СНсФВ.
Заключение. Снижение концентрации катестатина в сыворотке было связано с наличием СНсФВ и с гиперэкспрессией биомаркеров сердечной недостаточности и воспаления. Более того, сывороточные значения катестатина имели отрицательную взаимосвязь с параметрами ремоделирования ЛЖ, тогда как со значениями ВРС взаимосвязи обнаружено не было.
Что уже известно о предмете исследования?
- Суррогатные маркеры состояния кишечной стенки и микробиоты (кальпротектин и зонулин) рассматриваются как новые неклассические факторы риска сердечно-сосудистых заболеваний, однако исследования выполнены в основном у пациентов с воспалительными заболеваниями кишечника и ревматологическими заболеваниями.
Что нового?
- Показана высокая распространенность повышенных уровней кальпротектина и зонулина в популяционной выборке жителей СанктПетербурга с метаболическими нарушениями, что ассоциировано с атеросклеротическим поражением сонных артерий.
- Продемонстрирована ассоциация уровней кальпротектина и зонулина с особенностями питания, дислипидемией, ожирением, циркулирующими биомаркерами и коморбидностью.
Возможный вклад в клиническую практику
- Выявление повышенного уровня кальпротектина и зонулина у пациентов с начальными метаболическими нарушениями позволит сосредоточиться врачу на приоритетных направлениях профилактики — поиске атеросклеротических изменений артерий и изменений диетических паттернов.
Суррогатные маркеры, количественно оценивающие выраженность кишечного воспаления (фекальный кальпротектин) и кишечную проницаемость (фекальный зонулин), в настоящее время рассматриваются как нетрадиционные факторы сердечно-сосудистого риска.
Цель. Изучить связь уровней фекального зонулина и кальпротектина с факторами сердечно-сосудистого риска и поражением органов-мишеней среди участников с метаболическими нарушениями из популяционной выборки жителей Санкт-Петербурга 35-75 лет.
Материал и методы. У пациентов когорты жителей Санкт-Петербурга, приглашенных на повторное обследование в рамках эпидемиологического исследования "ЭССЕ-РФ" с метаболическими нарушениями (избыточная масса тела, гипергликемия), было выполнено глубокое фенотипирование. Всем пациентам проведено анкетирование (физическая активность, курение, употребление алкоголя, сон, стресс, тревога и депрессия, оценка жалоб со стороны желудочно-кишечного тракта, частота употребления продуктов питания). Кроме того, было проведено измерение артериального давления и пульса, антропометрия, биохимический и гормональный анализ крови, эхокардиография, аппланационная тонометрия, объемная сфигмография, дуплексное сканирование сонных артерий, определение уровней фекального зонулина и кальпротектина.
Результаты. Обследованная когорта (86 человек, средний возраст 56 [44,7;63,5] лет, 49,5% — мужчины) характеризовалась высокой распространенностью абдоминального ожирения (80,2%), дислипидемии (липопротеиды низкой плотности >3 ммоль/л — 76,7%, триглицериды ³1,7 ммоль/л — 43%, общий холестерин >4,9 ммоль/л — 77,9%) и инсулинорезистентности (64%) с небольшими гендерными различиями. Повышение кальпротектина встречается у 23,3% пациентов, зонулина — у 30,3%, повышение кальпротектина и/ или зонулина встречается почти у половины обследованных (47,7%). Уровень фекального кальпротектина ассоциируется с показателями дислипидемии, ожирения, воспаления и атеросклеротического поражения сосудов, а также с диетическими паттернами и социально-экономическими показателями. Уровень зонулина связан с уровнем N-концевого промозгового натрийуретического пептида и наличием дефицита витамина Д, заболеваниями желчного пузыря и диетическими паттернами (благоприятными при потреблении овощей, зерновых и отрицательными при употреблении бекона).
Заключение. Повышение уровня хотя бы одного маркера кишечной проницаемости и воспаления кишечной стенки встречается примерно у половины участников с метаболическими нарушениями из популяционной выборки жителей Санкт-Петербурга. Помимо связи кальпротектина и зонулина с метаболическими факторами риска и диетическими паттернами, уровень кальпротектина ассоциировался с атеросклеротическими изменениями сонных артерий.
- Аритмии широко распространены у пациентов с недифференцированной дисплазией соединительной ткани и нередко являются причиной внезапной сердечной смерти.
- Ассоциация N-концевого промозгового натрийуретического пептида с желудочковой экстрасистолией и митральной регургитацией у молодых пациентов с недифференцированной дисплазией соединительной ткани свидетельствует о диагностической роли биомаркера у данной когорты пациентов.
- Результаты исследования в будущем могут способствовать разработке индивидуальных программ ведения пациентов с дисплазиями соединительной ткани.
Цель. Изучить взаимосвязь уровня N-концевого промозгового натрийуретического пептида (NT-proBNP) с морфофункциональными изменениями миокарда у пациентов с нарушениями ритма сердца на фоне недифференцированной дисплазии соединительной ткани (НДСТ).
Материал и методы. В одномоментное сравнительное исследование включены пациенты молодого и среднего возраста с аритмическим синдромом на фоне НДСТ: группа 1 (18-44 лет, n=127), группа 3 (45-59 лет, n=10). В группы контроля (n=30, группа 2; n=8, группа 4) включены добровольцы с единичными фенотипическими признаками НДСТ, сопоставимые по возрасту и полу. Выполнено стандартное клиническое обследование, 72-часовое мониторирование электрокардиограммы, Speckle-tracking эхокардиография, оценка уровня NT-proBNP.
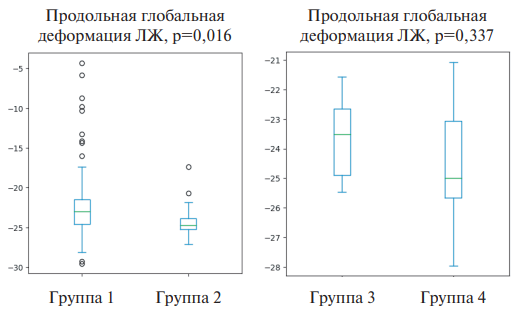
Результаты. У пациентов 1 и 3 групп отмечено статистически значимое повышение концентрации NT-proBNP по сравнению с группами контроля. При этом средний уровень NT-proBNP в исследуемых группах не превышал референсных значений. Выявлены достоверные корреляционные связи между NT-proBNP и частотой сердечных сокращений (r1=0,462, p=0,010; r3=0,397, p=0,034), уровнем диагностического порога НДСТ (r1=0,496, p=0,001; r3=0,401, p=0,043), наличием пролапса митрального клапана (r1=0,469, p=0,002) и митральной регургитации (r1=0,53, p=0,008), желудочковой экстрасистолией (ЖЭС) III (r1=0,582, p=0,045), IVa (r1=0,39, p=0,042) и V классов (r1=0,397, p=0,037); сердечным индексом (r1=-0,329, p=0,037) и фракцией выброса (r1=-0,407, p=0,044). Однако достоверной корреляции между глобальной продольной деформацией левого желудочка с уровнем NT-proBNP не выявлено.
Заключение. В исследовании продемонстрирована ассоциация уровня NTproBNP с диагностическим порогом НДСТ, пролапсом митрального клапана, митральной регургитацией, ЖЭС, что позволяет использовать данный биомаркер в качестве дополнительного диагностического критерия изменения сердечной мышцы на фоне НДСТ.
СТРЕСС В ПОПУЛЯЦИИ
- В неорганизованной популяции лиц трудоспособного возраста высокий уровень хронического стресса выявляется в среднем у каждого десятого.
- В отдельных городах выявляются гендерные различия по частоте высокого хронического стресса.
- В то же время средний уровень хронического стресса определен в 43% случаев в популяции лиц трудоспособного возраста.
Цель. Оценить распространенность хронического стресса во взрослой популяции во Владимирской области с учетом гендерных особенностей.
Материал и методы. В пяти городах Владимирской области (Владимире, Коврове, Муроме, Юрьеве-Польском и Вязниках) было организовано одномоментное популяционное исследование в период с мая 2018г по март 2020г. Из шести лечебно-профилактических учреждений были отобраны 9 терапевтических участков, затем по спискам прикрепленного населения в возрасте 30-69 лет с каждого участка на исследование были приглашены респонденты. Для выявления подверженности хроническому стрессу использовали опросник Reeder, позволяющий выявить 3 вида нарушений: низкий, средний и выраженный стресс. В исследовании проанализированы полностью заполненные вопросники Reeder, L. для оценки хронического стресса 1081 респондентом (393 мужчины и 688 женщин).
Результаты. Среди мужчин у каждого второго определен низкий уровень хронического стресса. У 42% мужчин выявлен средний уровень стресса, в то же время высокий хронический стресс обнаружен в 6,4% случаев. Среди женщин наблюдается аналогичная тенденция. Высокий уровень хронического стресса был выявлен у 8% женщин, также разрыв между частотой низкого и среднего уровня хронического стресса был минимальным. В целом частота различного уровня хронического стресса между мужчинами и женщинами была сопоставимая без достоверных различий. Выявлена гендерная вариабельность частоты хронического стресса в различных городах Владимирской области. Во Владимире частота высокого стресса среди мужчин оказалась в 3 раза больше по сравнению с женщинами, в то же время в Вязниках и Коврове наблюдается обратная закономерность. В остальных двух городах (Муроме и Юрьеве-Польском) распространенность высокого хронического стресса между мужчинами и женщинами была сопоставимая.
Заключение. Таким образом, в неорганизованной популяции лиц трудоспособного возраста высокий уровень хронического стресса выявляется до 10% случаев, в отдельных городах встречаются гендерные различия между мужчинами и женщинами. Средний уровень хронического стресса определен в 42-43% случаев. Полученные результаты свидетельствуют о необходимости проведения масштабных профилактических мер по борьбе с хроническим стрессом среди мужчин и женщин трудоспособного возраста Владимирской области.
- Клиническое взаимодействие как жанр межчеловеческого общения является полноценным фактором влияния на процессы патогенеза и салютогенеза через психосоматические взаимосвязи.
- Биографическая сторона медицинских проблем связана с уникальной для каждого человека системой смыслов, сложившихся в течение всей жизни и определяющих переживание каждого нового события и новой информации.
- В отличие от биомедицинского подхода к явлениям болезни и патологии, биографический подход требует от медицинского работника развитых гуманитарных и коммуникативных компетенций.
- Правовые и этические императивы медицинской деятельности могут быть реализованы только при полноценном учёте в практике явлений биосоциального патогенеза и биографического (нарративного) компонента состояний здоровья и болезни.
Современное представление о заболевании как ситуации, событии, всё больше включает в себя социальную сторону наряду с биологической. Хотя по-прежнему биомедицинская сторона проблемы доминирует, такие факторы, как приверженность, принятие решений и дача информированного согласия либо отказ, психосоциальные аспекты этиопатогенеза и другие не биологические компоненты развития болезни, становятся частью оказания помощи. Безусловно, социальная сторона вопроса учитывалась и раньше; до развития научной медицины она была преобладающей. Но в современном контексте развитие гуманитарных и социальных наук, нейронауки, психологии даёт возможность учитывать биографический нарратив личности пациента как неотъемлемую часть взаимоотношений врач-пациент. На стыке "биологического" и "биографического"в природе заболевания находится ряд факторов — таких как одиночество, стресс, социально-направленные эмоции, — которые овеществляют, воплощают (reify, enact) социальное Я человека в соматическую патологию либо в соматическое здоровье. Проблема соединения гуманитарного и естественно-научного знания очень сложна ввиду принципиальной разницы способов изучения, однако для современной медицины такое соединение совершенно необходимо.
СОВРЕМЕННЫЕ НАУЧНЫЕ ТЕХНОЛОГИИ
- Модели связей параметров восходящей аорты (ВА) с другими признаками, построенные с использованием машинного обучения, могут использоваться при выборе метода лечения и объема коррекции аневризмы ВА.
- При аортальной недостаточности оправдан более агрессивный подход к хирургической коррекции расширения ВА.
- Для прогнозирования течения аортопатии нецелесообразно использовать индексированные к площади поверхности тела диаметры грудной аорты.
- Перспективным является забор стенки ВА в виде циркулярного среза с последующим сплошным патогистологическим исследованием и последующим проспективным наблюдением.
Цель. Поиск связей патологических изменений стенки восходящей аорты (ВА) с ее планиметрическими характеристиками при несиндромной несемейной (спорадической) аневризме и расширении ВА.
Материал и методы. В исследование были включены 174 пациента со спорадическими аневризмами и расширениями ВА, планово оперированные в период с I.2010 по VII.2015гг и разделенные на 2 группы: больные с аневризмой ВА (АВА) (диаметр ВА >50 мм) и трехстворчатым аортальным клапаном (АК) со значимым аортальным стенозом (АС) или регургитацией (группа АВА, n=120), и лица с пограничным расширением ВА (диаметр ВА 45-50 мм), ассоциированным с двустворчатым АК и значимым АС (группа пограничного расширения, n=54). Использовались стандартные лабораторные тесты, инструментальные методы, патогистологическое исследование стенки ВА. Статистическая обработка осуществлялась в среде разработки SPYDER 4.1.5 (язык Python 3.8) и включала однофакторный корреляционный анализ, логистический регрессионный анализ, а также методы машинного обучения (МО) с учителем (машина опорных векторов, метод k-ближайшего соседа, случайный лес).
Результаты. При логистическом регрессионном анализе были выявлены положительные связи между атеросклерозом ВА и возрастом, кистозным медианекрозом (КМ) и диаметрами синусов Вальсальвы. Метод машины опорных векторов продемонстрировал тенденции к расширению ВА на уровне СВ у лиц с КМ (точность 60,5%), а также к расширению тубулярной части ВА при атеросклерозе (точность 79,2%). В ходе анализа методом "случайный лес" первым этапом были построены деревья решений для предсказания трех исходов: наличие КМ, атеросклероза либо нормальной структуры аорты; точность модели составила 64,2%. Далее переменные "КМ" и "атеросклероз" были объединены, и предсказание осуществлялось для исходов "нормальная структура стенки ВА" и "патологическая структура стенки ВА"; точность модели составила 73,5%.
Заключение. Использование МО открывает новые возможности для прогнозирования аортопатии и пациент-ориентированного подхода к лечению. При аортальной недостаточности оправдан более агрессивный подход к вмешательству на ВА. Для прогнозирования аортопатий нецелесообразно использовать индексированные к площади поверхности тела диаметры грудной аорты. Перспективными могут стать заборы образцов стенки аорты в виде циркулярных срезов с последующим сплошным патологическим исследованием.
КЛИНИКА И ФАРМАКОТЕРАПИЯ
- Пациенты с артериальной гипертензией и множественными факторами риска сложнее поддаются антигипертензивной терапии (АГТ), даже в виде тройной свободной комбинации препаратов.
- Повышение эффективности АГТ путем назначения тройной фиксированной комбинации амлодипина/индапамида/периндоприла (Трипликсам) через 3 мес. лечения обеспечивает достижение целевого уровня артериального давления у подавляющего большинства пациентов и отчетливое улучшение показателей суточного мониторирования артериального давления.
- Терапия тройной фиксированной комбинацией амлодипина/индапамида/периндоприла оказывает выраженный кардио- и вазопротективный эффекты, которые находят свое отражение в регрессе гипертрофии левого желудочка, улучшении его диастолической функции и снижении жесткости артериальной стенки.
Цель. Оценить антигипертензивную и органопротективную эффективность тройной фиксированной комбинации (ФК) амлодипина/индапамида/периндоприла у пациентов с артериальной гипертензией (АГ), не достигших целевых значений артериального давления (АД) на предшествующей антигипертензивной терапии (АГТ).
Материал и методы. В исследование было включено 47 пациентов с АГ и множественными факторами риска, которые не достигли целевых уровней АД на фоне предшествующей антигипертензивной терапии. В связи с чем им была назначена тройная ФК амлодипин/индапамид/периндоприл с предварительным назначением амлодипина, индапамида и периндоприла в виде свободных комбинаций. Исходно и через 3 мес. АГТ была проанализирована динамика показателей суточного мониторирования АД (СМАД), эхокардиографии (ЭхоКГ) и жесткости артериальной стенки.
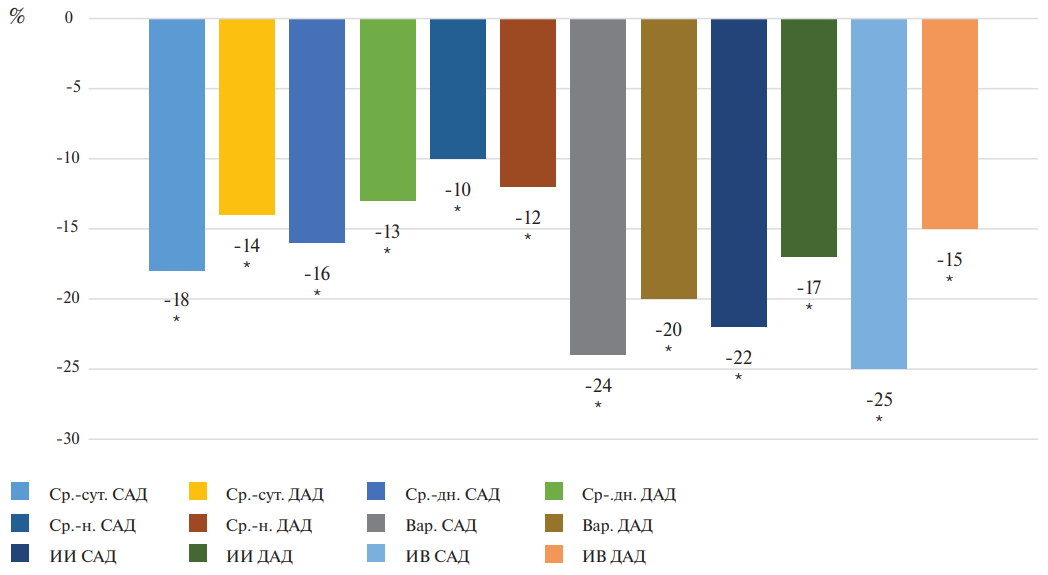
Результаты. Исходно у пациентов, включенных в исследование, были повышены основные показатели СМАД и изменен суточный профиль АД в пользу превалирования non dipper и reduced dipper (66% больных). Результаты ЭхоКГ свидетельствовали о наличии гипертрофии левого желудочка (ЛЖ) (ГЛЖ) по показателям индекса массы миокарда левого желудочка (ИММЛЖ), толщины задней стенки ЛЖ (ТЗСЛЖ) и межжелудочковой перегородки (МЖП) и его диастолической дисфункции по показателю Е/А, а увеличение индекса CAVI и биологического возраста сосудов (БВ) отражало повышение жесткости сосудистой стенки. Через 3 мес. АГТ регистрировались статистически значимые (р£0,05) изменения показателей СМАД и преобладание суточного профиля АД по типу dipper более чем у половины пациентов (53%). Снижение ИММЛЖ, ТЗСЛЖ и МЖП на 7%, 12% и 8%, соответственно (р£0,05), и повышение Е/А на 12% отражало регресс ГЛЖ и улучшение диастолической функции ЛЖ. Об уменьшении жесткости артериальной стенки свидетельствовало снижение (р£0,05) CAVI в среднем на 10% и БВ — на 4 года.
Заключение. Терапия тройной ФК амлодипин/индапамид/периндоприл через 3 мес. лечения обеспечила достижение целевого уровня АД у 78% пациентов, улучшение показателей СМАД и выраженный кардиои вазопротективный эффекты, нашедшие свое отражение в регрессе ГЛЖ, улучшении диастолической функции ЛЖ и снижении жесткости артериальной стенки.
ISSN 2618-7620 (Online)