Перейти к:
Машинное обучение при поиске взаимоотношений размеров и структуры стенки восходящей аорты при ее расширении различной степени
https://doi.org/10.15829/1560-4071-2023-5527
EDN: VYAEUP
Аннотация
Цель. Поиск связей патологических изменений стенки восходящей аорты (ВА) с ее планиметрическими характеристиками при несиндромной несемейной (спорадической) аневризме и расширении ВА.
Материал и методы. В исследование были включены 174 пациента со спорадическими аневризмами и расширениями ВА, планово оперированные в период с I.2010 по VII.2015гг и разделенные на 2 группы: больные с аневризмой ВА (АВА) (диаметр ВА >50 мм) и трехстворчатым аортальным клапаном (АК) со значимым аортальным стенозом (АС) или регургитацией (группа АВА, n=120), и лица с пограничным расширением ВА (диаметр ВА 45-50 мм), ассоциированным с двустворчатым АК и значимым АС (группа пограничного расширения, n=54). Использовались стандартные лабораторные тесты, инструментальные методы, патогистологическое исследование стенки ВА. Статистическая обработка осуществлялась в среде разработки SPYDER 4.1.5 (язык Python 3.8) и включала однофакторный корреляционный анализ, логистический регрессионный анализ, а также методы машинного обучения (МО) с учителем (машина опорных векторов, метод k-ближайшего соседа, случайный лес).
Результаты. При логистическом регрессионном анализе были выявлены положительные связи между атеросклерозом ВА и возрастом, кистозным медианекрозом (КМ) и диаметрами синусов Вальсальвы. Метод машины опорных векторов продемонстрировал тенденции к расширению ВА на уровне СВ у лиц с КМ (точность 60,5%), а также к расширению тубулярной части ВА при атеросклерозе (точность 79,2%). В ходе анализа методом "случайный лес" первым этапом были построены деревья решений для предсказания трех исходов: наличие КМ, атеросклероза либо нормальной структуры аорты; точность модели составила 64,2%. Далее переменные "КМ" и "атеросклероз" были объединены, и предсказание осуществлялось для исходов "нормальная структура стенки ВА" и "патологическая структура стенки ВА"; точность модели составила 73,5%.
Заключение. Использование МО открывает новые возможности для прогнозирования аортопатии и пациент-ориентированного подхода к лечению. При аортальной недостаточности оправдан более агрессивный подход к вмешательству на ВА. Для прогнозирования аортопатий нецелесообразно использовать индексированные к площади поверхности тела диаметры грудной аорты. Перспективными могут стать заборы образцов стенки аорты в виде циркулярных срезов с последующим сплошным патологическим исследованием.
Ключевые слова
Для цитирования:
Успенский В.Е., Сапранков В.Л., Мазин В.И., Заварзина Д.Г., Малашичева А.Б., Иртюга О.Б., Моисеева О.М., Гордеев М.Л. Машинное обучение при поиске взаимоотношений размеров и структуры стенки восходящей аорты при ее расширении различной степени. Российский кардиологический журнал. 2023;28(11):5527. https://doi.org/10.15829/1560-4071-2023-5527. EDN: VYAEUP
For citation:
Uspenskiy V.E., Saprankov V.L., Mazin V.I., Zavarzina D.G., Malashicheva A.B., Irtyuga O.B., Moiseeva O.M., Gordeev M.L. Machine learning in assessing the association between the size and structure of the ascending aortic wall in patients with aortic dilatation of varying severity. Russian Journal of Cardiology. 2023;28(11):5527. (In Russ.) https://doi.org/10.15829/1560-4071-2023-5527. EDN: VYAEUP
Аневризма восходящей аорты (АВА) — мультифакториальное заболевание. Основными факторами риска (ФР) АВА являются артериальная гипертензия (АГ), двустворчатый аортальный клапан (ДАК), моногенные заболевания соединительной ткани [1, 2]. Вместе с тем расширение аорты — естественный процесс, протекающий в течение всей жизни, и бывает непросто квалифицировать его как патологическое [3]. Считается, что точный ответ на вопрос об этиологии расширения аорты может дать гистологическое исследование ее стенки. Типичными находками являются разрушение, фрагментация или уменьшение числа эластических волокон с образованием псевдокист — кистозный медианекроз (КМ), нарушение целостности эндотелия, фиброз, разрежение и апоптозы гладкомышечных клеток [4]. Есть сведения, что у пациентов с преобладающей аортальной регургитацией (АР) наблюдаются более выраженные дегенеративные изменения стенки аорты. Вместе с тем таких исследований относительно немного, и они включают небольшие и разнородные группы больных как с трехстворчатым, так и с двустворчатым аортальным клапаном (АК) [5]. На сегодняшний день отсутствуют однозначные данные о встречаемости нарушений гистологической структуры стенки восходящей аорты (ВА) при ее расширении различной степени у лиц с различными нарушениями функции АК. Машинное обучение (МО) — активно развивающееся направление, и многообещающим представляется его использование для изучения этиопатогенеза и прогноза при расширении ВА [6].
Цель — поиск связей патологических изменений стенки ВА с ее планиметрическими характеристиками при несиндромной несемейной аневризме и расширении данной локализации.
Материал и методы
Для достижения поставленной цели мы изучили данные 588 пациентов с различными заболеваниями ВА, планово оперированных в нашей клинике в период с января 2010г по июль 2015г. Дизайн исследования: обсервационное, одноцентровое, одномоментное, ретроспективное, когортное. Были исключены больные с расслоениями аорты, аортопатиями специфического генеза, моногенными заболеваниями соединительной ткани, семейными АВА, инфекционным эндокардитом, ревматизмом, ранее перенесшие операции на аорте, а также имеющие пограничное расширение аорты и трехстворчатый АК. Углубленному анализу были подвергнуты 174 человека со спорадическими патологическими расширениями ВА, разделенные на 2 группы по принципу степени выраженности расширения: больные с АВА (максимальный диаметр аорты >50 мм) и гемодинамически значимым аортальным стенозом (АС) или АР (группа АВА, n=120), и лица с пограничным расширением аорты (максимальный диаметр ВА 45-50 мм), ассоциированным с ДАК и значимым АС (группа пограничного расширения (ПР), n=54). Исследование было выполнено в соответствии со стандартами надлежащей клинической практики (Good Clinical Practice) и принципами Хельсинкской декларации, одобрено локальным этическим комитетом (протокол № 95 от 13.05.2013), у участников было получено письменное информированное согласие.
Методы включали стандартные лабораторные тесты, электрокардиографию в 12 отведениях, обзорную рентгенографию грудной клетки, трансторакальную эхокардиографию (аппарат Vivid 7, GE, США), рентгеновскую компьютерно-томографическую ангиографию аорты (128-спиральный компьютерный томограф III поколения Somatom Definition, Siemens, Германия). Оценивались ФР осложнений, ассоциированных с аортой: личный анамнез аневризм и/или расслоений любых артерий, семейный анамнез аневризм, расслоений аорты и/или внезапных смертей, АГ, коарктация аорты, дефект межжелудочковой перегородки, расширение ВА ≥3 мм/год [1]. Аневризматически измененные зоны стенки ВА иссекались, помещались в 10% формалин и направлялись на стандартное патогистологическое исследование с окраской гематоксилином-эозином и по Ван Гизон и микроскопией парафиновых срезов.
Статистическая обработка данных проводилась на персональном компьютере с операционной системой macOS Monterey версии 12.6.7 с использованием программного продукта Microsoft Excel 2016 for Mac версии 16.16.27, а также в среде разработки с открытым исходным кодом SPYDER (Scientific PYthon Development EnviRonment) версии 4.1.5 с применением языка программирования Python 3.8 и библиотек Pandas, NumPy, SciPy, Seaborn, Matplotlib, Pylab, Scikit-Learn. Нормальность распределения оценивалась тестами Колмогорова-Смирнова, ШапироУилка и Андерсона-Дарлинга. Непрерывные данные представлены в виде медиан и значений 25-го и 75- го процентилей, категориальные — в виде единиц и процентов (долей). Значимость различий непрерывных данных рассчитывалась с использованием U-критерия Манна-Уитни, категориальных — критерия χ2. Различия признавались значимыми при p<0,05. Для поиска связей между переменными был применен однофакторный корреляционный анализ с использованием критерия Спирмена, а также логистический регрессионный анализ. Для построения моделей использовались методы МО: машина опорных векторов (параметр ядра — "linear", остальные параметры соответствуют значениям по умолчанию), метод k-ближайшего соседа (число соседей — 5, метод измерения расстояний — manhattan, соотношение обучающей/тестовой выборок — 75%/25%, остальные параметры соответствуют значениям по умолчанию), случайный лес (количество деревьев — 100, соотношение обучающей/тестовой выборок — 70%/30%, остальные параметры соответствуют значениям по умолчанию).
Результаты
В 76 (43,7%) случаях преобладала АР, в 51 (29,3%)— АС. Из ФР следует отметить АГ (n=40, 23,0%) и семейный анамнез аортопатий (n=2, 1,2%). Сочетания аортопатии с дефектом межжелудочковой перегородки и/или коарктацией аорты отсутствовали (табл. 1). Пациенты с погранично расширенной аортой закономерно имели меньшие диаметры фиброзного кольца АК и других отделов ВА; тубулярный отдел был максимально расширен наиболее часто. В группе аневризм аорты ДАК встречался у 56 (46,7%) пациентов, преобладали лица с АР. В группе пограничных расширений ДАК имелся у всех больных, наиболее часто встречался АС (табл. 2). При гистологическом исследовании стенки аорты в общей когорте наиболее часто обнаруживалось отсутствие патологических изменений (n=69, 39,7%), на втором месте располагался КМ (n=3, 36,2%), причем последний чаще выявлялся при преобладающей АР (n=34, 44,7%). В большинстве случаев преобладающего АС стенка аорты имела нормальное строение (n=31, 60,8%) (табл. 3). При корреляционном анализе были выявлены значимые связи между возрастом и диаметром дуги аорты, классом хронической сердечной недостаточности и выраженностью легочной гипертензии, а также размерами, объемами левого желудочка и диаметрами ВА на уровне фиброзного кольца, синусов Вальсальвы и синотубулярного соединения (рис. 1).
При логистическом регрессионном анализе были выявлены положительные связи между атеросклерозом аорты и возрастом, КМ и диаметром корня аорты, отрицательные связи нормальной структуры аорты с ее диаметрами на уровне синусов Вальсальвы (табл. 4). Для большинства значимых зависимостей модуль коэффициента регрессии (β1) был невелик (максимально 0,714), в связи с чем от определения граничных параметров значимых предикторов методом ROC-анализа было решено воздержаться и дальнейшую обработку данных выполнить с помощью МО с учителем. С учетом того, что у подавляющего большинства пациентов с сочетанием КМ и атеросклеро за последний не превышал 2 стадию, признаки "КМ", "КМ + атеросклероз" и "дисплазия стенки аорты" были объединены в один признак "КМ", и далее выполнялось прогнозирование бинарных исходов для трех признаков: "КМ", "атеросклероз", "нормальная структура аорты". При анализе методом машины опорных векторов наблюдались тенденции к расширению аорты на уровне корня у лиц с КМ (точность 60,5%, рис. 2 А), а также к расширению тубулярной части аорты при атеросклерозе (точность 79,2%, рис. 2 Б).
При анализе связей строения стенки ВА с другими переменными методом k-ближайшего соседа в перечень непрерывных предикторов вошли диаметры грудной аорты, пиковый градиент давления на АК, рост. В группу категориальных предикторов вошли вид нарушения функции АК, врожденная аномалия АК, локализация максимального расширения аорты. Точность такой модели оказалась невысокой (49,1%). Исключение категориальных предикторов увеличило точность до 61,4%. Введение в перечень переменных типа ДАК не повысило точность модели.
Завершающим этапом обработки данных был анализ методом "случайный лес". Первым этапом были построены деревья решений для предсказания трех исходов: наличие КМ, атеросклероза либо нормальной структуры аорты. Индексированные параметры ВА не вошли в перечень значимых предикторов. Наиболее значимыми предикторами оказались пиковый градиент давления на АК, размеры и сократительная функция левого желудочка, диаметры аорты, рост; точность модели составила 64,2% (рис. 3). Далее переменные "КМ" и "атеросклероз" были объединены, и предсказание осуществлялось для исходов "нормальная структура стенки аорты" и "патологическая структура стенки аорты". Точность модели составила 73,5% (рис. 4 А). Показатель precision для переменных "нормальная структура стенки аорты" и "патологическая структура стенки аорты" составил 0,77 и 0,72, соответственно; показатель recall для переменных "нормальная структура стенки аорты" и "патологическая структура стенки аорты" — 0,48 и 0,91, соответственно (рис. 4 Б).
Таблица 1
Характеристика пациентов

Примечание: данные распределены нормально.
Сокращения: ВА — восходящая аорта, ХСН — хроническая сердечная недо- статочность, NYHA — New York Heart Association.
Таблица 2
Эхокардиографические характеристики
Признак | Группа ПР (n=54) Медиана (25-й; 75-й процентиль) | Группа АВА (n=120) Медиана (25-й; 75-й процентиль) | Р-уровеньU |
КДО ЛЖ, мл | 139,5 (113; 194) | 190,5 (151; 265) | 5,17×10-5 |
Индекс КДО ЛЖ, мм/м2 | 72,6 (57,6; 95,6) | 98,0 (75,1; 125,0) | 7,79×10-5 |
ФВ ЛЖ, % | 66 (59; 69) | 61 (52; 65) | 0,0005 |
Толщина МЖП, мм | 15 (14; 19) | 13 (12; 16) | 8,98×10-5 |
Толщина ЗС ЛЖ, мм | 14 (12; 15) | 12 (11; 14) | 0,0004 |
ММ ЛЖ, г | 390 (279; 474) | 383 (293; 513) | 0,327 |
Индекс ММ ЛЖ, г/м2 | 192,6 (149,2; 247,7) | 195,3 (148,5; 243,9) | 0,433 |
Пиковый градиент давления на АК, мм рт.ст. | 77 (53,8; 104,0) | 17,1 (10,5; 49,1) | 9,30×10-13 |
n (%) | n (%) | Р-уровеньX2 | |
АН 2 и более степени | 20 (37%) | 90 (75%) | 0,0001 |
Двустворчатый АК | 54 (100%) | 56 (46,7%) | 1,53×10-8 |
Ведущая АР | 7 (13%) | 69 (57,5%) | 4,83×10-6 |
Ведущий АС | 32 (59,2%) | 19 (15,8%) | 7,83×10-7 |
Равнозначные АР+АС | 15 (27,8%) | 32 (26,7%) | 0,999 |
Сокращения: АВА — аневризма восходящей аорты, АК — аортальный клапан, АН — аортальная недостаточность, АР — аортальная регургитация, АС — аор- тальный стеноз, ЗС — задняя стенка, КДО — конечно-диастолический объем, ЛЖ — левый желудочек, МЖП — межжелудочковая перегородка, ММ — масса миокарда, ПР — пограничное расширение, ФВ — фракция выброса, U — U-критерий Манна-Уитни, X2 — критерий χ2.
Таблица 3
Гистологические характеристики стенки ВА при ее расширении
Нарушение функции АР (n=76) РX2 АС (n=51) РX2 Комб. (n=47) РX2 АК D ВА, мм D ВА, мм D ВА, мм | |||
Изменения стенки ВА 45-50 | >50 45-50 >50 45-50 >50 | ||
КМ, n 1 | 33 0,236 8 3 0,742 5 13 0,891 | ||
Атеросклероз, n 0 | 14 0,419 4 2 0,978 1 3 0,953 | ||
Атеросклероз + КМ, n 0 | 9 0,596 2 1 0,989 0 4 0,359 | ||
Дисплазия стенки, n 0 | 0 — 0 0 — 1 1 0,854 | ||
Нет изменений, n | 6 | 13 0,0005 | 18 13 0,690 8 11 0,467 |
Всего, n 7 | 69 — 32 19 — 15 32 — | ||
Сокращения: АК — аортальный клапан, АР — аортальная регургитация, ВА — восходящая аорта, КМ — кистозный медианекроз, Комб. — комбинированный порок аортального клапана, D — диаметр, РX2 — Р-уровень значимости различий, критерий χ2.
Таблица 4
Результаты логистического регрессионного анализа
Предиктор | Исход | β0 | β1 (ОШ) | 95% ДИ | P-уровень |
Возраст | Атеросклероз | -6,619 | 0,080 | 0,031; 0,129 | 0,0004 |
Синусы Вальсальвы | Норма | 2,875 | -0,070 | -0,106; -0,034 | 0,00004 |
Синотубулярная зона | Норма | 3,401 | -0,083 | -0,122; -0,004 | 0,000004 |
Тубулярная часть ВА | Атеросклероз | -5,644 | 0,068 | 0,026; 0,110 | 0,002 |
ФК АК | АС | 9,084 | -0,384 | -0,548; -0,220 | 8,75*10-8 |
ФК АК индекс к росту | АС | 9,858 | -0,714 | -1,046; -0,381 | 1,03*10-6 |
Синусы Вальсальвы | АР | -6,179 | 0,123 | 0,081; 0,166 | 9,46*10-12 |
Синусы Вальсальвы | АС | 5,819 | -0,148 | -0,204; -0,093 | 5,50*10-11 |
Синотубулярная зона | АР | -6,066 | 0,124 | 0,080; 0,167 | 5,68*10-11 |
Синотубулярная зона | АС | 6,615 | -0,170 | -0,230; -0,111 | 1,28*10-12 |
Сокращения: АР — аортальная регургитация, АС — аортальный стеноз, ВА — восходящая аорта, ДИ — доверительный интервал, ОШ — отношение шансов, ФК АК — фиброзное кольцо аортального клапана, β0 — точка пересечения, β1 — коэффициент регрессии.

Рис. 1. Матрица корреляций между параметрами ВА и другими переменными (критерий Cпирмена).
Примечание: коэффициенты корреляции указаны в ячейках, цвет ячейки отражает силу связи. Для пары «NYHA — СДЛА» р=0,002, во всех остальных случаях p<0,0001. Цветное изображение доступно в электронной версии журнала.
Сокращения: АН — аортальная недостаточность, Ао — аорта, иКДО — индекс к площади поверхности тела конечно-диастолического объема, иКДР — индекс к площади поверхности тела конечно-диастолического размера, иММ — индекс к площади поверхности тела массы миокарда, иППТ — индекс к площади поверх- ности тела, иРост — индекс к росту, КДО — конечно-диастолический объем, КДР — конечно-диастолический размер, ЛЖ — левый желудочек, ММ — масса миокарда, СВ — синусы Вальсальвы, СДЛА — систолическое давление в легочной артерии, СТС — синотубулярное соединение, ФВ — фракция выброса, ФК АК — фиброзное кольцо аортального клапана, dP peak — пиковый градиент давления на аортальном клапане, NYHA — класс хронической сердечной недостаточности по New York Heart Association.
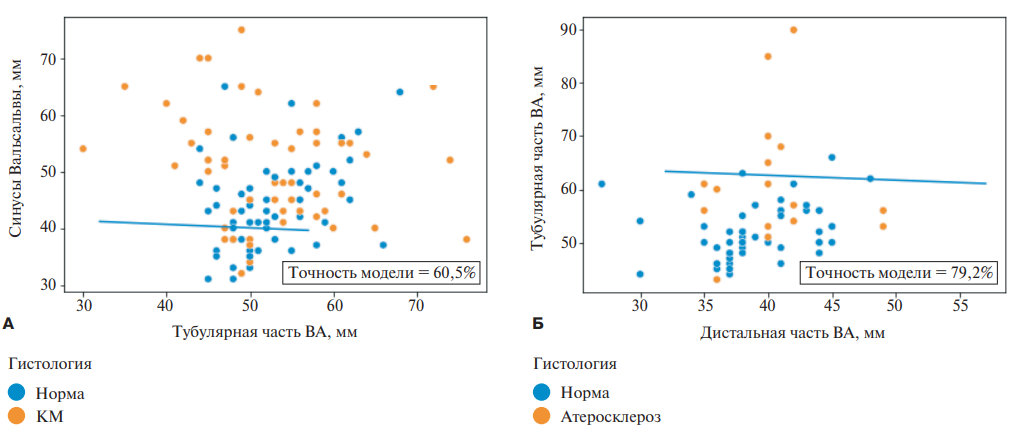
Рис. 2. Диаметры грудной аорты у пациентов с различными вариантами гистологических изменений стенки ВА (машина опорных векторов).
Примечание: гиперплоскости разделяют 2 категории пациентов.
Сокращения: ВА — восходящая аорта, КМ — кистозный медианекроз.
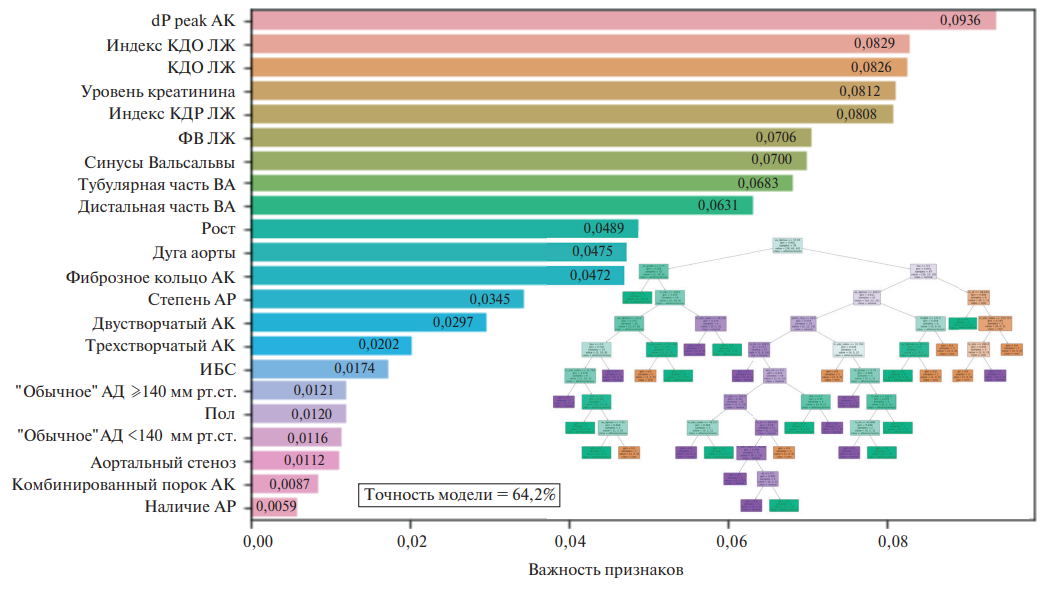
Рис. 3. Модель предсказания наличия КМ, атеросклероза или нормального строения стенки ВА (случайный лес).
Сокращения: АД — артериальное давление, АК — аортальный клапан, АР — аортальная регургитация, ВА — восходящая аорта, ИБС — ишемическая болезнь сердца, КДО — конечно-диастолический объем, КДР — конечно-диастолический размер, ЛЖ — левый желудочек, ФВ — фракция выброса, dP peak — пиковый градиент давления.
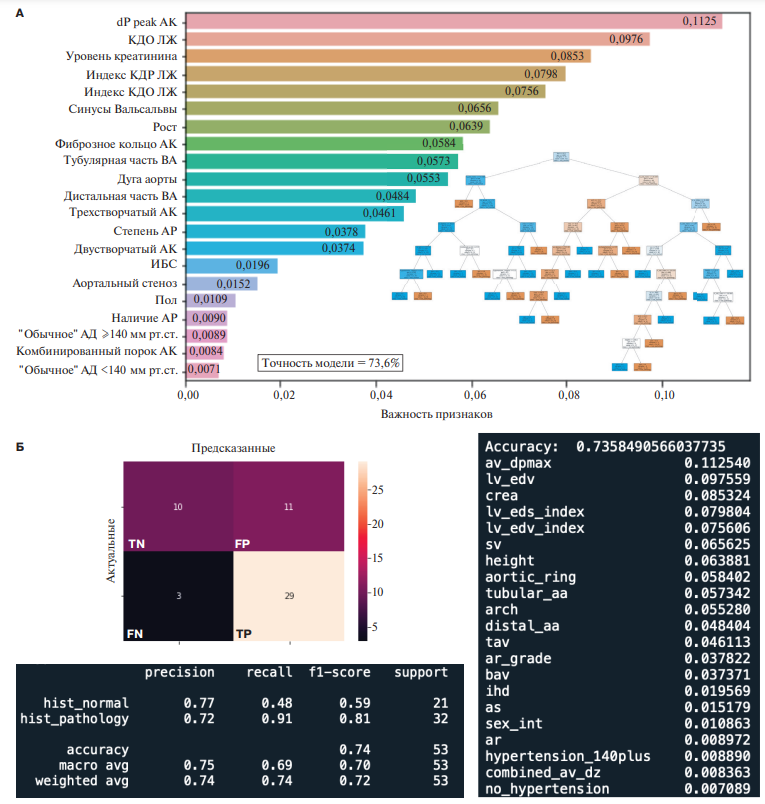
Рис. 4. Модель предсказания наличия или отсутствия патологических изменений стенки ВА (случайный лес).
Сокращения: АД — артериальное давление, АК — аортальный клапан, АР — аортальная регургитация, ВА — восходящая аорта, ИБС — ишемическая болезнь сердца, КДО — конечно-диастолический объем, КДР — конечно-диастолический размер, ЛЖ — левый желудочек, dP peak — пиковый градиент давления, FN — ложные негативы, FP — ложные позитивы, TN — истинные негативы, TP — истинные позитивы.
Обсуждение
Преобладание изменений по типу КМ при АР, а также отсутствие "явных" нарушений структуры аорты при доминирующем АС согласуются с данными других исследователей [4, 7]. Большая доля пациентов с гистологически нормальной структурой аортальной стенки также может быть объяснена вкладом лиц с ДАК, преобладающим АС и пограничным расширением аорты. Схожие результаты были получены в исследовании Ю.В. Белова и др. [8]. Другой причиной отсутствия выявления патологических изменений стенки аорты может быть мозаичность нарушений ее структуры и локализация патологических изменений в таких зонах, что участок с наиболее значимыми микроструктурными нарушениями может остаться неисследованным. В аневризматически расширенном корне аорты по сравнению с тубулярной частью имеется повышенное содержание коллагена и фиброз, а также сниженное содержание эластина [4]. Козлов Б. Н. и др. продемонстрировали, что при несемейной несиндромной АВА в стенке дистальной части ВА имеются более выраженные фиброзные и воспалительные изменения, лизис эластических и коллагеновых волокон с кистозной дегенерацией медиального слоя [9]. Для детального анализа требуется забор материала из нескольких участков, например, на границах анастомозов с сосудистыми протезами. Схожая встречаемость разных гистологических нарушений при расширении ВА разной степени может указывать на преимущественный вклад в дилатацию индивидуальных нарушений структуры аорты без четкой связи со степенью расширения: КМ может выявляться при пограничном расширении аорты, а при аневризме ее стенка гистологически может иметь нормальное строение, что говорит о присутствии других факторов, обусловливающих наличие аневризмы. Результаты анализа с применением МО свидетельствуют о двух тенденциях: отрицательной связи между возрастом и КМ, и положительной — между возрастом и атеросклеротическими изменениями аорты. Следствием может быть представление о различиях патогенеза спорадических АВА у лиц разного возраста и, соответственно, различия в подходах к лечению в "пограничных" ситуациях: более агрессивный подход к лечению у более молодых пациентов и консервативная тактика — у более возрастных. Выявленные предикторы указывают на связь с патологией ВА расширения левого желудочка, которое, вероятно, вторично и развивается на фоне АР или декомпенсированного АС, но имеет более высокую значимость (важность), чем сами по себе диаметры аорты на разных уровнях и "традиционные" ФР аортопатий (возраст, мужской пол, АГ) [10]. Актуальным является отсутствие связи между изменениями стенки аорты и ее индексированными параметрами к площади поверхности тела, что подтверждает роль гемодинамического влияния АД на стенку аорты, связанного с абсолютными значениями диаметра: согласно закону Лапласа, напряжение стенки увеличивается пропорционально радиусу аорты и обратно пропорционально ее толщине [11]. Ряд авторов продемонстрировал связь фенотипа АК с расширением ВА [12]. В нашем исследовании добавление к модели анатомических особенностей ДАК (типы 0, 1, 2, LR и т.д.) либо не повышали (реже), либо снижали (чаще) точность модели. К ограничениям исследования относится небольшое число пациентов, а также искусственный характер формирования когорты, что повысило доли ДАК и пограничных расширений аорты. Возможности корректного анализа "традиционных" ФР аортопатий в изученной когорте ограничены, в связи с этим прямое сравнение пациентов с АВА и погранично расширенной аортой по изученным признакам не выполнялось. Другими ограничениями являются одноцентровой дизайн и ограниченное количество доступных данных.
Заключение
Использование МО для поиска связей параметров ВА с другими признаками расширяет арсенал клиницистов и открывает новые возможности для прогнозирования аортопатии и пациент-ориентированного лечения [13]. Построенные модели могут использоваться при выборе метода лечения и объема резекции аорты. При АР оправдан более агрессивный подход к вмешательству на ВА. Для прогнозирования аортопатий нецелесообразно использовать индексированные к площади поверхности тела диаметры аорты. Многообещающими могут стать заборы аорты в виде циркулярных срезов с последующим сплошным патогистологическим исследованием, а также проспективным наблюдением. Роль АС в прогнозировании структурных изменений стенки аорты требует более углубленного изучения.
Отношения и деятельность. Работа выполнена в рамках выполнения плановой темы государственного задания "Разработка устройства для клапаносохраняющей коррекции аортальной недостаточности", номер ЕГИСУ 123021000152-9.
Список литературы
1. Isselbacher EM, Preventza O, Hamilton Black J, 3rd, et al. 2022 ACC/AHA Guideline for the diagnosis and management of aortic disease: a report of the American Heart Association/ American College of Cardiology Joint Committee on Clinical Practice Guidelines. Circulation. 2022;146:e334-e482. doi:10.1161/CIR.0000000000001106.
2. Chew NWS, Phua K, Ho YJ, et al. Prognostic implications of bicuspid and tricuspid aortic valve phenotype on progression of moderate aortic stenosis and ascending aorta dilatation. Am J Cardiol. 2021;161:76-83. doi:10.1016/j.amjcard.2021.08.050.
3. Cheung K, Boodhwani M, Chan KL, et al. Thoracic aortic aneurysm growth: role of sex and aneurysm etiology. J Am Heart Assoc. 2017;6:e003792. doi:10.1161/JAHA.116.003792.
4. Surman TL, Abrahams JM, Manavis J, et al. Histological regional analysis of the aortic root and thoracic ascending aorta: a complete analysis of aneurysms from root to arch. J Cardiothorac Surg. 2021;16:255. doi:10.1186/s13019-021-01641-5.
5. Roberts WC, Vowels TJ, Ko JM, et al. Comparison of the structure of the aortic valve and ascending aorta in adults having aortic valve replacement for aortic stenosis versus for pure aortic regurgitation and resection of the ascending aorta for aneurysm. Circulation. 2011;123(8):896-903. doi:10.1161/CIRCULATIONAHA.110.972406.
6. Greener JG, Kandathil SM, Moffat L, et al. A guide to machine learning for biologists. Nat Rev Mol Cell Biol. 2022;23:40-55. doi:10.1038/s41580-021-00407-0.
7. Lee Y, Hwang HY, Park EA, et al. Suture reduction of the borderline ascending aortic dilatation during aortic valve replacement. J Cardiovasc Surg (Torino). 2021;62:618-24. doi:10.23736/S0021-9509.21.11543-5.
8. Белов Ю. В., Федоров Д. Н., Тааев Б. К. и др. Особенности гистологического строения стенки восходящей аорты при аневризме. Кардиология и сердечно-сосудистая хирургия. 2013;2:34-6.
9. Козлов Б. Н., Панфилов Д. С., Гутор С. С. и др. Морфологическое состояние аортальной стенки при аневризме восходящей аорты. Клиническая и экспериментальная хирургия. 2018;6:43-8. doi:10.24411/2308-1198-2018-14006.
10. Rogers IS, Massaro JM, Truong QA, et al. Distribution, determinants, and normal reference values of thoracic and abdominal aortic diameters by computed tomography (from the Framingham Heart Study). Am J Cardiol. 2013;111:1510-6. doi:10.1016/j.amjcard.2013.01.306.
11. Emmott A, Garcia J, Chung J, et al. Biomechanics of the ascending thoracic aorta: a clinical perspective on engineering data. Can J Cardiol. 2016;32(1):35-47. doi:10.1016/j.cjca.2015.10.015.
12. Merritt BA, Turin A, Markl M, et al. Association between leaflet fusion pattern and thoracic aorta morphology in patients with bicuspid aortic valve. J Magn Reson Imaging. 2014;40:294-300. doi:10.1002/jmri.24376.
13. Liu M, Liang L, Ismail Y, et al. Computation of a probabilistic and anisotropic failure metric on the aortic wall using a machine learning-based surrogate model. Comput Biol Med. 2021;137:104794. doi:10.1016/j.compbiomed.2021.104794.
Об авторах
В. Е. УспенскийРоссия
Успенский Владимир Евгеньевич — доктор медицинских наук, заведующий НИЛ заболеваний аорты и аортального клапана Института сердца и сосудов
Санкт-Петербург
В. Л. Сапранков
Россия
Сапранков Валерий Леонидович — очный аспирант по специальности "сердечно-сосудистая хирургия", младший научный сотрудник НИЛ заболеваний аорты и аортального клапана Института сердца и сосудов
Санкт-Петербург
В. И. Мазин
Россия
Мазин Виктор Игоревич — очный аспирант по специальности "сердечно-сосудистая хирургия"
Санкт-Петербург
Д. Г. Заварзина
Россия
Заварзина Дарья Геннадьевна — очный аспирант по специальности "сердечно-сосудистая хирургия"
Санкт-Петербург
А. Б. Малашичева
Россия
Малашичева Анна Борисовна — доктор биологических наук, зав. НИЛ молекулярной кардиологии и генетики Института молекулярной биологии и генетики
Санкт-Петербург
О. Б. Иртюга
Россия
Иртюга Ольга Борисовна — кандидат медицинских наук, доцент кафедры кардиологии Института медицинского образования
Санкт-Петербург
О. М. Моисеева
Россия
Моисеева Ольга Михайловна — доктор медицинских наук, директор Института сердца и сосудов
Санкт-Петербург
М. Л. Гордеев
Россия
Гордеев Михаил Леонидович — доктор медицинских наук, профессор, главный научный сотрудник НИО кардиоторакальной хирургии Института сердца и сосудов
Санкт-Петербург
Дополнительные файлы
- Модели связей параметров восходящей аорты (ВА) с другими признаками, построенные с использованием машинного обучения, могут использоваться при выборе метода лечения и объема коррекции аневризмы ВА.
- При аортальной недостаточности оправдан более агрессивный подход к хирургической коррекции расширения ВА.
- Для прогнозирования течения аортопатии нецелесообразно использовать индексированные к площади поверхности тела диаметры грудной аорты.
- Перспективным является забор стенки ВА в виде циркулярного среза с последующим сплошным патогистологическим исследованием и последующим проспективным наблюдением.
Рецензия
Для цитирования:
Успенский В.Е., Сапранков В.Л., Мазин В.И., Заварзина Д.Г., Малашичева А.Б., Иртюга О.Б., Моисеева О.М., Гордеев М.Л. Машинное обучение при поиске взаимоотношений размеров и структуры стенки восходящей аорты при ее расширении различной степени. Российский кардиологический журнал. 2023;28(11):5527. https://doi.org/10.15829/1560-4071-2023-5527. EDN: VYAEUP
For citation:
Uspenskiy V.E., Saprankov V.L., Mazin V.I., Zavarzina D.G., Malashicheva A.B., Irtyuga O.B., Moiseeva O.M., Gordeev M.L. Machine learning in assessing the association between the size and structure of the ascending aortic wall in patients with aortic dilatation of varying severity. Russian Journal of Cardiology. 2023;28(11):5527. (In Russ.) https://doi.org/10.15829/1560-4071-2023-5527. EDN: VYAEUP
JATS XML

















































