Перейти к:
Коррекция дефицита железа у пациентов с инфарктом миокарда: открытое проспективное исследование эффективности терапии дефицита железа с использованием препаратов железа для внутривенного введения по сравнению с приемом пероральных препаратов железа с целью оценки влияния на систолическую функцию левого желудочка у пациентов с инфарктом миокарда OPERA-MI
https://doi.org/10.15829/1560-4071-2026-6759
EDN: QAEGHC
Аннотация
Цель. Определить эффективность внутривенного введения железа карбоксимальтозата (ЖКМ) по сравнению с пероральным железом (сульфатом железа (СЖ)) в отношении систолической функции левого желудочка (ЛЖ), оцениваемой по индексу суммарной подвижности миокарда (ИСПМ) ЛЖ с помощью эхокардиографии, у пациентов с инфарктом миокарда (ИМ) и дефицитом железа (ДЖ).
Материал и методы. В исследование включено 322 пациента с ИМ, из них у 199 пациентов был установлен ДЖ, у 123 пациентов ДЖ не было. Пациенты с ДЖ были рандомизированы в 2 группы: получавшую ЖКМ и получавшую СЖ. Всем пациентам при включении и через 3, 6 и 12 мес. оценены ИСПМ ЛЖ, качество жизни по Канзасскому опроснику больных кардиомиопатией (KCCQ). Период наблюдения составил 12 мес. Первичной конечной точкой (ПКТ) было любое уменьшение ИСПМ ЛЖ за 12 мес.
Результаты. За 12 мес. ПКТ наступила у 53 (53,5%) пациентов в группе ЖКМ, у 58 (58%) пациентов в группе СЖ и у 46 (46,5%) пациентов в группе контроля без ДЖ (р>0,05). Доля пациентов с увеличением суммы баллов по KCCQ на ≥5 пунктов в группе ЖКМ на визите 3 мес. составила 36,4%, в группе СЖ — 18%, в контрольной группе — 17,2% пациентов (р=0,002). На всех визитах доля пациентов с увеличением суммы баллов на ≥5 пунктов была достоверно выше в группе ЖКМ в сравнении с группой СЖ. Доля пациентов со значимым увеличением суммы баллов на ≥10 пунктов была достоверно выше в группе ЖКМ на визитах 6 (40,4% vs 19% в группе СЖ, р<0,001) и 12 мес. (45,5% vs 22% в группе СЖ, р=0,003).
Заключение. Лечение пациентов с ИМ и ДЖ препаратами железа привело к аналогичной частоте наступления ПКТ во всех группах: группе ЖКМ, группе СЖ и у пациентов с ИМ без ДЖ. Не было преимущества какого-либо препарата железа. Лечение ЖКМ ассоциировано с существенным улучшением качества жизни пациентов.
Ключевые слова
Для цитирования:
Хастиева Д.Р., Тарасова Н.А., Хасанов Н.Р., Кузнецов М.С., Валеева И.Х., Капралова Л.И., Закирова Э.Б., Малкова М.И., Клюшкина Ю.А. Коррекция дефицита железа у пациентов с инфарктом миокарда: открытое проспективное исследование эффективности терапии дефицита железа с использованием препаратов железа для внутривенного введения по сравнению с приемом пероральных препаратов железа с целью оценки влияния на систолическую функцию левого желудочка у пациентов с инфарктом миокарда OPERA-MI. Российский кардиологический журнал. 2026;31(2):6759. https://doi.org/10.15829/1560-4071-2026-6759. EDN: QAEGHC
For citation:
Khastieva D.R., Tarasova N.A., Khasanov N.R., Kuznetsov M.S., Valeeva I.Kh., Kapralova L.I., Zakirova E.B., Malkova M.I., Klyushkina Yu.A. Iron deficiency treatment in patients with myocardial infarction: an open-label, prospective study of the efficacy of intravenous iron versus oral iron therapy to evaluate the impact on left ventricular systolic function in patients with myocardial infarction (OPERA-MI). Russian Journal of Cardiology. 2026;31(2):6759. (In Russ.) https://doi.org/10.15829/1560-4071-2026-6759. EDN: QAEGHC
Одной из основных причин смерти от сердечно-сосудистых заболеваний в мире является инфаркт миокарда (ИМ)1. Дефицит железа (ДЖ) относится к числу наиболее распространённых состояний, возникающих в результате снижения запасов или уменьшения функционального пула железа в организме человека [1]. Исследования, проведенные in vitro и на моделях животных, показали, что миокардиальный и системный ДЖ связан с большим размером ИМ, снижением скорости сокращения миокарда, патологическим ремоделированием левого желудочка (ЛЖ) и ишемической кардиомиопатией [2-6]. Коррекция ДЖ внутривенным введением железа карбоксимальтозата (ЖКМ) может способствовать уменьшению объема инфаркта и улучшению сократимости миокарда [6][7]. Вместе с тем большинство исследований, посвященных роли ДЖ и эффектам препаратов железа, было проведено у пациентов с сердечной недостаточностью. Критериями ДЖ в этих исследованиях были: ферритин плазмы крови <100 мкг/л (абсолютный ДЖ) и уровень ферритина плазмы 100-300 мкг/л при коэффициенте насыщения трансферрина железом (КНТЖ) <20% (функциональный ДЖ) [8-10]. По действующим клиническим рекомендациям определение показателей железа не входит в план обследования пациентов с ИМ. Исследований, посвященных изучению влияния ДЖ и его коррекции у пациентов с ИМ, достаточно мало, и необходимы проспективные исследования для изучения роли ДЖ и его коррекции на течение ИМ [11].
В открытом проспективном рандомизированном исследовании OPERA-MI (ClinicalTrials.gov, NCT05309499) оценивалась эффективность внутривенного введения ЖКМ по сравнению с пероральным приемом сульфата железа (СЖ) в отношении влияния на систолическую функцию ЛЖ, качество жизни и развитие нежелательных сердечно-сосудистых осложнений у пациентов с ИМ и ДЖ.
Материал и методы
Исследование OPERA-MI является открытым проспективным рандомизированным одноцентровым исследованием, выполненным при поддержке компании Вифор (Интернэшнл) Инк. (Швейцария). Дизайн исследования был опубликован ранее [12].
Всего было скринировано 964 пациента с ИМ, госпитализированных в кардиологические отделения — ГАУЗ "Городская клиническая больница № 7 им. М. Н. Садыкова" г. Казани (клиническая база Казанского государственного медицинского университета) в период с декабря 2021г по апрель 2024г. В исследование включено 199 пациентов с ДЖ и 123 пациента без ДЖ (рис. 1). ДЖ определялся по уровню ферритина сыворотки <100 мкг/л или 100-299 мкг/л при КНТЖ <20%. Пациенты с ДЖ были рандомизированы методом конвертов в две группы: 99 пациентов вошли в группу лечения ЖКМ и 100 пациентов — в группу лечения СЖ. Не соответствовали критериям включения/невключения (табл. 1) 642 пациента. Исследование проводилось в соответствии с правилами качественной клинической практики и Хельсинкской декларации Всемирной медицинской ассоциации. Все включенные пациенты подписали информированное согласие. Протокол исследования был одобрен локальным этическим комитетом ФГБОУ ВО "Казанский ГМУ" Минздрава России (протокол № 4 от 20.04.2021).
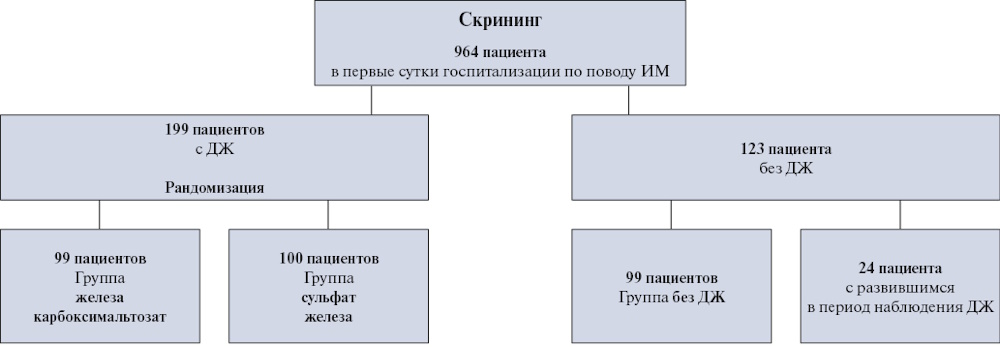
Рис. 1. Схема исследования OPERA-MI.
Сокращения: ДЖ — дефицит железа, ИМ — инфаркт миокарда.
Таблица 1
Критерии включения и невключения в исследование OPERA-MI
|
Критерии включения |
Критерии невключения |
|
Пациенты (≥18 лет), подписавшие информированное согласие |
Приобретенный гемосидероз, недавнее получение (в течение 3 мес.) средства, стимулирующего эритропоэтин, внутривенное введение железа или гемотрансфузий |
|
Госпитализация по поводу инфаркта миокарда с гипокинезией или акинезией как минимум в двух соединенных сегментах левого желудочка по данным эхокардиографии, полученным в течение первых 24 ч после инфаркта миокарда |
Сердечная недостаточность II-IV степени по Killip на скрининговом визите |
|
Гемоглобин >90 г/л и <150 г/л во время скринингового визита |
Гемодиализ или перитонеальный диализ (текущий или планируемый в течение следующих 6 мес.), или рСКФ <15 мл/мин/1,73 м2
|
|
Ферритин сыворотки <100 мкг/л или 100-299 мкг/л при КНТЖ <20% |
Подтвержденное заболевание печени или активный гепатит |
|
Текущее или недавнее (в течение 3 лет) злокачественное новообразование, за исключением базальноклеточного рака, плоскоклеточного рака кожи или цервикальной интраэпителиальной неоплазии |
|
|
Активное желудочно-кишечное кровотечение |
|
|
Реакции гиперчувствительности на компоненты сульфата железа или ЖКМ |
|
|
Наличие противопоказаний к препаратам исследования согласно локальным инструкциям по применению |
Сокращения: ЖКМ — железа карбоксимальтозат, КНТЖ — коэффициент насыщения трансферрина железом, рСКФ — расчетная скорость клубочковой фильтрации.
Пациенты, соответствующие критериям включения и не имеющие критериев невключения, включались в исследование в первые сутки от начала развития клинической картины ИМ. ИМ устанавливался на основании Четвертого универсального определения ИМ (2018) [13]. Ведение всех пациентов осуществлялось на основе Российских клинических рекомендаций по ИМ с подъемом сегмента ST электрокардиограммы и острому коронарному синдрому без подъема сегмента ST электрокардиограммы [14][15].
При включении в исследование у всех пациентов собирался анамнез, проводилось физикальное исследование. Учитывались сопутствующие заболевания, получаемая пациентом лекарственная терапия. Всем пациентам в первые сутки госпитализации проводилась эхокардиография с расчетом индекса суммарной подвижности миокарда (ИСПМ) ЛЖ [16], клинический и биохимический анализ крови, оценка качества жизни по Канзасскому опроснику больных кардиомиопатией (KCCQ) [17]. Кроме базового лечения, пациенты с ДЖ, в соответствии с рандомизацией, получали либо ЖКМ в дозе, рассчитанной по инструкции к препарату с учетом веса пациента и уровня гемоглобина крови, в одной или двух внутривенных инфузиях, либо СЖ 200 мг в сутки в 2 приема по 100 мг в течение 3 мес. Через 3 мес. оценивалось достижение пациентами компенсации ДЖ. Дальнейший контроль проводился через 6 и 12 мес. Всем пациентам на визитах 3, 6 и 12 мес. проводилась эхокардиография с подсчетом ИСПМ ЛЖ, оценка качества жизни по KCCQ, определение уровня ферритина, сывороточного железа, общей железосвязывающей способности сыворотки, КНТЖ и общий анализ крови.
Первичной конечной точкой (ПКТ) было любое уменьшение ИСПМ ЛЖ за 12 мес. Вторичная конечная точка: составная конечная точка, включающая смерть от сердечно-сосудистых заболеваний, нефатальные ИМ и инсульт, госпитализацию по поводу декомпенсации сердечной недостаточности.
Статистический анализ и визуализация полученных данных проводились с использованием среды для статистических вычислений R 4.5.1 (R Foundation for Statistical Computing, Вена, Австрия). Описательные статистики представлены в виде абсолютной и относительной частот для категориальных переменных, медианы (1-й; 3-й квартиль) и среднего (± стандартное отклонение) для количественных переменных. Соответствие выборочного распределения количественных переменных нормальному распределению проводилось с использованием теста Андерсона-Дарлинга. Кроме того, производилась оценка коэффициента асимметрии (в качестве критического значения использовали абсолютное значение коэффициента >1,96). Для сравнения групп в отношении количественных переменных использовались t-тест Уэлча и тест Манна-Уитни. Для сравнения групп в отношении бинарных показателей использовался точный тест Фишера. При анализе времени до развития события использовался метод Каплана-Мейера, лог-ранговый тест и однофакторные модели пропорциональных рисков Кокса. При проведении попарных post hoc сравнений для контроля инфляции частоты ошибок I рода использовалась процедура Холма. В рамках анализа ассоциации между количественными переменными оценивался коэффициент ранговой корреляции ρ Спирмена с соответствующим 95% доверительным интервалом. Различия между группами и ассоциацию между показателями считали статистически значимыми при p<0,05.
Результаты
В группе пациентов без признаков ДЖ на момент включения в исследование у 24 человек в течение 12 мес. наблюдения развился ДЖ. Эти пациенты не вошли в основной анализ, но был проведен отдельный анализ ПКТ среди пациентов с ДЖ, получавших препараты железа, и пациентов с исходным отсутствием и развившимся ДЖ, не получавших препараты железа. Пациенты с ДЖ (199 человек), по сравнению с пациентами без ДЖ (99 человек), были несколько старше (медиана возраста составила 64 (59; 72) и 61 (50; 68) год, соответственно, р=0,002), среди них была выше доля женщин (44,7% (89 человек) и 24,2% (24 человека), соответственно, р<0,001), чаще наблюдалась анемия (32 (16,1%) и 7 (7,1%) пациентов, соответственно, р=0,03) и фибрилляция предсердий (26 (13,1%) и 5 (5,1%) пациентов, соответственно, р=0,043). По частоте встречаемости других заболеваний, перенесенной реваскуляризации коронарных артерий, антропометрическим данным, значениям фракции выброса ЛЖ и ИСПМ ЛЖ пациенты с наличием и отсутствием ДЖ при включении в исследование не различались. Данные представлены в таблице 2. Только в группе ДЖ были пациенты, получавшие при включении недигидропиридиновые антагонисты кальция (15 (7,5%) и 0 (0%), соответственно, р=0,003). Других отличий в лекарственной терапии между пациентами с ДЖ и без ДЖ не было (табл. 3).
Таблица 2
Общие характеристики пациентов с ДЖ и без ДЖ на момент включения в исследование
|
Группа лечения препаратами железа (n=199) |
Пациенты без ДЖ (n=99) |
p |
|
|
Возраст (лет) |
64 (59; 72) |
61 (50; 68) |
0,002 |
|
Пол |
<0,001 |
||
|
Женский, n (%) |
89 (44,7%) |
24 (24,2%) |
|
|
Мужской, n (%) |
110 (55,3%) |
75 (75,8%) |
|
|
Масса тела (кг) |
76 (70; 86) |
80 (70; 89) |
0,302 |
|
ИМТ (кг/м2)
|
27,9 (25,1; 30,7) |
27,7 (24,1; 30,8) |
0,274 |
|
ФВ (%) |
48 (45; 54) |
48 (46; 54) |
0,991 |
|
ИСПМ ЛЖ |
1,25 (1,188; 1,625) |
1,25 (1,125; 1,562) |
0,955 |
|
ИМпST, n (%) |
150 (75,4%) |
77 (77,8%) |
0,668 |
|
ИМ в анамнезе, n (%) |
35 (17,6%) |
16 (16,2%) |
0,171 |
|
ЧКВ в анамнезе, n (%) |
28 (14,1%) |
10 (10,1%) |
0,363 |
|
АКШ в анамнезе, n (%) |
3 (1,5%) |
2 (2%) |
>0,999 |
|
АГ, n (%) |
155 (77,9%) |
86 (86,9%) |
0,085 |
|
ФП, n (%) |
26 (13,1%) |
5 (5,1%) |
0,043 |
|
ХСН, n (%) |
117 (58,8%) |
46 (46,5%) |
0,332 |
|
Анемия, n (%) |
32 (16,1%) |
7 (7,1%) |
0,03 |
|
Гиперхолестеринемия, n (%) |
100 (54,3%) |
55 (59,1%) |
0,522 |
|
Инсульт/ТИА, n (%) |
18 (9%) |
7 (7,1%) |
0,661 |
|
Астма или ХОБЛ, n (%) |
11 (5,6%) |
2 (2%) |
0,232 |
|
ХБП, n (%) |
11 (5,5%) |
5 (5,1%) |
>0,999 |
|
СД 2 типа, n (%) |
43 (21,6%) |
15 (15,2%) |
0,215 |
Сокращения: АГ — артериальная гипертензия, АКШ — аортокоронарное шунтирование, ДЖ — дефицит железа, ИСПМ ЛЖ — индекс суммарной подвижности миокарда левого желудочка, ИМ — инфаркт миокарда, ИМпST — инфаркт миокарда с подъемом ST, ИМТ — индекс массы тела, СД — сахарный диабет, ТИА — транзиторная ишемическая атака, ФВ — фракция выброса, ФП — фибрилляция предсердий, ХБП — хроническая болезнь почек, ХОБЛ — хроническая обструктивная болезнь легких, ХСН — хроническая сердечная недостаточность, ЧКВ — чрескожное коронарное вмешательство.
Таблица 3
Медикаментозная терапия пациентов на момент включения в исследование
|
Группа лечения препаратами железа (n=199) |
Пациенты без ДЖ (n=99) |
p |
|
|
Ингибиторы АПФ, n (%) |
129 (64,8%) |
75 (75,8%) |
0,064 |
|
БРА, n (%) |
9 (4,5%) |
8 (8,1%) |
0,288 |
|
β-блокаторы, n (%) |
131 (65,8%) |
74 (74,7%) |
0,144 |
|
Дигидропиридиновые БКК, n (%) |
6 (3%) |
3 (3%) |
>0,999 |
|
Недигидропиридиновые БКК, n (%) |
15 (7,5%) |
0 (0%) |
0,003 |
|
Диуретики, n (%) |
7 (3,5%) |
7 (7,1%) |
0,076 |
|
АМР, n (%) |
9 (4,5%) |
3 (3%) |
0,757 |
|
АСК, n (%) |
198 (99,5%) |
97 (98%) |
0,257 |
|
Ингибиторы рецепторов P2Y12, n (%) |
196 (98,5%) |
98 (100%) |
0,553 |
|
Статины, n (%) |
196 (98,5%) |
97 (98%) |
>0,999 |
Сокращения: АПФ — ангиотензинпревращающий фермент, АМР — антагонисты минералокортикоидных рецепторов, АСК — ацетилсалициловая кислота, БКК — блокаторы кальциевых каналов, БРА — блокаторы рецепторов ангиотензина II, ДЖ — дефицит железа.
Таблица 4
Общие характеристики пациентов с ДЖ лечения ЖКМ и СЖ
на момент включения в исследование
|
ЖКМ (n=99) |
СЖ (n=100) |
p |
|
|
Возраст (лет) |
66,3 (±10,2) |
64,3 (±8,8) |
0,155 |
|
Пол |
0,201 |
||
|
Женский, n (%) |
49 (49,5%) |
40 (40%) |
|
|
Мужской, n (%) |
50 (50,5%) |
60 (60%) |
|
|
ИМТ (кг/м2)
|
27,7 (24,2; 29,2) |
28,6 (26; 31,2) |
<0,001 |
|
ИМ в анамнезе, n (%) |
17 (17,2%) |
18 (18%) |
0,879 |
|
ЧКВ в анамнезе, n (%) |
15 (15,2%) |
13 (13%) |
0,689 |
|
АКШ в анамнезе, n (%) |
1 (1%) |
2 (2%) |
>0,999 |
|
АГ, n (%) |
76 (76,8%) |
79 (79%) |
0,735 |
|
ФП, n (%) |
22 (22,2%) |
4 (4%) |
<0,001 |
|
ХСН, n (%) |
60 (60,6%) |
57 (57%) |
0,794 |
|
ФВ ЛЖ (%) |
48 (45; 55) |
48 (45; 53) |
0,386 |
|
WMSI |
1,25 (1,188; 1,562) |
1,375 (1,188; 1,688) |
0,084 |
|
Анемия, n (%) |
27 (27,3%) |
5 (5%) |
<0,001 |
|
Гиперхолестеринемия, n (%) |
57 (64%) |
43 (45,3%) |
0,056 |
|
Инсульт/ТИА, n (%) |
5 (5,1%) |
13 (13%) |
0,081 |
|
Астма или ХОБЛ, n (%) |
3 (3,1%) |
8 (8%) |
0,214 |
|
СД 2 типа, n (%) |
19 (19,2%) |
24 (24%) |
0,491 |
|
ХБП, n (%) |
8 (8,1%) |
3 (3%) |
0,134 |
Сокращения: АГ — артериальная гипертензия, АКШ — аортокоронарное шунтирование, ЖКМ — железа карбоксимальтозат, ИМ — инфаркт миокарда, ИМТ — индекс массы тела, ЛЖ — левый желудочек, СД — сахарный диабет, СЖ — сульфат железа, ТИА — транзиторная ишемическая атака, ФВ — фракция выброса, ФП — фибрилляция предсердий, ХБП — хроническая болезнь почек, ХОБЛ — хроническая обструктивная болезнь легких, ХСН — хроническая сердечная недостаточность, ЧКВ — чрескожное коронарное вмешательство, WMSI — суммарный индекс подвижности стенок.
Таблица 5
Данные лабораторных исследований крови в группах пациентов с ДЖ на момент включения в исследование
|
ЖКМ (n=99) |
СЖ (n=100) |
p |
|
|
Гемоглобин (г/л) |
131 (121,5; 136) |
136 (131; 141) |
<0,001 |
|
Эритроциты (1012/л)
|
4,52 (4,24; 4,94) |
4,8 (4,33; 5,06) |
0,193 |
|
Тромбоциты (109/л)
|
228 (195; 247) |
253 (206; 311,2) |
0,007 |
|
Лейкоциты (109/л)
|
8,6 (7,2; 10,55) |
10,1 (8,7; 12,8) |
<0,001 |
|
Сывороточное железо (мкмоль/л) |
6,3 (5,5; 9,3) |
8,6 (7,6; 12) |
<0,001 |
|
ОЖСС (мкмоль/л) |
56 (49,9; 60) |
52,6 (48,5; 59,8) |
0,274 |
|
КНТЖ (%) |
12,8 (10,2; 17) |
17,3 (12,6; 20,4) |
<0,001 |
|
Ферритин (мкг/л) |
99,3 (76,4; 163) |
77,5 (56; 101,9) |
0,001 |
|
ЛНП (ммоль/л) |
3,45 (2,73; 4,52) |
3,72 (3,43; 4,24) |
0,167 |
|
Глюкоза сывороточная (ммоль/л) |
7,1 (5,67; 8,6) |
7,46 (6,06; 9,33) |
0,097 |
|
Креатинин (ммоль/л) |
91 (79,5; 99,8) |
87,5 (81; 97,9) |
0,804 |
|
Тропонин при поступлении (нг/мл) |
25,6 (2,5; 500) |
40,4 (0,8; 500) |
0,818 |
|
Билирубин (мкмоль/л) |
8,6 (6,9; 13,2) |
9,1 (6,5; 12,1) |
0,784 |
|
СРБ (мг/л) |
4,7 (2,9; 9,2) |
5,25 (2,37; 8,2) |
0,445 |
Сокращения: ЖКМ — железа карбоксимальтозат, КНТЖ — коэффициент насыщения трансферрина железом, ЛНП — липопротеиды низкой плотности, ОЖСС — общая железосвязывающая способность сыворотки, СЖ — сульфат железа, СРБ — С-реактивный белок.
Таблица 6
Медикаментозная терапия пациентов с ДЖ на момент включения в исследование
|
ЖКМ (n=99) |
СЖ (n=100) |
p |
|
|
Ингибиторы АПФ, n (%) |
59 (59,6%) |
70 (70%) |
0,139 |
|
БРА, n (%) |
7 (7,1%) |
2 (2%) |
0,101 |
|
БКК, n (%) |
6 (6,1%) |
15 (15%) |
0,212 |
|
β-блокаторы, n (%) |
62 (62,6%) |
69 (69%) |
0,372 |
|
Тиазидные диуретики, n (%) |
4 (4%) |
0 (0%) |
0,121 |
|
Петлевые диуретики, n (%) |
3 (3%) |
0 (0%) |
0,121 |
|
АМР, n (%) |
6 (6,1%) |
3 (3%) |
0,329 |
|
АСК, n (%) |
99 (100%) |
99 (99%) |
>0,999 |
|
Ингибиторы P2Y12, n (%) |
97 (98%) |
99 (99%) |
0,621 |
|
Статины, n (%) |
97 (98%) |
99 (99%) |
0,621 |
|
Блокатор протонной помпы, n (%) |
21 (21,2%) |
19 (19%) |
0,726 |
Сокращения: АПФ — ангиотензинпревращающий фермент, АМР — антагонисты минералокортикоидных рецепторов, АСК — ацетилсалициловая кислота, БКК — блокаторы кальциевых каналов, БРА — блокаторы рецепторов ангиотензина II, ЖКМ — железа карбоксимальтозат, СЖ — сульфат железа.
На визите 2 через 3 мес. наблюдения ДЖ был скомпенсирован у 72 (72,7%) пациентов в группе ЖКМ и у 36 (36%) в группе СЖ (р<0,001). Через 12 мес. наблюдения в группе ЖКМ компенсация ДЖ наблюдалась у 79 (79,8%) пациентов, в группе СЖ — у 28 (28%) пациентов (р<0,001).
За 12 мес. ПКТ наступила у 53 (53,5%) пациентов в группе ЖКМ, у 58 (58%) пациентов в группе СЖ и у 46 (46,5%) пациентов в группе контроля без ДЖ (р>0,05 для сравнения трех групп между собой) (рис. 2). При сравнении групп лечения между собой и с группой контроля достоверных различий риска достижения ПКТ получено не было (табл. 7).

Рис. 2. Кумулятивная частота наступления ПКТ в группах пациентов с ДЖ и в группе контроля.
Сокращение: ДЖ — дефицит железа.
Таблица 7
Риск наступления ПКТ в группах пациентов с ДЖ и в группе контроля
|
Группы пациентов |
HR |
95% ДИ |
p |
|
Железа карбоксимальтозат vs сульфат железа |
0,78 |
0,5; 1,23 |
0,391 |
|
Железа карбоксимальтозат vs группа контроля |
1,17 |
0,72; 1,9 |
0,435 |
|
Сульфат железа vs группа контроля |
1,5 |
0,93; 2,4 |
0,124 |
Сокращения: ДИ — доверительный интервал, HR — отношение рисков.
Всего было 9 случаев наступления вторичной составной конечной точки в группах пациентов с исходным ДЖ и в группе контроля за 12 мес. наблюдения. Из них 8 (4%) случаев в группах ДЖ и 1 (1%) случай в группе контроля (р=0,161). Ввиду малого количества событий наступления вторичной конечной точки, ее анализ не представляется возможным.
Анализ результатов опроса включенных пациентов по KCCQ показал лучшие результаты в группе пациентов с исходным ДЖ, получавших ЖКМ, уже через 3 мес. Доля пациентов с увеличением суммы балов по KCCQ на ≥5 баллов в группе ЖКМ на визите 3 мес. составил 36,4%, в то время как в группе СЖ — 18%, в контрольной группе — 17,2% пациентов (р=0,002). На всех визитах доля пациентов с увеличением суммы баллов на ≥5 пунктов была достоверно выше в группе ЖКМ в сравнении с группой СЖ. Доля пациентов со значимым увеличением суммы баллов на ≥10 пунктов была достоверно выше в группе ЖКМ на визитах 6 и 12 мес. (табл. 8).
Таблица 8
Изменение суммы балов по KCCQ для больных кардиомиопатиями за 12 мес. наблюдения
|
Изменение суммы балов |
Визит |
ЖКМ, n (%) |
СЖ, n (%) |
Пациенты без ДЖ, n (%) |
p |
|
Δ ≥5 |
3 мес. |
36 (36,4%) |
18 (18%) |
17 (17,2%) |
0,002 |
|
6 мес. |
49 (49,5%) |
26 (26%) |
39 (39,4%) |
0,003 |
|
|
12 мес. |
50 (50,5%) |
26 (26%) |
50 (50,5%) |
<0,001 |
|
|
Δ ≥10 |
3 мес. |
16 (16,2%) |
16 (16%) |
15 (15,2%) |
0,971 |
|
6 мес. |
44 (44,4%) |
19 (19%) |
32 (32,3%) |
<0,001 |
|
|
12 мес. |
45 (45,5%) |
22 (22%) |
36 (36,4%) |
0,003 |
Сокращения: ДЖ — дефицит железа, ЖКМ — железа карбоксимальтозат, СЖ — сульфат железа.
Отдельно был проведен анализ достижения ПКТ среди пациентов группы контроля с исходным нормальным уровнем железа и развившимся за период наблюдения ДЖ в сравнении с пациентами с исходным ДЖ, получавшими препараты железа. Среди 24 пациентов с развившимся ДЖ ПКТ наступила у 6 (25%) пациентов (рис. 3). В группах лечения препаратами железа суммарно ПКТ наступила у 111 (55,8%, р=0,009). Риск наступления ПКТ у пациентов с ИМ и ДЖ на фоне лечения препаратами железа составил 3,12 (95% доверительный интервал: 1,12; 8,72, р=0,024).

Рис. 3. Кумулятивная частота наступления ПКТ в группах лечения и у пациентов группы контроля с развившимся за период наблюдения ДЖ.
Сокращение: ДЖ — дефицит железа.
Обсуждение
Настоящее исследование на сегодняшний день является наиболее крупным рандомизированным проспективным клиническим исследованием по оценке влияния препаратов железа на систолическую функцию ЛЖ у пациентов с ДЖ, перенесших ИМ, и первым, в котором проводилось сравнение влияния внутривенного введения ЖКМ и перорального применения СЖ на систолическую функцию ЛЖ, нежелательные сердечно-сосудистые события и качество жизни пациентов [12].
Среди пациентов с ДЖ чаще встречалась ФП, что в определенной мере подтвердило ранее полученные нами данные о большей частоте развития пароксизмов ФП после кардиоверсии у пациентов с ДЖ [18]. Среди пациентов с исходным ДЖ, его компенсация через 3 мес. лечения достоверно чаще наблюдалась в группе ЖКМ, чем в группе СЖ (72,7% (72) и 36% (36) пациентов, соответственно, р<0,001). Результаты настоящего исследования демонстрируют аналогичное улучшение систолической функции, оцениваемой по уменьшению величины ИСПМ ЛЖ, у пациентов с ИМ без ДЖ и у пациентов с исходным ДЖ, получавших препараты железа. Различий между группами ЖКМ и СЖ по достижению ПКТ за 12 мес. наблюдения не было. Развитие ДЖ у 24 (19,5%) пациентов из числа группы контроля с исходно нормальным уровнем железа и не получавших ЖКМ или СЖ, позволило нам провести дополнительный анализ наступления ПКТ среди этих пациентов и сравнить с группами лечения. Частота наступления ПКТ была значимо выше у пациентов с ИМ и ДЖ, получавших препараты железа, чем у пациентов с ДЖ, не получавших препараты железа. Лечение препаратами железа более, чем в 3 раза повышало шанс улучшения систолической функции ЛЖ у пациентов с ДЖ. В данном исследовании были in vivo подтверждены данные, полученные in vitro, о негативном влиянии ДЖ на миокард [3][4] и возможности улучшения его систолической функции при помощи препаратов железа [3][4][7].
Улучшение качества жизни, оценивавшееся по KCCQ для больных кардиомиопатиями, наблюдалось достоверно чаще в группе пациентов с исходным ДЖ, получавших ЖКМ, чем в группе лечения СЖ и в группе контроля без ДЖ. Таким образом, данное исследование показало значительное преимущество ЖКМ в улучшении качества жизни у пациентов с ИМ и ДЖ.
Полученные результаты свидетельствуют о необходимости выявления ДЖ у пациентов с острым ИМ и его коррекции препаратами железа. Применение внутривенно ЖКМ показало лучший результат, чем пероральный СЖ в достижении коррекции ДЖ и улучшении качества жизни пациентов с ИМ и ДЖ. Улучшение систолической функции ЛЖ, оцениваемое по снижению ИСПМ ЛЖ, было аналогичным в группах лечения препаратами железа и у пациентов с отсутствием ДЖ, а среди пациентов с ДЖ без его лечения наблюдалось значимо реже. Таким образом, возникает вопрос о необходимости внесения дополнений в клинические рекомендации по ИМ, посвященных выявлению и коррекции ДЖ. Вместе с тем представляет большой интерес проведение новых рандомизированных клинических исследований с включением большего числа пациентов с ИМ и ДЖ и с твердыми сердечно-сосудистыми конечными точками в качестве ПКТ исследования.
Ограничения исследования. Основным ограничением исследования OPERA-MI было небольшое число пациентов. Еще одним ограничением явилось малое количество случаев наступления вторичной составной конечной точки, включавшей смерть от сердечно-сосудистых заболеваний, нефатальные ИМ и инсульт, госпитализацию по поводу декомпенсации сердечной недостаточности, не позволившее провести анализ твердых конечных точек.
Заключение
В исследовании OPERA-MI лечение пациентов с ИМ и ДЖ препаратами железа привело к аналогичной частоте наступления ПКТ (снижению ИСПМ ЛЖ) в группах лечения ЖКМ, СЖ и у пациентов без ДЖ. Не было преимущества какого-либо препарата железа. У пациентов с ИМ и ДЖ, не получавших препаратов железа, улучшение систолической функции ЛЖ наблюдалось значимо реже, чем в группах лечения ЖКМ и СЖ. Лечение ЖКМ ассоциировано с существенным улучшением качества жизни пациентов, чем лечение СЖ.
Отношения и деятельность. Финансирование исследования осуществляется за счёт спонсорской поддержки компании Вифор (Интернэшнл) Инк., Швейцария.
1. WHO Factsheet on Cardiovascular Diseases. https://www.who.int/news-room/fact-sheets/detail/cardiovascular-diseases-(cvds).
Список литературы
1. Miller JL. Iron deficiency anemia: A common and curable disease. Cold Spring Harb Perspect Med. 2013;3(7):a011866. doi:10.1101/cshperspect.a011866.
2. Haddad S, Wang Y, Galy B, et al. Iron-regulatory proteins secure iron availability in cardiomyocytes to prevent heart failure. Eur Heart J. 2017;38:362-72. doi:10.1093/eurheartj/ehw333.
3. Inserte J, Barrabés JA, Aluja D, et al. Implications of iron deficiency in STEMI patients and in a murine model of myocardial infarction. JACC Basic Transl Sci. 2021;6:567-80. doi:10.1016/j.jacbts.2021.05.004.
4. Reinhold J, Papadopoulou C, Baral R, Vassiliou VS. Iron deficiency for prognosis in acute coronary syndrome — A systematic review and meta-analysis. Int J Cardiol. 2021;328:46-54. doi:10.1016/j.ijcard.2020.12.021.
5. Huang C, Chang CC, Kuo CL, et al. Serum Iron Concentration, but Not Hemoglobin, Correlates with TIMI Risk Score and 6-Month Left Ventricular Performance after Primary Angioplasty for Acute Myocardial Infarction. PLOS ONE. 2014;9(8):e104495. doi:10.1371/journal.pone.0104495.
6. Corradi F, Masini G, Bucciarelli T, De Caterina R. Iron deficiency in myocardial ischaemia: molecular mechanisms and therapeutic perspectives. Cardiovascular Research. 2023;119:2405-20. doi:10.1093/cvr/cvad146.
7. Florian A, Ludwig A, Rösch S, et al. Positive effect of intravenous iron-oxide administration on left ventricular remodelling in patients with acute ST-elevation myocardial infarction — a cardiovascular magnetic resonance (CMR) study. Int. J. Cardiol. 2014;173;184-9. doi:10.1016/j.ijcard.2014.02.016.
8. Jankowska EA, Kirwan BA, Kosiborod M, et al. The effect of intravenous ferric carboxymaltose on health-related quality of life in iron-deficient patients with acute heart failure: the results of the AFFIRM-AHF study. Eur Heart J. 2021;42(31):3011-20. doi:10.1093/eurheartj/ehab234.
9. Ponikowski, P, Kirwan BA, Anker SD, et al. Ferric Carboxymaltose for Iron Deficiency at Discharge after Acute Heart Failure: A Multicentre, Double-Blind, Randomised, Controlled Trial. Lancet. 2020;396:1895-904. doi:10.1016/S0140-6736(20)32339-4.
10. Kalra PR, Cleland JGF, Petrie MC, et al. Intravenous Ferric Derisomaltose in Patients with Heart Failure and Iron Deficiency in the UK (IRONMAN): An Investigator-Initiated, Prospective, Randomised, Open-Label, Blinded-Endpoint Trial. Lancet. 2022;400:2199-209. doi:10.1016/S0140-6736(22)02083-9.
11. Misiewicz A, Badura K, Matuszewska-Brycht O, et al. Iron Deficiency as a Factor of Worse Prognosis in Patients with Acute Myocardial Infarction. Biomedicines. 2025;13:769. doi:10.3390/biomedicines13040769.
12. Хастиева Д. Р., Малкова М. И., Закирова Э. Б. и др. Обоснование и дизайн открытого проспективного рандомизированного исследования эффективности терапии дефицита железа c использованием препаратов железа для внутривенного введения по сравнению с приемом пероральных препаратов железа с целью улучшения систолической функции левого желудочка у пациентов с инфарктом миокарда (OPERA-MI). Российский кардиологический журнал. 2022;27(S2):4961. doi:10.15829/1560-4071-2022-4961. EDN: KBMJME.
13. Thygesen K, Alpert JS, Jaffe AS, et al. Fourth universal definition of myocardial infarction (2018). Circulation. 2018;138(20):e618-e651. doi:10.1161/CIR.0000000000000617.
14. Аверков О. B., Арутюнян Г. К., Дупляков Д. В. и др. Острый инфаркт миокарда с подъемом сегмента ST электрокардиограммы. Клинические рекомендации 2024. Российский кардиологический журнал. 2025;30(3):6306. doi:10.15829/1560-4071-2025-6306. EDN: IVJCUK.
15. Аверков О. B., Арутюнян Г. К., Дупляков Д. В. и др. Острый коронарный синдром без подъема сегмента ST электрокардиограммы. Клинические рекомендации 2024. Российский кардиологический журнал. 2025;30(5):6319. doi:10.15829/1560-4071-2025-6319. EDN: CXJUIB.
16. Okyay K, Tavil Y, Sahinarslan A, et al. Plasma osteopontin levels in prediction of prognosis in acute myocardial infarction. Acta Cardiol. 2011;66(2):197-202. doi:10.1080/ac.66.2.2071251.
17. Green CP, Porter CB, Bresnahan DR, et al. Development and evaluation of the Kansas City Cardiomyopathy Questionnaire: A new health status measure for heart failure. J. Am. Coll. Cardiol. 2000;35:1245-55. doi:10.1016/S0735-1097(00)00531-3.
18. Валеев М. Х., Хасанов Н. Р. Ассоциация дефицита железа с развитием рецидивов фибрилляции предсердий после фармакологической кардиоверсии. Российский кардиологический журнал. 2023;28(2S):5369. doi:10.15829/1560-4071-2023-5369. EDN BZYOCD.
Об авторах
Д. Р. ХастиеваРоссия
К.м.н., старший преподаватель кафедры пропедевтики внутренних болезней им. проф. С. С. Зимницкого
ул. Маршала Чуйкова, д. 54, корп. 2, Казань
Н. А. Тарасова
Россия
Ассистент кафедры пропедевтики внутренних болезней им. проф. С. С. Зимницкого
ул. Маршала Чуйкова, д. 54, корп. 2, Казань
Н. Р. Хасанов
Россия
Д.м.н., профессор, зав. кафедрой пропедевтики внутренних болезней им. проф. С. С. Зимницкого
ул. Маршала Чуйкова, д. 54, корп. 2, Казань
М. С. Кузнецов
Россия
Старший лаборант кафедры пропедевтики внутренних болезней им. проф. С. С. Зимницкого
ул. Маршала Чуйкова, д. 54, корп. 2, Казань
И. Х. Валеева
Россия
Д.б.н., с.н.с. центральной научно-исследовательской лаборатории
ул. Маршала Чуйкова, д. 54, корп. 2, Казань
Л. И. Капралова
Россия
Старший лаборант кафедры пропедевтики внутренних болезней им. проф. С. С. Зимницкого
ул. Маршала Чуйкова, д. 54, корп. 2, Казань
Э. Б. Закирова
Россия
К.м.н., зам. главного врача по диагностике
ул. Маршала Чуйкова, д. 54, корп. 2, Казань
М. И. Малкова
Россия
К.м.н., ассистент кафедры пропедевтики внутренних болезней им. проф. С. С. Зимницкого, зав. отделением функциональной диагностики
ул. Маршала Чуйкова, д. 54, корп. 2, Казань,
ул. Маршала Чуйкова, д. 54, корп. 2, Казань
Ю. А. Клюшкина
Россия
Зав. отделением ультразвуковой диагностики
ул. Маршала Чуйкова, д. 54, корп. 2, Казань
- Лечение дефицита железа (ДЖ) у пациентов с инфарктом миокарда (ИМ), независимо от способа коррекции, позволило достичь аналогичное с группой пациентов без ДЖ количество случаев улучшения систолической функции левого желудочка.
- У пациентов с ИМ и ДЖ, не получавших препараты железа, наблюдалась меньшая частота улучшения систолической функции левого желудочка, по сравнению с пациентами, у которых проводилась коррекция ДЖ. Эти данные подчеркивают необходимость скрининга на наличие ДЖ и его коррекции у пациентов с ИМ.
- Лечение железа карбоксимальтозатом ассоциировано с существенным улучшением качества жизни пациентов с ИМ и ДЖ, чем лечение сульфатом железа.
Рецензия
Для цитирования:
Хастиева Д.Р., Тарасова Н.А., Хасанов Н.Р., Кузнецов М.С., Валеева И.Х., Капралова Л.И., Закирова Э.Б., Малкова М.И., Клюшкина Ю.А. Коррекция дефицита железа у пациентов с инфарктом миокарда: открытое проспективное исследование эффективности терапии дефицита железа с использованием препаратов железа для внутривенного введения по сравнению с приемом пероральных препаратов железа с целью оценки влияния на систолическую функцию левого желудочка у пациентов с инфарктом миокарда OPERA-MI. Российский кардиологический журнал. 2026;31(2):6759. https://doi.org/10.15829/1560-4071-2026-6759. EDN: QAEGHC
For citation:
Khastieva D.R., Tarasova N.A., Khasanov N.R., Kuznetsov M.S., Valeeva I.Kh., Kapralova L.I., Zakirova E.B., Malkova M.I., Klyushkina Yu.A. Iron deficiency treatment in patients with myocardial infarction: an open-label, prospective study of the efficacy of intravenous iron versus oral iron therapy to evaluate the impact on left ventricular systolic function in patients with myocardial infarction (OPERA-MI). Russian Journal of Cardiology. 2026;31(2):6759. (In Russ.) https://doi.org/10.15829/1560-4071-2026-6759. EDN: QAEGHC
JATS XML


















































