Перейти к:
Медикаментозная терапия фибрилляции предсердий. Стратегия "контроль ритма" (обзор)
https://doi.org/10.15829/1560-4071-2025-6709
EDN: TRARTN
Аннотация
Фибрилляция предсердий (ФП) является наиболее распространенной наджелудочковой тахиаритмией и ассоциируется с ростом сердечно-сосудистых осложнений и смертности. Современная парадигма ведения пациентов смещается от стратегии "контроль частоты" к раннему и проактивному "контролю ритма", что подтверждено крупными рандомизированными исследованиями и актуальными европейскими и российскими рекомендациями. В обзоре рассмотрены патофизиологические основы аритмогенеза при ФП, включая уровни электрического, механического, структурного и вегетативного ремоделирования предсердий, а также ключевые механизмы инициации и поддержания аритмии (эктопическая активность, ре-ентри, триггерная активность/поздние постдеполяризации). Особое внимание уделено фармакологической стратегии контроля ритма с использованием антиаритмических препаратов I и III классов по Vaughan-Williams: анализируются молекулярные мишени, фармакокинетика, клиническая эффективность и профиль безопасности пропафенона, флекаинида, лаппаконитина гидробромида (аллапинина), этацизина, амиодарона, соталола и др., включая препараты, доступные преимущественно в России. На основе текущих данных и рекомендаций предложен алгоритмический подход к выбору противорецидивной терапии с учётом фенотипа пациента (пароксизмальная или персистирующая ФП, наличие структурной патологии миокарда, сердечной недостаточности, ишемической болезни сердца, гипертрофии левого желудочка), уровня ремоделирования предсердий, особенностей проводящей системы, коморбидности и лекарственных взаимодействий. Отдельно обсуждаются принципы антиаритмической терапии в ранний период после кардиоверсии и после катетерной изоляции устьев легочных вен как части гибридной стратегии (инвазивное + медикаментозное лечение). Представленный обзор ориентирован на практикующего кардиолога и аритмолога и призван облегчить индивидуализацию выбора антиаритмических препаратов в рамках безопасной и эффективной стратегии контроля ритма при ФП.
Ключевые слова
Для цитирования:
Тарасов А.В., Казанцева Е.В. Медикаментозная терапия фибрилляции предсердий. Стратегия "контроль ритма" (обзор). Российский кардиологический журнал. 2025;30(4S):6709. https://doi.org/10.15829/1560-4071-2025-6709. EDN: TRARTN
For citation:
Tarasov A.V., Kazantseva E.V. Pharmacotherapy for atrial fibrillation. The rhythm control strategy (review). Russian Journal of Cardiology. 2025;30(4S):6709. (In Russ.) https://doi.org/10.15829/1560-4071-2025-6709. EDN: TRARTN
Фибрилляция предсердий (ФП) является наиболее распространенной тахиаритмией в клинической практике и ассоциируется с повышенным риском развития сердечно-сосудистых событий и смертности. Высокая распространенность и сложность терапии обусловлены мультифакторностью причин и неполным пониманием механизмов аритмогенеза, которые могут трансформироваться и сочетаться, поддерживая устойчивые формы нарушения ритма [1]. В настоящий момент при ведении пациентов с ФП общеприняты три взаимодополняющих стратегии:
- стратегия контроля ритма (поддержание синусового ритма (СР) путем купирования пароксизмов и профилактики рецидивов антиаритмическими препаратами (ААП) и/или хирургическими методами лечения);
- стратегия контроля частоты (урежение частоты сокращений желудочков на фоне сохраняющейся ФП препаратами для контроля частоты сердечных сокращений (ЧСС));
- профилактика тромбоэмболических осложнений (ТЭО) у пациентов с повышенным риском, применяемая вне зависимости от выбора стратегии ритма или частоты.
Цель обзора — обобщить современную доказательную базу и клинические рекомендации по фармакологическому контролю ритма при ФП, сфокусировавшись на роли ААП I и III классов, и предложить практико-ориентированный алгоритм выбора противорецидивной терапии с учетом фенотипа пациента, коморбидности, уровня ремоделирования предсердий и предполагаемого механизма аритмогенеза.
Настоящая работа представляет собой нарративный (аналитический) обзор литературы. Поиск публикаций проводился в базах данных eLIBRARY, PubMed/MEDLINE, Cochrane Library, Embase с использованием сочетаний ключевых слов на английском и русском языках: atrial fibrillation, rhythm control, antiarrhythmic drugs, class IC, class III, amiodarone, sotalol, "фибрилляция предсердий", "контроль ритма", "антиаритмические препараты", "класс IС", "класс III" и др. В обзор преимущественно включены международные и национальные клинические рекомендации, рандомизированные контролируемые исследования, метаанализы и крупные наблюдательные регистры, опубликованные преимущественно за период 2000-2024гг, а также классические экспериментальные работы, заложившие основы представлений о ремоделировании предсердий и механизмах аритмогенеза. Особое внимание уделено последним рекомендациям Европейского общества кардиологов по ведению пациентов с ФП, российским клиническим рекомендациям 2025г и ключевым исследованиям, определяющим стратегию раннего контроля ритма (включая EAST-AFNET 4). Анализ выполнялся с позиций клинической применимости для практикующего кардиолога и аритмолога с фокусом на выборе ААП для противорецидивной терапии в различных клинико-патофизиологических сценариях (пароксизмальная, персистирующая ФП, структурное заболевание сердца, постаблационный период).
Последние десятилетия шла дискуссия о преимуществах контроля ритма против контроля частоты. Два классических рандомизированных исследования — AFFIRM (Atrial Fibrillation Follow-up Investigation of Rhythm Management) (2002) и RACE (Rate Control versus Electrical cardioversion) (2002) — сформировали исходную парадигму, согласно которой стратегия контроля ритма не продемонстрировала преимуществ над контролем частоты по выживаемости и крупным сердечно-сосудистым событиям. В исследовании AFFIRM (n=4060, пожилые пациенты с факторами риска инсульта) стратегия восстановления/поддержания СР ААП и повторными кардиоверсиями не сопровождалась снижением общей смертности по сравнению с контролем ЧСС, при этом частота госпитализаций и лекарственных нежелательных явлений были выше [2]. В исследовании RACE (n=522) было показано, что у пациентов с персистирующей ФП после кардиоверсии контроль частоты оказался не хуже контроля ритма по комбинированной конечной точке (сердечно-сосудистая смертность, сердечная недостаточность (СН), инсульт/эмболии, кровотечения, побочные эффекты ААП), при меньшей потребности в госпитализациях и вмешательствах. Важно, что в эпоху AFFIRM/RACE антикоагуляция и стратегии предупреждения ТЭО были менее стандартизированы, что могло повлиять на исходы [3][4].
Современная парадигма сместилась в сторону раннего контроля ритма. Исследование EAST-AFNET 4 (2020) продемонстрировало, что ранняя стратегия контроля ритма, начатая в течение 12 мес. от дебюта ФП (медиана ~5 нед.), снизила риск первичной комбинированной конечной точки (сердечно-сосудистая смерть, инсульт, госпитализация по поводу декомпенсации СН или острого коронарного синдрома) по сравнению со стандартной тактикой (отношение рисков 0,79; 96% доверительный интервал: 0,66-0,94; p=0,005), при сопоставимой частоте серьезных нежелательных явлений [5]. Терапевтическая программа включала ААП первого/второго ряда и катетерную аблацию. По данным анализа, достижение и поддержание СР ассоциировано с лучшими исходами, включая подгруппы с симптомами/признаками СН [6][7]. Таким образом, ранняя инициация контроля ритма не только уменьшает симптомы, но и улучшает прогноз у пациентов с ФП, останавливая риск развития осложнений за счет замедления электрического и структурного ремоделирования предсердий, сохранения насосной функции и улучшения гемодинамики. Другой вопрос, как добиться эффективной и самое главное безопасной стратегии "контроля ритма"!
Выбор противорецидивной терапии основывается на:
- клиническом течении аритмии;
- терапии и контроле коморбидных состояний, создающих субстрат ФП;
- степени ремоделирования левого предсердия (ЛП)/левого желудочка (ЛЖ) и состоянии проводящей системы сердца;
- преобладающем механизме аритмогенеза на текущем этапе.
Выбор стратегии лечения ФП прежде всего зависит от клинического течения аритмии. Согласно Российским клиническим рекомендациям по терапии фибрилляции и трепетания предсердий 2025г стратегия контроля ритма обоснована у симптомных пациентов или при негативном влиянии аритмии на гемодинамику и течение коморбидных заболеваний, в этих случаях восстановление СР и противорецидивная терапия целесообразны для уменьшения симптомов и улучшения гемодинамики. У пациентов с бессимптомным течением аритмии, удовлетворительной переносимостью типичных физических нагрузок и отсутствием нарушений гемодинамики в первую очередь следует рассматривать профилактику ТЭО и стратегию контроля частоты [8]. Принятие решения о переходе к контролю ритма должно осуществляться в рамках совместного обсуждения с пациентом после разъяснения потенциальных выгод/рисков и динамической оценки функционального состояния сердца. Переоценка показаний проводится после периода наблюдения и оптимизации факторов риска, фиксированный порог времени не регламентирован.
Каким пациентам с ФП требуется назначение противорецидивной терапии ААП? Прежде чем ответить, уточним критерии эффективности антиаритмической терапии (ААТ): основная задача ААП при пароксизмальной ФП — снижение бремени аритмии (частоты, длительности и выраженности приступов) и тем самым улучшение симптомов/качества жизни, а не полное подавление эпизодов аритмии. Если пароксизмы ФП редкие (<1-2 раза в год) или первый эпизод протекает гемодинамически стабильно, постоянная противорецидивная терапия обычно не показана [9]. В этом случае приоритет — устранение модифицируемых триггеров/субстратов (артериальной гипертензии (АГ), ночного апноэ, избыточной массы тела, злоупотребление алкоголя, кофеина/симпатомиметиков, коррекция электролитов, тиреоидной дисфункции и т.п.) и оценка показаний к антикоагулянтной терапии по риску ТЭО. Возможна стратегия "таблетка в кармане" для редких симптомных эпизодов у пациентов без структурного поражения сердца (пропафенон в сочетании с атриовентрикулярным (АВ)-узловым блокатором) [1]. Постоянную ААТ целесообразно рассматривать при частых (≥3 раз в год), устойчивых формах или рецидивах с выраженным влиянием на гемодинамику, либо по предпочтению пациента после информированного обсуждения.
Терапия основного заболевания или состояний, которые создали условия для нарушений ритма сердца — это и есть основа противорецидивной терапии. ААТ модифицирует электрические свойства миокарда и подавляет патологические триггеры, но если не воздействовать на факторы, поддерживающие аритмогенез, то эффект ААП будет ограниченным и со временем станет "ускользающим". С другой стороны, на фоне нескорректированных коморбидных факторов риск проаритмии возрастает. Поэтому комплекс: терапия основного заболевания + таргетное подавление аритмии — ключ к эффективной и безопасной противорецидивной стратегии [10].
Нарушения ритма в большинстве случаев это вторичные состояния и развиваются на фоне кардиальной или экстракардиальной патологии, усугубляя ее течение и иногда становясь прямой причиной осложнений этих заболеваний [8][10]. ФП возникает, когда структурные и электрофизиологические изменения в предсердиях создают субстрат для формирования и распространения патологических импульсов. Такие изменения чаще развиваются на фоне АГ, ишемической болезни сердца (ИБС) или СН, что ведет к диастолической дисфункции ЛЖ, повышению давления в ЛП и электрической нестабильности предсердий [11]. У этих пациентов активируется ренин-ангиотензин-альдостероновая система, что способствует к ремоделированию межклеточных соединений и изменению ионных токов, повышая склонность к аритмиям [12]. Существенна и роль автономной нервной системы — дисбаланс симпатического и парасимпатического тонуса может инициировать/поддерживать ФП [1][11]. Были получены подтверждения участия вегетативной дисрегуляции в инициации ФП и доказательства, что симпатическая стимуляция повышает внутриклеточный Ca²⁺ (запуская триггерную/автоматическую активность). У пациентов без структурной патологии сердца при высоком парасимпатическом тонусе (обильный прием пищи перед сном, ночное апноэ и др.) может возникать аритмия — вагус-индуцированная ФП [11][13].
Принципы терапии ФП у коморбидных больных:
- коморбидность определяет выбор стратегии (ритм/частота контроль) и эффективность и безопасность ААТ. Приоритет — коррекция основного заболевания и модифицируемых факторов риска (АГ, ожирение, синдром обструктивного апноэ сна, тиреоидная дисфункция и др.);
- перед выбором ААТ требуется уточнить степень функциональных нарушений и наличие структурной болезни сердца (эхокардиография/магнитно-резонансная томография по показаниям), чтобы подобрать эффективную и безопасную противорецидивную терапию;
- полипрагмазия у коморбидных пациентов повышает риск лекарственных взаимодействий и побочных эффектов, затрудняет контроль эффективности и снижает приверженность — необходима регулярная "лекарственная ревизия" [10].
Выбор противорецидивной терапии зависит от наличия и степени ремоделирования сердца
В последних рекомендациях четко обозначена концепция раннего контроля ритма, т.к. чем дольше длится ФП, тем труднее восстановить СР фармакологическими или электрическими методами и удерживать его в дальнейшем [13]. По данным Kato T, et al. (2014), при 14-летнем наблюдении независимо от схем ААТ ФП у значимой доли пациентов прогрессировала в постоянную форму (кумулятивно 77,2%; ~5,5% в год) [14]. Ключевой механизм — самоподдерживающееся ремоделирование предсердий, при котором "ФП порождает ФП". В связи с этим терапия должна быть направлена на удержание СР и профилактику перехода пароксизмальной ФП в персистирующую/постоянную. Концепция ремоделирования предсердий включает несколько уровней: электрическое ремоделирование (изменения электрофизиологических свойств), механическое ремоделирование (снижение сократимости, дилатация), структурное ремоделирование (гибель кардиомиоцитов, интерстициальный фиброз) и вегетативные изменения [15].
Электрическое ремоделирование. В эксперименте Wijffels MC, et al. (1995) показали, что при поддержании ФП ≥24 ч эффективный рефрактерный период (ЭРП) предсердий значимо укорачивается и нарушается нормальная частотно-зависимая адаптация ЭРП. После восстановления СР через ~1 нед. эти параметры в значительной степени нормализуются [16]. В клинических исследованиях Franz MR, et al. (1997) продемонстрировали сокращение длительности потенциала действия (ПД) кардиомиоцитов ЛП при продолжительной стимуляции, что подтверждает формирование электрического ремоделирования [17][18]. На ионном уровне доминирует снижение тока L-типа Ca²⁺ (ICaL), что объясняет укорочение ПД и ЭРП при тахикардии. Электрическое ремоделирование способствует ранним рецидивам ФП после кардиоверсии и прогрессированию аритмии [19]. При персистирующей форме ФП (длительность приступа аритмии >7 сут.) в большинстве случаев развивается электрическое ремоделирование предсердий, на рисунке 1 продемонстрировано как отличается ЭРП у пациентов, поступивших для инвазивного лечения аритмии с пароксизмальной ФП на СР и персистирующей формой аритмии [20].

Рис. 1. Изменение ПД и ЭРП у пациентов при СР (А) и персистирующей ФП (В), измеренных в правом предсердии, ЛП, легочных венах и области пограничного гребня, (С) продолжительность ПД у пациентов при СР и ФП, (D) максимальная скорость ПД (dV/dt) у пациентов при СР и ФП, (Е) величина потенциала покоя у пациентов при СР и ФП [20].
Сокращения: ЛВ — легочные вены, ЛП — левое предсердие, ППД — поздняя постдеполяризация, ПГ — пограничный гребень, ПП — правое предсердие, ППк — потенциал покоя СР — синусовый ритм, ФП — фибрилляция предсердий, dV/dt — максимальная скорость ПД.
Механическое ремоделирование. Перегрузка ЛП давлением/объемом (кардиопатии, клапанные болезни, СН) и высокая частота деполяризации при ФП приводят к растяжению стенки, снижению сократимости и дилатации ЛП [21]. Эти факторы формируют следующий уровень атриопатии. Электрическое и механическое ремоделирование могут развиваться параллельно, причем восстановление сократимости после купирования ФП занимает недели-месяцы (по данным эхокардиографии) [17].
Важно подчеркнуть, что электрическое и механическое ремоделирование в значительной степени обратимы, однако существенно влияют на эффективность ААТ и инвазивных методов противорецидивной терапии [22].
Структурное ремоделирование. При длительной ФП развивается фиброз, клеточная диссоциация и ультраструктурные изменения, что замедляет проведение и поддерживает механизмы повторного входа (ре-ентри) — электрофизиологическую основу устойчивых форм ФП [23]. Важно, что структурное ремоделирование может быть следствием не только персистирующей ФП, но и иных состояний (воспаление, амилоидоз, токсические влияния), приводящих к необратимому замещению миокарда фиброзом, у таких пациентов даже первый эпизод ФП может быть резистентным к купирующей и противорецидивной терапии [22].
Выбор противорецидивной терапии зависит от механизма аритмогенеза ФП
Немаловажным вопросом при выборе стратегии является понимание ремоделирования сердца, коморбидности и доминирующего механизма аритмогенеза, который у одного и того же пациента может меняться на разных этапах течения заболевания. Несмотря на достижения в технологиях и накопленные знания об ионных и физиологических основах аритмогенеза, механизмы инициации и поддержания ФП остаются многокомпонентными, что ограничивает возможность полного контроля аритмии лишь средствами ААТ и инвазивного лечения [24].
Инициация. Потенциальным механизмом запуска пароксизма ФП является быстрая активность эктопических предсердных фокусов (патологического автоматизма), при пароксизмальной форме ФП эктопический механизм преобладает. Степень ремоделирования предсердий определяет, станет ли эктопический пусковой момент основой для дальнейших механизмов поддержания [25-27].
Поддержание. В 1959г Moe GK, et al. (1959) описали "гипотезу множественных волн/роторов", расширив представления о роли повторного входа (ре-ентри) в инициировании и особенно в поддержании ФП [28]. Согласно этой теории, при наличии подходящего предсердного субстрата формируется критическое число возвращающихся фронтов возбуждения (роторов), их устойчивое существование ведет к самоподдерживающейся активации предсердий и дезорганизации активности миокарда предсердий (рис. 2). Различия локальной скорости проведения и рефрактерности в разных участках формируют хаотичную фибрилляционную проводимость (f-волны на электрокардиограмме (ЭКГ)). То есть механизм ре-ентри является вторым после эктопического в инициации, но и в поддержании ФП.

Рис. 2. Мембранные потенциалы располагаются по прямой линии (от A до D), проходящей по часовой стрелке по контуру ре-ентри в ткани предсердий, с продолжительностью цикла 105 миллисекунд [24].
Примечание: волокна 3 и 4, расположенные в центре круга, активизируются в 2 раза чаще, но они не достигают нормальной амплитуды и не могут распространяться за пределы центра круга, что делает его функционально невозбудимым, поскольку ткань постоянно деполяризуется.
Концепция "разные механизмы для запуска и поддержания". Признано, что инициируют ФП чаще эктопические очаги, а поддерживают ее различные формы микро-ре-ентри с длиной цикла, зависящей от рефрактерности предсердной ткани [29]. При продолжающейся ФП (в большинстве случаев >48) и нарастания хаотичных контуров ре-ентри предсердные миоциты теряют нормальную частотную адаптацию, формируется электрическое ремоделирование (укорочение ЭРП), что повышает число роторов и стабилизирует аритмию.
Триггерная активность. Предсердные кардиомиоциты при продолжающейся ФП начинают "экономить" на стадии расслабления (реполяризации). Эти процессы способствуют возникновению поздних постдеполяризаций (ППД) — третьему механизму аритмогенеза, а именно, триггерной активации. ППД возникают после завершения реполяризации мембраны и связаны с перегрузкой Ca²⁺: ишемия, β-адренергическая стимуляция, гипокальциемия внеклеточная, тахикардия и др. [30][31]. Чем выше частота, тем короче интервал до триггерного ответа и чаще эпизоды ППД, что поддерживает персистирование ФП.
О границе персистирующей ФП. Персистирующая ФП определяется как эпизод, продолжающийся >7 сут. или требующий кардиоверсии, клиническая граница 7 сут. соответствует периоду, к которому электрическое ремоделирование обычно уже закрепляется, преобладает механизм триггерной активации и спонтанное восстановление СР маловероятно. Купирование на этом этапе чаще требует электрической или фармакологической кардиоверсии ААП III класса.
Клиническое значение. Сложность лечения ФП обусловлена вкладом трех механизмов (эктопический механизм, ре-ентри, триггерная активность/ППД), которые по-разному доминируют на разных стадиях. Задача врача — идентифицировать ведущий механизм, оценить стадию ремоделирования предсердий, состояние проводящей системы и контроль коморбидности, чтобы выбрать наиболее эффективную и безопасную противорецидивную стратегию.
ААП для противорецидивной терапии ФП
Согласно Российским рекомендациям по диагностике и лечению ФП 2025г выбор ААП в большей степени определяется аспектами безопасности, а не эффективностью препарата [8].
ААП традиционно разделяются по классификации предложенной E. M. Vaughan-Williams в 1970 г. ААП представлены в таблице 1.
Таблица 1
Классификация ААП Vaughan-Williams (с изменениями и дополнениями [8][32][33])
|
Класс I. Препараты, блокирующие натриевые каналы |
|
|
Класс IА. Умеренное замедление проведения, умеренное удлинение ПД |
Хинидин Прокаинамид |
|
Класс IВ. Минимальное замедление проведения, укорочение ПД |
Лидокаин Мексилетин Фенитоин** |
|
Класс IС. Выраженное замедление проведения, минимальное удлинение ПД |
Пропафенон Флекаинид Этацизин* Аллапинин (Лаппаконитинна гидробромид)* |
|
Класс II. β-адреноблокаторы |
Пропраналол Атенолол Метопролол Бисопролол |
|
Класс III. Препараты блокирующие калиевые каналы, удлиняющие ПД |
Амиодарон Соталол Ибутилид** Дофетилид** Рефралон* |
|
Класс IV. Препараты блокирующие кальциевые каналы |
Верапамил Дилтиазем |
Примечание: * — лекарственные препараты зарегистрированы только в России и странах СНГ, ** — лекарственные препараты в России не зарегистрированы и аналогов нет.
Сокращение: ПД — потенциал действия.
Классификация Vaughan-Williams не дает точной характеристики каждого ААП и носит несколько условный характер, т.к. ААП часто оказывают смешанное действие на сердечные клетки, т.к. в той или иной степени могут обладать свойствами различных классов, соответственно препараты одной и той же группы могут проявлять себя различными электрофизиологическими эффектами, однако с доминирующим влиянием на одни ионные каналы своего класса. С другой стороны, воздействие одного и того же ААП на разные состояния миокарда с нормальным функционированием без органической патологии сердца или на миокард с патологическими нарушениями проводимости, может приводить к противоположному эффекту и вызывать новые, порой опасные аритмии, так называемые "проаритмии" или другие гемодинамические осложнения [34].
Важность и популярность классификации обусловлена способностью характеризовать различные эффекты препаратов, особенно I и III классов на Na- и K-каналы, а значит, на скорость проведения и рефрактерные периоды. Она предлагает общую схему характеристики даже для препаратов, трудно поддающихся классификации, что делает ее удобной для практического применения. На основные механизмы аритмогенеза ФП влияют ААП I и III классов, препараты II и IV классов применяются для стратегии "частота контроль" или сочетаются с основными ААП при противорецидивной терапии для безопасности первых и усиления антиаритмических эффектов.
Роль и место I класса ААП в стратегии контроля ритма при ФП
В современной парадигме контроля ритма у пациентов с пароксизмальной ФП ААП I класса занимают нишу преимущественно за счет подгруппы IС (пропафенон, флекаинид), они эффективны для фармакологической кардиоверсии и поддержания СР у тщательно отобранных пациентов без значимого структурного поражения миокарда [1][8][12]. Применение противопоказано при клинически значимом структурном заболевании сердца (ИБС с постинфарктным рубцом, выраженная гипертрофия ЛЖ (ГЛЖ), сниженная фракции выброса (ФВ) ЛЖ) из-за риска проаритмии и повышения смертности, что исторически показано в исследовании CAST (энкаинид/флекаинид после инфаркта миокарда (ИМ)) [35]. Подгруппы IА (хинидин, прокаинамид, дизопирамид) и IВ (лидокаин, мексилетин) имеют ограниченное применение при ФП, их рутинное использование для противорецидивной терапии не рекомендуется современными руководствами [1][8][12].
ААП I класса
ААП I класса — блокаторы быстрых, управляемых напряжением Na⁺-каналов Nav1.5 (SCN5A) с преобладанием частотно-зависимого эффекта (use-dependent): при высокой ЧСС блокада канала усиливается, снижается скорость нарастания фазы 0 (Vmax) и замедляется проведение (расширение QRS) [36]. Подклассы различаются по кинетике связывания/диссоциации с каналом, влиянию на длительность ПД и ЭРП [36][37] (рис. 3).

Рис. 3. Влияние ААП классов IА, IВ и IС (пунктирные линии) на потенциалы активности кардиомиоцитов (фиолетовые линии).
ААП IC класса. Характеризуются "медленной" кинетикой диссоциации, выраженно замедляют проведение в предсердиях и в триггерных зонах, включая устья легочных вен (УЛВ) [1]. Влияние на ЭРП минимальное, поэтому в редких случаях возможна организация ФП в трепетание предсердий (ТП) — рассмотреть сопутствующий АВ-узловой блокатор (β-блокатор или недигидропиридиновые блокаторы кальциевых каналов (БКК)) [1][12]. Эффективны для купирования (пропафенон) и поддержания ритма у пациентов без выраженного структурного поражения миокарда, возможна стратегия "таблетка в кармане" [1][38]. Противопоказаны при ИБС с постинфарктным рубцом/ишемией, выраженной ГЛЖ, сниженной ФВ ЛЖ, синдроме Бругада [1][12]. Инициация и титрация требуют ЭКГ-контроля: увеличение QRS >25% от исходного и/или абсолютный QRS >120-150 мс, PR ≥240 мс — повод к снижению дозы/отмене, QTc ≥500 мс также требует пересмотра терапии, учитывая вклад расширения QRS в расчет QTc [1][12].
Пропафенон
Механизм действия. Блокатор быстрых, управляемых напряжением Na⁺-каналов Nav1.5 (SCN5A) с выраженной частотно-зависимой блокадой, дополнительно обладает слабой β-адреноблокирующей активностью [39]. Замедляет деполяризацию фазы 0, снижает Vmax и внутрипредсердное/внутрижелудочковое проведение, что может проявляться удлинением PR и редко расширением QRS, на QTc нет прямого влияния, а прямое воздействие на реполяризацию в терапевтических дозах минимально [36]. Замедляет проведение по дополнительным путям проведения, удлиняет внутрисердечные интервалы AH (проведение через АВ-узел) и HV (проведение по системе Гиса-Пуркинье) [40]. За счет уменьшения скорости проведения и легкого увеличения эффективной рефрактерности возрастает длина волны возбуждения, когда длина волны становится сопоставимой с геометрией доступного пути ре-ентри либо превосходит ее, круговое проведение затухает, и происходит купирование ФП [32].

Химическая формула пропафенона.
Фармакокинетика. Почти полностью абсорбируется, Cmax ~2-3 ч [41]. Vd ~2-3 л/кг, связывание с белками плазмы >95% [41]. Метаболизм печеночный: CYP2D6 → 5-гидроксипропафенон, CYP3A4/1A2 → норпропафенон (оба активные метаболиты) [42]. Фенотип CYP2D6 определяет Т1/2 (~2-10 ч у быстрых метаболизаторов CYP2D6 и ~10-32 ч у медленных метаболизаторов) [43]. Равновесная концентрация достигается через 3-5 сут. при регулярном приеме, экспозиция растет непропорционально дозе из-за насыщаемого метаболизма первого прохождения [41]. Выводится преимущественно в виде метаболитов, неизменного препарата в моче <1% [42][43].
Дозирование при ФП:
- Поддерживающая терапия: 150-300 мг 3 раза/сут., общая суточная доза 450-900 мг, с титрацией переносимой дозы и ЭКГ-контролем [1][12]. Доля пациентов без рецидива при монотерапии оценивается порядка~60-75% на горизонте 6-12 (-24) мес. в отобранных к IС популяциях [44].
- "Таблетка в кармане":600 мг однократно (или 450 мг при массе <70 кг) только у пациентов без структурной патологии миокарда, желателен прием на фоне β-блокатора или недигидропиридинового БКК для профилактики ТП 1:1 [1][12].
Мониторинг и безопасность. Инициация/титрация под контролем ЭКГ. На фоне стабильной концентрации возможна оценка частотно-зависимого расширения QRS (нагрузочный тест/тест с умеренной ЧСС) [45]. Если QRS увеличился >25% от исходного — снизить дозу или отменить, избегать при исходном QRS >120 мс [46]. Контролировать ЧСС/PR/QRS/QTc и электролиты [46].
Противопоказания и предосторожности. Структурное заболевание миокарда (ИБС с перенесенным ИМ/ишемией, выраженная ГЛЖ, сниженная ФВ ЛЖ/СН), синдром Бругада, выраженная синоатриальная (СА) блокада, АВ-блокада II-III без электрокардиостимулятора (ЭКС), выраженная брадикардия, тяжелая печеночная недостаточность [1][12][47]. При ТП высок риск проведения 1:1 — рассмотреть сопутствующий прием блокатора АВ-узла [1][12].
Лекарственные взаимодействия. Ингибиторы CYP2D6/3A4/1A2 (например, ритонавир, грейпфрутовый сок) повышают экспозицию пропафенона и риск проаритмии, индукторы (например, рифампицин, карбамазепин) снижают эффективность [36]. Пропафенон повышает уровни дигоксина (ингибирование P-гликопротеина), варфарина, метопролола и пропранолола, при сочетании с β-блокаторами/недигидропиридиновыми БКК возможны брадикардия/АВ-блокада — требуется мониторинг и коррекция доз [48].
Флекаинид
Механизм действия. Селективный блокатор быстрых, управляемых напряжением Na-каналов Nav1.5 (SCN5A) с медленной кинетикой диссоциации и выраженной частотно-зависимой блокадой [49]. Основной эффект — замедление внутрипредсердного и внутрижелудочкового проведения: дозозависимое удлинение PR и расширение QRS, QT удлиняется преимущественно вторично за счет расширения QRS, влияние на реполяризацию минимально [50]. Возможна организация ФП в ТП с проведением 1:1 (рассмотреть сопутствующий АВ-узловой блокатор, особенно при купировании) [36]. Угнетает проведение по дополнительным путям проведения антеградно и ретроградно [51]. Влияние на СА-узел минимальное, но у пациентов с синдромом слабости синусового узла возможно снижение автоматизма [52]. На фоне блокады Na-каналов возможна манифестация скрытого фенотипа синдрома Бругада [53].

Химическая формула флекаинида.
Фармакокинетика. Пероральная биодоступность ~90% (без значимого эффекта первого прохождения), метаболизм преимущественно через CYP2D6, ~30% дозы выводится почками в неизмененном виде (риск кумуляции при хронической болезни почек) [50][54]. Т1/2 ~2-3 ч [50].
Дозирование при ФП. Поддерживающая терапия: обычно 50-150 мг 2 раза/сут. с индивидуальной титрацией под ЭКГ-контролем (максимально 300-400 мг/сут. в зависимости от переносимости) [1][12].
Мониторинг и безопасность. На старте или при изменении дозы — ЭКГ мониторинг (желательно с оценкой на пике концентрации спустя 2-3 ч), затем периодически [55]. Ожидаемое расширение QRS ~12-20%, если QRS >25% от исходного — снизить дозу/отменить, при базовом QRS >120-130 мс — повод к неназначению препарата [56]. Рекомендован нагрузочный тест после стабилизации дозы для выявления частотно-зависимого расширения QRS [57]. Контролировать PR/QRS/QTc и электролиты [1]. У пациентов с имплантированными устройствами — проверка порогов стимуляции/чувствительности [58].
Лекарственные взаимодействия. Ингибиторы CYP2D6 (флуоксетин, пароксетин, дулоксетин) повышают уровень флекаинида [59]. Амиодарон повышает концентрацию флекаинида, что требует уменьшения дозы и усиления ЭКГ-контроля [60]. Возможно повышение концентрации дигоксина [61]. Сочетание с β-блокаторами — потенциально отрицательный инотропный/хронотропный эффект [36]. Избегать комбинаций с препаратами, существенно удлиняющими QT или вызывающими электролитные сдвиги, корректировать K⁺/Mg²⁺ [59].
Аллапинин (лаппаконитина гидробромид)
Механизм действия. Основная мишень — быстрые, управляемые напряжением Na-каналы (Nav1.5) (SCN5A) [62]. Для препарата характерны состояние- и частотно-зависимые эффекты (предпочтительное связывание с открытыми/инактивированными каналами и усиление блока при высокой ЧСС), что приводит к снижению Vmax фазы 0, замедлению проведения в предсердиях, АВ-соединении и системе Гиса-Пуркинье и, как следствие, удлинению PR и расширению QRS при минимальном влиянии на реполяризацию (QT/QTc клинически значимо обычно не увеличивается), воздействие более выражено в быстро активирующихся аритмогенных зонах, чем в интактном миокарде [62]. Также аллапинин обладает умеренным М-холиноблокирующим (ваголитическим) действием, за счет частичного подавления вагус-опосредованного замедления проводимости снижаются резкие колебания АВ-проводимости и ЧСС, характерные для вагус-индуцированной ФП [63]. Совокупность эффектов (частотно-зависимое замедление проведения + выравнивание рефрактерности + мягкая ваголитическая активность) обусловливает снижение частоты рецидивов ФП без значимого удлинения QT.

Химическая формула аллапинина.
История создания. Разработан в конце 70-х годов в Институте химии растительных веществ АН Узбекистана, в 1982г поступил для клинических испытаний и в 1989г разрешен к клиническому применению [64]. Представляет собой бромистоводородную соль алкалоида, получаемого из корней и наземной части дикорастущего многолетнего растения аконита белоустого (Aconitum leucostomum) и аконита северного (Aconitum septentrionale) семейства лютиковых [63].
Фармакокинетика
- Форма немедленного высвобождения. Пероральная биодоступность составляет 40-60%, Tmax 1,5-2 ч, Cmax — через 1,5-2 ч, Т1/2 — 4-6 ч, что обосновывает прием 3 раза в сутки [63]. Ускорение всасывания (прием натощак, запивание теплой жидкостью) ведет к более высокому Cmax и росту дозозависимых неврологических нежелательных явлений, поэтому рекомендуется прием после еды, запивая прохладной водой [64]. Почечная экскреция не превышает 10% дозы, ведущий путь элиминации — печеночный метаболизм с образованием нескольких активных метаболитов, прежде всего N-дезацетиллаппаконитина, обладающего сопоставимой антиаритмической активностью и более низкой токсичностью [64].
- Пролонгированная форма(аллапинин-ретард, аллафорте). Tmax 4-4,5 ч, Cmax становится в 2-3 раза ниже, Т1/2 достигается через 8-9 ч, что позволяет переходить на двукратный прием препарата и обеспечивает более ровный профиль плазменных концентраций, повышение доли активного метаболита и меньшую частоту дозозависимых побочных эффектов [65].
Рекомендуемая доза при ФП. 25-50 мг внутрь 3 раза/сут. после еды с ЭКГ-контролем через 1-2 ч, при недостаточном эффекте титрация до 150-300 мг/сут. при условии прироста QRS ≤25% и PQ <240 мс. Пролонгированные формы: 25-50 мг 2 раза/сут. [63].
Мониторинг и безопасность. Контролировать PR/QRS/QTc и электролиты при каждом повышении дозы, далее 1 раз в 3-6 мес., ориентироваться на правило IC класса: если QRS увеличился >25% от исходного — снизить дозу/отменить [63]. Избегать старта при исходном QRS >120-130 мс или PR ≥240 мс. Рассмотреть мониторинг функции печени при длительной терапии.
Противопоказания и предосторожности. ИБС, перенесенный ИМ, выраженная ГЛЖ (≥1,4 см), СН (New York Heart Association (классификация сердечной недостаточности) III-IV), тяжелые печеночные/почечные нарушения, СА-блокада, АВ-блокада II-III без ЭКС, значимое нарушение внутрижелудочковой проводимости, подозрение на синдром Бругада [63].
Побочные эффекты. Дозозависимые симптомы со стороны центральной нервной системы: головокружение, парестезии, нарушение аккомодации [63]. Удлинение PQ и расширение QRS, крайне редко — проаритмия у пациентов с новоявленной ИБС или выраженной ГЛЖ [62].
Лекарственные взаимодействия. В комбинации с β-адреноблокаторами усиливается антиаритмическое действие и устраняют β-адреностимулирующие эффекты аллапинина. [63]. Избегать комбинаций с препаратами, существенно удлиняющими QT, и коррегировать K⁺/Mg²⁺ при диуретической терапии.
Этацизин (диэтиламинопропионилэтоксикарбониламинофенотиазин)
Механизм действия. Основной антиаритмический механизм реализуется за счет быстрой и относительно стойкой блокады Na⁺-каналов Nav1.5 в фазу 0 ПД, что приводит к выраженному снижению скорости нарастания мембранного потенциала и замедлению проведения по предсердиям, АВ-узлу и системе Гиса-Пуркинье [45][66]. Обладает умеренной блокадой медленных Ca²⁺-каналов и отрицательным дромотропным действием на АВ-узел, что делает влияние этацизина на проводящую систему более выраженным, что может сильнее влиять на АВ-проводимость по сравнению с отдельными представителями класса IC (флекаинид, пропафенон) [45]. Бета-адреноблокирующей/адреномиметической активности клинически значимо не проявляет, гемодинамическое влияние, как правило, умеренное, однако уязвимы пациенты с нарушениями проводимости и/или сниженным резервом ЛЖ. Наряду с этим этацизин оказывает холинолитическое действие, что делает его эффективным в отношении вагус-зависимых аритмий, развившихся на фоне брадикардии [66][67].
На ЭКГ это проявляется удлинением PQ, расширением QRS, возможны небольшие изменения сегмента ST без клинически значимого удлинения QTc, риск torsades de pointes (TdP) низок при корректном отборе пациентов [32].

Химическая формула этацизина.
Фармакокинетика. Биодоступность ~40%, метаболизм печеночный с образованием активного метаболита (моно-N-деэтилированный этацизин), Cmax — через 2-3 ч, Т1/2 ~2,5 ч, выводится почками в виде метаболитов, продолжительность действия ~6-8 ч, что позволяет назначать 2-3 раза/сут. [32].
Дозировка. 50 мг 3 раза/сут., при недостаточной эффективности — до 200-300 мг/сут. под ЭКГ-контролем.
Мониторинг и безопасность. Контроль ЭКГ через 2-3 дня от старта/изменения дозы, если интервал PQ не превышает 0,24 с, комплекс QRS не более 0,12 с или отсутствует его удлинение более чем на 25% от первоначальной величины, допустимо увеличение дозы, затем повторная оценка через 2-3 дня [68]. Критерии снижения дозы/отмены: увеличение длительности QRS >25%, АВ-блокада II-III ст., СА-блокада II-III ст., синусовая брадикардия [69].
Противопоказания. ИБС, хроническая СН, ГЛЖ 1,4 см, полная блокада ножек пучка Гиса, выраженные нарушения функции печени и почек [68][69]. Соблюдать осторожность при нарушении СА- и АВ-проводимости [69].
Побочные эффекты. Слабость, головокружение, парестезии, онемение языка, зрительные расстройства, расширение QRS, АВ-блокада, желудочковые аритмии.
Лекарственные взаимодействия. Эффективность этацизина повышается при его совместном применении с препаратами, замедляющими АВ-проведение (β-блокаторы). Сочетание этацизина с соталолом и амиодароном не рекомендовано из-за высоко риска проаритмических эффектов [70][71].
ААП III класса
Особое место среди ААП у больных с органической патологией сердца занимают средства III класса по классификации Vaughan-Williams. Эти препараты удлиняют реполяризацию кардиомиоцитов за счет блокады реполяризующих K⁺-каналов, тем самым повышая рефрактерность и препятствуя повторному входу возбуждения, что чаще создает фиброзная ткань [1].
Фармакологическая характеристика III класса ААП
ААП III класса удлиняют ПД и ЭРП преимущественно за счет блокады реполяризующих K⁺-токов (прежде всего быстрого задержанного выпрямляющего калиевого тока (IKr), реже медленного задержанного выпрямляющего калиевого тока (IKs)/внутреннего выпрямляющего калиевого тока (IK1)), отдельные представители обладают мультиканальными эффектами (дополнительная блокада Na⁺/Ca²⁺, β-адреноблокирующие свойства) [72]. Удлинение ЭРП создает электрофизиологический барьер для повторного входа возбуждения (ре-ентри), особенно при наличии гетерогенных путей проведения или рубцовой ткани, подавляет ре-ентри и лежит в основе антиаритмической эффективности при ФП [49]. Для большинства "чистых" IKr-блокаторов характерна обратная частотная зависимость — максимальное удлинение ПД/QT наблюдается при низкой ЧСС/длинных паузах, что, в условиях сниженного реполяризационного резерва, повышает риск ранних постдеполяризаций и TdP, особенно при гипоK⁺/гипоMg²⁺, органическом поражении миокарда и совместном приеме, QT-продлевающих лекарственных средств [73][74] (рис. 4).

Рис. 4. Влияние ААП III класса (пунктирные линии) на потенциалы активности кардиомиоцитов (фиолетовые линии).
Амиодарон
Механизм действия. Амиодарон занимает особое место в арсенале ААП для контроля ритма при ФП у пациентов с органическим поражением сердца, сочетая высокую эффективность в поддержании СР и низкий риск проаритмического эффекта, по сравнению с большинством других препаратов III класса (частота TdP <1% при корректном отборе и мониторинге) [75][76]. Это объясняется его мультиканальным профилем и минимально выраженной обратной частотной зависимостью [77]. Тем не менее применение ограничивается внекардиальной токсичностью, что требует регулярного мониторинга. С фармакодинамической точки зрения, амиодарон демонстрирует мультиклассовую активность: помимо блокады K⁺-каналов — IKr, IKs, IK1 (класс III), он блокирует Na⁺-каналы (класс I), обладает β-адреноблокирующим действием (класс II) и угнетает Ca²⁺-каналы (класс IV), благодаря чему равномерно удлиняет ПД/ЭРП без характерной для "чистых" IKr-блокаторов обратной частотной зависимости [75]. Удлинение QT ожидаемо и требует рутинного контроля, но само по себе меньше коррелирует с развитием TdP [78].

Химическая формула амиодарона.
Фармакокинетика. Высоколипофильный, с большим объемом распределения (Vd) ~66 л/кг, медленно насыщает ткани и так же медленно элиминируется (Т1/2 амиодарона 15-142 дня, дезэтиламидарон 14-75 дней) [79]. Метаболизм: CYP3A/CYP2C8 → дезэтиламидарон (главный активный метаболит), элиминация биллиарная, почечная экскреция минимальна, не диализируется [79]. Эффект в/в формы развивается в течение минут, но "короткий" кажущийся T1/2 обусловлен перераспределением, а не быстрой элиминацией, для пероральной терапии необходимы нагрузочные схемы [79][80].
Дозировка. Старт с пероральной "нагрузки" с последующим переходом на минимальную эффективную поддерживающую дозу: 600 мг/сут. на 1-2 нед., 400 мг/сут. на 1-2 нед., затем по 200 мг/сут. длительно [8]. Всегда применяется наименьшая эффективная доза с учетом ЭКГ и профиля безопасности.
Мониторинг и безопасность. Перед началом: ЭКГ (ЧСС, АВ-проводимость, QTc), тиреотропный гормон/тироксин, аланинаминотрансфераза (АЛТ)/аспартатаминотрансфераза (АСТ), рентген грудной клетки, спирометрия, коррекция K⁺/Mg²⁺/Ca²⁺, далее — тиреотропный гормон/тироксин через 3-6 мес. и каждые 6-12 мес. (и до 12 мес. после отмены), АЛТ/АСТ каждые 6-12 мес., ежегодный рентген органов грудной клетки, периодический ЭКГ-контроль [81][82].
Побочные эффекты. Широкий спектр внекардиальной токсичности: тиреоидная дисфункция (амиодарон-индуцированные гипо-/тиреотоксикоз), пульмональная токсичность (интерстициальный пневмонит/фиброз, ~1-5% с ростом риска при дозах >400 мг/сут., длительной терапии, у пожилых и при исходной патологии легких), гепатотоксичность (частые умеренные ↑АЛТ/АСТ, реже клинически значимые поражения), офтальмологическая токсичность (корнеальные микродепозиты, оптическая нейропатия), неврологическая токсичность (тремор, атаксия, периферическая нейропатия), дерматологическая токсичность (фоточувствительность, "сине-серое" окрашивание), симптомы со стороны желудочно-кишечного тракта, кардиальные эффекты включают брадикардию/АВ-блокаду при низком риске TdP по сравнению с "чистыми" IKr-блокаторами [78][79][82][83].
Лекарственные взаимодействия. При сопутствующем приеме варфарина эмпирически уменьшить дозу на 25-50% с частым контролем международного нормализованного отношения (действие варфарина усиливается при тиреотоксикозе и ослабевает при гипотиреозе), при сопутствующем приеме дигоксина снизить дозу на ~50% и мониторировать ЭКГ (риск дигиталисной интоксикации) [81][84]. Амиодарон увеличивает экспозицию дабигатрана (~50%) и эдоксабана (~40%), применять с осторожностью, учитывая функцию почек [85]. Избегать совместного применения с противовирусными препаратами HCV — риск симптомной брадикардии. Ингибиторы и индукторы CYP3A4 могут повышать или понижать концентрацию амиодарона в сыворотке крови, что может привести к усилению токсичности или снижению его эффективности.
Соталол
Механизм действия. Соталол — рацемат 1:1, состоящий из двух энантиомеров: L-соталол обладает β-адреноблокирующей активностью (класс II), которая преобладает при приеме низких доз (25-80 мг/сут.), тогда как оба энантиомера (D-соталол и L-соталол) проявляют активность III класса (блокада IKr), значимую при дозах >160 мг/сут., что удлиняет ПД и сопровождается удлинением QT и феноменом обратной частотной зависимости (риск TdP при брадикардии и электролитных нарушениях) [86]. Антиаритмическая активность соталола в первую очередь обусловлена свойствами III класса, которые приводят к удлинению ПД и ЭРП в предсердиях и АВ-узле, что клинически проявляется дозозависимым удлинением интервала QT (в среднем +40-100 мс при 160-320 мг/сут.), QRS обычно не изменяется (желудочковая проводимость при нормальной ЧСС сохранна), возможны умеренное урежение СР и незначительное удлинение PR за счет β-блокады [87].

Химическая формула соталола.
Фармакокинетика. Биодоступность соталола близка к 100%, Tmax достигается в течение 2-3 ч, T1/2 ~7-15 ч, не метаболизируется в печени, не подвергается эффекту первого прохождения, выводится преимущественно через почки, поэтому период его полувыведения напрямую зависит от клиренса креатинина и скорости клубочковой фильтрации (противопоказан при клиренсе креатинина <40 мл/мин) [88].
Дозирование и титрация. 80 мг 2 раза/сут. с госпитальной инициацией и непрерывным ЭКГ-мониторингом с максимальной титрацией до 240-320 мг/сут. (шаг ~3 дня с повторной оценкой ЭКГ/электролитов), при условии, что интервал QTc <500 мс и сохраняется клиническая эффективность/переносимость [89].
Мониторинг и безопасность. Не начинать, если QTc >450 мс, при терапии снизить дозу/отменить, если QTc ≥500 мс. Корректировать K⁺/Mg²⁺, избегать сочетаний с лекарственными средствами, удлиняющими QT. Обладает отрицательным инотропным действием: у пациентов со сниженной ФВ ЛЖ возможны снижение сердечного индекса и повышение давления наполнения с риском декомпенсации — применять с осторожностью при дисфункции ЛЖ, противопоказан при ФВ ЛЖ <20% [86]. Риск TdP выше при брадикардии, гипоK⁺/гипоMg²⁺, женском поле, нарушенной функции почек. Учитывая отрицательный инотропный эффект и потенциальную проаритмию, соталол противопоказан при хронической СН с декомпенсацией, удлиненном QT, при выраженной брадикардии и значимой дисфункции ЛЖ [12]. Начало терапии и повторное повышение дозы под ЭКГ-мониторингом [35].
Побочные эффекты. Удлинение QTc с возможным развитием TdP на фоне обратной частотной зависимости, вероятность возрастает при брадикардии, гипоK⁺/гипоMg²⁺, у женщин, при дозах ≥160-320 мг/сут. и нарушении функции почек [1][90]. Брадикардия, АВ-блокада, гипотензия, может оказывать отрицательное инотропное действие [86][91]. Бронхоспазм, усталость, похолодание конечностей, маскировка симптомов гипогликемии [35].
Противопоказания/предосторожности. Синдром слабости синусового узла, АВ-блокада II-III (без ЭКС), врожденный/приобретенный удлиненный QTS или факторы риска TdP, кардиогенный шок/декомпенсация СН, симптомная гипотензия, стенокардия Принцметала, феномен Рейно/тяжелая периферическая ишемия, клиренс креатинина <40 мл/мин, бронхиальная астма/бронхоспазм, K <4 ммоль/л, в сочетании с лекарственными средствами, удлиняющими QT; необходимы коррекция электролитов, контроль симптомов СН. Противопоказан при ФВ ЛЖ <20% [86]. D-соталол ассоциирован с повышением смертности у пациентов после ИМ с дисфункцией ЛЖ (исследование SWORD (Survival With Oral d-Sotalol)) [91].
Лекарственные взаимодействия. Избегать сочетаний с препаратами, удлиняющими QT из-за риска TdP. β2-агонисты могут быть менее эффективны и повышать риск бронхоспазма. Средства, вызывающие гипоK⁺/гипоMg²⁺ (петлевые/тиазидные диуретики и др.), усиливают удлинение QT — корректировать электролиты [92].
В таблице 2 представлены общие данные ААП, применяемых для противорецидивной терапии ФП.
Таблица 2
Сводная таблица ААП для поддержания СР у пациентов с ФП
|
ЛС |
Основной механизм/мишени |
Дозы для поддержания СР |
Ключевые ЭКГ-эффекты и пороги безопасности |
Эффективность (6-12 мес.) |
Основные противопоказания |
Важные взаимодействия |
|
Пропафенон (IC) |
Блок INa (Nav1.5) с медленной диссоциацией; слабая β-блокада; слабый IKr |
150-300 мг 3 раза/сут. (450-900 мг/сут.) с титрацией и ЭКГ-контролем |
PR↑, QRS↑; снизить/отменить: QRS↑ >25% от исходного, "абс." QRS >120-150 мс. |
~60-75% |
Структурное сердце (ИБС/ИМ, выраженная ГЛЖ), ↓ФВ ЛЖ/СН, Бругада; СА/AВ-блок без ЭКС; выраженная брадикардия; тяжёлая печёночная недостаточность |
Ингибирование/индукция CYP2D6/3A4/1A2; ↑ дигоксина (P-gp), варфарина, метопролола/пропранолола |
|
Флекаинид (IC) |
Блок INa (Nav1.5) с медленной диссоциацией; подавление триггерной активности |
50-150 мг 2 раза/сут. (макс. 300-400 мг/сут.) |
PR↑, QRS↑ (~4-10% ожидаемо); снизить/отменить при QRS↑ >25%; избегать старта при исходном QRS >120 мс |
~50-70% |
Структурное сердце (ИБС/ИМ, выраженная ГЛЖ), ↓ФВ ЛЖ/СН, Бругада; СА/AВ-блок без ЭКС |
Ингибиторы CYP2D6; амиодарон ↑ экспозицию (снизить дозу); ± ↑ дигоксина |
|
Аллапинин (IC) |
Блок INa (use/state-dependent), минимальное влияние на реполяризацию; мягкое М-холиноблокирующее действие |
25-50 мг 3 раза/сут.; ретард: 25-50 мг 2 раза/сут. |
PR↑, QRS↑; снизить/отменить при QRS↑ >25%, PR ≥240 мс; избегать старта при QRS >120-130 мс |
~50-60% |
ИБС/ИМ, выраженная ГЛЖ (≥14 мм), СН III-IV, тяжелая печеночная/почечная дисфункция, СА/AВ-блок, значимая интравентрикулярная блокада |
Аддитивная брадикардия/AВ-блок с β-АБ/недигидропиридиновыми БКК; избегать QT-продлевающих сочетаний; коррекция K⁺/Mg²⁺ |
|
Этацизин (IC) |
Блок INa (быстрый и стойкий) + умеренный блок ICaL; отрицательный дромотропный эффект на AВ-узел |
50 мг 3 раза/сут.; титрация до 200-300 мг/сут. |
PR↑, QRS↑; QTc обычно ≈; снизить/отменить при QRS↑ >25%, AВ/СА-блок II-III, выраженной брадикардии; избегать старта при QRS >120-130 мс |
~45-60% |
ИБС/ИМ, ХСН, выраженная ГЛЖ, полная БНПГ, тяжёлая печёночная/почечная дисфункция |
С β-АБ/недигидропиридиновыми БКК — риск брадикардии/AВ-блокады; с амиодароном/соталолом — ↑ влияние на проводимость/QTc; коррекция электролитов |
|
Амиодарон (III, мульти-канальный) |
Блок IKr/IKs/IK1 + INa + ICaL + β-блокада; минимальная обратная частотная зависимость |
Нагрузка: 600 мг/сут. 1-2 нед. → 400 мг/сут. 1-2 нед.; поддержание 200 мг/сут. (у пожилых 100-200 мг/сут.) |
QTc↑ (реже TdP vs "чистые" IKr); возможны PR/QRS↑, брадикардия/AВ-блок; системный мониторинг токсичности |
~50-75% |
СА/AВ-блок без ЭКС, выраженная брадикардия, тяжёлая тиреоидная дисфункция, выраженная пульмонопатия/гепатопатия, беременность/лактация |
Варфарин (-25-50% дозы), дигоксин (-≈50%), ↑ дабигатран/эдоксабан; HCV-DAA — брадикардия; множественные через CYP3A/P-gp |
|
Соталол (III + β) |
Блок IKr (D/L) + β-блокада (L); выраженная обратная частотная зависимость |
80 мг 2 раза/сут. с госпитальным стартом → титрация до 240-320 мг/сут. (шаг ~3 дня) |
QTc↑; не начинать при QTc >450 мс; снизить/отменить при QTc ≥500 мс; отношение рисков↓; PR немного↑; QRS обычно ≈ |
~30-50% |
Удлиненный QTS, брадикардия/AВ-блок без ЭКС, декомпенсация СН, КК <40 мл/мин, K⁺ <4,0 ммоль/л, астма/бронхоспазм |
QT-продлевающие ЛС; диуретики → гипоK⁺/гипоMg²⁺; ↓эффективность β2-агонистов; аддитивная AВ-блокада с дигоксином/недигидропиридиновые. БКК |
Сокращения: АВ — атриовентрикулярный (–ое), БКК — блокаторы кальциевых каналов, БНПГ — блокада ножек пучка Гиса, ГЛЖ — гипертрофия левого желудочка, ИБС — ишемическая болезнь сердца, ИМ — инфаркт миокарда, КК — клиренс креатинина, ЛЖ — левый желудочек, ЛС — лекарственные средства, СА — синоатриальный (–ое), СН — сердечная недостаточность, СР — синусовый ритм, ФВ — фракция выброса, ЭКГ — электрокардиограмма, ЭКС — электрокардиостимулятор, β-АБ — бета-адреноблокаторы, CYP1A2/CYP2C8/CYP2D6/CYP3A4 — изоферменты цитохрома P450, HCV — Hepatitis C virus, IK1 — внутренний выпрямляющий калиевый ток, IKr — быстрый задержанный выпрямляющий калиевый ток, IKs — медленный задержанный выпрямляющий калиевый ток, INa — быстрый натриевый ток, ICaL-L-тип кальциевого тока, Nav1.5 — сердечный натриевый канал (белок), P-gp — P-гликопротеин, TdP — torsades de pointes.
В клинической практике выбор препарата всегда должен учитывать индивидуальные характеристики пациента: наличие сопутствующих заболеваний, потенциальные лекарственные взаимодействия, переносимость и предпочтения самого пациента.
Принципы подбора противорецидивной терапии
Длительная медикаментозная ААТ рекомендуется в рамках стратегии контроля ритма в трех клинических ситуациях [1][8]:
- у пациентов с симптомными, рецидивирующими пароксизмами ФП;
- после успешной электрической или медикаментозной кардиоверсии при персистирующей форме ФП;
- у пациентов после проведения инвазивной изоляции УЛВ в течение 3-х мес. или неопределенно долго, в составе гибридной (инвазивной и медикаментозной) стратегии.
Пациенты с рецидивирующей пароксизмальной ФП. Применение стратегии ритм контроль у пациентов с рецидивирующей пароксизмальной формой ФП является основной долей назначения ААТ. Так как пациенты с пароксизмальной формой ФП будут иметь основной механизм аритмогенеза эктопический и микро-ре-ентри и в большинстве случаев электрическое и механическое ремоделирование ЛП будет отсутствовать, препаратами выбора на первом месте должны быть ААП 1С класса (пропафенон, флекаинид, аллапинин или этацизин). Данные ААП является мембранстабилизирующими, замедляющим максимальную скорость патологической деполяризации путем ингибирования быстрых Na-каналов, цель которых направлена на подавление микро-ре-ентри и эктопической активности, прежде всего на уровне предсердной ткани [24]. Однако перед выбором данного класса ААП, врач должен исключить органическую патологию сердца, а именно ИБС с перенесенным ИМ, выраженную ГЛЖ >14 мм, сниженную систолическую функцию ЛЖ (ФВ <40%), т.к. данные состояния, а прежде всего наличие фиброзного изменения миокарда желудочков сердца, которое может создать условия для ре-ентри желудочковой тахикардии, могут привести к проаритмогенным осложнениям. Также необходимо исключить нарушения проводящей системы сердца, а именно значимые нарушения проведения внутрижелудочковой проводимости (комплекс QRS должен быть не более 120 мс) по ЭКГ, значимых нарушений проводимости на уровне СА-узла и АВ-соединения. Если у пациента сочетается ФП и ТП или ФП трансформируется в макро ре-ентри предсердные тахикардии для профилактики проведения ТП с проведением 1:1 рекомендовано к АПП 1С класса добавить бета-адреноблокаторы или недигидроперидиновые БКК [34].
Мониторинг при терапии IC. После назначения для профилактики рецидивов ФП ААП 1С класса необходимо мониторировать динамику ЭКГ и прежде всего интервалы PQ и ширину QRS, ЧСС и возможное нарушение проводящей системы сердца по суточному мониторированию ЭКГ, переносимость препарата, развитие нежелательных экстракардиальных эффектов и собственно эффективность препарата. Сроки динамического наблюдения очень дискутабельные и разнятся в рекомендательных документах от 1 до 30 сут. приема ААП, чаще это в течение первых 7-14 сут. [1][8].
Альтернатива при противопоказаниях к ААП IC класса. Только при наличии противопоказаний к препаратам 1С класса для профилактики пароксизмальной формы ФП возможно рекомендовать препараты III класса (амиодарон и/или в редких клинических случаях соталол) [1]. Амиодарон с фармакодинамической точки зрения имеет мультиклассовую активность: помимо блокады К⁺-каналов, он также оказывает влияние на Na⁺-каналы, обладает β-адреноблокирующим действием, поэтому он будет эффективен при эктопическом и микро ри-ентри механизме, однако из-за высокого риска развития экстракардиальных побочных эффектов (~50% в год) данный препарат должен быть на второй линии и должен быть четко обоснован [34]. Соталол при противорецидивной терапии теряет свои позиции и большинство экспертов отказываются от его применения из-за того, что малые дозы соталола (до 160 мг в сут.) малоэффективны, т.к. не оказывают влияние на патологическую фазу деполяризации, а именно на основной механизм аритмогенеза при пароксизмальных формах ФП, а большие дозы соталола (>160 мг в сут.) вызывают высокий риск развития проаритмических осложнений и прежде всего риск TdP до 8% [1]. Место соталола — это профилактика рецидивов пароксизмов ФП у пациентов с перенесенным ИМ в прошлом при условии сохранной ФВ ЛЖ. Основные принципы подбора противорецидивной терапии пароксизмальной ФП представлены рисунке 5.
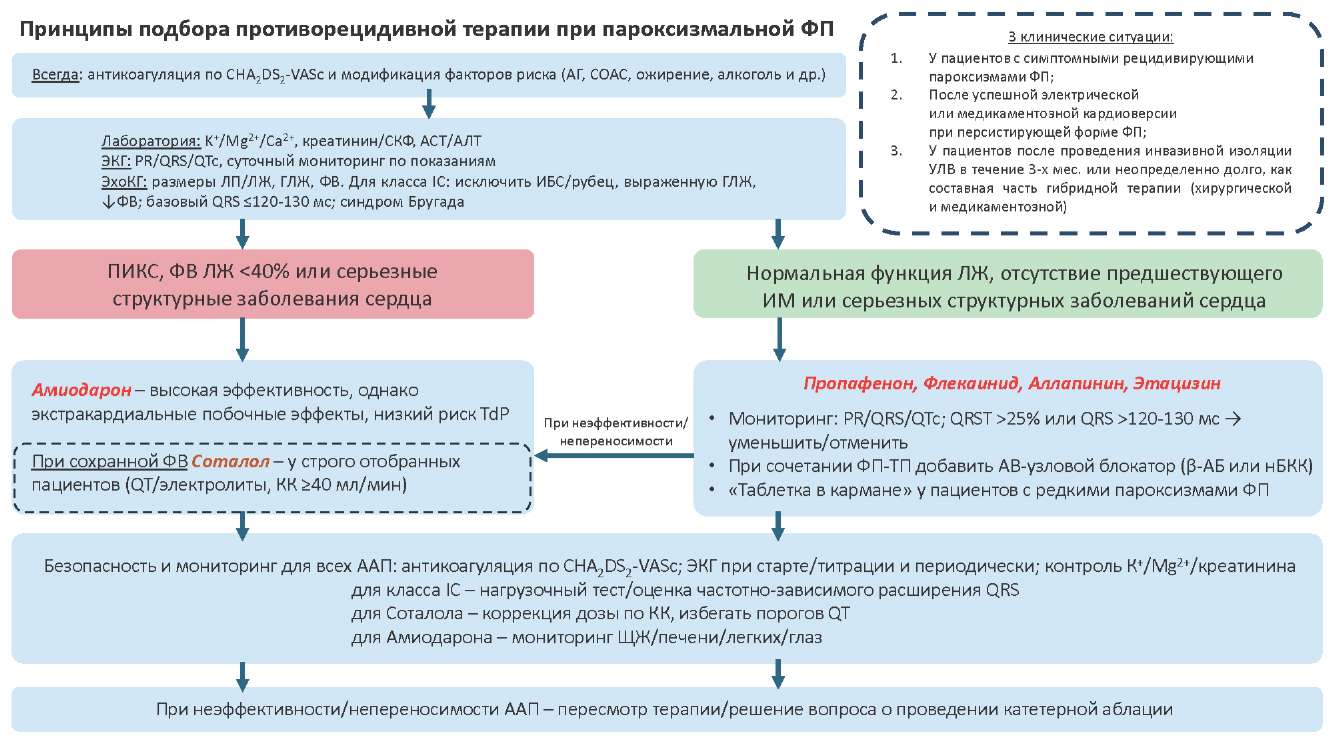
Рис. 5. Принципы подбора противорецидивной терапии ФП.
Сокращения: ААП — антиаритмические препараты, АВ — атриовентрикулярный(-ое), АГ — артериальная гипертензия, АЛТ — аланинаминотрансфераза, АСТ — аспартатаминотрансфераза, ГЛЖ — гипертрофия левого желудочка, ИБС — ишемическая болезнь сердца, ИМ — инфаркт миокарда, КК — клиренс креатинина, ЛЖ — левый желудочек, ЛП — левое предсердие, нБКК — недигидроперидиновые блокаторы кальциевых каналов, ПИКС — постинфарктный кардиосклероз, ТП — трепетание предсердий, СКФ — скорость клубочковой фильтрации, СОАС — синдром обструктивного апноэ сна, УЛВ — устья лёгочных вен, ФВ — фракция выброса, ФП — фибрилляция предсердий, ЩЖ — щитовидная железа, ЭКГ — электрокардиограмма, ЭхоКГ — эхокардиография, TdP — torsades de pointes, β-АБ –бета-адреноблокаторы.
Другая категория больных с ФП для противорецидивной терапии — это пациенты с персистирующей формой ФП. Пациенты, которые длительно находились с продолжающейся аритмией и после инверсии СР после электрической и/или медикаментозной кардиоверсии определенное время от суток до несколько месяцев будут находится в состояние электрического и механического ремоделирования предсердий [22]. В качестве основного механизма аритмогенеза будет преобладать триггерная активность с укорочением интервалов ЭРП. Поэтому особенно у больных с длительно персистирующими формами ФП после купирования аритмии препаратами выбора будут ААП III класса (амиодарон или соталол), т.к. данные ААТ увеличивают рефрактерный период кардиомиоцитов путем блокирования К-каналов, приводя к снижению активности К-каналов, и угнетению медленной диастолической деполяризации клеток сердца, тем самым влияя на процессы реполяризации, которые являются ключевыми при триггерной активации [32]. Учитывая механизмы аритмогенеза сразу после восстановления персистирующей формы ФП на 1-3 мес. препаратами первой линии в пользу III класса и только после прекращения электрического ремоделирования (в исследованиях в большинстве случаев до 3 мес.) перейти на ААП 1С класса при условии их безопасности [29]. Вот почему важны понимание механизма аритмогенеза и уровень ремоделирования предсердий!
После инвазивной изоляции УЛВ. Особая категория больных после проведения инвазивной изоляции УЛВ. В раннем периоде после процедуры изоляции аритмогенного очага (период от 72 ч до 3 мес. после аблации — слепой период "blanking period") часто возникают рецидивы предсердных аритмий от пароксизмов ФП до предсердных тахикардий с регулярным циклом проведения и с частотой 16-84% [93]. Этиология данных рецидивов — воспаление и реакция автономной нервной системы сердца на инвазивное воздействие, поэтому оправдано назначение ААП в первые 3 мес. после аблации ФП если возникают рецидивы предсердных аритмий при пароксизмальной форме ФП и обязательны для пациентов с персистирующей формой ФП. Если пациент направлен на аблацию на СР (пароксизмальная форма ФП), препараты выбора пропафенон или флекаинид. При их противопоказании, ААП — III класса. Если больной направлен на аблацию ФП в продолжающейся аритмии (персистирующая форма) — препараты выбора ААП I или III класса [94]. Если рецидивы ФП возникают после раннего послеоперационного периода необходимо решать о повторной аблации или неопределенно долго продолжать ААТ, как составная часть гибридной терапии при ее эффективности и безопасности [8].
Заключение
Выбор противорецидивной терапии при ФП индивидуализируют с учетом клинического фенотипа, влияния на гемодинамику и коморбидность, предполагаемого механизма аритмогенеза, переносимости и предпочтений пациента. Приоритет — безопасность при доказанной клинической эффективности.
Отношения и деятельность: все авторы заявляют об отсутствии потенциального конфликта интересов, требующего раскрытия в данной статье.
Список литературы
1. Van Gelder IC, Rienstra M, Bunting KV, et al. 2024 ESC Guidelines for the management of atrial fibrillation developed in collaboration with the European Association for CardioThoracic Surgery (EACTS). European Heart Journal. 2024;45:3314-414. doi:10.1093/eurheartj/ehae176.
2. Wyse DG, Waldo AL, DiMarco JP, et al. A comparison of rate control and rhythm control in patients with atrial fibrillation. N Engl J Med. 2002;347:1825-33. doi:10.1056/NEJMoa021328.
3. Hagens VE, Van Gelder IC, Crijns HJGM, RAte Control Versus Electrical Cardioversion Of Persistent Atrial Fibrillation (RACE) Study Group. The RACE study in perspective of randomized studies on management of persistent atrial fibrillation. Card Electrophysiol Rev. 2003;7:118-21. doi:10.1023/a:1027439430017.
4. Van Gelder IC, Hagens VE, Bosker HA, et al. A Comparison of Rate Control and Rhythm Control in Patients with Recurrent Persistent Atrial Fibrillation. N Engl J Med. 2002;347:1834-40. doi:10.1056/NEJMoa021375.
5. Kirchhof P, Camm AJ, Goette A, et al. Early Rhythm-Control Therapy in Patients with Atrial Fibrillation. N Engl J Med. 2020;383:1305-16. doi:10.1056/NEJMoa2019422.
6. Eckardt L, Sehner S, Suling A, et al. Attaining sinus rhythm mediates improved outcome with early rhythm control therapy of atrial fibrillation: the EAST-AFNET 4 trial. Eur Heart J. 2022;43:4127-44. doi:10.1093/eurheartj/ehac471.
7. Rillig A, Magnussen C, Ozga A-K, et al. Early Rhythm Control Therapy in Patients With Atrial Fibrillation and Heart Failure. Circulation. 2021;144:845-58. doi:10.1161/CIRCULATIONAHA.121.056323.
8. Голицын С.П., Голухова Е.З., Михайлов Е.Н. и др. Фибрилляция и трепетание предсердий. Клинические рекомендации 2025. Российский кардиологический журнал. 2025;30(11):6668. doi:10.15829/1560-4071-2025-6668. EDN: MGXGON.
9. Andrade JG, Aguilar M, Atzema C, et al. The 2020 Canadian Cardiovascular Society/ Canadian Heart Rhythm Society Comprehensive Guidelines for the Management of Atrial Fibrillation. Canadian Journal of Cardiology. 2020;36:1847-948. doi:10.1016/j.cjca.2020.09.001.
10. Оганов Р.Г., Симаненков В.И., Бакулин И.Г. и др. Коморбидная патология в клинической практике. Алгоритмы диагностики и лечения. Кардиоваскулярная терапия и профилактика. 2019;18(1):5-66. doi:10.15829/1728-8800-2019-1-5-66.
11. Schotten U, Verheule S, Kirchhof P, Goette A. Pathophysiological mechanisms of atrial fibrillation: a translational appraisal. Physiol Rev. 2011;91:265-325. doi:10.1152/physrev.00031.2009.
12. Joglar JA, Chung MK, Armbruster AL, et al. 2023 ACC/AHA/ACCP/HRS Guideline for the Diagnosis and Management of Atrial Fibrillation: A Report of the American College of Cardiology/American Heart Association Joint Committee on Clinical Practice Guidelines. Circulation. 2024;149:e1 e156. doi:10.1161/CIR.0000000000001193.
13. Jahangir A, Lee V, Friedman PA, et al. Long-Term Progression and Outcomes With Aging in Patients With Lone Atrial Fibrillation: A 30-Year Follow-Up Study. Circulation. 2007;115:3050-6. doi:10.1161/CIRCULATIONAHA.106.644484.
14. Kato T, Yamashita T, Sagara K, et al. Progressive nature of paroxysmal atrial fibrillation. Observations from a 14 year follow-up study. Circ J. 2004;68:568-72. doi:10.1253/circj.68.568.
15. Piña PG, Chicos AB. Early Cardioversion in Atrial Fibrillation: Earlier Is Better, but Not Always and (Maybe) Not Immediately. Curr Atheroscler Rep. 2017;19:3. doi:10.1007/s11883-017-0638-1.
16. Wijffels MCEF, Kirchhof CJHJ, Dorland R, Allessie MA. Atrial Fibrillation Begets Atrial Fibrillation: A Study in Awake Chronically Instrumented Goats. Circulation. 1995;92:1954- 68. doi:10.1161/01.CIR.92.7.1954.
17. Schotten U, Neuberger H-R, Allessie MA. The role of atrial dilatation in the domestication of atrial fibrillation. Progress in Biophysics and Molecular Biology. 2003;82:151-62. doi:10.1016/S0079-6107(03)00012-9.
18. Franz MR, Karasik PL, Li C, et al. Electrical Remodeling of the Human Atrium: Similar Effects in Patients With Chronic Atrial Fibrillation and Atrial Flutter. Journal of the American College of Cardiology. 1997;30:1785-92. doi:10.1016/S0735-1097(97)00385-9.
19. Yue L, Feng J, Gaspo R, et al. Ionic Remodeling Underlying Action Potential Changes in a Canine Model of Atrial Fibrillation. Circulation Research. 1997;81:512-25. doi:10.1161/01.RES.81.4.512.
20. Sánchez J, Gomez JF, Martinez-Mateu L, et al. Heterogeneous Effects of FibroblastMyocyte Coupling in Different Regions of the Human Atria Under Conditions of Atrial Fibrillation. Front Physiol. 2019;10:847. doi:10.3389/fphys.2019.00847.
21. Casaclang-Verzosa G, Gersh BJ, Tsang TSM. Structural and Functional Remodeling of the Left Atrium. Journal of the American College of Cardiology. 2008;51:1-11. doi:10.1016/j.jacc.2007.09.026.
22. Тарасов А.В., Каракиян А.А., Поваров В.О. Механизмы ремоделирования предсердий у пациентов с фибрилляцией предсердий и их взаимосвязь с эффективностью различных методов лечения. Фарматека. 2024;31(9):20-8. EDN: IZJTHU.
23. Thijssen VLJL, Ausma J, Liu GS, et al. Structural Changes of Atrial Myocardium During Chronic Atrial Fibrillation. Cardiovascular Pathology. 2000;9:17-28. doi:10.1016/S1054-8807(99)00038-1.
24. Waks JW, Josephson ME. Mechanisms of Atrial Fibrillation — Reentry, Rotors and Reality. Arrhythm Electrophysiol Rev. 2014;3:90-100. doi:10.15420/aer.2014.3.2.90.
25. Garrey WE. The nature of fibrillary contraction of the heart — its relation to tissue mass and form. American Journal of Physiology-Legacy Content. 1914;33:397-414. doi:10.1152/ajplegacy.1914.33.3.397.
26. Mayor AG. Rhythmical pulsation in Scyphomedusae. Washington, D.C.: Carnegie Institution of Washington, 1906. p. 86.
27. Mines GR. On dynamic equilibrium in the heart. J Physiol. 1913;46:349-83. doi:10.1113/jphysiol.1913.sp001596.
28. Moe GK, Abildskov JA. Atrial fibrillation as a self-sustaining arrhythmia independent of focal discharge. Am Heart J. 1959;58:59-70. doi:10.1016/0002-8703(59)90274-1.
29. Shiroshita-Takeshita A, Brundel BJJM, Nattel S. Atrial fibrillation: basic mechanisms, remodeling and triggers. J Interv Card Electrophysiol. 2005;13:181-93. doi:10.1007/s10840-005-2362-y.
30. Katra RP, Laurita KR. Cellular mechanism of calcium-mediated triggered activity in the heart. Circ Res. 2005;96:535-42. doi:10.1161/01.RES.0000159387.00749.3c.
31. Coetzee WA, Opie LH. Effects of components of ischemia and metabolic inhibition on delayed afterdepolarizations in guinea pig papillary muscle. Circ Res. 1987;61:157- 65. doi:10.1161/01.res.61.2.157.
32. Метелица В.И. Справочник по клинической фармакологии сердечно-сосудистых лекарственных средств. 3 е изд., перераб. и доп. М.: ООО "Медицинское информационное агентство", 2005. 1528 с. ISBN: 5-89481-320-4.
33. Благова О.В. Медикаментозное лечение нарушений ритма сердца. Сулимов В.А. (ред.). М.: ГЭОТАР-Медиа, 2011. 438 с. ISBN: 978-5- 9704-1823-9.
34. Тарасов А.В. Вопросы безопасности антиаритмической терапии. Consilium Medicum. 2014;16(10):44-9. EDN: SXCNNF.
35. Echt DS, Liebson PR, Mitchell LB, et al. Mortality and morbidity in patients receiving encainide, flecainide, or placebo. The Cardiac Arrhythmia Suppression Trial. N Engl J Med. 1991;324:781-8. doi:10.1056/NEJM199103213241201.
36. Martínez-Rubio A, Tamargo J, Dan G-A, editors. Antiarrhythmic Drugs. 2nd ed. Cham: Springer Nature Switzerland AG, 2024. 521 p. ISBN: 978-3-031-74045-9.
37. Abriel H, Rougier J-S, Jalife J. Ion Channel Macromolecular Complexes in Cardiomyocytes: Roles in Sudden Cardiac Death. Circ Res. 2015;116:1971-88. doi:10.1161/CIRCRESAHA.116.305017.
38. Alboni P, Botto GL, Baldi N, et al. Outpatient treatment of recent-onset atrial fibrillation with the "pill-in-the-pocket" approach. N Engl J Med. 2004;351:2384-91. doi:10.1056/NEJMoa041233.
39. Edrich T, Wang S-Y, Wang GK. State-dependent block of human cardiac hNav1.5 sodium channels by propafenone. J Membr Biol. 2005;207:35-43. doi:10.1007/s00232-005-0801-4.
40. Connolly SJ, Kates RE, Lebsack CS, et al. Clinical efficacy and electrophysiology of oral propafenone for ventricular tachycardia. Am J Cardiol. 1983;52:1208-13. doi:10.1016/0002-9149(83)90575-1.
41. Hollmann M, Brode E, Hotz D, et al. Investigations on the pharmacokinetics of propafenone in man. Arzneimittelforschung. 1983;33:763-70.
42. Siddoway LA, Thompson KA, McAllister CB, et al. Polymorphism of propafenone metabolism and disposition in man: clinical and pharmacokinetic consequences. Circulation. 1987;75:785-91. doi:10.1161/01.cir.75.4.785.
43. Tran QT, Baek I-H, Han N-Y, et al. The Effect of CYP2D6 Phenotypes on the Pharmacokinetics of Propafenone: A Systematic Review and Meta-Analysis. Pharmaceutics. 2022;14:1446. doi:10.3390/pharmaceutics14071446.
44. Valderrábano M, Singh BN. Electrophysiologic and Antiarrhythmic Effects of Propafenone: Focus on Atrial Fibrillation. J Cardiovasc Pharmacol Ther. 1999;4:183-98. doi:10.1177/107424849900400308.
45. Царегородцев Д.А., Окишева Е.А., Грачева Е.И. и др. Новый подход к оценке эффективности и безопасности этацизина у пациентов без структурной патологии сердца. Кардиология и сердечно-сосудистая хирургия. 2014;7(2):89-96.
46. Gao X, Guha A, Buck B, et al. Initiation and outcomes with Class Ic antiarrhythmic drug therapy. Indian Pacing Electrophysiol J. 2018;18:68-72. doi:10.1016/j.ipej.2017.12.001.
47. Jespersen CHB, Krøll J, Bhardwaj P, et al. Use of Nonrecommended Drugs in Patients With Brugada Syndrome: A Danish Nationwide Cohort Study. J Am Heart Assoc. 2023;12:e028424. doi:10.1161/JAHA.122.028424.
48. Holm J, Lindh JD, Andersson ML, Mannheimer B. The effect of amiodarone on warfarin anticoagulation: a register-based nationwide cohort study involving the Swedish population. J Thromb Haemost. 2017;15:446-53. doi:10.1111/jth.13614.
49. Merino JL, Tamargo J, Blomström-Lundqvist C, et al. Practical compendium of antiarrhythmic drugs: a clinical consensus statement of the European Heart Rhythm Association of the European Society of Cardiology. Europace. 2025;27:euaf076. doi:10.1093/europace/euaf076.
50. Andrikopoulos GK, Pastromas S, Tzeis S. Flecainide: Current status and perspectives in arrhythmia management. World J Cardiol. 2015;7:76-85. doi:10.4330/wjc.v7.i2.76.
51. Crozier I. Flecainide in the Wolff-Parkinson-White syndrome. Am J Cardiol. 1992;70:26A 32A. doi:10.1016/0002-9149(92)91074-e.
52. Hellestrand KJ, Nathan AW, Bexton RS, Camm AJ. Electrophysiologic effects of flecainide acetate on sinus node function, anomalous atrioventricular connections, and pacemaker thresholds. Am J Cardiol. 1984;53:30B 38B. doi:10.1016/00029149(84)90499-5.
53. Behr ER, Winkel BG, Ensam B, et al. The diagnostic role of pharmacological provocation testing in cardiac electrophysiology: a clinical consensus statement of the European Heart Rhythm Association and the European Association of Percutaneous Cardiovascular Interventions (EAPCI) of the ESC, the ESC Working Group on Cardiovascular Pharmacotherapy, the Association of European Paediatric and Congenital Cardiology (AEPC), the Paediatric & Congenital Electrophysiology Society (PACES), the Heart Rhythm Society (HRS), the Asia Pacific Heart Rhythm Society (APHRS), and the Latin American Heart Rhythm Society (LAHRS). Europace. 2025;27(4):euaf067. doi:10.1093/europace/euaf067.
54. Tamargo J, Le Heuzey J-Y, Mabo P. Narrow therapeutic index drugs: a clinical pharmacological consideration to flecainide. Eur J Clin Pharmacol. 2015;71:549-67. doi:10.1007/s00228-015-1832-0.
55. Lavalle C, Magnocavallo M, Straito M, et al. Flecainide How and When: A Practical Guide in Supraventricular Arrhythmias. J Clin Med. 2021;10:1456. doi:10.3390/jcm10071456.
56. Bordier P, Garrigue S, Bernard V, et al. Flecainide-induced Increase in QRS Duration and Proarrhythmia during Exercise. Clin Drug Investig. 1997;13:326-37. doi:10.2165/00044011-199713060-00005.
57. Vallurupalli S, Pothineni NVK, Deshmukh A, Paydak H. Utility of Routine Exercise Testing to Detect Rate-Related QRS Widening in Patients Without Structural Heart Disease on Class Ic Antiarrhythmic Agents (Flecainide and Propafenone). Am J Cardiol. 2015;116:730-32. doi:10.1016/j.amjcard.2015.05.039.
58. Rivner H, Lambrakos LK. Flecainide Toxicity Leading to Loss of Pacemaker Capture and Cardiac Arrest. JACC Case Rep. 2021;3:586-90. doi:10.1016/j.jaccas.2020.11.030.
59. Mar PL, Horbal P, Chung MK, et al. Drug Interactions Affecting Antiarrhythmic Drug Use. Circ Arrhythm Electrophysiol. 2022;15:e007955. doi:10.1161/CIRCEP.121.007955.
60. Shea P, Lal R, Kim SS, Schechtman K, Ruffy R. Flecainide and amiodarone interaction. J Am Coll Cardiol. 1986;7:1127-30. doi:10.1016/s0735-1097(86)80234-0.
61. Lewis GP, Holtzman JL. Interaction of flecainide with digoxin and propranolol. Am J Cardiol. 1984;53:52B 57B. doi:10.1016/0002-9149(84)90502-2.
62. Вахитова Ю.В., Фарафонтова Е.И., Хисамутдинова Р.Ю. и др. К механизму антиаритмического действия Аллапинина. Биоорганическая химия. 2013;39(1):105. doi:10.7868/S0132342313010119.
63. Соколов С.Ф. Результаты клинического изучения препарата аллапинин и современные подходы к лечению больных с нарушениями ритма сердца. Вестник аритмологии. 2011;(64):60-70.
64. Эрлих А.Д. Изучение доказательной базы использования лаппаконитина гидробромида у пациентов с фибрилляцией предсердий. Кардиология. 2016;56(3):48-53. doi:10.18565/cardio.2016.3.48-53.
65. Арчакова О.А., Багаева Н.С., Комаров Т.Н. и др. Изучение фармакокинетики пролонгированного антиаритмического препарата лаппаконитина гидробромида (Аллафорте®, АО "Фармцентр ВИЛАР", Россия). Разработка и регистрация лекарственных средств. 2022;11(1):140-7. doi:10.33380/2305-2066-2022-11-1-140-147.
66. Логинова А. И., Миронов Н.Ю., Свиридова В.В. и др. Применение этацизина для подавления желудочковой экстрасистолии у пациентов после неэффективной катетерной аблации. Эффективная фармакотерапия. 2025;21(19):46-50. doi:10.33978/2307-3586-2025-21-19-46-50.
67. Дощицин В.Л., Тарзиманова А.И. Исторические аспекты применения антиаритмических препаратов в клинической практике. Рациональная Фармакотерапия В Кардиологии. 2022;18(3):350-8. doi:10.20996/1819-6446-2022-06-07.
68. Царегородцев Д.А., Окишева Е.А., Сулимов В.А. Место антиаритмических препаратов I класса в современной терапии нарушений ритма сердца. Кардиология и сердечно-сосудистая хирургия. 2012;5(6):54-7.
69. Голицын С.П., Панченко Е.П., Миронов Н.Ю. и др. Евразийские клинические рекомендации по диагностике и лечению фибрилляции предсердий у взрослых (2025). Евразийский Кардиологический Журнал. 2025;(3):6- 77. doi:10.38109/2225-1685-2025-3-6-77.
70. Павлов Е.Г., Чапурных А.В., Соловьев О.В. Применение этацизина в комбинированной терапии рецидивирующей фибрилляции предсердий. Кардиология и сердечно-сосудистая хирургия. 2010;3(1):64-70.
71. Соколов С.A., Бомонина Е.В. Сравнительная эффективность и безопасность аллапинина, этацизина и амиодарона и выбор оптимальной антиаритмической терапии по контролю ритма при пароксизмальной мерцательной аритмии. Кардиология: Новости, Мнения, Обучение. 2015;(3):65-75.
72. Zimetbaum P. Antiarrhythmic drug therapy for atrial fibrillation. Circulation. 2012;125:381-9. doi:10.1161/CIRCULATIONAHA.111.019927.
73. Hondeghem LM, Snyders DJ. Class III antiarrhythmic agents have a lot of potential but a long way to go. Reduced effectiveness and dangers of reverse use dependence. Circulation. 1990;81:686-90. doi:10.1161/01.cir.81.2.686.
74. Horváth B, Hézső T, Kiss D, et al. Late Sodium Current Inhibitors as Potential Antiarrhythmic Agents. Front Pharmacol. 2020;11:413. doi:10.3389/fphar.2020.00413.
75. Șorodoc V, Indrei L, Dobroghii C, et al. Amiodarone Therapy: Updated Practical Insights. J Clin Med. 2024;13:6094. doi:10.3390/jcm13206094.
76. Singh BN, Singh SN, Reda DJ, et al. Amiodarone versus sotalol for atrial fibrillation. N Engl J Med. 2005;352:1861-72. doi:10.1056/NEJMoa041705.
77. Van Herendael H, Dorian P. Amiodarone for the treatment and prevention of ventricular fibrillation and ventricular tachycardia. Vasc Health Risk Manag. 2010;6:465-72. doi:10.2147/vhrm.s6611.
78. Tisdale JE, Chung MK, Campbell KB, et al.; American Heart Association Clinical Pharmacology Committee of the Council on Clinical Cardiology and Council on Cardiovascular and Stroke Nursing. Drug-Induced Arrhythmias: A Scientific Statement From the American Heart Association. Circulation. 2020;142:e214 e233. doi:10.1161/CIR.0000000000000905.
79. Vassallo P, Trohman RG. Prescribing amiodarone: an evidence-based review of clinical indications. JAMA. 2007;298:1312-22. doi:10.1001/jama.298.11.1312.
80. Freedman MD, Somberg JC. Pharmacology and pharmacokinetics of amiodarone. J Clin Pharmacol. 1991;31:1061-9. doi:10.1002/j.1552-4604.1991.tb03673.x.
81. Siddoway LA. Amiodarone: guidelines for use and monitoring. Am Fam Physician. 2003;68:2189-96.
82. Bartalena L, Bogazzi F, Chiovato L, et al. 2018 European Thyroid Association (ETA). Guidelines for the Management of Amiodarone-Associated Thyroid Dysfunction. Eur Thyroid J. 2018;7:55-66. doi:10.1159/000486957.
83. Wolkove N, Baltzan M. Amiodarone pulmonary toxicity. Can Respir J. 2009;16:43-8. doi:10.1155/2009/282540.
84. Carpenter M, Berry H, Pelletier AL. Clinically Relevant Drug-Drug Interactions in Primary Care. Am Fam Physician. 2019;99:558-64.
85. Wiggins BS, Dixon DL, Neyens RR, et al. Select Drug-Drug Interactions With Direct Oral Anticoagulants: JACC Review Topic of the Week. J Am Coll Cardiol. 2020;75:1341-50. doi:10.1016/j.jacc.2019.12.068.
86. Kpaeyeh JA, Wharton JM. Sotalol. Card Electrophysiol Clin. 2016;8:437-52. doi:10.1016/j.ccep.2016.02.007.
87. Anderson JL, Prystowsky EN. Sotalol: An important new antiarrhythmic. Am Heart J. 1999;137:388-409. doi:10.1016/s0002-8703(99)70484-9.
88. Antonaccio MJ, Gomoll A. Pharmacology, pharmacodynamics and pharmacokinetics of sotalol. Am J Cardiol. 1990;65:12A 21A; discussion 35A 36A. doi:10.1016/0002-9149(90)90196-8.
89. Biswas M, Levy A, Weber R, et al. Multicenter Analysis of Dosing Protocols for Sotalol Initiation. J Cardiovasc Pharmacol Ther. 2020;25:212-8. doi:10.1177/1074248419887710.
90. Lehmann MH, Hardy S, Archibald D, et al. Sex difference in risk of torsade de pointes with d, l-sotalol. Circulation. 1996;94:2535-41. doi:10.1161/01.cir.94.10.2535.
91. Waldo AL, Camm AJ, deRuyter H, et al. Effect of d-sotalol on mortality in patients with left ventricular dysfunction after recent and remote myocardial infarction. The SWORD Investigators. Survival With Oral d-Sotalol. Lancet. 1996;348:7-12. doi:10.1016/s0140-6736(96)02149-6.
92. McKibbin JK, Pocock WA, Barlow JB, et al. Sotalol, hypokalaemia, syncope, and torsade de pointes. Br Heart J. 1984;51:157-62. doi:10.1136/hrt.51.2.157.
93. Тарасов А.В., Давтян К.В., Миллер (Павенко) О.Н. Рациональная антиаритмическая терапия в послеоперационном периоде катетерной изоляции устьев легочных вен с учетом ее эффективности и безопасности для профилактики ранних рецидивов предсердных тахиаритмий. Consilium Medicum. 2017;19(1):81-7. doi:10.26442/2075-1753_2017.19.1.81-87.
94. Goldenberg GR, Burd D, Lodzinski P, et al. Antiarrhythmic therapy as an adjuvant to promote post pulmonary vein isolation success-a meta-analysis. J Interv Card Electrophysiol. 2016;47:171-6. doi:10.1007/s10840-016-0157-y.
Об авторах
А. В. ТарасовРоссия
Д.м.н., зав. отделением хирургического лечения сложных нарушений ритма сердца и электрокардиостимуляции; преподаватель учебного центра
Петроверигский пер., д. 10, стр. 3, Москва, 101990,
Б. Сухаревская пл., д. 3, Москва, 129090
Е. В. Казанцева
Россия
Аспирант кафедры факультетской терапии № 2 ИКМ им. Н. В. Склифосовского; преподаватель учебного центра
ул. Трубецкая, д. 8, стр. 2, Москва, 119048,
Б. Сухаревская пл., д. 3, Москва, 129090
- Обзор ориентирован на практикующего кардиолога и аритмолога.
- Индивидуализация выбора антиаритмических препаратов является важной в рамках безопасной и эффективной стратегии контроля ритма при фибрилляции предсердий.
- Контроль модифицируемых факторов риска, оптимизация сопутствующей терапии и минимизация полипрагмазии являются неотъемлемой частью стратегии "контроль ритма" и снижают риск проаритмии.
Рецензия
Для цитирования:
Тарасов А.В., Казанцева Е.В. Медикаментозная терапия фибрилляции предсердий. Стратегия "контроль ритма" (обзор). Российский кардиологический журнал. 2025;30(4S):6709. https://doi.org/10.15829/1560-4071-2025-6709. EDN: TRARTN
For citation:
Tarasov A.V., Kazantseva E.V. Pharmacotherapy for atrial fibrillation. The rhythm control strategy (review). Russian Journal of Cardiology. 2025;30(4S):6709. (In Russ.) https://doi.org/10.15829/1560-4071-2025-6709. EDN: TRARTN
JATS XML


















































