Перейти к:
Клинические и сывороточные факторы риска рестенозирования коронарных артерий у пациентов с ишемической болезнью сердца
https://doi.org/10.15829/1560-4071-2025-6252
EDN: JEURZG
Аннотация
Цель. Исследование факторов риска рестенозирования коронарных артерий в ретроспективном (выявление пациентов с рестенозом) и проспективном (анализ биомаркеров) исследовании.
Материал и методы. При наблюдении были определены пациенты с коронарным стенозом в течение 7 лет после первичной установки стента. У 181 пациента, из которых 67 — с коронарным рестенозом и 114 — без него, был исследован клинико-демографический и сывороточный биомаркерный профили пациентов.
Результаты. Частота коронарного рестеноза была значительно чаще у мужчин (82,1% и 69,3%, p=0,047). Для балансирования групп по полу был использован Propensity Score Matching и в результате для группы рестеноза была показана более высокая наследственная предрасположенность по сердечнососудистым заболеваниям (p=0,024), синусовый ритм (p=0,020), низкий сывороточный уровень аполипопротеина А1 (p=0,048) и высокий уровень аланинаминотрансферазы (p=0,023).
Заключение. Для рестенозов коронарных артерий был характерен мужской пол, синусовый ритм, наследственная предрасположенность, повышение аланинаминотрансферазы и снижение аполипопротеина А1.
Ключевые слова
Для цитирования:
Еникеева А.М., Газизова Л.Ю., Николаева И.Е., Бадыкова Е.А., Лакман И.А., Рахимова Р.Ф., Черемисина К.А., Барабошкина А.В., Аглетдинов Э.Ф., Загидуллин Н.Ш. Клинические и сывороточные факторы риска рестенозирования коронарных артерий у пациентов с ишемической болезнью сердца. Российский кардиологический журнал. 2025;30(8):6252. https://doi.org/10.15829/1560-4071-2025-6252. EDN: JEURZG
For citation:
Enikeeva A.M., Gazizova L.Yu., Nikolaeva I.E., Badykova E.A., Lackman I.A., Rakhimova R.F., Cheremisina K.A., Baraboshkina A.V., Agletdinov E.F., Zagidullin N.Sh. Clinical and serum risk factors for coronary restenosis in patients with coronary artery disease. Russian Journal of Cardiology. 2025;30(8):6252. (In Russ.) https://doi.org/10.15829/1560-4071-2025-6252. EDN: JEURZG
В Российской Федерации сердечно-сосудистые заболевания (ССЗ) являются главной причиной смертности населения. Ведущей нозологией в структуре ССЗ, ответственной за смертность и потерю трудоспособности, является ишемическая болезнь сердца (ИБС). Рестеноз остается значимой проблемой при коронарных внутрисосудистых процедурах. Понимание основных механизмов рестеноза было уточнено за последние 20 лет [1]. Неадекватное расширение артерий, а также эластичное растяжение артерии были отмечены в первоначальных клинических исследованиях. При анализе патологических механизмов рестеноза нужно учитывать не только толщину неоинтимы, но и патологические изменения, которые происходят в стенке сосуда и адвентиции [2]. Благодаря многочисленным исследованиям, можно утверждать, что одну из главных ролей в профилактике рестеноза играет корректная установка стента, полное расправление и оптимальный диаметр стента [3][4]. Кроме того, важным фактором риска является сложность процедуры из-за многососудистого поражения, бифуркационных поражений, поражений сосудов малого диаметра, выраженной кальцификации [5][6].
Рестенозы в стентах значительно ухудшают прогноз ИБС. Несмотря на появление стентов с лекарственным покрытием, рестеноз внутри стента развивается по разным данным в 2-10% случаев после перенесенного чрескожного коронарного вмешательства (ЧКВ) [1]. По сравнению с реваскуляризацией поражений de novo, лечение рестеноза стента связано с повышенной сложностью и худшими клиническими исходами. Все это обусловливает неблагоприятный прогноз течения заболевания и необходимость повторных реваскуляризаций. Исходя из этого, возрастает роль определения риска развития рестеноза. В настоящее время известные факторы риска рестеноза внутри стента можно разделить на три группы: связанные с пациентом, связанные с сосудом и связанные с процедурой. Факторы риска, связанные с пациентом, включают возраст пациента, сопутствующие заболевания (например, сахарный диабет), генетические заболевания и системное воспаление; связанные с коронарными артериями, включают сложные кальцинированные, бифуркационные, протяженные поражения сосудов, а также поражение сосудов малого диаметра и многососудистое поражение; и, наконец, факторы риска, связанные с ЧКВ, которые включают недораскрытие стента, чрезмерную дилатацию стента, перелом стента и повреждение полимера. Предикторы рестеноза, связанные с коронарными артериями, включают сложные кальцинированные, бифуркационные, протяженные поражения сосудов, а также поражение сосудов малого диаметра и многососудистое поражение. В ряде исследований были выделены гены, связанные с развитием воспалительных процессов в сосудистой стенке и последующего рестеноза [7]. Поиск новых факторов риска, в т.ч. сывороточных, позволит скорректировать и улучшить результаты лечения путем выработки персонализированной схемы лечения, используемых материалов и особенностей стентирования и амбулаторного мониторинга пациента.
Цель исследования: анализ особенностей пациентов c рестенозами в коронарных артериях в ретроспективном (выявление пациентов с рестенозом) и проспективном (анализ биомаркеров) исследовании.
Материал и методы
Дизайн исследования — комбинация ретроспективного (выявление пациентов с рестенозом коронарных артерий) и проспективного исследования (исследование биомаркеров рестеноза).
На первом этапе был проведен анализ 15 тыс. историй болезни пациентов, перенесших коронароангиографию за период с 2015 по 2020гг в Республиканском кардиологическом центре (рис. 1). В исследование было включено 798 пациентов, у которых во время КАГ были выявлены гемодинамически значимые стенозы, которые в последующем привели к проведению эндоваскулярного вмешательства — стентирования. Среди 798 пациентов были выявлены пациенты со случившимся рестенозом (516) и без рестеноза (282). На данном этапе исследования проводился статистический анализ демографических показателей, сопутствующих патологий и факторов риска.
Критерием включения явилось перенесенное первичное плановое ЧКВ, а именно стентирование коронарных артерий. Критерии невключения были следующие: возраст пациентов моложе 18 лет; ранний рестеноз и тромбоз стента (до 30 дней с момента ЧКВ); наличие трансплантированного сердца; тяжелые заболевания соединительной ткани, требующие постоянного приема глюкокортикостероидов и другой базисной терапии; ранее диагностированная семейная гиперхолестеринемия; онкологические заболевания, потребовавшие проведения химио- и лучевой терапии в период после проведенного ЧКВ.
На втором этапе пациенты был приглашены для анализа сывороточных биомаркеров крови. Пациенты отбирались в 2 группы по наличию и отсутствию гемодинамически значимого рестеноза. Гемодинамически значимым считался рестеноз в стенте коронарных артерий >75%, либо рестеноз в стенте левой коронарной артерии >50%, который повлек за собой потребность в рестентировании. В группу пациентов с рестенозом было отобрано при ретроспективном анализе сплошным образом 67 человек, в контрольную группу пациентов без гемодинамически значимого рестеноза — 114 пациентов. Всем пациентам первично были установлены стенты с лекарственным покрытием, такие как Calipso, Promus ELITE, Orsiro, Xience Alpine, Resolute Integrity. Рестеноз развивался через 18,5 (13,8;26,4) мес. после стентирования. Анализ сывороточных маркеров проводился через 26,4 (21,7;31,2) мес. после наступления рестеноза. В исследование не включались пациенты с серьезными техническими осложнениями во время процедуры, такими как перелом, чрезмерная дилатация или недораскрытие стента.
Концентрация биомаркеров аполипопротеина А1 (Апо А1), аполипопротеина В, N-концевого промозгового натрийуретического пептида, цистатина С, белка, связывающего жирные кислоты, стимулирующего фактора роста, экспрессирующегося геном 2, определялась с помощью иммуноферментного анализа (АО "Вектор-Бест", Россия).
Исследование проводилось в соответствии с Хельсинкской декларацией и было одобрено этическим комитетом ФГБОУ ВО БГМУ Минздрава России № 9 на заседании от 17.11.2021. Все больные подписали соответствующие информированное согласие на проведение обследования.
Статистический анализ. Было проведено сравнение клинико-демографических характеристик у пациентов с рестенозом (n=67) и пациентов без рестеноза (n=114). Было выявлено статистически значимое различие в распределении по полу у сформированных групп (р=0,047). В связи с этим для корректного сравнения групп пациентов с рестенозом и без него к 60-му мес. наблюдения после проведенного стентирования была проведена процедура псевдорандомизации методом Propensity Score Matching (PSM), где в качестве конфаундера выступал пол пациента. Для формирования индекса склонности попадания в группу пациентов с рестенозом и без него была оценена модель логистической регрессии с переменной, отвечающей за пол пациента, в качестве фактора влияния. В качестве способа сопоставления (мэтчинга) для выравнивания в группах применялся метод "ближайшего соседа", позволивший получить сбалансированные группы пациентов с рестенозом и без него по 66 пациентов в каждой (выравнивание по объему групп проводилось в соотношении 1:1, причем группа меньшая по объему учитывалась полностью). Качество процедуры псевдорандомизации контролировали по близости к 1 разницы в вариационном отношении.
В группах пациентов проводили сравнение клинико-демографических характеристик и показателей биомаркеров сыворотки крови, полученных в самом начале исследования. Распределение непрерывных числовых признаков представляли в виде медианы и межквартильного размаха (I квартиль; III квартиль), для категориальных признаков использовали абсолютную и относительную (в %) частоты встречаемости. Медианы непрерывных числовых признаков сравнивали с помощью критерия Манна-Уитни, частоты категориальных признаков сравнивали с помощью критерия Хи-квадрат. Считали различия значимыми, если нулевая гипотеза об отсутствии различий отклонялась при уровне значимости p<0,05. Для наглядности сравнения уровней показателей у пациентов с рестенозом и без него строили бокс-плоты по медиане и межквартильному размаху. Для всей статистической обработки в исследовании использовали язык R.
Результаты
Проведен сбор всех необходимых данных на основе ретроспективного анализа в период с 2015 по 2020гг (выборка 5 лет). Далее пациенты вызывались для анализа сывороточных биомаркеров крови сплошным образом. В результате сплошным методом было сформировано 2 группы: 67 пациентов с рестенозом и 114 — без рестеноза. У всех отобранных пациентов исследовались кардиоваскулярные биомаркеры.
В таблице 1 представлено сравнение клинико-демографических показателей двух групп: 1 — группа пациентов без рестеноза, 2 — с рестенозом. Рестеноз гораздо чаще наблюдался у мужчин по сравнению с отсутствием рестеноза (p=0,047). При сравнении сывороточных биомаркеров в исследуемых группах различия выявлены не были (p>0,05, табл. 2).
Обе группы были проанализированы по принимаемой терапии. Оценивался прием статинов, дезагрегантов, тикагрелора/клопидогрела, антикоагулянтов, β-адреноблокаторов, антагонистов кальция и ингибиторов ангиотензинпревращающего фермента или блокаторов рецепторов к ангиотензину 2. В обеих группах не было выявлено статистически значимого различия по частоте приема указанных групп препаратов.
Группы были несбалансированны по полу (больше мужчин в группе рестеноза (p<0,05)), и для получения статистически значимых результатов потребовалось проведение процедуры выравнивания (PSM). Была подтверждена гипотеза о том, что пол пациентов является конфаундером, обеспечивающим смещение в результатах сравнения: результаты логистической регрессии, где в качестве зависимой переменной выступает фактор наличие или отсутствие рестеноза спустя 60 мес. после стентирования, а в качестве фактора влияния — пол больного, приведены в таблице 3. Процедура PSM была произведена успешно — разница в вариационном соотношении до проведения псевдорандомизации составляла 0,65, после — 1. На рисунке 2 показано сравнение распределения по полу в сформированных группах по признаку наличия рестеноза до и после процедуры PSM. После проведения PSM группы по полу имели одинаковое распределение.
В таблице 4 представлены результаты сравнения частот встречаемости факторов у пациентов в новых группах после PSM с наличием и отсутствием рестеноза в период до 5 лет после стентирования. Отягощенная наследственность определялась как развитие ранних ССЗ у ближайших родственников, у мужчин до 55 лет и у женщин до 65 лет, и значимо чаще встречалась в группе с рестенозом (p=0,024), синусовый ритм также значимо преобладал среди пациентов с рестенозом (p=0,020), а по остальным признакам значимых различий выявлено не было (p>0,05).
В таблице 5 приводится результат сравнения непрерывных признаков для пациентов с наличием и отсутствием рестеноза в период до 5 лет наблюдения после процедуры "выравнивания" показателей за счет метода PSM. У пациентов с рестенозом по сравнению с пациентами без рестеноза было отмечено повышение биомаркера аланинаминотрансферазы (АЛТ) (p=0,031) и снижение — Apo А1 (p=0,048).
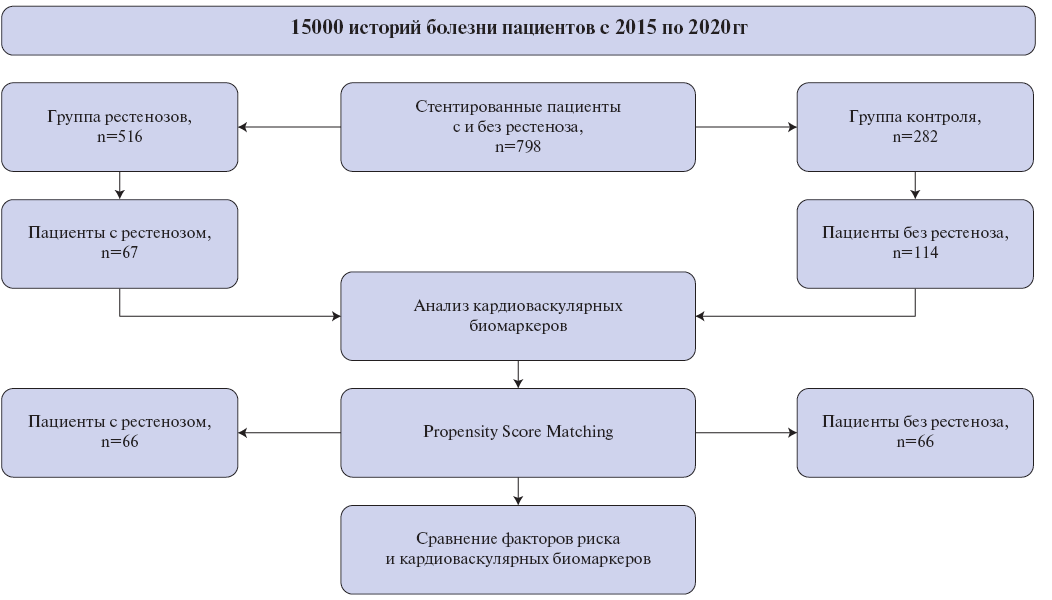
Рис. 1. Дизайн исследования.
Таблица 1
Клинико-демографическое сравнение особенностей пациентов c ИБС с наличием и отсутствием рестеноза коронарных артерий
|
Показатели |
Все пациенты (n=181) |
Без рестеноза (n=114) |
С рестенозом (n=67) |
p-уровень |
|
Me (Q1, Q3) или частота (%) |
||||
|
Пол (муж./жен.), n (%) |
134/47 (74,0/26) |
79/35 (69,3/30,7) |
55/12 (82,1/17,9) |
p=0,047* |
|
Возраст, лет |
67,5 (62,0;72,0) |
68 (62;72,6) |
67 (62,5;71,5) |
p=0,301 |
|
ИМТ, кг/м2 |
29 (26,2;32) |
29 (26,6;3) |
28,7 (25,3;31,4) |
p=0,542 |
|
Наследственность, n (%) |
32 (17,7) |
17 (14,9) |
15 (22,4) |
p=0,303 |
|
Курение, n (%) |
43 (23,8) |
24 (21,1) |
19 (28,4) |
p=0,265 |
|
Синусовый ритм, n (%) |
160 (90,4) |
98 (90) |
62 (92,5) |
p=0,071 |
|
Фибрилляция предсердий, n (%) |
21 (11,9) |
13 (11,4) |
8 (11,9) |
p=0,919 |
|
Трепетание предсердий, n (%) |
17 (9,4) |
10 (8,8) |
7 (10,4) |
p=0,892 |
|
ИМ в анамнезе, n (%) |
111 (61,3) |
76 (66,7) |
35 (52,2) |
p=0,090 |
|
АГ, n (%) |
168 (92,8) |
103 (90,4) |
65 (97,0) |
p=0,200 |
|
СД2, n (%) |
44 (24,3) |
28 (24,6) |
16 (23,9) |
p=0,675 |
|
САД, мм рт.ст. |
130 (126;150) |
130 (130;145,5) |
130 (124;150) |
p=0,675 |
|
ДАД, мм рт.ст. |
84 (80;90) |
84 (80;85,5) |
84 (80;90) |
p=0,752 |
|
ФВ ЛЖ, % |
58 (48;65) |
58 (46;65) |
59 (49;64) |
p=0,757 |
Примечание: * — p<0,05.
Сокращения: АГ — артериальная гипертензия, ДАД — диастолическое артериальное давление, ИМ — инфаркт миокарда, ИМТ — индекс массы тела, САД — систолическое артериальное давление, СД2 — сахарный диабет 2 типа, ФВ ЛЖ — фракция выброса левого желудочка.
Таблица 2
Сравнение сывороточных биомаркеров у больных с ИБС с наличием и отсутствием рестеноза коронарных артерий
|
Показатели |
Все пациенты (n=181) |
Без рестеноза (n=114) |
С рестенозом (n=67) |
p-уровень |
|
Me (Q1, Q3) или частота (%) |
||||
|
Холестерин, ммоль/л |
4 (3,43;4,57) |
3,97 (3,52;4,55) |
4,07 (3,26;4,84) |
p=0,914 |
|
Триглицериды, ммоль/л |
1,66 (1,17;2,34) |
1,66 (1,1;2,36) |
1,66 (1,24;2,23) |
p=0,951 |
|
AСТ, ед./л |
23,0 (18,8;30,3) |
23,2 (19,0;33,0) |
22,0 (18,5;29,5) |
р=0,372 |
|
AЛТ, ед./л |
23,8 (16,0;34,3) |
25,0 (17,0;37,0) |
22,0 (15,5;29,0) |
р=0,152 |
|
KФK, ед./л |
98 (71;161) |
107 (70;167) |
94 (72;145,5) |
р=0,919 |
|
Мочевина, ммоль/л |
6,1 (5,0;8,1) |
6,2 (5,2;8,2) |
5,8 (4,7;7,7) |
р=0,115 |
|
KФК-МВ, ед./л |
13,1 (7,9;21,9) |
12,2 (7,9;22,7) |
14,5 (8,4;20,9) |
р=0,847 |
|
Глюкоза, ммоль/л |
6,8 (5,9;8,6) |
6,8 (5,9;8,6) |
6,7 (5,9;8,6) |
р=0,994 |
|
Магний, ммоль/л |
0,85 (0,77;0,92) |
0,85 (0,77;0,91) |
0,87 (0,78;0,95) |
р=0,341 |
|
ЛНП, ммоль/л |
1,83 (1,46;2,2) |
1,83 (1,48;2,19) |
1,81 (1,41;2,40) |
p=0,675 |
|
ЛВП, ммоль/л |
0,96 (0,86;1,15) |
0,98 (0,89;1,12) |
1,01 (0,86;1,18) |
p=0,957 |
|
Апо А1, мг/дл |
120 (106;142) |
126 (108;143) |
117 (104,5;137,5) |
p=0,186 |
|
Апо В1, мг/дл |
76 (60;90) |
78 (62,5;89) |
72 (59;96) |
p=0,575 |
|
NT-proBNP, пг/мл |
8,44 (0;100,3) |
9,37 (0;102,66) |
0 |
p=0,431 |
|
Тропонин I, нг/л |
0,02 (0,004;0,47) |
0,02 (0,01;0,06) |
0,02 (0,00;0,04) |
p=0,157 |
|
Миоглобин, мкг/л |
12,47 (7,84;17,79) |
12,3 (7,9;17,5) |
12,81 (7,58;18,14) |
p=0,609 |
|
Цистатин С, мг/л |
1 (0,74;1,18) |
1 (0,73;1,18) |
0,97 (0,76;1,18) |
p=0,545 |
|
СРБ, мг/л |
4,28 (1,64;9,77) |
4,77 (1,7;10,2) |
3,39 (1,38;6,43) |
p=0,129 |
|
БСЖК, нг/мл |
0,18 (0,10;0,28) |
0,18 (0,11;0,31) |
0,18 (0,09;0,24) |
p=0,428 |
|
ST2, нг/мл |
15,8 (13,9;26,7) |
15,4 (13,7;25,7) |
15,92 (14,41;27,39) |
p=0,128 |
Сокращения: АЛТ — аланинаминотрансфераза, Апо А1 — аполипопротеин А1, Апо В1 — аполипопротеин В1, АСТ — аспартатаминотрансфераза, БСЖК — белок, связывающий жирные кислоты, КФК — креатинфосфокиназа, КФК-МВ — креатинфосфокиназа-МВ, ЛВП — липопротеины высокой плотности, ЛНП — липопротеины низкой плотности, СРБ — С-реактивный белок, NT-proBNP — N-концевой промозговой натрийуретический пептид, ST2 — стимулирующий фактор роста, экспрессирующийся геном 2.
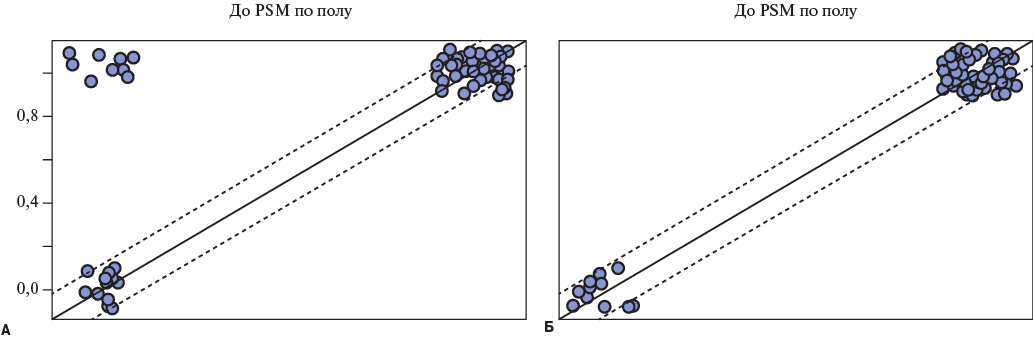
Рис. 2. Графики eQQ Plots при сравнении распределения по полу в сформированных группах по признаку наличия рестеноза до (А) и после (Б) процедуры псевдорандомизации.
Сокращение: PSM — Propensity Score Matching.
Таблица 3
Логистическая регрессия конфаундеров при проведении PSM
|
Конфаундер |
Коэффициент |
Стандартная ошибка коэффициента |
z-статистика |
Р-уровень |
|
Свободный член |
-1,186 |
0,345 |
-3,441 |
<0,001** |
|
Пол (мужской) |
0,824 |
0,387 |
2,13 |
0,033* |
Примечание: *, ** — отличие коэффициентов от нуля при уровне значимости p<0,05 и p<0,001, соответственно.
Таблица 4
Сравнение кардиоваскулярных анамнестических факторов риска развития коронарного рестеноза после проведения PSM
|
Показатели |
Без рестеноза (n=66) |
С рестенозом (n=66) |
Р-уровень различий |
|
Абсолютная и относительная частота (%) |
|||
|
Наследственность |
3 (4,5%) |
11 (16,7%) |
р=0,024* |
|
Курение |
13 (19,7%) |
15 (22,7%) |
р=0,671 |
|
Синусовый ритм |
55 (83,3%) |
64 (97%) |
р=0,020*,# |
|
Фибрилляция предсердий |
7 (10,6%) |
7 (10,6%) |
р=1,0 |
|
Трепетание предсердий |
3 (4,5%) |
7 (10,6%) |
р=0,189 |
|
ИМ в анамнезе |
40 (60,6%) |
35 (53%) |
р=0,380 |
|
АГ |
58 (87,9%) |
64 (97%) |
р=0,101# |
|
СД2 |
18 (27,3%) |
16 (24,2%) |
р=0,691 |
Примечание: * — различия значимы при p<0,05, # — в тесте хи-квадрат выполнялась поправка на правдоподобие.
Сокращения: АГ — артериальная гипертензия, ИМ — инфаркт миокарда, СД2 — сахарный диабет 2 типа.
Таблица 5
Результаты сравнения клинико-демографических признаков и кардиоваскулярных биомаркеров пациентов с наличием и отсутствием рестеноза после проведения PSM
|
Показатели |
Отсутствие рестеноза (n=66) |
Наличие рестеноза (n=66) |
Р-уровень различий |
|
Me (Q1, Q3) |
|||
|
Возраст |
66 (62;71) |
67,5 (61;72) |
р=0,959 |
|
ФВ ЛЖ,% |
58,5 (49;64,3) |
60 (48;65) |
р=0,773 |
|
ИМТ, кг/м2 |
28,98 (26,2;31,5) |
28,85 (26,5;33,25) |
р=0,337 |
|
AСТ, ед./л |
22 (18,5;29,5) |
23,0 (19,5;32,5) |
р=0,349 |
|
AЛТ, ед./л |
22 (15,5;29,0) |
27,4 (19,1;37,5) |
р=0,031* |
|
KФK, ед./л |
94,1 (72;145,5) |
116,5 (74,0;171,8) |
р=0,707 |
|
Мочевина, ммоль/л |
5,8 (4,7;7,7) |
6,2 (5,1;7,7) |
р=0,405 |
|
KФК-МВ, ед./л |
11,8 (8,4;20,8) |
11,8 (8,4;20,8) |
р=0,766 |
|
Холестерин, ммоль/л |
3,89 (3,37;4,5) |
3,89 (3,37;4,5) |
р=0,613 |
|
Триглицериды, ммоль/л |
1,47 (1,1;2,24) |
1,63 (1,24;2,24) |
р=0,540 |
|
ЛВП, ммоль/л |
0,96 (0,86;1,08) |
1,0 (0,86;1,19) |
р=0,279 |
|
ЛНП, ммоль/л |
1,82 (1,47;2,09) |
1,79 (1,41;2,41) |
р=0,948 |
|
Глюкоза, ммоль/л |
6,7 (5,6;8,5) |
6,7 (5,9;8,6) |
р=0,543 |
|
Магний, ммоль/л |
0.86 (0,77;0,91) |
0,87 (0,78;0,95) |
р=0,393 |
|
Apo А1, мг/дл |
126 (108;143) |
115 (103;134) |
р=0,048* |
|
Apo В1, мг/дл |
77 (63,3;86,3) |
71,5 (59;96) |
р=0,969 |
|
NT-proBNP, пг/мл |
3,8 (0,0;62,8) |
0,0 (0,0;80,16) |
р=0,934 |
|
TnI, нг/л |
0,018 (0,004;0,05) |
0,017 (0,004;0,038) |
р=0,289 |
|
Миоглобин, мкг/л |
11,01 (7,28;16,19) |
12,8 (7,9;18,4) |
р=0,706 |
|
Цистатин С, мг/л |
0,94 (0,77;1,15) |
0,99 (0,78;1,18) |
р=0,415 |
|
CРБ, мг/л |
3,89 (1,71;9,06) |
3,42 (1,48;6,54) |
р=0,479 |
|
БСЖК, нг/мл |
0,149 (0,098;0,267) |
0,179 (0,096;0,243) |
р=0,715 |
|
ST2, нг/мл |
15,2 (13,7;24,1) |
16,9 (14,9;27,9) |
р=0,068 |
Примечание: * — различия значимы при p<0,05 и p<0,1, соответственно.
Сокращения: АЛТ — аланинаминотрансфераза, Апо А1 — аполипопротеин А1, Апо В1 — аполипопротеин В1, АСТ — аспартатаминотрансфераза, БСЖК — белок, связывающий жирные кислоты, ИМТ — индекс массы тела, КФК — креатинфосфокиназа, КФК-МВ — креатинфосфокиназа-МВ, ЛВП — липопротеины высокой плотности, ЛНП — липопротеины низкой плотности, СРБ — С-реактивный белок, ФВ ЛЖ — фракция выброса левого желудочка, NT-proBNP — N-концевой промозговой натрийуретический пептид, ST2 — стимулирующий фактор роста, экспрессирующийся геном 2.
Обсуждение
Широкое распространение ЧКВ позволило значительно уменьшить смертность и другие неблагоприятные исходы у пациентов с ИБС. В свою очередь, использование стентов с лекарственным покрытием значительно снизило частоту развития рестенозов стентов [8]. Несмотря на это, рестенозирование коронарных артерий до сих пор остается одним из самых главных осложнений ЧКВ.
В нашем предыдущем исследовании было показано, что отягощенная сердечно-сосудистая наследственность, сахарный диабет 2 типа, артериальная гипертония, курение и употребление алкоголя, отмена аспирина, использование нерационально низких доз статинов, выраженные кальцинированные поражения, ≥3 имплантированных стентов за одно ЧКВ, длина стента ≥30 мм, диаметр стента <3 мм и тандемное стентирование были факторами риска рестеноза внутри стента в течение 2 лет после ЧКВ. Мужской пол и наличие инфаркта миокарда в анамнезе также определялись как факторы риска рестеноза [9].
В данном исследовании нами было проведено сплошное обсервационное ретроспективное обследование 181 пациента с ИБС, которым первично было проведено стентирование коронарных артерий. Проведенное ретроспективное обследование спустя 60 мес. после стентирования выявило у 67 пациентов рестеноз в той же коронарной артерии, а у 114 — он отсутствовал. У всех данных пациентов исследовались клинико-демографические факторы и кардио- васкулярные биомаркеры. При сравнении групп между собой было показано отсутствие различий между группами по всем параметрам, кроме пола (p=0,047). Поэтому для балансирования групп по данному показателю был использован PSM анализ. По результатам при рестенозе был показан тренд к увеличению частоты его развития при наличии генетической предрасположенности к ССЗ, но различие не было статистически значимым (p=0,24). Отягощенная наследственность была признана фактором риска ССЗ еще во Фремингемском исследовании, а позднее была показана значимость молекулярных/генетических механизмов атеросклероза [10], что концептуально соответствует нашим результатам. Более редкое развитие рестеноза у пациентов с фибрилляцией или трепетанием предсердий в сравнении с пациентами с синусовым ритмом может быть связано с антикоагулянтной терапией у данной группы. Также, на наш взгляд, это свидетельствует о большей роли дисфункции эндотелия и нарушения коа- гуляции, чем о развитии атеросклероза в локации стента. В литературе описаны подобные результаты. В частности, в исследовании Wang Z, et al. (2024) сравнивались две группы пациентов после рестеноза бедренных стентов, одна из которых получала терапию аспирином и ривароксабаном, а другая — двойную дезагрегантную терапию [11]. В течение 12 мес. наблюдения было выявлено 15 случаев рецидива рестеноза, при этом в группе, получающей антикоагулянты, частота рецидивов была значимо ниже, чем в группе двойной антиагрегантной терапии (p<0,05).
В результате анализа кардиоваскулярных биомаркеров в сыворотке крови было выявлено статистически значимое повышение АЛТ (p=0,031), снижение уровня Apo А1 (p=0,048) у пациентов с рестенозом по сравнению с пациентами без рестеноза. Наши результаты сопоставимы с результатами исследования Wang X, et al. (2022), где было исследовано 604 пациента с рестенозом коронарных артерий. В многофакторном логистическом регрессионном анализе была показана отрицательная взаимосвязь между уровнем Apo A1 и развитием рестеноза в коронарных стентах [12]. Кроме того, кардиопротективный эффект Apo A1 был доказан при повышении его концентрации в сыворотке крови [13]. Также в некоторых исследованиях была показана взаимосвязь между атеросклерозом и печеночной дисфункцией [14], о чем может свидетельствовать повышение АЛТ.
Заключение
Таким образом, в комбинации ретроспективного (анализ рестенозов) и проспективного (анализ биомаркеров) исследований у больных с ИБС и рестенозом коронарных артерий, было показано, что данный синдром более характерен для мужчин, чаще встречался у пациентов с наследственной предрасположенностью к ССЗ и синусовым ритмом, а также у них отмечалось повышение АЛТ и снижение Аpo А1 в сыворотке крови.
Список литературы
1. Aoki J, Tanabe K, Hoye A, et al. Mechanisms of drug-eluting stent restenosis. Cardiovasc Intervention and Therapeutics. 2021;36(1):23-9. doi:10.1007/s12928-020-00734-7.
2. Еникеева А. М., Газизова Л. Ю., Гареева Д. Ф. и др. Факторы риска коронарного рестеноза. Вестник современной клинической медицины. 2023;16(4):83-9. doi:10.20969/VSKM.2023.16(4).83-89.
3. Шамес Д. В., Галявич А. С., Галеева З. М. и др. Предсказательная ценность препроцедурных лабораторных данных у пациентов с рестенозами коронарных артерий в различных типах стентов. Российский кардиологический журнал. 2019;(3):54-9. doi:10.15829/1560-4071-2019-3-54-59.
4. Omar A, Pendyala LK, Ormiston JA, et al. Review: Stent fracture in the drug-eluting stent era. Cardiovasc Revasc Med. 2016;17(6):404-11. doi:10.1016/j.carrev.2016.06.002.
5. Buccheri D, Piraino D, Andolina G, et al. Understanding and managing in-stent restenosis: a review of clinical data, from pathogenesis to treatment. J Thorac Dis. 2016;8(10): E1150-E1162. doi:10.21037/jtd.2016.10.93.
6. Мазаев В. П., Комков А. А., Рязанова С. В. Клиническое состояние и факторы сердечно-сосудистого риска как отражение неоатеросклероза в стентированных коронарных артериях при позднем развитии рестенозов. Кардиоваскулярная терапия и профилактика. 2016;15(5):64-9. doi:10.15829/1728-8800-2016-5-64-69.
7. Shahsanaei F, Gharibzadeh A, Behrooj S, et al. A systematic review and bioinformatic study on clinical, paraclinical, and genetic factors predisposing to stent restenosis following percutaneous coronary intervention. BMC Cardiovasc Disord. 2024;14;24(1):304. doi:10.1186/s12872-024-03955-3.
8. Shlofmitz E, Case BC, Chen Y, et al. In-Stent Restenosis Classification: A MechanismBased Approach to the Treatment of Restenosis. Cardiovasc Revasc Med. 2021;33:62-7. doi:10.1016/j.carrev.2021.06.004.
9. Enikeeva AM, Gazizova LY, Buzaev IV, et al. Prediction of in-stent restenosis based on systematic and retrospective analyses. Global Translational Medicine. 2024;3(4):4957. doi:10.36922/gtm.4957.
10. Nayor M, Brown KJ, Vasan RS. The Molecular Basis of Predicting Atherosclerotic Cardiovascular Disease Risk. Circ Res. 2021;128(2):287-303. doi:10.1161/CIRCRESAHA.120.315890.
11. Wang Z, Sheng L, Gu H, et al. Rivaroxaban and Aspirin in Drug-Coated Balloon Angioplasty for Femoropopliteal In-Stent Restenosis: A Retrospective Cohort Study. Ann Vasc Surg. 2024;108:338-45. doi:10.1016/j.avsg.2024.05.031.
12. Wang X, Zhang M, Cheng J, et al. Association of serum apoA-I with in-stent restenosis in coronary heart disease. BMC Cardiovasc Disord. 2022;22(1):355. doi:10.1186/s12872-022-02762-y.
13. Cochran BJ, Ong KL, Manandhar B, et al. APOA1: a Protein with Multiple Therapeutic Functions. Curr Atheroscler Rep. 2021;23(3):11. doi:10.1007/s11883-021-00906-7.
14. Jamalinia M, Zare F, Noorizadeh K, et al. Systematic review with meta-analysis: Steatosis severity and subclinical atherosclerosis in metabolic dysfunction-associated steatotic liver disease. Aliment Pharmacol Ther. 2024:445-58. doi:10.1111/apt.17869.
Об авторах
А. М. ЕникееваРоссия
Алина Мухаматдаутовна Еникеева — аспирант кафедры пропедевтики внутренних болезней
Уфа
Л. Ю. Газизова
Россия
Люция Юлаевна Газизова — врач-кардиолог
Уфа
И. Е. Николаева
Россия
Ирина Евгеньевна Николаева — главный внештатный кардиолог Министерства Здравоохранения Республики Башкортостан, главный врач
Уфа
Е. А. Бадыкова
Россия
Елена Альбертовна Бадыкова — к.м.н., доцент кафедры пропедевтики внутренних болезней
Уфа
И. А. Лакман
Россия
Ирина Александровна Лакман — к.тех.н., зав. лабораторией исследования социально-экономических проблем регионов
Уфа
Р. Ф. Рахимова
Россия
Розана Фанисовна Рахимова — аспирант кафедры пропедевтики внутренних болезней
Уфа
К. А. Черемисина
Россия
Ксения Александровна Черемисина — к.б.н., начальник научно-производственной лаборатории
Новосибирск
А. В. Барабошкина
Россия
Анастасия Васильевна Барабошкина — с.н.с. отдела биохимии
Новосибирск
Э. Ф. Аглетдинов
Россия
Эдуард Феликсович Аглетдинов — д.м.н., зам. генерального директора по научной работе
Новосибирск
Н. Ш. Загидуллин
Россия
Науфаль Шамилевич Загидуллин — д.м.н., профессор, зав. кафедры пропедевтики внутренних болезней
Уфа
Дополнительные файлы
- Отягощенная наследственность является значимым фактором риска развития рестеноза.
- Рестеноз значительно чаще развивается у мужчин.
- Аполипопротеин А1 обладает кардиопротективным эффектом. У пациентов с рестенозом выявлено значимое его снижение.
- Значимое повышение уровня аланинаминотрансферазы у пациентов с рестенозом может быть фактором риска развития рестеноза.
Рецензия
Для цитирования:
Еникеева А.М., Газизова Л.Ю., Николаева И.Е., Бадыкова Е.А., Лакман И.А., Рахимова Р.Ф., Черемисина К.А., Барабошкина А.В., Аглетдинов Э.Ф., Загидуллин Н.Ш. Клинические и сывороточные факторы риска рестенозирования коронарных артерий у пациентов с ишемической болезнью сердца. Российский кардиологический журнал. 2025;30(8):6252. https://doi.org/10.15829/1560-4071-2025-6252. EDN: JEURZG
For citation:
Enikeeva A.M., Gazizova L.Yu., Nikolaeva I.E., Badykova E.A., Lackman I.A., Rakhimova R.F., Cheremisina K.A., Baraboshkina A.V., Agletdinov E.F., Zagidullin N.Sh. Clinical and serum risk factors for coronary restenosis in patients with coronary artery disease. Russian Journal of Cardiology. 2025;30(8):6252. (In Russ.) https://doi.org/10.15829/1560-4071-2025-6252. EDN: JEURZG

















































