Перейти к:
Практические аспекты терапии верицигуатом у пациентов с сердечной недостаточностью со сниженной фракцией выброса. Резолюция совета экспертов
https://doi.org/10.15829/1560-4071-2023-5423
Аннотация
Целью совещания экспертов было обсуждение места верицигуата в алгоритме лечения хронической сердечной недостаточности со сниженной фракцией выброса и необходимых условий для его успешного практического применения.
Для цитирования:
Бойцов С.А., Терещенко С.Н., Виллевальде С.В., Галявич А.С., Гарганеева А.А., Глезер М.Г., Дупляков Д.В., Жиров И.В., Кобалава Ж.Д., Лопатин Ю.М., Недогода С.В., Тарловская Е.И. Практические аспекты терапии верицигуатом у пациентов с сердечной недостаточностью со сниженной фракцией выброса. Резолюция совета экспертов. Российский кардиологический журнал. 2023;28(4):5423. https://doi.org/10.15829/1560-4071-2023-5423
For citation:
Boytsov S.A., Tereshchenko S.N., Villevalde S.V., Galyavich A.S., Garganeeva A.A., Glezer M.G., Duplyakov D.V., Zhirov I.V., Kobalava Zh.D., Lopatin Yu.M., Nedogoda S.V., Tarlovskaya E.I. Practical aspects of vericiguat therapy in patients with heart failure with reduced ejection fraction. Expert council resolution. Russian Journal of Cardiology. 2023;28(4):5423. (In Russ.) https://doi.org/10.15829/1560-4071-2023-5423
Ранее опубликованные основные результаты [1] и ряд субанализов [2-8] международного проспективного рандомизированного двойного слепого контролируемого исследования VICTORIA по изучению эффектов терапии стимулятором растворимой гуанилатциклазы (рГЦ) верицигуатом в целевой дозе 10 мг 1 раз/сут. в сравнении с плацебо при добавлении к стандартной терапии у пациентов с симптоматической хронической сердечной недостаточностью (СН) и фракцией выброса (ФВ) левого желудочка (ЛЖ) <45%, недавно перенесших эпизод декомпенсации СН, требуют практической интерпретации в свете изменения подходов к лечению согласно обновленным клиническим рекомендациям Европейского общества кардиологов [9]. Целью совещания экспертов было обсуждение места верицигуата в алгоритме лечения хронической СН со сниженной ФВ (СНнФВ) и необходимых условий для его успешного практического применения.
Изменение подходов к терапии СНнФВ на основании недавно завершившихся рандомизированных клинических исследований (РКИ)
Эпидемиологические данные свидетельствуют о росте распространенности СН в России и мире: число пациентов с указанным диагнозом в нашей стране может составлять 12 млн, а глобально превышает 60 млн человек. При этом, несмотря на существенные успехи в разработке и внедрении новых терапевтических подходов, СНнФВ по-прежнему является состоянием, связанным с высокой смертностью (до 50-75% за 5 лет наблюдения) и неблагоприятным прогнозом [10-13].
Упрощенный терапевтический алгоритм, представленный в клинических рекомендациях Европейского общества кардиологов по лечению СН 2021г, подразумевает инициацию четырех классов препаратов после постановки диагноза СНнФВ: ингибитор ангиотензинпревращающего фермента или ангиотензиновых рецепторов и неприлизина ингибитор (АРНИ), бета-адреноблокатор, антагонист минералокортикоидных рецепторов и ингибитор натрий-глюкозного котранспотера 2-го типа (иНГК2) (дапаглифлозин или эмпаглифлозин); а при наличии застоя добавление петлевых диуретиков [9]. К предполагаемым преимуществам одновременной или быстрой (в течение 1 мес.) инициации 4-компонентной терапии относятся раннее наступление клинического эффекта в виде улучшения самочувствия, снижения риска госпитализаций по причине СН и риска смерти от сердечно-сосудистых заболеваний (ССЗ), а также улучшение приверженности к лечению и преодоление терапевтической инертности.
Вместе с тем, даже у пациентов с СН, включенных в РКИ, сохранялся высокий остаточный риск клинических событий, несмотря на терапию в соответствии с рекомендациями и применение современных методов лечения. Так, в исследованиях по изучению дапаглифлозина и эмпаглифлозина у пациентов с СНнФВ в группах активного лечения у 16,3% и 19,4% пациентов, соответственно, получавших терапию, согласно актуальным клиническим рекомендациям, наступала смерть от ССЗ или госпитализация по причине СН1 в течение периода наблюдения (медиана — 18,2 и 16 мес., соответственно) [14][15]. Это свидетельствует о прогрессировании заболевания в виде повторных эпизодов декомпенсации СН, ведущих к сокращению продолжительности жизни [16][17].
Современной концепцией ведения пациентов с СНнФВ, нашедшей отражение в клинических рекомендациях и согласительных документах, является фенотипирование (профилирование) пациентов с целью стратификации по риску развития осложнений и обеспечения индивидуализированного подхода к выбору терапии на каждом этапе заболевания [9][17]. Фенотипирование может проводиться на основании различных характеристик, к которым можно отнести уровень артериального давления (АД), частоту сердечных сокращений, состояние функции почек и электролитного баланса, наличие фибрилляции предсердий и ряда других сопутствующих заболеваний. По мнению ряда авторов, к отдельному фенотипу следует относить пациентов, госпитализированных с декомпенсацией СН [17]. Это связано с тем, что эпизоды декомпенсации СН дополнительно увеличивают риск повторных госпитализаций по причине СН и смерти от ССЗ, который наиболее высок в первые недели и месяцы после выписки из стационара (так называемый уязвимый период). Частота повторных госпитализаций в течение 1 мес. после события, связанного с декомпенсацией СН, может достигать 56%, а доля умерших пациентов в течение 1 года — 25,1% [18][19], что указывает на необходимость оптимизации болезнь-модифицирующей терапии после перехода на пероральный прием диуретиков во время госпитализации и в первые недели после нее [9][20].
В связи с тем, что пациенты с СНнФВ, нуждаются в дополнительном усилении терапии для улучшения прогноза, особенно, в уязвимый период течения болезни после эпизода декомпенсации СН и стабилизации состояния, продолжается поиск механизмов прогрессирования заболевания, которые могут быть мишенью для медикаментозного воздействия, независимо от блокады нейрогуморальных патогенетических процессов [20]. В качестве такой потенциальной терапевтической мишени может выступать рГЦ, являющаяся центральным звеном сигнального пути "оксид азота (NO) — рГЦ — циклический гуанозинмонофосфат", в норме поддерживающего физиологические функции сердечно-сосудистой системы. При СНнФВ угнетение активности рГЦ на фоне оксидативного стресса, эндотелиальной дисфункции и снижения продукции NO может быть ассоциировано с миокардиальными и сосудистыми нарушениями, ведущими к развитию декомпенсации [21-23]. Верицигуат напрямую стимулирует рГЦ и одновременно увеличивает ее чувствительность к эндогенному NO, что приводит к повышению концентрации внутриклеточного циклического гуанозинмонофосфата, в итоге потенциально способствуя снижению миокардиальной и сосудистой жесткости, вазодилатации, уменьшению явлений гипертрофии, воспаления и фиброза в сердечной мышце [21-23]. Представленный механизм действия позволяет предположить благоприятные эффекты верицигуата при СНнФВ и является патогенетическим обоснованием его изучения в рамках клинических исследований.
Дизайн и основные результаты исследования VICTORIA [1]
В международном рандомизированном плацебо-контролируемом двойном слепом исследовании III фазы VICTORIA эффекты терапии верицигуатом оценивались среди пациентов ≥18 лет (n=5050) с симптоматической (II-IV функциональный класс) хронической СН и ФВ ЛЖ <45%, госпитализированных по причине СН в предшествующие 6 мес. или амбулаторно получавших внутривенную диуретическую терапию в связи с СН в предшествующие 3 мес. Дизайн исследования VICTORIA представлен на рис. 1.
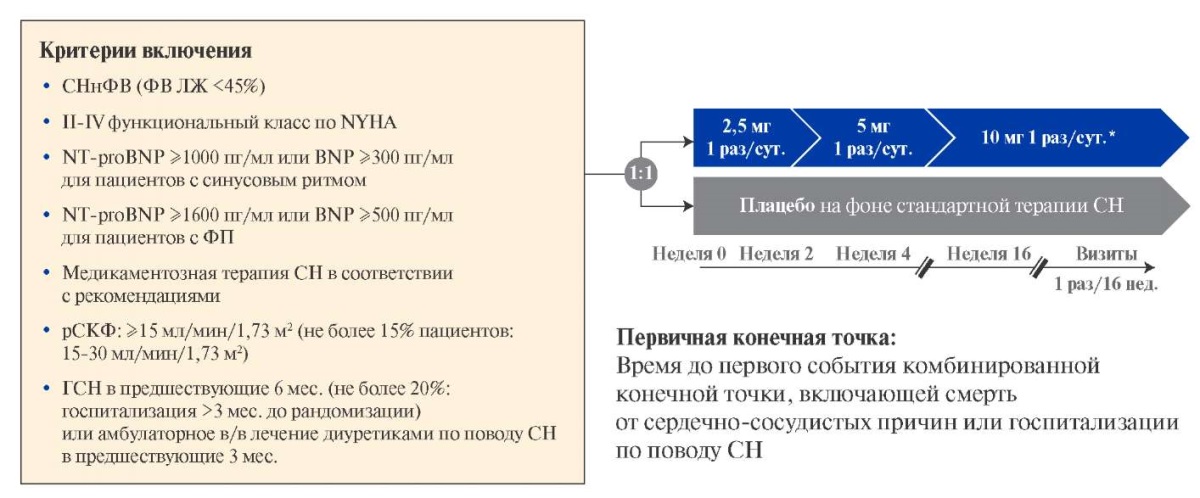
Рис. 1. Дизайн исследования VICTORIA.
Примечание: * — при невозможности увеличения дозы препарата и достижения целевой дозы (10 мг) в установленные сроки, попытки титрования предпринимались на последующих визитах в порядке, установленном протоколом.
Сокращения: в/в — внутривенный, ГСН — госпитализация по поводу сердечной недостаточности, ЛЖ — левый желудочек, СН — сердечная недостаточность, СНнФВ — сердечная недостаточность со сниженной фракцией выброса, рСКФ — расчетная скорость клубочковой фильтрации, ФВ — фракция выброса, ФП — фибрилляция предсердий, BNP — натрийуретический пептид B-типа, NT-proBNP — N-концевой промозговой натрийуретический пептид, NYHA — Нью-Йоркская ассоциация сердца.
В исследовании VICTORIA эпизод декомпенсации СН определялся как нарастание симптомов и признаков СН, требовавшее госпитализации и/или внутривенного введения диуретических препаратов амбулаторно [1]. Это обусловлено тем, что за рубежом получила распространение практика коротких периодов внутривенного введения диуретиков без госпитализации при ухудшении течения заболевания. В недавних согласительных документах была предложена и более широкая трактовка эпизода декомпенсации с включением пациентов, которым необходимо увеличение дозы пероральных диуретиков, что приводит к некоторым противоречиям в используемых определениях [17].
В России же декомпенсацией СН традиционно считается быстрое нарастание тяжести клинических проявлений (одышки, выраженности артериальной гипоксемии, возникновение артериальной гипотонии), ставшее причиной срочного обращения за медицинской помощью и экстренной госпитализации [13]. Вместе с тем на решение о госпитализации пациента с СН может влиять ряд как клинических (возраст, сопутствующая патология, тяжесть состояния, наличие шока и дыхательной недостаточности, степень гиперволемии), так и не клинических факторов (региональная инфраструктура амбулаторной и стационарной помощи, предпочтения пациентов и конкретная жизненная ситуация). При этом в части случаев пациенты могут быть госпитализированы в отсутствие явлений декомпенсации.
Исходя из вышеперечисленного, в качестве надежного и четкого критерия декомпенсации СН мы рекомендуем рассматривать сочетание потребности в госпитализации и необходимости внутривенной диуретической терапии.
Инициация терапии верицигуатом или плацебо проводилась в амбулаторных или стационарных условиях после стабилизации состояния пациентов, определявшейся как уровень систолического АД (САД) ≥100 мм рт.ст. и отсутствие внутривенной терапии в течение ≥24 ч. Стартовая доза верицигуата/плацебо составляла 2,5 мг, при условии переносимости под контролем АД ее повышали сначала до 5 мг, а затем до 10 мг (рис. 1).
Основными критериями исключения были: потребность в приеме нитратов длительного действия, ингибиторов фосфодиэстеразы 5 типа или риоцигуата; ожидание трансплантации сердца, длительная внутривенная терапия инотропными средствами, имплантация (планируемая или в анамнезе) вспомогательного устройства кровообращения; расчетная скорость клубочковой фильтрации (рСКФ) <15 мл/мин/1,73 м2 или постоянный гемодиализ; тяжелое заболевание легких, требующее длительной кислородотерапии, или интерстициальное заболевание легких; тяжелая печеночная недостаточность (например, при наличии печеночной энцефалопатии); корректируемые сопутствующие заболевания сердечно-сосудистой системы.
Прямое сравнение исследования VICTORIA с другими крупными РКИ при СНнФВ невозможно в связи с особенностями дизайна (недавний эпизод декомпенсации как обязательный критерий включения), которые позволили изучить эффекты применения верицигуата у пациентов высокого риска, наиболее нуждающихся в усилении терапии.
Исходные характеристики подтверждают высокий риск неблагоприятных исходов у включенных пациентов: медиана N-концевого промозгового натрийуретического пептида (NT-proBNP) при скрининге была равна 2816 пг/мл, 84% больных были госпитализированы по причине СН в предшествующие 6 мес., и 41% участников имели III-IV функциональный класс СН по классификации Нью-Йоркской ассоциации сердца (NYHA). Нарушения функции почек (рСКФ <60 мл/мин/1,73 м2) имелись более чем у половины (53%) пациентов.
Терапия верицигуатом в целевой дозе 10 мг 1 раз/сут. приводила к статистически значимому снижению риска госпитализации по причине СН или смерти от ССЗ у пациентов с симптоматической хронической СН (ФВ ЛЖ <45%), перенесших недавний эпизод декомпенсации СН, в сравнении с плацебо при добавлении к стандартной терапии СНнФВ: частота событий комбинированной первичной конечной точки в группе верицигуата составляла 33,6 случаев на 100 пациенто-лет по сравнению с 37,8 случаев на 100 пациенто-лет в группе плацебо (отношение рисков (ОР) 0,90; 95% доверительный интервал (ДИ): 0,82-0,98; p=0,02) при медиане продолжительности периода наблюдения 10,8 мес. (рис. 2). Исходя из представленных результатов, абсолютное снижение риска у пациентов, получавших верицигуат, составило 4,2 события на 100 пациенто-лет по сравнению с плацебо. На основании этого показателя можно рассчитать количество пациентов, которые должны получать верицигуат в течение 1 года для предотвращения события первичной конечной точки (number needed to treat, NNT), — оно составляет примерно 24 пациента.
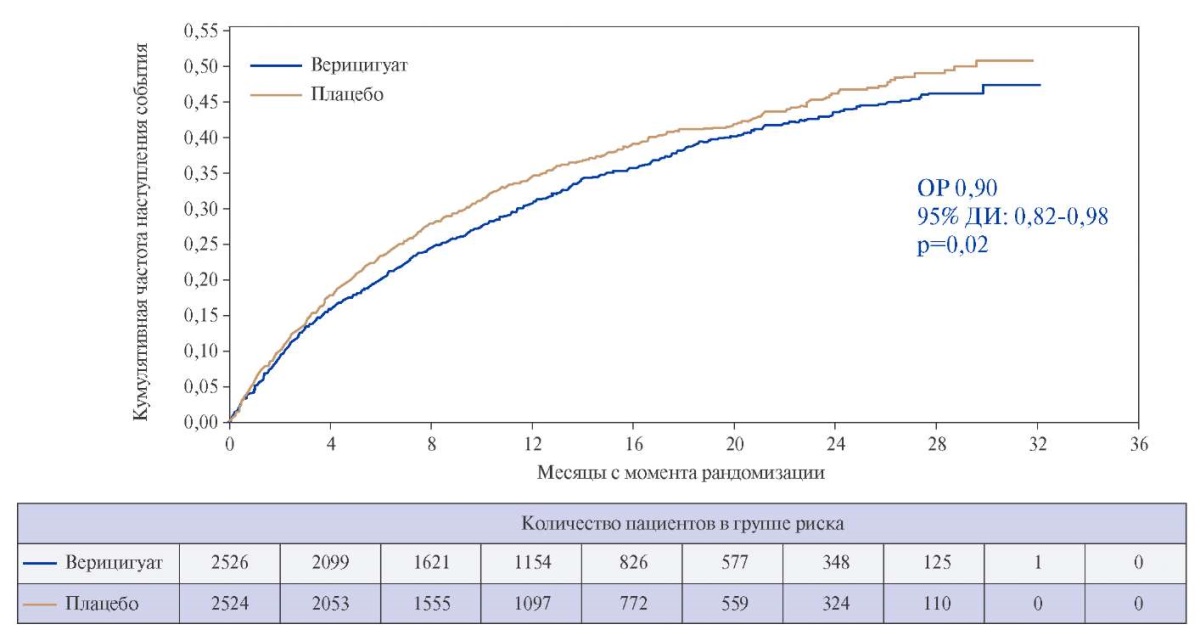
Рис. 2. Основные результаты исследования VICTORIA: верицигуат снижал риск смерти от ССЗ и госпитализации по причине СН (событий первичной конечной точки) у пациентов, недавно перенесших эпизод декомпенсации СНнФВ, при добавлении к стандартной терапии по сравнению с плацебо (ОР 0,90, 95% ДИ: 0,82-0,98).
Сокращения: ДИ — доверительный интервал, ОР — отношение рисков.
Верицигуат в исследовании VICTORIA характеризовался благоприятным профилем безопасности. Примерно через 1 год большинство (90,3%) пациентов достигли целевой дозы исследуемого препарата (89,2% в группе верицигуата и 91,4% в группе плацебо). Частота нежелательных явлений (НЯ) (80,5% vs 81,0%) и серьезных НЯ (32,8% vs 34,8%), а также их профиль были сходными в группах верицигуата и плацебо. Также не отмечалось статистически значимых различий между пациентами, получавшими верицигуат и плацебо, по частоте НЯ особого интереса, к которым относились симптоматическая артериальная гипотония (9,1% vs 7,9%) и синкопальные состояния (4,0% vs 3,5%).
Результаты субанализов исследования VICTORIA и их практическая значимость
Результаты опубликованных субанализов исследования VICTORIA позволяют подробно охарактеризовать эффекты терапии верицигуатом в различных группах пациентов и ответить на практические вопросы по его применению.
- Эффекты терапии верицигуатом в зависимости от индексного события и времени начала терапии
Риск смерти от ССЗ или госпитализации по причине СН в исследовании VICTORIA вне зависимости от возраста и факторов риска был наибольшим у пациентов ближе к моменту индексной госпитализации по поводу СН, т.е. рандомизированных в стационаре и в первые 3 мес. после выписки из него (67% всей популяции). Однако верицигуат снижал частоту наступления первичной конечной точки в исследовании VICTORIA вне зависимости от индексного события (госпитализация или амбулаторное введение диуретиков) и его давности (госпитализация в предшествующие 3 мес. vs 3-6 мес. назад), р для взаимодействия =0,43. Профиль безопасности верицигуата по серьезным НЯ и НЯ особого интереса также был сопоставим с плацебо у пациентов с разными индексными событиями и временем между рандомизацией и госпитализацией [2].
При отсутствии формальных ограничений по месту инициации терапии верицигуатом на основании данных исследования VICTORIA следует отдать предпочтение стационарному этапу ввиду необходимости как можно более раннего усиления терапии и снижения риска повторных эпизодов декомпенсации, а также с целью обеспечения преемственности оказания медицинской помощи и повышения приверженности к терапии. При условии стабилизации состояния пациента верицигуат может быть назначен как перед выпиской из стационара (включая дневной стационар), так и в поликлинике после неё.
- Профиль эффективности верицигуата у пациентов с сопутствующими заболеваниями (фибрилляция предсердий и ишемическая болезнь сердца)
Эффективность верицигуата в отношении первичной конечной точки (р для взаимодействия =0,45), смерти от ССЗ (р для взаимодействия =0,18) и госпитализаций по причине СН (р для взаимодействия =0,44) статистически значимо не различалась между пациентами с фибрилляцией предсердий и без нее [3]. Аналогичное утверждение справедливо и в отношении ишемической болезни сердца (перенесенного инфаркта миокарда, чрескожного коронарного вмешательства или коронарного шунтирования): ОР наступления первичной конечной точки на фоне терапии верицигуатом по сравнению с плацебо у пациентов с таким анамнезом составило 0,92 (95% ДИ: 0,82-1,03) vs 0,85 (95% ДИ: 0,74-0,98), р для взаимодействия =0,78 [4].
- Профиль безопасности верицигуата в отношении развития синкопе и симптоматической артериальной гипотонии
В целом в исследовании VICTORIA частота симптоматической артериальной гипотонии или синкопе была невысокой (23 случая на 100 пациенто-лет) и сопоставимой в группах лечения, включая заранее предопределенные подгруппы. Этапный анализ показал, что верицигуат не увеличивал вероятность развития указанных НЯ после окончания титрования препарата: ОР 1,13 (95% ДИ: 0,93-1,37), р=0,22. При этом динамика САД в группе верицигуата была сопоставимой с плацебо даже среди пациентов со склонностью к артериальной гипотонии: в возрасте >75 лет (n=1395), с исходным уровнем САД <110 мм рт.ст. (n=1344) и исходно принимавших АРНИ (n=730). Кроме того, профиль эффективности верицигуата в отношении первичной комбинированной конечной точки не зависел от исходного уровня САД (р для взаимодействия =0,32) [5].
- Эффекты терапии верицигуатом в зависимости от сопутствующей терапии другими болезнь-модифицирующими препаратами и приверженности пациентов
Профиль эффективности верицигуата по первичной конечной точке сохранялся в большинстве подгрупп, выделенных в зависимости от приема других классов болезнь-модифицирующих препаратов (ингибиторы ренин-ангиотензин-альдостероновой системы и бета-адреноблокаторы) и степени приверженности к ним, т.е. у пациентов, получавших <50% и ≥50% целевых доз с учетом показаний, противопоказаний и переносимости2. Результаты исследования VICTORIA были также однородными вне зависимости от исходного приема АРНИ: среди пациентов, получавших валсартан/сакубитрил, ОР наступления событий первичной комбинированной конечной точки составил 0,88 (95% ДИ: 0,70-1,11) в группе верицигуата по сравнению с плацебо, а при отсутствии приема АРНИ 0,90 (95% ДИ: 0,81-0,99), значение p для взаимодействия =0,8971. Частота артериальной гипотонии и гиперкалиемии в целом была выше у пациентов, получавших валсартан/сакубитрил, однако добавление верицигуата к терапии АРНИ, как и к другой стандартной терапии, не приводило к статистически значимому увеличению риска наступления НЯ3. Таким образом, большинство пациентов в исследовании VICTORIA получали стандартную терапию в соответствии с действовавшими клиническими рекомендациями, включая значительную долю пациентов (14,9%) на терапии АРНИ, при этом значимых различий эффектов верицигуата в зависимости от применения других классов препаратов не наблюдалось.
С учетом повышения риска повторных событий и смерти уже после первого эпизода декомпенсации СНнФВ целесообразно как оптимизировать базовую терапию, так и рассмотреть добавление верицигуата, изучение которого подразумевало инициацию в т.н. уязвимый период (первые 6 мес. после выписки из стационара), чтобы максимально отсрочить повторную декомпенсацию и прогрессирование заболевания. Поскольку эпизод декомпенсации приводит к значительному ухудшению прогноза пациентов с СН, такое событие следует рассматривать как повод к применению дополнительного класса препаратов.
На момент проведения исследования VICTORIA иНГК2 не были зарегистрированы для лечения пациентов с СНнФВ, поэтому данные о применении комбинации верицигуата и глифлозинов в рамках РКИ отсутствуют. Имеются теоретические предпосылки для синергии положительных эффектов указанных препаратов — прежде всего, это независимый механизм действия верицигуата, его вклад в улучшение прогноза и благоприятный профиль безопасности, характерный также и для иНГК2. Следовательно, ожидание результатов исследования4, потенциально способного подтвердить благоприятное действие стимулятора рГЦ на фоне одновременного применения иНГК2, не должно стать препятствием для внедрения верицигуата в практику.
- Профиль эффективности верицигуата в зависимости от исходного уровня NT-proBNP
При первичном анализе результатов был обнаружен более выраженный терапевтический эффект верицигуата в трех нижних квартилях значений NT-proBNP при рандомизации (≤5314 пг/мл) в отношении как первичной комбинированной конечной точки, так и ее компонентов (р для взаимодействия от 0,001 до 0,05). Для изучения ассоциации эффекта лечения в отношении событий первичной конечной точки и уровня NT-proBNP при рандомизации (в качестве непрерывной переменной) был проведен дополнительный ретроспективный субанализ, показавший снижение риска неблагоприятных исходов у пациентов с концентрацией NT-proBNP ≤8000 пг/мл, которые составляли 86% популяции исследования VICTORIA. ОР наступления событий первичной конечной точки у этих больных составлял 0,85 (95% ДИ: 0,76-0,95), что сопровождалось абсолютным снижением риска на 5,4% в год, также снижались частота смерти от ССЗ (ОР 0,84; 95% ДИ: 0,71-0,99) и первой госпитализации по причине СН (ОР 0,84; 95% ДИ: 0,75-0,95) [6]. При этом уровень NT-proBNP на фоне терапии верицигуатом снижался по сравнению с исходными значениями в большей степени, чем в группе плацебо (р от <0,001 до 0,006 через 16-48 нед.)5.
Значения NT-proBNP >8000 пг/мл у 14% пациентов, включенных в исследование VICTORIA, могли свидетельствовать о тяжести СН, ее переходе в далеко зашедшую (терминальную) стадию или отсутствии компенсации заболевания. При этом концентрация данного показателя была в целом выше, чем в основных исследованиях АРНИ и иНГК2, в т.ч. по критериям включения (≥1000 пг/мл при синусовом ритме). Учитывая изменчивость NT-proBNP в динамике и его снижение на фоне терапии верицигуатом и относительно низкую ценность анализа подгрупп в РКИ, возможно начинать терапию верицигуатом в т.ч. у пациентов, которым не проводилось измерение NT-proBNP, ориентируясь на клинический статус пациентов.
- Эффекты терапии верицигуатом в зависимости от наличия анемии и динамика концентрации гемоглобина в исследовании VICTORIA
В исследование VICTORIA было включено 1070 (21,2%) пациентов, страдавших анемией. При этом в ходе исследования в группе верицигуата было зарегистрировано больше НЯ анемии, чем в группе плацебо (7,6% vs 5,7%). Эффект терапии верицигуатом в отношении первичной конечной точки был однороден вне зависимости от значений гемоглобина при рандомизации и в динамике при повторных измерениях. Средние различия между группами верицигуата и плацебо по уровню гемоглобина не превышали 3 г/л в течение всего периода наблюдения и были клинически незначимыми. К тому же, после 16-й нед. лечения дальнейшего снижения гемоглобина у пациентов, получавших верицигуат, не отмечалось [7].
- Профиль эффективности и безопасности верицигуата у пациентов с нарушением функции почек, ее динамика и уровень электролитов на фоне лечения
Профиль эффективности верицигуата был однородным в различных категориях рСКФ (≤30, от >30 до ≤60 и >60 мл/мин/1,73 м2; p для взаимодействия в отношении первичной конечной точки 0,48). В течение 48 нед. лечения отмечалась сходная динамика значений рСКФ и сывороточного креатинина в группах верицигуата и плацебо, статистически значимые различия отсутствовали (p=0,50 и p=0,18, соответственно). Количество НЯ было выше у пациентов с выраженным нарушением функции почек, однако частота НЯ в исследовании VICTORIA была сопоставима в исследуемых группах верицигуата и плацебо, в т.ч. у пациентов с нарушением функции почек. Влияние верицигуата на сывороточную концентрацию калия статистически значимо не отличалось от плацебо (р=0,68) [8].
Инициация, титрование и дальнейшая терапия верицигуатом не требуют дополнительных к рутинно выполняемым обследованиям (в т.ч. лабораторным) у пациентов с СНнФВ согласно действующим клиническим рекомендациям. Это положение поддерживают данные об отсутствии статистически значимого снижения АД по сравнению с плацебо, успешного титрования дозы в исследовании VICTORIA и отсутствие известных межлекарственных взаимодействий. Как упомянуто выше, эффекты верицигуата не различались в зависимости от наличия ряда сопутствующих заболеваний.
После регистрации верицигуата в России следует включить его в клинические рекомендации для применения у пациентов с СН и ФВ ЛЖ <45%, перенесших эпизод декомпенсации, в дополнение к стандартной терапии. Эта формулировка основана на представленных положительных результатах по первичной "жесткой" конечной точке, в которую входили госпитализация по причине СН и смерть от ССЗ, полученных в исследовании VICTORIA, выполненном по всем стандартам проведения многоцентровых клинических испытаний III фазы, и благоприятном профиле безопасности верицигуата.
Эксперты, обсудив результаты исследования VICTORIA, пришли к следующему заключению:
- С учетом сложившихся в Российской Федерации условий оказания медицинской помощи эпизодом декомпенсации СН следует считать усиление клинических проявлений СН, требующее госпитализации и внутривенного введения диуретиков.
- Пациенты, недавно перенесшие эпизод декомпенсации СН, представляют собой особую популяцию (фенотип), которая имеет наибольшую потребность в усилении терапии и высокие остаточные риски неблагоприятных исходов даже на фоне современных методов лечения.
- Учитывая особенности популяции пациентов с СН, изученной в рамках исследования VICTORIA, благоприятный профиль безопасности и независимый от других болезнь-модифицирующих препаратов механизм действия, целесообразно рассмотреть назначение верицигуата у пациентов, перенесших эпизод декомпенсации СНнФВ после гемодинамической стабилизации (САД ≥100 мм рт.ст., отсутствие внутривенной диуретической терапии в течение 24 ч), в дополнение к стандартной терапии.
- В случае отсутствия в терапии какого-либо класса препаратов первой линии на момент декомпенсации, вопрос о его назначении следует рассматривать параллельно с инициацией верицигуата.
- Измерение NT-proBNP не требуется перед назначением верицигуата.
- Инициация верицигуата возможна как в стационаре, так и в амбулаторных условиях. Начало терапии перед выпиской из стационара является более предпочтительным, поскольку в раннем периоде после эпизода декомпенсации риски повторных событий наиболее высоки.
- Прием верицигуата не требует дополнительного клинического и лабораторного мониторирования по отношению к рутинной практике наблюдения пациентов с СНнФВ.
- После регистрации верицигуата в Российской Федерации по соответствующему показанию следует рекомендовать его включение в клинические рекомендации.
After discussing the results of the VICTORIA study, the experts came to the following conclusion:
- Considering accepted practices of health care management in the Russian Federation, decompensated HF should be defined as increasing clinical manifestations of HF which require hospitalization and intravenous administration of diuretics.
- Patients who have recently had a decompensated HF represent a distinctive population (phenotype) that has the greatest need for intensification of therapy and high residual risks of adverse outcomes even in spite of contemporary treatment methods.
- Considering the characteristics of HF patients studied in the VICTORIA study, a favorable safety profile and a mechanism of action independent of other guideline-recommended drugs, initiation of vericiguat is reasonable in patients who have had decompensated HFrEF after hemodynamic stabilisation (SBP ≥100 mm Hg, no intravenous diuretic therapy for 24 hours), in addition to standard treatment.
- In the absence of any class of first-line drugs at the time of decompensation, its prescription should be considered in parallel with the initiation of vericiguat.
- Measurement of NT-proBNP is not required before prescription of vericiguat.
- Initiation of vericiguat is possible both in hospital and outpatient setting. Starting therapy before discharge from hospital is preferable, since in the early period after the decompensation, the risks of recurrent events are the highest.
- Vericiguat use does not require additional clinical and laboratory monitoring besides the routine follow-up of HFrEF patients.
- After approval of vericiguat in the Russian Federation, with respective indication, we recommend it inclusion into clinical guidelines.
Отношения и деятельность. Статья опубликована при поддержке АО "Байер". Текст резолюции подготовлен при участии медицинского советника АО "Байер" П. В. Лазарева.
1. В исследовании DAPA-HF в состав комбинированной первичной конечной точки входили смерть от ССЗ и ухудшение течения СН (госпитализация или неотложный визит в связи с СН).
2. Ezekowitz JA, McMullan CJ, Westerhout CM, et al. Effect of Vericiguat in VICTORIA According to Guideline-Directed Medical Therapy. Доклад на конгрессе HFSA 2020. Доступно: https://thecvc.ca/wp-content/uploads/2017/01/SOC-in-VICTORIA-HFSA-v5-FINAL-LBT-Ezekowitz-2020-10-05.pdf (по состоянию на 8 июня 2022г).
3. Senni M, Alemayehu W, Sim D, et al. Efficacy and safety of vericiguat in patients with HFrEF treated with sacubitril/valsartan: results from the VICTORIA trial. Доклад на конгрессе ESC 2021. Доступно: https://esc365.escardio.org/presentation/235048 (по состоянию на 8 июня 2022г).
4. A Study of Vericiguat (MK-1242) in Participants With Chronic Heart Failure With Reduced Ejection Fraction (HFrEF) (MK-1242-035) (VICTOR). Available at: https://clinicaltrials.gov/ct2/show/NCT05093933 (по состоянию на 2 августа 2022г).
5. Ezekowitz JA, Zheng Y, Lund LH, et al. Change in NT-proBNP and Clinical Outcomes in the Vericiguat Global Study in Subjects with Heart Failure with Reduced Ejection Fraction (VICTORIA). Доклад на конгрессе HFSA 2020. Доступно: https://thecvc.ca/wp-content/uploads/2017/01/VICTORIA-Serial-NT-proBNP-for-HFA.pdf (по состоянию на 8 июня 2022г).
Список литературы
1. Armstrong PW, Pieske B, Anstrom KJ, et al. Vericiguat in Patients with Heart Failure and Reduced Ejection Fraction. N Engl J Med. 2020;382(20):1883-93. doi:10.1056/NEJMoa1915928.
2. Lam CSP, Giczewska A, Sliwa K, et al. Clinical Outcomes and Response to Vericiguat According to Index Heart Failure Event: Insights From the VICTORIA Trial. JAMA Cardiol. 2021;6(6):706-12. doi:10.1001/jamacardio.2020.6455.
3. Ponikowski P, Alemayehu W, Oto A, et al. Vericiguat in patients with atrial fibrillation and heart failure with reduced ejection fraction: insights from the VICTORIA trial. Eur J Heart Fail. 2021;23(8):1300-12. doi:10.1002/ejhf.2285.
4. Saldarriaga C, Atar D, Stebbins A, et al. Vericiguat in patients with coronary artery disease and heart failure with reduced ejection fraction. Eur J Heart Fail. 2022;24(5):782-90. doi:10.1002/ejhf.2468.
5. Lam CSP, Mulder H, Lopatin Y, et al. Blood Pressure and Safety Events With Vericiguat in the VICTORIA Trial. J Am Heart Assoc. 2021;10(22):e021094. doi:10.1161/JAHA.121.021094.
6. Ezekowitz JA, O’Connor CM, Troughton RW, et al. N-Terminal Pro-B-Type Natriuretic Peptide and Clinical Outcomes: Vericiguat Heart Failure With Reduced Ejection Fraction Study. JACC Heart Fail. 2020;8(11):931-9. doi:10.1016/j.jchf.2020.08.008.
7. Ezekowitz JA, Zheng Y, Cohen-Solal A, et al. Hemoglobin and Clinical Outcomes in the Vericiguat Global Study in Patients With Heart Failure and Reduced Ejection Fraction (VICTORIA). Circulation. 2021;144(18):1489-99. doi:10.1161/CIRCULATIONAHA.121.056797.
8. Voors AA, Mulder H, Reyes E, et al. Renal function and the effects of vericiguat in patients with worsening heart failure with reduced ejection fraction: insights from the VICTORIA (Vericiguat Global Study in Subjects with HFrEF) trial. Eur J Heart Fail. 2021;23(8):1313-21. doi:10.1002/ejhf.2221.
9. McDonagh TA, Metra M, Adamo M, et al. 2021 ESC Guidelines for the diagnosis and treatment of acute and chronic heart failure. Eur Heart J. 2021;42(36):3599-726. doi:10.1093/eurheartj/ehab368.
10. Поляков Д. С., Фомин И. В., Беленков Ю. Н. и др. Хроническая сердечная недостаточность в Российской Федерации: что изменилось за 20 лет наблюдения? Результаты исследования ЭПОХА-ХСН. Кардиология. 2021;61(4):4-14. doi:10.18087/cardio.2021.4.n1628.
11. Savarese G, Becher PM, Lund LH, et al. Global burden of heart failure: A comprehensive and updated review of epidemiology. Cardiovasc Res. 2023;118(17):3272-87. doi:10.1093/cvr/cvac013.
12. Бойцов С. А., Драпкина О. М., Зайратьянц О. В. и др. Пути решения проблемы статистики сердечной недостаточности в клинической практике. Кардиология. 2020;60(10):13-9. doi:10.18087/cardio.2020.10.n1039.
13. Российское кардиоло гическое общество (РКО). Хроническая сердечная недостаточность. Клинические рекомендации 2020. Российский кардиологический журнал. 2020;25(11):4083. doi:10.15829/1560-4071-2020-4083.
14. McMurray JJV, Solomon SD, Inzucchi SE, et al. Dapagliflozin in Patients with Heart Failure and Reduced Ejection Fraction. N Engl J Med. 2019;381(21):1995-2008. doi:10.1056/NEJMoa1911303.
15. Packer M, Anker SD, Butler J, et al. Cardiovascular and Renal Outcomes with Empagliflozin in Heart Failure. N Engl J Med. 2020;383(15):1413-24. doi:10.1056/NEJMoa2022190.
16. Greene SJ, Fonarow GC, Butler J. Risk Profiles in Heart Failure: Baseline, Residual, Worsening, and Advanced Heart Failure Risk. Circ Heart Fail. 2020;13(6):e007132. doi:10.1161/CIRCHEARTFAILURE.120.007132.
17. Rosano GMC, Moura B, Metra M, et al. Patient profiling in heart failure for tailoring medical therapy. A consensus document of the Heart Failure Association of the European Society of Cardiology. Eur J Heart Fail. 2021;23(6):872-81. doi:10.1002/ejhf.2206.
18. Butler J, Yang M, Manzi MA, et al. Clinical Course of Patients With Worsening Heart Failure With Reduced Ejection Fraction. J Am Coll Cardiol. 2019;73(8):935-44. doi:10.1016/j.jacc.2018.11.049.
19. Поляков Д. С., Фомин И. В., Вайсберг А. Р. ЭПОХА-ДХСН: гендерные различия в прогнозе жизни больных ХСН при острой декомпенсации сердечной недостаточности (часть 2*). Кардиология. 2019;59(4S):33-43. doi:10.18087/cardio.2654.
20. Виллевальде С. В., Соловьева А. Е. Декомпенсация сердечной недостаточности с низкой фракцией выброса: преодоление барьеров для улучшения прогноза в "уязвимый" период после выписки. Кардиология. 2021;61(12):82-93. doi:10.18087/cardio.2021.12.n1860.
21. Кобалава Ж. Д., Лазарев П. В. Значение сигнального пути "оксид азота — растворимая гуанилатциклаза — циклический гуанозинмонофосфат" в патогенезе сердечной недостаточности и поиске новых терапевтических мишеней. Кардиоваскулярная терапия и профилактика. 2021;20(6):3035. doi:10.15829/1728-88002021-3035.
22. Breitenstein S, Roessig L, Sandner P, Lewis KS. Novel sGC Stimulators and sGC Activators for the Treatment of Heart Failure. Handb Exp Pharmacol. 2017;243:225-47. doi:10.1007/164_2016_100.
23. Sandner P, Follmann M, Becker-Pelster E, et al. Soluble GC stimulators and activators: Past, present and future. Br J Pharmacol. 2021. doi:10.1111/bph.15698. Epub ahead of print.
Об авторах
С. А. БойцовРоссия
Академик РАН, профессор, генеральный директор
С. Н. Терещенко
Россия
Доктор медицинских наук, профессор, руководитель отдела заболеваний миокарда и сердечной недостаточности
С. В. Виллевальде
Россия
Доктор медицинских наук, профессор, начальник службы анализа и перспективного планирования, заведующий кафедрой кардиологии
А. С. Галявич
Россия
Доктор медицинских наук, профессор, заведующий кафедрой факультетской терапии и кардиологии
А. А. Гарганеева
Россия
Доктор медицинских наук, профессор, заведующий отделением общеклинической кардиологии и эпидемиологии сердечно-сосудистых заболеваний научно-исследовательского института кардиологии
М. Г. Глезер
Россия
Доктор медицинских наук, профессор кафедры профилактической и неотложной кардиологии НИО
Д. В. Дупляков
Россия
Доктор медицинских наук, заместитель главного врача по медицинской части ГБУЗ "Самарский областной клинический кардиологический диспансер", профессор кафедры кардиологии и сердечно-сосудистой хирургии ИПО ФГБОУ ВО "Самарский государственный медицинский университет" Минздрава России
И. В. Жиров
Россия
Доктор медицинских наук, ведущий научный сотрудник отдела заболеваний миокарда и сердечной недостаточности
Ж. Д. Кобалава
Россия
Член-корреспондент РАН, профессор, заведующий кафедрой внутренних болезней с курсом кардиологии и функциональной диагностики им. В. С. Моисеева, Медицинский институт
Ю. М. Лопатин
Россия
Член-корреспондент РАН, профессор, заведующий кафедрой кардиологии, сердечно-сосудистой и торакальной хирургии Института непрерывного медицинского и фармацевтического образования
С. В. Недогода
Россия
Доктор медицинских наук, профессор, заведующий кафедрой внутренних болезней Института непрерывного медицинского и фармацевтического образования
Е. И. Тарловская
Россия
Доктор медицинских наук, профессор, заведующий кафедрой терапии и кардиологии
Рецензия
Для цитирования:
Бойцов С.А., Терещенко С.Н., Виллевальде С.В., Галявич А.С., Гарганеева А.А., Глезер М.Г., Дупляков Д.В., Жиров И.В., Кобалава Ж.Д., Лопатин Ю.М., Недогода С.В., Тарловская Е.И. Практические аспекты терапии верицигуатом у пациентов с сердечной недостаточностью со сниженной фракцией выброса. Резолюция совета экспертов. Российский кардиологический журнал. 2023;28(4):5423. https://doi.org/10.15829/1560-4071-2023-5423
For citation:
Boytsov S.A., Tereshchenko S.N., Villevalde S.V., Galyavich A.S., Garganeeva A.A., Glezer M.G., Duplyakov D.V., Zhirov I.V., Kobalava Zh.D., Lopatin Yu.M., Nedogoda S.V., Tarlovskaya E.I. Practical aspects of vericiguat therapy in patients with heart failure with reduced ejection fraction. Expert council resolution. Russian Journal of Cardiology. 2023;28(4):5423. (In Russ.) https://doi.org/10.15829/1560-4071-2023-5423
JATS XML


















































