Перейти к:
Осложнения катетерной аблации фибрилляции предсердий и способы их профилактики (обзор)
https://doi.org/10.15829/1560-4071-2025-6728
EDN: RJZQCQ
Аннотация
Интервенционное лечение одного из самых распространенных нарушений ритма сердца — фибрилляции предсердий заключается в проведении различных методов аблации, возможности которой в последние годы расширяются за счет того, что кроме уже ставших классическими термических воздействий на миокард (радиочастотная или криоаблация) доступно использование электромагнитного поля (электропорации). Проведение оперативного лечения любого вида сопряжено с определенным риском возникновения различных осложнений, часть которых свойственна в большей степени классическим методикам, другая часть — новым; спектр возможных осложнений, список исследований на данную тему обширны, что требует дальнейшего изучения с целью лучшего понимания проблемы и лечения пациентов в клинической практике. В обзоре приведены основные типы возможных осложнений, ассоциированных с аблацией фибрилляции предсердий, и проведен анализ данных актуальных крупных исследований.
Для цитирования:
Немцов С.В., Лебедев Д.С. Осложнения катетерной аблации фибрилляции предсердий и способы их профилактики (обзор). Российский кардиологический журнал. 2025;30(4S):6728. https://doi.org/10.15829/1560-4071-2025-6728. EDN: RJZQCQ
For citation:
Nemtsov S.V., Lebedev D.S. Complications of catheter ablation for atrial fibrillation and their prevention: review. Russian Journal of Cardiology. 2025;30(4S):6728. (In Russ.) https://doi.org/10.15829/1560-4071-2025-6728. EDN: RJZQCQ
Ввиду высокой распространенности фибрилляции предсердий (ФП), социального, научного, экономического развития, растет и количество оперативных вмешательств для ее лечения [1]. Раннее проведение катетерной аблации приводит к хорошим результатам в поддержании синусового ритма, улучшению качества жизни пациента и снижению нагрузки на систему здравоохранения. При этом ожидаемо встречается определенный уровень осложнений (табл. 1). Целью обзора является описание наиболее часто встречающихся осложнений, обобщение имеющихся данных по указанной тематике и определение перспектив лечения с учетом современных подходов к лечению ФП.
Таблица 1
Вероятность возникновения осложнений
|
Название исследования |
Год публикации |
Годы исследования |
Вид аблации |
Количество центров наблюдения/статей |
Тип исследования |
Количество участников |
Крупные осложнения, % |
Малые осложнения, % |
Сосудистые осложнения |
Пневмоторакс, % |
Крупное кровотечение, % |
Гемоперикард/тампонада |
Повреждение пищевода, % |
ОНМК, % |
ТИА, % |
Гемолиз, % |
Стеноз ЛВ, % |
Повреждение диафрагмального нерва, % |
Гипомотильность желудка, % |
Спазм коронарных артерий, % |
Смертность, % |
||||
|
Всего, % |
Всего, % |
Предсердно-пищеводная фистула |
Любое |
||||||||||||||||||||||
|
Псевдоаневризма |
Артериовенозная фистула |
Перикардиоцентез |
Стернотомия |
Транзиторное |
Стойкое |
||||||||||||||||||||
|
Gupta, et al. [74] |
2013 |
2001-2012 |
РЧА |
192 |
метаанализ |
83236 |
2,6 |
1,4 |
0,15 |
1,7 |
0,4 |
0,4 |
0,4 |
0,2 |
0,06 |
||||||||||
|
0,5 |
0,4 |
||||||||||||||||||||||||
|
Providência, et al. [75] |
2019 |
2014-2015 |
РЧА и КБА |
7 |
обсервационное |
2497 |
2,6 |
0,7 |
0,2 |
0,1 |
1,5 |
0,1 |
|||||||||||||
|
Benali, et al. [2] |
2023 |
2013-2017 |
РЧА и КБА |
89 |
метаанализ |
15701 |
3,08 |
2,23 |
1,53 |
0,98 |
0,04 |
0,21 |
0,07 |
0,06 |
|||||||||||
|
2018-2022 |
1,87 |
1,9 |
1,11 |
0,62 |
0,17 |
||||||||||||||||||||
|
Kusano, et al. [47] |
2025 |
2023 |
РЧА и КБА |
549 |
проспективно |
102584 |
0,76 |
0,47 |
0,11 |
0,13 |
0,32 |
0,09 |
0,06 |
||||||||||||
|
MANIFEST-PF [76] |
2022 |
2021 |
ЭП |
24 |
ретроспективно |
1758 |
1,6 |
3,86 |
3,51 |
0,39 |
0,11 |
0,46 |
0,06 |
0,06 |
|||||||||||
|
MANIFEST-17K [69] |
2024 |
2022-2023 |
ЭП |
106 |
ретроспективно |
17642 |
0,98 |
3,21 |
0,3 |
0,36 |
0,04 |
0,12 |
0,03 |
0,06 |
0,14 |
0,03 |
|||||||||
|
EU-PORIA [77] |
2023 |
2021-2022 |
ЭП |
7 |
ретроспективно |
1233 |
1,7 |
1,9 |
1,1 |
0,41 |
0,16 |
0,32 |
0,08 |
||||||||||||
|
Jackel, et al. [78] |
2025 |
2013-2021 |
КБА |
114 |
ретроспективно |
184616 |
1,35 |
1,3 |
0,13 |
1,15 |
0,27 |
||||||||||||||
|
1,03 |
0,12 |
||||||||||||||||||||||||
|
РЧА |
321 |
118984 |
0,79 |
0,5 |
0,09 |
0,55 |
0,26 |
||||||||||||||||||
|
0,5 |
0,05 |
||||||||||||||||||||||||
|
Eckardt, et al. [15] |
2023 |
2005-2025 |
РЧА |
4 |
ретроспективно |
30361 |
1,1 |
0,22 |
0,67 |
0,16 |
0,04 |
||||||||||||||
|
POTTER-AF [32] |
2023 |
1996-2022 |
РЧА |
214 |
ретроспективно |
553729 |
0,038 |
||||||||||||||||||
|
КБА |
0,0015 |
||||||||||||||||||||||||
|
YET I [38] |
2022 |
2012-2019 |
КБА |
33 |
ретроспективно |
17356 |
4,2 |
0,1 |
|||||||||||||||||
|
Friedman, et al. [15] |
2020 |
2013-2017 |
РЧА и КБА |
Medicare* |
ретроспективно |
102398 |
0,61 |
||||||||||||||||||
|
NCDR [79] |
2025 |
2019-2022 |
РЧА и КБА |
186 |
проспективно |
70296 |
1,0 |
1,19 |
0,406 |
0,1 |
0,4 |
0,11 |
0,1 |
0,003 |
|||||||||||
|
0,1 |
0,006 |
0,3 |
0,1 |
0,1 |
0,02 |
||||||||||||||||||||
Примечание: * — Centers for Medicare & Medicaid Services, Балтимор, Мэрилэнд, США.
Сокращения: КБА — криобаллонная аблация, ЛВ — легочные вены, ОНМК — острое нарушение мозгового кровообращения, РЧА — радиочастотная катетерная аблация, ТИА — транзиторная ишемическая атака, ЭП — электропорация.
Повреждение магистральных сосудов. Гематомы мягких тканей, забрюшинного пространства
Сосудистые осложнения являются наиболее частыми серьезными осложнениями катетерной аблации при ФП и включают возникновение гематомы мягких тканей бедра, забрюшинные гематомы, псевдоаневризмы сосудов, артериовенозные фистулы. Частота их возникновения находится в пределах от 1 до 4% [2][3]. Большинство указанных осложнений можно лечить консервативно или компрессионным методом (путем осуществления мануального гемостаза, в т.ч. посредством ультразвукового датчика с последующим наложением давящей повязки на 6-12 ч или инъекцией тромбина [4]), а контроль достигается посредством ультразвуковых методов диагностики. Однако в случае серьезной кровопотери может потребоваться переливание крови и/или проведения хирургического открытого или чрескожного пособия. Частота возникновения осложнений может быть связана с опытом оператора, количеством и размером используемых интродьюсеров, использованием дополнительного артериального доступа в процессе лечения и антикоагулянтной терапией [5]. При подготовке пациента к операции возможно применение тактики непрерывной терапии антикоагулянтами без перевода на низкомолекулярный гепарин. Рандомизированные исследования не выявили повышенного риска сосудистых осложнений при проведении непрерывной терапии пероральными антикоагулянтами по сравнению с непрерывным применением антагонистов витамина К [6].
Профилактика осложнений определяется методикой доступа к бедренной вене, а также использованием вспомогательных средств визуализации сосудов. При использовании низкого доступа (>2 см ниже паховой связки) к бедренной вене могут быть повреждены ветви бедренной артерии (a. pudenda ext.), проходящие поверх бедренной вены, что может привести к серьезному интраоперационному кровотечению, образованию псевдоаневризмы и гематоме. С другой стороны, при применении высокого доступа (непосредственно под паховой связкой) повышаются риски забрюшинного кровотечения и гематомы (рис. 1). Применение ультразвукового контроля значимо понижает риски повреждения сосудов при проведении радиочастотной катетерной аблации (РЧА) ФП [7].
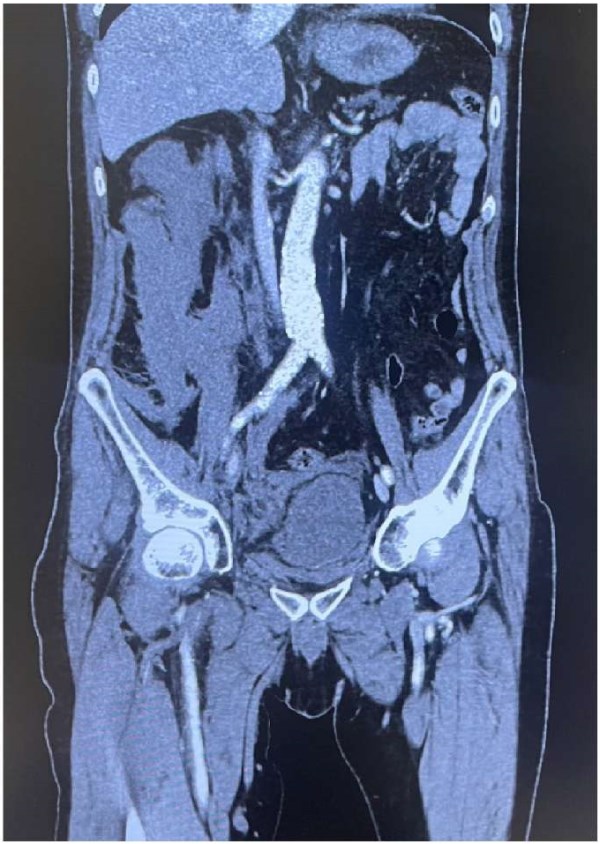
Рис. 1. КТ-картина крупной забрюшинной гематомы справа у пациента после радиочастотной изоляции ЛВ.
Стеноз и окклюзия сосудов сердца
Стенозирование сосудов в процессе оперативного лечения может касаться как легочных вен (ЛВ), так и коронарных артерий; определяется сужением сосуда на <50% (незначительный), умеренный (50-70%), серьезный (>70%) вследствие нанесенного воздействия и в случае стеноза ЛВ может проявить себя на 8-12 нед. после операции [8]. Указанное осложнение возникает ввиду термического повреждения ткани сосуда, прогрессирующей сосудистой реакцией и замещения коллагеном поврежденного миокарда [9]. Также его возникновение находится в прямой зависимости от методики оперативного лечения (дистального нанесения воздействий при циркулярной изоляции ЛВ), а также количества аппликаций. К типичным потенциально возможным областям, в которых возможно повреждение коронарных артерий, можно отнести: латеральная поверхность сердца эпикардиально, вены сердца, основание ушка левого предсердия (ЛП), митральный истмус или септальная поверхность верхней полой вены (с возможностью повреждения в т.ч. артерии синусового узла с вероятностью до 0,09% как при РЧА, так и при криобаллонной аблации (КБА) ФП [10][11] и развитии клинически значимой брадикардии [12]) (рис. 2). В случае необходимости нанесения аппликаций эпикардиально для уточнения точной анатомии коронарных сосудов рекомендовано предварительное выполнение коронарографии. При повреждении коронарных сосудов возникают типичные признаки острой ишемии миокарда, фибрилляция желудочков и остановка сердечной деятельности, что требует немедленной реваскуляризации миокарда [13]. При соблюдении техники безопасности во время оперативного вмешательства частота поражения коронарных артерий при РЧА или КБА ФП крайне редка. Встречаемость же стеноза ЛВ более распространена: в ранних исследованиях сообщалось о вероятности до 38% [14]. С эволюцией подходов к лечению ФП наблюдается и значимое его снижение до 0,05% [3]. В случае незначительного стенозирования ЛВ чаще протекает асимптомно. В случае более серьезного поражения сосуда может протекать с более частым возникновением пневмонии у пациента, кашлем, одышкой, а также гемоптизом. Проведение компьютерной томографии (КТ) грудной клетки с контрастированием сердца и сосудов поможет верифицировать диагноз, а для лечения методом выбора является баллонная ангиопластика и стентирование целевого сосуда (рис. 3). В случае окклюзии ЛВ может наблюдаться компенсаторная дилатация ипсилатеральных ЛВ.
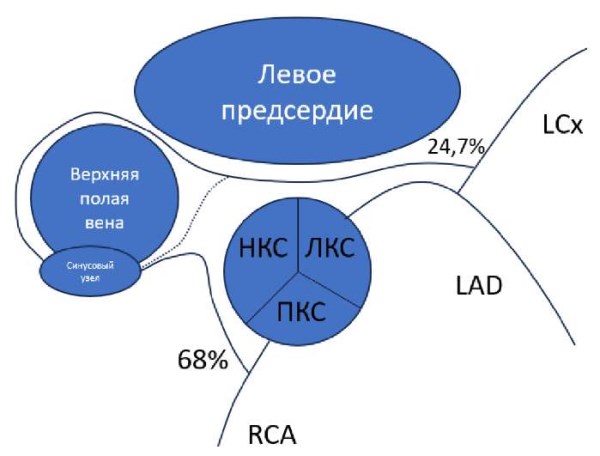
Рис. 2. Варианты отхождения артерии синусового узла.
Примечание: повреждение артерии наиболее вероятно в области верхней трети межпредсердной перегородки, верхней части левого предсердия, области ушка правого предсердия, дистально в коронарном синусе.
Сокращения: ЛКС — левый коронарный синус, ПКС — правый коронарный синус, НКС — некоронарный синус. LCx — левая огибающая артерия, LAD — передняя межжелудочковая артерия, RCA — правая коронарная артерия.

Рис. 3. Пациент 43 лет.
Примечание: в течение года после проведенной РЧА ипсилатеральных ЛВ описывает кашель, одышку, а также многократное возникновение пневмонии, требовавшей проведения антибактериальной терапии. A — данные КТ, стрелкой показаны пораженные сосуды: окклюзия верхнедолевого ствола ЛВ, стеноз среднедолевого ствола ЛВ (50%) справа. И этапы интервенционного лечения: B — контрастирование сосудов и сердца до проведения ангиопластики; C — ангиопластика верхнедолевого ствола правой ЛВ; D — конечный результат операции после проведенного стентирования ЛВ.
Сокращения: КТ — компьютерная томография, ЛВ — легочные вены, РЧА — радиочастотная катетерная аблация.
Повреждение стенки сердца, аорты и ЛВ. Гемоперикард
Повреждение стенки сердца и, как следствие, гемоперикард — наиболее частое жизнеугрожающее осложнение при аблации ФП. Недавние крупные метаанализы докладывает среднюю встречаемости данного осложнения порядка 0,7-0,8% на настоящий момент, констатируя тренд постепенного снижения числа этого грозного осложнения, что может быть связано как с ростом опыта, так и с усовершенствованием технического обеспечения оперативного пособия [15]. В НМИЦ им. В. А. Алмазова также отмечается явная тенденция к снижению частоты встречаемости данного осложнения: если на момент 2019г количество составляло 10 случаев на 1000 пациентов, то к 2024г уже наблюдалось двукратное его снижение. К предрасполагающим факторам можно отнести повреждение стенки сердца и проникновение инструмента в перикардиальное пространство или корень аорты при выполнении транссептальной пункции (при этом риск возникновения осложнения увеличивается при использовании >1 транссептального доступа), перегрев ткани при проведении аблации и возникновение явления, известного как "steam pop", нанесение множественных аблаций, а также чрезмерная интраоперационная гипокоагуляция, а также отказ от использования внутрисердечной эхокардиографии (ЭхоКГ) [16]. Предшествующие операции на сердце в большинстве случае предохраняют его от возникновения данного осложнения при проведении РЧА ввиду развития выраженного спаечного процесса в перикардиальной полости. В случае возникновения острого повреждения с одномоментным излитием значительного количества крови в полость перикарда кроме стремительного снижения уровня артериального давления, возможно возникновение синоатриальной и/или атриовентрикулярной блокады, остановки сердечной деятельности и электромеханической диссоциации. В ином случае медленное накопление жидкости можно обнаружить в течение нескольких часов после выполнения оперативного вмешательства при проведении ЭхоКГ (и обнаружении жидкости, превышающей физиологичный объем в 15-50 мл), проведение субксифоидальной пункции перикарда для ее эвакуации (которая служит методом выбора при лечении большинства случаев гемоперикарда) может не потребоваться. Следует учитывать, что скопление значимого количества жидкости в полости перикарда, а также лечебные манипуляции являются фактором риска возникновения асептического и констриктивного перикардита [17][18]. Золотым стандартом определения количества жидкости в полости перикарда является ЭхоКГ, однако проведение диагностики также возможно методом рентгенографии интраоперационно, как правило, при скоплении значительного количества жидкости в перикардиальной полости (рис. 4). После успешного выполнения пункции перикарда и его дренирования, в случае продолжения накопления жидкости может потребоваться проведение открытого хирургического вмешательства для ушивания дефекта сердца. При проведении аблации, манипуляция инструментом создает предпосылки к повреждению не только сердца, но и ЛВ. Описаны случаи их повреждения при манипуляции инструментом на фоне проведения КБА с развитием жизнеугрожающего гемоптиза (кровохарканья), потребовавшего селективной интубации левого легкого, баллонирования скомпрометированного бронха для остановки кровотечения и в последующем резекции нижней доли правого легкого [19].
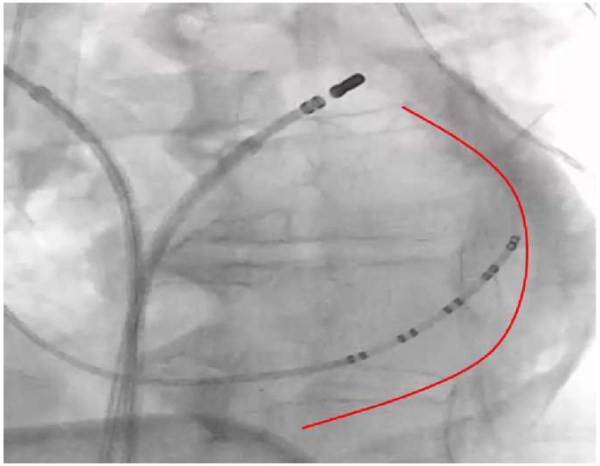
Рис. 4. Гемоперикард в ходе катетерной аблации. Определяется "двойной контур" сердца, свидетельствующий о наличии жидкости в полости перикарда.
Повреждение клапанного аппарата сердца
Возникновение данного осложнения возможно в результате защемления катетера клапанами сердца и относится к редким и опасным осложнениям аблации ФП. Чаще встречается при манипуляциях диагностическими катетерами, такими как циркулярный многополюсный электрод с целью его установки в левые ЛВ. В случае возникновения значимого сопротивления важно не применять силу для высвобождения электрода, т.к. это может привести к травме клапанного аппарата и даже отрыву папиллярных мышц, и потребовать открытого хирургического лечения [20][21], а также к отлому кончика катетера, что также требует его удаления эндоваскулярным способом посредством петли, либо открытой операции [22]. При подозрении на это осложнение важно подтвердить диагноз с помощью ЭхоКГ. Одним из вариантов высвобождения электрода является введение высокой дозы аденозинтрифосфата для того, чтобы вызвать полную атриовентрикулярную блокаду или применить высокочастотную стимуляцию желудочков, тем самым снимая напряжение на митральном клапане для высвобождения кончика катетера [23]. Чтобы предотвратить это осложнение, следует с особой осторожностью манипулировать диагностическими катетерами вблизи митрального клапана. Кроме того, стоит придерживаться особой бдительности при манипуляциях катетером вблизи механических протезов ввиду повышенного риска их защемления. В случае с диагностическим катетером для высокоплотного картирования камер сердца PENTARAY (Biosense Webster — подразделение Johnson & Johnson MedTech, США), наличие механического протеза картируемой камеры сердца определено прямым противопоказанием к использованию непосредственно производителем устройства. В случае защемления многополюсного электрода механическим клапаном, чрезмерное давление увеличивает риск его механического повреждения, для его высвобождения может быть применена техника проведения аблационного электрода через управляемый интродьюсер непосредственно к заклинившей створке митрального клапана с целью создания давления на нее и высвобождения катетера [24].
Синдром жёсткого ЛП
Впервые описанный после операции на митральном клапане, синдром жёсткого ЛП признан редким осложнением катетерной аблации ЛП и обычно возникает после проведения множественных аблаций, особенно у пациентов с уже имеющимися фиброзными изменениями миокарда после перенесенного воспалительного и/или инфекционного процесса, что подтверждается ЭхоКГ исследованиями [25][26]. Осложнение проявляется признаками перегрузки правых камер сердца, включая легочную гипертензию, повышением давления в ЛП. В качестве медикаментозной терапии описано применение диуретиков, а в случае отсутствия эффекта — силденафила [27][28].
Повреждение пищевода
Термическое повреждение пищевода радиочастотной энергией и образование предсердно-пищеводной фистулы является одним из наиболее опасных и часто фатальных осложнений аблации ФП. Анатомическое расположение пищевода вариабельно, но ~70% всех случаев он расположен ближе к левым ЛВ; также особенности топографии пищевода могут зависеть от индивидуальных особенностей пациента и сопутствующих заболеваний (грыжа пищеводного отверстия диафрагмы и др.). Пищевод является подвижной структурой, его положение относительно ЛП может меняться во время и после проведения оперативного вмешательства и смещаться вбок до нескольких сантиметров. Помимо расстояния между пищеводом и задней стенкой ЛП, еще одним анатомическим фактором, влияющим на вероятность термического повреждения пищевода, является наличие перикардиальных жировых отложений вокруг каждой ЛВ, которые могут защищать от повреждений пищевод во время аблации. Движение пищевода может быть ограничено структурами средостения (аорта, позвоночник), что может способствовать повреждению пищевода во время аблации. Воздействие радиочастотным током на артериолы, кровоснабжающие пищевод, ухудшает приток крови к пораженной ткани, что вызывает изъязвления пищевода, часто бессимптомные и встречающееся от 3 до 10% всех случаев изоляции ЛВ и зависит от мощности подаваемого радиочастотного тока [29-31]. Изъязвления могут прогрессировать в течение нескольких недель до предсердно-пищеводной фистулы (в среднем от 18 до 21 дня). В случае возникновения последней, вероятность летального исхода приближается к 80%. В крупном регистре POTTER-AF (553729 процедур) частота возникновения предсердно-пищеводных фистул составила порядка 0,025%. При этом частота возникновения значительно различалась между включенными медицинскими центрами (от 0,007% до 0,4%), что может указывать на высокую значимость применяемой техники проведения катетерной аблации [32].
Повреждения пищевода наблюдаются в большей степени после РЧА, хотя описаны редкие случаи возникновения данного осложнения и после проведения КБА ФП (0,038% при РЧА, 0,0015% при КБА) [33]. Симптоматика может включать дисфагию, загрудинные боли, кровохарканье, лихорадку, судороги, общемозговую симптоматику при быстром прогрессировании. Учитывая, что формирование предсердно-пищеводной фистулы, как правило, занимает десятки дней, проведение эзофагоскопии может быть оправдано у пациентов на раннем этапе (рис. 5), в ином случае ее выполнение строго противопоказано, т.к. инсуффляция газа при проведении исследования влечет за собой его попадание в большой круг кровообращения; в ходе диагностики должна быть выполнена КТ органов грудной клетки с контрастированием сосудов. Профилактика осложнения достигается интраоперационным применением термических датчиков, проточно-промывных систем для охлаждения пищевода в процессе аблации и ограничением количества подаваемых аппликаций.
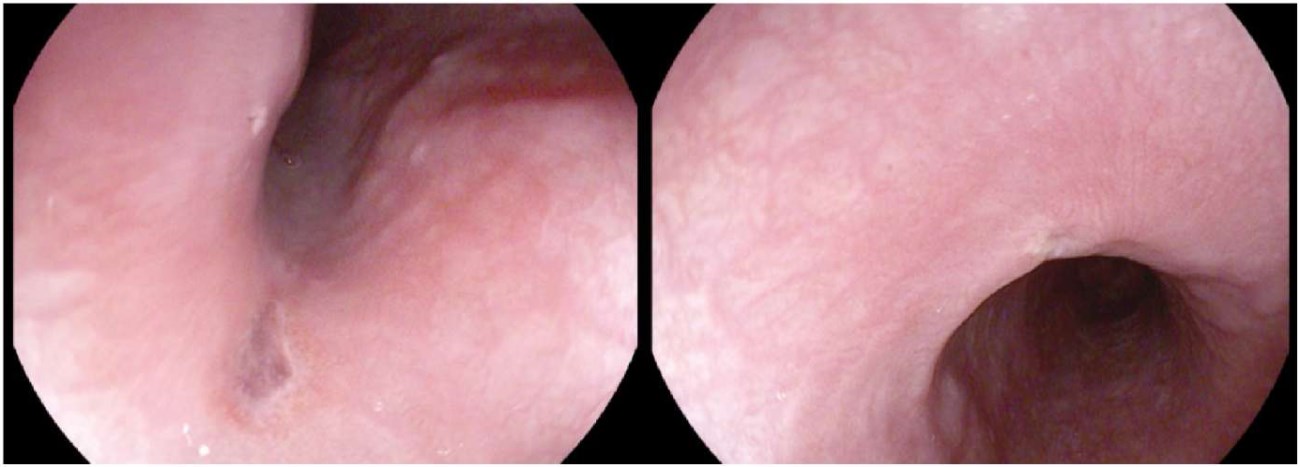
Рис. 5. Фиброэзофагоскопия пациентки 46 лет.
Примечание: слева — изъязвление пищевода, выявленное на 3-и сутки после РЧА. Справа — контрольное исследование на 5‑е сутки лечения, включавшее в себя диету с ограничением жесткой пищи, назначение гастропротекторной терапии, антибактериальных препаратов.
Сокращение: РЧА — радиочастотная катетерная аблация.
Повреждение диафрагмального нерва
Парез или паралич диафрагмального нерва (ДН), проходящего кпереди от правых ЛВ, по свободной стенке правого предсердия, возникает в результате прямого его повреждения чаще в процессе КБА [34], но также описаны случаи его возникновения и при проведении РЧА ФП: при изоляции верхней полой вены (чаще), антральной изоляции ЛВ [35]. При парезе ДН, т.е. частичной утрате его функции, симптоматика ограничивается затрудненным дыханием, кашлем, ограничением подвижности диафрагмы, тогда как при его параличе происходит полная утрата произвольных движений мышцы, клиническая картина расширяется значимым чувством нехватки воздуха, удушьем. Также повышается риск возникновения пневмонии. Частота интраоперационного поражения ДН может достигать 13,5% прооперированных пациентов методом КБА [36]. В абсолютном большинстве случаев поражается правый ДН, поскольку он проходит в непосредственной близости от правых, в особенности от правой верхней ЛВ, в связи с чем повреждение ДН при воздействии в ней составляет >80% от всех зарегистрированных событий [37][38]. Повреждение левого ДН происходит крайне редко (0,3%), т.к. дистанция от него до левых ЛВ составляет 7-10 мм и чаще сопряжено с воздействиями в области ушка ЛП.
В большинстве случаев повреждение ДН является транзиторным и разрешается еще до окончания операции [39]. В иных случая восстановление функции ДН занимает от нескольких недель до 12 мес. (до 97%) [38], в редких случаях до 2 лет [40]. Хроническое поражение (паралич) ДН наблюдается у 0,1% пациентов. Рентгенологически наблюдается высокое стояние купола диафрагмы (рис. 6), быстрая диагностика также возможна путем проведения ультразвуковых методов диагностики.
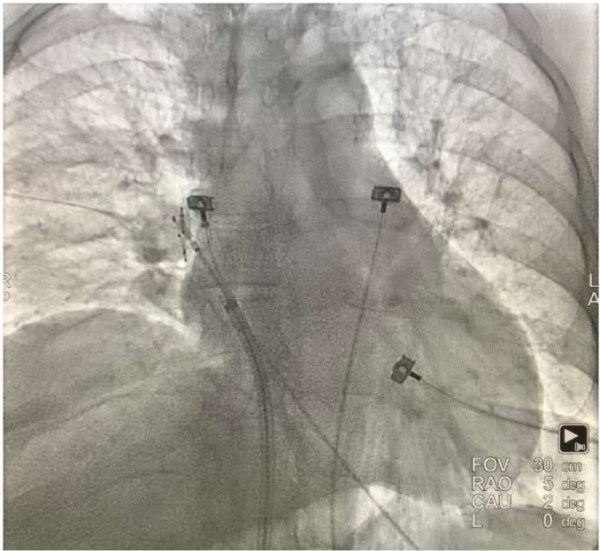
Рис. 6. Рентгенологическая картина при возникшем парезе ДН после КБА в правой верхней ЛВ. Обращает на себя внимание высокое стояние правого купола диафрагмы. При наблюдении отмечается отсутствие спонтанных движений диафрагмы.
Профилактика осложнения достигается методиками непрерывного мониторинга функции ДН путем его стимуляции из подключичной или верхней полой вены в процессе аппликации, проведением различных вариантов диафрагмальной электромиографии и измерением амплитуды измеренных потенциалов (уменьшение амплитуды миопотенциала на 30%) [41][42], пальпацией живота во время процедуры, использованием баллона подходящего размера, без заведения его дистально в сосуд — проведением антральной изоляции ЛВ, избегать нанесения излишнего количества аппликаций [43].
У пациентов с выраженной симптоматикой физиотерапия межреберных и лестничных мышц может улучшить дыхание. Пациентам с параличом ДН может быть показано хирургическое лечение методом диафрагмальной пликации.
Пневмоторакс
Относится к серьезным, но достаточно редким осложнениям интервенционного лечения ФП. Связано это с возможностью использования бедренного доступа в качестве альтернативного для позиционирования диагностического катетера, таким образом использование подключичного доступа в клинической практике сводится к минимуму. В случае же предпочтительности использования подключичного доступа по любым причинам (технические трудности при пункции бедренных вен, нестабильность положения диагностического электрода в коронарном синусе, скудная выраженность периферических вен и др.) частота возникновения пневмоторакса составит 0,5-6,6% [44, 45]. Вероятность находится в прямой зависимости от опыта оператора, использования вспомогательных средств визуализации (рентгенография, ультразвуковые средства диагностики), экстренности выполнения процедуры. Очевидными альтернативами подключичному доступу с минимальными рисками возникновения данного осложнения являются яремный и подмышечный, однако при их использовании сохраняются риски ранения артериальных сосудов с возникновением кровотечения и/или клинически значимых гематом.
Гемоторакс
Относится к редким, но потенциально грозным осложнениям и встречается до 0,02% случаев в крупных исследованиях. В литературе встречаются упоминания в связи с повреждением подключичной, внутренней грудной, правой восьмой межреберной артерии [46]. Диагностика осуществляется методом рентгенологического, ультразвукового, лечение, как правило, консервативное, в ряде случаев требуется проведение пункции плевральной полости для эвакуации жидкости.
Тромбоэмболические осложнения. Острое нарушение мозгового кровообращения
Тромбоэмболические осложнения относятся к значимым осложнениям аблации ФП, в большинстве своем представляя собой нарушения мозгового кровообращения. Частота их возникновения составляет 0,14-0,5% всех случаев оперативного лечения и чаще возникают в течение суток после процедуры [47][48]. Однако различными исследованиями было доказано, что 1,7-38% поражений головного мозга в послеоперационном периоде может протекать бессимптомно [49]. В основе тромбоэмболических осложнений лежит образование тромбов, нагара на интродьюсерах или электроде или попадание воздуха в сердце через транссептальные интродьюсеры, как правило, ввиду нарушения техники их промывания при замене или удалении инструмента с возникновением воздушной эмболии. Наиболее часто происходит миграция воздуха в правую коронарную артерию с возникновением транзиторных признаков острой ишемии миокарда, нарушениями генерации/проведения электрических импульсов, изредка отмечается остановка сердечной деятельности, электромеханическая диссоциация. При развитии воздушной эмболии с поражением головного мозга наблюдается очаговая, общемозговая симптоматика. В таком случае быстрое придание пациенту положения Тренделенбурга, проведение инфузионной, оксигенотерапии, направленной на максимизацию перфузии головного мозга, позволит значимо увеличить скорость абсорбции азота из попавшего в кровеносное русло воздуха. Соблюдение правил предоперационной подготовки пациента, антикоагуляции, гепаринизация до проведения транссептальной пункции [50], поддержание активированного частичного тромбопластинового времени в пределах целевых значений (300-400 сек), соблюдение техники безопасности во время оперативного лечения, интраоперационное промывание интродьюсеров снижает риски данных осложнений [51]. Недавний крупный метаанализ показал наличие взаимосвязи между щелевидным левосторонним дефектом межпредсердной перегородки (отсутствием сращения первичной и вторичной межпредсердной перегородки) и возникновением острого нарушения мозгового кровообращения (ОНМК) [52] ввиду возможности образования в имеющемся дефекте тромбов, что увеличивает настороженность при проведении чреспищеводного ЭхоКГ исследования перед операцией и может повлечь за собой откладывание процедуры [53]. В противном случае смещение тромба при манипуляциях инструментами или при проведении электроимпульсной терапии с высокой долей вероятности влечет за собой возникновение ОНМК и необходимость применения чрескожных вмешательств на головном мозге — проведения тромбэкстракции. Применение коротких аппликаций высокой мощности >70 Вт, увеличивает частоту возникновения немых инсультов [54].
Гипомоторика желудка. Гастропарез. Пилороспазм
Гипомоторика желудка, а также гастропарез (расстройство, характеризующееся задержкой опорожнения желудка при отсутствии для этого механических причин) может возникнуть при аблации ФП до 17,3% случаев, чаще при КБА ФП и возникает из-за повреждения переднего пищеводного сплетения в большей степени при воздействиях в области нижних ЛВ. Хотя впервые данное осложнение было описано еще в 2005г [55], на сегодня оно является одним из наиболее недооцененных. Установлено, что расстояние между пищеводом и правой нижней ЛВ <18,2 мм (что может быть выявлено при проведении КТ органов грудной клетки перед операцией) является предиктором нарушения моторики желудка после проведения аблации ФП [56][57]. Клиническая картина включает в себя: эпизодические боли в животе, вздутие живота, тошноту, рвоту, возникающие преимущественно в течение 24 ч после операции. Время восстановления, как правило, занимает от 2 нед. до 3 мес. Диагностика включает в себя проведение фиброгастроскопии, рентгеноскопии с бариевым раствором, КТ органов брюшной полости (для оценки количества остаточной пищи в желудке).
Лечение зависит от выраженности симптоматики и в первую очередь предполагает модификацию диеты: малые порции обезжиренной пищи с низким содержанием клетчатки. Медикаментозное лечение предусматривает назначение препаратов, улучшающих моторику желудка и противорвотных препаратов (метоклопрамид). Обосновано применение прокинетиков нового поколения, в частности агонистов рецепторов 5-HT 4 (прукалоприд, наронаприд и др.) [58]; следует учесть, что некоторые прокинетики, к примеру антагонисты дофаминовых рецепторов (домперидон), могут обладать проаритмогенным эффектом в виде удлинения интервала QT >60 мс и должны назначаться с осторожностью [59]. В более поздних работах встречается описание эффектов эритромицина, который также может быть эффективен в лечении данного осложнения [60]. У пациентов с преобладающим пилороспазмом в качестве вариантов лечения предлагаются интрапилорические инъекции ботулотоксина или различные виды хирургических вмешательств на привратнике желудка [61].
Электропорация — новый метод катетерной аблации
Применение электропорации определяет новый этап в лечении ФП, предполагающий применение нетермического метода нанесения воздействия. Электропорация предполагает нанесение сверхчастых (микро- или наносекунды) электрических импульсов для генерации электрического поля, вызывающего образование пор в мембране кардиомиоцитов с последующим некрозом клеток. Применение данной технологии может помочь избежать части серьезных осложнений в лечении ФП. Определено, что осложнения могут быть ассоциированы как с доступом и манипуляциями инструментом (гемоперикард, тампонада сердца), так и непосредственно с применением электропорации (спазм коронарных артерий, ОНМК, гемолиз). Первыми, в т.ч. многоцентровыми, исследованиями на данную тему (MANIFEST-PF, IMPULSE, PEFCAT и др.) не было выявлено признаков повреждения пищевода, стеноза ЛВ, паралича ДН. При дальнейших наблюдениях выясняется, что хотя некоторые многоцентровые исследования (MANIFEST-17K) не описывают ранее упомянутых осложнений, другие все же выявляют случаи возникновения стойкого повреждения ДН [62]; электропорация также способна вызывать повреждение пищевода, не носящее трансмуральный характер и обычно разрешающееся к 14 дням после воздействия [63]. Более серьезным вопросом является воздействие на коронарные сосуды. При применении электропорации в непосредственной близости от коронарных артерий, как это было показано в экспериментах "in vivo", приводит к необратимому фиброзу медии сосуда [64], что может потенциально ограничивать ее применение при эпикардиальных аблациях. На настоящем этапе в клинической практике электропорация используется эндокардиально, при этом доказанным является возможность возникновения значимого спазма коронарных сосудов на фоне аблации, которое может сохраняться в течение нескольких месяцев после операции, а также угрожать развитием хронического стеноза пораженного сосуда [65]. Частота возникновения осложнений, ассоциированных с поражением коронарных сосудов, в несколько раз выше при проведении электропорации, чем при традиционных методах аблации, но в большей степени зависит от того, дополняется ли классическая изоляция ЛВ воздействиями в митральном, кавотрикуспидальном истмусах или иных областях, где есть риск повреждения артерии. Если в сравнительном исследовании от 2025г приводятся данные о повреждении коронарных сосудов при электропорации в 5,8%, 0,6% при РЧА [66], то в уже упомянутом крупном исследовании MANIFEST-17K указывается на 0,14% событий, что сравнимо с большинством предшествовавших исследований РЧА (0,04-0,6%) и КБА (0,17-0,34%) ФП [10][67-69]. При возникновении признаков спазма коронарных сосудов эффективным является применение нитроглицерина [70].
Острое повреждение почек. Гемолиз
Нарушение функции почек при проведении РЧА или КБА встречается редко и в большей степени ассоциировано с применением контрастного вещества, особенно у пациентов с уже имеющейся патологией почек, однако при выполнении электропорации данное осложнение имеет большую значимость. Еще в 1977г было описано воздействие сильного электромагнитного поля на клетки крови. Установлено, что хотя эритроциты устойчивы к механическому воздействию, они особенно восприимчивы к электропорации, которая вызывает повреждение эритроцитов и последующее высвобождение гемоглобина в зависимости от выраженности воздействующего на них электрического поля [71][72]. В недавнем многоцентровом проспективном исследовании установлено, что лабораторные признаки гемолиза выявляются у большинства, перенесших процедуру электропорации: 94,3% vs 6,8% при РЧА и сопровождается снижением уровня гаптоглобина, значительно более высоким уровнем свободного гемоглобина в плазме крови, билирубина, лактатдегидрогеназы. При этом уровень креатинина был ассоциирован со скоростью клубочковой фильтрации пациента и значимо повышался (>5 ммоль/л) при величине <50 мл/мин; гемоглобинурия встречалась у 36,4% пациентов [73]. Важным является факт того, что всеми исследованиями отмечается прямая зависимость степени гемолиза и его влияния на функцию почек от количества нанесенных аппликаций. В ряде случаев это может привести к развитию острой почечной недостаточности и необходимости проведения гемодиализа. Также установлено, что острое повреждение почек чаще наблюдаются у пациентов пожилого возраста, с уже имеющейся хронической болезнью почек, артериальной гипертензией, сахарным диабетом, сниженной фракцией выброса левого желудочка и более выраженным гемолизом.
Заключение
Несмотря на значительный технологический прогресс в проведении аблации ФП за последние годы, зарегистрированные показатели осложнений и смертности остаются значимыми. Перечень осложнений варьируется в зависимости от методики лечения пациента. При детальном изучении отмечается тенденция к уменьшению числа возникающих осложнений с течением времени, что, вероятно, связано с увеличением количества проводимых операций и модификации техники проведения оперативного лечения.
Отношения и деятельность: все авторы заявляют об отсутствии потенциального конфликта интересов, требующего раскрытия в данной статье.
Список литературы
1. Van Gelder IC, Rienstra M, Bunting KV, et al.; ESC Scientific Document Group. 2024. ESC Guidelines for the management of atrial fibrillation developed in collaboration with the European Association for Cardio-Thoracic Surgery (EACTS). Eur Heart J. 2024;45(36):3314- 414. doi:10.1093/eurheartj/ehae176. Erratum in: Eur Heart J. 2025;46(41):4349. doi:10.1093/eurheartj/ehaf306.
2. Arbelo E, Brugada J, Blomström-Lundqvist C, et al. Contemporary management of patients undergoing atrial fibrillation ablation: in-hospital and 1 year follow-up findings from the ESC-EHRA atrial fibrillation ablation long-term registry. Eur Heart J. 2017;38(17):1303-16. doi:10.1093/eurheartj/ehw564.
3. Benali K, Khairy P, Hammache N, et al. Procedure-Related Complications of Catheter Ablation for Atrial Fibrillation. J Am Coll Cardiol. 2023;81(21):2089-99. doi:10.1016/j.jacc.2023.03.418.
4. Sareena G, Mintz AriJ, Sanjum S, et al. Current Treatment Options for Femoral Pseudoaneurysms. Early detection, monitoring, and appropriate treatment for femoral pseudoaneurysms are important to reduce morbidity. Cardiac Interventions Today. 2023;17(4):55-9.
5. Waigand J, Uhlich F, Gross CM, et al. Percutaneous treatment of pseudoaneurysms and arteriovenous fistulas after invasive vascular procedures. Catheter Cardiovasc Interv. 1999;47(2):157-64. doi:10.1002/(SICI)1522-726X(199906)47:23.0.CO;2-Y.
6. Kirchhof P, Haeusler KG, Blank B, et al. Apixaban in patients at risk of stroke undergoing atrial fibrillation ablation. Eur Heart J. 2018;39(32):2942-55. doi:10.1093/eurheartj/ehy176.
7. Ströker E, de Asmundis C, Kupics K, et al. Value of ultrasound for access guidance and detection of subclinical vascular complications in the setting of atrial fibrillation cryoballoon ablation. Europace. 2019;21(3):434-9. doi:10.1093/europace/euy154.
8. Dong J, Vasamreddy CR, Jayam V, et al. Incidence and predictors of pulmonary vein stenosis following catheter ablation of atrial fibrillation using the anatomic pulmonary vein ablation approach: results from paired magnetic resonance imaging. J Cardiovasc Electrophysiol. 2005;16(8):845-52. doi:10.1111/j.1540-8167.2005.40680.x.
9. Taylor GW, Kay GN, Zheng X, et al. Pathological effects of extensive radiofrequency energy applications in the pulmonary veins in dogs. Circulation. 2000;101(14):1736-42. doi:10.1161/01.cir.101.14.1736.
10. Chugh A, Makkar A, Yen Ho S, et al. Manifestations of coronary arterial injury during catheter ablation of atrial fibrillation and related arrhythmias. Heart Rhythm. 2013;10(11):1638- 45. doi:10.1016/j.hrthm.2013.09.001.
11. Yamaji K, Fujihara K, Fukawa Y, et al. Sinus node dysfunction caused by a sinus node artery occlusion during catheter ablation and sinus rhythm restoration post-PCI. HeartRhythm Case Rep. 2024;10(12):886-9. doi:10.1016/j.hrcr.2024.08.022.
12. Kitamura T, Fukamizu S, Arai K, et al. Transient sinus node dysfunction following sinus node artery occlusion due to radiofrequency catheter ablation of the septal superior vena cava-right atrium junction. J Electrocardiol. 2016;49(1):18-22. doi:10.1016/j.jelectrocard.2015.11.001.
13. Takahashi Y, Jaïs P, Hocini M, et al. Acute occlusion of the left circumflex coronary artery during mitral isthmus linear ablation. J Cardiovasc Electrophysiol. 2005;16(10):1104-7. doi:10.1111/j.1540-8167.2005.50124.x.
14. European Heart Rhythm Association (EHRA); European Cardiac Arrhythmia Scoiety (ECAS); American College of Cardiology (ACC); American Heart Association (AHA); Society of Thoracic Surgeons (STS); Calkins H, Brugada J, Packer DL, et al. HRS/EHRA/ ECAS expert Consensus Statement on catheter and surgical ablation of atrial fibrillation: recommendations for personnel, policy, procedures and follow-up. A report of the Heart Rhythm Society (HRS) Task Force on catheter and surgical ablation of atrial fibrillation. Heart Rhythm. 2007;4(6):816-61. doi:10.1016/j.hrthm.2007.04.005. Erratum in: Heart Rhythm. 2009;6(1):148.
15. Eckardt L, Doldi F, Anwar O, et al. Major in-hospital complications after catheter ablation of cardiac arrhythmias: individual case analysis of 43031 procedures. Europace. 2023;26(1):euad361. doi:10.1093/europace/euad361.
16. Friedman DJ, Pokorney SD, Ghanem A, et al. Predictors of Cardiac Perforation With Catheter Ablation of Atrial Fibrillation. JACC Clin Electrophysiol. 2020;6(6):636-45. doi:10.1016/j.jacep.2020.01.011.
17. Fukasawa K, Umetani K, Yano T, et al. Constrictive pericarditis following atrial fibrillation catheter ablation with cardiac tamponade. HeartRhythm Case Rep. 2021;7(12):836-9. doi:10.1016/j.hrcr.2021.09.007.
18. Sudo K, Shigeta T, Oda A, et al. Pulmonary Vein Perforation and Life-Threatening Hemoptysis During Cryoballoon Ablation for Persistent Atrial Fibrillation. JACC Case Rep 2022;4(7):418-23. doi:10.1016/j.jaccas.2021.11.026.
19. Grove R, Kranig W, Coppoolse R, et al. Demand for open heart surgery due to entrapment of a circular mapping catheter in the mitral valve in a patient undergoing atrial fibrillation ablation. Clin Res Cardiol. 2008;97(9):628-9. doi:10.1007/s00392-008-0677-2.
20. Kesek M, Englund A, Jensen SM, et al. Entrapment of circular mapping catheter in the mitral valve. Heart Rhythm. 2007;4(1):17-9. doi:10.1016/j.hrthm.2006.09.016.
21. Tavernier R, Duytschaever M, Taeymans Y. Fracture of a circular mapping catheter after entrapment in the mitral valve apparatus during segmental pulmonary vein isolation. Pacing Clin Electrophysiol. 2003;26(8):1774-5. doi:10.1046/j.1460-9592.2003.t01-1-00268.x.
22. Kim EJ, Gerstenfeld EP, Pellegrini CN. Use of Adenosine to Release an Entrapped Catheter During Ablation of Premature Ventricular Complexes. JACC Case Rep. 2021;3(4):610-3. doi:10.1016/j.jaccas.2021.02.011.
23. Yagishita A, Ayabe K, Sakama S, et al. A Novel Technique to Release a PentaRay Entrapped in a Mechanical Mitral Valve Using an Ablation Catheter. JACC Clin Electrophysiol. 2020;6(12):1597-8. doi:10.1016/j.jacep.2020.08.017.
24. Gibson DN, Di Biase L, Mohanty P, et al. Stiff left atrial syndrome after catheter ablation for atrial fibrillation: clinical characterization, prevalence, and predictors. Heart Rhythm. 2011;8(9):1364-71. doi:10.1016/j.hrthm.2011.02.026.
25. Moon I, Lee SY, Lee E, et al. Extensive left atrial ablation was associated with exacerbation of left atrial stiffness and dyspnea. J Cardiovasc Electrophysiol. 2019;30(12):2782-9. doi:10.1111/jce.14241.
26. Witt C, Powell B, Holmes D, et al. Recurrent dyspnea following multiple ablations for atrial fibrillation explained by the "stiff left atrial syndrome". Catheter Cardiovasc Interv. 2013;82(5):E747-9. doi:10.1002/ccd.24556.
27. Wong GR, Lau DH, Baillie TJ, et al. Novel use of sildenafil in the management of pulmonary hypertension due to post-catheter ablation ‘stiff left atrial syndrome’. Int J Cardiol. 2015;181:55-6. doi:10.1016/j.ijcard.2014.12.012.
28. Chen S, Chun KRJ, Tohoku S, et al. Esophageal Endoscopy After Catheter Ablation of Atrial Fibrillation Using Ablation-Index Guided High-Power: Frankfurt AI-HP ESO-I. JACC Clin Electrophysiol. 2020;6(10):1253-61. doi:10.1016/j.jacep.2020.05.022.
29. Kaneshiro T, Kamioka M, Hijioka N, et al. Characteristics of Esophageal Injury in Ablation of Atrial Fibrillation Using a High-Power Short-Duration Setting. Circ Arrhythm Electrophysiol. 2020;13(10):e008602. doi:10.1161/CIRCEP.120.008602.
30. Müller J, Berkovitz A, Halbfass P, et al. Acute oesophageal safety of high-power short duration with 50 W for atrial fibrillation ablation. Europace. 2022;24(6):928-37. doi:10.1093/europace/euab329.
31. Schoene K, Arya A, Grashoff F, et al. Oesophageal Probe Evaluation in Radiofrequency Ablation of Atrial Fibrillation (OPERA): results from a prospective randomized trial. Europace. 2020;22(10):1487-94. doi:10.1093/europace/euaa209.
32. Tilz RR, Schmidt V, Pürerfellner H, et al. A worldwide survey on incidence, management, and prognosis of oesophageal fistula formation following atrial fibrillation catheter ablation: the POTTER-AF study. Eur Heart J. 2023;44(27):2458-69. doi:10.1093/eurheartj/ehad250.
33. Piccini JP, Braegelmann KM, Simma S, et al. Risk of atrioesophageal fistula with cryoballoon ablation of atrial fibrillation. Heart Rhythm O2. 2020;1(3):173-9. doi:10.1016/j.hroo.2020.05.007.
34. Andrade JG, Wells GA, Deyell MW, et al. EARLY-AF Investigators. Cryoablation or Drug Therapy for Initial Treatment of Atrial Fibrillation. N Engl J Med. 2021;384(4):305-15. doi:10.1056/NEJMoa2029980.
35. Mörtsell D, Arbelo E, Dagres N, et al. ESC-EHRA Atrial Fibrillation Ablation Long-Term Registry investigators. Cryoballoon vs. radiofrequency ablation for atrial fibrillation: a study of outcome and safety based on the ESC-EHRA atrial fibrillation ablation long-term registry and the Swedish catheter ablation registry. Europace. 2019;21(4):581-9. doi:10.1093/europace/euy239.
36. Packer DL, Kowal RC, Wheelan KR, et al. STOP AF Cryoablation Investigators. Cryoballoon ablation of pulmonary veins for paroxysmal atrial fibrillation: first results of the North American Arctic Front (STOP AF) pivotal trial. J Am Coll Cardiol. 2013;61(16):1713-23. doi:10.1016/j.jacc.2012.11.064.
37. Tokuda M, Yamashita S, Sato H, et al. Long-term course of phrenic nerve injury after cryoballoon ablation of atrial fibrillation. Sci Rep. 2021;11(1):6226. doi:10.1038/s41598-021-85618-3.
38. Heeger CH, Sohns C, Pott A, et al. Phrenic Nerve Injury During Cryoballoon-Based Pulmonary Vein Isolation: Results of the Worldwide YETI Registry. Circ Arrhythm Electrophysiol. 2022;15(1):e010516. doi:10.1161/CIRCEP.121.010516.
39. Mol D, Renskers L, Balt JC, et al. Netherlands Heart Registration Ablation Committee. Persistent phrenic nerve palsy after atrial fibrillation ablation: Follow-up data from The Netherlands Heart Registration. J Cardiovasc Electrophysiol. 2022;33(3):559-64. doi:10.1111/jce.15368.
40. Sacher F, Monahan KH, Thomas SP, et al. Phrenic nerve injury after atrial fibrillation catheter ablation: characterization and outcome in a multicenter study. J Am Coll Cardiol. 2006;47(12):2498-503. doi:10.1016/j.jacc.2006.02.050.
41. Miyazaki S, Hachiya H, Taniguchi H, et al. Prospective Evaluation of Bilateral Diaphragmatic Electromyograms During Cryoballoon Ablation of Atrial Fibrillation. J Cardiovasc Electrophysiol. 2015;26(6):622-8. doi:10.1111/jce.12671.
42. Marinelli A, Trachanas K, Corso M, et al. An alternative method for phrenic nerve monitoring during cryoballoon procedures. Heart Rhythm O2. 2025;6(6):739-44. doi:10.1016/j.hroo.2025.03.016.
43. Andrade JG, Khairy P, Guerra PG, et al. Efficacy and safety of cryoballoon ablation for atrial fibrillation: a systematic review of published studies. Heart Rhythm. 2011;8(9):1444-51. doi:10.1016/j.hrthm.2011.03.050.
44. Cleland JG, Daubert JC, Erdmann E, et al.; CARE-HF study Steering Committee and Investigators. The CARE-HF study (CArdiac REsynchronisation in Heart Failure study): rationale, design and end-points. Eur J Heart Fail. 2001;3(4):481-9. doi:10.1016/s1388-9842(01)00176-3.
45. Tsotsolis N, Tsirgogianni K, Kioumis I, et al. Pneumothorax as a complication of central venous catheter insertion. Ann Transl Med. 2015;3(3):40. doi:10.3978/j.issn.2305-5839.2015.02.11.
46. Makita T, Kuwahara T, Takahashi K, et al. Severe hemothorax complications during atrial fibrillation ablation: Lessons from two cases. HeartRhythm Case Rep. 2022;8(8):586-90. doi:10.1016/j.hrcr.2022.05.018.
47. Kusano K, Inoue K, Kanaoka K, et al. J‐AB registry investigators. The Japanese Catheter Ablation Registry (J-AB): Annual report in 2022. J Arrhythm. 2024;40(5):1053-8. doi:10.1002/joa3.13141.
48. Wu L, Narasimhan B, Ho KS, et al. Safety and complications of catheter ablation for atrial fibrillation: Predictors of complications from an updated analysis the National Inpatient Database. J Cardiovasc Electrophysiol. 2021;32(4):1024-34. doi:10.1111/jce.14979.
49. Zheng T, Kong Y, Wu L, et al. Silent cerebral lesions after catheter ablation for atrial fibrillation using cryoballoon, hotballoon, laserballoon and radiofrequency catheters: a Bayesian network meta-analysis. Front Cardiovasc Med. 2025;11:1510468. doi:10.3389/fcvm.2024.1510468.
50. Asbach S, Biermann J, Bode C, et al. Early Heparin Administration Reduces Risk for Left Atrial Thrombus Formation during Atrial Fibrillation Ablation Procedures. Cardiol Res Pract. 2011;2011:615087. doi:10.4061/2011/615087.
51. Briceno DF, Villablanca PA, Lupercio F, et al. Clinical Impact of Heparin Kinetics During Catheter Ablation of Atrial Fibrillation: Meta-Analysis and Meta-Regression. J Cardiovasc Electrophysiol. 2016;27(6):683-93. doi:10.1111/jce.12975.
52. Tyrak K, Batko J, Hołda J, et al. Association between the left-sided atrial septal pouch and the cryptogenic stroke — an updated systematic review and meta-analysis. Sci Rep. 2025;15(1):37432. doi:10.1038/s41598-025-21285-y.
53. Moser H, Go D, Lai E, et al. Left atrial septal pouch thrombus prior to catheter ablation for atrial fibrillation. JACC. 2023; 81. doi:10.1016/S0735-1097(23)04336-X.
54. Boga M, Suhai FI, Orbán G, et al. Incidence and predictors of stroke and silent cerebral embolism following very high-power short-duration atrial fibrillation ablation. Europace. 2023;25(11):euad327. doi:10.1093/europace/euad327.
55. Shah D, Dumonceau JM, Burri H, et al. Acute pyloric spasm and gastric hypomotility: an extracardiac adverse effect of percutaneous radiofrequency ablation for atrial fibrillation. J Am Coll Cardiol. 2005;46(2):327-30. doi:10.1016/j.jacc.2005.04.030.
56. Aksu T, Golcuk S, Guler TE, et al. Gastroparesis as a Complication of Atrial Fibrillation Ablation. Am J Cardiol. 2015;116(1):92-7. doi:10.1016/j.amjcard.2015.03.045.
57. Miyazaki S, Nakamura H, Taniguchi H, et al. Gastric hypomotility after second-generation cryoballoon ablation-Unrecognized silent nerve injury after cryoballoon ablation. Heart Rhythm. 2017;14(5):670-7. doi:10.1016/j.hrthm.2017.01.028.
58. Camilleri M, Atieh J. New Developments in Prokinetic Therapy for Gastric Motility Disorders. Front Pharmacol. 2021;12:711500. doi:10.3389/fphar.2021.711500.
59. Field J, Wasilewski M, Bhuta R, et al. Effect of Chronic Domperidone Use on QT Interval: A Large Single Center Study. J Clin Gastroenterol. 2019;53(9):648-52. doi:10.1097/MCG.0000000000001183.
60. Janssens J, Peeters TL, Vantrappen G, et al. Improvement of gastric emptying in diabetic gastroparesis by erythromycin. Preliminary studies. N Engl J Med. 1990;322(15):1028- 31. doi:10.1056/NEJM199004123221502.
61. Zheng T, Camilleri M. Management of Gastroparesis. Gastroenterol Hepatol (N Y). 2021;17(11):515-25.
62. Chéhirlian L, Koutbi L, Mancini J, et al. High incidence of phrenic nerve injury in patients undergoing pulsed field ablation for atrial fibrillation. Heart Rhythm. 2025;22(12):e1206 e1213. doi:10.1016/j.hrthm.2025.08.010.
63. Nies M, Koruth JS, Mlček M, et al. Is the esophagus spared during pulsed field ablation? Early histopathology and in vivo esophageal retraction. Heart Rhythm. 2025; S1547- 5271(25)02612-8. doi:10.1016/j.hrthm.2025.06.033.
64. Higuchi S, Im SI, Stillson C, et al. Gerstenfeld EP. Effect of Epicardial Pulsed Field Ablation Directly on Coronary Arteries. JACC Clin Electrophysiol. 2022;8(12):1486-96. doi:10.1016/j.jacep.2022.09.003.
65. Tam MTK, Chan JYS, Chan CP, et al. Effect of Pulsed-Field Ablation on Human Coronary Arteries: A Longitudinal Study With Intracoronary Imaging. JACC Clin Electrophysiol. 2025;11(7):1478-88. doi:10.1016/j.jacep.2025.03.014.
66. Cho MS, Lee SR, Black-Maier E, et al. Complications associated with pulsed field ablation vs radiofrequency catheter ablation of atrial fibrillation. Heart Rhythm. 2025;22(9):2194- 200. doi:10.1016/j.hrthm.2024.10.063.
67. Miyazaki S, Kobori A, Sasaki Y, et al. Real-World Safety Profile of Atrial Fibrillation Ablation Using a Second-Generation Cryoballoon in Japan: Insight From a Large Multicenter Observational Study. JACC Clin Electrophysiol. 2021;7(5):604-13. doi:10.1016/j.jacep.2020.11.016.
68. Nakamura T, Takami M, Fukuzawa K, et al. Incidence and Characteristics of Coronary Artery Spasms Related to Atrial Fibrillation Ablation Procedures — Large-Scale Multicenter Analysis. Circ J. 2021;85(3):264-71. doi:10.1253/circj.CJ-20-1096.
69. Ekanem E, Neuzil P, Reichlin T, et al. Safety of pulsed field ablation in more than 17,000 patients with atrial fibrillation in the MANIFEST 17K study. Nat Med. 2024;30(7):2020-9. doi:10.1038/s41591-024-03114-3.
70. Reddy VY, Petru J, Funasako M, et al. Coronary Arterial Spasm During Pulsed Field Ablation to Treat Atrial Fibrillation. Circulation. 2022;146(24):1808-19. doi:10.1161/CIRCULATIONAHA.122.061497.
71. Sowers AE, Lieber MR. Electropore diameters, lifetimes, numbers, and locations in individual erythrocyte ghosts. FEBS Lett. 1986;205(2):179-84. doi:10.1016/0014-5793(86)80893-6.
72. Peng W, Yue Y, Zhang Y, et al. Scheduled dosage regimen by irreversible electroporation of loaded erythrocytes for cancer treatment. APL Bioeng. 2023;7(4):046102. doi:10.1063/5.0174353.
73. Popa MA, Venier S, Menè R, et al. Characterization and Clinical Significance of Hemolysis After Pulsed Field Ablation for Atrial Fibrillation: Results of a Multicenter Analysis. Circ Arrhythm Electrophysiol. 2024;17(10):e012732. doi:10.1161/CIRCEP.124.012732.
74. Gupta A, Perera T, Ganesan A, et al. Complications of catheter ablation of atrial fibrillation: a systematic review. Circ Arrhythm Electrophysiol. 2013;6(6):1082-8. doi:10.1161/CIRCEP.113.000768.
75. Providência R, Adragão P, de Asmundis C, et al. Impact of Body Mass Index on the Outcomes of Catheter Ablation of Atrial Fibrillation: A European Observational Multicenter Study. J Am Heart Assoc. 2019;8(20):e012253. doi:10.1161/JAHA.119.012253.
76. Ekanem E, Reddy VY, Schmidt B, et al. MANIFEST-PF Cooperative. Multi-national survey on the methods, efficacy, and safety on the post-approval clinical use of pulsed field ablation (MANIFEST-PF). Europace. 2022;24(8):1256-66. doi:10.1093/europace/euac050. Erratum in: Europace. 2023;25(2):449. doi:10.1093/europace/euac250.
77. Schmidt B, Bordignon S, Neven K, et al. EUropean real-world outcomes with Pulsed field ablatiOn in patients with symptomatic atRIAl fibrillation: lessons from the multicentre EU-PORIA registry. Europace. 2023;25(7):euad185. doi:10.1093/europace/euad185.
78. Jäckel M, Kaier K, Steinfurt J, et al. In-hospital safety of cryoballoon and radiofrequency ablation in patients with atrial fibrillation-German nationwide analysis of more than 300,000 procedures. Heart Rhythm. 2025;22(12):3131-9. doi:10.1016/j.hrthm.2025.02.024.
79. Kattel S, Tan Z, Lin Z, et al. Procedural volume and outcomes with atrial fibrillation ablation: A report from the NCDR AFib Ablation Registry. Heart Rhythm. 2025;22(1):37-48. doi:10.1016/j.hrthm.2024.06.056.
Об авторах
С. В. НемцовРоссия
Немцов Сергей Викторович — врач — сердечно-сосудистый хирург отделения РХЛслНРС и ЭКС
ул. Аккуратова, д. 2, Санкт-Петербург, 197341
Д. С. Лебедев
Россия
Лебедев Дмитрий Сергеевич — г.н.с., руководитель научно-исследовательского отдела аритмологии, профессор кафедры сердечно-сосудистой хирургии, зав. образовательным центром "Академия аритмологии" института медицинского образования
ул. Аккуратова, д. 2, Санкт-Петербург, 197341
Рецензия
Для цитирования:
Немцов С.В., Лебедев Д.С. Осложнения катетерной аблации фибрилляции предсердий и способы их профилактики (обзор). Российский кардиологический журнал. 2025;30(4S):6728. https://doi.org/10.15829/1560-4071-2025-6728. EDN: RJZQCQ
For citation:
Nemtsov S.V., Lebedev D.S. Complications of catheter ablation for atrial fibrillation and their prevention: review. Russian Journal of Cardiology. 2025;30(4S):6728. (In Russ.) https://doi.org/10.15829/1560-4071-2025-6728. EDN: RJZQCQ
JATS XML


















































