Перейти к:
Сосудистые когнитивные расстройства у пациентов после острого инфаркта миокарда
https://doi.org/10.15829/1560-4071-2025-6087
EDN: MPFWGC
Аннотация
Пациенты с острым инфарктом миокарда (ОИМ) выделены российскими и зарубежными экспертами в группу риска развития умеренных сосудистых когнитивных расстройств (СКР) и сосудистой деменции. В результате различных патогенетических механизмов у пациентов с ОИМ развивается так называемый кардиоцеребральный синдром, вносящий весомый вклад в нарушение глобального когнитивного функционирования в данной группе больных. Влияние ОИМ на риск развития когнитивных расстройств и их прогрессирование является одним из ключевых звеньев на пути к улучшению прогноза и качества жизни у пациентов, перенесших ОИМ. Цель обзора: проанализировать частоту встречаемости умеренных СКР и сосудистой деменции у пациентов в ОИМ в остром и отдаленном периодах заболевания.
Ключевые слова
Для цитирования:
Петрова М.М., Лейман А.Р., Устюгов С.А., Шнайдер Н.А., Петров А.В. Сосудистые когнитивные расстройства у пациентов после острого инфаркта миокарда. Российский кардиологический журнал. 2025;30(6S):6087. https://doi.org/10.15829/1560-4071-2025-6087. EDN: MPFWGC
For citation:
Petrova M.M., Leiman A.R., Ustyugov S.A., Schneider N.A., Petrov A.V. Vascular cognitive impairment in patients after acute myocardial infarction. Russian Journal of Cardiology. 2025;30(6S):6087. (In Russ.) https://doi.org/10.15829/1560-4071-2025-6087. EDN: MPFWGC
Пациенты с острым инфарктом миокарда (ОИМ) выделены российскими и зарубежными экспертами в группу риска развития умеренных сосудистых когнитивных расстройств (СКР) и сосудистой деменции [1][2]. Известно, что умеренные СКР представляют собой стадию когнитивного снижения, выходящего за рамки нормального старения, но не соответствующего диагностическим критериям сосудистой деменции [3], но они приводят к 10-16% годовому приросту риска развития сосудистой деменции [4]. Принимая во внимание то, что для умеренных СКР и сосудистой деменции характерно прогрессирующее снижение глобального когнитивного функционирования, исполнительских функций и памяти, важно всестороннее изучение рассматриваемой проблемы в современной кардиологии и кардионеврологии [5-8]. Это может позволить разработать новые диагностические и терапевтические стратегии для уменьшения бремени сосудистой деменции у пациентов, перенесших ОИМ [9-15].
В последние годы в контексте рассматриваемой проблемы различными исследовательскими группами активно изучается частота встречаемости СКР и сосудистой деменции у пациентов, перенесших острый коронарный синдром (ОКС), включая ОИМ с подъемом сегмента ST и ОИМ без подъема сегмента ST, патофизиологическими субстратами которых являются окклюзия коронарной артерии и неокклюзирующий коронарный атеросклероз, соответственно [16-19]. Согласно четвертому универсальному определению Европейского кардиологического общества (2018) [20], принятому Российским кардиологическим обществом1, дефиниция "инфаркт миокарда" обозначает острое повреждение миокарда с клиническими доказательствами ишемии, а его клинико-лабораторными маркерами являются: повышение или снижение уровня сердечного тропонина (тропониновый тест) в сочетании хотя бы с одним из следующих маркеров: симптомы ишемии миокарда; вновь возникшие ишемические изменения на электрокардиограмме; появление патологического зубца Q на электрокардиограмме; выявление диагностики новых участков нежизнеспособного миокарда либо новых участков нарушения локальной сократимости предположительно ишемической этиологии (по данным лучевых методов диагностики); выявление тромба в коронарных артериях (по данным коронароангиографии и/или аутопсии) [20].
Одним из патогенетических механизмов, связывающих ОИМ с развитием СКР и их прогрессированием с последующей трансформацией в сосудистую деменцию, является снижение фракции выброса левого желудочка и артериальная гипотензия, которые приводят к хронической церебральной гипоперфузии у пациентов, перенесших ОИМ. В свою очередь, микрососудистая церебральная ишемия на фоне хронической церебральной гипоперфузии может инициировать каскад системного и локального воспалительного ответа и гиперпродукцию провоспалительных цитокинов, что приводит к дисфункции нейроваскулярных единиц, изменению их метаболизма с последующими микро- и макроструктурным изменениями, включая поражения белого вещества и атрофию серого вещества [21]. Однако ранее проведенные исследования продемонстрировали противоречивые результаты о частоте встречаемости и степени тяжести СКР в остром периоде ОИМ [10][22]. Исследования частоты встречаемости и темпов прогрессирования СКР в долгосрочной перспективе после перенесенного ОИМ пока одиночные и не всегда хорошо документированы. В таких исследованиях часто отсутствует повторная стандартизированная оценка когнитивных функций у пациентов с ишемической болезнью сердца (ИБС) до и после ОИМ, или в исследования СКР включались как пациенты с ОИМ, так и с другими ССЗ, прежде всего с артериальной гипертензией [23], фибрилляцией предсердий [24] и хронической сердечной недостаточностью [25]. Кроме того, недостаточно изучена взаимосвязь СКР у пациентов с ОИМ в остром и отдаленном периодах заболевания с расовой и этнической принадлежностью [26] и полом [27] пациентов, а также нуждается в дальнейших исследованиях роль повторного ОИМ на когнитивные функции у пациентов с ИБС.
Цель настоящего обзора — проанализировать частоту встречаемости умеренных СКР и сосудистой деменции у пациентов в ОИМ в остром и отдаленном периодах заболевания.
Методология исследования
Проведен поиск российских и зарубежных публикаций в русскоязычной и англоязычных базах данных: e-Library, PubMed, Scopus, ClinicalKeys, OxfordPress, Springer, Google Scholar и Google Search. Выбор библиографических баз данных был обусловлен характером исследовательского вопроса. Google Scholar и Google Search использовались в качестве дополнительных инструментов при предварительном поиске публикаций.
Критерии включения: 1) тип публикации — полнотекстовые статьи, включая оригинальные исследования, выполненные в различных странах мира, тематические и систематические обзоры, метаанализы, кокрейновские обзоры; 2) тип исследования — продольные (кросс-секционные) и поперечные (лонгитюдные) исследования взаимосвязи между ОИМ и СКР (или сосудистой деменцией); 3) язык публикации — русский, английский; 4) дата публикации — с 15 января 2018г до 15 января 2024г; 5) ключевые слова — острый инфаркт миокарда, когнитивные функции, когнитивное снижение, сосудистые когнитивные расстройства, сосудистая деменция.
Критерии исключения: 1) тип публикации — тезисы и материалы научных конференций, редакционные статьи, рецензии, обзоры книг, различные типы интервью; 2) постеры; 3) отсутствие доступа к полной версии статьи; 4) язык публикации — любой, кроме русского и английского; 5) дата публикации — до 15 января 2018г.
Следующая информация была извлечена из включенных исследований: 1) ссылка на исследование; 2) страна; 3) цель исследования; 4) характеристика выборки; 5) метод сбора данных (продолжительность исследования); 6) методы исследования когнитивных функций у пациентов, перенесших ОКС или ОИМ; 7) основные выводы.
Ни одно исследование не было исключено только на основании качества. Все исследования, соответствующие критериям включения, были включены в обзор независимо от их оценки качества.
Кроме того, в настоящий систематический обзор включались более ранние публикации, представленные во введении, а также в дискуссии для обеспечения возможности сравнения проанализированных нами результатов исследований СКР и сосудистой деменции у пациентов, перенесших ОКС и/или ОИМ, последних лет с более ранними исследованиями.
Блок-схема проведенного систематического обзора, выполненная с использованием руководства PRISMA2, представлена на рисунке 1.
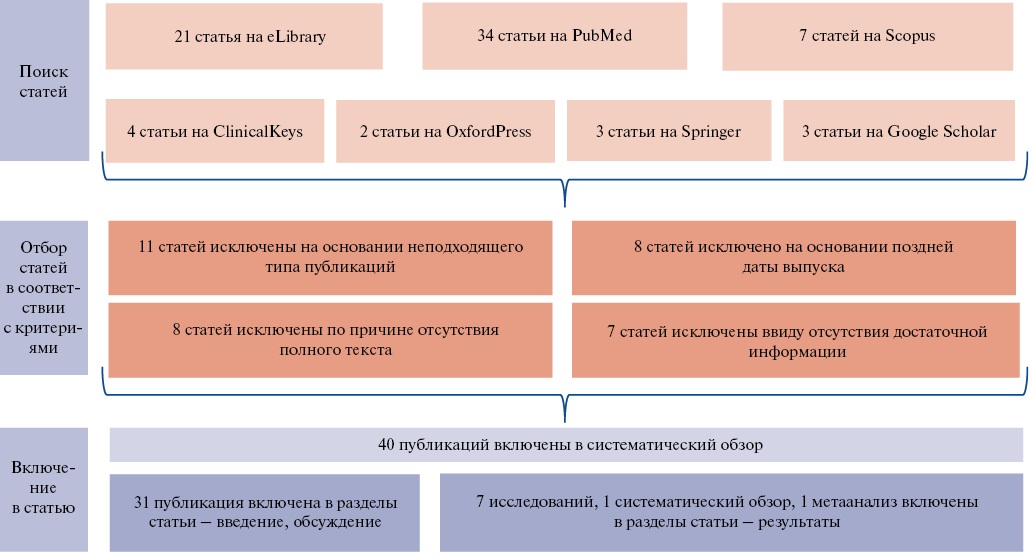
Рис. 1. Блок-схема систематического обзора.
Результаты
По данным когортного исследования Johansen MC, et al. (2023) [28], выполненного в США в период с июля 2021г по январь 2022г с участием 1033 пациентов, перенесших ОИМ, и анализа ранее проведенных 24 исследований в США в период с 1971 по 2019гг, с использованием модифицированных стандартов гармонизации СКР (Vascular Cognitive Impairment Harmonization Standards) было показано, что ОИМ не приводил к острому снижению глобальных когнитивных функций (-0,18 баллов; 95% доверительный интервал (ДИ): от -0,52 до 0,17 баллов), исполнительских функций (-0,17 баллов; 95% ДИ: от -0,53 до 0,18 баллов) и памяти (0,62 балла; 95% ДИ: от -0,07 до 1,31 балла). Однако авторы продемонстрировали, что в группе пациентов, перенесших ОИМ, в течение многих последующих лет отмечалось более быстрое снижение показателей глобальных когнитивных функций (-0,15 балла в год; 95% ДИ: от -0,21 до -0,10 балла в год), памяти (-0,13 балла в год; 95% ДИ: от -0,22 до -0,04 балла в год) и исполнительских функций (-0,14 балла в год; 95% ДИ: от -0,20 до -0,08 балла в год) по сравнению с таковыми показателями до ОИМ.
Альтернативные результаты получены в лонгитюдном исследовании здоровья и выхода на пенсию в Китае, проведенного Shang J, et al. (2024) [29] с участием 421 пациента (средний возраст -60,0±9,0 лет), перенесшего ОИМ. Авторы оценивали эпизодическую память, зрительно-пространственные способности, способность ориентироваться во времени, способность к расчету и вниманию. Были проанализированы исходные характеристики когнитивных функций у участников исследования с ОИМ и без него, в т. ч. в динамике: первый визит — в период с 2011 по 2012гг; второй визит — с интервалом в 2-3 года до 2018г. Исходные показатели когнитивных функций в группе пациентов с ОИМ статистически значимо не отличались от таковых у пациентов контрольной группы сопоставимого возраста без ОИМ. В этом исследовании оценивались "острые" СКР в течение первых дней от развития ОИМ, но авторами не найдено статистически значимого изменения глобального показателя когнитивных функций (-0,013 баллов в год; 95% ДИ: от -0,085 до 0,111 балла в год; p=0,792). Кроме того, оценивались "отдаленные" СКР в течение последующих 2-3 лет после ОИМ, при этом тренд когнитивного снижения у пациентов, перенесших ОИМ, статистически значимо не отличался от такового до ОИМ (-0,007 баллов в год; 95% ДИ: от -0,040 до 0,027 баллов в год; p=0,69).
Противоположные результаты получены в многоцентровом проспективном когортном исследовании, проведенном в Великобритании Gu SZ, et al. (2019) [30], которые оценивали когнитивный статус у пациентов, перенесших ОКС без подъема сегмента ST, с использованием Монреальской когнитивной шкалы (MoCA — Montreal Cognitive Assessment) у 271 пациента в возрасте старше 65 лет, в период с ноября 2012г по декабрь 2015г. Частота встречаемости СКР была высокой и достигала 48,0% (<26 баллов), из них: в 70,8% случаев выявлены легкие СКР; в 23,8% — умеренные СКР; в 5,4% — тяжелые СКР, которые соответствовали уровню сосудистой деменции. Кроме того, 211 из 271 пациентов, перенесших ОКС без подъема сегмента ST и инвазивные методы лечения (стентирование, пластика и др.), были протестированы повторно через 12 мес. Общий балл по шкале MoCA через 12 мес. по сравнению с исходным уровнем (в остром периоде ОКС без подъема сегмента ST) составил 24,7±3,7 vs 25,4±3,2 (-0,6±3,3 балла, р=0,007).
Sundbøll J, et al. (2018) [31] провели общенациональное популяционное когортное исследование в Дании с участием 314911 пациентов, перенесших ОИМ, из них были рандомизированы индивидуумы по году рождения (1980-2012гг). Данные о ранее уточненном диагнозе сосудистой деменции у стационарных и амбулаторных пациентов были получены из Датского национального реестра пациентов [32] и Датского центрального психиатрического исследовательского регистра [33]. Авторы оценивали риск развития сосудистой деменции через 12 мес. после перенесенного ОИМ. Контрольную группу составили 1573193 человека сопоставимого пола и возраста. В результате этого исследования продемонстрировано, что перенесенный ОИМ статистически значимо повышает риск развития сосудистой деменции (отношение шансов (ОШ) 1,35; 95% ДИ: 1,28-1,43). При этом этот риск был значимо выше у пациентов, перенесших инсульт после ОИМ (ОШ 4,48; 95% ДИ: 3,29-6,12). Такая коморбидность кардиоваскулярной и цереброваскулярной патологии (синдром перекреста или синдром взаимного отягощения) в клинической практике кардиолога и невролога является нередким, т. к. известным фактором развития ОИМ и ишемического инсульта является атеросклеротическое поражение сосудов.
Альтернативные результаты получены в польском проспективном многоцентровом исследовании Kasprzak D, et al. (2023) [34], которые обследовали 468 пациентов, перенесших ИМпST и ИМбпST, у которых когнитивные функции тестировались в остром и отдаленном (через 6 мес.) периодах заболевания с использованием краткой шкалы психического статуса (MMSE — Mini-Mental State Examination), шкалы депрессии Бека (BDI — Beck Depression Inventory), модифицированной шкалы открытой агрессии (OAS-M — Overt Aggression Scale Modified), Афинской шкалы бессонницы (AIS — Athens insomnia scale), Шкалы сонливости Эпворта (ESS — Epworth Sleepiness Scale) и Индекса тяжести бессонницы (ISI—Insomnia Severity Index). СКР были диагностированы в остром периоде ОИМ в 37% случаев при использовании шкалы MMSE. Однако через 6 мес. отмечено значительное улучшение когнитивных функций, при этом СКР при тестировании пациентов в динамике (через 6 мес.) были идентифицированы в 25% случаев по шкале MMSE (-12%). В то же время в 8,8% случаев СКР впервые были выявлены через 6 мес. после ОИМ у пациентов, у которых в остром периоде заболевания были нормативные возрастные показатели по данным MMSE. К сожалению, в этом исследовании авторы не анализировали биомаркеры межиндивидуальной вариабельности положительной и отрицательной динамики когнитивного статуса у наблюдаемых пациентов в отдаленном периоде ОИМ.
В британском продольном когортном исследовании Xie W, et al. (2019) [22] приняли участие 7888 пациентов (средний возраст 62,1±10,2 года), которым в течение всего периода исследования (12 лет) был диагностирован ОИМ и/или стенокардия. Общая выборка пациентов была обследована трижды: 1 волна — в период 2002-2003гг; 2 волна — 2004-2005гг; 3 волна — 2016-2017гг. Для оценки когнитивных функций авторы использовали тест на немедленное и отсроченное запоминание 10 не связанных между собой слов, тест на беглость семантической речи и оценку ориентации во времени (текущая дата, день недели, месяц, год). В результате показано, что ИБС (ОИМ и/или стенокардия) ускоряли когнитивное снижение в течение периода наблюдения за пациентами в основной группе по сравнению с группой контроля (пациенты без ИБС). При этом перенесенный ОИМ статистически значимо повышал риск и темпы прогрессирования СКР, включая глобальное когнитивное снижение, вербальную память и беглость семантической речи; в то время как стенокардия статистически значимо повышала только риск прогрессирующего нарушения ориентации во времени.
В австралийском исследовании Gallagher R, et al. (2021) [35] с участием 40 пациентов, перенесших ОКС и чрескожное коронарное вмешательство, авторы оценивали когнитивные функции в начале, в конце и через 3 мес. по завершении курса кардиологической реабилитации с использованием следующих тестов: способность к вербальному обучению (Rey Auditory Verbal Learning Test — RAVLT); скорость обработки информации (Trail Making Test Part A — TMT-A); исполнительские функции (Trail Making Test, part B — TMT-B); зрительное внимание (Cogstate detection test — Cogstate DET); оценка тревоги и депрессии (Hospital Anxiety and Depression Scale — HADS). Курс кардиореабилитации начинался через 2-3 нед. после выписки из стационара и продолжался 6 нед., включая индивидуально подобранные контролируемые структурированные аэробные и силовые тренировки по 1 часу 1-2 раза в нед. и домашнюю 30-минутную программу физических упражнений не менее 5 дней в нед. В начале курса кардиореабилитации у 62,5% пациентов диагностированы умеренные СКР по одному из вышеперечисленных когнитивных тестов и у 22,5% — по нескольким когнитивным тестам. В конце курса кардиореабилитации умеренные СКР по одному из когнитивных тестов были диагностированы у 52,5% пациентов (-10,0%, р=0,002) и у 15,0% пациентов по нескольким когнитивным тестам (-7,5%, р=0,021). При исследовании когнитивных функций в динамике через 3 мес. по завершении курса кардиореабилитации у пациентов, перенесших и чрескожное коронарное вмешательство, умеренные СКР по одному из тестов были идентифицированы только в 32,5% случаев (-20,0%, р=0,019), а по нескольким тестам — в 7,0% (-8,0%, р=0,05). Наиболее часто у наблюдаемых пациентов нарушались такие когнитивные функции, как вербальное обучение (52,5%) и скорость обработки информации (25,6%).
В систематическом обзоре Zhao E, et al. (2019) [36] проведена оценка частоты встречаемости СКР у пациентов, перенесших ОКС, по результатам 9 исследований. Общий объем выборки составил 6457 участников (объем выборок варьировал от 53 до 2174, средний возраст пациентов — от 51,3 до 77,4 лет). Частота развития СКР после перенесенного ОКС варьировала в очень широком диапазоне — от 9% до 85%. Это может быть объяснено вариабельным объемом выборок, разными скрининговыми инструментами для оценки когнитивных функций, вариабельной продолжительностью исследований и временных точек когнитивного скрининга.
В метаанализе Liang X, et al. (2021) [9], который включал 28 исследований, изучающих взаимосвязь между ИБС и риском развития СКР и сосудистой деменции, убедительно продемонстрировано, что ИБС повышает риск развития когнитивных расстройств любой этиологии (ОШ 1,27, 95% ДИ: 1,18-1,36, I²=82,8%, p<0,001), включая СКР (ОШ 1,34, 95% ДИ: 1,28-1,39, I²=36,1%, p=0,196). Кроме того, показано, что перенесенный ОИМ повышает риск развития когнитивных расстройств любой этиологии (ОШ 1,49, 95% ДИ: 1,20-1,84, I²=76,0%, p<0,001), хотя статистически значимой связи между перенесенным ОИМ и риском СКР (сосудистой деменции) авторами не найдено (тест Бегга: p=0,34; тест Эггера: p=0,519).
Обсуждение
Проведенный нами обзор исследований последних лет (табл. 1), посвященных взаимосвязи ОКС и его исходов (ОИМ, включая ОИМ с подъемом сегмента ST и ОИМ без подъема сегмента ST), свидетельствует о том, что единого мнения о взаимосвязи между ОКС/ОИМ и риском развития умеренных СКР и сосудистой деменции пока нет, поскольку опубликованные ранее результаты оригинальных исследований, проведенных в различных странах мира, а также систематические обзоры и метаанализы демонстрируют противоречивые результаты. Тем не менее в большом числе исследований найдена статистически значимая связь между перенесенным ОКС или ОИМ с развитием и темпами прогрессирования умеренных СКР и сосудистой деменции. Однако высказаться о роли этноса и расы, а также возраста пациентов на риск развития СКР после перенесенного ОИМ пока не представляется возможным, поскольку необходимо проведение однородных по дизайну доклинических [37] и клинических исследований, включая: объем выборок; возраст и пол пациентов; когнитивные тесты; продолжительность исследования и временные точки когнитивного тестирования.
Таблица 1
Краткая характеристика исследований взаимосвязи между ОИМ и СКР
|
Автор, год |
Страна (размер выборки) |
Методы оценки когнитивных функций |
Основные результаты |
|
Johansen MC, et al. (2023) [28] |
США (1033 пациентов, перенесших ОИМ) |
Модифицированные стандарты гармонизации СКР (Vascular Cognitive Impairment Harmonization Standards) |
ОИМ не приводил к острому снижению когнитивных функций |
|
Shang J, et al. (2024) [29] |
Китай (421 пациент, перенесший ОИМ) |
Тест для оценки эпизодической памяти Тест для оценки зрительно-пространственных способностей Тест для оценки способности ориентироваться во времени Тест для оценки способности к расчету и вниманию |
ОИМ не приводил к острому снижению когнитивных функций |
|
Gu SZ, et al. (2019) [30] |
Великобритания (271 пациент, перенесший ОКС без подъема сегмента ST) |
Монреальская когнитивная шкала (MoCA) |
ОКС без подъема сегмента ST приводил к снижению когнитивных функций на разном уровне |
|
Sundbøll J, et al. (2018) [31] |
Дания (314911 пациентов, перенесших ОИМ) |
Данные об уточненном диагнозе сосудистой деменции у стационарных и амбулаторных пациентов получены из Датского национального реестра пациентов и Датского центрального психиатрического исследовательского регистра |
ОИМ повышал риск сосудистой деменции |
|
Kasprzak D, et al. (2023) [34] |
Польша (468 пациентов, перенесших ИМпST и ИМбпST) |
Краткая шкала психического статуса (MMSE), шкала депрессии Бека (BDS) Модифицированная шкала открытой агрессии (OAS-M) Афинская шкалы бессонницы (AIS) Эпвортовская шкала сонливости (ESS) Индекс тяжести бессонницы (ISI) |
ОИМ повышал риск развития СКР |
|
Xie W, et al. (2019) [22] |
Великобритания (7888 пациентов, которым был диагностирован ОИМ и/или стенокардия) |
Тест на немедленное и отсроченное запоминание 10-ти не связанных между собой слов Тест на беглость семантической речи Тест на оценку ориентации во времени (текущая дата, день недели, месяц, год) |
ОИМ повышал риск развития и темпы прогрессирования СКР |
|
Gallagher R, et al. (2021) [35] |
Австралия (40 пациентов, перенесших ОКС и чрескожное коронарное вмешательство) |
Тест для оценки способности к вербальному обучению (RAVLT) Тест для оценки скорости обработки информации (TMT-A) Тест для оценки исполнительских функций (TMT-B) Тест для оценки зрительного внимания (Cogstate DET) Госпитальная шкала тревоги и депрессии (HADS). |
ОКС повышал риск СКР. Кардиореабилитация приводит к улучшению когнитивных функций |
Сокращения: ИМпST — острый инфаркт миокарда с подъемом сегмента ST, ИМбпST — острый инфаркт миокарда без подъема сегмента ST, ОИМ — острый инфаркт миокарда, ОКС — острый коронарный синдром, СКР — сосудистые когнитивные расстройства.
Почему частота развития и скорость снижения когнитивных функций у пациентов, перенесших ОКС/ОИМ, варьирует в таком широком диапазоне? На эти показатели могут влиять как внешние факторы (в частности, дизайн и продолжительность исследования), так и ключевые механизмы патофизиологии СКР. Хотя инсульт и ОИМ, в основном, являются результатом атеросклероза и фибрилляции предсердий, когнитивные паттерны в остром и отдаленном периодах этих заболеваний различны. Это позволяет высказать гипотезу о том, что когнитивный дефицит до ОКС/ОИМ может быть обусловлен не только сосудистыми, но и не сосудистыми факторами риска (например, курением, ожирением, низкой физической активностью, изменением гормонального статуса, сахарным диабетом [38]), а также генетической предрасположенностью. Эти факторы могут оказывать аддитивный (взаимоотягощающий) эффект на когнитивное функционирование у рассматриваемой категории пациентов. Однако модифицируемые факторы риска СКР и сосудистой деменции у пациентов, перенесших ОКС/ОИМ, могут изменяться во времени и, таким образом, их трудно скорректировать, если рассматривать только базовую временную точку (острый период ОКС или его неблагоприятного исхода — ОИМ). Если наша гипотеза верна, то важен поиск чувствительных и специфичных генетических и негенетических биомаркеров, ассоциированных с высоким риском развития и быстрым темпом прогрессирования СКР и сосудистой деменции в отдаленный период после перенесенного ОКС/ОИМ. Это представляется очень важным направлением будущих исследований, поскольку позволит персонализировано оценить индивидуальный риск развития СКР у конкретного пациента и не упустить временного терапевтического окна сосудистой деменции, т. е. замедлить темпы снижения глобальных когнитивных функций, исполнительских функций, вербальной и семантической памяти, ориентации во времени у пациентов кардиологического профиля [39].
Ограничения исследования. Ограниченное количество исследований, включенных в наш обзор, ограничили нашу способность ответить на исследовательские вопросы, касающиеся механизмов, посредством которых изменяется негативный эффект ОКС/ОИМ на глобальное когнитивное функционирование у людей в остром и отдаленном периодах заболевания, а также вопросы о том, влияют ли контекстуальные факторы, такие как географический регион, пол, этнос/раса, продолжительность пребывания в стационаре и продолжительность кардиореабилитации, а также продолжительность исследования, на промежуточные и конечные результаты (частоту и тяжесть СКР в остром и отдаленном периодах после перенесенного ОИМ).
Тем не менее в ответ на эти вопросы нам удалось привести некоторые предварительные данные, которые могут послужить основой для дальнейших исследований в этой области. Некоторые вероятные важные факторы, влияющие на эффективность ранней диагностики СКР и оценку риска развития сосудистой деменции у пациентов, перенесших ОКС или ОИМ, включают использование валидных инструментов (диагностических шкал и вопросников) для специалистов (кардиологов, неврологов, психиатров), участвующих в процессе мониторинга нарушений когнитивных функций у пациентов с рассматриваемой сердечно-сосудистой патологией, и ранее существовавшие убеждения относительно способности кардиологов участвовать в прогнозировании, диагностике и лечении СКР в остром и отдаленном периодах после перенесенного ОИМ.
Заключение
Ранний скрининг умеренных СКР и динамическое наблюдение за их прогрессированием у пациентов, перенесших ОКС и его неблагоприятный исход — ОИМ, могут помочь кардиологу идентифицировать пациентов группы высокого риска сосудистой деменции. Это позволит разработать новые персонализированные подходы к диагностике, диспансерному наблюдению, немедикаментозной и медикаментозной кардиореабилитации и нейрореабилитации. Пациенты группы высокого риска, включая индивидуумов с быстрым темпом прогрессирования СКР и сосудистой деменции после перенесенного ОКС/ОИМ, вероятно, нуждаются не только в кардиореабилитации, но и в более агрессивной фармакотерапии с целью нейропротекции для сохранения их качества жизни, функциональных резервов сердечно-сосудистой и центральной нервной систем, а также для достижения экономии прямых и непрямых расходов на здравоохранение.
Отношения и деятельность: все авторы заявляют об отсутствии потенциального конфликта интересов, требующего раскрытия в данной статье.
1. Рубрикатор клинических рекомендаций. Клинические рекомендации — Острый инфаркт миокарда с подъемом сегмента ST электрокардиограммы: https://cr.minzdrav.gov.ru/schema/157_4.
2. Prisma3D: https://prisma3d.net/.
Список литературы
1. Боголепова А. Н., Васенина Е. Е., Гомзякова Н. А. и др. Клинические рекомендации "Когнитивные расстройства у пациентов пожилого и старческого возраста". Журнал неврологии и психиатрии им. С. С. Корсакова. 2021;121(10-3):6-137. doi:10.17116/jnevro20211211036.
2. Яхно Н. Н., Преображенская И. С., Захаров В. В. и др. Распространенность когнитивных нарушений при неврологических заболеваниях (анализ работы специализированного амбулаторного приема). Неврология, нейропсихиатрия, психосоматика. 2012;2:30-5.
3. Дамулин И. В., Струценко А. А. Умеренные когнитивные расстройства сосудистого генеза. Трудный пациент. 2018;16(10):28-31. doi:10.24411/2074-1995-2018-10017.
4. Tsoi KKF, Chan JYC, Hirai HW, et al. Recall tests are effective to detect mild cognitive impairment: A systematic review and meta-analysis of 108 diagnostic studies. J Am Med Dir Assoc. 2017;18(9):807.e17-807.e29. doi:10.1016/j.jamda.2017.05.016.
5. Алиев Д. Ф. Социальный феномен деменции: вызовы современного общества. Социальная политика и социология. 2021;20(4):36-43. doi:10.17922/2071-3665-2021-20-4-36-43.
6. Wimo A, Guerchet M, Ali GC, et al. The worldwide costs of dementia 2015 and comparisons with 2010. Alzheimers Dement. 2017;13(1):1-7. doi:10.1016/j.jalz.2016.07.150.
7. Остроумова Т. М., Парфенов В. А., Остроумова О. Д. Когнитивные нарушения у пациентов с артериальной гипертензией: взаимосвязь с уровнем и суточным профилем артериального давления и патогенетические механизмы. Рациональная фармакотерапия в кардиологии. 2019;15(2):258-64. doi:10.20996/1819-6446-2019-15-2-258-264.
8. Levine DA, Gross AL, Briceño EM, et al. Association between blood pressure and later-life cognition among Black and White individuals. JAMA Neurol. 2020;77(7):810-9. doi:10.1001/jamaneurol.2020.0568.
9. Liang X, Huang Y, Han X. Associations between coronary heart disease and risk of cognitive impairment: A meta-analysis. Brain Behav. 2021;11(5):e02108. doi:10.1002/brb3.2108.
10. Wolters FJ, Segufa RA, Darweesh SKL, et al. Coronary heart disease, heart failure, and the risk of dementia: A systematic review and meta-analysis. Alzheimers Dement. 2018; 14(11):1493-504. doi:10.1016/j.jalz.2018.01.007.
11. Vishwanath S, Qaderi V, Steves CJ, et al. Cognitive decline and risk of dementia in individuals with heart failure: A systematic review and meta-analysis. J Card Fail. 2022; 28(8):1337-48. doi:10.1016/j.cardfail.2021.12.014.
12. Heshmatollah A, Dommershuijsen LJ, Fani L, et al. Long-term trajectories of decline in cognition and daily functioning before and after stroke. J Neurol Neurosurg Psychiatry. 2021;92(11):1158-63. doi:10.1136/jnnp-2021-326043.
13. Поспелова М. Л., Алексеева Т. М., Рыжкова Д. В. и др. Состояние когнитивных функций и перфузии головного мозга при хронической ишемии мозга на фоне асимптомного каротидного атеросклероза. Современные проблемы науки и образования. 2020;6:182. doi:10.17513/spno.30446.
14. Яковлева О. В., Ляшенко Е. А. Нарушение социальных когнитивных функций при различных нейродегенеративных заболеваниях. Colloquium-Journal. 2020;1-3(53):71-5.
15. Костенко Е. В., Энеева М. А., Петрова Л. В. и др. Когнитивные нарушения и нейропсихиатрические последствия, связанные с COVID-19. Доктор.Ру. 2021;20(5):6-12. doi:10.31550/1727-2378-2021-20-5-6-12.
16. Стогний Н. Ю., Цирятьева С. Б., Крашенинин Д. В. и др. Исторические аспекты учения об остром коронарном синдроме. Медицинская наука и образование Урала. 2020;21(3):140-2. doi:10.36361/1814-8999-2020-21-3-140-142.
17. Reed GW, Menon V. Reducing the incidence and mortality from myocardial infarction. Lancet Public Health. 2022;7(3):e202-e203. doi:10.1016/S2468-2667(22)00027-5.
18. Гордеев И. А., Куторова Е. Э., Акимова Н. С. Инфаркт миокарда как предиктор когнитивных нарушений у пациентов сердечно-сосудистого профиля: обзор литературы. Кардиология в Беларуси. 2023;3:376-81. doi:10.34883/PI.2023.15.3.009.
19. Thong EHE, Quek EJW, Loo JH, et al. Acute myocardial infarction and risk of cognitive impairment and dementia: A review. Biology (Basel). 2023;12(8):1154. doi:10.3390/biology12081154.
20. Thygesen K, Alpert JS, Jaffe AS, et al. Fourth Universal Definition of Myocardial Infarction (2018). Circulation. 2018;138(20):e618-e651. doi:10.1161/CIR.0000000000000617.
21. Jinawong K, Apaijai N, Chattipakorn N, et al. Cognitive impairment in myocardial infarction and heart failure. Acta Physiol (Oxf). 2021;232(1):e13642. doi:10.1111/apha.13642.
22. Xie W, Zheng F, Yan L, Zhong B. Cognitive Decline Before and After Incident Coronary Events. J Am Coll Cardiol. 2019;73(24):3041-50. doi:10.1016/j.jacc.2019.04.019.
23. Остроумова Т. М., Захаров В. В. Когнитивные нарушения у пациентов среднего возраста, страдающих артериальной гипертензией. Эффективная фармакотерапия. 2020; 16(23):6-12. doi:10.33978/2307-3586-2020-16-23-6-12.
24. Парфенов В. А. Когнитивные нарушения у пациентов с фибрилляцией предсердий. Consilium Medicum. 2023;25(2):81-5. doi:10.26442/20751753.2023.2.202220.
25. Аксенова Ю. О., Осмоловская Ю. Ф., Петрухина А. А. и др. Когнитивные нарушения при хронической сердечной недостаточности. Как влияют новые терапевтические возможности лечения хронической сердечной недостаточности на когнитивные функции? Евразийский кардиологический журнал. 2024;1(46):100-6. doi:10.38109/2225-1685-2024-1-100-106.
26. Kornblith E, Bahorik A, Boscardin WJ, et al. Association of race and ethnicity with incidence of dementia among older adults. JAMA. 2022;327(15):1488-95. doi:10.1001/jama.2022.3550.
27. McCarrey AC, An Y, Kitner-Triolo MH, et al. Sex differences in cognitive trajectories in clinically normal older adults. Psychol Aging. 2016;31(2):166-75. doi:10.1037/pag0000070.
28. Johansen MC, Ye W, Gross A, et al. Association Between Acute Myocardial Infarction and Cognition. JAMA Neurol. 2023;80(7):723-31. doi:10.1001/jamaneurol.2023.1331.
29. Shang J, Dong J, Zhu S, et al. Trends in cognitive function before and after myocardial infarction: findings from the China Health and Retirement Longitudinal Study. Front Aging Neurosci. 2024;16:1283997. doi:10.3389/fnagi.2024.1283997.
30. Gu SZ, Beska B, Chan D, et al. Cognitive decline in older patients with non-ST elevation acute coronary syndrome. J Am Heart Assoc. 2019;8(4):e011218. doi:10.1161/JAHA.118.011218.
31. Sundbøll J, Horváth-Puhó E, Adelborg K, et al. Henderson VW, Sørensen HT. Higher risk of vascular dementia in myocardial infarction survivors. Circulation. 2018;137(6):567-77. doi:10.1161/CIRCULATIONAHA.117.029127.
32. Schmidt M, Schmidt SA, Sandegaard JL, et al. The Danish National Patient Registry: a review of content, data quality, and research potential. Clin Epidemiol. 2015;7:449-90. doi:10.2147/CLEP.S91125.
33. Mors O, Perto GP, Mortensen PB. The Danish Psychiatric Central Research Register. Scand J Public Health. 2011;39(suppl):54-7. doi:10.1177/1403494810395825.
34. Kasprzak D, Kaczmarek-Majer K, Rzeźniczak J, et al. Cognitive Impairment in Cardiovascular Patients after Myocardial Infarction: Prospective Clinical Study. J Clin Med. 2023;12(15):4954. doi:10.3390/jcm12154954.
35. Gallagher R, Woolaston A, Tofler G, et al. Cognitive impairment and psychological state in acute coronary syndrome patients: A prospective descriptive study at cardiac rehabilitation entry, completion and follow-up. Eur J Cardiovasc Nurs. 2021;20(1):56-63. doi:10.1177/1474515120933105.
36. Zhao E, Lowres N, Woolaston A, et al. Prevalence and patterns of cognitive impairment in acute coronary syndrome patients: A systematic review. Eur J Prev Cardiol. 2020; 27(3):284-93. doi:10.1177/2047487319878945.
37. Petrov AV, Evsyukov AA, Petrova MM, et al. Limitations of the use of animal models of acute myocardial infarction for experimental studies of vascular cognitive dysfunction: Brief review. Personalized Psychiatry and Neurology. 2024;4(2):25-31. doi:10.52667/2712-9179-2024-4-2-25-31.
38. Гацких И. В., Окладникова Е. В., Шалда Т. П. и др. Связь тревожно-депрессивных расстройств с когнитивными нарушениями у пациентов с сахарным диабетом. Сибирское медицинское обозрение. 2018;2:94-9.
39. Frankish H, Horton R. Prevention and management of dementia: a priority for public health. Lancet. 2017;390:2614-5. doi:10.1016/S0140-6736(17)31756-7.
Об авторах
М. М. ПетроваРоссия
Марина Михайловна Петрова — д. м. н., профессор, зав. кафедрой.
Красноярск
Конфликт интересов:
все авторы заявляют об отсутствии потенциального конфликта интересов, требующего раскрытия в данной статье
А. Р. Лейман
Россия
Алена Руслановна Лейман — аспирант, врач-кардиолог.
Красноярск
Конфликт интересов:
все авторы заявляют об отсутствии потенциального конфликта интересов, требующего раскрытия в данной статье
С. А. Устюгов
Россия
Сергей Александрович Устюгов — к. м. н., доцент; зав. кардиологическим отделением № 3.
Красноярск
Конфликт интересов:
все авторы заявляют об отсутствии потенциального конфликта интересов, требующего раскрытия в данной статье
Н. А. Шнайдер
Россия
Наталья Алексеевна Шнайдер — д. м. н., профессор, в. н. с., зам. руководителя Института персонализированной психиатрии и неврологии.
Красноярск, Санкт-Петербург
Конфликт интересов:
все авторы заявляют об отсутствии потенциального конфликта интересов, требующего раскрытия в данной статье
А. В. Петров
Россия
Артем Владимирович Петров — студент.
Красноярск
Конфликт интересов:
все авторы заявляют об отсутствии потенциального конфликта интересов, требующего раскрытия в данной статье
Дополнительные файлы
- Сосудистая деменция и сосудистые когнитивные расстройства (СКР) являются междисциплинарной проблемой здравоохранения, а ее всестороннее изучение может позволить разработать новые диагностические и терапевтические стратегии для уменьшения бремени сосудистой деменции для семей и общества.
- Единого мнения о взаимосвязи между острым инфарктом миокарда и риском развития умеренных СКР и сосудистой деменции пока нет.
- На основании представленных исследований выявлена статистически значимая связь между перенесенным инфарктом миокарда с развитием и темпами прогрессирования умеренных СКР и сосудистой деменции.
Рецензия
Для цитирования:
Петрова М.М., Лейман А.Р., Устюгов С.А., Шнайдер Н.А., Петров А.В. Сосудистые когнитивные расстройства у пациентов после острого инфаркта миокарда. Российский кардиологический журнал. 2025;30(6S):6087. https://doi.org/10.15829/1560-4071-2025-6087. EDN: MPFWGC
For citation:
Petrova M.M., Leiman A.R., Ustyugov S.A., Schneider N.A., Petrov A.V. Vascular cognitive impairment in patients after acute myocardial infarction. Russian Journal of Cardiology. 2025;30(6S):6087. (In Russ.) https://doi.org/10.15829/1560-4071-2025-6087. EDN: MPFWGC
JATS XML

















































