Перейти к:
Тяжелый инфекционный эндокардит у пациента с обструктивной гипертрофической кардиомиопатией: 12 лет после сочетанной операции. Клинический случай
https://doi.org/10.15829/1560-4071-2024-6076
EDN: LVUBIY
Аннотация
Краткое описание. У пациента 40 лет с обструктивной гипертрофической кардиомиопатией (ГКМП) после выполнения каротидной эндартерэктомии появились эпизоды лихорадки до 39,0° С с ознобами. Было диагностировано наличие инфекционного эндокардита митрального и аортального клапана, вызванного Enterococcus faecium. Антибактериальная терапия продолжалась на протяжении 3 мес. В результате удалось подавить инфекционновоспалительный процесс, однако тяжелая недостаточность митрального и аортального клапана требовала хирургического лечения.
В ходе операции пациенту было выполнено протезирование двух пораженных клапанов, а также проведена расширенная миоэктомия и имплантирован кардиовертер-дефибриллятор с целью профилактики внезапной сердечной смерти. Спустя 12 лет после хирургического лечения инфекционного эндокардита и ГКМП состояние пациента стабильное.
Дискуссия. Пациенты с ГКМП имеют повышенный риск развития инфекционного эндокардита, однако при своевременной диагностике и активном лечении эндокардита возможен хороший отдаленный прогноз. В настоящем клиническом случае крайне важную роль сыграла сочетанная операция.
Ключевые слова
Для цитирования:
Лутохина Ю.А., Осадчая В.А., Морозова Н.В., Чичкова Н.В., Ганиева Н.А., Пигалицына М.А., Дземешкевич С.Л. Тяжелый инфекционный эндокардит у пациента с обструктивной гипертрофической кардиомиопатией: 12 лет после сочетанной операции. Клинический случай. Российский кардиологический журнал. 2024;29(10S):6076. https://doi.org/10.15829/1560-4071-2024-6076. EDN: LVUBIY
For citation:
Lutokhina Yu.A., Osadchaya V.A., Morozova N.V., Chichkova N.V., Ganieva N.A., Pigalitsyna M.A., Dzemeshkevich S.L. Severe infective endocarditis in a patient with hypertrophic obstructive cardiomyopathy: 12 years after combined surgery. A case report. Russian Journal of Cardiology. 2024;29(10S):6076. (In Russ.) https://doi.org/10.15829/1560-4071-2024-6076. EDN: LVUBIY
Введение
Гипертрофическая кардиомиопатия (ГКМП) — это генетически детерминированное заболевание миокарда, характеризующееся гипертрофией левого (ЛЖ) и/или правого желудочка >1,5 cм, преимущественно асимметричного характера за счет утолщения межжелудочковой перегородки (МЖП), которая не является следствием гемодинамической перегрузки давлением при отсутствии иного сердечного или системного заболевания, связанного с гипертрофией ЛЖ [1]. ГКМП является самой распространенной из генетически детерминированных кардиомиопатий. Ее частота среди взрослых достигает 0,2%, хотя фактически может быть и выше за счет бессимптомных пациентов, которые не обращаются за медицинской помощью [2]. Кардиологами активно обсуждается тот факт, что генетически измененный миокард при ГКМП является благоприятной мишенью для присоединения вирусных инфекций и миокардита [3]. Однако не менее важным является понимание того, что изменение внутрисердечной гемодинамики при ГКМП может приводить к микроповреждению эндотелия, что делает эту группу пациентов подверженной развитию инфекционного эндокардита (ИЭ) [4].
Ниже представлен клинический случай тяжелого ИЭ у пациента с ГКМП с успешным хирургическим лечением, в ходе которого было не только выполнено протезирование двух пораженных клапанов, но и проведена расширенная миоэктомия, а также имплантирован кардиовертер-дефибриллятор (ИКД).
Клинический случай
2.1. Информация о пациенте
Пациент 40 лет в декабре 2011г поступил в Факультетскую терапевтическую клинику им. В. Н. Виноградова для установления причины лихорадки неясного генеза.
При поступлении предъявлял жалобы на эпизоды повышения температуры тела по вечерам до 37,7 С, что сопровождалось недомоганием и болью в голеностопных суставах, одышку и тяжесть за грудиной при подъеме на 2 этаж и ходьбе быстрым шагом на расстояние до 500 м.
Анамнез заболевания (рис. 1). С 35 лет стал отмечать подъемы артериального давления (АД) до 160/90 мм рт.ст., в 36 лет при эхокардиографии (ЭхоКГ) стало известно о наличии обструктивной ГКМП (градиент давления в выносящем тракте ЛЖ 84 мм рт.ст.) с гипертрофией МЖП до 18 мм, митральная регургитация (МР) 1 ст., аортальная регургитация 0-1 ст. Получал антигипертензивную терапию, бета-блокаторы, на фоне чего АД находилось на целевом уровне, физические нагрузки переносил удовлетворительно. С 38 лет появились одышка и тяжесть за грудиной при умеренных физических нагрузках, а также эпизоды головокружения. При коронароангиографии коронарные артерии интактны. Обращался к кардиохирургам с целью хирургического лечения ГКМП, однако в лечении было отказано в связи с технической сложностью вмешательства и умеренной выраженностью симптомов сердечной недостаточности.
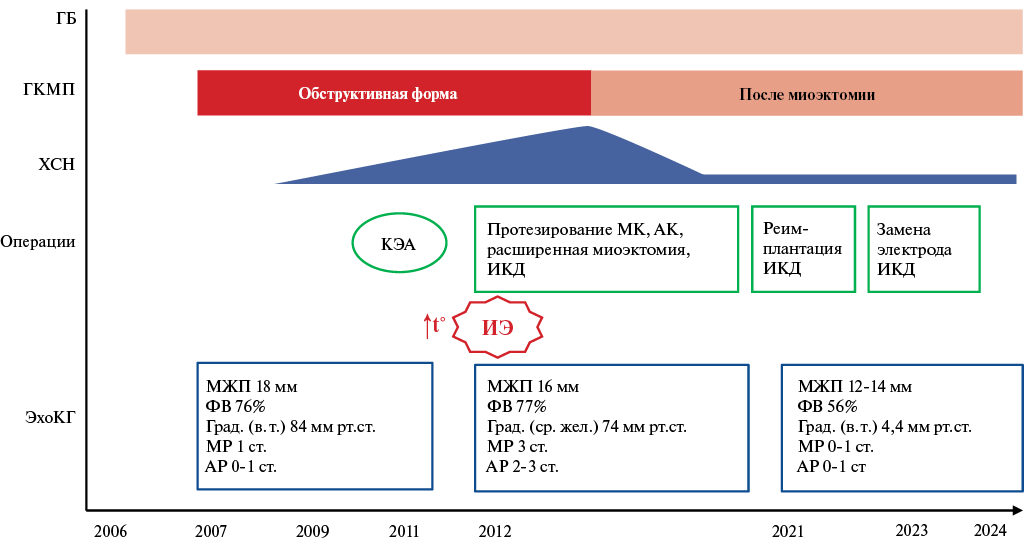
Рис. 1. Графический анамнез пациента.
Сокращения: АК — аортальный клапан, АР — аортальная регургитация, ГБ — гипертоническая болезнь, ГКМП — гипертрофическая кардиомиопатия, ИКД — имплантируемый кардиовертер-дефибриллятор, ИЭ — инфекционный эндокардит, КЭА — каротидная эндартерэктомия, МК — митральный клапан, МЖП — межжелудочковая перегородка, МР — митральная регургитация, ФВ — фракция выброса, ХСН — хроническая сердечная недостаточность, ЭхоКГ — эхокардиография, в. т. — выносящий тракт левого желудочка, град. — градиент, ср. жел. — средняя треть левого желудочка.
Для уточнения природы головокружения в августе 2011г была выполнена ультразвуковая допплерография брахиоцефальных артерий: выявлены гемодинамически значимые стенозы сонных артерий (справа: стеноз ампулы внутренней сонной артерии — 70% с нестабильной бляшкой, общей сонной артерии — 65%; слева: стеноз ампулы внутренней сонной артерии — 80% с нестабильной бляшкой, внутренней сонной артерии — 40%). В этом же месяце проведена каротидная эндартерэктомия с обеих сторон (первым этапом слева, а спустя неделю справа). В раннем послеоперационном периоде в течение нескольких дней отмечалась субфебрильная лихорадка. Спустя 2 нед. после второй эндартерэктомии появились эпизоды повышения температуры до 39,0 С по вечерам с ознобами, повышенная потливость, общая слабость. Данных за послеоперационные осложнения, которые могли бы послужить причиной лихорадки, получено не было.
Пациенту амбулаторно назначались различные антибактериальные препараты: амоксициллин с клавулановой кислотой (3 дня), азитромицин (6 дней), моксифлоксацин (5 дней), доксициклин (10 дней), вновь моксифлоксацин (5 дней) с неполным эффектом (температура повышалась периодически в течение дня до 37,5-37,7 С). Обратился в Факультетскую терапевтическую клинику им. В. Н. Виноградова для дальнейшего обследования и лечения.
2.2. Результаты физикального осмотра
Состояние средней степени тяжести. Температура тела 36,7 С. Кожные покровы бледные, на шее с обеих сторон в области сонных треугольников рубцы после каротидной эндартерэктомии. Голеностопные суставы отечны, теплые на ощупь, болезненны при пальпации и активных движениях. Периферические лимфоузлы не увеличены. В легких дыхание везикулярное, проводится во все отделы, хрипов нет, частота дыхательных движений 16 в мин. Тоны сердца приглушены, систолический шум в области верхушки сердца, который проводится в левую подмышечную область. Частота сердечных сокращений (ЧСС) 66 уд./мин. АД 120/80 мм рт.ст. Язык чистый, влажный. Живот мягкий, безболезненный при пальпации. Печень не увеличена, при пальпации край гладкий, безболезненный. Селезенка не пальпируется. Симптом Пастернацкого отрицательный. Очаговой неврологической симптоматики не выявлено. Щитовидная железа при пальпации не увеличена.
2.3. Предварительный диагноз
Обструктивная ГКМП. Вторичный ИЭ с поражением митрального клапана?
2.4. Временная шкала (рис. 1)
2.5. Диагностическая оценка
При обследовании в Факультетской терапевтической клинике им. В. Н. Виноградова верифицировано наличие ИЭ с поражением митрального клапана. При посевах крови получен рост Enterococcus faecium, чувствительного к ванкомицину и хлорамфениколу. При трансторакальной и чреспищеводной ЭхоКГ подтверждено наличие обструктивной ГКМП, а также выявлено поражение митрального клапана с вегетацией до 3 мм и развитием МР 3 ст.; фракция выброса (ФВ) 64%, левое предсердие (ЛП) 118 мл, остальные камеры сердца не расширены. Начата антибактериальная терапия ванкомицином (4,5 нед.) в сочетании с гентамицином (2 нед.), однако к моменту окончания курса лечения ванкомицином у пациента возобновились эпизоды субфебрильной лихорадки, а также появился диастолический шум в точке Боткина-Эрба. Проведена повторная чреспищеводная ЭхоКГ, при которой выявлено подвижное нитевидное эхопозитивное образование на аортальном клапане, отмечено появление аортальной регургитации 2-3 ст., которая отсутствовала ранее в дополнение к уже имеющейся МР 3 ст. Схема антибактериальной терапии была изменена на комбинацию даптомицина и кларитромицина. На этом фоне температура тела нормализовалась, однако на последующем чреспищеводном ЭхоКГ спустя 12 дней отмечено появление второй струи регургитации, что расценено как деструкция клапана, нельзя было исключить возникновение абсцесса клапана.
В процессе обследования пациента рост Enterococcus faecium получен в материале мазка из зева. При осмотре отоларинголога данных за патологию ЛОР-органов не получено. Пациент был проконсультирован стоматологом: выполнена экстракция двух кариозных зубов с явлениями пародонтита, проведена полная санация ротовой полости. По всей видимости, наряду с хирургическим вмешательством, которое предшествовало развитию лихорадки, вклад в развитие бактериемии и ИЭ мог вносить одонтогенный компонент.
В повторных посевах крови роста микроорганизмов не выявлено.
В результате длительной антибактериальной терапии удалось подавить инфекционно-воспалительный процесс, однако тяжелая недостаточность митрального и аортального клапана требовала хирургического лечения.
Пациент был проконсультирован в РНЦХ им. Б. В. Петровского. По данным контрольной ЭхоКГ, выполненной до операции, сохранялись аортальная регургитация 2-3 ст. и МР 3 ст. с передне-систолическим движением створок митрального клапана в сторону МЖП. Кроме того, помимо обструкции выносящего тракта ЛЖ (градиент давления 51 мм рт.ст.) в полости ЛЖ отмечено наличие гипертрофированной папиллярной мышцы, в связи с чем в систолу происходила облитерация полости ЛЖ, градиент давления в средней трети ЛЖ достигал 74 мм рт.ст., толщина МЖП до 16 мм, ФВ 77%. Таким образом, у пациента имели место митральная и аортальная недостаточность в рамках перенесенного ИЭ в сочетании с обструктивной ГКМП с признаками внутрижелудочковой обструкции и обструкции выносящего тракта ЛЖ.
2.6. Клинический диагноз
Основное комбинированное заболевание:
- Обструктивная ГКМП (внутрижелудочковая обструкция, обструкция выносящего тракта ЛЖ).
- Подострый вторичный ИЭ с поражением митрального и аортального клапана, вызванный Enterococcus faecium.
Осложнения: митральная недостаточность 3 ст., аортальная недостаточность 2-3 ст. Хроническая сердечная недостаточность IIa стадии, 2-3 функциональный класс по NYHA.
Фоновое заболевание: стенозирующий атеросклероз брахиоцефальных артерий, билатеральная каротидная эндартерэктомия (август 2011г). Кариес, пародонтит и экстракция зубов 1.5 и 4.6.
Сопутствующие заболевания: гипертоническая болезнь II ст., 2 степени повышения АД, риск сердечно-сосудистых осложнений — 4. Метаболический синдром (гиперлипидемия, гиперурикемия, ожирение 1 ст.).
2.7. Дифференциальная диагностика
Исходно при обследовании пациента проводилась дифференциальная диагностика синдрома гипертрофии миокарда с болезнями накопления, инфильтративными и митохондриальными заболеваниями, для которых также характерен фенотип ГКМП. В процессе диагностики ИЭ исключались иные причины лихорадки и воспалительных изменений в крови, диагноз ИЭ был поставлен в соответствии в действующими на тот момент критериями Duke [5].
2.8. Медицинские вмешательства
В феврале 2012г в условиях искусственного кровообращения и холодовой кардиоплегии пациенту выполнено универсальное хордосохраняющее протезирование митрального клапана, расширенная миоэктомия МЖП и протезирование аортального клапана. Были применены механические двустворчатые протезы. Также был имплантирован ИКД в рамках первичной профилактики внезапной сердечной смерти.
По результатам гистологического исследования материала, полученного интраоперационно, в ткани перегородки выявлено хаотичное неупорядоченное расположение гипертрофированных кардиомиоцитов, что характерно для ГКМП. В папиллярной мышце — явления дистрофии кардиомиоцитов. Аортальный клапан — признаки хронического продуктивного эндокардита склерозированных створок с признаками обострения процесса; митральный клапан — очаговые явления хронического эндокардита, склероз хорд митрального клапана.
2021г: реимплантация ИКД в связи с истощением источника питания.
2023г: реимплантация шокового электрода ИКД в связи с его переломом.
2.9. Динамика и исходы
После операции самочувствие пациента существенно улучшилось. Умеренные физические нагрузки с тех пор переносит удовлетворительно. Регулярно проводились проверки ИКД: неоднократно регистрировались пробежки неустойчивой желудочковой тахикардии, однако устойчивых желудочковых нарушений ритма и адекватных срабатываний ИКД не было.
В апреле 2024г (в 53 года), спустя 12 лет после операции, пациент проходил плановое обследование в Факультетской терапевтической клинике им. В. Н. Виноградова. На момент поступления получал бисопролол, периндоприл, индапамид, аторвастатин и варфарин. Пациента беспокоили лишь нечастые эпизоды гипотонии (АД 80/60 мм рт.ст.), которые регрессировали после коррекции антигипертензивной терапии.
На электрокардиограмме синусовый ритм, отмечаются признаки блокады передней ветви левой ножки пучка Гиса, дилатации ЛП и межпредсердной блокады. Отсутствуют классические вольтажные критерии гипертрофии ЛЖ (сумма амплитуд зубца S в отведении V1 плюс вольтаж зубца R в отведении V5 или V6 <35 мм), однако имеются критерии гипертрофии ЛЖ Peguero-Lo Presti (сумма максимального вольтажа зубца S (в любом отведении) и вольтажа зубца S в отведении V4 ≥28 мм (≥28 мм для мужчин; ≥23 мм для женщин), Cornell (зубец S в отведении V3 + зубец R в отведении aVL >28 мм для мужчин; ≥20 мм для женщин), а также сумма зубцов R в I отведении и S в III >25 мм) (рис. 2). При суточном мониторировании электрокардиограммы на фоне 15 мг бисопролола ЧСС в пределах оптимальных значений (днем 68-96 уд./мин. (средняя ЧСС — 72 уд./мин), ночью 63-82 уд./мин (средняя ЧСС — 68 уд./мин), PQ максимально до 200 мс), зарегистрировано 122 желудочковых экстрасистолы 3 морфологий, 1 эпизод неустойчивой желудочковой тахикардии из 7 комплексов QRS.
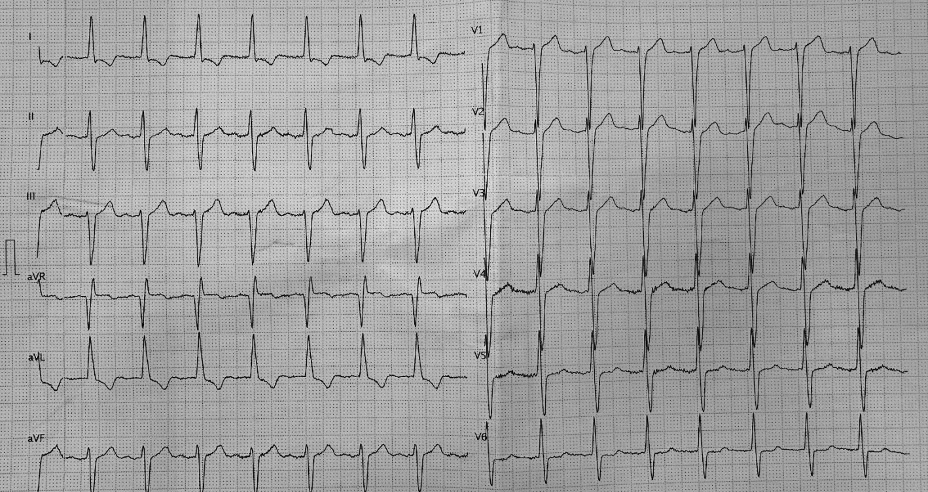
Рис. 2. Электрокардиограмма пациента.
По данным ЭхоКГ данных за дисфункцию протезов митрального и аортального клапанов не получено. Отмечается гипертрофия ЛЖ до 12 мм в средней трети МЖП, в верхней трети до 14 мм без признаков обструкции выносящего тракта ЛЖ, задняя стенка ЛЖ. Отношение массы миокарда ЛЖ к площади поверхности тела 118 г/м2. Глобальная и локальная сократимость ЛЖ не нарушены (ФВ ЛЖ 56%). Присутствует дилатация полости ЛП (передне-задний диаметр ЛП — 5,6 см, объем ЛП — 116 мл, индексированный объем ЛП — 51,3 мл/м2), остальные камеры сердца не расширены: конечно-диастолический размер ЛЖ — 5,0 см, конечно-диастолический объем ЛЖ — 101 мл; передне-задний размер правого желудочка — 3,4 см; объем правого предсердия — 72 мл, индексированный объем правого предсердия — 31,9 мл/м2.
С учетом факторов риска ишемической болезни сердца, в т. ч. стенозирующего атеросклероза брахиоцефальных артерий в анамнезе, проведена сцинтиграфия миокарда. В покое данных за очаговые дефекты перфузии не получено. При нагрузке достигнута ЧСС 145 уд./мин (87% от максимальной расчетной ЧСС): признаков достоверной очаговой преходящей ишемии миокарда ЛЖ не выявлено.
При ультразвуковой допплерографии брахиоцефальных артерий признаков рестенозов не выявлено. Уровень липопротеинов низкой плотности на фоне приема статинов в сочетании с эзетимибом соответствует целевому и составляет 1,63 ммоль/л.
Обсуждение
Актуальным вопросом является профилактика ИЭ у пациентов с ГКМП. Подход к назначению антибиотиков пациентам с ГКМП при вмешательствах, сопровождающихся риском бактериемии, меняется с каждой новой редакцией рекомендаций по ИЭ. До 2007г антибактериальная профилактика рекомендовалась всем пациентам с ГКМП перед инвазивными процедурами, особенно при наличии обструкции выносящего тракта ЛЖ. В дальнейшем профилактика ИЭ была отменена для пациентов с ГКМП из-за сомнений в её эффективности и риске развития антибиотикорезистентности, связанной с профилактической терапией [6]. В настоящее время пациенты с ГКМП относятся к категории промежуточного риска ИЭ и рутинно им не показана антибиотикопрофилактика [4]. Вместе с тем следует отметить, что риск развития ИЭ при ГКМП в 32,8 раза выше, чем в общей популяции [7]. Особенно высок риск ИЭ у пациентов с обструктивной ГКМП в сочетании с дилатацией ЛП [8], что как раз имело место в представленном клиническом случае.
Сочетанные операции у пациентов с ГКМП не являются редкостью. Миоэктомия может выполняться одномоментно с аортокоронарным шунтированием, имплантацией ИКД или протезированием клапанов. Тем не менее именно протезирование клапанов при ГКМП требуется нечасто и не превышает 1-2% в структуре сочетанных операций в экспертных центрах, где выполняется миоэктомия [9]. Особенно редким при хирургическом лечении ГКМП является протезирование клапанов, пораженных инфекционным процессом, что значительно повышает сложность оперативного вмешательства. Показания к замене клапанов в этом случае стандартны: сердечная недостаточность, которая, несомненно, имелась у нашего пациента, неконтролируемая инфекция и высокий риск эмболических осложнений [1].
Уникальность представленного наблюдения состоит в выборе оптимального объема хирургического лечения и прекрасных отдаленных результатах, которые были оценены спустя 12 лет после перенесенного эндокардита и операции. Аналогичных случаев в литературе обнаружить не удалось. В регистр отделения сердечно-сосудистой хирургии клиники Mayo, в который набирались пациенты с ГКМП, осложненной присоединением ИЭ, за 23 года вошло 43 пациента: 95% больных в этом регистре была выполнена септальная миоэктомия, в 58% случаев одномоментно выполнялись вмешательства на клапанах (протезирование или вальвулопластика) [10]. При этом лишь двоим пациентам было одномоментно произведено протезирование сразу двух клапанов, однако ни одному из них не выполнялась миоэктомия, в отличие от представленного нами наблюдения.
Заключение
Пациенты с ГКМП имеют повышенный риск развития ИЭ, однако при своевременной диагностике и активном лечении эндокардита возможен хороший отдаленный прогноз. В настоящем клиническом случае крайне важную роль сыграло хирургическое лечение пациента, в ходе которого было выполнено не только протезирование митрального и аортального клапана, пораженных в рамках ИЭ, но и одномоментно осуществлено хирургическое лечение ГКМП в объеме расширенной миоэктомии и имплантации ИКД.
Прогноз для пациента
С учетом соблюдения всех рекомендаций и удовлетворительного состояния на момент обследования в апреле 2024г прогноз для пациента является относительно благоприятным.
Информированное согласие
Пациент дал письменное добровольное информированное согласие на публикацию описания клинического случая (дата подписания: 15 апреля 2024г).
Отношения и деятельность: все авторы заявляют об отсутствии потенциального конфликта интересов, требующего раскрытия в данной статье.
Список литературы
1. Габрусенко С. А., Гудкова А. Я., Козиолова Н. А. и др. Гипертрофическая кардиомиопатия. Клинические рекомендации 2020. Российский кардиологический журнал. 2021; 26(5):4541. doi:10.15829/1560-4071-2021-4541.
2. Arbelo E, Protonotarios A, Gimeno JR, et al. ESC Guidelines for the management of cardiomyopathies. Eur Heart Journal. 2023;44(37):3503-626. doi:10.1093/eurheartj/ ehad194.
3. Лутохина Ю. А., Благова О. В., Коган Е. А. и др. Распространенность миокардита и его вклад в течение заболевания у пациентов с синдромом первичной гипертрофии миокарда. Российский кардиологический журнал. 2023;28(11):5528. doi:10.15829/1560-40712023-5528.
4. Delgado V, Marsan NA, Waha S, et al. ESC Guidelines for the management of endocarditis: Developed by the task force on the management of endocarditis of the European Society of Cardiology (ESC) Endorsed by the European Association for Cardio-Thoracic Surgery (EACTS) and the European Association of Nuclear Medicine (EANM). European Heart Journal. 2023;44(39):3948-4042. doi:10.1093/eurheartj/ehad193.
5. Li JS, Sexton DJ, Mick N, et al. Proposed modifications to the Duke criteria for the diagnosis of infective endocarditis. Clin Infect Dis. 2000;30(4):633-8. doi:10.1086/313753.
6. Dominguez F, Ramos A, Bouza E, et al. Infective endocarditis in hypertrophic cardiomyopathy: A multicenter, prospective, cohort study. Medicine (Baltimore). 2016;95(26): e4008. doi:10.1097/MD.0000000000004008.
7. Thornhill MH, Jones S, Prendergast B, et al. Quantifying infective endocarditis risk in patients with predisposing cardiac conditions. Eur Heart J. 2018;39(7):586-95. doi:10.1093/eurheartj/ehx655.
8. Spirito P, Rapezzi C, Bellone P, et al. Infective endocarditis in hypertrophic cardiomyopathy: prevalence, incidence, and indications for antibiotic prophylaxis. 1999;99(16): 2132-7. doi:10.1161/01.cir.99.16.2132.
9. Дземешкевич С. Л. Кардиохирургия. Уровень доказательности экспертный. МЕДпресс-информ, 2024. 344 с. ISBN: 978-5-907760-67-7.
10. Oberoi M, Schaff HV, Nishimura RA, et al. Surgical Management of Hypertrophic Cardiomyopathy Complicated by Infective Endocarditis. Ann Thorac Surg. 2022;114(3): 744-9. doi:10.1016/j.athoracsur.2022.01.016.
Об авторах
Ю. А. ЛутохинаРоссия
Юлия Александровна Лутохина — к.м.н., доцент кафедры факультетской терапии № 1
Москва
В. А. Осадчая
Россия
Вера Анатольевна Осадчая — врач-терапевт Факультетской терапевтической клиники им. В. Н. Виноградова
Москва
Н. В. Морозова
Россия
Наталья Владимировна Морозова — к.м.н., зав. терапевтическим отделением Факультетской терапевтической клиники им. В. Н. Виноградова
Москва
Н. В. Чичкова
Россия
Наталья Васильевна Чичкова — д.м.н., доцент, профессор кафедры факультетской терапии № 1
Москва
Н. А. Ганиева
Россия
Нармин Ахмедовна Ганиева — cтудент
Москва
М. А. Пигалицына
Россия
Мария Алексеевна Пигалицына — cтудент
Москва
С. Л. Дземешкевич
Россия
Сергей Леонидович Дземешкевич — д.м.н., профессор, г.н.с. отделения хирургического лечения дисфункции миокарда и сердечной недостаточности
Москва
Дополнительные файлы
- Пациенты с гипертрофической кардиомиопатией имеют повышенный риск развития инфекционного эндокардита.
- Оптимальный выбор объема хирургического лечения у пациента с сочетанием обструктивной гипертрофической кардиомиопатии и инфекционного эндокардита имеет важное значение для отдаленных исходов заболевания.
- Комплексное лечение и своевременная диагностика инфекционного эндокардита способствуют благоприятному прогнозу.
Рецензия
Для цитирования:
Лутохина Ю.А., Осадчая В.А., Морозова Н.В., Чичкова Н.В., Ганиева Н.А., Пигалицына М.А., Дземешкевич С.Л. Тяжелый инфекционный эндокардит у пациента с обструктивной гипертрофической кардиомиопатией: 12 лет после сочетанной операции. Клинический случай. Российский кардиологический журнал. 2024;29(10S):6076. https://doi.org/10.15829/1560-4071-2024-6076. EDN: LVUBIY
For citation:
Lutokhina Yu.A., Osadchaya V.A., Morozova N.V., Chichkova N.V., Ganieva N.A., Pigalitsyna M.A., Dzemeshkevich S.L. Severe infective endocarditis in a patient with hypertrophic obstructive cardiomyopathy: 12 years after combined surgery. A case report. Russian Journal of Cardiology. 2024;29(10S):6076. (In Russ.) https://doi.org/10.15829/1560-4071-2024-6076. EDN: LVUBIY
JATS XML

















































