Перейти к:
Вакцинация против новой коронавирусной инфекции и предикторы ее развития у пациентов после трансплантации сердца: Российское многоцентровое наблюдательное исследование
https://doi.org/10.15829/1560-4071-2024-6067
EDN: CGBHVK
Аннотация
У пациентов после перенесенной трансплантации сердца (ТС) имеется высокий риск развития инфекционных осложнений, в т.ч. госпитализации и смерти при заражении SARS-CoV-2. Однако и пациенты с хронической сердечной недостаточностью и реципиенты сердца часто сталкиваются с отказом в вакцинации из-за недостаточного количества данных о ее безопасности в данной популяции.
Цель. Оценка эффективности и безопасности вакцинации против новой коронавирусной инфекции (COVID-19) у лиц, перенесших ТС.
Материал и методы. Проведен ретроспективный анализ результатов многоцентрового регистра, созданного на основе "Базы данных пациентов после трансплантации сердца в зависимости от выполненной вакцинации против новой коронавирусной инфекции COVID-19", (№ 2022622422, Симоненко М. А., Федотов П. А.), и включившего 47 показателей и заслепленные результаты наблюдения за 367 реципиентами сердца, получавшими посттрансплантационную поддержку с февраля 2020г по май 2023г и проживавших в 7 регионах России.
Результаты. Большинство пациентов, включенных в исследование, были мужчинами (80%, n=294). Средний возраст больных на момент вакцинации был 53±13 лет. Индукция иммуносупрессии была проведена у 82,3% пациентов и далее они получали поддерживающую иммуносупрессивную терапию ингибиторами кальциневрина, микофеноловой кислотой/микофенолатом мофетилом или эверолимусом, а половина из них — по срокам после ТС — глюкокортикостероидами. 67% (n=245) реципиентов, включенных в анализ, не болели COVID-19 до ТС, и еще 33% (n=122) перенесли COVID-19 после ТС, не будучи вакцинированы. На май 2023г почти половина участников регистра (47%; n=174) были привиты против COVID-19 с применением вакцин "ГамКовидВак" (Спутник V) у 94% (n=164) лиц и у 6% (n=10) — "Спутник Лайт". До ТС иммунизация была проведена лишь у 6,5% исследованных. У 17% (n=30) пациентов в течение 24-48 ч после вакцинации развились нетяжелые побочные эффекты в виде субфебрилитета (10%), фебрилитета (4%), общей слабости (11%) или головной боли (2%). 18% (n=32) пациентов из группы вакцинированных были впоследствии инфицированы COVID-19, из них только у 5 человек было среднетяжелое течение. Через 1,5-2 мес. у двоих пациентов развились постковидные осложнения в виде обострения бронхиальной астмы (n=1) и постковидного альвеолита (n=1), которые были купированы применением глюкокортикостероидов. При отсутствии вакцинации относительный риск развития COVID-19 по сравнению с вакцинированными пациентами составил 2,66 (95% доверительный интервал: 1,88-3,75). Вакцинация от COVID-19 ассоциируется со снижением абсолютного риска COVID-19 на 30,9%, а для предотвращения 1 случая COVID-19 необходимо вакцинировать 4 реципиентов сердца (NNT=3,2).
Заключение. Вакцинация против COVID-19 у реципиентов сердца безопасна и ассоциирована с меньшей частотой развития COVID-19 и более легким ее течением по сравнению с невакцинированными больными. Предикторами инфицирования COVID-19 в исследованной выборке были мужской пол, применение микофеноловой кислоты/микофенолата мофетила и индукция иммуносупрессии.
Ключевые слова
Для цитирования:
Симоненко М.А., Федотов П.А., Костомаров А.Н., Космачева Е.Д., Колодина М.В., Утьманова И.В., Головина Т.С., Мельников И.Ю., Зубарева И.Г., Горбунова Н.А., Климова М.О., Карпенко М.Ф., Ситникова М.Ю. Вакцинация против новой коронавирусной инфекции и предикторы ее развития у пациентов после трансплантации сердца: Российское многоцентровое наблюдательное исследование. Российский кардиологический журнал. 2024;29(9):6067. https://doi.org/10.15829/1560-4071-2024-6067. EDN: CGBHVK
For citation:
Simonenko M.A., Fedotov P.A., Kostomarov A.N., Kosmachova E.D., Kolodina M.V., Utmanova I.V., Golovina T.S., Melnikov I.Yu., Zubareva I.G., Gorbunova N.A., Klimova M.O., Karpenko M.A., Sitnikova M.Yu. Vaccination against a COVID-19 and predictors of COVID-19 development in patients after heart transplantation: a Russian multicenter observational study. Russian Journal of Cardiology. 2024;29(9):6067. (In Russ.) https://doi.org/10.15829/1560-4071-2024-6067. EDN: CGBHVK
У пациентов после перенесенной трансплантации сердца (ТС) имеется высокий риск развития инфекционных осложнений, в т. ч. госпитализации и смерти при заражении SARS-CoV-21, 2, 3 [1]. При ретроспективной оценке мировых данных смертность от новой коронавирусной инфекции (COVID-19) за 2020г среди реципиентов сердца составляла 15-40% [2][3], с последующим снижением до 6%1 [4] в связи с применением вакцин и разработки методов лечения COVID-19.
Кандидатам на трансплантацию следует рекомендовать вакцинацию в короткие сроки из-за риска инфекционных осложнений и сниженного после пересадки сердца поствакцинального ответа, развивающихся вследствие иммуносупрессивной терапии (класс I, уровень доказанности — С)2 [5]. Однако и пациенты с хронической сердечной недостаточностью (ХСН), и реципиенты сердца часто сталкиваются с отказом в вакцинации из-за недостаточного количества данных о ее безопасности в данной популяции. Поэтому целью данной работы была оценка эффективности и безопасности вакцинации против COVID-19 у лиц, перенесших ТС.
Материал и методы
Проведен ретроспективный анализ результатов многоцентрового регистра, созданного на основе "Базы данных пациентов после трансплантации сердца в зависимости от выполненной вакцинации против новой коронавирусной инфекции COVID-19", (№ 2022622422, Симоненко М. А., Федотов П. А.), и включившего 47 показателей и заслепленные результаты наблюдения за 367 реципиентами сердца, получавшими посттрансплантационную поддержку с февраля 2020г по май 2023г и проживавших в 7 регионах России: г. Санкт-Петербург — 156 пациентов, г. Краснодар — 97, г. Кемерово — 41, г. Уфа — 27, г. Красноярск — 27, г. Челябинск — 8, г. Екатеринбург — 8, г. Ханты-Мансийск — 3. Исследование было выполнено в соответствии с принципами Хельсинкской декларации, и все больные подписывали информированное согласие для наблюдения у врача-кардиолога-трансплантолога того профильного трансплантационного центра, где наблюдались.
Результаты
Клиническая характеристика больных представлена в таблице 1, генез ХСН отражен на рисунке 1. Индукция иммуносупрессии была проведена у 82,3% пациентов и далее они получали поддерживающую иммуносупрессивную терапию ингибиторами кальциневрина, микофеноловой кислотой/микофенолатом мофетилом или эверолимусом, а половина из них — по срокам после ТС — глюкокортикостероидами. У 26 пациентов медикаментозная терапия была неизвестна.
Таблица 1
Характеристика реципиентов сердца, включенных в регистр
|
Показатели |
Величина (n=367) |
|
|
Мужчины, n (%) |
294 (80%) |
|
|
Возраст на момент ТС, лет (М±sd) |
48±13 |
|
|
Возраст на момент вакцинации, лет (М±sd) |
53±13 |
|
|
Лет после ТС, когда выполнена вакцинация, лет (М±sd) |
4,9±3,4 |
|
|
Индукция иммуносупрессии в момент ТС, n (%) |
302 (82,3%) |
|
|
Прием такролимуса, n (%) |
335 (91,3%) |
|
|
Прием циклоспорина, n (%) |
6 (1,6%) |
|
|
Прием эверолимуса, n (%) |
56 (15,3%) |
|
|
Прием ММФ, n (%) |
286 (77,9%) |
|
|
Прием ГКС, n (%) |
180 (49,0%) |
|
|
COVID-19 до ТС, n (%) |
39 (10,6%) |
|
|
Наличие антител против COVID-19 до вакцинации, n (%) |
61 (16,6%) |
|
|
Особенности вакцинации |
||
|
Вакцинация против COVID-19 до ТС, n (%) |
24 (6,5%) |
|
|
Название вакцины до ТС |
Спутник V (ГамКовидВак), n (%) |
17 (4,6%) |
|
Спутник Лайт, n (%) |
3 (0,8%) |
|
|
КовиВак, n (%) |
1 (0,3%) |
|
|
Не указано, n (%) |
3 (0,8%) |
|
|
Вакцинация против COVID-19 после ТС, n (%) |
174 (47,4%) |
|
|
Период после ТС, когда была выполнена вакцинация, лет (М±sd) |
4,9±3,4 |
|
|
Название вакцины против COVID-19 после ТС |
Спутник V (ГамКовидВак), n (%) |
164 (44,7%) |
|
Спутник Лайт, n (%) |
9 (2,5%) |
|
|
Moderna, n (%) |
1 (0,3%) |
|
|
Ревакцинация, n (%) |
43 (11,7%) |
|
|
Название вакцины для ревакцинации |
Спутник V (ГамКовидВак), n (%) |
17 (4,6%) |
|
Спутник Лайт, n (%) |
26 (7,1%) |
|
|
Сроки ревакцинации после первой вакцинации, мес. (М±sd) |
11,1±2,5 |
|
|
Характеристики течения COVID-19 после вакцинации |
||
|
Развитие COVID-19, n (%) |
32 (8,7%) |
|
|
Сроки возникновения COVID-19 после вакцинации, мес., n (%) |
5,9±2,5 |
|
|
Тяжесть течения COVID-19 после вакцинации |
Бессимптомная, n (%) |
4 (1,1%) |
|
Легкая, n (%) |
23 (6,3%) |
|
|
Средняя, n (%) |
5 (1,4%) |
|
|
Тяжелая, n (%) |
0 |
|
|
Лечение COVID-19 |
Амбулаторное, n (%) |
27 (7,4%) |
|
Стационарное, n (%) |
5 (1,4%) |
|
|
В отделении реанимации, n (%) |
0 |
|
|
% поражения легких по МСКТ (%) |
от 0 до 40 |
|
|
День начала лечения COVID-19, развившегося после вакцинации, дни, Ме [Q1; Q3] |
1 [ 1; 2] |
|
|
Осложнения COVID-19 у вакцинированных пациентов, n (% от переболевших) |
3 (0,8%) |
|
|
Сроки развития осложнений COVID-19 у вакцинированных пациентов, мес. |
2 (1-2) |
|
|
Выживаемость при COVID-19, перенесенной после вакцинации, n (% от переболевших) |
32 (100%) |
|
Сокращения: ГКС — глюкокортикостероиды, ММФ — микофенолата мофетил/микофеноловая кислота, МСКТ — мультиспиральная компьютерная томография, ТС — трансплантация сердца, COVID-19 — новая коронавирусная инфекция.
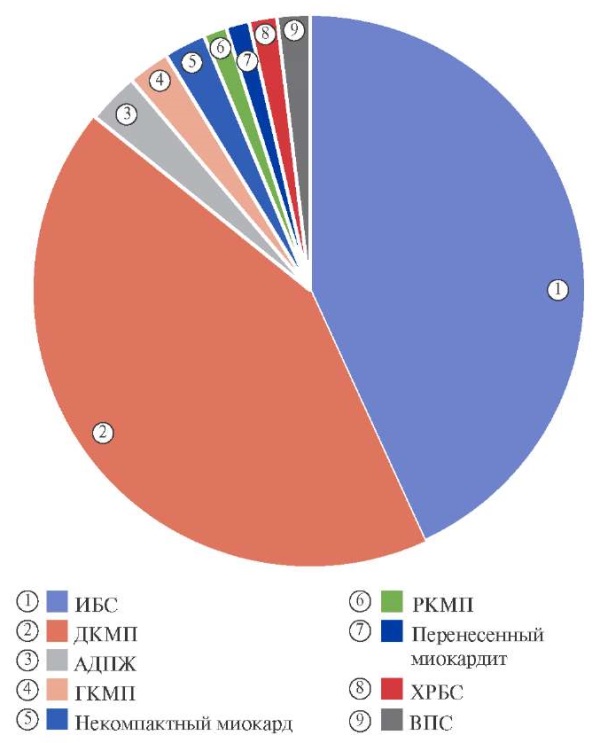
Рис. 1. Генез ХСН у реципиентов сердца, включенных в регистр.
Примечание: 43% (n=158) — ИБС, ишемическая болезнь сердца, 42,5% (n=156) — ДКМП, дилатационная кардиомиопатия, 3% (n=11) — АДПЖ, аритмогенная дисплазия правого желудочка; 2,5% (n=9) — ГКМП, гипертрофическая кардиомиопатия; 2,5% (n=9) — некомпактный миокард; 1,4% (n=5) — РКМП, рестриктивная кардиомиопатия; 1,4% (n=5) — перенесенный миокардит; 1,6% (n=6) — ХРБС, хроническая ревматическая болезнь сердца; 1,9% (n=7) — ВПС, врожденный порок сердца.
67% (n=245) реципиентов, включенных в анализ, не болели COVID-19 до ТС, и еще 33% (n=122) перенесли COVID-19 после ТС, не будучи вакцинированы. На май 2023г почти половина участников регистра (47%; n=174) были привиты против COVID-19 с применением вакцин "ГамКовидВак" у 94% (n=164) лиц и у 6% (n=10) — "Спутник Лайт". До ТС иммунизация была проведена лишь у 6,5% исследованных. У 17% (n=30) пациентов в течение 24-48 ч после вакцинации развились нетяжелые побочные эффекты в виде субфебрилитета (10%), фебрилитета (4%), общей слабости (11%) или головной боли (2%).
Инфицирование COVID-19 у вакцинированных реципиентов сердца. Выполнен ретроспективный анализ инфицирования COVID-19 у реципиентов сердца до и после их вакцинации. Реципиенты сердца, которым не выполнялась в дальнейшем вакцинация, в данный анализ не были включены. Среди вакцинированных пациентов (n=174) — двое больных были исключены из анализа в связи с отсутствием информации об их судьбе. 18% (n=32) пациентов из группы вакцинированных были впоследствии инфицированы COVID-19, из них только у 5 человек было среднетяжелое течение. Через 1,5-2 мес. у двоих пациентов развились постковидные осложнения в виде обострения бронхиальной астмы (n=1) и постковидного альвеолита (n=1), которые были купированы применением глюкокортикостероидов. Для выявления предикторов развития COVID-19 реципиенты сердца (n=172) были разделены на 2 группы (табл. 2): группа 1 — пациенты, которые не болели COVID-19 до вакцинации (n=92), группа 2 — пациенты, которые перенесли новую коронавирусную инфекцию до вакцинации (n=80). Критерием для включения в группу 2 было подтверждение перенесенной COVID-19 либо по результатам полимеразной цепной реакции мазка из ротоглотки/носоглотки, либо по результатам компьютерной томографии органов грудной клетки, либо при наличии IgM к SARS-CoV-2 и/или IgG к SARS-CoV-2.
Таблица 2
Характеристика реципиентов сердца
в зависимости от статуса по COVID-19 до вакцинации
|
Показатели Группа |
Группа 1 (не болели COVID-19 до вакцинации) |
Группа 2 (болели COVID-19 до вакцинации) |
р-level |
|
|
Всего (n) |
92 |
80 |
||
|
Мужской пол, % (n) |
76% (n=70) |
70% (n=56) |
0,392 |
|
|
Возраст на момент вакцинации, лет (М±sd) |
51,7±14,8 |
52,5±11,6 |
0,828 |
|
|
Лет после ТС, когда выполнена вакцинация, лет (М±sd) |
4,1±3,1 |
4,8±3,0 |
0,151 |
|
|
Этиология ХСН |
||||
|
ИБС, % (n) |
38% (n=35) |
41% (n=33) |
0,887 |
|
|
ДКМП, % (n) |
46% (n=42) |
35% (n=28) |
||
|
РКМП, % (n) |
1% (n=1) |
4% (n=3) |
||
|
ГКМП, % (n) |
4% (n=4) |
4% (n=3) |
||
|
Некомпактный миокард, % (n) |
2% (n=2) |
8% (n=6) |
||
|
АДПЖ, % (n) |
2% (n=2) |
5% (n=4) |
||
|
Миокардит, % (n) |
2% (n=2) |
0 |
||
|
ХРБС, % (n) |
1% (n=1) |
3% (n=2) |
||
|
ВПС, % (n) |
3% (n=3) |
1% (n=1) |
||
|
Характер иммуносупрессии |
||||
|
Индукция иммуносупрессии в момент ТС, % (n) |
74% (n=68) |
89% (n=71) |
0,019 |
|
|
Прием такролимуса, % (n) |
98% (n=90) |
99% (n=78) |
1,0 |
|
|
Прием циклоспорина, % (n) |
2% (n=2) |
3% (n=2) |
1,0 |
|
|
Прием эверолимуса, % (n) |
22% (n=20) |
32% (n=25) |
0,165 |
|
|
Прием ММФ, % (n) |
74% (n=68) |
67% (n=53) |
0,4 |
|
|
Прием ГКС, % (n) |
36% (n=33) |
34% (n=27) |
0,873 |
|
|
Характеристики статуса по COVID-19 |
||||
|
COVID-19, перенесенный до ТС, % (n) |
15% (n=14) |
1% (n=1) |
0,001 |
|
|
Наличие антител до вакцинации, % (n) |
7% (n=6) |
52% (n=43) |
<0,001 |
|
|
Вакцинация против COVID-19 до ТС, % (n) |
7% (n=6) |
0 |
0,031 |
|
|
Название вакцины до ТС |
Спутник V (ГамКовидВак), % (n) |
33% (n=2) |
0 |
1,0 |
|
Спутник Лайт, % (n) |
67% (n=4) |
0 |
||
Сокращения: АДПЖ — аритмогенная дисплазия правого желудочка, ВПС — врожденный порок сердца, ГКМП — гипертрофическая кардиомиопатия, ГКС — глюкокортикостероиды, ДКМП — дилатационная кардиомиопатия, ИБС — ишемическая болезнь сердца, ММФ — микофенолата мофетил/микофеноловая кислота, РКМП — рестриктивная кардиомиопатия, ТС — трансплантация сердца, ХРБС — хроническая ревматическая болезнь сердца, ХСН — хроническая сердечная недостаточность, COVID-19 — новая коронавирусная инфекция.
По результатам логистической регрессии была выявлена зависимость развития COVID-19 от ряда факторов, описывается уравнением (рис. 2):
p=1/(1+e-z)*100%
z=-2,1-5,6*XКДТС+2,1*XИИТС+4,2АТДТС (1),
где p — вероятность возникновения COVID-19 после перенесенной ТС до выполнения вакцинации (%), XКДТС — перенесенная COVID-19 до выполнения ТС, XИИТС — индукция иммуносупрессии в момент ТС, XАТДТС — наличие антител к COVID-19 до ТС.
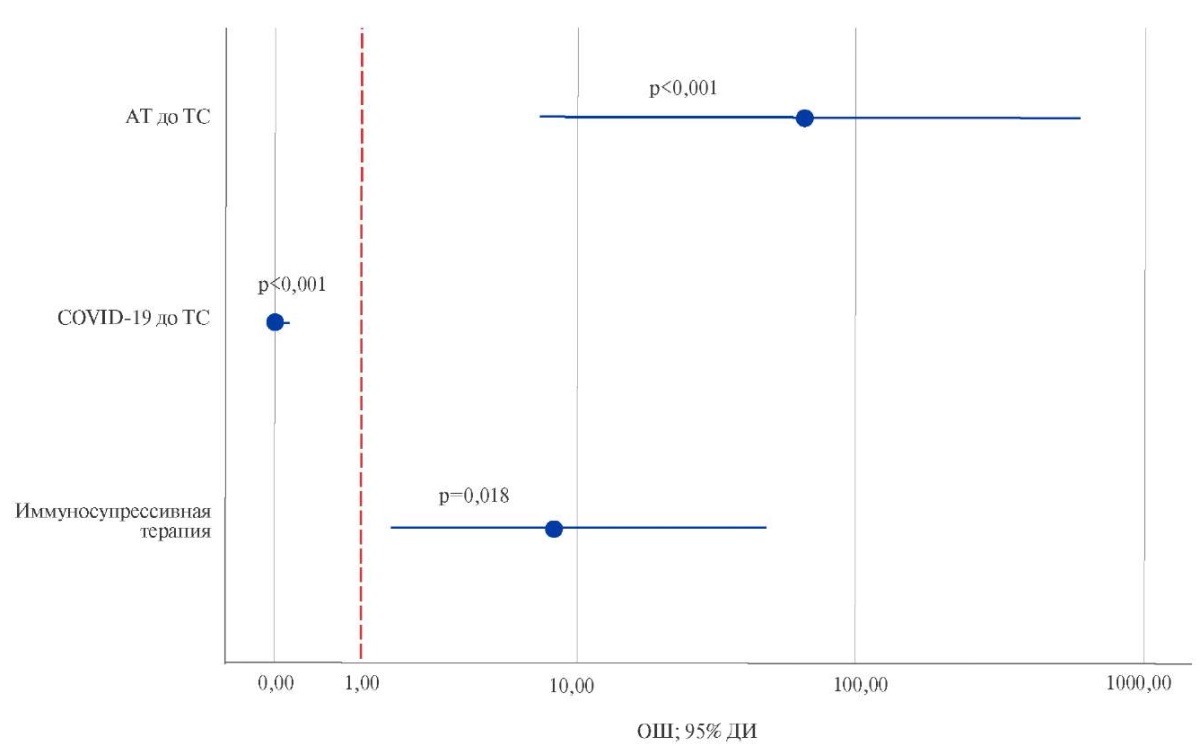
Рис. 2. Предикторы развития COVID-19 у реципиентов сердца.
Примечание: АТ до ТС — наличие антител к SARS-CoV-2 до трансплантации сердца, COVID-19 до ТС — перенесенная COVID-19 до трансплантации сердца, Иммуносупрессивная терапия — применение индукции в раннем послеоперационном периоде у реципиентов сердца.
Сокращения: АТ — антитела, ДИ — доверительный интервал, ОШ — отношение шансов, ТС — трансплантация сердца, COVID-19 — новая коронавирусная инфекция.
Полученная регрессионная модель является статистически значимой (p<0,001). Исходя из значения коэффициента детерминации Найджелкерка, модель (1) учитывает 70% факторов, определяющих вероятность возникновения COVID-19 после ТС до выполнения вакцинации. Чувствительность модели — 94%, специфичность — 63%. Данная модель позволяет прогнозировать COVID-19 у больных после ТС без вакцинации и позволит принимать решение о необходимости вакцинации, что важно у пациентов с рисками осложнений вакцинации: при наличии в анамнезе онкопатологии, диагностированными аутоиммунными заболеваниями и при перенесенном миокардите до ТС.
Для проведения оценки эффективности вакцинации против COVID-19 исследуемые (n=172) были разделены на две группы (табл. 3): группа 3 — пациенты, которые не болели COVID-19 после завершения вакцинации — 140 человек; группа 4 — пациенты, которые перенесли COVID-19 после завершения вакцинации — 32 человека. У 1 пациента из группы 3 была неизвестна медикаментозная терапия.
Таблица 3
Характеристика реципиентов сердца
в зависимости от инфицирования COVID-19 в поствакцинальном периоде
|
Группа Показатели |
Группа 3 (не болели COVID-19 после вакцинации) (n=140) |
Группа 4 (болели COVID-19 после вакцинации) (n=32) |
р-level |
|
|
Пол |
Мужской, % (n) |
78% (n=109) |
53% (n=17) |
0,007 |
|
Женский, % (n) |
22% (n=31) |
47% (n=15) |
||
|
Возраст на момент ТС, лет (М±sd) |
47,5±13,4 |
46,2±13,5 |
0,635 |
|
|
Возраст на момент вакцинации, лет (М±sd) |
51,8±13,5 |
52,2±13,4 |
0,889 |
|
|
Лет после ТС, когда выполнена вакцинация, лет (М±sd) |
4,2±3,1 |
5,6±2,7 |
0,018 |
|
|
Этиология ХСН |
||||
|
1) ИБС, % (n) |
42% (n=59) |
28% (n=9) |
0,044 |
|
|
2) ДКМП, % (n) |
41% (n=58) |
38% (n=12) |
||
|
3) РКМП, % (n) |
1% (n=2) |
6% (n=2) |
||
|
4) ГКМП, % (n) |
4% (n=5) |
6% (n=2) |
||
|
5) Некомпактный миокард, % (n) |
5% (n=7) |
3% (n=1) |
||
|
6) АДПЖ, % (n) |
3% (n=4) |
6% (n=2) |
||
|
7) Миокардит, % (n) |
1% (n=2) |
0 |
||
|
8) ХРБС, % (n) |
0 |
9% (n=3) |
||
|
9) ВПС, % (n) |
2% (n=3) |
3% (n=1) |
||
|
Характер иммуносупрессии |
||||
|
Индукция иммуносупрессии в момент ТС, % (n) |
78% (n=109) |
94% (n=30) |
0,046 |
|
|
Прием такролимуса, % (n) |
99% (n=138) |
94% (n=30) |
0,09 |
|
|
Прием циклоспорина, % (n) |
1% (n=1) |
6% (n=2) |
0,09 |
|
|
Прием эверолимуса, % (n) |
23% (n=32) |
41% (n=13) |
0,048 |
|
|
Прием ММФ, % (n) |
75% (n=104) |
53% (n=17) |
0,019 |
|
|
Прием ГКС, % (n) |
37% (n=52) |
25% (n=8) |
0,221 |
|
|
Статус по COVID-19 |
||||
|
COVID-19 до ТС, % (n) |
11% (n=15) |
0 |
0,077 |
|
|
COVID-19 после ТС, % (n) |
45% (n=63) |
53% (n=17) |
0,437 |
|
|
Наличие антител до вакцинации, % (n) |
64% (n=40) |
53% (n=9) |
0,576 |
|
|
Вакцинация против COVID-19 после ТС, % (n) |
100% (n=140) |
100% (n=32) |
1,0 |
|
|
Название вакцины против COVID-19 после ТС |
Спутник V (ГамКовидВак), % (n) |
96% (n=133) |
94% (n=30) |
0,709 |
|
Спутник Лайт, % (n) |
3% (n=5) |
6% (n=2) |
||
|
Moderna, % (n) |
1% (n=1) |
0 |
||
|
COVID-19 между двумя вакцинациями, % (n) |
4% (n=5)* |
16% (n=5) |
0,023 |
|
|
Сроки возникновения COVID-19 после вакцинации, мес. (М±sd) |
– |
5,9±2,5 |
||
|
Тяжесть течения COVID-19 после вакцинации |
Бессимптомная, % (n) |
– |
13% (n=4) |
|
|
Легкая, % (n) |
– |
72% (n=23) |
||
|
Средняя, % (n) |
– |
15% (n=5) |
||
|
Тяжелая, % (n) |
– |
0 |
||
|
Лечение COVID-19 |
Амбулаторное, % (n) |
– |
84% (n=27) |
|
|
Стационарное, % (n) |
– |
16% (n=5) |
||
|
Отделение реанимации, % (n) |
– |
0 |
||
|
% поражения легких по МСКТ (%) |
– |
0 (0-40) |
нз |
|
|
Выживаемость при COVID-19 после вакцинации |
Жив, % (n) |
– |
97% (n=31) |
|
|
Умер, % (n) |
– |
3% (n=1) |
||
|
День начала лечения COVID-19, развившегося после вакцинации, дни, Ме [ Q1; Q3] |
– |
1 [ 1; 2] |
0,333 |
|
|
Развитие постковидных осложнений, % (n) |
– |
7% (n=2) |
||
|
Варианты постковидных осложнений, n |
– |
Альвеолит — 1 Обострение бронхиальной астмы — 1 |
||
|
Сроки развития постковидных осложнений, мес. |
– |
2 (1-2) |
||
|
Ревакцинация, % (n) |
28% (n=36) |
23% (n=7) |
0,655 |
|
|
Название вакцины для ревакцинации |
Спутник V (ГамКовидВак), % (n) |
46% (n=16) |
– |
0,033 |
|
Спутник Лайт, % (n) |
54% (n=19) |
100% (n=7) |
||
|
Сроки ревакцинации после первой вакцинации, месяцы (М±sd) |
10,9±2,7 |
12,3±0,8 |
0,012 |
|
Примечание: * — пациенты были инфицированы после 1-й инъекции и до получения 2-й. Но после получения двух инъекций повторного инфицирования не было.
Сокращения: АДПЖ — аритмогенная дисплазия правого желудочка, ВПС — врожденный порок сердца, ГКМП — гипертрофическая кардиомиопатия, ГКС — глюкокортикостероиды, ДКМП — дилатационная кардиомиопатия, ИБС — ишемическая болезнь сердца, ММФ — микофенолата мофетил/микофеноловая кислота, МСКТ — мультиспиральная компьютерная томография, РКМП — рестриктивная кардиомиопатия, ТС — трансплантация сердца, ХРБС — хроническая ревматическая болезнь сердца, ХСН — хроническая сердечная недостаточность, COVID-19 — новая коронавирусная инфекция.
Расчет относительного и абсолютного рисков развития COVID-19 после ТС в зависимости от вакцинации представлен в таблице 4. При отсутствии вакцинации относительный риск развития COVID-19 по сравнению с вакцинированными пациентами составил 2,66 (95% доверительный интервал: 1,88-3,75). Вакцинация против COVID-19 ассоциируется со снижением абсолютного риска COVID-19 на 30,9%, а для предотвращения 1 случая COVID-19 необходимо вакцинировать 4 реципиентов сердца (NNT=3,2).
Таблица 4
Таблица сопряженности признаков вакцинации и случаев развития COVID-19
|
Исход* Вакцинация |
COVID-19 |
Всего |
|
|
Да |
Нет |
||
|
COVID-19 до вакцинации |
90 |
92 |
182 |
|
COVID-19 после вакцинации |
32 |
140 |
172 |
|
Всего |
122 |
232 |
354 |
Примечание: * — Исход = новый случай развития COVID-19.
Сокращение: COVID-19 — новая коронавирусная инфекция.
Обсуждение
У реципиентов трансплантации солидных органов высок риск тяжелого течения COVID-19 и связанной с ним смертности. По рекомендациям Российской Федерации (РФ) такие пациенты относятся к приоритетной группе для выполнения вакцинации против COVID-194. Однако в связи с применением иммуносупрессивной терапии у трансплантированных пациентов после вакцинации у них может развиться сниженный иммунный ответ (низкое количество антител IgG к SARS-CoV-2) или иммунитет вообще не сформируется [6-9], поэтому они имеют более высокий риск заражения COVID-19, чем население в целом2, 3 [4]. Очевидно, что текущая иммуносупрессивная терапия у реципиентов не может быть отменена в связи с риском потери трансплантата и смерти больного1, 2 [5], поэтому необходимо проводить оценку эффективности формирования противоинфекционного иммунитета у этого контингента больных.
Результаты международных исследований вакцинации от гриппа и/или пневмококка у реципиентов после трансплантации солидных органов показали снижение заболеваемости респираторными инфекциями и преимущество в выживаемости в случае развития инфекционных осложнений по сравнению с больными, которым вакцинация не была выполнена ни до, ни после операции [10][11].
После ТС вакцинацию можно выполнять инактивированными вакцинами, при отсутствии текущего инфекционного процесса и не ранее, чем через месяц после купирования инфекции, при условии удовлетворительной работы сердечного трансплантата1, 2 [5]. Выполнение вакцинации от COVID-19 проводится амбулаторно по месту жительства после получения разрешения от лечащего врача.
С февраля 2021г по рекомендациям Международного сообщества трансплантации сердца и легких (International Society for Heart and Lung Transplantation, ISHLT) вакцинация от COVID-19 разрешена у реципиентов после ТС вакцинами Moderna и Pfizer, с апреля 2021г список вакцин для применения после ТС расширился, и в него вошла российская комбинированная векторная вакцина — Спутник V (ГамКовидВак), которая была зарегистрирована в РФ 11.08.20201, 5 [12].
Исследования эффективности прививок против COVID-19 у этого контингента лиц немногочисленны и не описывают использование вакцин отечественного производства. По результатам одноцентрового ретроспективного исследования Cherrett C, et al., с января 2020 по сентябрь 2022гг 132 реципиента сердца были инфицированы COVID-19, 124 (94%) из которых получили ранее как минимум 2 инъекции вакцины мРНК, и большинство из них перенесли легкое течение заболевания, а уровни госпитализации (16%) и смертности (6%) были ниже по сравнению с данными до начала вакцинации [13].
Согласно рекомендациям ISHLT, с учетом перенесенной ТС и иммунокомпрометированного статуса больного, вакцинацию в РФ разрешено выполнить только вакциной "Гам-Ковид-Вак" (Спутник V). Также по рекомендациям показано проводить приоритетную вакцинацию лицам, осуществляющим уход за трансплантированными больными и членам их семей2, 3 [5]. Однако в настоящее время отсутствуют данные о безопасности и эффективности вакцинации против COVID-19 Спутником V трансплантированных пациентов.
По результатам нашего исследования с мая 2021г по май 2023г 174 реципиентам сердца, наблюдавшимся в 8 центрах РФ, была выполнена вакцинация; 23% из них были ревакцинированы через год после первой инъекции, и у большинства (63%) не было побочных поствакцинальных явлений: только у 9 человек был субфебрилитет в первые 24-48 ч после прививки.
79% реципиентов сердца после перенесенной вакцинации в течение оцениваемого периода не заболели COVID-19, 13% вакцинированных перенесли COVID-19 бессимптомно, у 72% заболевание протекало легко и 84% вакцинированных лиц были пролечены на дому. Выживаемость вакцинированных реципиентов в случае инфицирования COVID-19 составила 97%, что сопоставимо с международными данными среди неиммунокомпрометированных пациентов: выживаемость вакцинированных больных составила 93% по сравнению с невакцинированными — 7% [14].
Согласно одноцентровому исследованию, проведенному в Великобритании в 2022г, у реципиентов абдоминальной трансплантации (печень, почка) после получения двух доз вакцинации против COVID-19 смертность, ассоциированная с COVID-19, снизилась с 12,6% до 7,7% [15]. Вакцинированные против COVID-19 в любые сроки относительно ТС реципиенты сердца значимо реже (в 4,5 раза) инфицировались COVID-19 по сравнению с теми, у кого не было вакцинации (табл. 4). Нами были выявлены следующие предикторы развития COVID-19 у вакцинированных реципиентов сердца: мужской пол и индукция иммуносупрессии в раннем послеоперационном периоде. Все эти факторы немодифицируемы.
Профилактическая вакцинация реципиентов сердца должна проводиться еще до ТС, ведь развитие инфекционных процессов в течение 6 мес. после начала иммуносупрессии является ожидаемым осложнением, что и ограничивает проведение иммунизации в этот период. Стратегия проведения вакцинации именно на этапе статуса кандидата на трансплантацию общепринята, она позволяет выработать поствакцинальный ответ до развития иммунокомпрометированного состояния. В силу того, что преобладающая часть реципиентов-участников представленного регистра перенесли ТС еще до развития пандемии, их охват прививочной программой пришелся на период текущей полноразмерной иммуносупрессивной терапии (среди участников регистра лишь 6,5% были вакцинированы до ТС), однако эффективность иммунизации оказалась высокой, а безопасность соотносилась с данными по популяции здорового населения [16].
Ограничения исследования: исследование ретроспективное. У большинства пациентов отсутствуют лабораторные показатели до выполнения вакцинации и в раннем периоде после ее проведения, в т. ч. уровня IgM к COVID-19.
Заключение
- Вакцинация против COVID-19 у реципиентов сердца безопасна и ассоциирована с меньшей частотой развития COVID-19 и более легким ее течением по сравнению с невакцинированными больными.
- Предикторами инфицирования COVID-19 в исследованной выборке были мужской пол, применение микофеноловой кислоты/микофенолата мофетила и индукция иммуносупрессии.
Отношения и деятельность: все авторы заявляют об отсутствии потенциального конфликта интересов, требующего раскрытия в данной статье.
1. ISHLT SARS-CoV-2 Vaccination in Heart and Lung Transplantation, MCS and PH: Recommendations from ISHLT COVID-19 Task Force, 21.05.2021.
2. Joint statement about COVID-19 vaccination in organ transplant candidates and recipients: ASTS, AST, ISHLT, 15.11.2022.
3. Ging P, Ison M, Patel J, et al. New ISHLT COVID-19 therapeutics guidance, 2023г.
4. Временные методические рекомендации РФ "Профилактика, диагностика и лечение новой коронавирусной инфекции (COVID-19), версия 18" от 26.10.2023.
5. Временные методические рекомендации РФ "Порядок проведения вакцинации взрослого населения против COVID-19", 2021г.
Список литературы
1. Симоненко М.А., Федотов П.А., Сазонова Ю.В. и др. Ведение реципиентов после трансплантации сердца с COVID-19: регистр ФГБУ "НМИЦ им. В.А. Алмазова". Кардиология. 2020;60(12):4-12. doi:10.18087/cardio.2020.12.n1342.
2. Diaz-Arocutipa C, Carvallo-Castaneda D, Luiz-Ybanez O, et al. COVID-19 in heart transplant recipients during February-August 2020: a systematic review. Clinical Transplantation. 2021;35:e14390. doi:10.1111/ctr.14390.
3. Azzi Y, Bartash R, Scalea J, et al. COVID-19 and solid organ transplantation: a review article, Transplantation. 2021;105(1):37-55. doi:10.1097/TP.0000000000003523.
4. Cherrett C, Cao J, Adams C, et al. Coronavirus disease 2019 outcomes in heart transplant recipients: a large Australian cohort. J Heart Lung Transplant. 2023;S10.53- 2498(23):2016-8. doi:10.1016/j.healun.2023.09.007.
5. Velleca A, Shullo MA, Dhital K, et al. The International Society for Heart and Lung Transplantation (ISHLT) Guidelines for the care of heart transplant recipients. J Heart Lung Transplant. 2023;42(5):E1-E141. doi:10.1016/j.healun.2022.09.023.
6. Boyarsky BJ, Werbel WA, Avery RA, et al. Antibody Response to 2-Dose SARS-CoV-2 mRNA Vaccine Series in Solid Organ Transplant Recipients. JAMA. 2021;325(21): 2204-6. doi:10.1001/jama.2021.7489.
7. Benotmane I, Gautier-Vargas G, Cognard N, et al. Weak anti-SARS-CoV-2 antibody response after the first injection of an mRNA COVID-19 vaccine in kidney transplant recipients. Kidney Int. 2021;99(6):1487-9. doi:10.1016/j.kint.2021.03.014.
8. Yi SG, Knight RJ, Graviss EA, et al. Kidney Transplant Recipients Rarely Show an Early Antibody Response Following the First COVID-19 Vaccine Administration. Transplantation. 2021;105(7):e72-e73. doi:10.1097/TP.0000000000003764.
9. Peled Y RE, Lavee J, Sternik L, et al. BNT162b2 vaccination in heart transplant recipients: clinical experience and antibody response. J Heart Lung Transplant. 2021;40(8):759- 62. doi:10.1016/j.healun.2021.04.003.
10. Narasimhan MML, Clark AE, Usmani A, et al. Serological Response in Lung Transplant Recipients after Two Doses of SARS-CoV-2 mRNA Vaccines. Vaccines (Basel). 2021;9(7):708. doi:10.3390/vaccines9070708.
11. Pinana JL, Perez A, Montoro J, et al. Clinical Effectiveness of Influenza Vaccination After Allogeneic Hematopoietic Stem Cell Transplantation: A Cross-sectional, Prospective, Observational Study. Clin Infect Dis. 2019;68:1894-903. doi:10.1093/cid/ciy792.
12. Danziger‐Isakov L, Kumar D and Practice TAICo. Vaccination of solid organ transplant candidates and recipients: Guidelines from the American society of transplantation infectious diseases community of practice. Clinical Transplantation. 2019;33(9):e13563. doi:10.1111/ctr.13563.
13. Masetti M, Scuppa MF, Aloisio M, et al. Effect of a fourth dose of mRNA vaccine and of immunosuppression in preventing SARS-CoV-2 breakthrough infections in heart transplant patients. Microorganisms. 2023;11(755):1-13. doi:10.3390/microorganisms11030755.
14. Noor M, Islam MF, Islam R.How did mortality rates from COVID-19 differ between vaccinated and unvaccinated people in a tertiary level hospital of Bangladesh? Mymensingh Med J. 2023;32(4):1198-202.
15. Ravanan R, Mumford L, Ushiro-Lumb I, et al. OTDT Clinical Team Two Doses of SARSCoV-2 Vaccines Reduce Risk of Death Due to COVID-19 in Solid Organ Transplant Recipients: Preliminary Outcomes From a UK Registry Linkage Analysis. Transplantation. 2021;105:e263-e264. doi:10.1097/TP.0000000000003908.
16. Beladiya J, Kumar A, Vasava Y, et al. Safety and efficacy of COVID-19 vaccines: a systematic review and meta-analysis of controlled and randomized clinical trials. Reviews in Medical Virology. 2023;34(1):e2507. doi:10.1002/rmv.2507.
Об авторах
М. А. СимоненкоРоссия
Симоненко Мария Андреевна — с.н.с. НИЛ Высокотехнологичных методов лечения сердечной недостаточности, врач-кардиолог-трансплантолог КДЦ
Санкт-Петербург
П. А. Федотов
Россия
Федотов Петр Алексеевич — к.м.н., зав. НИЛ высокотехнологичных методов лечения сердечной недостаточности, доцент кафедры кардиологии ИМО
Санкт-Петербург
А. Н. Костомаров
Россия
Костомаров Артем Николаевич — ведущий специалист Отдела информационного обеспечения и Телемедицины, врач-кардиолог КДЦ
Санкт-Петербург
Е. Д. Космачева
Россия
Космачева Елена Дмитриевна — д.м.н., профессор, зам. главного врача
Краснодар
М. В. Колодина
Россия
Колодина Маргарита Витальевна — врач-кардиолог-трансплантолог КДП
Краснодар
И. В. Утьманова
Россия
Утьманова Ирина Васильевна — врач-кардиолог отделения кардиохирургии
Красноярск
Т. С. Головина
Россия
Головина Татьяна Сергеевна — врач-кардиолог
Кемерово
И. Ю. Мельников
Россия
Мельников Илья Юльевич — врач-кардиолог
Челябинск
И. Г. Зубарева
Россия
Зубарева Инна Геннадьевна — врач-кардиолог отделения кардиохирургии № 2
Уфа
Н. А. Горбунова
Россия
Горбунова Наталья Александровна — врач-кардиолог клинико-диагностической поликлиники
Екатеринбург
М. О. Климова
Россия
Климова Маргарита Олеговна — врач-кардиолог
Ханты-Мансийск
М. Ф. Карпенко
Россия
Карпенко Михаил Алексеевич — д.м.н., профессор, первый зам. генерального директора
Санкт-Петербург
М. Ю. Ситникова
Россия
Ситникова Мария Юрьевна — д.м.н., профессор, г.н.с., руководитель НИО СН
Санкт-Петербург
Дополнительные файлы
- Вакцинация против новой коронавирусной инфекции (COVID-19) у реципиентов сердца безопасна и ассоциирована с меньшей частотой развития COVID-19 и более легким ее течением по сравнению с невакцинированными больными.
- Вакцинация ассоциируется со снижением абсолютного риска COVID-19 на 30,9%.
- Предикторами инфицирования COVID-19 у реципиентов сердца являются мужской пол и применение иммуносупрессии.
- Нами была создана модель, которая позволяет прогнозировать COVID-19 у больных после трансплантации сердца без вакцинации, для принятия решения о необходимости вакцинации, что важно у пациентов с рисками осложнений вакцинации.
Рецензия
Для цитирования:
Симоненко М.А., Федотов П.А., Костомаров А.Н., Космачева Е.Д., Колодина М.В., Утьманова И.В., Головина Т.С., Мельников И.Ю., Зубарева И.Г., Горбунова Н.А., Климова М.О., Карпенко М.Ф., Ситникова М.Ю. Вакцинация против новой коронавирусной инфекции и предикторы ее развития у пациентов после трансплантации сердца: Российское многоцентровое наблюдательное исследование. Российский кардиологический журнал. 2024;29(9):6067. https://doi.org/10.15829/1560-4071-2024-6067. EDN: CGBHVK
For citation:
Simonenko M.A., Fedotov P.A., Kostomarov A.N., Kosmachova E.D., Kolodina M.V., Utmanova I.V., Golovina T.S., Melnikov I.Yu., Zubareva I.G., Gorbunova N.A., Klimova M.O., Karpenko M.A., Sitnikova M.Yu. Vaccination against a COVID-19 and predictors of COVID-19 development in patients after heart transplantation: a Russian multicenter observational study. Russian Journal of Cardiology. 2024;29(9):6067. (In Russ.) https://doi.org/10.15829/1560-4071-2024-6067. EDN: CGBHVK
JATS XML

















































