Перейти к:
Ассоциация новых биомаркеров системного воспаления с развитием атеросклероза и его выраженностью
https://doi.org/10.15829/1560-4071-2024-6025
EDN: FIDYSH
Аннотация
Цель. Сравнить уровни новых биомаркеров системного воспаления у пациентов с атеросклерозом и без него, а также между группами пациентов с различной его выраженностью.
Материал и методы. Были включены пациенты с подозрением на ишемическую болезнь сердца, которым выполнена селективная коронароангиография. Включен в анализ 901 пациент, средний возраст 61±10 лет, 60% (n=549) мужчин. Пациенты были разделены на две группы: с атеросклерозом и без него. Для статистической поправки на исходные клинические различия использован метод Propensity Score Matching.
Результаты. В группе с атеросклерозом показатели индекса системного воспалительного ответа (SIRI), индекса системного воспаления (SII) и совокупного индекса системного воспаления (AISI) были статистически значимо выше, чем у пациентов без атеросклероза: 0,906 (0,632; 1,36) vs 0,745 (0,519; 1,02), p<0,001; 457 (350; 641) vs 425 (313; 547), p=0,005 и 233 (148; 346) vs 179 (121; 263), p<0,001, соответственно. По результатам ROC анализа пороговые значения изучаемых показателей составили: для SIRI >1,05 площадь под кривой (AUC), доверительный интервал (ДИ) 0,615 (0,571-0,658), p<0,001, чувствительность 42,6%, специфичность 77,3%; для SII >368 AUC, ДИ 0,572 (0,528-0,616), p=0,004, чувствительность 72,1%, специфичность 43,4% и для AISI >248 AUC, ДИ 0,604 (0,560-0,647), p<0,001, чувствительность 47,4%, специфичность 71,1%. У SIRI AUC была наибольшей. При сравнении 6 групп по классификации Coronary Artery Surgery Study Class (CASSC) были обнаружены статистически значимые отличия по SIRI и AISI, p<0,001 и p=0,0016, соответственно. Однако эти различия не имели логической закономерности.
Заключение. Новые маркеры системного воспаления: SIRI, SII и AISI были статистически значимо выше у пациентов с подтвержденным атеросклерозом, чем у пациентов без него. Пороговые уровни, ассоциированные с атеросклерозом, для SIRI >1,05, для SII >368, для AISI >248.
Ключевые слова
Для цитирования:
Шварц В.А., Талибова С.М., Сокольская М.А., Испирян А.Ю., Шварц Е.Н., Петросян А.Д., Мерзляков В.Ю., Скопин А.И., Донаканян С.А. Ассоциация новых биомаркеров системного воспаления с развитием атеросклероза и его выраженностью. Российский кардиологический журнал. 2024;29(8):6025. https://doi.org/10.15829/1560-4071-2024-6025. EDN: FIDYSH
For citation:
Shvarts V.A., Talibova S.M., Sokolskaya M.A., Ispiryan A.Yu., Shvarts E.N., Petrosyan A.D., Merzlyakov V.Yu., Skopin A.I., Donakanyan S.A. Association of novel biomarkers of systemic inflammation with atherosclerosis and its severity. Russian Journal of Cardiology. 2024;29(8):6025. (In Russ.) https://doi.org/10.15829/1560-4071-2024-6025. EDN: FIDYSH
Сердечно-сосудистые заболевания (ССЗ) в настоящее время являются основной причиной смертности во всем мире. На ишемическую болезнь сердца (ИБС) приходится 16% всех смертей в мире [1]. Основой патогенеза ИБС является атеросклероз коронарных артерий — хронический воспалительный процесс, характеризующийся интенсивной иммунологической активностью, основной мишенью которого являются артерии. Основными участниками данного процесса являются эндотелиальные клетки, лейкоциты, гладкомышечные клетки и интима. Учитывая важную роль хронического воспаления в патогенезе ИБС, провоспалительные маркеры имеют ключевое значение, отражая активность процесса. Согласно проведенным ранее исследованиям, была доказана связь уровней фибриногена, С-реактивного белка, маркеров семейства интерлейкинов (интерлейкин-1, -3, -6, -8, -10), фактора некроза опухоли и других провоспалительных маркеров с риском развития атеросклероза [2-5].
В последние годы в мировой литературе были опубликованы научные исследования, описывающие так называемые новые биомаркеры системного воспаления: индекс системного воспаления (Systemic Inflammation Index — SII), индекс системного воспалительного ответа (Systemic Inflammation Response Index — SIRI) и совокупный индекс системного воспаления (Aggregate Inflammation Systemic Index — AISI). В нескольких исследованиях было показано их влияние на прогноз пациентов с онкопатологией [6][7]. Эти биомаркеры являются расчетными индексами, основанными на соотношении количества лейкоцитов и их подтипов. В настоящее время в мире активно изучается их роль при ССЗ [8][9].
Цель исследования: провести сравнительную оценку уровней новых биомаркеров системного воспаления у пациентов с атеросклерозом и без него, а также у пациентов с различной выраженностью атеросклероза.
Материал и методы
Изучаемая популяция
Исследование носило когортный характер. Данные были собраны из медицинской информационной системы "MedWork" ФГБУ "НМИЦ ССХ им. А. Н. Бакулева" Минздрава России. В исследование были включены пациенты старше 18 лет, проходившие стационарное обследование в 2021г в отделении хирургического лечения интерактивной патологии, которым была проведена диагностическая селективная коронароангиография.
Критериями невключения являлись: онкологические заболевания в анамнезе, предшествующие открытые операции на сердце и грудной клетке, прием кортикостероидов и других гормональных препаратов в последний месяц, скорость клубочковой фильтрации <60 мл/мин, хронические заболевания печени, наличие аутоиммунных заболеваний, инфекционный эндокардит в анамнезе, предшествующие любые операции за последний год в анамнезе, дилатационная кардиомиопатия. Из 1258 пациентов были отобраны истории болезней пациентов, соответствовавшие критериям включения и исключения.
Сбор данных. Определения
Изучаемые параметры включали в себя клинические данные, данные лабораторных и инструментальных методов исследования. Изучаемые индексы системного воспаления были рассчитаны по следующим формулам: SIRI — индекс системного воспалительного ответа = количество нейтрофилов × количество моноцитов ÷ количество лимфоцитов; SII — индекс системного воспаления = количество нейтрофилов × количество тромбоцитов ÷ количество лимфоцитов; AISI — совокупный системный индекс воспаления = количество нейтрофилов × количество моноцитов × количество тромбоцитов ÷ количество лимфоцитов. Отношение нейтрофилов к лимфоцитам (NLR), отношение тромбоцитов к лимфоцитам (PLR) и отношение моноцитов к лимфоцитам (MLR) были рассчитаны, соответственно, как отношения количества нейтрофилов, тромбоцитов и моноцитов к количеству лимфоцитов.
Начальные признаки атеросклероза — определялись по данным коронароангиографии наличием неровности контуров коронарных артерий. CASSC — количественная оценка степени поражения коронарных артерий оценивалась по классификации "Coronary Artery Surgery Study Class (CASSC)", по которой присваивается 1 балл за стеноз >70% в крупной коронарной артерии (передняя межжелудочковая нисходящая артерия, огибающая артерия, правая коронарная артерия) и 2 балла за стеноз левой основной (ствола) коронарной артерии >50%. Периферический атеросклероз — определялся по данным ультразвуковых методов диагностики периферических артерий (брахиоцефальных, артерий верхних и нижних конечностей) наличием атеросклеротических бляшек со степенью стеноза >30%. Группа пациентов с атеросклерозом — в данном исследовании определялась наличием атеросклеротического поражения любой степени выраженности и любой локализации. Данное определение включало в себя все вышеперечисленные состояния: начальные признаки атеросклероза и/или CASSC от 1 балла и выше и/или периферический атеросклероз, также ранее выполненное чрескожное коронарное вмешательство (ЧКВ).
Статистический анализ. Количественные параметры представлены в виде среднего и стандартного отклонения (M±SD) при нормальном распределении и в виде медианы и интерквартильного диапазона (Me (Q1; Q3)) при распределении, отличном от нормального. Для сравнения двух независимых выборок использовали параметрический T-критерий или непараметрический U-критерий Манна-Уитни для количественных переменных и критерий хи-квадрат Пирсона для категориальных переменных. Статистически значимым считалось различие между группами при p<0,05.
Для статистической поправки на исходные гендерные, возрастные и другие клинические различия был использован метод сопоставления оценок склонности (Propensity Score Matching (PSM)) в соотношении 1:1. Баллы склонности были рассчитаны для каждого пациента с использованием многомерной логистической регрессии, основанной на следующих ковариатах: возраст, пол, площадь поверхности тела, вес, диабет, фибрилляция предсердий, хроническая обструктивная болезнь легких, артериальная гипертония, курение. Статистический анализ проводился с помощью программ STATISTICA 10 (Statsoft, США), MedCalc (MedCalc Software Ltd, Бельгия). PSM был выполнен с помощью IBM SPSS® Statistics 28.0 (США).
Результаты
В исследование был включен 901 пациент среднего возраста 61±10 лет, из них 60% выборки составили мужчины (n=549). Пациенты были разделены на две группы: с атеросклерозом и без атеросклероза. В группу атеросклероза вошло 609 пациентов, без него — 292. После PSM были получены 2 группы по 251 человеку, для каждой из которых были рассчитаны показатели изучаемых индексов системного воспаления (табл. 1).
В группе пациентов с атеросклерозом все изучаемые нами показатели: SIRI, SII и AISI были статически значимо выше, чем у пациентов без атеросклероза: 0,906 (0,632; 1,36) vs 0,745 (0,519; 1,02), p<0,001; 457 (350; 641) vs 425 (313; 547), p=0,005 и 233 (148; 346) vs 179 (121; 263), p<0,001, соответственно (табл. 2). Кроме того, статистически значимые отличия наблюдались по уровням NLR и MLR. Не было отличий по уровню PLR: 112 (89,9; 142) у пациентов с атеросклерозом, vs 115 (89,8; 141) — у пациентов без атеросклероза, p=0,857 (табл. 2).
При проведении ROC-анализа были определены пороговые значения изучаемых показателей, которые составили: для SIRI >1,05 площадь под кривой (AUC), 95% доверительный интервал (ДИ) 0,615 (0,571-0,658), p<0,001, чувствительность 42,6%, специфичность 77,3%; для SII >368 AUC, 95% ДИ 0,572 (0,528-0,616), p=0,004, чувствительность 72,1%, специфичность 43,4% и AISI >248 AUC, 95% ДИ 0,604 (0,560-0,647), p<0,001, чувствительность 47,4%, специфичность 71,1% (рис. 1). При сравнении всех значимых ROC-кривых (для SIRI, SII, AISI, NLR и MLR) наибольшая AUC была для SIRI и чуть меньше для AISI (табл. 3, рис. 2).
Для сравнительной оценки уровней изучаемых биомаркеров системного воспаления у пациентов с различной выраженностью атеросклероза была проанализирована исходная когорта (n=901). Распределение в ней пациентов по степени CASSC было неоднородным, что логично. Пациенты с многососудистым поражением (с баллами 4 и 5 по CASSC) встречались крайне редко. Наибольшее число пациентов наблюдалось с баллами 0 и 1. При сравнении 6 групп (критерий Краскела-Уоллиса), с поправкой Бонферрони на количество групп, по уровням биомаркеров были обнаружены статистически значимые отличия только по SIRI и AISI, p<0,001 и p=0,002, соответственно. Однако эти различия не носили закономерности и визуально на графике выглядели хаотично (рис. 3).
Таблица 1
Сравнительная характеристика групп пациентов до PSM и после PSM
Параметры | До PSM | После PSM | ||||
С Аск (n=609) | Без Аск (n=292) | p | С Аск (n=251) | Без Аск (n=251) | p | |
Клинические данные | ||||||
Возраст, лет | 62±9,9 | 57±10 | <0,001* | 60±11 | 59±10 | 0,184 |
Муж. пол, % | 71 | 41 | <0,001* | 54 | 48 | 0,104 |
Площадь поверхности тела, м2 | 2,03 (1,9; 2,2) | 1,98 (1,8; 2,1) | <0,001* | 2,02 (1,86; 2,18) | 2,0 (1,83; 2,1) | 0,135 |
Вес, кг | 86 (76; 97) | 82 (72; 93) | <0,001* | 86 (75; 97) | 82 (73; 93) | 0,057 |
ИМТ, кг/м2 | 30 (26,4; 32,8) | 28,7 (26; 32,4) | 0,083 | 30,3 (27; 33) | 29 (26; 33) | 0,914 |
Перенесенный ИМ, % | 36 | 0 | <0,001* | 29 | 0 | <0,001* |
ЧКВ, % | 42 | 0 | <0,001* | 31 | 0 | <0,001* |
Диабет, % | 24 | 10 | <0,001* | 24 | 11 | 0,063 |
Фибрилляция предсердий, % | 22 | 33 | <0,001* | 29 | 31 | 0,643 |
ХОБЛ, % | 3 | 1 | 0,075 | 4 | 2 | 0,537 |
Артериальная гипертензия, % | 91 | 71 | <0,001* | 89 | 76 | 0,018* |
Инсульт/ТИА/ОНМК, % | 6 | 3 | 0,122 | 4 | 4 | 0,877 |
Курение, % | 28 | 15 | <0,001* | 25 | 17 | 0,089 |
Инструментальные данные | ||||||
ФВ ЛЖ, % | 59 (55; 63) | 63 (59; 65) | <0,001* | 59 (55; 63) | 62 (59; 65) | 0,017* |
КСР ЛЖ, мм | 34 (31; 37) | 32 (30; 35) | <0,001* | 33 (31; 36) | 32 (30; 35) | 0,084 |
КДР ЛЖ, мм | 50 (46; 53) | 48 (46; 52) | <0,001* | 49 (46; 53) | 48 (46; 52) | 0,106 |
КСО ЛЖ, мл | 47 (38; 58) | 41 (35; 51) | <0,001* | 44 (36; 56) | 41 (35; 51) | 0,034* |
КДО ЛЖ, мл | 118 (97; 135) | 108 (92; 130) | <0,001* | 112 (95; 132) | 108 (92; 130) | 0,126 |
Размер ЛП, см | 4,2 (3,9; 4,6) | 4,0 (3,6; 4,3) | <0,001* | 4,2 (3,9; 4,6) | 4,0 (3,6; 4,3) | 0,023* |
Медикаментозная терапия | ||||||
Бета-блокаторы, % | 71 | 53 | <0,001* | 73 | 54 | <0,001* |
Ингибиторы АПФ, % | 65 | 53 | <0,001* | 65 | 53 | 0,013* |
БКК, % | 30 | 15 | <0,001* | 30 | 15 | 0,002* |
Статины, % | 60 | 27 | <0,001* | 60 | 29 | <0,001* |
Аспирин, % | 56 | 24 | <0,001* | 47 | 26 | <0,001* |
Другие дезагреганты, % | 31 | 4 | <0,001* | 24 | 4 | <0,001* |
Тиазидные диуретики, % | 12 | 14 | 0,501 | 14 | 15 | 0,757 |
Петлевые диуретики, % | 13 | 4 | 0,032* | 15 | 5 | 0,044* |
Калийсберегающие диуретики, % | 16 | 8 | 0,047* | 18 | 8 | 0,054 |
Нитраты, % | 6 | 1 | 0,306 | 6 | 1 | 0,395 |
Примечание: * — статистически значимые отличия.
Сокращения: Аск — атеросклероз, АПФ — ангиотензинпревращающий фермент, БКК — блокаторы кальциевых каналов, ИМ — инфаркт миокарда, ИМТ — индекс массы тела, КДО — конечно-диастолический объем, КДР — конечно-диастолический размер, КСО — конечно-систолический объем, КСР — конечно-систолический размер, ЛЖ — левый желудочек, ЛП — левое предсердие, ОНМК — острое нарушение мозгового кровообращения, ТИА — транзиторная ишемическая атака, ФВ — фракция выброса, ХОБЛ — хроническая обструктивная болезнь легких, ЧКВ — чрескожное коронарное вмешательство, PSM — Propensity Score Matching.
Таблица 2
Сравнительная характеристика индексов системного воспаления
Параметры | С Аск (n=51) | Без Аск (n=251) | p |
SIRI | 0,906 (0,632; 1,36) | 0,745 (0,519; 1,02) | <0,001* |
SII | 457 (350; 641) | 425 (313; 547) | 0,005* |
AISI | 233 (148; 346) | 179 (121; 263) | <0,001* |
NLR | 1,86 (1,46; 2,37) | 1,68 (1,3; 2,05) | <0,001* |
PLR | 112 (89,9; 142) | 115 (89,8; 141) | 0,857 |
MLR | 0,222 (0,172; 0,281) | 0,201 (0,149; 0,265) | 0,002* |
Примечание: * — статистически значимые отличия.
Сокращения: Аск — атеросклероз, AISI — совокупный индекс системного воспаления (Aggregate Inflammation Systemic Index), MLR — отношение моноцитов к лимфоцитам, NLR — отношение нейтрофилов к лимфоцитам, PLR — отношение тромбоцитов к лимфоцитам, SII — индекс системного воспаления (Systemic Inflammation Index), SIRI — индекс системного воспалительного ответа (Systemic Inflammation Response Index).
Таблица 3
Результаты ROC-анализа определения пороговых значений уровней изучаемых индексов
Параметр | Пороговое значение | AUC | 95% ДИ | p |
SIRI | >1,04 | 0,615 | 0,571-0,658 | <0,0001* |
SII | >368,3 | 0,502 | 0,528-0,616 | 0,0046* |
AISI | >249 | 0,604 | 0,560-0,647 | <0,0001* |
NLR | >2,05 | 0,587 | 0,542-0,630 | <0,0006* |
PLR | ≤75 | 0,505 | 0,460-0,549 | 0,8574 |
MLR | >0,16 | 0,579 | 0,534-0,623 | 0,0019* |
Примечание: * — статистически значимые отличия.
Сокращения: ДИ — доверительный интервал, AUC — площадь под кривой, AISI — совокупный индекс системного воспаления (Aggregate Inflammation Systemic Index), MLR — отношение моноцитов к лимфоцитам, NLR — отношение нейтрофилов к лимфоцитам, PLR — отношение тромбоцитов к лимфоцитам, SII — индекс системного воспаления (Systemic Inflammation Index), SIRI — индекс системного воспалительного ответа (Systemic Inflammation Response Index).
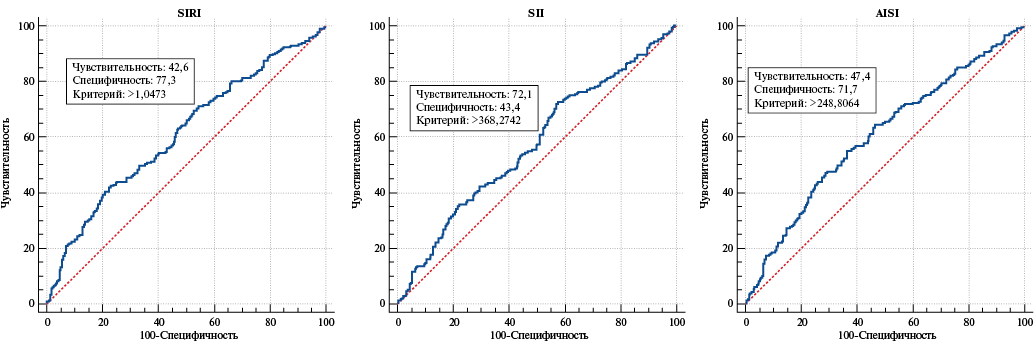
Рис. 1. ROC-кривые определения пороговых значений уровней изучаемых индексов (SIRI, SII, AISI).
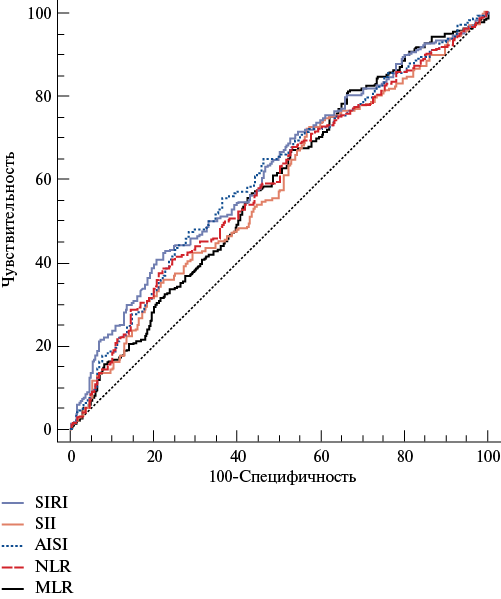
Рис. 2. ROC-кривые для SIRI, SII, AISI, NLR и MLR.
Примечание: цветное изображение доступно в электронной версии журнала.
Сокращения: AISI — совокупный индекс системного воспаления (Aggregate Inflammation Systemic Index), MLR — отношение моноцитов к лимфоцитам, NLR — отношение нейтрофилов к лимфоцитам, SII — индекс системного воспаления (Systemic Inflammation Index), SIRI — индекс системного воспалительного ответа (Systemic Inflammation Response Index).

Рис. 3. Сравнение пациентов по уровням биомаркеров в зависимости от степени поражения коронарного русла по классификации CASSC.
Сокращения: AISI — совокупный индекс системного воспаления (Aggregate Inflammation Systemic Index), CASSC — классификация степени поражения коронарных артерий (Coronary Artery Surgery Study Class), SII — индекс системного воспаления (Systemic Inflammation Index), SIRI — индекс системного воспалительного ответа (Systemic Inflammation Response Index).
Обсуждение
Проведенные ранее когортные исследования показали, что лейкоциты крови и их подтипы (в т. ч. нейтрофилы, моноциты, лимфоциты), были связаны с повышенным риском развития ИБС, инсульта и смертности от всех причин, являясь при этом недорогим и простым в исполнении анализом. Показатели, основанные на лейкоцитарной формуле, такие как NLR, PLR и MLR, широко изучались ранее и продолжают изучаться в качестве индексов хронического воспаления. Их прогностическая ценность в отношении смертности от всех причин и смертности от ССЗ оказалась выше, чем оценка воспаления, основанная на абсолютном уровне лейкоцитов [10][11].
Изучаемые нами так называемые новые биомаркеры воспаления (SII, SIRI и AISI), являются по сути модифицированными индексами, на основе тех же лейкоцитарных подтипов клеток. Оценка их роли в патогенезе заболеваний в мировой литературе появилась совсем недавно и пока не накоплено достаточно данных. Тем не менее несколько исследований продемонстрировали потенциальный интерес к ним. Например, было выявлено, что они более точно предсказывают неблагоприятный прогноз у пациентов с колоректальным раком и раком пищевода по сравнению с NLR, PLR и MLR [6][7].
В нашем исследовании было проведено сравнение уровня новых маркеров системного воспаления (SIRI, SII, AISI) в зависимости от наличия или отсутствия подтверждённых данных об атеросклерозе артерий любой локализации. Набранная когорта исходно была достаточно гетерогенна и группы статистически отличались между собой по возрасту, гендерным и важным клиническим характеристикам. После статистической поправки методом Propensity Score Matching в соотношении 1:1, эти различия были нивелированы и в итоговый анализ вошло по 502 пациента (по 251 пациенту в каждую группу). При сравнении было получено, что все три новых индекса системного воспаления (SIRI, SII и AISI) статистически значимо были выше у пациентов с атеросклерозом коронарных и периферических артерий, чем у пациентов без него.
В мировой литературе представлено всего несколько схожих работ, оценивающих роль этих новых индексов воспаления у пациентов с ИБС и сердечно-сосудистой патологией в целом, результаты которых схожи с результатами нашего исследования.
Yang Y-L, et al. предоставили данные, показывающие, что более высокие показатели SII (≥694,3) были независимо связаны с большими кардиальными событиями: смерть, тромбоз стента, повторная реваскуляризация, госпитализация по поводу острого коронарного синдрома. Показатель SII лучше прогнозировал основные ССЗ, чем традиционные факторы риска у пациентов с ИБС после коронарного вмешательства [12].
Li Q, et al. (2022) изучали пациентов с острым коронарным синдромом, которые перенесли ЧКВ. Авторы оценили прогностическое значение 5 индексов воспаления (PLR, NLR, MLR, SII и SIRI) на развитие больших кардиальных событий (MACE). Многофакторный анализ Кокса показал, что все 5 индексов были независимыми предикторами развития MACE, а SIRI показал лучшие результаты (отношение шансов (ОШ): 3,847 при 95% ДИ: 2,623-5,641, p<0,001). Добавление NLR, MLR, SII или SIRI к шкале риска Глобального регистра острых коронарных событий (GRACE), особенно SIRI, превзошел показатель риска GRACE в прогнозировании риска. Таким образом, авторы сделали заключение, что новые воспалительные индексы на основе лейкоцитов независимо связаны с риском развития MACE у пациентов, перенесших ЧКВ, а индекс SIRI показал наилучшую прогностическую значимость в качестве предиктора MACE: в комбинации со шкалой GRACE он может более точно предсказать серьезные неблагоприятные сердечно-сосудистые события [13].
Крупное ретроспективное исследование Xia Y, et al. (2023), в которое было включено 42875 человек, со сроком наблюдения 20 лет, показало, что пациенты с уровнем SII >655,56 имели более высокую смертность от всех причин (ОШ: 1,29 при 95% ДИ: 1,18-1,41) и смертность от ССЗ (ОШ: 1,33 при 95% ДИ: 1,11-1,59), чем пациенты с уровнем SII <335,36. Пациенты с уровнем SIRI >1,43 имели более высокий риск смерти от всех причин (ОШ: 1,39 при 95% ДИ: 1,26-1,52) и смерти от ССЗ (ОШ: 1,39; 95% ДИ: 1,14-1,68), чем пациенты с уровнем SIRI <0,68. В общей популяции лиц старше 60 лет, повышение SII или SIRI было связано с риском смерти от всех причин [14].
В нашем исследовании пороговый уровень, который статистически значимо ассоциировался с наличием атеросклероза, для SIRI был >1,05; для SII >368 и для AISI >248. Данные цифры схожи с теми, что получил Xia Y, et al., в общей популяции, и ниже, чем пороговые значения, в двух других исследованиях (Yang Y-L, et al.; Li Q, et al.). Это вполне логично, поскольку в нашей работе были пациенты как с ИБС, так и "условно здоровые", что делало нашу когорту эквивалентом общей популяции, но с меньшей статистической мощностью. Внутри когорты пациентов с ИБС, уровни новых маркеров воспаления, вероятно, прямо коррелируют с тяжестью заболевания, поэтому независимыми предикторами развития MACE являются уже уровни выше тех, что были получены нами в данном исследовании.
Что касается наших данных, полученных при сравнении уровней биомаркеров между группами с различной выраженностью атеросклероза (CASSC 0-5), то эти данные не согласуются с результатами исследования Dziedzic EA, et al. [15], в котором авторы получили наиболее высокие значения SII и SIRI у пациентов с трехсосудистым поражением коронарных артерий, т. е. у пациентов с CASSC 3 и более балла по сравнению с пациентами с CASSC 0-2 балла. На наш взгляд, эти результаты обусловлены большой гетерогенностью в численности пациентов по группам (рис. 3). Из рисунка видно, что пациентов с CASSC 0, например, было 597 человек, а с CASSC 5 всего 8 человек, из общей когорты в 901 пациента. Вероятно, полученные результаты обусловливаются мощными погрешностями в анализе данных. Поэтому какие-либо умозаключения про наличие или отсутствие ассоциаций между уровнями биомаркеров с выраженностью атеросклероза делать рано. Требуются дополнительные исследования с большей выборкой данных.
Ограничения исследования. Данная работа, на наш взгляд, имеет некоторые непринципиальные ограничения, которые присущи всем исследованиям с ретроспективным подходом. Во-первых, все данные были собраны из общей электронной базы данных нашей клиники "Medwork" со стандартным вводом данных, это не исключает частичной потери данных. Во-вторых, хотя для статистической поправки был использован метод Propensity Score Matching, некоторые клинические параметры оставались отличающимися между группами. Нужно понимать, что данный метод не является заменой рандомизации, а лишь одним из возможных инструментов, чтобы уравновесить группы, сделав их более гомогенными. В рекомендациях по использованию метода также подчеркивается, что важно ограничиваться незначительным набором ковариат, по которым будем выполнено сопоставление.
Заключение
Новые маркеры системного воспаления: SIRI, SII и AISI были статистически значимо выше у пациентов с подтвержденным атеросклерозом, чем у пациентов без него. Пороговые уровни, ассоциированные с атеросклерозом, были: для SIRI >1,05, для SII >368, для AISI >248. Данные индексы рассчитываются на основе клинического анализа крови с развернутой лейкоцитарной формулой, являясь доступными в рутинной практике. Необходимо дальнейшее изучение данных биомаркеров для оценки их прогностической значимости в развитии и течении ССЗ.
Отношения и деятельность: все авторы заявляют об отсутствии потенциального конфликта интересов, требующего раскрытия в данной статье.
Список литературы
1. Драпкина О. М., Бубнова М. Г., Самородская И. В. и др. Динамика показателей смертности от острых форм ишемической болезни сердца в Российской Федерации за период с 2015 по 2019 годы. Российский кардиологический журнал. 2021;26(5):4441. doi:10.15829/1560-4071-2021-4441.
2. Булаева Н. И., Голухова Е. З. Эндотелиальная дисфункция и оксидативный стресс: роль в развитии кардиоваскулярной патологии. Креативная кардиология. 2013;1:14-22.
3. Ежов М. В., Кухарчук В. В., Сергиенко И. В. и др. Нарушения липидного обмена. Клинические рекомендации 2023. Российский кардиологический журнал. 2023;28(5):5471. doi:10.15829/1560-4071-2023-5471.
4. Weber C, Noels H. Atherosclerosis: current pathogenesis and therapeutic options. Nat Med. 2011;17(11):1410-22. doi:10.1038/nm.2538.
5. Москаленко С. А., Шувалова Ю. А., Каминный А. И. Роль системы интерлейкина-6 в развитии атеросклероза. Атеросклероз и дислипидемии. 2020;2(39):5-11. doi:10.34687/2219-8202.JAD.2020.02.0001.
6. Qi Q, Zhuang L, Shen Y, et al. A novel systemic inflammation response index (SIRI) for predicting the survival of patients with pancreatic cancer after chemotherapy. Cancer. 2016;122(14):2158-67. doi:10.1002/cncr.3005.
7. Geng Y, Zhu D, Wu C, et al. A novel systemic inflammation response index (SIRI) for predicting postoperative survival of patients with esophageal squamous cell carcinoma. Int Immunopharmacol. 2018;65:503-10. doi:10.1016/j.intimp.2018.10.002.
8. Li J, He D, Yu J, et al. Dynamic Status of SII and SIRI Alters the Risk of Cardiovascular Diseases: Evidence from Kailuan Cohort Study. J Inflamm Res. 2022;15:5945-57. doi:10.2147/JIR.S378309.
9. Jin Z, Wu Q, Chen S, et al. The Associations of Two Novel Inflammation Indexes, SII and SIRI with the Risks for Cardiovascular Diseases and All-Cause Mortality: A Ten-Year Follow-Up Study in 85,154 Individuals. J Inflamm Res. 2021;14:131-40. doi:10.2147/JIR.S283835.
10. Wheeler JG, Mussolino ME, Gillum RF, et al. Associations between differential leucocyte count and incident coronary heart disease: 1764 incident cases from seven prospective studies of 30,374 individuals. Eur Heart J. 2004;25(15):1287-92. doi:10.1016/j.ehj.2004.05.002.
11. Joshi A, Bhambhani A, Barure R, et al. Neutrophil-lymphocyte ratio and platelet-lymphocyte ratio as markers of stable ischemic heart disease in diabetic patients: An observational study. Medicine. 2023;102(5):e32735. doi:10.1097/MD.0000000000032735.
12. Yang YL, Wu CH, Hsu PF, et al. Systemic immune-inflammation index (SII) predicted clinical outcome in patients with coronary artery disease. Eur J Clin Invest. 2020;50(5):e13230. doi:10.1111/eci.13230.
13. Li Q, Ma X, Shao Q, et al. Prognostic Impact of Multiple Lymphocyte-Based Inflammatory Indices in Acute Coronary Syndrome Patients. Front Cardiovasc Med. 2022;9:811790. doi:10.3389/fcvm.2022.811790.
14. Xia Y, Xia C, Wu L, et al. Systemic Immune Inflammation Index (SII), System Inflammation Response Index (SIRI) and Risk of All-Cause Mortality and Cardiovascular Mortality: A 20-Year Follow-Up Cohort Study of 42,875 US Adults. J Clin Med. 2023;12(3):1128. doi:10.3390/jcm12031128.
15. Dziedzic EA, Gąsior JS, Tuzimek A, et al. Investigation of the Associations of Novel Inflammatory Biomarkers-Systemic Inflammatory Index (SII) and Systemic Inflammatory Response Index (SIRI)-With the Severity of Coronary Artery Disease and Acute Coronary Syndrome Occurrence. Int J Mol Sci. 2022;23(17):9553. doi:10.3390/ijms23179553.
Об авторах
В. А. ШварцРоссия
Шварц Владимир Александрович — д. м. н., в. н. с. отделения хирургического лечения интерактивной патологии, профессор кафедры сердечно-сосудистой хирургии с курсом аритмологии и клинической электрофизиологии.
Москва
Конфликт интересов:
Нет
С. М. Талибова
Россия
Талибова Саялы М. — аспирант, врач-кардиолог.
Москва
Конфликт интересов:
Нет
М. А. Сокольская
Россия
Сокольская Мария А. — к. м. н., н. с. отделения хирургического лечения интерактивной патологии, доцент кафедры кардиологии, функциональной и ультразвуковой диагностики с курсом детской кардиологии.
Москва
Конфликт интересов:
Нет
А. Ю. Испирян
Россия
Испирян Артак Ю. — к. м. н., с. н. с. отделения хирургического лечения интерактивной патологии, кардиолог.
Москва
Конфликт интересов:
Нет
Е. Н. Шварц
Россия
Шварц Елена Н. — м. н. с. центра координации фундаментальной научной деятельности.
Москва
Конфликт интересов:
Нет
А. Д. Петросян
Россия
Петросян Андрей Д. — к. м. н., сердечно-сосудистый хирург.
Москва
Конфликт интересов:
Нет
В. Ю. Мерзляков
Россия
Мерзляков Вадим Ю. — д. м. н., зав. отделением хирургического лечения ИБС и малоинвазивной коронарной хирургии, профессор кафедры сердечно-сосудистой хирургии с курсом аритмологии и клинической электрофизиологии.
Москва
Конфликт интересов:
Нет
А. И. Скопин
Россия
Скопин Антон И. — к. м. н., сердечно-сосудистый хирург отделения хирургического лечения ИБС и малоинвазивной коронарной хирургии.
Москва
Конфликт интересов:
Нет
С. А. Донаканян
Россия
Донаканян Сергей А. — д. м. н., зав. отделением хирургического лечения интерактивной патологии, профессор кафедры сердечно-сосудистой хирургии с курсом аритмологии и клинической электрофизиологии, сердечно-сосудистый хирург.
Москва
Конфликт интересов:
Нет
Дополнительные файлы
Что уже известно о предмете исследования?
- Описанные недавно так называемые новые биомаркеры воспаления, основанные на количестве лейкоцитов крови и их подтипов: индекс системного воспаления, индекс системного воспалительного ответа и совокупный индекс системного воспаления, — потенциально демонстрируют важную роль в течении сердечно-сосудистых заболеваний.
Что нового?
- Данные новые маркеры системного воспаления статистически значимо выше у пациентов с подтвержденным атеросклерозом, чем у пациентов без него.
Возможный вклад в клиническую практику
- Новые маркеры воспаления являются простым в исполнении и финансово доступным в рутинной клинической практике методом определения хронического воспалительного статуса у пациентов с ишемической болезнью сердца.
Рецензия
Для цитирования:
Шварц В.А., Талибова С.М., Сокольская М.А., Испирян А.Ю., Шварц Е.Н., Петросян А.Д., Мерзляков В.Ю., Скопин А.И., Донаканян С.А. Ассоциация новых биомаркеров системного воспаления с развитием атеросклероза и его выраженностью. Российский кардиологический журнал. 2024;29(8):6025. https://doi.org/10.15829/1560-4071-2024-6025. EDN: FIDYSH
For citation:
Shvarts V.A., Talibova S.M., Sokolskaya M.A., Ispiryan A.Yu., Shvarts E.N., Petrosyan A.D., Merzlyakov V.Yu., Skopin A.I., Donakanyan S.A. Association of novel biomarkers of systemic inflammation with atherosclerosis and its severity. Russian Journal of Cardiology. 2024;29(8):6025. (In Russ.) https://doi.org/10.15829/1560-4071-2024-6025. EDN: FIDYSH
JATS XML

















































