Перейти к:
Сравнительный анализ мониторинга гемодинамики с помощью катетеризации легочной артерии и трансторакальной эхокардиографии у пациентов с кардиогенным шокомхокардиографии у пациентов с кардиогенным шоком
https://doi.org/10.15829/1560-4071-2024-5990
EDN: SOJKZQ
Аннотация
Цель. Сравнить основные показатели центральной гемодинамики, снятые путем катетеризации легочной артерии и с помощью трансторакальной эхокардиографии (ТЭхоКГ).
Материал и методы. Выполнено проспективное исследование с участием 20 пациентов с острым инфарктом миокарда, осложненным истинным кардиогенным шоком. Всем пациентам практически синхронно выполнялось измерение ряда показателей центральной гемодинамики с помощью катетера Свана-Ганца и тех же показателей с помощью ТЭхоКГ. Сравнение обеих методик проводилось путем корреляционного анализа Спирмена и построения диаграмм Бланда-Альтмана с помощью программы STATISTICA 8.0.
Результаты. Нами обнаружено довольно много согласованностей между показателями, снятыми двумя методиками у одного и того же пациента примерно в одно и то же время. Так, сердечный индекс (СИ) хорошо измеряется обеими методиками. При этом корреляционный коэффициент был значимо выше при измерении СИ посредством VTI (r=0,81 vs r=0,81) по сравнению с расчетом СИ через объемы ЛЖ, поэтому мы считаем первый способ предпочтительным. Значения общего периферического сосудистого сопротивления (ОПСС), высчитанные по давлению в правом предсердии, не выявили согласования методик, в то же время, высчитанные по центральному венозному давлению — выявили. Не показало согласованности методик измерение давления заклинивания легочной артерии. Мы считаем, что это связано с тем, что оценка диастолической функции, через которую впоследствии производится расчет, у реанимационных пациентов в режиме фокусного ТЭхоКГ может быть затруднена и недостаточно корректна.
Заключение. ТЭхоКГ можно применять для мониторинга центральной гемодинамики в случаях удовлетворительной и умеренно сниженной визуализации изображений сердца. Статистически согласованными являются как результаты измерений СИ с помощью формулы Бернулли, так и СИ, рассчитанного, исходя из разницы объемов левого желудочка, а также измерение ОПСС с помощью центрального венозного давления. Измерение ОПСС с помощью давления в правом предсердии и измерение давления заклинивания легочной артерии не продемонстрировали согласованности разных методик. Мы считаем, что ТЭхоКГ можно использовать для мониторирования СИ и ОПСС у пациентов с инфарктом миокарда, осложненным истинным кардиогенным шоком.
Для цитирования:
Рябов В.В., Сыркина А.Г., Керчева М.А., Ёлгин И.И., Пантелеев О.О. Сравнительный анализ мониторинга гемодинамики с помощью катетеризации легочной артерии и трансторакальной эхокардиографии у пациентов с кардиогенным шокомхокардиографии у пациентов с кардиогенным шоком. Российский кардиологический журнал. 2024;29(7):5990. https://doi.org/10.15829/1560-4071-2024-5990. EDN: SOJKZQ
For citation:
Ryabov V.V., Syrkina A.G., Kercheva M.A., Yolgin I.I., Panteleev O.O. Comparative analysis of hemodynamic monitoring with pulmonary artery catheter and transthoracic echocardiography in patients with cardiogenic shock. Russian Journal of Cardiology. 2024;29(7):5990. (In Russ.) https://doi.org/10.15829/1560-4071-2024-5990. EDN: SOJKZQ
Кардиогенный шок (КШ) — одно из самых тяжелых осложнений инфаркта миокарда (ИМ), приводящее к высокой летальности, усугубляющее течение коморбидных заболеваний, отрицательно влияющее на ближайший и отдаленный прогноз. Несмотря на все усилия, последнее время летальность от КШ колеблется в пределах 30-50% без тенденции к дальнейшему снижению [1]. Таким образом, существует необходимость поиска новых подходов к диагностике и терапии данного состояния.
Понимание гемодинамических механизмов возникновения и течения КШ — ключ к адекватной и эффективной его терапии. Особенно это актуально при сочетании шоков разного генеза у одного и того же пациента. Так, у пациентов с истинным КШ нередко присоединяется септический шок, в ряде случаев — геморрагический. В этих ситуациях особенно актуальным становится мониторирование основных параметров центральной гемодинамики.
Практически любой вид шока инициируется интенсивным и достаточно резким снижением сердечного выброса (СВ). Оценка данного показателя в сочетании с преднагрузкой и постнагрузкой позволяет дифференцировать основные варианты острого расстройства циркуляции — гиповолемический, вазоплегический и кардиогенный; в последнем случае ведущий механизм связан со снижением сократительной функции левого желудочка (ЛЖ) [2].
СВ как один из основных признаков шока и критериев эффективности его лечения является интегральным показателем, в основе которого лежит нарушение структуры и функции ЛЖ. Кроме этого параметра патогенетическая составляющая шока лежит в плоскости значений общего периферического сосудистого сопротивления (ОПСС), давления заклинивания легочной артерии (ДЗЛА) и волемического статуса [3][4]. Грамотное лечение конкретного пациента предполагает снятие абсолютных значений этих показателей в текущий момент времени, вследствие чего назначение препаратов становится более очевидным и обоснованным.
Существует множество способов мониторирования центральной гемодинамики (МЦГ), однако до сих пор нет четких рекомендаций по использованию той или иной методики, в частности, при КШ [5].
Золотой стандарт МЦГ в виде катетеризации легочной артерии (ЛА) по методу Свана-Ганца уже давно используется в практике, однако имеет ряд неудобств, в т. ч. для пациента, поскольку является инвазивной процедурой. С развитием в последние годы эхокардиографии в целом и с появлением такого понятия как фокусная эхокардиография, данный подход стал чрезвычайно востребованным в условиях палаты интенсивной терапии, где решения нужно принимать быстро, и где они могут часто меняться [6].
На практике достаточно основных показателей центральной гемодинамики для быстрого и верного принятия того или иного решения. В то же время количество исследований по этой проблеме недостаточно [7].
Альтернативный подход к МЦГ с помощью трансторакальной эхокардиографии (ТЭхоКГ) целесообразен и оправдан, удобен для пациента, является неинвазивным, не обладает минусами, которые есть у методики Свана-Ганца [8].
Однако в настоящее время нет однозначного мнения, может ли МЦГ с помощью ТЭхоКГ стать заменой аналогичным измерениям при катетеризации ЛА.
Цель: сравнить основные показатели центральной гемодинамики, снятые путем катетеризации ЛА и с помощью ТЭхоКГ.
Гипотеза. Метод ТЭхоКГ для определения СВ, ОПСС и ДЗЛА не хуже, чем методика Свана-Ганца для этих же целей.
Материал и методы
В исследование включено 20 пациентов с острым ИМ, осложненным истинным КШ, согласно четвертому универсальному определению ИМ и клинико-лабораторным общепринятым критериям КШ [9][10].
Исследование было одобрено комитетом по биомедицинской этике при НИИ кардиологии Томского НИМЦ (протокол заседания № 190 от 13.11.2019). У всех пациентов было подписано информированное согласие, предусматривающее, что пациент не в состоянии самостоятельно подписать данную форму, поскольку практически каждый из них на момент включения в исследование находился в бессознательном состоянии. В данной ситуации подписание документа проводилось двумя незаинтересованными лицами из врачебного персонала реанимации.
Критерии включения:
- Возраст более 18 лет;
- Наличие КШ согласно общепринятым клиническим и лабораторным критериям.
Критерии исключения:
- Постоянная форма фибрилляции предсердий;
- Выраженный аортальный стеноз;
- Регургитация 2-4 степени на аортальном и/или митральном клапанах;
- Активное большое кровотечение;
- Механические осложнения острого ИМ;
- Противопоказания к установке катетера Свана-Ганца.
Всем пациентам практически синхронно выполнялось измерение ряда показателей центральной гемодинамики (табл. 1) с помощью катетера Свана-Ганца и тех же показателей с помощью ТЭхоКГ.
Катетеризация ЛА проводилась в рамках рутинной практики [11][12]. В асептических условиях под местной инфильтративной анестезией в просвет правой внутренней ярёмной вены при помощи ультразвуковой навигации по методике Сельдингера устанавливался интродьюсер 8 Fr. После фиксации интродьюсера к коже одиночной лигатурой, через просвет интродьюсера в верхнюю полую вену вводили баллонный катетер для термодилюции Corodyn TD, Brаun (Германия) (далее катетер Свана-Ганца) и раздували баллон на дистальном конце катетера. Катетер продвигали далее — в полость правого предсердия (ПП), правого желудочка и лёгочный ствол под контролем изменения кривой давления. Далее катетер продвигали дистально, по ходу ветвей ЛА, до появления на мониторе кривой с характерным для заклинивания ЛА паттерном. Положение баллона в позиции "заклинивания" верифицировали повторными дефляцией и инфляцией баллона, и промыванием порта инвазивного давления.
После верификации заклинивания ЛА баллон повторно раздували, прекращали вентиляцию лёгких и выполняли измерение ДЗЛА. После измерения ДЗЛА баллон сдували. Полученный результат сохраняли в мониторе для дальнейших расчётов.
Измерение СВ выполняли при помощи метода препульмональной термодилюции: через термистор, в проксимальный порт катетера Свана-Ганца вводили стандартный объём предварительно охлаждённого до 4 С изотонического раствора хлорида натрия и регистрировали динамику изменения температуры на дистальном конце катетера. Процедуру повторяли 5 раз, сохраняя в монитор полученное среднее значение.
После введения данных о поле, возрасте, росте и массе тела пациента, монитор Drager Infinity Delta (Германия) производил расчёты параметров гемодинамики пациента.
Попутно всем пациентам выполнялась ТЭхоКГ с использованием мобильного эхокардиографа Philips Affiniti 70 (Нидерланды). При исследовании осуществляли измерение структурных и допплерографических параметров сердца по общепринятой методике, из стандартных позиций (парастернальная по длинной и по короткой оси ЛЖ, апикальная 5-, 4- и 2-камерная, субкостальная) в В-режиме. В части случаев (4 пациента) визуализация оценена как неудовлетворительная или ближе к таковой, впоследствии эти пациенты были исключены из расчетов.
Для характеристики геометрической формы ЛЖ использовали следующие показатели: конечный диастолический объем (КДО), конечный систолический объем (КСО) рассчитывали в В-режиме из 4-камерной позиции. Глобальная систолическая функция оценивалась по уравнению Симпсона в В-режиме.
Ударный объем ЛЖ рассчитывался двумя способами. Во-первых, по разнице между КДО и КСО, далее СВ рассчитывали как:
УО*ЧСС/1000,
где УО — ударный объем ЛЖ, ЧСС — частота сердечных сокращений.
Во-вторых, по значению VTI в выводном отделе ЛЖ (ВОЛЖ) с учетом его диаметра по формуле:
VTI ВОЛЖ*площадь ВОЛЖ,
где ВОЛЖ — выводной отдел ЛЖ.
Затем проводилась индексация показателей к площади поверхности тела и получалась конечная искомая цифра — сердечный индекс (СИ), исходя из значения которой принимались решения по терапии и прогнозу.
Для расчета ДЗЛА необходимо было оценить диастолическую функцию по отношению скоростей раннего наполнения ЛЖ и скорости раннего диастолического движения латеральной и медиальной части фиброзного кольца митрального клапана (Е/Е'), с дальнейшим расчетом среднего арифметического.
Уровень ДЗЛА рассчитывался по формуле:
1,24*(Е/Е' среднее)+1,9.
Для расчета ОПСС использовались две методики: 1) по эмпирическому уровню давления в ПП с градацией от 5 до 20 мм рт.ст. в зависимости от реакции нижней полой вены, степени трикуспидальной регургитации и размеров ПП; 2) исходя из значений центрального венозного давления (ЦВД), измеренного через центральный венозный катетер в см водного столба.
В первом случае формула выглядит так:
ОПСС=(80*(среднее АД—давление в ПП))/СВ.
Во втором случае так:
ОПСС=(80*(среднее АД—ЦВД в мм рт.ст.))/СВ,
где АД — артериальное давление.
Референсными значениями считались 900-1300
дин*с*см-5.
Формула перевода значений ЦВД из водного столба в ртутный была следующей:
0,74*ЦВД в мм вод.ст.
Полученные данные сформировали электронную базу данных.
Сравнение обеих методик проводилось с помощью корреляционного анализа Спирмена и построения диаграммы Бланда-Альтмана с помощью программы STATISTICA 8.0. При этом для оценки уровня систематических отклонений анализировалась разница между двумя измерениями, также сравнивались стандартные отклонения разностей измерений с величиной самого показателя и оценивалось отсутствие/наличие зависимости разности измерений от величины оцениваемого показателя. Хороший уровень воспроизводимости констатировали тогда, когда разности значений двух измерений попадали в зону ±1,96 стандартного отклонения средней разности измеренного показателя либо выходили из нее не чаще чем в 4% случаев.
Данное исследование (дизайн, сбор информации, анализ, интерпретация данных и т. д.) выполнялось в рамках Государственного задания на оказание государственных услуг (выполнение работ) № 075-00712-24-04 от 02.04.2024, лаборатория инфаркт-ассоциированного шока.
Результаты
В общей сложности нами было выполнено 20 катетеризаций ЛА без осложнений и технических трудностей. Чаще всего измерения показателей центральной гемодинамики проводились 1 раз в сутки. У разных пациентов было выполнено от 1 до 4 измерений; чаще всего единственное измерение было связано с гибелью больного ко 2-м суткам исследования. Чаще всего каждому из пациентов выполнялось по 3 измерения. Окончательному анализу подверглось 61 параллельное измерение.
Далее мы провели корреляционный анализ с помощью критерия Спирмена среди одних и тех же показателей, снятых обеими методиками (табл. 2, 3).
Получена статистически значимая корреляция для всех сравниваемых параметров. Наиболее высокое значение коэффициента корреляции было получено для ударного объема, СВ, СИ, измеренных с помощью VTI, для обоих способов измерения ОПСС, что говорит о тесной линейной связи, однако для оценки согласованности этого недостаточно. Наиболее слабая корреляционная связь получена для ДЗЛА. Ниже с целью определения согласованности обеих методик приведены диаграммы Бланда-Альтмана по основным параметрам (рис. 1-5).
Таблица 1
Прямые и расчетные показатели центральной гемодинамики, полученные с помощью катетера Свана-Ганца и с помощью ТЭхоКГ
Параметры |
Центральное венозное давление |
Ударный объем |
Сердечный выброс |
Сердечный индекс |
Общее периферическое сосудистое сопротивление |
Давление заклинивания легочной артерии |
Таблица 2
Корреляция между двумя способами измерения СИ
Параметры | УО, расчет из объемов ЛЖ | МОК, расчет из объемов ЛЖ | СИ, расчет из объемов ЛЖ | УО, расчет по VTI | МОК расчет по VTI | СИ расчет по VTI |
УО | r=0,48 | r=0,05 | r=-0,04 | r=0,83 | r=0,54 | r=0,49 |
МОК | r=0,34 | r=0,46 | r=0,34 | r=0,67 | r=0,81 | r=0,73 |
СИ | r=0,28 | r=0,37 | r=0,33 | r=0,65 | r=0,81 | r=0,81 |
Примечание: строка легенды — показатели гемодинамики, полученные ТЭхоКГ; столбец легенды — показатели гемодинамики, полученные катетером Свана-Ганца. Цветом выделены статистически значимые коэффициенты корреляции.
Сокращения: ЛЖ — левый желудочек, МОК — минутный объем кровообращения, СИ — сердечный индекс, ТЭхоКГ — трансторакальная эхокардиография, УО — ударный объем.
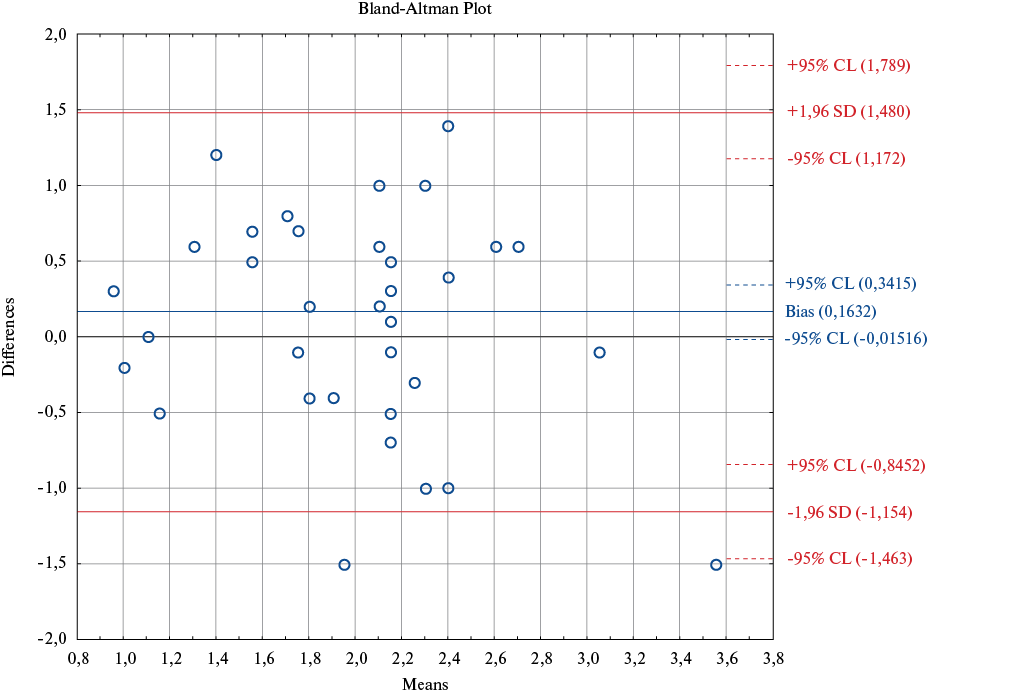
Рис. 1. Сравнение СИ, измеренного с помощью ТЭхоКГ, исходя из объемов ЛЖ, против катетера Свана-Ганца.
Таблица 3
Корреляция между разными способами измерения ДЗЛА, ОПСС, ЦВД
Параметры | ДЗЛА | ЦВД | ОПСС, расчет из давления в ПП | ОПСС, расчет из уровня ЦВД |
ДЗЛА | r=0,27 | r=0,07 | r=0,30 | r=0,14 |
ЦВД | r=0,18 | r=0,40 | r=0,40 | r=0,31 |
ОПСС | r=-0,32 | r=-0,35 | r=0,67 | r=0,70 |
Примечание: строка легенды — показатели гемодинамики, полученные ТЭхоКГ и ЦВД, измеренного через центральный венозный катетер; столбец легенды — показатели гемодинамики, полученные катетером Свана-Ганца. Цветом выделены статистически значимые коэффициенты корреляции.
Сокращения: ДЗЛА — давление заклинивания легочной артерии, ОПСС — общее периферическое сосудистое сопротивление, ПП — правое предсердие, ТЭхоКГ — трансторакальная эхокардиография, ЦВД — центральное венозное давление.
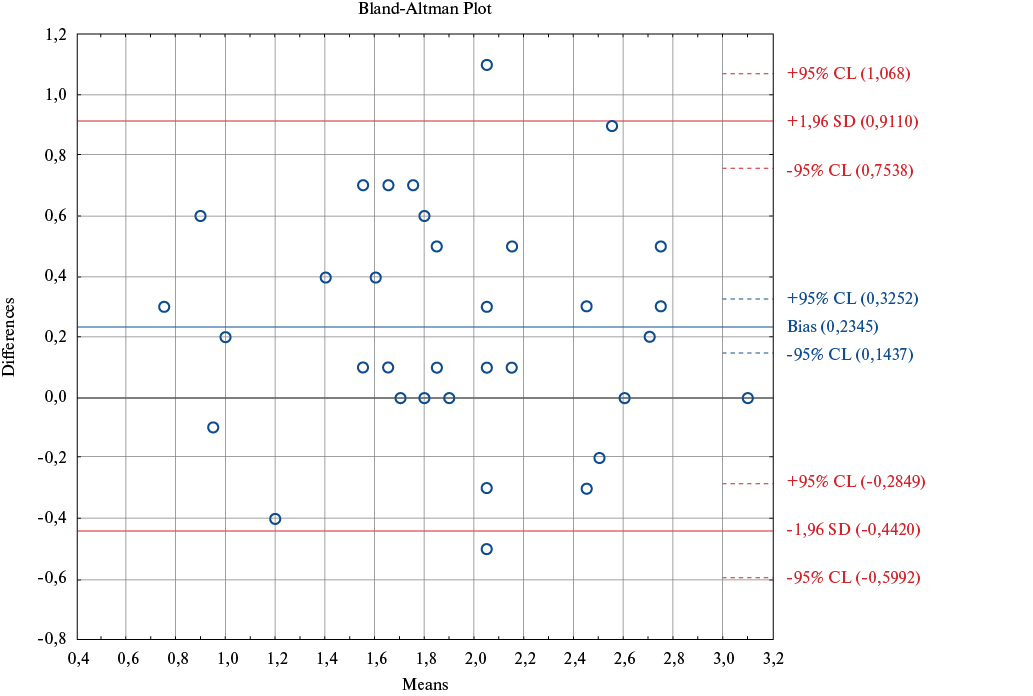
Рис. 2. Сравнение СИ, измеренного с помощью ТЭхоКГ, исходя из VTI ВОЛЖ, против катетера Свана-Ганца.
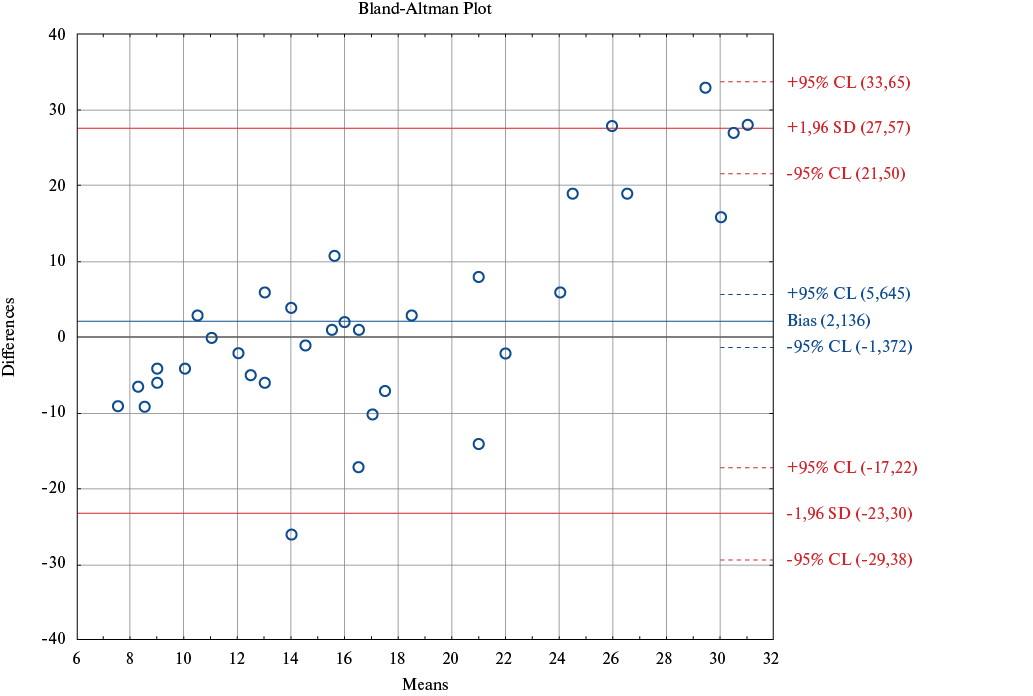
Рис. 3. Сравнение ДЗЛА, измеренного с помощью ТЭхоКГ, против катетера Свана-Ганца.
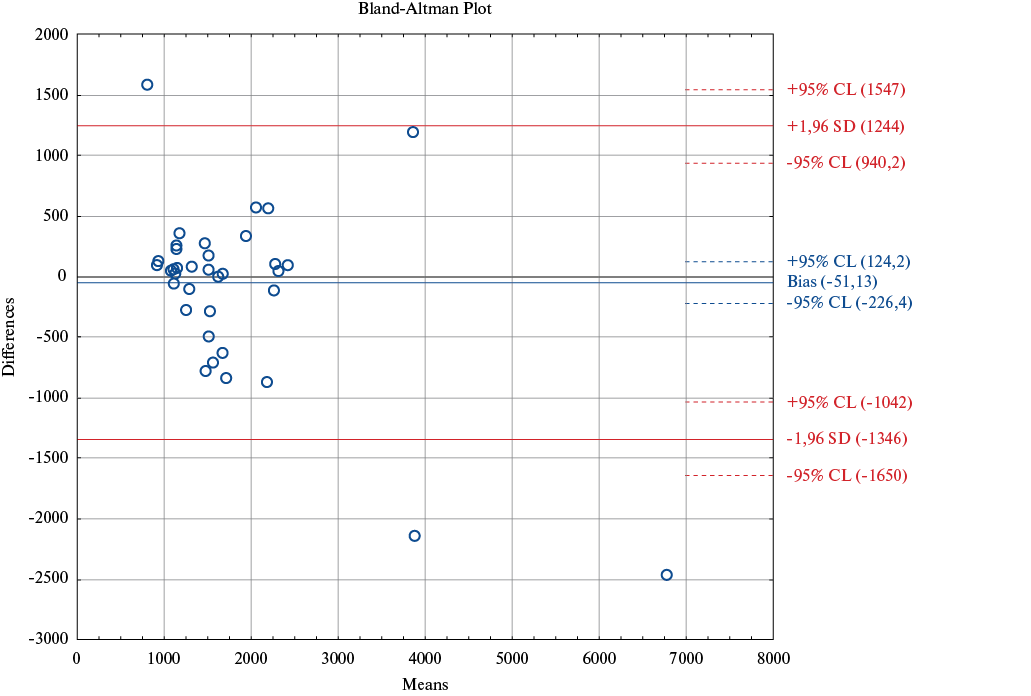
Рис. 4. Сравнение ОПСС, измеренного с помощью ТЭхоКГ по давлению в ПП, против катетера Свана-Ганца.
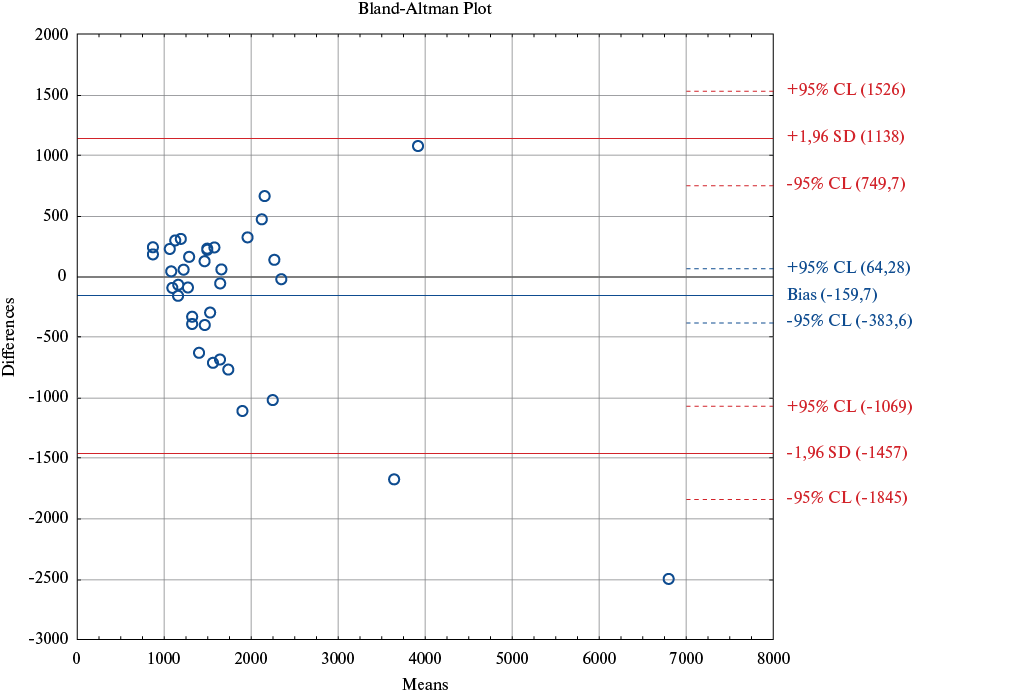
Рис. 5. Сравнение ОПСС, измеренного с помощью ТЭхоКГ по уровню ЦВД, против катетера Свана-Ганца.
Обсуждение
В целом нами обнаружено довольно много согласованностей между показателями, снятыми двумя методиками у одного и того же пациента примерно в одно и то же время.
Однако разные показатели демонстрировали разную степень согласованности.
Так, значения ОПСС по давлению в ПП не выявили согласования, в то время как по ЦВД — выявили. Отсюда мы делаем вывод, что использование объективного значения ЦВД более корректно.
Наши данные согласуются с мнением других авторов о том, что нет преимуществ в измерении ОПСС между ТЭхоКГ и катетеризацией ЛА [13].
СИ хорошо измеряется обеими методиками. В то же время мы полагаем, что у более широкого спектра пациентов более корректным будет измерение СИ посредством VTI, поскольку в данном случае оценивается непосредственный выброс из ЛЖ в аорту, без оглядки на клапанные регургитации, в частности на митральном и аортальном клапанах.
Не показало согласованности методик измерение ДЗЛА. Мы считаем, что это связано с тем, что оценка диастолической функции, через которую впоследствии производится расчет, у реанимационных пациентов в режиме фокусного ТЭхоКГ может быть затруднена и недостаточно корректна. Для получения полноценных кривых необходимы более оптимальная визуализация и более параллельное ультразвуковому лучу направление потоков крови. Для получения четкой кривой движения фиброзного кольца митрального клапана при тканевой допплерографии также требуется более качественное изображение сердца.
В целом же мы считаем, что ТЭхоКГ можно использовать для мониторирования СИ и ОПСС у пациентов с КШ [14].
Ограничения исследования. Катетеризация ЛА требует специальных навыков врача анестезиолога-реаниматолога, является инвазивной методикой с повышенными рисками перипроцедуральных и инфекционных осложнений по сравнению с ТЭхоКГ, является дополнительным травмирующим фактором для пациента, при этом довольно затратна финансово.
ТЭхоКГ ограничена окном локации; у некоторых пациентов в вынужденном положении на спине и находящихся на искусственной вентиляции легких это особенно актуально.
Также ограничения связаны с особенностями расчетов. Так, наличие в формуле квадратной степени от диаметра ВОЛЖ, при некорректном измерении может значительно искажать реальные результаты. Некоторые клапанные патологии, например, выраженный стеноз и/или недостаточность клапана, также могут исказить спектральную кривую потока, на которой базируется расчет. СИ, рассчитанный исходя из различий КДО и КСО, в случае митральной регургитации, особенно выраженной, нуждается в поправках (расчете объема митральной регургитации).
Заключение
Мы считаем, что ТЭхоКГ можно применять для МЦГ в случаях удовлетворительной и умеренно сниженной визуализации изображений сердца.
Статистически согласованными являются как результаты измерений СИ с помощью формулы Бернулли, так и СИ, рассчитанного, исходя из разницы КДО и КСО, а также измерение ОПСС с помощью ЦВД.
Корреляционный коэффициент был значимо выше при измерении СИ посредством VTI, поэтому мы считаем этот способ предпочтительным.
Измерение ОПСС с помощью давления в ПП и измерение ДЗЛА не продемонстрировали согласованности разных методик.
Таким образом, ТЭхоКГ можно использовать для мониторирования СИ и ОПСС у пациентов с КШ.
Отношения и деятельность. Государственное задание на оказание государственных услуг (выполнение работ) № 075-00712-24-04 от 02.04.2024, лаборатория инфаркт-ассоциированного шока.
Список литературы
1. Berg DD, Bohula EA, Morrow DA. Epidemiology and causes of cardiogenic shock. Curr Opin Crit Care. 2021;27(4):4018. doi:10.1097/MCC.0000000000000845.
2. Кузьков В. В., Киров М. Ю. Инвазивный мониторинг гемодинамики в интенсивной терапии и анестезиологии. Архангельск: Северный государственный медицинский университет, 2015. 392 с. ISBN: 9785917021805.
3. Zeymer U, Bueno H, Granger BCh, et al. Acute Cardiovascular Care Association position statement for the diagnosis and treatment of patients with acute myocardial infarction complicated by cardiogenic shock: A document of the Acute Cardiovascular Care Association of the European Society of Cardiology. Eur Heart J Acute Cardiovasc Care. 2020;9(2):18397. doi:10.1177/2048872619894254.
4. Йовенко И. А., Кобеляцкий Ю. Ю., Царев А. В. и др. Гемодинамический мониторинг в практике интенсивной терапии критических состояний. Медицина неотложных состояний. 2016;5(76):426. doi:10.22141/22240586.5.76.2016.76433.
5. Сыркина А. Г., Рябов В. В. Мониторинг центральной гемодинамики у пациентов с кардиогенным шоком. Терапевтический архив. 2021;93(4):5028. doi:10.26442/00403660.2021.04.200688.
6. McLean AS. Echocardiography in shock management. Crit Care. 2016;20:275. doi:10.1186/s1305401614017.
7. Papadimitriou L, Georgiopoulou VV, Kort S, et al. Echocardiography in Acute Heart Failure: Current Perspectives. J Card Fail. 2016;22(1):8294. doi:10.1016/j.cardfail.2015.08.001.
8. Simeoli PS, Moscardelli S, Urbani A, et al. Use and Implications of Echocardiography in the Hemodynamic Assessment of Cardiogenic Shock. Curr Probl Cardiol. 2023; 48(11):101928. doi:10.1016/j.cpcardiol.2023.101928.
9. Четвертое универсальное определение инфаркта мио карда (2018). Российский кардиологический журнал. 2019;24(3):10738. EDN ZAQSQP.
10. Kapur NK, Kanwar M, Sinha SS, et al. Criteria for Defining Stages of Cardiogenic Shock Severity. J Am Coll Cardiol. 2022;80(3):18598. doi:10.1016/j.jacc.2022.04.049.
11. Bootsma IT, Boerma EC, de Lange F, et al. The contemporary pulmonary artery catheter. Part 1: placement and waveform analysis. J Clin Monit Comput. 2022;36:515. doi:10.1007/s10877021006628.
12. Bootsma IT, Boerma EC, Scheeren TWL, et al. The contemporary pulmonary artery catheter. Part 2: measurements, limitations, and clinical applications. J Clin Monit Comput. 2022;36:1731. doi:10.1007/s10877021006735.
13. Gaubert M, Resseguier N, Thuny F, et al. Doppler echocardiography for assessment of systemic vascular resistances in cardiogenic shock patients. Eur Heart J Acute Cardiovasc Care. 2020;9(2):1027. doi:10.1177/2048872618795514.
14. Muñoz-Rodríguez R, García-González MJ, Jorge-Pérez P, et al. Ultrasound Assessment in Cardiogenic Shock Weaning: A Review of the State of the Art. J Clin Med. 2021;10(21):5108. doi:10.3390/jcm10215108.
Об авторах
В. В. РябовРоссия
д. м. н., зам. директора по научной и клинической работе, и. о. зав. отделением неотложной кардиологии.
Томск
Конфликт интересов:
нет
А. Г. Сыркина
Россия
к. м. н., с. н. с. отделения неотложной кардиологии.
Томск
Конфликт интересов:
нет
М. А. Керчева
Россия
к. м. н., н. с. отделения неотложной кардиологии, и. о. зав. лабораторией инфаркт-ассоциированного шока.
Томск
Конфликт интересов:
нет
И. И. Ёлгин
Россия
врач функциональной диагностики отделения неотложной кардиологии.
Томск
Конфликт интересов:
нет
О. О. Пантелеев
Россия
н. с. отделения неотложной кардиологии.
Томск
Конфликт интересов:
нет
Дополнительные файлы
- Фокусная эхокардиография не хуже катетеризации легочной артерии в части мониторирования сердечного индекса и общего периферического сосудистого сопротивления у пациентов с инфарктом миокарда, осложненным кардиогенным шоком.
- Более предпочтительным способом для расчета сердечного индекса мы считаем измерение VTI выводного отдела левого желудочка.
Рецензия
Для цитирования:
Рябов В.В., Сыркина А.Г., Керчева М.А., Ёлгин И.И., Пантелеев О.О. Сравнительный анализ мониторинга гемодинамики с помощью катетеризации легочной артерии и трансторакальной эхокардиографии у пациентов с кардиогенным шокомхокардиографии у пациентов с кардиогенным шоком. Российский кардиологический журнал. 2024;29(7):5990. https://doi.org/10.15829/1560-4071-2024-5990. EDN: SOJKZQ
For citation:
Ryabov V.V., Syrkina A.G., Kercheva M.A., Yolgin I.I., Panteleev O.O. Comparative analysis of hemodynamic monitoring with pulmonary artery catheter and transthoracic echocardiography in patients with cardiogenic shock. Russian Journal of Cardiology. 2024;29(7):5990. (In Russ.) https://doi.org/10.15829/1560-4071-2024-5990. EDN: SOJKZQ
JATS XML

















































