Перейти к:
Роль индекса объема левого предсердия и неишемического паттерна контрастирования миокарда в прогнозе продолженного ремоделирования левого желудочка у пациентов с ишемической кардиомиопатией: данные магнитно-резонансной томографии
https://doi.org/10.15829/1560-4071-2024-5954
EDN: XWKOQI
Аннотация
Цель. У пациентов с ишемической кардиомиопатией оценить морфологические особенности сердца и значимость неишемического паттерна контрастирования миокарда в аспекте прогнозирования продолженного ремоделирования левого желудочка (ЛЖ) в среднесрочном периоде после хирургического вмешательства.
Материал и методы. Проанализированы результаты магнитно-резонансной томографии сердца (МРТ) с парамагнитным контрастным усилением у 31 пациента с ишемической кардиомиопатией среднего возраста 58,4±7,6 лет перед комплексным хирургическим лечением. Оценивали морфологические особенности камер сердца и наличие неишемического паттерна контрастирования в сегментах миокарда отдаленных от зоны инфаркта, по данным МРТ с контрастированием.
Результаты. Обнаружено, что у пациентов с неишемическим паттерном контрастирования выше значения индекса объема левого предсердия (ЛП) (р=0,02), конечного систолического индекса ЛЖ (р=0,03), размеры правого желудочка (р=0,01). Обнаружена взаимосвязь индекса объема ЛП и ремоделирования сердца в послеоперационном периоде (p<0,005, коэффициент корреляции r=0,53).
Заключение. Наличие неишемического паттерна контрастирования миокарда сопровождается увеличением объема ЛП, что, в свою очередь, является предиктором продолженного ремоделирования ЛЖ у пациентов с ишемической кардиомиопатией в послеоперационном периоде.
Ключевые слова
Для цитирования:
Шелковникова Т.А., Андреев С.Л., Максимова А.С., Усов В.Ю., Завадовский К.В. Роль индекса объема левого предсердия и неишемического паттерна контрастирования миокарда в прогнозе продолженного ремоделирования левого желудочка у пациентов с ишемической кардиомиопатией: данные магнитно-резонансной томографии. Российский кардиологический журнал. 2024;29(11):5954. https://doi.org/10.15829/1560-4071-2024-5954. EDN: XWKOQI
For citation:
Shelkovnikova T.A., Andreev S.L., Maksimova A.S., Usov V.Yu., Zavadovsky K.V. Left atrial volume index and non-ischemic myocardial contrast pattern as a predictor of continued left ventricular remodeling in patients with ischemic cardiomyopathy: magnetic resonance imaging data. Russian Journal of Cardiology. 2024;29(11):5954. (In Russ.) https://doi.org/10.15829/1560-4071-2024-5954. EDN: XWKOQI
Известно, что ремоделирование левого желудочка (ЛЖ) у пациентов с ишемической болезнью сердца начинается с острого инфаркта, приводящего к повреждению миокарда, и включает в себя прогрессирующую группу изменений (длины, ширины, организации миоцитов; активацию множества клеточных, молекулярных и внеклеточных процессов), как в остром, так и в отдаленном периоде [1]. Гибель кардиомиоцитов и деградация внеклеточного матрикса сердца в инфарцированном миокарде высвобождают сигналы, активирующие врожденные иммунные механизмы и вызывающие интенсивную воспалительную реакцию. Приток воспалительных клеток приводит к разрушению коллагеновых каркасов, помогающих поддерживать форму желудочков [2], региональному истончению и расширению миокарда в зонах инфаркта [3], а приток фибробластов к месту повреждения миокарда способствует формированию новой коллагеновой матрицы, способствующей образованию рубцов в ближайшем постинфарктном периоде [4].
Жизнеспособный миокард также претерпевает ряд изменений, подвергаясь эксцентрической компенсаторной гипертрофии, в связи с повышенной нагрузкой [2], которая со временем приводит к увеличению конечного систолического и конечного диастолического объемов ЛЖ.
Использование магнитно-резонансной томографии (МРТ) может предоставить дополнительную информацию в отношении ремоделирования сердца, не только для более точного определения массы и объема ЛЖ [2], но и в оценке образования, локализации рубца, характера трансмуральности некроза и микрососудистой обструкции, являющимися предикторами дилатации ЛЖ [5], позволяет оценить обратимость повреждения миокарда.
В последние десятилетия активно изучается роль левого предсердия (ЛП) в патофизиологии сердечной недостаточности (СН) [6]. Как было показано, изменения в структуре и функции ЛП могут быть либо маркером тяжести СН, либо механизмом, активно способствующим прогрессированию сердечной дисфункции, т. к. ЛП непосредственно участвует в наполнении ЛЖ, сердечном выбросе, поддерживая динамическое с ним взаимодействие. Так, в работе Kim M, et al. [7] продемонстрирована роль объема и жесткости ЛП в диастолической функции ЛЖ, а также определена взаимосвязь функциональных параметров ЛП с фиброзом ЛЖ при неишемических кардиомиопатиях. В работе Yingchoncharoen T, et al. (2016) обнаружена взаимосвязь очагового и диффузного фиброза миокарда ЛЖ по данным МРТ с его ремоделированием у пациентов с неишемической кардиомиопатией [8]. Поскольку и при ишемической кардиомиопатии (ИКМП) развитие ремоделирования сердца связано в т. ч. с активацией воспалительного процесса и неблагоприятными эффектами на ткани миокарда, отдаленными от области инфаркта, целью данного исследования являлась оценка морфологических особенностей сердца и значимости неишемического паттерна контрастирования (НИПК) миокарда в аспекте прогнозирования продолженного ремоделирования ЛЖ в среднесрочном периоде после хирургического вмешательства.
Материал и методы
Пациенты и дизайн исследования
Данная работа представляет собой post-hoc анализ ранее выполненного исследования "Разработка и оценка эффективности способа формирования полости ЛЖ сердца у пациентов с передне-перегородочными аневризмами при его реконструкции по методу Menicanti". У 31 пациента с ИКМП были проанализированы результаты МРТ сердца с парамагнитным контрастным усилением (ПМКУ), проведённой перед плановым оперативным вмешательством (коронарным шунтированием, реконструкцией ЛЖ и коррекцией митрального клапана при необходимости) в период с марта 2013г по декабрь 2017г.
Критериями включения являлись: фракция выброса (ФВ) ЛЖ <40% по данным трансторакальной эхокардиографии (ТТЭхоКГ); конечно-систолический индекс ЛЖ (КСИ) >60 мл/м² по данным эхокардиографии, СН II-IV функционального класса по NYHA, инфаркт миокарда (ИМ) в анамнезе и многососудистое гемодинамически значимое атеросклеротическое поражение коронарных артерий.
Пациентам проведена оценка факторов риска при кардиохирургических вмешательствах по шкале EuroSCOR E. Из исследования исключались пациенты с пороками сердца инфекционного, ревматического генеза, пациенты с острым нарушением мозгового кровообращения и острой стадией ИМ, пациенты с наличием правожелудочковой недостаточности и больные с противопоказаниями к операции с искусственным кровообращением.
МРТ сердца с ПМКУ проводилась всем пациентам за 3-5 дней до оперативного лечения. В ранний послеоперационный период и через 9-12 мес. после хирургического вмешательства выполнялась ТТЭхоКГ для оценки объема и сократимости ЛЖ (дизайн исследования представлен на рисунке 1). При увеличении КСИ или снижении его ≤10% относительно раннего послеоперационного периода у пациентов диагностировалось продолженное ремоделирование ЛЖ [9].
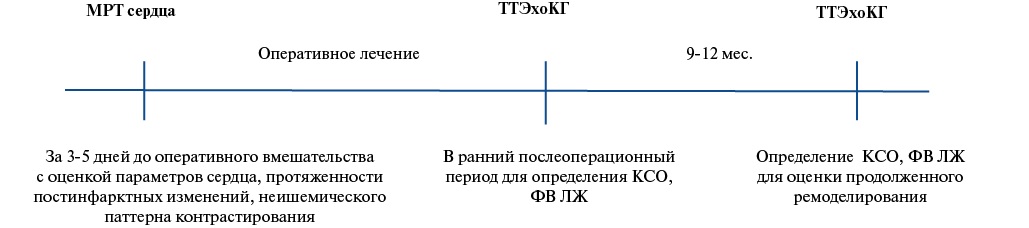
Рис. 1. Схема обследования пациентов, включенных в исследование.
Сокращения: КСО — конечно-систолический объем, ЛЖ — левый желудочек, МРТ — магнитно-резонансная томография, ТТЭхоКГ — трансторакальная эхокардиография, ФВ — фракция выброса.
По данным МРТ в отсроченную фазу контрастирования оценивали наличие НИПК, который был определен как интрамуральное и/или субэпикардиальное накопление контрастного вещества в сегментах миокарда, отдаленных от зоны инфаркта (участка трансмурального или субэндокардиального накопления контрастного вещества) [10].
В зависимости от наличия у пациентов НИПК по данным МРТ, пациенты были разделены на две группы, с последующим анализом функциональных параметров сердца.
Исследование было одобрено локальным комитетом по биомедицинской этике и проведено в соответствии с этическими нормами, изложенными в Хельсинкской декларации с пересмотром 2008г. Все пациенты дали согласие на участие в исследовании.
МРТ сердца с контрастированием
МРТ сердца с ПМКУ сердца до оперативного вмешательства проведено пациентам на магнитно-резонансном томографе Vantage Titan (Toshiba) 1,5 Тл с электрокардиографической синхронизацией и получением изображений миокарда по короткой и длинной осям, до и после введения контрастного препарата (Гадовист из расчета 0,1 мл на 1 кг массы тела пациента). Толщина срезов составляла 5-7 мм при отсутствии промежутков между ними, с записью в матрицу 256×256. Протокол МРТ-исследования включал Т1-, Т2-взвешенные последовательности и последовательность с подавлением сигнала от жировой ткани для оценки состояния миокарда, динамические SSFP-последовательности для оценки объемов и функции ЛЖ, градиентные последовательности инверсия-восстановление (GR-IR) для выявления участков патологического контрастирования. Время инверсии подбиралось индивидуально (в среднем: TI =300±10 мс). Оценка измененных участков в миокарде осуществлялась с учетом 17-сегментной системы топической характеристики миокарда ЛЖ.
Параметры ЛЖ рассчитывали в абсолютных цифрах в обе фазы сердечного цикла, отнесенные к площади поверхности тела. Для расчета использовали КСИ, конечно-диастолический индекс ЛЖ, ФВ ЛЖ, массу миокарда ЛЖ, индекс сферичности (отношение короткой к длинной оси ЛЖ). У каждого пациента был определен индекс объема ЛП (ИОЛП), соответствующий объему ЛП, отнесенного к площади поверхности тела и рассчитанный на основе рекомендаций Американского общества эхокардиографии [11].
Параметры правого желудочка (ПЖ) сердца рассчитывали в четырехкамерной проекции, использовали максимальный линейный размер ПЖ в диастолу, выраженный в миллиметрах.
Постинфарктные рубцовые изменения определяли как участки задержки вымывания парамагнетика субэндокардиальной и трансмуральной локализации высокой интенсивности с четкими внешними контурами. Проводили оценку количества сегментов с патологическим контрастированием и, отдельно, сегментов с высокой трансмуральностью у каждого пациента (с включением парамагнетика >50% толщины стенки ЛЖ). Расчет массы жизнеспособного миокарда выполняли с использованием пакета программного обеспечения "Segment" (http://medviso.com).
Хирургическое лечение ИКМП
Предоперационная подготовка и интраоперационный мониторинг были стандартными для кардиохирургических операций. Доступ к сердцу, основные этапы операции (формирование дистальных анастомозов между целевыми коронарными артериями и аутовенозными трансплантатами, реконструкция ЛЖ, наложение эндовентрикулярного кисетного шва и коррекция митральной недостаточности при наличии хронической ишемической митральной регургитации, наложение проксимальных анастомозов аортокоронарных шунтов) описаны подробно в наших ранее изданных статьях [12].
Статистическая обработка данных. Статистическую обработку результатов проводили в программном пакете STATISTICA v10 и MedCalc 12.1.14.0. Проверка выборок на соответствие нормальному закону распределения проводилась с помощью критерия Шапиро-Вилка (Shapiro-Wilk). Критический уровень значимости нулевой статистической гипотезы (p) принимался равным 0,05. Анализ независимых данных, подчиняющихся нормальному закону распределения, проводился с помощью t-критерия Стьюдента. Количественные данные, подчиняющиеся нормальному закону распределения, представлены в виде среднего и стандартного отклонения — M±SD. С помощью медианы (Me) и межквартильного интервала (Q25-Q75) данные представлены при распределении, отличающемся от нормального. Достоверность различий в группах оценивали при помощи непараметрических тестов Манна-Уитни и Вилкоксона. Качественные данные отображались частотой встречаемости и процентом. Для поиска предикторов ремоделирования ЛЖ в послеоперационном периоде был выполнен однофакторный и многофакторный логистический регрессионный анализ, рассчитаны отношения шансов (ОШ) и доверительный интервал (ДИ). Определение чувствительности и специфичности показателя, точек отсечения проводилось с помощью ROC-анализа.
Результаты
Клиническая характеристика пациентов, вошедших в исследование, представлена в таблице 1. В выборке преобладали пациенты мужского пола (97,2%). Среднее значение EuroSCORE составило 5,3±2 баллов.
Таблица 1
Клиническая характеристика групп
|
Показатель |
Вся выборка (n=31) |
НИПК+ (n=22) |
НИПК- (n=9) |
р-value |
|
Возраст, лет |
58,4±7,6 |
56,9±7,2 |
62,1±7,6 |
p=0,08 |
|
Мужчины n, % |
30 (96,7%) |
21 (95,4%) |
9 (100%) |
p=0,8 |
|
Индекс массы тела, кг/м² |
27,5±3,9 |
27,6±4,0 |
26,8±3,5 |
p=0,7 |
|
Функциональный класс сердечной недостаточности по NYHA, n (%): — I — II — III |
0 (0) 8 (36,4%) 14 (63,6%) |
0 (0) 3 (33,3%) 6 (66,7%) |
p=0,9 p=0,8 |
|
|
Функциональный класс стенокардии напряжения, n (%): — I — II — III — IV |
0 (0) 8 (32,4%) 13 (62,1%) 1 (4,5%) |
0 (0) 2 (28,5%) 7 (51,1%) 0 (0) |
p=0,5 p=0,6 p=0,5 |
|
|
Гипертоническая болезнь 3-й стадии, n (%) |
28 (90,3%) |
19 (86,3%) |
9 (100%) |
p=0,7 |
Сокращение: НИПК — неишемический паттерн контрастирования.
При сравнительном анализе установлено, что группы пациентов НИПК+ (n=22) и НИПК- (n=9) были сопоставимы по возрасту, функциональному классу стенокардии и баллам шкалы рисков оперативного вмешательства EuroSCORE (5,6±1,6 и 4,4±2,5, p=0,12).
Дополнительно с аортокоронарным шунтированием коррекция митрального клапана была проведена 12 (54,5%) пациентам из группы с НИПК+ и 1 (11,1%) пациенту в НИПК- (χ²=1,32, p=0,25), реконструкция ЛЖ 12 (54,5%) пациентам с НИПК+ и 7 (77,7%) с НИПК- (χ²=0,7, p=0,7). Следовательно, группы достоверно не различались по данным показателям.
Оценка МРТ-параметров сердца выявила статистически значимые различия показателей КСИ ЛЖ, ИОЛП и линейных размеров ПЖ (табл. 2) в группах с НИПК+ и НИПК-, при отсутствии значимого различия ФВ ЛЖ, объема поврежденного миокарда (выраженного в % от общей массы миокарда ЛЖ), а также количества поврежденных сегментов ЛЖ с высокой трансмуральностью.
Таблица 2
Результаты МРТ сердца у пациентов обеих групп в зависимости от наличия НИМК
|
Показатель |
НИПК+ (n=22) |
НИПК- (n=9) |
p-value |
|
КСИ, мл |
83,7±22,9 |
66,2±11,1 |
0,03 |
|
ФВ, % |
30,6±7,5 |
34,1±5,2 |
0,22 |
|
ИМ, % |
25,7 [ 17,0;31,6] |
26,3 [ 19,2;31,8] |
0,76 |
|
Количество сегментов с трансмуральностью >50% |
4,4 [ 2;7] |
3,5 [ 3;6] |
0,46 |
|
КДР ПЖ, мм |
39,9±6,8 |
33,5±5,7 |
0,01 |
|
ИОЛП, мл |
46,8±12,6 |
32,7±5,6 |
0,02 |
Сокращения: ИМ — глобальный размер инфаркта миокарда в % от массы миокарда левого желудочка, ИОЛП — индекс объема левого предсердия, КДР ПЖ — конечно-диастолический размер правого желудочка, КСИ — конечно-систолический индекс, НИПК — неишемический паттерн контрастирования, ФВ — фракция выброса левого желудочка.
Частота продолженного ремоделирования ЛЖ за период 9-12 мес. после оперативного вмешательства имела тенденцию (χ²=2,5, p=0,1) к более частому развитию в группе НИПК+, по сравнению с НИПК-: 7 (31,8%) и 0 случаев, соответственно. Результаты ТТЭхоКГ на точке раннего послеоперационного периода и через 9-12 мес. после оперативного вмешательства в группах показаны в таблице 3. В обеих группах за время наблюдения отмечено значимое снижение КСИ ЛЖ по сравнению с показателями в ранний послеоперационный период (p<0,005), при сохранении статистически значимых различий КСИ ЛЖ между группами с НИПК+ и НИПК-.
Таблица 3
Результаты ТТЭхоКГ сердца с ПМКУ у пациентов в ранний послеоперационный период и через 9-24 мес. после оперативного вмешательства
|
Показатель |
НИПК+ (n=22) |
НИПК- (n=9) |
p-value |
|
ФВ, % ранний п/о период |
30,6±7,5 |
34,1±5,2 |
p>0,05 |
|
ФВ, % через 9-12 мес. |
34,4±6,2 |
39,1±9,4 |
p>0,05 |
|
КСИ, мл, ранний п/о период |
83,7±22,9 |
66,2±11,1* |
p<0,05 |
|
КСИ, мл, через 9-12 мес. |
68,7±19,7* |
50,1±14,7* |
p<0,05 |
Примечание: * — статистически значимые различия между ранним п/о периодом и исследованием через 9-12 мес.
Сокращения: КСИ — конечно-систолический индекс, НИПК — неишемический паттерн контрастирования, ФВ — фракция выброса левого желудочка.
На рисунке 2 представлены МРТ-изображения пациентов с очагами фиброза в миокарде неишемического генеза и продолженным ремоделированием ЛЖ в послеоперационном периоде.
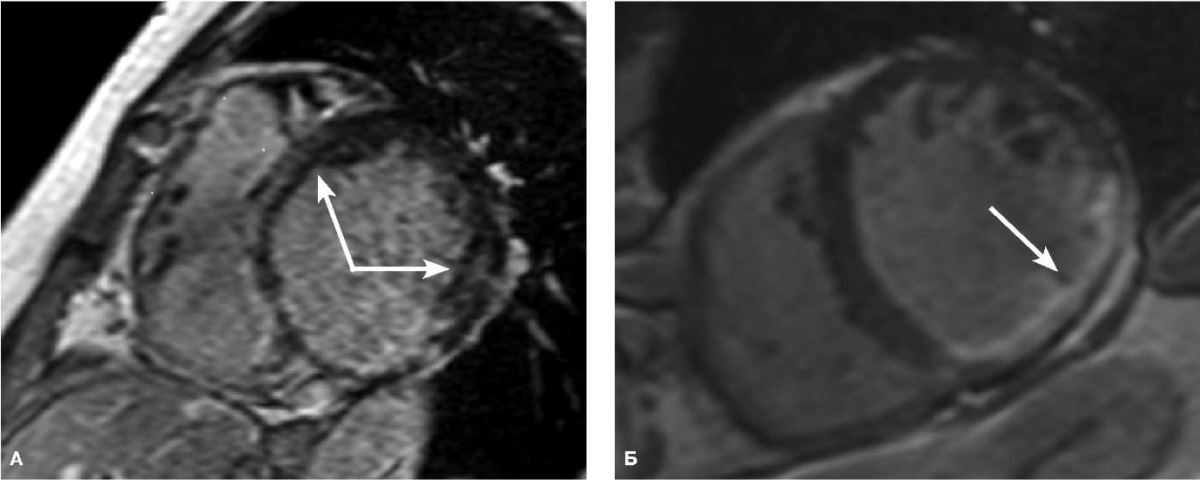
Рис. 2. А. МРТ сердца с контрастным усилением (короткая ось аксиальная проекция) у пациента с ИКМП и НИПК+ (указано стрелками), продолженным ремоделированием ЛЖ в среднесрочном послеоперационном периоде. Б. МРТ сердца с контрастным усилением (короткая ось аксиальная проекция) у пациента с ИКМП и НИПК- без продолженного ремоделирования ЛЖ в среднесрочном послеоперационном периоде, стрелкой указана зона постинфарктного склероза.
При проведении корреляционного анализа Спирмана между дооперационными функциональными и объемными показателями МРТ сердца у пациентов и данными эхокардиографии в среднесрочном периоде после хирургического вмешательства, в целом по группе выявлена отрицательная взаимосвязь средней силы между ИОЛП и ФВ (p<0,005, коэффициент корреляции r=-0,54) и положительная взаимосвязь ИОЛП и КСИ (p<0,005, коэффициент корреляции r=0,53).
По результатам однофакторного регрессионного анализа было установлено, что показатели ИОЛП, размеры ПЖ были статистически значимыми предикторами продолженного ремоделирования ЛЖ (табл. 4).
Таблица 4
Предикторы продолженного ремоделирования ЛЖ по данным однофакторного логистического регрессионного анализа
|
Показатель |
ОШ |
95% ДИ |
p-value |
|
Возраст |
0,8987 |
0,7910-1,0210 |
0,1 |
|
EuroSCORE |
1,4570 |
0,8859-2,3963 |
0,4 |
|
Количество сегментов с трансмуральностью >50% |
1,1118 |
0,8441-1,4642 |
0,4 |
|
ИОЛП, мл/м² |
1,2191 |
1,0301-1,4428 |
0,02 |
|
ФК МК, мм |
1,2094 |
0,9122-1,6032 |
0,18 |
|
ОМК |
1,3585 |
0,8107-2,2764 |
0,2 |
|
ПЖ, мм |
1,1951 |
1,0117-1,4118 |
0,03 |
|
МЖМ, мм |
1,0075 |
0,9863-1,0292 |
0,49 |
|
КМ, % |
0,9926 |
0,9091-1,0838 |
0,86 |
|
ИНЛС |
1,6148 |
0,0821-31,7490 |
0,75 |
|
Количество артериальных шунтов |
0,4813 |
0,1800-1,2867 |
0,14 |
Сокращения: ДИ — доверительный интервал, ИНЛС — индекс нарушения локальной сократимости, ИОЛП — индекс объема левого предсердия, МЖМ — масса жизнеспособного миокарда, ОМК — оперативное вмешательство на митральном клапане, ОШ — отношение шансов, ФК МК — размер фиброзного кольца митрального клапана, ПЖ — поперечный размер правого желудочка, КМ — % миокарда, накопившего контрастный препарат, относительно массы миокарда левого желудочка, p-value — величина уровня значимости.
Дальнейшее исследование с помощью многофакторной логистической регрессии показало, что только ИОЛП является единственным независимым предиктором развития продолженного ремоделирования ЛЖ через 9-12 мес. после хирургического вмешательства, ОШ 1,2271, 95% ДИ: 1,0269-1,4664, p=0,039. По данным ROC анализа, чувствительность дооперационного показателя ИОЛП в предсказании ремоделирования ЛЖ в послеоперационном периоде составила — 75,0%, специфичность — 66,7%, cut-off value =40,9, AUC =0,720.
Обсуждение
В результате данного исследования были установлены следующие факты: 1) неишемический паттерн повреждения миокарда по данным МРТ с отсроченным контрастированием ассоциирован с дилатацией не только ЛЖ, но и других полостей сердца в группе пациентов с ИКМП; 2) при проведении корреляционного анализа выявлена взаимосвязь ИОЛП с продолженным ремоделированием ЛЖ через 9-12 мес. после оперативного вмешательства; 3) ИОЛП является единственным независимым предиктором развития продолженного ремоделирования ЛЖ через 9-12 мес. после хирургического вмешательства.
Насколько нам известно, данная работа впервые демонстрирует значение НИПК и объёма ЛП, выявленных по данным МРТ, в прогнозе ремоделирования ЛЖ при хронической ИКМП в среднесрочном послеоперационном периоде.
Полученные результаты дополняют имеющиеся сведения о МРТ-семиотике ИКМП и прогностической значимости этой диагностической модальности в оценке ремоделирования ЛЖ после хирургического вмешательства.
Наши данные согласуются с работой Kim M, et al. (2022) [7], в которой подтверждается роль фиброза ЛЖ в функциональном состоянии ЛП. По результатам этого исследования фиброз ЛЖ ограничивает его наполнение, за счет нарушения активной релаксации и увеличения пассивной жесткости, а повышение давления ЛП приводит к дилатации камер и растяжению миокарда предсердий.
То, что размер ЛП является чувствительным маркером хронической формы повышенного напряжения ЛЖ, показано и в работе Ibrahim SH, et al. (2021) [6]. Так, увеличение индексов объема предсердий представляет собой новые параметры, отражающие ремоделирование сердца и свидетельствующие о множестве патофизиологических нарушений, каждое из которых может ухудшать восстановление сердца после острой сердечной катастрофы, и тесно связаны с выживаемостью у пациентов (ОШ 0,57, 95% ДИ: 0,30-1,05, p=0,074).
Большинство проводимых ранее исследований у пациентов ИКМП с использованием данных МРТ с контрастированием, были сосредоточены, в основном, на объемах постинфарктного кардиосклероза [13], в то время как нами выявлен дополнительный, НИПК, указывающий на более выраженные структурные изменения миокарда ЛЖ, сформированные, вероятно, на фоне воспалительного ответа на ишемию и перегрузку. Определена взаимосвязь ИОЛП с продолженным ремоделированием ЛЖ в среднесрочном послеоперационном периоде.
Прогностическое значение МРТ сердца у пациентов с ИКМП
МРТ сердца рассматривается в качестве неинвазивного эталонного метода для оценки структурных, функциональных и тканевых характеристик предсердий и желудочков. МРТ позволяет визуализировать очаги фиброза в миокарде, а локализация фиброзных изменений дает возможность определить причину их формирования. Фиброз сердца характерен для конечной стадии почти всех форм сердечных заболеваний [13].
Несмотря на острую необходимость замедлить или обратить вспять развитие фиброза сердца для поддержания сердечной функции, не существует одобренных методов лечения, которые непосредственно воздействуют на внеклеточный матрикс. Улучшенное понимание многих факторов, которые стимулируют активацию фибробластов, может дать возможность определить новые терапевтические мишени. Показано, что иммунная система играет роль в формировании фиброза как в ответ на перегрузку давлением, так и на течение ИМ [2]. Эффективный переход от этапа воспаления к фазе заживления и развития стабильного рубца имеет решающее значение для последующего прогноза. Продолжающееся воспаление и активация фибробластов могут привести к расширению зоны инфаркта и нарушению сердечной функции.
Ограничения исследования. К ограничениям нашего исследования необходимо отнести малый объем выборки, вариабельность в продолжительности наблюдения за пациентами, технические различия при выполнении хирургического вмешательства у обследованными пациентов. Тем не менее нам удалось выявить МРТ-паттерны продолженного ремоделирования ЛЖ у пациентов с ИКМП через 9-12 мес. после хирургического вмешательства.
Заключение
Наличие НИПК миокарда сопровождается увеличением объема ЛП, что, в свою очередь, является предиктором продолженного ремоделирования ЛЖ у пациентов с ИКМП в послеоперационном периоде. Пациенты с незначительным увеличением ЛП и отсутствием в миокарде очагов фиброза некоронарогенного генеза, по-видимому, имеют наилучший прогноз после проведения хирургического вмешательства. Наше исследование подтверждает, что оценка ИОЛП и структуры миокарда ЛЖ на предмет очагов фиброза неишемического генеза может быть полезна для определения стратегий ведения пациентов с ИКМП.
Отношения и деятельность: все авторы заявляют об отсутствии потенциального конфликта интересов, требующего раскрытия в данной статье.
Список литературы
1. Bhatt AS, Ambrosy AP, Velazquez EJ. Adverse Remodeling and Reverse Remodeling After Myocardial Infarction. Curr Cardiol Rep. 2017;19(8):71. doi:10.1007/s11886-017-0876-4.
2. Calvieri C, Riva A, Sturla F, et al. Left Ventricular Adverse Remodeling in Ischemic Heart Disease: Emerging Cardiac Magnetic Resonance Imaging Biomarkers. J Clin Med. 2023; 12(1):334. doi:10.3390/jcm12010334.
3. Jiang H, Fang T, Cheng Z. Mechanism of heart failure after myocardial infarction. J Int Med Res. 2023;51(10):3000605231202573. doi:10.1177/03000605231202573.
4. Казаков В. А. Морфологические аспекты послеоперационного ремоделирования левого желудочка у больных ишемической кардиомиопатией. Артериальная гипертензия. 2009;15(3):376-83. doi:10.18705/1607-419X-2009-15-3-376-383.
5. Guglielmo M, Pontone G. Clinical implications of cardiac magnetic resonance imaging fibrosis. Eur Heart J Suppl. 2022;12;24 (Suppl I):I123-I126. doi:10.1093/eurheartjsupp/suac085.
6. Ibrahim SH, Bilchick KC, Miller MS, et al. Increased left and right atrial volume indices are associated with decreased survival times post-cardiac arrest. Resuscitation. 2022;170:306-13. doi:10.1016/j.resuscitation.2021.10.023.
7. Kim M, Chung H, Kim IS, et al. Effects of left atrial function on pulmonary arterial pressure in acute myocardial infarction, hypertrophic and dilated cardiomyopathy. BMC Cardiovasc Disord. 2022;22(1):507. doi:10.1186/s12872-022-02952-8.
8. Yingchoncharoen T, Jellis C, Popovic ZB, et al. Focal fibrosis and diffuse fibrosis are predictors of reversed left ventricular remodeling in patients with non-ischemic cardiomyopathy. Int J Cardiol. 2016;221:498-504. doi:10.1016/j.ijcard.2016.06.095.
9. Шипулин В. М., Пряхин А. С., Андреев С. Л. и др. Современные клинико-фундаментальные аспекты в диагностике и лечении пациентов с ишемической кардиомиопатией (обзор). Сибирский журнал клинической и экспериментальной медицины. 2021;36(1):20-9. doi:10.29001/2073-8552-2021-36-1-20-29.
10. Kawel-Boehm N, Hetzel SJ, Ambale-Venkatesh B, et al. Reference ranges ("normal values") for cardiovascular magnetic resonance (CMR) in adults and children: 2020 update. J Cardiovasc Magn Reson. 2020;22(1):87. doi:10.1186/s12968-020-00683-3.
11. Chan WX, Kaura A, Mulla A, Papadimitriou D, et al. Diagnostic and prognostic value of an ejection fraction adjusted for myocardial remodeling. Front Cardiovasc Med. 2024;11:1349338. doi:10.3389/fcvm.2024.1349338.
12. Шелковникова Т. А., Андреев С. Л., Завадовский К. В. и др. Объемно-миокардиальные индексы при прогнозировании течения раннего послеоперационного периода у пациентов с ишемической кардиомиопатией. Ангиология и сосудистая хирургия. Журнал им. академика А. В. Покровского. 2023; 29(1):42-9. doi:10.33029/1027-6661-2023-29-1-42-49.
13. Czubryt MP, Hale TM. Cardiac fibrosis: Pathobiology and therapeutic targets. Cell Signal. 2021;85:110066. doi:10.1016/j.cellsig.2021.110066.
Об авторах
Т. А. ШелковниковаРоссия
Шелковникова Татьяна Александровна — к. м. н., с. н. с. отделения рентгеновских и томографических методов диагностики.
Томск
Конфликт интересов:
Нет
С. Л. Андреев
Россия
Андреев Сергей Леонидович — к.м.н., с.н.с., отделение сердечно-сосудистой хирургии.
Томск
Конфликт интересов:
Нет
А. С. Максимова
Россия
Максимова Александра Сергеевна — к.м.н., н.с. отделения рентгеновских и томографических методов диагностики.
Томск
Конфликт интересов:
Нет
В. Ю. Усов
Россия
Усов Владимир Юрьевич — д.м.н., профессор, в.н.с. отделения рентгеновских и томографических методов диагностики.
Томск
Конфликт интересов:
Нет
К. В. Завадовский
Россия
Завадовский Константин Валерьевич — д.м.н., зав. отделом лучевой диагностики.
Томск
Конфликт интересов:
Нет
Дополнительные файлы
- Наличие неишемического паттерна контрастирования миокарда сопровождается увеличением объема левого предсердия, что, в свою очередь, является предиктором продолженного ремоделирования левого желудочка у пациентов с ишемической кардиомиопатией в послеоперационном периоде.
Рецензия
Для цитирования:
Шелковникова Т.А., Андреев С.Л., Максимова А.С., Усов В.Ю., Завадовский К.В. Роль индекса объема левого предсердия и неишемического паттерна контрастирования миокарда в прогнозе продолженного ремоделирования левого желудочка у пациентов с ишемической кардиомиопатией: данные магнитно-резонансной томографии. Российский кардиологический журнал. 2024;29(11):5954. https://doi.org/10.15829/1560-4071-2024-5954. EDN: XWKOQI
For citation:
Shelkovnikova T.A., Andreev S.L., Maksimova A.S., Usov V.Yu., Zavadovsky K.V. Left atrial volume index and non-ischemic myocardial contrast pattern as a predictor of continued left ventricular remodeling in patients with ischemic cardiomyopathy: magnetic resonance imaging data. Russian Journal of Cardiology. 2024;29(11):5954. (In Russ.) https://doi.org/10.15829/1560-4071-2024-5954. EDN: XWKOQI
JATS XML

















































