Перейти к:
Временная механическая циркуляторная поддержка трансаортальным устройством с пульсирующим кровотоком iVAC 2L при чрескожном коронарном вмешательстве высокого риска — многоцентровой опыт
https://doi.org/10.15829/1560-4071-2025-5856
EDN: UYZAVW
Аннотация
Цель. Провести анализ многоцентрового международного опыта процедур защищенного чрескожного коронарного вмешательства (ЧКВ) высокого риска с применением устройства временной механической циркуляторной поддержки (МЦП) трансаортальным устройством с пульсирующим кровотоком iVAC 2L (PulseCath B. V., Нидерланды).
Материал и методы. В пилотное проспективно-ретроспективное международное многоцентровое наблюдательное исследование включались пациенты с многососудистым и/или комплексным поражением коронарного русла, показаниями к коронарной реваскуляризации и отказом кардио-команды от операции коронарного шунтирования и незащищенного ЧКВ ввиду высокого риска осложнений. ЧКВ проводилось с одномоментной временной МЦП устройством iVAC 2L в пяти клиниках России и Белоруссии.
Результаты. С февраля 2023г по февраль 2024г в исследование включено 24 пациента. Медиана возраста составила 69,0 лет (интерквартильный размах (ИКР): 63,5-71,8), 87,5% были мужчины. 20 пациентам (83,3%) проведено плановое ЧКВ и 4 пациентам (16,7%) при остром коронарном синдроме (ОКС): 3 с инфарктом миокарда без подъема сегмента ST и 1 с инфарктом миокарда с подъемом сегмента ST (ИМпST). Пациенту с ИМпST ЧКВ проводилось на фоне острой сердечной недостаточности (ОСН). Медиана времени МЦП составила 66,0 мин (ИКР: 43,0-98,0). Технический успех ЧКВ был достигнут у 100% пациентов. Медиана исходной и резидуальной оценки по шкале SYNTAX составили 35,0 баллов (ИКР: 25,6-41,4) и 8,0 баллов (ИКР: 5,0-17,5), соответственно. Медиана фракции выброса левого желудочка до ЧКВ и через 7 дней после составила 44,0% (ИКР: 31,0-54,0) и 48,0% (ИКР: 36,5-53,5), соответственно. В двух случаях (8,3%) отмечалось развитие крупных кровотечений из места доступа устройства МЦП. Наблюдалось 2 летальных исхода: во время планового ЧКВ в результате прогрессирования острой левожелудочковой недостаточности и в отсроченном периоде в результате септического шока после экстренного ЧКВ.
Заключение. ЧКВ с одномоментной МЦП устройством iVAC 2L является применимой и относительно безопасной тактикой коронарной реваскуляризации у пациентов с высоким риском осложнений, в т.ч. в условиях ОКС и ОСН.
Ключевые слова
Для цитирования:
Аветисян Э.А., Дорогун О.Б., Красноперова Е.В., Тарасов Р.С., Ганюков В.И., Баев А.Е., Шестакова Л.Г., Полонецкий О.Л., Базылев В.В., Евдокимов М.Е., Шматков М.Г., Певзнер Д.В. Временная механическая циркуляторная поддержка трансаортальным устройством с пульсирующим кровотоком iVAC 2L при чрескожном коронарном вмешательстве высокого риска — многоцентровой опыт. Российский кардиологический журнал. 2025;30(1):5856. https://doi.org/10.15829/1560-4071-2025-5856. EDN: UYZAVW
For citation:
Avetisyan E.A., Dorogun O.B., Krasnoperova E.V., Tarasov R.S., Ganyukov V.I., Baev A.E., Shestakova L.G., Polonetsky O.L., Bazylev V.V., Evdokimov M.E., Shmatkov M.G., Pevzner D.V. Temporary mechanical circulatory support with the iVAC 2L transaortic device in high-risk percutaneous coronary intervention — a multicenter experience. Russian Journal of Cardiology. 2025;30(1):5856. (In Russ.) https://doi.org/10.15829/1560-4071-2025-5856. EDN: UYZAVW
Коронарная реваскуляризация, наряду с оптимальной медикаментозной терапией, является интервенцией, позволяющей улучшить функциональный статус и/или прогноз у пациентов с хронической ишемической болезнью сердца, многососудистым поражением коронарного русла и хронической сердечной недостаточностью. Методом выбора у пациентов с многососудистым или комплексным поражением является коронарное шунтирование, однако именно у этих пациентов зачастую операция на открытом сердце сопряжена с высоким риском осложнений [1]. В этом случае может быть рассмотрена реваскуляризация методом чрескожного коронарного вмешательства (ЧКВ), но даже в малоинвазивной процедуре пациенту может быть отказано ввиду высокого риска перипроцедурных и поздних осложнений, нивелирующих пользу интервенции [1].
Одним из вариантов осуществления относительно безопасной реваскуляризации у этих больных является методика защищенного ЧКВ с применением устройств временной механической циркуляторной поддержки (МЦП) [1].
Защищенное ЧКВ предполагает имплантацию временного устройства МЦП непосредственно перед коронарной интервенцией, обеспечение вспомогательного кровообращения в период вмешательства и иногда в ранний послеоперационный период с целью снижения риска осложнений и/или обеспечения эффективного кровообращения в условиях развития осложнений (ишемия миокарда, гемодинамическая нестабильность, жизнеугрожающие нарушения ритма и проводимости, остановка кровообращения).
Показание к проведению защищенного ЧКВ определяется понятием ЧКВ высокого риска, которое включает риски, связанные с пациентом, объемом сосудистого поражения и гемодинамическим статусом [2]. В определении ЧКВ высокого риска ФГБНУ "НИИ комплексных проблем сердечно-сосудистых заболеваний" особое место занимает оценка объема жизнеспособного миокарда, кровоснабжаемого целевым сосудом, по шкале Jeopardy [3][4].
Устройство МЦП, применяемое для защиты ЧКВ, должно обеспечивать эффективное вспомогательное кровообращение, иметь хороший профиль безопасности и не быть противопоказано конкретному пациенту. На сегодняшний день трансаортальные непрерывно-поточные устройства семейства Impella рекомендованы для защиты ЧКВ высокого риска, т. к. являются наиболее изученными [2][4]. Однако они не зарегистрированы на территории Российской Федерации, что ограничивает их использование.
Альтернативным устройством трансаортальной МЦП является iVAC 2L (PulseCath B. V., Нидерланды) [5]. Доказательные данные по применению этого устройства ограничены, однако схожий по характеру с устройством Impella гемодинамический эффект и хороший профиль безопасности позволяют ожидать позитивного влияния на прогноз [6].
Материал и методы
Исследование было выполнено в соответствии со стандартами надлежащей клинической практики (Good Clinical Practice), принципами Хельсинкской декларации и одобрено Этическими комитетами всех участвующих клинических центров. До включения в исследование у всех участников было получено письменное информированное согласие.
В пилотное международное многоцентровое исследование включались пациенты с многососудистым и/или комплексным поражением коронарного русла, которым было отказано в проведении коронарного шунтирования, а риски ЧКВ определялись как высокие.
Все клинические решения принимались кардио-командой учреждения. Риск ЧКВ оценивался по шкале CHIP (Complex High-Risk Indicated PCI) или на основании критериев ФГБНУ "НИИ комплексных проблем сердечно-сосудистых заболеваний" [2-4].
С целью МЦП применялась трансаортальная система с пульсирующим кровотоком iVAC 2L, состоящая из наружного двухкамерного мембранного насоса, кровяная камера которого соединена с катетером диаметром 17 Fr, а воздушная присоединяется к консоли для внутриаортальной баллонной контрпульсации (рис. 1). Чрескожный сосудистый доступ обеспечивался установкой интродьюсера 18 Fr в бедренную артерию, гемостаз — двумя сшивающими устройствами ProGlide.
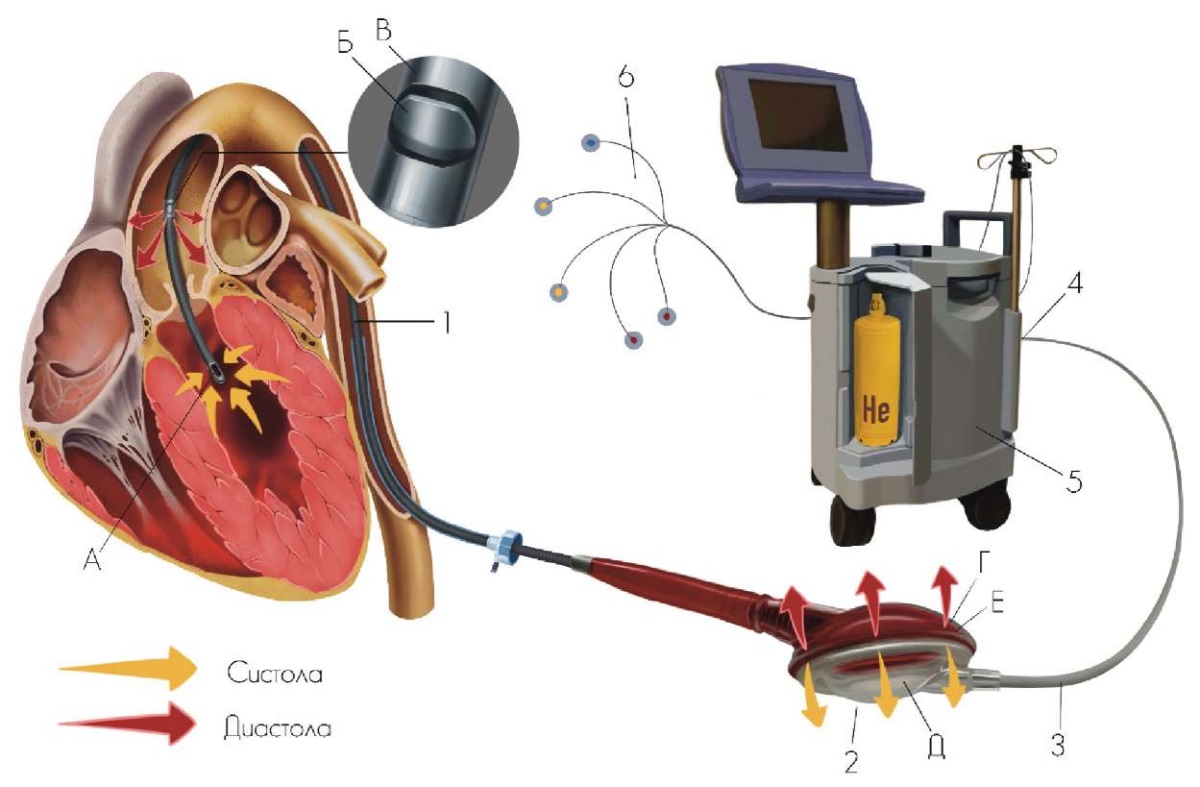
Рис. 1. Дизайн и принцип работы устройства iVAC 2L.
Примечание: кровоток в устройстве iVAC 2L поддерживается наполнением кровью камеры мембранного насоса в систолу (через дистальную заборную часть в левом желудочке) и выбросом крови из нее в диастолу (через проксимальную возвратную часть в восходящей аорте) благодаря нагнетанию в воздушную камеру мембранного насоса гелия консолью для внутриаортальной баллонной контрпульсации. Объем камеры мембранного насоса составляет 40 мл, объем вспомогательного выброса из левого желудочка при каждом цикле — 21 мл. Составные части системы: 1 — катетер насоса (А — заборная дистальная часть, Б — возвратная проксимальная часть, В — двусторонний клапан), 2 — мембранный двухкамерный насос (Г — камера крови, Д — камера гелия, Е — мембрана), 3 — воздушная линия, 4 — адаптер, 5 — консоль для внутриаортальной баллонной контрпульсации, 6 — электроды электрокардиографические. Цветное изображение доступно в электронной версии журнала.
Катетер iVAC 2L позиционировался в левый желудочек (ЛЖ) на 2-3 см ниже клапана аорты под прямым рентгеноскопическим контролем (рис. 2). Синхронизация с фазами сердечного цикла осуществлялась по ЭКГ или проводилась асинхронная поддержка в условиях бради- и тахиаритмий, сердечно-легочной реанимации.
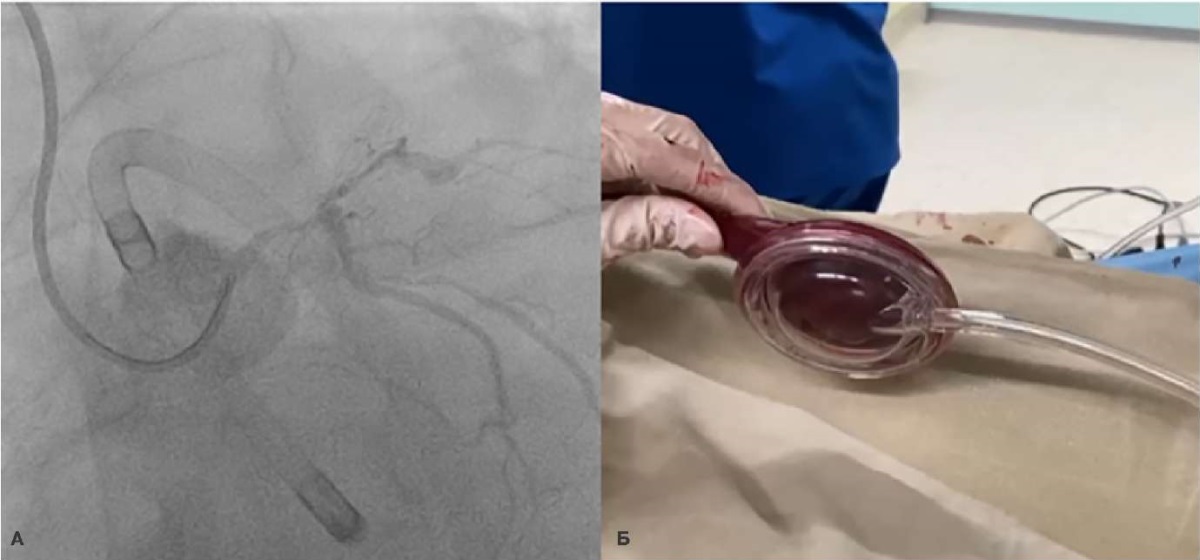
Рис. 2. А — устройство iVAC 2L в трансаортальной позиции. Б — мембранный насос.
Антикоагуляция в течение процедуры обеспечивалась введением нефракционированного гепарина с достижением значений активированного времени свертывания не менее 200 сек.
Предварительно у всех пациентов были исключены противопоказания к имплантации устройства (табл. 1).
Таблица 1
Противопоказания к применению iVAC 2L [5]
|
Стеноз бедренной артерии (диаметр <6 мм) |
|
Стеноз или недостаточность аортального клапана |
|
Механический аортальный клапан |
|
Тромбоз левого желудочка |
|
Правожелудочковая недостаточность* |
|
Дефект межжелудочковой перегородки |
|
Разрыв свободной стенки левого желудочка |
|
Тампонада сердца |
|
Недавнее (<6 мес.) острое нарушение мозгового кровообращения |
|
Недавнее (<6 мес.) крупное кровотечение |
Примечание: * — недостаточность правого желудочка является условным ограничением, нежели противопоказанием.
Стентирование коронарных артерий проводилось стентами с лекарственным покрытием 3 поколения. Внутрисосудистая визуализация применялась по усмотрению оперирующей бригады.
С целью анализа статистических данных использовалось программное обеспечение The IBM® SPSS® Statistics. Оценка нормальности распределения количественных переменных проводилась с помощью критерия Шапиро-Уилка. Выбор статистического критерия для сравнения количественных параметров для связанных выборок зависел от распределения: парный Т-тест Стьюдента для нормального распределения и критерий Уилкоксона для ненормального распределения.
Результаты
В серию клинических наблюдений было включено 24 пациента из 5 учреждений (22 пациента проспективно, 2 пациента ретроспективно). У 20 пациентов (83,7%) защищенное ЧКВ было плановым, у 4 пациентов (16,7%) процедура проводилась в условиях острого коронарного синдрома (ОКС), в т. ч. у 1 пациента с острой сердечной недостаточностью (ОСН). Исходные клинико-демографические характеристики указаны в таблице 2. Медиана фракции выброса ЛЖ составила 44,0% (интерквартильных размах (ИКР): 31,0-54,0), у 16,7% (n=4/24) отмечалась тяжелая митральная регургитация. Подавляющее большинство пациентов (83,3%) имели трехсосудистое поражение коронарного русла, медиана по шкале SYNTAX составила 35,0 баллов (ИКР: 25,6-41,4).
Таблица 2
Исходная клинико-демографическая характеристика пациентов
|
Характеристика |
Значение |
|
Медиана возраста (ИКР), годы |
69,0 (63,5-71,8) |
|
Мужской пол, % (n) |
87,5 (21) |
|
Медиана ИМТ (ИКР), кг/м² |
28,4 (24,2-31,2) |
|
Факторы риска |
|
|
Курение, % (n) |
33,3 (8) |
|
Артериальная гипертензия, % (n) |
91,7 (22) |
|
Сахарный диабет, % (n) |
25,0 (6) |
|
Дислипидемия, % (n) |
75,0 (18) |
|
Анамнестические данные |
|
|
Хроническая сердечная недостаточность, % (n) |
|
|
— со сниженной фракцией выброса |
41,7 (10) |
|
— с умеренно сниженной фракцией выброса |
20,8 (5) |
|
— с сохранной фракцией выброса |
8,3 (2) |
|
Инфаркт миокарда в анамнезе, % (n) |
62,5 (15) |
|
Предшествующие ЧКВ, % (n) |
25,0 (6) |
|
Предшествующие коронарные шунтирования, % (n) |
8,3 (2) |
|
Желудочковые нарушения ритма, % (n) |
16,7 (4) |
|
Фибрилляция предсердий, % (n) |
25,0 (6) |
|
ОНМК, % (n) |
20,8 (5) |
|
Заболевание периферических артерий, % (n) |
50,0 (12) |
|
Хроническая болезнь почек (стадия С3а по KDIGO и выше), % (n) |
37,5 (9) |
|
Онкологическое заболевание, % (n) |
12,5 (3) |
|
Эхокардиографические параметры |
|
|
Недостаточность митрального клапана (3 степени и выше), % (n) |
16,7 (4) |
|
Медиана фракция выброса левого желудочка (ИКР), % |
44,0 (31,0-54,0) |
Сокращения: ИКР — интерквартильный размах, ИМТ — индекс массы тела, ОНМК — острое нарушение мозгового кровообращения, ЧКВ — чрескожное коронарное вмешательство.
Всем пациентам была выполнена успешная имплантация устройства МЦП, медиана времени работы устройства составила 66,0 мин (ИКР: 43,0-98,0), у одного пациента МЦП была прекращена досрочно в связи с дислокацией устройства, в остальных случаях — после завершения ЧКВ. 13 пациентам процедура проводилась на фоне местной аналгезии и умеренной внутривенной седации. 11 процедур проводилось на фоне общей анестезии и инвазивной механической вентиляции легких в связи с явлениями ОСН до процедуры и после плановой интубации. 1 пациент был переведен на искусственную вентиляцию легких (ИВЛ) во время процедуры в связи с развитием остановки кровообращения.
У 2 из 24 пациентов процедура осложнилась остановкой кровообращения. У одного пациента остановка кровообращения по механизму желудочковой тахикардии наблюдалась на фоне ИВЛ, ОСН, после позиционирования iVAC 2L в полость ЛЖ во время баллонной предилатации места стеноза в стволе левой коронарной артерии. После успешных реанимационных мероприятий наблюдалась дислокация устройства в восходящую аорту. Далее МЦП проводилась в супрааортальной позиции, выполнено успешное полное ЧКВ с отлучением от МЦП в рентген-операционной. Разрешение ОСН и отлучение от ИВЛ наблюдалось в течение суток после реваскуляризации. У второго пациента остановка кровообращения наблюдалась после выполнения планового ЧКВ вследствие прогрессирования левожелудочковой недостаточности.
Данные о технических характеристиках вмешательства и перипроцедурных осложнениях представлены в таблице 3.
Таблица 3
Характеристика выполненных процедур защищенного ЧКВ
|
Характеристика |
Значение |
|
Параметры коронарной ангиографии |
|
|
3-сосудистое поражение, % (n) |
83,3 (20) |
|
Поражение ствола левой коронарной артерии, % (n) |
50,0 (12) |
|
Медиана оценки по шкале SYNTAX (ИКР), баллы |
35,0 (25,6-41,4) |
|
Параметры ЧКВ |
|
|
Показание к ЧКВ: |
|
|
— стабильная стенокардия, % (n) |
75,0 (18) |
|
— ОКС, % (n) |
16,7 (4) |
|
Медиана длительности механической поддержки (ИКР), мин |
66,0 (43,0-98,0) |
|
Режим работы устройства: |
|
|
— internal, % (n) |
29,2 (7) |
|
— синхронизация по ЭКГ, % (n) |
66,7 (16) |
|
Использование внутрисосудистого ультразвукового исследования, % (n) |
20,8 (5) |
|
Медиана объема использованного контрастного вещества (ИКР), мл |
300,0 (200,0-400,0) |
|
Осложнения во время ЧКВ: |
|
|
— гипотензия/шок, % (n) |
12,5 (3) |
|
— сердечно-легочная реанимация, % (n) |
8,3 (2) |
|
— дислокация устройства, % (n) |
8,3 (2) |
|
— экстренная интубация, % (n) |
4,2 (1) |
|
— желудочковая экстрасистолия, % (n) |
25,0 (6) |
|
Смерть во время ЧКВ, % (n) |
4,2 (1) |
Сокращения: ИКР — интерквартильный размах, ОКС — острый коронарный синдром, ЧКВ — чрескожное коронарное вмешательство, ЭКГ — электрокардиограмма.
Технический успех процедуры ЧКВ был достигнут в 100% случаев. Максимальная, по мнению оператора, реваскуляризация была выполнена у всех пациентов с достижением среднего резидуального SYNTAX 8,0 баллов (ИКР: 5,0-17,5). Отмечался статистически значимый прирост медианы фракции выброса ЛЖ до 48,0% через 7 дней после ЧКВ (р=0,028).
91,7% пациентов (22/24) были выписаны из стационара с улучшением общего состояния. Один пациент скончался во время элективного вмешательства от прогрессирования недостаточности ЛЖ и второй в отдаленные сроки от экстренного ЧКВ на фоне ОКС и ОСН вследствие септического шока, источником которого служила внутрибольничная бактериальная пневмония. Данные о результатах вмешательства представлены в таблице 4.
Таблица 4
Результаты защищенного ЧКВ
|
Характеристика |
Значение |
|
Успешное стентирование, % (n) |
100,0 (15) |
|
Средняя резидуальная оценка по шкале SYNTAX (ИКР), баллы |
8,0 (5,0-17,5) |
|
Медиана количества стентированных стенозов (ИКР), n |
3,0 (2,0-3,0) |
|
Медиана ФВ ЛЖ через 7 дней после ЧКВ (ИКР), % |
48,0 (36,5-53,5) |
|
Осложнения после ЧКВ в течение госпитализации: |
|
|
— ОНМК, % (n) |
0,0 (0) |
|
— ОИМ, % (n) |
0,0 (0) |
|
— ОПП, % (n) |
4,2 (1) |
|
— Крупное кровотечение из места доступа по BARC (3 тип), % (n) |
8,3 (2) |
|
— Гемотрансфузии, % (n) |
8,3 (2) |
|
— Крупное кровотечение из иного источника по BARC (3 тип), % (n) |
0,0 (0) |
|
— Гемолиз, % (n) |
0,0 (0) |
|
Смерть после ЧКВ в течение госпитализации, % (n) |
4,2 (1) |
Сокращения: ИКР — интерквартильный размах, ОНМК — острое нарушение мозгового кровообращения, ОИМ — острый инфаркт миокарда, ОПП — острое почечное повреждение, ФВ ЛЖ — фракция выброса левого желудочка, ЧКВ — чрескожное коронарное вмешательство, BARC — Bleeding Academic Research Consortium.
9 пациентам (37,5%) проводилась инвазивная оценка гемодинамики путем катетеризации правых отделов сердца до вмешательства, на фоне МЦП и после отлучения. Результаты представлены в таблице 5.
Таблица 5
Инвазивная оценка гемодинамики
|
Медиана ЧСС (ИКР), уд./мин |
Медиана среднего АД (ИКР), мм рт.ст. |
Медиана сердечного выброса (ИКР), л/мин |
Медиана ДЗЛА (ИКР), мм рт.ст. |
|
|
До МЦП |
67,0 (61,0-86,0) |
87,0 (76,0-97,0) |
4,64 (3,61-5,43) |
15,0 (13,0-16,0) |
|
На фоне МЦП |
68,5 (63,5-102,3) |
82,5 (72,5-89,0) |
4,41 (3,98-5,08) |
16,0 (15,0-18,0) |
|
Значимость (двухсторонняя) |
р=0,36 |
р=0,24 |
р=0,62 |
р=0,046 |
|
После МЦП* |
67,0 (57,0-98,0) |
88,0 (80,5-92,0) |
4,07 (3,76-4,88) |
16,0 (13,5-20,5) |
Примечание: * — у 3 пациентов отсутствуют данные инвазивной гемодинамики после процедуры.
Сокращения: АД — артериальное давление, ДЗЛА — давление заклинивания легочной артерии, ИКР — интерквартильный размах, МЦП — механическая циркуляторная поддержка, ЧСС — частота сердечных сокращений.
Обсуждение
В современной отечественной практике доступными методиками МЦП являются внутриаортальная баллонная контрпульсация и вено-артериальная экстракорпоральная мембранная оксигенация. Однако для процедуры защищенного ЧКВ рекомендованы трансаортальные насосы [2]. При этом, по результатам серии крупных исследований, среди трансаортальных устройств рекомендованы микроаксиальные насосы семейства Impella (Abiomed, США) [4].
Устройство iVAC 2L имеет ограниченную доказательную базу. Безопасность и эффективность при ЧКВ высокого риска были продемонстрированы в ряде клинических случаев и в небольших наблюдательных исследованиях. В них было показано, что устройство имеет хороший профиль безопасности, обладает существенным влиянием на гемодинамику и, вероятно, улучшает исходы в сравнении с ЧКВ без МЦП.
В работах den Uil CA, et al. (n=14) и Samol A, et al. (n=20) использование устройства ассоциировалось с увеличением сердечного выброса и среднего артериального давления, при этом доля успешных ЧКВ достигла 100% [7][8]. В исследовании Ameloot K, et al. сравнивалось использование нескольких видов устройств МЦП (iVAC 2L, Impella CP, HeartMate PHP (Abbott, США)) при ЧКВ высокого риска с проведением незащищенных процедур (n=69 vs n=129). По его итогам было выявлено, что защита ЧКВ устройством МЦП позволяет значимо повысить выживаемость в первые 24 ч и 30 дней (100% vs 95%, p=0,04 за 24 ч, 98% vs 87%, отношение шансов 10,32, 95% доверительный интервал: 1,34-79,31, p=0,006 за 30 дней). Устройство iVAC 2L применялось у 38% пациентов, субанализ по различным устройствам не проводился [9].
На сегодняшний день самым крупным исследованием, определившим ответчиков для устройства iVAC 2L, является PULSE Trial [10]. По его результатам улучшение параметров гемодинамики наиболее выражено у пациентов с перенесенным ОКС и тяжелой митральной регургитацией.
В нашем исследовании представлены наиболее крупные совокупные данные о применении трансаортального устройства PulseCath iVAC 2L в России и Белоруссии. Впервые представлены данные о защищенном ЧКВ устройством iVAC 2L у пациентов с ОКС и ОСН.
Оценка гемодинамического эффекта iVAC 2L проводилась с помощью катетеризации правых отделов сердца и препульмональной термодиллюции у 9 пациентов (37,5%). Значимого прироста сердечного выброса на фоне гемодинамической поддержки не отмечалось. С нашей точки зрения, это связано с принципом работы трансаортальных устройств и возможным перипроцедурным дефицитом ОЦК вследствие кровопотери при установке устройства и ЧКВ.
Как показано на рисунке 3 А, на фоне работы трансаортальных устройств (на примере постоянно-поточного насоса Impella) происходит постепенное снижение собственного сердечного выброса по мере нарастания производительности насоса. При этом начальный темп прироста суммарного выброса в системную циркуляцию (при производительности насоса до 1,5-2 л/мин) небольшой, а на фоне абсолютного дефицита ОЦК, а также пульсового характера вспомогательного кровотока, он может вовсе отсутствовать.
На рисунке 3 Б показано, как меняется кривая давление-объем ЛЖ на фоне работы iVAC 2L — происходит ее объемная разгрузка. Это снижает работу желудочка, натяжение миокарда и потребление им кислорода, улучшается коронарная перфузия. Все эти гемодинамические эффекты, наряду с протезированием насосной функции сердца в моменты критического снижения собственного выброса могут позволить избежать фатальных осложнений ЧКВ.
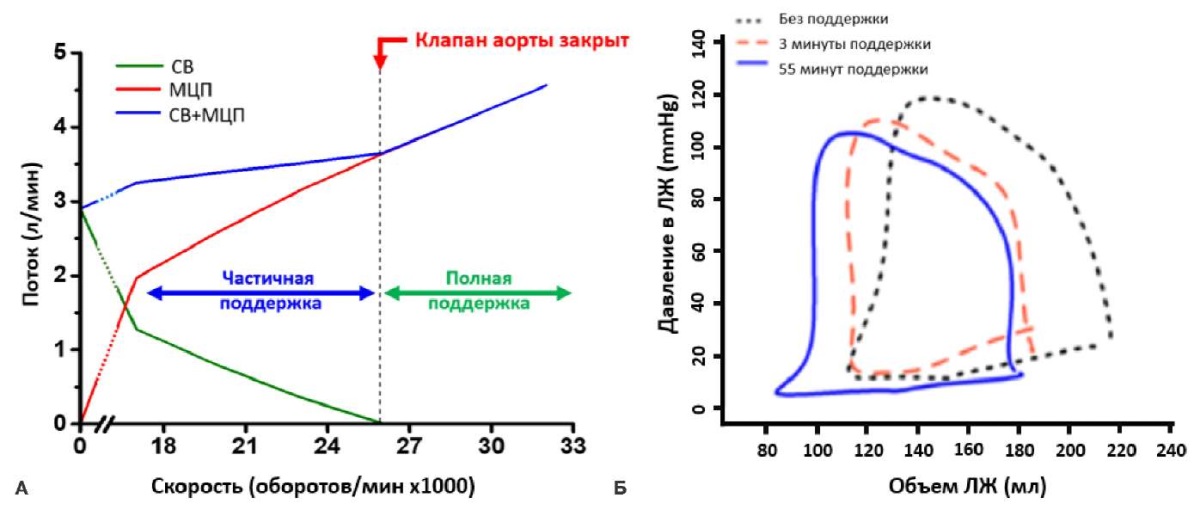
Рис. 3. А — динамика сердечного выброса и суммарного выброса в системную циркуляцию на фоне работы постоянно-поточного трансаортального насоса. Б — кривая давление-объем ЛЖ на фоне поддержки устройством iVAC 2L [5].
Примечание: цветное изображение доступно в электронной версии журнала.
Сокращения: ЛЖ — левый желудочек, МЦП — механическая циркуляторная поддержка, СВ — сердечный выброс.
В нашем пилотном исследовании у 2 пациентов (8,3%) наблюдались значимые кровотечения (3 тип по классификации BARC — Bleeding Academic Research Consortium) в ранний послеоперационный период из места артериального доступа устройства. Следует отметить, что у одного из пациентов отмечался выраженный кальциноз общей бедренной артерии, что послужило причиной несостоятельности швов ProGlide. Данный аспект в будущем учитывался при подборе пациентов.
По данным регистра PulseCath наиболее частыми осложнениями являются крупное кровотечение, значимое сосудистое осложнение или дыхательная недостаточность во время процедуры (10,7%), гемодинамическая нестабильность (7,7%), острое почечное повреждение, цереброваскулярное событие (острое нарушение мозгового кровообращения, транзиторная ишемическая атака), осложнение места доступа (по 6,1%)1.
Самым частым ассоциированным с МЦП осложнением в серии наших наблюдений выступали аритмии. У 5 пациентов (20,8%) в процессе работы устройства регистрировалась частая желудочковая экстрасистолия с эпизодами аллоритмии (преимущественно бигеминии) и пароксизмами неустойчивой мономорфной желудочковой тахикардии. Аритмии купировались при отключении устройства и возобновлялись с началом поддержки, что позволило судить об их связи с работой насоса. С точки зрения авторов, патогенез данных аритмий кроется в механическом раздражении выносящего тракта ЛЖ заборной частью катетера iVAC 2L.
В литературе нет данных о частоте развития насос-ассоциированных аритмий при поддержке iVAC 2L и методах их коррекции. У наших пациентов аритмии не имели очевидного негативного эффекта на гемодинамику, показатели работы устройства оставались целевыми, удавалось добиться технического успеха ЧКВ. В связи с этим, вероятно, аритмии при работе устройства iVAC 2L имеют доброкачественный характер и не требуют прерывания поддержки при условии стабильной гемодинамики.
В литературе данные о применении iVAC 2L при экстренных ЧКВ и ОСН ограничены [11][12], но наш позитивный опыт позволяет задуматься о расширении показаний к применению МЦП устройством iVAC 2L при ЧКВ очень высокого риска.
Ограничения исследования. Небольшое количество наблюдений и отсутствие группы сравнения, что не позволяет судить о сравнительной эффективности и безопасности процедуры защищенного ЧКВ устройством iVAC 2L. Также у 3 пациентов отсутствовали данные инвазивной гемодинамики после процедуры.
Заключение
В статье представлен уникальный опыт трансаортальной МЦП устройством iVAC 2L при ЧКВ очень высокого риска у четырех пациентов с ОКС, из них у одного пациента с ОСН.
Отношения и деятельность: все авторы заявляют об отсутствии потенциального конфликта интересов, требующего раскрытия в данной статье.
1. Pulsecath IVAC 2L Post-¬Market Surveillance Registry Report. https://www.pulsecath.com/wp-content/uploads/2022/12/PMS_report_marketing_R1058-1-2022.pdf (23 March 2024).
Список литературы
1. Neumann FJ, Sousa-Uva M, Ahlsson A, et al. 2018 ESC/EACTS Guidelines on myocardial revascularization. Eur Heart J. 2019;40(2):87-165. doi:10.1093/eurheartj/ehy394.
2. Chieffo A, Dudek D, Hassager C, et al. Joint EAPCI/ACVC expert consensus document on percutaneous ventricular assist devices. Eur Heart J Acute Cardiovasc Care. 2021;10(5):570-83. doi:10.1093/ehjacc/zuab015.
3. Ganyukov V, Sucato V, Vereshchagin I, et al. Outcome of extracorporeal membrane oxygenation support for high-risk percutaneous coronary intervention in non-ST-segment elevation acute coronary syndrome. J Cardiovasc Med (Hagerstown). 2021;22(5):423-4. doi:10.2459/JCM.0000000000001141.
4. Simonton C, Thompson C, Wollmuth JR, et al. The Role of Hemodynamic Support in High-risk Percutaneous Coronary Intervention. US Cardiol Rev. 2020;14:e13. doi:10.15420/icr.2015.10.1.39.
5. Bastos MB, Van Wiechen MP, Van Mieghem NM. PulseCath iVAC2L: next-generation pulsatile mechanical circulatory support. Future Cardiol. 2020;16(2):103-12. doi:10.2217/fca-2019-0060.
6. Samol A, Wiemer M, Kaese S. Comparison of a pulsatile and a continuous flow left ventricular assist device in high-risk PCI. Int J Cardiol. 2022;360:7-12. doi:10.1016/j.ijcard.2022.05.038.
7. Den Uil C, Daemen J, Lenzen M, et al. Pulsatile iVAC 2L circulatory support in high-risk percutaneous coronary intervention. EuroIntervention. 2017;12(14):1689-96. doi:10.4244/EIJ-D-16-00371.
8. Samol A, Schmidt S, Zeyse M, et al. High-risk PCI under support of a pulsatile left ventricular assist device — First German experience with the iVAC2L system. Int J Cardiol. 2019;297:30-5. doi:10.1016/j.ijcard.2019.10.020.
9. Ameloot K, B Bastos M, Daemen J, et al. New-generation mechanical circulatory support during high-risk PCI: a cross-sectional analysis. EuroIntervention. 2019;15(5):427-33. doi:10.4244/EIJ-D-18-01126.
10. Bastos MB, McConkey H, Malkin O, et al. Effect of Next Generation Pulsatile Mechanical Circulatory Support on Cardiac Mechanics: The PULSE Trial. Cardiovasc Revasc Med. 2022;42:133-42. doi:10.1016/j.carrev.2022.03.013.
11. Tzikas S, Papadopoulos CH, Evangeliou AP, et al. First implantation of the pulsatile left ventricular assist device iVAC2L in a heart failure patient infected with influenza type A. Hellenic J Cardiol. 2021;62(4):326-8. doi:10.1016/j.hjc.2020.05.002.
12. Delmas C, Porterie J, Jourdan G, et al. Effectiveness and Safety of a Prolonged Hemodynamic Support by the IVAC2L System in Healthy and Cardiogenic Shock Pigs. Front Cardiovasc Med. 2022;9:809143. doi:10.3389/fcvm.2022.809143.
Об авторах
Э. А. АветисянРоссия
Аветисян Эрик Арменович — врач-кардиолог блока интенсивной терапии отдела неотложной кардиологии.
Москва
Конфликт интересов:
Нет
О. Б. Дорогун
Россия
Дорогун Олег Борисович — ординатор отдела неотложной кардиологии.
Москва
Конфликт интересов:
Нет
Е. В. Красноперова
Россия
Красноперова Елизавета Витальевна — ординатор отдела неотложной кардиологии.
Москва
Конфликт интересов:
Нет
Р. С. Тарасов
Россия
Тарасов Роман Сергеевич — д. м. н., доцент, зав. лабораторией рентгенэндоваскулярной и реконструктивной хирургии сердца и сосудов отдела хирургии сердца и сосудов.
Кемерово
Конфликт интересов:
Нет
В. И. Ганюков
Россия
Ганюков Владимир Иванович — д. м. н., зав. отделом хирургии сердца и сосудов.
Кемерово
Конфликт интересов:
Нет
А. Е. Баев
Россия
Баев Андрей Евгеньевич — к.м.н., зав. отделением рентгенохирургических методов диагностики и лечения.
Томск
Конфликт интересов:
Нет
Л. Г. Шестакова
Беларусь
Шестакова Лиана Геннадьевна — д. м. н., профессор, зав. отделом экстракорпоральной поддержки жизни.
Минск
Конфликт интересов:
Нет
О. Л. Полонецкий
Беларусь
Полонецкий Олег Леонидович — к.м.н., зав. отделением рентген-эндоваскулярной хирургии.
Минск
Конфликт интересов:
Нет
В. В. Базылев
Россия
Базылев Владлен Владленович — д.м.н., профессор, главный врач.
Пенза
Конфликт интересов:
Нет
М. Е. Евдокимов
Россия
Евдокимов Михаил Евгеньевич — к.м.н., зав. отделением анестезиологии-реанимации.
Пенза
Конфликт интересов:
Нет
М. Г. Шматков
Россия
Шматков Марк Георгиевич — к.м.н., зав. отделением рентген-эндоваскулярной хирургии.
Пенза
Конфликт интересов:
Нет
Д. В. Певзнер
Россия
Певзнер Дмитрий Вольфович — д. м. н., руководитель отдела неотложной кардиологии.
Москва
Конфликт интересов:
Нет
Дополнительные файлы
- В исследовании описан позитивный опыт использования устройства iVAC 2L при чрескожном коронарном вмешательстве высокого риска, в т. ч. при остром коронарном синдроме.
- В условиях механической циркуляторной поддержки устройством iVAC 2L технический успех процедуры чрескожного коронарного вмешательства был достигнут в 100% случаев.
- Одним из самых частых осложнений использования устройства является развитие насос-ассоциированных аритмий, которые носят доброкачественный характер.
Рецензия
Для цитирования:
Аветисян Э.А., Дорогун О.Б., Красноперова Е.В., Тарасов Р.С., Ганюков В.И., Баев А.Е., Шестакова Л.Г., Полонецкий О.Л., Базылев В.В., Евдокимов М.Е., Шматков М.Г., Певзнер Д.В. Временная механическая циркуляторная поддержка трансаортальным устройством с пульсирующим кровотоком iVAC 2L при чрескожном коронарном вмешательстве высокого риска — многоцентровой опыт. Российский кардиологический журнал. 2025;30(1):5856. https://doi.org/10.15829/1560-4071-2025-5856. EDN: UYZAVW
For citation:
Avetisyan E.A., Dorogun O.B., Krasnoperova E.V., Tarasov R.S., Ganyukov V.I., Baev A.E., Shestakova L.G., Polonetsky O.L., Bazylev V.V., Evdokimov M.E., Shmatkov M.G., Pevzner D.V. Temporary mechanical circulatory support with the iVAC 2L transaortic device in high-risk percutaneous coronary intervention — a multicenter experience. Russian Journal of Cardiology. 2025;30(1):5856. (In Russ.) https://doi.org/10.15829/1560-4071-2025-5856. EDN: UYZAVW
JATS XML

















































