Перейти к:
Факторы, определяющие исходы у пациентов с тромбоэмболией легочной артерии и недавней перенесенной инфекцией COVID-19
https://doi.org/10.15829/1560-4071-2024-5633
EDN: UIDPDN
Аннотация
Цель. Изучить факторы, влияющие на исходы у пациентов с тромбоэмболией легочной артерии (ТЭЛА) и недавней перенесенной новой коронавирусной инфекцией (COVID-19).
Материал и методы. Проведено ретроспективное наблюдательное исследование с участием пациентов, госпитализированных в отделение неотложной кардиологии в период с января 2020г по декабрь 2021г. Анализировались две группы пациентов в зависимости от наличия анамнеза недавней (до 3 мес.) перенесенной COVID-19.
Результаты. 113 пациентов, госпитализированных с ТЭЛА в изучаемый период, соответствовали необходимым критериям включения. Из них 44 составляли пациенты с недавним анамнезом COVID-19, 69 — без анамнеза инфекции. При оценке раннего периода пандемии 2020-2021гг летальность составила 23,5% и 7,5% в группе с анамнезом новой коронавирусной инфекции и без анамнеза, соответственно, p=0,023 (χ2=5,19). Пациенты с недавней COVID-19 чаще имели периферическое тромботическое поражение легочной артерии, реже — классические признаки ТЭЛА. Пациенты с летальным исходом чаще страдали сахарным диабетом 2 типа, имели выше уровни тропонина крови, расчетные значения по шкалам риска, ниже средние значения тромбоцитов, скорости клубочковой фильтрации, имели хуже показатели гемодинамики в момент госпитализации, выше давление в легочной артерии по данным эхокардиографии. Среди всех факторов наибольшим неблагоприятным влиянием обладали низкие значения систолического и диастолического артериального давления на момент госпитализации, снижение скорости клубочковой фильтрации, высокий риск по шкале sPESI.
Заключение. Даже с учетом окончания пандемии, важным является изучение факторов, влияющих на течение ТЭЛА при COVID-19. Это может иметь значение при оценке отдаленных осложнений. Пациенты с ТЭЛА и недавней перенесенной COVID-19 имеют отличительные особенности клинической картины и тенденцию к более высокой летальности в ранний период пандемии. Летальность выше при наличии как факторов, обусловленных тяжестью предшествующей инфекции, так и ранее изученных факторов, определяющих неблагоприятный прогноз ТЭЛА.
Ключевые слова
Для цитирования:
Кононов С.К., Соловьёв О.В., Краев А.Р., Ральникова У.А., Гребенева Е.В. Факторы, определяющие исходы у пациентов с тромбоэмболией легочной артерии и недавней перенесенной инфекцией COVID-19. Российский кардиологический журнал. 2024;29(9):5633. https://doi.org/10.15829/1560-4071-2024-5633. EDN: UIDPDN
For citation:
Kononov S.K., Solovev O.V., Kraev A.R., Ralnikova U.A., Grebeneva E.V. Determinants of outcomes in patients with pulmonary embolism and recent COVID-19 infection. Russian Journal of Cardiology. 2024;29(9):5633. (In Russ.) https://doi.org/10.15829/1560-4071-2024-5633. EDN: UIDPDN
Венозные тромбоэмболии, в т. ч. тромбоэмболия легочной артерии (ТЭЛА), при новой коронавирусной инфекции (COVID-19) встречаются чаще, чем при других вирусных пневмониях. До пандемии частота легочной эмболии (ЛЭ) у пациентов c вирусными пневмониями в отделениях интенсивной терапии или с респираторным дистресс синдромом составляла 1,3-7,5% [1]. В одном из метаанализов 27 исследований с участием 3342 пациентов из разных стран c COVID-19 в первые 6 мес. 2020г показано, что частота ЛЭ и тромбоза глубоких вен (ТГВ) была 16,5% и 14,8%, соответственно [2]. При обычном скрининговом подходе к проведению компьютерной томографии (КТ), ЛЭ может чаще выявляться в отделениях интенсивной терапии (24,7% vs 10,5% в обычных отделениях). В одном из исследований по сравнению частоты ТГВ до и во время пандемии показано, что частота выявления тромбоза возросла с 3,9 до 15,1% [3]. Результаты российских регистров демонстрируют частоту выявления ТГВ и ТЭЛА <1% даже среди стационарных больных [4]. В одном из немногих отечественных исследований демонстрируется частота смертельных исходов, нефатальной ТЭЛА, ТГВ на уровне 8,9% [5]. Данные указывают, возможно, на недостаточный скрининг на тромбоэмболические осложнения в российских условиях [6]. В сравнении с зарубежными работами, существует относительно небольшое количество отечественных публикаций, в которых изучались тромбоэмболические исследования у пациентов с COVID-19.
Данные о прогностической роли ЛЭ при COVID-19 противоречивы. Пациенты с тромбоэмболическими осложнениями могут иметь выше риск смерти. На 74% выше, как в одном крупном метаанализе. При этом ЛЭ может выявляться только посмертно, недостаточный скрининг может искажать наши представления о влиянии ЛЭ на прогноз [7]. В любом случае, публикуемые показатели летальности выше, чем летальность при вирусных пневмониях в регистрах до пандемии [8]. Пациенты с диагностированными тромбоэмболиями на фоне COVID-19 могут чаше лечиться в условиях отделений интенсивной терапии, иметь более длительные сроки госпитализации, им чаще проводится искусственная вентиляция легких, но это не всегда ассоциировано с ухудшением прогноза. Это демонстрируется в исследовании с участием 1240 пациентов. Показано: ЛЭ не связана с повышенной летальностью, пациенты с COVID-19 без ЛЭ имеют сопоставимую летальность [8].
Риск развития ЛЭ при COVID-19 не укладывается в традиционные тромбоэмболические факторы риска [9]. Традиционные алгоритмы диагностики недостаточно эффективны. Шкалы, такие как Wells, для определения претестовой вероятности, хорошо валидированные для классической ЛЭ, не изучены у больных с COVID-19 и неэффективны на практике [10]. Недостаточно изученным является возможность применения расчетных прогностических индексов Pulmonary Embolism Severity Index (PESI), Simplified PESI (sPESI) у больных с COVID-19 [11].
Особенности клинической картины ЛЭ в остром периоде COVID-19 хорошо изучены. Результаты многих исследований клинической картины ЛЭ согласуются — в остром периоде инфекции чаще наблюдается локализация тромботического процесса в субсегментарных и сегментарных ветвях [12-16]. Исследований вне острого периода мало. При этом до пандемии поражение мелких ветвей при ЛЭ было связано с низкой смертностью, смертность в большей степени зависела от наличия поражения правых отделов сердца [17].
Временные рамки между инфекцией и ЛЭ могут быть достаточно широкими. Неясно, является ли диагностированная ЛЭ проявлением постковидного состояния. Доказательная база по данной проблеме ограничена небольшими исследованиями, часто клиническими случаями [18-22].
В исследовании нами проведен анализ клиники и исходов, определены факторы, ассоциированные с летальным исходом у пациентов с ЛЭ, диагностированной после перенесенной COVID-19.
Цель исследования: изучить факторы, влияющие на развитие неблагоприятного исхода у пациентов с ТЭЛА и недавней перенесенной COVID-19.
Материал и методы
В ретроспективное наблюдательное исследование включались пациенты кардиологического отделения Центра кардиологии и неврологии, госпитализированные с диагнозом ЛЭ в период с января 2020г по декабрь 2021г. Критерием включения являлось наличие подтвержденного диагноза ЛЭ КТ-ангиографией легких. Из исследования исключались пациенты с предполагаемой острой формой инфекции и лабораторно подтвержденным выделением вируса, пациенты с неизвестным статусом по COVID-19, в т. ч. с невозможностью определения наличия специфических антител, пациенты с наличием антител к SARS-CoV-2 с неизвестным статусом по вакцинации в период проведения вакцинации в регионе. Также исключались пациенты с известной давностью инфекции >3 мес. (постковидный период). У всех пациентов, включенных в исследование, определялись основные клинико-демографические, лабораторные, инструментальные характеристики. Госпитальная летальность оценивалась за весь изучаемый период и отдельно за более ранний период до начала массовой вакцинации в регионе в феврале 2021г. Анализировались предикторы неблагоприятного исхода ЛЭ.
Статистический анализ проводился с использованием статистического пакета MS Excel. С учетом характера распределения использовались параметрические и непараметрические методы статистики, в т. ч. критерии Стьюдента, Манна-Уитни, а также χ² и точный критерий Фишера для качественных признаков. Различия считались значимыми при p<0,05. Оценка прогностической значимости количественных признаков проводилась с помощью логистического регрессионного анализа. Оценка значимости качественных признаков производилась с помощью расчета отношения шансов (ОШ).
Результаты
С учетом критериев включения и исключения проведен анализ клиники и исходов у 113 пациентов с ЛЭ. Выделено 2 группы пациентов: 44 пациента с анамнезом перенесенной COVID-19, средний возраст 64,3±13,5 г, женщины 52,3%. Во второй группе 69 пациентов без анамнеза инфекции, средний возраст 62,7±13,8, женщины 52,2%. Среди пациентов без анамнеза COVID-19 64 (93%) были госпитализированы в период до пандемии.
Пациенты обеих групп были сопоставимы по основным факторам риска и сопутствующей патологии. Наблюдалась тенденция к более высокой частоте сахарного диабета (СД) в группе пациентов с COVID-19 27,3% (p=0,057, χ²=3,59). Среди пациентов с анамнезом COVID-19 было значимо меньше курильщиков: 2,3% vs 21,7% (р=0,004). Пациенты с перенесенной COVID-19 имели более высокий риск по средним значениям шкалы IMPROVE-DD: 2,07±1,57 балла против 1,16±1,11 в группе без анамнеза COVID-19 (р<0,001). При этом количество пациентов с высоким риском значимо не различалось.
Большинство пациентов в группе ЛЭ с перенесенной COVID-19 имели анамнез среднетяжелого течения инфекции. У 31 (70,5%) пациента инфекция протекала с пневмонией, из них у 50% наблюдалось распространенное поражение по данным рентгенологических исследований. У 70,1% пациентов с ЛЭ и анамнезом COVID-19 была точно известна дата постановки диагноза, при исключении анамнеза вакцинации (табл. 1).
Таблица 1
Характеристика пациентов с ЛЭ и анамнезом COVID-19
Признак | Значение |
Известна точная дата COVID-19, n (%) | 31 (70,1) |
Период от начала заболевания COVID-19 до выявления ЛЭ, M±σ, дней | 42,3±22,6 |
Тяжесть по КТ 3-4, % | 24 (54,5) |
Выздоровление после COVID-19, n (%): — выписаны домой — переведены на долечивание — не госпитализировались | 16 (36) 15 (34) 13 (30) |
Применение антикоагулянтов до развития ЛЭ, n (%): — профилактические дозы — лечебные дозы — без антикоагулянтов — нет данных | 16 (36) 3 (7) 5 (12) 20 (45) |
Применение глюкокортикостероидов до развития ЛЭ, n (%): — всего — из них, в высоких дозах | 17 (54,8) 12 (70,6) |
Другие препараты упреждающей противовоспалительной терапии (Олокизумаб, Тоцилизумаб, Левилимаб, Анакинра), n (%) | 5 (16) |
Применение антибиотиков до развития ЛЭ, n (%): — применялись различные схемы антибиотикотерапии | 20 (64,5) |
Применение противовирусных препаратов, n (%) | 14 (45) |
Сокращения: ЛЭ — легочная эмболия, КТ — компьютерная томография, COVID-19 — новая коронавирусная инфекция 2019.
У пациентов с анамнезом COVID-19 по данным КТ преобладало немассивное поражение дистальных отделов легочной артерии, реже встречался проксимальный ТГВ. Выявлены особенности лабораторных и инструментальных показателей (табл. 2, 3).
Таблица 2
Сравнительная характеристика
пациентов с ЛЭ и наличием или отсутствием анамнеза COVID-19
Признак | ЛЭ и COVID-19, n=44 | ЛЭ без анамнеза COVID-19, n=69 | Значимость различий |
#Уровень тромбов по КТ, n (%): — сегментарные ветви — долевые — главные | 13 (33,3) 14 (35,9) 12 (30,8) | 9 (13,4) 16 (23,9) 42 (62,7) | 0,004 (χ²=10,89)* 0,029* 0,185 0,002* |
#Массивная ЛЭ, n (%) Немассивная ЛЭ, n (%) | 19 (43,2) 25 (56,8) | 46 (68,7) 21 (31,3) | 0,008 (χ²=7,1)* |
САД, мм рт.ст., M±σ | 113,4±27,3 | 117,5±31,4 | 0,472 |
ДАД, мм рт.ст., M±σ | 70,7±16,9 | 72,1±22,3 | 0,699 |
spO2, M±σ, % | 90±7 | 89,2±6,96 | 0,589 |
#Тромбоз вен: — без тромбоза/дистальный тромбоз, n (%) — проксимальный тромбоз, n (%) | 24 (60) 16 (40) | 24 (40) 36 (60) | 0,049 (χ²=3,85)* |
Д-димер, Ме (Q1; Q3), мкг/л | 3480 (1625; 7540) | 10560 (4018; 19655) | <0,001*** |
Тропонин T hs, Ме (Q1; Q3), нг/л | 29 (20; 56) | 32 (16; 75) | 0,709 |
ПВ, M±σ, сек | 16,3±9,4 | 16,2±6,0 | 0,977 |
МНО, M±σ | 1,4±0,8 | 1,4±0,5 | 0,9 |
С-реактивный протеин, Ме (Q1; Q3), мг/л | 42,9 (12,8; 82,3) | 32,9 (10,1; 78,9) | 0,955 |
Эритроциты, M±σ, 10¹²/л | 4,3±0,6 | 4,5±0,8 | 0,07 |
Гемоглобин, M±σ, г/л | 121,8±20,9 | 133,4±25,1 | 0,009 |
Анемия, n (%) | 20 (45,5) | 19 (27,5) | 0,05* |
Гематокрит <N, n (%) | 28 (63,6) | 28 (41,2) | 0,02* |
Лейкоциты, M±σ, 10⁹/л | 9,1±3,7 | 11,8±6,0 | 0,004 |
Нейтрофилы >N, n (%) | 12 (30,8) | 32 (53,3) | 0,038* |
Лимфоциты >N, n (%) | 0 (0) | 2 (3,3) | 0,519 |
Лимфоциты <N, n (%) | 8 (20,5) | 11 (18) | 0,758 |
Тромбоциты, M±σ, 10⁹/л | 208,8±141,8 | 222±106,8 | 0,599 |
Тромбоцитопения, n (%) | 12 (27,3) | 9 (13) | 0,058* |
СКФ (EPI), M±σ, мл/мин | 72,5±22,6 | 64,2±22,9 | 0,06 |
Протеинурия, n (%) | 24 (58,5) | 38 (58) | 0,993 |
Общий билирубин, M±σ, мкмоль/л | 15±7,6 | 16,4±9 | 0,367 |
АСТ, M±σ, ЕД/л | 39,9±9,5 | 40,3±42,6 | 0,957 |
АЛТ, M±σ, ЕД/л | 44,3±46,7 | 42,2±46,4 | 0,819 |
Глюкоза, M±σ, ммоль/л | 6±2,6 | 5,5±2,6 | 0,322 |
ЛНП, M±σ, ммоль/л | 2,9±0,9 | 2,7±1,1 | 0,439 |
Калий, M±σ, ммоль/л | 4,2±0,8 | 4,2±0,8 | 0,807 |
Натрий, M±σ, ммоль/л | 140,3±3,4 | 139,5±3,8 | 0,311 |
Хлор, M±σ, ммоль/л | 104±3,2 | 101,5±5 | 0,024 |
Примечание: # — у части пациентов были доступы только заключения исследований, анализ локализации тромботического процесса был затруднен, * — χ², ** — точный критерий Фишера; *** — критерий Манна-Уитни.
Сокращения: АД — артериальное давление, АЛТ — аланинаминотрансфераза, АСТ — аспартатаминотрансфераза, ДАД — диастолическое артериальное давление, КТ — компьютерная томография, ЛЭ — легочная эмболия, ЛНП — липопротеины низкой плотности, МНО — международное нормализованное отношение, ПВ — протромбиновое время, САД — систолическое артериальное давление, СКФ — скорость клубочковой фильтрации, COVID-19 — новая коронавирусная инфекция 2019.
Таблица 3
Сравнительная характеристика показателей ЭКГ и ЭхоКГ
у пациентов с ЛЭ и наличием или отсутствием анамнеза COVID-19
Признак | ЛЭ и COVID-19, n=44 | ЛЭ без анамнеза COVID-19, n=69 | Значимость различий |
ЭКГ, ЧСС, M±σ, уд./мин | 91,4±23,5 | 95,9±23,1 | 0,346 |
Синусная тахикардия, n (%) | 24 (54,5) | 32 (46,4) | 0,513 |
ЭКГ, QIII SI TIII (симптом McGinn-White), n (%) | 8 (18,2) | 16 (23,2) | 0,526 |
ЭКГ, (-) Т в грудных отведениях (симптом Kosuge), n (%) | 11 (25) | 33 (47,8) | 0,015 (χ²=5,89)* |
ЭКГ, БПНПГ, n (%) | 1 (2,2) | 5 (7,4) | 0,4 |
ЭхоКГ, ПЖ >N, n (%) | 21 (51) | 37 (57) | 0,7 |
ЭхоКГ, ПЖ(4к), M±σ, мм | 41,5±8,9 | 42,8±6,3 | 0,418 |
ЭхоКГ, ПП, M±σ, мм | 43,2±8,1 | 44,2±7 | 0,513 |
ЭхоКГ, ИПП, M±σ, мм/м² | 22,8±3,8 | 23,4±4,5 | 0,473 |
ЭхоКГ, ППП, M±σ, мм | 19,1±5,6 | 21,4±5,6 | 0,037 |
ЭхоКГ, ЛП, M±σ, мм | 37,5±5,6 | 36,4±6,3 | 0,332 |
ЭхоКГ, ИЛП, M±σ | 19,8±3,1 | 19,2±3,3 | 0,393 |
ЭхоКГ, ОЛП, M±σ, мм | 60,4±27,2 | 71,5±34,9 | 0,07 |
ЭхоКГ, ИОЛП, M±σ, мм | 29,6±14 | 37,2±16,9 | 0,017 |
ЭхоКГ, КДРЛЖ, M±σ, мм | 42,6±5,5 | 44,6±7 | 0,109 |
ЭхоКГ, ММЛЖ, M±σ, г | 166,5±55,8 | 178,5±67,3 | 0,325 |
ЭхоКГ, ИММЛЖ, M±σ | 85,6±25,9 | 93,9±31,7 | 0,162 |
ЭхоКГ, ФВ, M±σ, % | 62,6±9,1 | 56,5±12,8 | 0,002 |
ЭхоКГ, СДЛА, M±σ, мм рт.ст. | 48,8±15,6 | 44,7±13,2 | 0,163 |
Регургитация МК 2-4, n (%) | 9 (22,5) | 36 (56) | <0,001* |
Регургитация ТК 3-4, n (%) | 5 (12) | 28 (43) | 0,002* |
Примечание: * — χ², ** — точный критерий Фишера, *** — критерий Манна-Уитни.
Сокращения: БПНПГ — блокада правой ножки пучка Гиса, ИПП — индекс правого предсердия, ИЛП — индекс левого предсердия, ИММЛЖ — индекс массы миокарда левого желудочка, ИОЛП — индекс объема левого предсердия, КДРЛЖ — конечно-диастолический размер левого желудочка, ЛП — левое предсердие, ЛЭ — легочная эмболия, МК — митральный клапан, ММЛЖ — масса миокарда левого желудочка, ОЛП — объем левого предсердия, ППП — площадь правого предсердия, ПП — правое предсердие, ПЖ — правый желудочек, СДЛА — систолическое давление легочной артерии, ТК — трикуспидальный клапан, ФВ — фракция выброса, ЧСС — частота сердечных сокращений, ЭКГ — электрокардиография, ЭхоКГ — эхокардиография, COVID-19 — новая коронавирусная инфекция 2019.
У пациентов обеих групп сопоставимая частота госпитализации в отделение интенсивной терапии, применения основных классов лекарственных препаратов, в т. ч. тромболитической терапии (ТЛТ). Наблюдаются различия в частоте использования варфарина и не витамин К зависимых пероральных антикоагулянтов. Длительность госпитализации у пациентов без анамнеза COVID-19 была больше (табл. 4).
Таблица 4
Терапия пациентов с ЛЭ и наличием или отсутствием анамнеза COVID-19
Признак | ЛЭ и COVID-19, n=44 | ЛЭ без анамнеза COVID-19, n=69 | Значимость различий |
Тромболитическая терапия, n (%) | 8 (18,1) | 13 (18,8) | 0,93 |
Отделение реанимации, n (%) | 34 (77,3) | 59 (85,5) | 0,263 |
ИВЛ, n (%) | 2 (4,5) | 0 (0) | 0,149 |
Оксигенотерапия, n | 27 (61,4) | 48 (69,6) | 0,368 |
#Антикоагулянты: — НФГ, n (%) — НМГ, n (%) — Варфарин, n (%) НОАК: — Дабигатран, n (%) — Ривароксабан, n (%) — Апиксабан, n (%) | 11 (25) 13 (29,5) 24 (54,5) 12 (27,3) 6 (13,6) 14 (31,8) | 12 (17,4) 19 (27,5) 56 (81,2) 12 (17,4) 10 (14,5) 2 (2,9) | 0,327 0,833 0,005* 0,309 0,899 <0,001** |
иАПФ, БРА, n (%) | 19 (43,2) | 31 (44,9) | 0,99 |
БКК, n (%) | 19 (43,2) | 26 (37,7) | 0,7 |
АСК, n (%) | 3 (6,8) | 0 (0) | 0,057 |
Клопидогрел, n (%) | 0 (0) | 3 (4,3) | 0,28 |
Статины, n (%) | 20 (45,5) | 44 (63,8) | 0,085 |
Бета-блокаторы, n (%) | 16 (36,4) | 11 (15,9) | 0,024 |
Амиодарон, n (%) | 2 (4,5) | 9 (13) | 0,197 |
Омепразол, n (%) | 41 (93,2) | 68 (98,6) | 0,325 |
Кровотечение/заместительная терапия, n (%) | 2 (4,5) | 4 (5,8) | 0,887 |
Препараты железа, n (%) | 12 (27,3) | 13 (18,8) | 0,412 |
Антибактериальная терапия, n (%) | 28 (63,6) | 44 (63,8) | 0,916 |
Глюкокортикостероиды, n (%) | 4 (9,1) | 1 (1,4) | 0,074 |
Длительность госпитализации, M±σ | 14±7,6 | 17,6±7,7 | 0,019 |
Примечание: # — часть пациентов получали несколько антикоагулянтов за время лечения, * — χ², ** — точный критерий Фишера, *** — критерий Манна-Уитни.
Сокращения: АСК — ацетилсалициловая кислота, БКК — блокатор кальциевых каналов, БРА — блокатор рецептора ангиотензина, ИВЛ — искусственная вентиляция легких, иАПФ — ингибитор ангиотензинпревращающего фермента, ЛЭ — легочная эмболия, НФГ — нефракционированный гепарин, НМГ — низкомолекулярные гепарины, НОАК — не витамин К зависимые пероральные антикоагулянты, COVID-19 — новая коронавирусная инфекция 2019.
Наблюдается тенденция к более высокой летальности у пациентов с анамнезом инфекции. В ранний период пандемии летальность значимо выше (табл. 5). Наблюдаются сопоставимые средние значения индексов PESI, sPESI, распределение пациентов по классам. Несмотря на это, наблюдается тенденция к более высокой летальности у пациентов с анамнезов COVID-19 при меньшем или сопоставимом с группой сравнения количестве баллов PESI, sPESI. При этом оба индекса позволяют выявлять пациентов с наиболее высоким риском летальности.
Таблица 5
Сравнительный анализ летальности
пациентов с ЛЭ и наличием или отсутствием анамнеза COVID-19
Признак | ЛЭ и COVID-19, n=44 | ЛЭ без анамнеза COVID-19, n=69 | Значимость различий |
Летальность 2020-2021гг, n (%) | 9 (20,5) | 6 (8,7) | 0,07 (χ²=3,22)* |
Летальность (в ранний период пандемии), n (%) | 8 (23,5) | 5 (7,5) | 0,023 (χ²=5,19)* |
Индекс PESI, M±σ | 98,1±29,6 | 97,7±27,4 | 0,937 |
PESI по классам: — 1, n (%) — 2, n (%) — 3, n (%) — 4, n (%) — 5, n (%) — 4-5, n (%) | 8 (18,2) 9 (20,5) 10 (22,7) 10 (22,7) 7 (15,9) 17 (38,6) | 7 (10,1) 18 (26,1) 13 (18,8) 17 (24,6) 12 (17,4) 29 (42) | 0,771 0,261 0,651 0,638 0,995 0,958 0,845 |
Летальность в расчетном классе PESI: — 1, n (%) — 2, n (%) — 3, n (%) — 4, n (%) — 5, n (%) — 4-5, n (%) | 0 (0) 1 (11,1) 1 (11,1) 4 (40) 3 (42,9) 7 (41,2) | 0 (0) 0 (0) 1 (7,1) 3 (17,6) 2 (16,7) 5 (17,2) | NS 0,333 0,802 0,364 0,305 0,07* |
sPESI M±σ | 1,5±0,98 | 1,8±1,1 | 0,176 |
sPESI по баллам: — 0, n (%) — 1, n (%) — 2, n (%) — 3, n (%) — 4, n (%) — ≥1, n (%) | 7 (15,9) 16 (36,3) 13 (29,5) 8 (18,2) 0 (0) 36 (82) | 8 (11,6) 22 (31,9) 21 (30,4) 14 (20,3) 4 (5,8) 61 (88) | 0,532 0,575 0,416 0,834 0,974 0,155 0,482 |
Летальность с учетом баллов sPESI: — 0, n (%) — 1, n (%) — 2, n (%) — 3, n (%) — 4, n (%) — ≥1, n (%) | 0 (0) 1 (6,3) 3 (23,1) 5 (62,5) 0 (0) 9 (24,3) | 0 (0) 0 (0) 2 (9,5) 3 (21,4) 1 (25) 6 (9,8) | NS 0,421 0,348 0,081 0,820 0,078** |
Риск ЛЭ: — низкий, n (%) — промежуточно-низкий, n (%) — промежуточно-высокий, n (%) — высокий, n (%) | 5 (62,5) 15 (34,1) 14 (31,8) 10 (22,7) | 6 (9,8) 23 (33,3) 22 (31,9) 18 (26,1) | 0,956 0,749 0,933 0,994 0,824 |
Летальность, группы риска на момент госпитализации: — низкий, n (%) — промежуточно-низкий, n (%) — промежуточно-высокий, n (%) — высокий, n (%) | 0 (0) 0 (0) 2 (22,2) 7 (77,8) | 0 (0) 0 (0) 4 (66,7) 2 (33,3) | NS 0,135 0,135 |
Нестабильная гемодинамика при поступлении, n (%) Среди умерших, n (%) | 10 (22,7) 7 (77,8) | 11 (15,9) 2 (33,3) | 0,458 0,085** |
Примечание: * — χ², ** — точный критерий Фишера, *** — критерий Манна-Уитни.
Сокращения: ЛЭ — легочная эмболия, COVID-19 — новая коронавирусная инфекция 2019, PESI — Pulmonary Embolism Severity Index, sPESI — Simplified PESI.
Среди умерших пациентов с анамнезом COVID-19 выделены факторы, которые встречались значимо чаще: СД 2 типа, хроническая болезнь почек (ХБП), старше возраст, снижение тромбоцитов, более высокие значения тропонина, нестабильность гемодинамики при поступлении в стационар, выше расчетные значения по шкалам PESI, sPESI. Среди умерших пациентов чаще проводилась искусственная вентиляция легких, ТЛТ (рис. 1). При этом традиционные признаки, определяющие тяжесть ЛЭ, такие как перегрузка правых отделов по электрокардиографии (ЭКГ), эхокардиографии (ЭхоКГ), встречались с одинаковой частотой. Массивная тромбоэмболия встречались не чаще в группе умерших и выживших пациентов, в 44,4% и в 42,9%, соответственно.
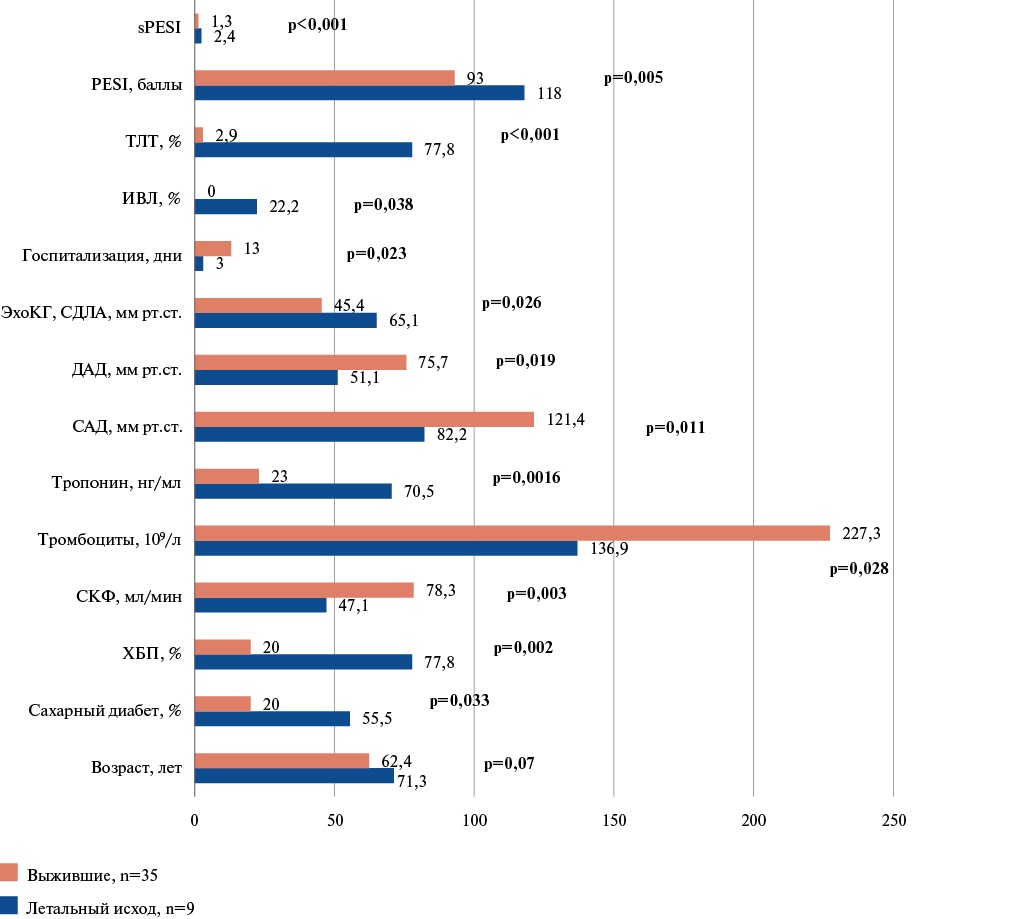
Рис. 1. Различия среди умерших и выживших в группе пациентов с ЛЭ и анамнезом COVID-19.
Сокращения: ДАД — диастолическое артериальное давление, ИВЛ — искусственная вентиляция легких, САД — систолическое артериальное давление, СДЛА — систолическое давление легочной артерии, СКФ — скорость клубочковой фильтрации, ТЛТ — тромболитическая терапия, ХБП — хроническая болезнь почек, ЭхоКГ — эхокардиография, PESI — Pulmonary Embolism Severity Index, sPESI — Simplified PESI.
При проведении корреляционного анализа были получены следующие данные: выявлены прямые умеренной силы взаимодействия между наличием неблагоприятного исхода и значением шкалы sPESI (r=0,496; p<0,001; 95% доверительный интервал (ДИ): 0,23-0,69), частотой применения искусственной вентиляции легких (r=0,43; p<0,004; 95% ДИ: 0,15-0,64), значением систолического давления легочной артерии (r=0,48; p<0,0015; 95% ДИ: 0,20-0,69), уровнем тропонина крови (r=0,5; p<0,001; 95% ДИ: 0,23-0,70), частотой наличия ХБП (r=0,58; p<0,0001; 95% ДИ: 0,34-0,74), сильная взаимосвязь с частотой применения ТЛТ (r=0,78; p<0,0001; 95% ДИ: 0,63-0,88), слабая взаимосвязь с значением шкалы PESI (r=0,34; p<0,02; 95% ДИ: 0,05-0,58), частотой наличия СД (r=0,32; p<0,03; 95% ДИ: 0,03-0,56). Также выявлена обратная умеренной силы взаимосвязь между неблагоприятным исходом и уровнями диастолического артериального давления (ДАД) (r=-0,59; p<0,0001; 95% ДИ: -0,76 — -0,36), систолического артериального давления (САД) (r=-0,59; p<0,0001; 95% ДИ: -0,75 — -0,35), уровнем скорости клубочковой фильтрации (СКФ) (r=-0,55; p<0,0002; 95% ДИ: -0,73 — -0,29), слабая взаимосвязь с длительностью госпитализации (r=-0,36; p<0,02; 95% ДИ: -0,59 — -0,07). Статистически значимых корреляционных взаимосвязей между летальным исходом и уровнем тромбоцитов крови, а также возрастом не выявлено.
При сравнительном анализе пациентов в группах в зависимости от прогноза 8 количественных показателей имели статистически значимые различия. При проведении логистического регрессионного анализа наибольшую прогностическую значимость показали 4 показателя: снижение значений САД и ДАД, снижение уровня СКФ и высокие значения sPESI. AUC составила 0,975 (p<0,05), данная модель обладает диагностической точностью 90,7%.
При построении ROC-кривой для САД была получена точка отсечения ≤100 мм рт.ст. (AUC=0,876, p<0,001), ДАД ≤60 мм рт.ст. (AUC=0,832, p=0,001), СКФ ≤58 мл/мин (AUC=0,868, p<0,001), sPESI >1 (AUC=0,835, p<0,001) (рис. 2).
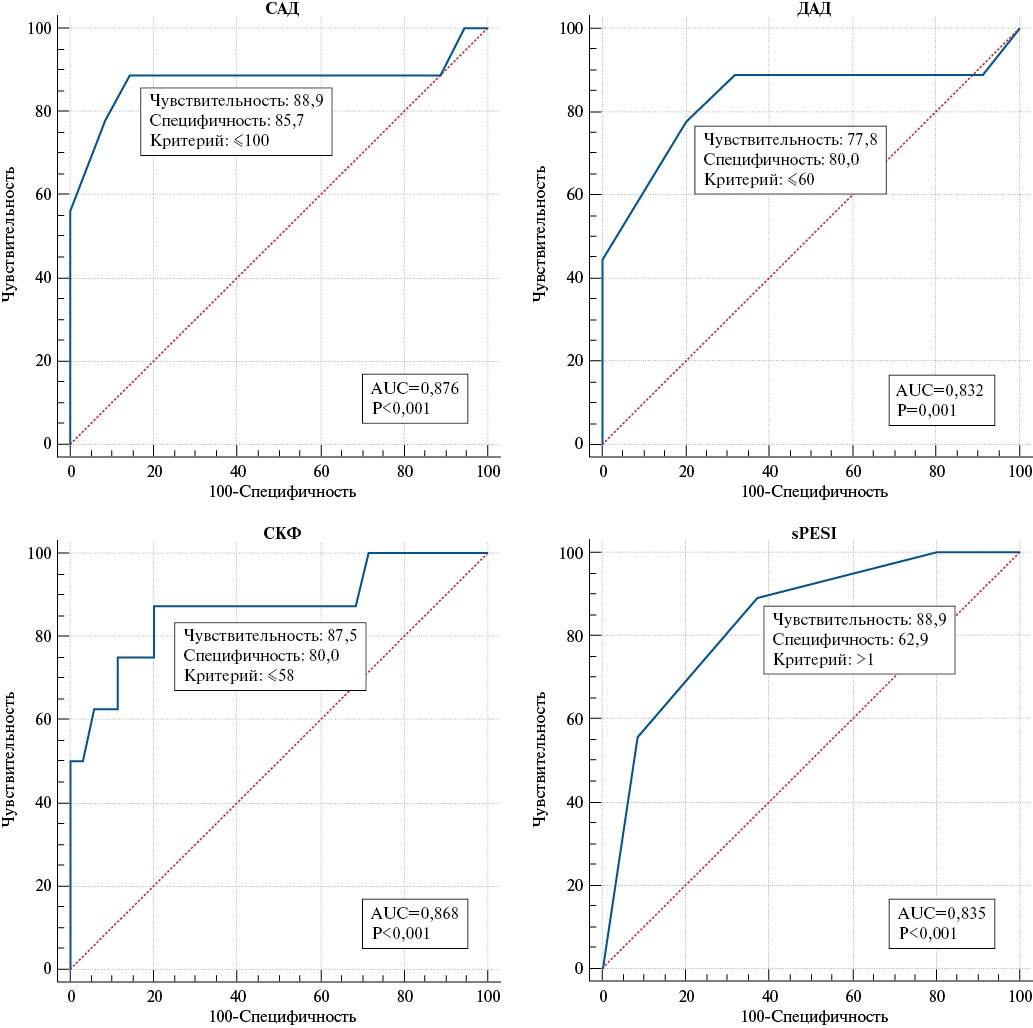
Рис. 2. ROC-кривые для САД, ДАД, СКФ и шкалы sPESI.
Сокращения: ДАД — диастолическое артериальное давление, САД — систолическое артериальное давление, СКФ — скорость клубочковой фильтрации, sPESI — Simplified PESI, AUC — Area Under Curve.
При анализе качественных показателей прогностическую значимость показали 2 показателя: ХБП (ОШ 5,44, 95% ДИ: 1,39-21,24) и необходимость проведения ТЛТ (ОШ 27,22, 95% ДИ: 2,96-250,57). Показатели характеризуют тяжесть состояния пациентов.
Обсуждение
В исследовании нами изучались пациенты с ЛЭ вне острого периода COVID-19, со средним периодом от момента диагностики инфекции до выявления ЛЭ >40 дней в различных периодах пандемии. Большинство опубликованных клинических исследований рассматривают острый период COVID-19 и преимущественно начальный период пандемии. В поздние периоды пандемии сложнее оценить анамнез перенесенной инфекции [14].
В нашем исследовании в группе с анамнезом COVID-19 выявлена тенденция к более частому наличию СД, тяжелой ХБП. С этим может быть ассоциировано тяжелое течение COVID-19, в т. ч. за счет повышения риска развития тромбоэмболий. Большинство пациентов имели тяжелые проявления предшествующей инфекции, в 51,9% выявлялось распространенное поражение легких, 54,5% пациентов получали терапию глюкокортикостероидами, в т. ч. в высоких дозах, что отражает реальную клиническую практику стационаров в изучаемый период (табл. 1).
Тромбоэмболии развивались у пациентов несмотря на применение антикоагулянтов в 61,3% случаев. Препараты назначались преимущественно в профилактических дозах. Наблюдалась тенденция к более частому назначению не-витамин-К-зависимых антикоагулянтов в случае анамнеза COVID-19 и варфарина в группе без анамнеза инфекции. Это отражает реальную клиническую практику в период пандемии. Более частым назначением варфарина, вероятно, обусловлена большая длительность госпитализации в группе пациентов без COVID-19. Вопрос эффективности тромбопрофилактики остается сложным с момента начала пандемии. На практике, вопрос тромбопрофилактики решался с учетом актуальных методических рекомендаций1. Наши результаты можно соотнести с результатами других исследований [23]. В метаанализе 28 исследований с участием 2928 пациентов в отделениях интенсивной терапии было показано, что подходы к тромбопрофилактике значительно различаются. Несмотря на тромбопрофилактику, тромботические осложнения выявлены у 34% (16,1% ТГВ, 12,6% ЛЭ, 12% артериальные тромбозы) [24]. Решение об инициации тромбопрофилактики до пандемии могло быть основано на расчетных шкалах, таких как IMPROVE. Недостаточно ясно, насколько валидирована эта шкала в случае COVID-19 [25]. В нашем исследовании пациенты с COVID-19 имели более высокий риск по шкале IMPROVE-DD. Это обусловлено наличием предшествующей госпитализации/иммобилизации у большинства пациентов с COVID-19. Возможно, данным пациентам должны чаще назначаться лечебные дозы антикоагулянтов. Продолжительность антикоагулянтной терапии после выписки из стационара также является сложным, недостаточно изученным вопросом.
Особенности клинической картины в нашем исследовании согласуются с результатами исследований острой фазы инфекции. В серии публикаций Испанского проекта UMC-19 (Unusual Manifestations of COVID-19) в части группы исследователей Spanish Investigators in Emergency Situations TeAm (SIESTA) также проанализированы особенности ЛЭ у пациентов c COVID-19 [15][26]. В SIESTA пациенты без COVID-19 и исследуемая группа отличались в 35 из 48 характеристик. Характерно поражение дистальных отделов легочной артерии. Реже поражение правых отделов и подтвержденный глубокий венозный тромбоз. Пациенты после госпитализации в равной степени лечились низкомолекулярными гепаринами, в 89% случаев в высоких дозах. Пациенты исследуемой группы чаще требовали перевода в отделение интенсивной терапии (18% vs 6,5% в группе COVID-19 без ЛЭ). В нашем исследовании в равной степени встречалось поражение сегментарных, долевых или главных ветвей легочной артерии. Поражение главных ветвей встречалось в 30,8% vs 62,7% пациентов без COVID-19. В 60% случаев отсутствовал ТГВ конечностей, либо тромбы располагались дистально. Пациенты с анамнезом инфекции характеризовались относительно более низкими значениями Д-димера в сочетании с более частой анемией со значительным снижением гематокрита, низкими значениями лейкоцитов и склонностью к тромбоцитопении. Все это может быть объяснено как тяжестью инфекции, так и влиянием терапии, в т. ч. применением упреждающей противовоспалительной терапии, глюкокортикостероидами. По результатам анализа у пациентов c анамнезом COVID-19 реже встречались признаки перегрузки правого желудочка по ЭКГ и ЭхоКГ. Самый частый признак на ЭКГ — это синусовая тахикардия, которая наблюдалась в 54,5% случаев. При анализе параметров ЭхоКГ реже выявлялись признаки поражения как правых отделов, так и дисфункция левого желудочка. Отсутствие дисфункции правого желудочка объясняется менее массивным тромботическим поражением легочной артерии. Для объяснения причин наличия менее выраженных изменений левых отделов сердца требуется дополнительный анализ, в т. ч. оценка влияния сопутствующей патологии.
Почему пациенты с дистальным поражением, меньшими размерами правого желудочка чаще выявляются при COVID-19? При COVID-19 осложнения могут быть проявлениями иммунотромбоза, первичного тромботического процесса in situ на уровне мелких сосудов легких, не ассоциированным с глубоким венозным тромбозом [12][27-29]. Возможно, симптомы инфекции в большей степени заставляют больных обращаться за медицинской помощью. У пациентов без инфекции поражение мелких ветвей проходит малосимптомно, и они реже обращаются за помощью [30].
Нами выявлена тенденция к более высокой летальности у пациентов с COVID-19, а в группе с перенесенной COVID-19 в 2020г и 2021г в периоде до начала масштабной вакцинации в регионе: 23,5% vs 7,5%. В объединенном анализе исследований PEPCOV и SIESTA летальность также была выше у COVID-19 пациентов: 12,8% vs 5,3% (p<0,001). Летальность была выше вне зависимости от размера ЛЭ, поражения правых отделов и индекса sPESI [13].
При оценке риска смерти с помощью индекса PESI мы выявили недооценку риска у пациентов с COVID-19. Среди пациентов с низким и умеренным риском по PESI умерли 2 человека в группе с анамнезом COVID-19 и 1 в группе без анамнеза инфекции. У пациентов с высоким и очень высоким риском летальность составила 41,2% и 17,2% в группах с анамнезом инфекции и без инфекции, соответственно (табл. 5). При этом расчетная величина 30-дневной смертности при таком риске не должна превышать 24%. В случае индекса sPESI при высоком расчетном риске наблюдаемая летальность 24,3% в исследуемой группе и 9,8% в группе без анамнеза инфекции. Расчетная прогнозируемая величина должна составлять только 9%. Таким образом, sPESI также недостаточно точно прогнозирует риск смерти в группе с анамнезом недавно перенесенной COVID-19. Результаты частично согласуются с результатами исследований при острой форме COVID-19. При попытке валидации шкалы PESI в одном из ретроспективных исследований демонстрируется недооценка с помощью шкалы риска смерти [31]. Шкала призвана выявлять пациентов низкого риска, позволяя рассматривать их для амбулаторного лечения. На практике, эти пациенты имеют высокий риск смерти и не должны лечиться амбулаторно. Более того, пациенты с 3-5 классом имеют смертность >15% и должны рассматриваться для лечения в условиях отделения интенсивной терапии, соотношение 3:1 между наблюдаемым и расчетным риском в наиболее высоких классах значительно дискредитирует шкалу у пациентов с COVID-19 [31].
При анализе нами выявлено несколько связанных со смертельным исходом параметров (рис. 2). Риск смерти при ЛЭ с недавним анамнезом COVID-19 в нашем исследовании был ассоциирован с наличием более высоких средних значений индекса PESI, sPESI, уровня тропонина крови, снижением средних значений тромбоцитов, СКФ, более высоким давлением в легочной артерии, наличием СД. Эти признаки могут иметь большее отношение к течению инфекции COVID-19. Среди умерших и выживших пациентов не было различий в классических признаках, определяющих прогноз: массивность тромбоэмболического процесса, наличие перегрузки правых отделов. При этом 77,8% умерших пациентов с анамнезом COVID-19 имели нестабильность гемодинамики на момент госпитализации в кардиологический стационар. Именно снижение артериального давления, наряду со снижением функции почек и высокие значения по шкале sPESI обладают наибольшим прогностическим влиянием на исход ЛЭ.
Риск тромбоэмболических осложнений может сохраняться длительный период. Неясно, связано ли это с персистенцией вируса и невозможностью его выявления доступными тестами. Особенности клинической картины ЛЭ, выявленной в отсроченном периоде, совпадают с описанными в литературе особенностями в остром периоде, что, возможно, указывает на их специфический для инфекции характер.
Ограничения исследования: на результаты исследования влияло несколько факторов. Во-первых, исследование носило ретроспективный характер. Во-вторых, среди пациентов с COVID-19 не проводился активный скрининг на выявление ЛЭ при начальной диагностике инфекции. В данном случае нельзя исключить развитие ЛЭ в более ранний период, чем это выявлено на практике. В-третьих, большинство пациентов имели анамнез госпитализации, что также может влиять на риск развития тромбоэмболических осложнений. С другой стороны, отсутствие активного скрининга отражает реальную клиническую практику и результаты исследования могут иметь большее практическое значение.
Заключение
По данным нашего исследования госпитальная летальность выше у пациентов с недавней COVID-19. У пациентов с летальным исходом выше уровень тропонина крови, чаще тромбоцитопения, СД 2 типа, нестабильность гемодинамики исходно, ниже СКФ. Высокие значения индексов PESI и sPESI также были ассоциированы с высокой летальностью, но наблюдается недооценка риска смерти с помощью данных шкал. Среди всех факторов наибольшим неблагоприятным влиянием обладали: низкие значения САД и ДАД на момент госпитализации, снижение СКФ, высокий риск по шкале sPESI. Требуют дальнейшего изучения особенности ЛЭ и исходы в различные периоды пандемии с учетом мутации вируса, изменения популяции. Необходим анализ отдаленных исходов и риск повторных событий. Это может быть ключевым при определении длительности антикоагулянтной терапии.
Отношения и деятельность: все авторы заявляют об отсутствии потенциального конфликта интересов, требующего раскрытия в данной статье.
1. Временные методические рекомендации "Профилактика, диагностика и лечение новой коронавирусной инфекции (COVID-19)" Версия 10 (08.02.2021). Утверждены Минздравом России.
Список литературы
1. Helms J, Tacquard C, Severac F, et al. High risk of thrombosis in patients with severe SARS-CoV-2 infection: a multicenter prospective cohort study. Intensive Care Med. 2020;46(6):1089-98. doi:10.1007/s00134-020-06062-x.
2. Suh YJ, Hong H, Ohana M, et al. Pulmonary Embolism and Deep Vein Thrombosis in COVID-19: A Systematic Review and Meta-Analysis. Radiology. 2021;298(2):E70-E80. doi:10.1148/radiol.2020203557.
3. Розыходжаева Г.А., Жураев З.А. Сравнительный ретроспективный анализ частоты тромбоза глубоких вен, выявленного методом дуплексного сканирования в учреждениях первичного звена здравоохранения. Кардиоваскулярная терапия и профилактика. 2022;21(7):3184. doi:10.15829/1728-8800-2022-3184.
4. Арутюнов Г.П., Тарловская Е.И., Арутюнов А.Г. и др. Анализ влияния коморбидной сердечно-сосудистой патологии на течение и исходы COVID-19 у госпитализированных пациентов в первую и вторую волну пандемии в Евразийском регионе. Кардиология. 2022;62(12):38-49. doi:10.18087/cardio.2022.12.n2125.
5. Порембская О.Я., Кравчук В.Н., Гальченко М.И. и др. Тромбоз сосудистого русла легких при COVID-19: клинико-морфологические параллели. Рациональная Фармакотерапия в Кардиологии 2022;18(4):376-84. doi:10.20996/1819-6446-2022-08-01.
6. Бойцов С.А., Погосова Н.В., Палеев Ф.Н. и др. Клиническая картина и факторы, ассоциированные с неблагоприятными исходами у госпитализированных пациентов с новой коронавирусной инфекцией COVID-19. Кардиология. 2021;61(2):4-14. doi:10.18087/cardio.2021.2.n1532.
7. Malas MB, Naazie IN, Elsayed N, et al. Thromboembolism risk of COVID-19 is high and associated with a higher risk of mortality: A systematic review and meta-analysis. EClinicalMedicine. 2020;29:100639. doi:10.1016/j.eclinm.2020.100639.
8. Эрлих А.Д., Атаканова А.Н., Неешпапа А.Г. и др. Российский регистр острой тромбоэмболии лёгочной артерии СИРЕНА: характеристика пациентов и лечение в стационаре. Российский кардиологический журнал. 2020;25(10):3849. doi:10.15829/1560-4071-2020-3849.
9. Fauvel C, Weizman O, Trimaille A, et al. Critical Covid-19 France Investigators. Pulmonary embolism in COVID-19 patients: a French multicentre cohort study. Eur Heart J. 2020; 41(32):3058-68. doi:10.1093/eurheartj/ehaa500.
10. Wells PS, Anderson DR, Rodger M, et al. Excluding pulmonary embolism at the bedside without diagnostic imaging: management of patients with suspected pulmonary embolism presenting to the emergency department by using a simple clinical model and d-dimer. Ann Intern Med. 2001;135(2):98-107. doi:10.7326/0003-4819-135-2-200107170-00010.
11. Kalaycı S, Köksal BG, Horuz E, et al. Pulmonary Embolism Severity Index Predicts Adverse Events in Hospitalized COVID-19 Patients: A Retrospective Observational Study. J Cardiothorac Vasc Anesth. 2022;36(12):4403-9. doi:10.1053/j.jvca.2022.08.009.
12. Kho J, Ioannou A, Van den Abbeele K, et al. Pulmonary embolism in COVID-19: Clinical characteristics and cardiac implications. Am J Emerg Med. 2020;38(10):2142-6. doi:10.1016/j.ajem.2020.07.054.
13. Miró Ò, Jiménez S, Llorens P, et al. SIESTA and PEPCOV research teams. Pulmonary embolism severity and in-hospital mortality: An international comparative study between COVID-19 and non-COVID patients. Eur J Intern Med. 2022;98:69-76. doi:10.1016/j.ejim.2022.01.035.
14. Freund Y, Drogrey M, Miró Ò, et al. Improving emergency care FHU Collaborators. Association Between Pulmonary Embolism and COVID-19 in Emergency Department Patients Undergoing Computed Tomography Pulmonary Angiogram: The PEPCOV International Retrospective Study. Acad Emerg Med. 2020;27(9):811-20. doi:10.1111/acem.14096.
15. Miró Ò, Jiménez S, Mebazaa A, et al. Spanish Investigators on Emergency Situations TeAm (SIESTA) network. Pulmonary embolism in patients with COVID-19: incidence, risk factors, clinical characteristics, and outcome. Eur Heart J. 2021;42(33):3127-42. doi:10.1093/eurheartj/ehab314.
16. Tan BK, Mainbourg S, Friggeri A, et al. Arterial and venous thromboembolism in COVID-19: a study-level meta-analysisThorax. 2021;76:970-9. doi:10.1136/thoraxjnl-2020-215383.
17. Wiener RS, Schwartz LM, Woloshin S.When a test is too good: how CT pulmonary angiograms find pulmonary emboli that do not need to be found. BMJ. 2013;347:f3368. doi:10.1136/bmj.f3368.
18. Mouzarou A, Ioannou M, Leonidou E, Chaziri I.Pulmonary Embolism in Post-CoviD-19 Patients, a Literature Review: Red Flag for Increased Awareness? SN Compr Clin Med. 2022;4(1):190. doi:10.1007/s42399-022-01273-3.
19. Краев А.Р., Соловьев О.В., Кононов С.К., Ральникова У.А. Тромботические осложнения у пациентов с перенесенной новой коронавирусной инфекцией. Вятский медицинский вестник. 2023;(2):36-31. doi:10.24412/2220-7880-2023-2-26-31.
20. Petramala L, Sarlo F, Servello A, et al. Pulmonary embolism post-Covid-19 infection: physiopathological mechanisms and vascular damage biomarkers. Clin Exp Med. 2023;23(8):4871-80. doi:10.1007/s10238-023-01150-w.
21. Шпилянский Э.М., Ройтман Е.В., Морозов К.М., Сухарева Т.В. Опыт лечения пациентов с артериальными и венозными тромбозами при COVID-19: клинические наблюдения. Комплексные проблемы сердечно-сосудистых заболеваний. 2021;10(4):131-41. doi:10.17802/2306-1278-2021-10-4-131-141.
22. Siddiqi HK, Mehra MR. COVID-19 illness in native and immunosuppressed states: a clinical-therapeutic staging proposal. J Heart Lung Transplant. 2020;39(5):405-7. doi:10.1016/j.healun.2020.03.012.
23. Miesbach W, Makris M. COVID-19: Coagulopathy, Risk of Thrombosis, and the Rationale for Anticoagulation. Clin Appl Thromb Hemost. 2020;26:1076029620938149. doi:10.1177/1076029620938149.
24. Jenner WJ, Kanji R, Mirsadraee S, et al. Thrombotic complications in 2928 patients with COVID-19 treated in intensive care: a systematic review. J Thromb Thrombolysis. 2021;51(3):595-607. doi:10.1007/s11239-021-02394-7.
25. Goldin M, Lin SK, Kohn N, et al. External validation of the IMPROVE-DD risk assessment model for venous thromboembolism among inpatients with COVID-19. J Thromb Thrombolysis. 2021;52:1032-5. doi:10.1007/s11239-021-02504-5.
26. Miró Ò, González Del Castillo J.Collaboration among Spanish emergency departments to promote research: on the creation of the SIESTA (Spanish Investigators in Emergency Situations TeAm) network and the coordination of the UMC-19 (Unusual Manifestations of COVID-19) macroproject. Emergencias. 2020; 32(4):269-77. English, Spanish.
27. Wichmann D, Sperhake JP, Lutgehetmann M, et al. Autopsy findings and venous thromboembolism in patients with COVID-19. Ann Intern Med. 2020;173(4). doi:10.7326/M20-2003.
28. Loo J, Spittle DA, Newnham M. COVID-19, immunothrombosis and venous thromboembolism: biological mechanisms. Thorax. 2021;76:412-20. doi:10.1136/thoraxjnl2020-216243.
29. Manolis AS, Manolis TA, Manolis AA, et al. COVID-19 Infection: Viral Macro- and MicroVascular Coagulopathy and Thromboembolism/Prophylactic and Therapeutic Management. J Cardiovasc Pharmacol Ther. 2021;26(1):12-24. doi:10.1177/1074248420958973.
30. Mumoli N, Conte G, Cei M, et al. In-hospital fatality and venous thromboembolism during the first and second COVID-19 waves at a center opting for standard-dose thromboprophylaxis. Thromb Res. 2021;203:82-4. doi:10.1016/j.thromres.2021.04.026.
31. Muñoz OM, Ruiz-Talero P, Hernández-Florez C, et al. Validation of the PESI Scale to Predict in-Hospital Mortality in Patients with Pulmonary Thromboembolism Secondary to SARS CoV-2 Infection. Clin Appl Thromb Hemost. 2022;28:10760296221102940. doi:10.1177/10760296221102940.
Об авторах
С. К. КононовРоссия
К.м.н., зав. отделением неотложной кардиологии, доцент кафедры факультетской терапии
Киров
О. В. Соловьёв
Россия
Д.м.н., профессор, заместитель главного врача, заведующий кафедрой факультетской терапии
Киров
А. Р. Краев
Россия
Врач кардиолог отделения неотложной кардиологии, аспирант кафедры факультетской терапии
Киров
У. А. Ральникова
Россия
Ассистент кафедры факультетской терапии
Киров
Е. В. Гребенева
Россия
Врач кардиолог
Киров
- Изучение особенностей тромбоэмболии легочной артерии (ТЭЛА), ассоциированной с новой коронавирусной инфекцией (COVID-19), является актуальным и после окончания пандемии инфекции.
- Определение факторов, влияющих на течение заболевания и прогноз при легочной эмболии, может помочь в анализе отсроченных последствий данных заболеваний.
- Летальные исходы развиваются при наличии как классических факторов риска неблагоприятного исхода ТЭЛА, так и факторов, связанных с тяжелым течением предшествующей COVID-19.
- Результаты работы подтверждают существующие рекомендации о необходимости продленной антикоагулянтной терапии у пациентов со среднетяжелым течением COVID-19.
Рецензия
Для цитирования:
Кононов С.К., Соловьёв О.В., Краев А.Р., Ральникова У.А., Гребенева Е.В. Факторы, определяющие исходы у пациентов с тромбоэмболией легочной артерии и недавней перенесенной инфекцией COVID-19. Российский кардиологический журнал. 2024;29(9):5633. https://doi.org/10.15829/1560-4071-2024-5633. EDN: UIDPDN
For citation:
Kononov S.K., Solovev O.V., Kraev A.R., Ralnikova U.A., Grebeneva E.V. Determinants of outcomes in patients with pulmonary embolism and recent COVID-19 infection. Russian Journal of Cardiology. 2024;29(9):5633. (In Russ.) https://doi.org/10.15829/1560-4071-2024-5633. EDN: UIDPDN
JATS XML


















































