Перейти к:
Тяжелое течение AL-амилоидоза сердца у пациентки пожилого возраста с многократной реинфекцией SARS-CoV-2. Клинический случай
https://doi.org/10.15829/1560-4071-2023-5443
EDN: JMSMHZ
Аннотация
Введение. Взаимосвязь системного амилоидоза и новой коронавирусной инфекции (COVID-19) к настоящему времени изучена недостаточно. В данной работе представлено клиническое наблюдение персистенции маркеров COVID-19 у пациентки пожилого возраста с системным амилоидозом.
Краткое описание. Пациентка 74 лет с сердечной недостаточностью с сохраненной фракцией выброса и сахарным диабетом 2 типа неоднократно была госпитализирована в связи с декомпенсацией сердечной недостаточности. На основании данных электрофоретического исследования белков сыворотки крови с иммунотипированием, биопсии подкожно-жировой клетчатки и костного мозга, эхокардиографических данных у пациентки был диагностирован системный AL-амилоидоз с поражением сердца. Во время госпитализаций в апреле, августе и декабре 2020г были получены положительные результаты полимеразной цепной реакции на SARS-CoV-2, при этом длительно отсутствовали клинические проявления инфекции и адекватная выработка антител.
Заключение. Клиническое наблюдение демонстрирует многократную реинфекцию SARS-CoV-2 у тяжелой коморбидной пациентки пожилого возраста, оказавшую негативное влияние на прогноз.
Ключевые слова
Для цитирования:
Резник Е.В., Нгуен Т., Эттингер О.А., Лазарев В.А., Борисовская С.В., Гусева А.И., Саликов А.В., Голухов Г.Н. Тяжелое течение AL-амилоидоза сердца у пациентки пожилого возраста с многократной реинфекцией SARS-CoV-2. Клинический случай. Российский кардиологический журнал. 2023;28(8):5443. https://doi.org/10.15829/1560-4071-2023-5443. EDN: JMSMHZ
For citation:
Reznik E.V., Nguyen T., Ettinger O.A., Lazarev V.A., Borisovskaya S.V., Guseva A.I., Salikov A.V., Golukhov G.N. Severe cardiac AL amyloidosis in an elderly patient with multiple SARS-CoV-2 reinfection: a case report. Russian Journal of Cardiology. 2023;28(8):5443. (In Russ.) https://doi.org/10.15829/1560-4071-2023-5443. EDN: JMSMHZ
Новая коронавирусная инфекция (COVID-19) охватила все континенты и привела к увеличению смертности во всем мире. Более 20% пациентов с COVID-19 имеют сопутствующие сердечно-сосудистые заболевания (ССЗ) [1]. Ведение и лечение пациентов с COVID-19 и ССЗ, в т.ч. сердечной недостаточностью (СН), представляет собой огромную клиническую проблему [1].
Одной из редко диагностируемых причин развития хронической СН (ХСН) является системный амилоидоз с поражением сердца. АL-амилоидоз — мультисистемное заболевание, при котором в различных органах и тканях откладывается гликопротеид амилоид, белком-предшественником которого являются легкие цепи иммуноглобулинов лямбда или каппа [2][3]. Заболевание развивается, главным образом, после 70 лет. Это самая частая форма системного амилоидоза. Сердце поражается при AL-амилоидозе у 60-90% пациентов [2][4]. С одной стороны, часто, особенно в условиях пандемии COVID-19, AL-амилоидоз при жизни может остаться недиагностированным [5]. С другой стороны, у пациентов с доказанным AL-амилоидозом инфицирование вирусом SARS-CoV-2 может приводить к тяжелым формам COVID-19 и серьезным последствиям.
В работе описана многократная реинфекция SARS-CoV-2 и тяжелое течение COVID-19 у пациентки с AL-амилоидозом сердца.
Цель статьи — привлечение внимания врачей на особенности течения и диагностики амилоидоза в условиях пандемии COVID-19.
Описание клинического случая
Информация о пациенте. Пациентка 74 лет была госпитализирована в стационар с жалобами на слабость, одышку при незначительной физической нагрузке и в положении лежа, боли в грудной клетке без четкой связи с физической нагрузкой.
Анамнез. Страдает в течение 4 лет сахарным диабетом (СД) 2 типа на фоне ожирения 2 степени. Впервые была госпитализирована в стационар в январе 2020г с вышеуказанными жалобами. По данным рентгенографии органов грудной клетки (ОГК), выявлено расширение границ сердца влево, двусторонний гидроторакс, по данным эхокардиографии (ЭхоКГ) — асимметричное утолщение стенки левого желудочка (ЛЖ) (индекс массы миокарда ЛЖ — 131 г/м2, относительная толщина стенки <0,45) с обструкцией выносящего тракта ЛЖ в покое (максимальный градиент давления — 188 мм рт.ст., средний — 69 мм рт.ст.), дилатацией левого предсердия до 41*54 мм, диастолической дисфункцией ЛЖ 1 типа (нарушением релаксации ЛЖ), значением фракции выброса (ФВ) 52%, повышением систолического давления в легочной артерии до 37 мм рт.ст. Кроме того, было выявлено уплотнение створок аортального и митрального клапанов, кальцинат в основании задней створки митрального клапана, градиент давления митрального клапана — 17/7,5 мм рт.ст., митральная, трикуспидальная и аортальная регургитации II степени. Острую ревматическую лихорадку в анамнезе пациентка отрицала. Максимальный уровень артериального давления в анамнезе составлял 150 и 90 мм рт.ст., что не соответствовало степени выраженности утолщения стенки ЛЖ и с малой вероятностью могло привести к развитию обструкции выходного отдела ЛЖ. Пациентке был установлен диагноз "Обструктивная гипертрофическая кардиомиопатия, ХСН с сохраненной ФВ ЛЖ", назначена терапия бисопрололом, эналаприлом, фуросемидом, спиронолактоном, гидрохлортиазидом с титрацией доз со стартовых до терапевтических под контролем показателей в соответствии с актуальными клиническими рекомендациями [6].
В начале марта 2020г у пациентки развился приступ интенсивных болей за грудиной, после которого стала отмечать прогрессирование одышки, несмотря на соблюдение врачебных рекомендаций. За медицинской помощью не обращалась вплоть до апреля 2020г, когда была госпитализирована в связи с внебольничной двусторонней полисегментар ной пневмонией. В этот момент впервые получен положительный результат полимеразной цепной реакции (ПЦР) на SARS-CoV-2 без характерных клинических проявлений вирусной инфекции, назначена терапия в соответствии с актуальными клиническими рекомендациями [7], а также аторвастатин, ацетилсалициловая кислота, клопидогрел, продолжена терапия бета-блокаторами, ингибиторами ангиотензинпревращающего фермента и диуретиками, выписана с улучшением.
В июле 2020г отмечалось нарастание отечного синдрома с развитием анасарки, и пациентка вновь была госпитализирована в терапевтическое отделение многопрофильного стационара, где находилась до начала сентября 2020г. На электрокардиограмме (ЭКГ) при поступлении зарегистрирована синусовая тахикардия с частотой сердечных сокращений 105 уд./мин, резкое отклонение электрической оси сердца влево, блокада передней ветви левой ножки пучка Гиса, нарушение внутрижелудочковой проводимости, недостаточное нарастание зубца r с V1 по V5 (рис. 1 А).
При ЭхоКГ было выявлено нарушение локальной сократимости ЛЖ, предположено наличие постинфарктного кардиосклероза. Толщина межжелудочковой перегородки (МЖП) составляла 1,5 см, задней стенки ЛЖ (ЗСЛЖ) 1,2 см, отмечено нарастание легочной гипертензии с систолическим давлением в легочной артерии 56 мм рт.ст. По данным ЭхоКГ от конца августа 2020г, отмечено дальнейшее утолщение МЖП до 2,1 см, ЗСЛЖ до 1,4 см (рис. 2). В биохимическом анализе крови обращал на себя внимание крайне низкий уровень альбумина (до 11 г/л) в сыворотке крови, обусловленный массивной протеинурией (10 г/л), при незначительном снижении расчетной скорости клубочковой фильтрации до 45 мл мин/1,73 м2 по формуле CKD-EPI. Размеры почек, по данным ультразвукового исследования, были в пределах нормы. Пациентке проводили лечение СН, заместительную терапию альбумином, многократно торакоцентез с целью удаления жидкости из плевральных полостей.
По данным компьютерной томографии (КТ) ОГК в июле 2020г, в правом лёгком в S1-2-3-4 и в левом лёгком в S1-2-3-4-6-8-9-10 определялись множественные участки уплотнения паренхимы по типу "матового стекла" с перибронхиальным и периферическим распределением и участками консолидации. В просветах плевральных полостей определялся выпот, толщиной до 7,5 см справа и до 4 см слева. Легочный рисунок с обеих сторон обогащен за счет сосудисто-интерстициального акцента. Поражение правого и левого легких достигало 50% (КТ-2-3). Определялись двусторонний гидроторакс, компрессионный ателектаз базальных сегментов нижней доли левого легкого и застой в малом круге кровообращения. В связи с трудностью дифференциации изменений в легких был повторно взят мазок на ПЦР для определения SARS-CoV-2, показавший положительный результат, при отсутствии повышения IgM: 0,2 г/л (норма <2 г/л) и IgG: 0,22 г/л (норма <10 г/л). В соответствии с положением о противоэпидемических мерах пациентка была переведена в обсервационное отделение, пролечена, выписана домой под наблюдение врача поликлиники.
В конце сентября 2020г пациентка была госпитализирована в ГКБ им. В. М. Буянова ДЗМ в связи с нарастанием явлений СН, обмороками при переходе из горизонтального в вертикальное положение, парестезиями в нижних конечностях. При поступлении результат ПЦР на SARS-CoV-2 отрицательный. Несмотря на ранее положительный результат ПЦР на SARS-CoV-2 от апреля и начала сентября 2020г, по-прежнему отсутствовали антитела к SARS-CoV-2 (IgM: 0,13 г/л (<2 г/л), IgG: 2,24 г/л (<10 г/л)). В данную госпитализацию отмечена выраженная артериальная гипотония, в связи с чем в течение 7 сут. проводилась инотропная поддержка. Обращало на себя внимание повышение D-димера до 1571 мкг/л при отсутствии данных за тромбоз вен нижних конечностей, креатинина до 139 мкмоль/л, снижение расчетной скорости клубочковой фильтрации (CKD-EPI) до 32 мл/мин/1,73 м2. Результаты ЭхоКГ показали, помимо утолщения стенок ЛЖ (МЖП до 2,1 см, ЗСЛЖ до 1,5 см), незначительное снижение ФВ ЛЖ (52%), отсутствие локального нарушения сократимости, малый объем ЛЖ (конечно-диастолический объем ЛЖ — 45 мл), специфическую "зернистость" миокарда. С учетом наличия у больной массивной протеинурии, хронической болезни почек, утолщения стенок ЛЖ на фоне уменьшенной полости с признаками его диастолической дисфункции, устойчивой артериальной гипотонии, периферической полиневропатии был заподозрен амилоидоз. По данным электрофореза белков сыворотки крови, был обнаружен парапротеин в области фракции β-1 глобулинов, представленный IgA и Ig lambda (рис. 3). В костно-мозговом пунктате при нормальной клеточности было повышено количество плазмацитов (9% при норме до 1,8%). В подкожно-жировой клетчатке и трепанобиоптате костного мозга были выявлены депозиты амилоида (в стенках сосудов) (Grade CR 3+, местами CR 4+) (рис. 4).
Типирование амилоида не было проведено по техническим причинам, тем не менее, с учетом плазматизации костного мозга и изменений белковых фракций сыворотки крови, диагностирован AL- амилоидоз.
На основании клинико-лабораторно-инструментальных данных, диагностирован системный амилоидоз (вероятно, AL-тип, Ig A, Ig lambda) с поражением сердца (амилоидная кардиомиопатия), почек (нефротический синдром, гипоальбуминемия, нефрогенная анемия легкой степени), нервной системы (дистальная сенсорная полиневропатия, автономная невропатия, ортостатическая гипотензия).
Лечение. Фуросемид 20 мг 1 раз/сут., ривароксабан 10 мг 1 раз/сут, омепразол 20 мг 1 раз/сут., бисопролол 2,5 мг 1 раз/сут., трансфузии альбумина.
Последующее наблюдение. На фоне проведенной терапии состояние улучшилось, пациентка была выписана с рекомендацией обращения к гематологу для назначения патогенетической терапии амилоидоза. Однако данную рекомендацию выполнить не удалось из-за малой мобильности пациентки и ухудшения состояния, очевидно, на фоне прекращения альбуминзаместительной терапии после выписки из стационара.
В ноябре 2020г пациентка вновь была госпитализирована. При поступлении результат ПЦР на SARS-CoV-2 отрицательный, определялись антитела к SARS-CoV-2 IgM — 4,55 г/л, IgG — 494,0 г/л как следствие перенесенной ранее инфекции.
На ЭКГ — синусовый ритм, частота сердечных сокращений 84 уд./мин, отклонение электрической оси сердца влево, блокада передней ветви левой ножки пучка Гиса, недостаточное нарастание зубца r с V1 по V5 (рис. 1 Б).
По данным рентгенографии ОГК, выявлен двусторонний гидроторакс, признаки застоя по малому кругу кровообращения. Назначена многокомпонентная терапия, на фоне которой удалось повысить уровень альбумина с 15 г/л до 22 г/л, уменьшить выраженность отечного синдрома. После короткого периода улучшения, несмотря на проводимую терапию, отмечено нарастание креатинина сыворотки крови со 127 до 227 мкмоль/л, снижение альбумина за счет массивной протеинурии с потерей белка до 13 граммов в сут.
По данным КТ ОГК от начала декабря 2020г, в правом лёгком в S4, S5, S6, S9 определялись участки уплотнения паренхимы по типу "матового стекла" с перибронхиальным и периферическим распределением. Левое легкое было ателектазировано и коллабировано за счет содержимого в левом главном бронхе и выпота в плевральной полости, толщиной слоя до 61 мм. В правой плевральной полости определялся выпот, толщиной слоя до 53 мм. Органы и сосуды средостения были смещены вправо. В полости перикарда находился выпот, толщиной слоя до 5 мм. Отмечался диффузный отек подкожно-жировой клетчатки. Была диагностирована правосторонняя пневмония с высокой степенью вероятности вирусной пневмонии, двусторонний гидроторакс, гидроперикард (рис. 5). Вновь положительный ПЦР-тест на SARS-CoV-2 при тех же показателях антител: IgM — 1,7 г/л; IgG — 351,4 г/л.
В связи с положительным результатом ПЦР пациентка по требованиям санэпидрежима и в связи с тяжелым состоянием была переведена в инфекционное отделение ГКБ им. Юдина, где находилась в течение 14 дней.
Пациентка была выписана с диагнозом:
Основное заболевание: 1. "Коронавирусная инфекция SARS-CoV-2, вирус идентифицирован. 2. Системный амилоидоз (AL-тип, Ig A, Ig lambda) с поражением сердца (амилоидная кардиомиопатия с выраженной ассиметричной псевдогипертрофией миокарда с обструкцией выходного отдела ЛЖ, с поражением клапанного аппарата с формированием умеренного митрального стеноза, митральной недостаточности II ст., аортальной недостаточности II степени, трикуспидальной недостаточности II ст.), почек (нефротический синдром, гипоальбуминемия, нефрогенная анемия легкой степени), нервной системы (дистальная полиневропатия сенсорного типа, автономная полиневропатия, ортостатическая гипотензия).
Фоновое заболевание: СД 2 типа, целевой уровень гликированного гемоглобина <8%.
Осложнения: Двусторонняя полисегментарная пневмония, средней тяжести. Дыхательная недостаточность II степени. ХСН с сохраненной ФВ ЛЖ IIБ степени, IV функциональный класс. Двусторонний гидроторакс, гидроперикард. Диабетическая микро-, макроангиопатия, ретинопатия, нефропатия. Хроническая болезнь почек 4 стадии (скорость клубочковой фильтрации 19 мл мин/1,73 м2 по CKD-EPI).
Сопутствующее заболевание: Хроническая ишемия головного мозга".
Исход. Через 4 дня после выписки пациентка скончалась дома. Причиной смерти послужило прогрессирование полиорганной недостаточности.
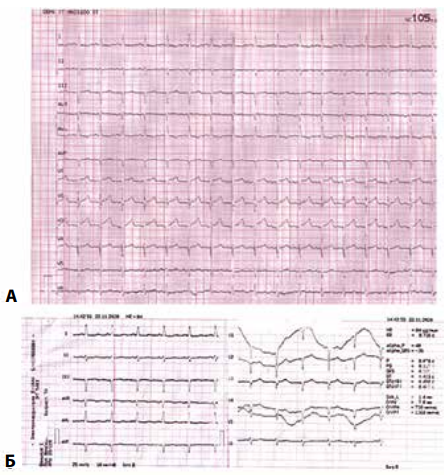
Рис. 1. ЭКГ пациентки при поступлении 7/2020 (А) и 11.2020 (Б) плевральных полостей — торакоцентезы.
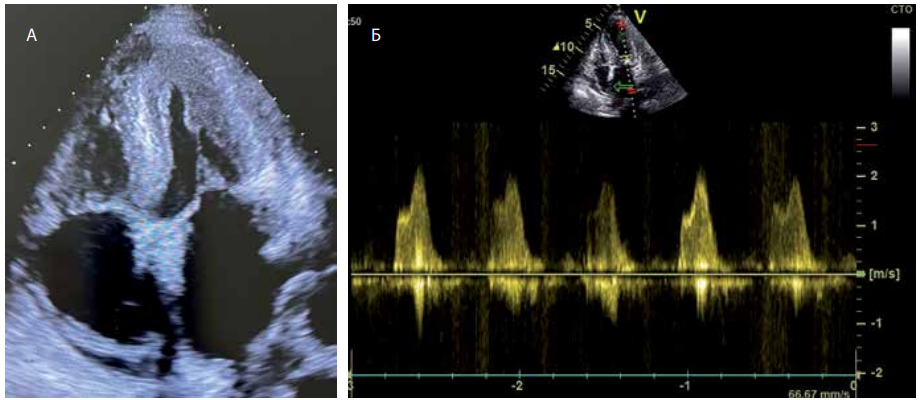
Рис. 2. Утолщение стенки ЛЖ, МЖП с дилатацией обоих предсердий, утолщение створок митрального и аортального клапанов (А). Нарушение релаксации (диастолическая дисфункция 1 типа), трансмитральный поток, импульсноволновая допплерография (Б).
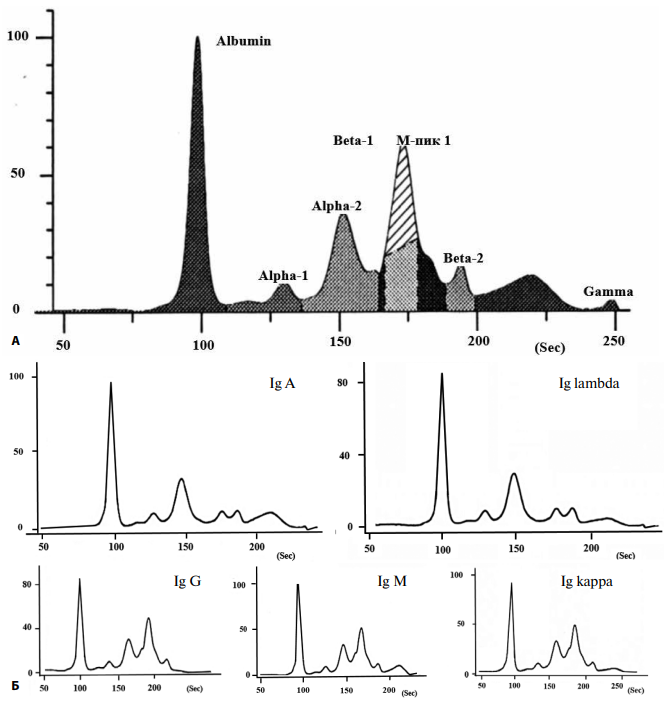
Рис. 3. Результаты электрофоретического исследования белков сыворотки крови с иммунотипированием.
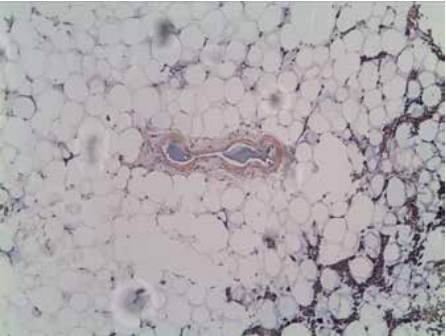
Рис. 4. Депозиты амилоида в подкожно-жировой клетчатке (в стенках сосудов) (Grade CR 3+), при окраске Конго красным (Е 20х). Из архива доктора Степановой Е. А.
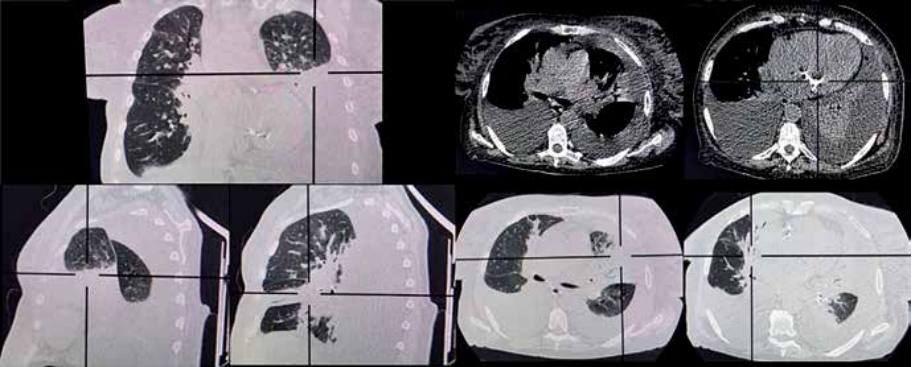
Рис. 5. КТ ОГК (начало декабря 2020г).
Обсуждение
У больных COVID-19 часто регистрируются ССЗ, ожирение и СД. Анализ 44672 случаев с подтвержденным диагнозом COVID-19 из Chinese Center for Disease Control and Prevention констатировал высокую летальность у больных с артериальной гипертонией (17,1%), ССЗ (16,4%) и СД (9,7%), тогда как летальность в общей популяции составляет 2,3% [8].
В Британском исследовании с участием почти 160 тыс. человек было подтверждено, что COVID-19 связана с более высоким риском ССЗ и смерти в краткосрочной и долгосрочной перспективе. По сравнению с неинфицированными людьми вероятность смерти пациентов с COVID-19 была в 81 раз выше в первые 3 нед. после заражения и оставалась в 5 раз выше в течение 18 мес. спустя [9]. Исследователи также выявили, что по сравнению с людьми с единичной инфекцией у реинфицированных был более высокий риск смерти, госпитализации и неблагоприятных исходов с поражением многих органов, включая и ССЗ. Bowe B, et al. при анализе медицинских карт 38 тыс. человек с реинфекцией COVID-19 обнаружили, что высокий риск смертности, госпитализаций и осложнений не зависел от вакцинации. Каждое инфицирование повышало риск осложнений как в краткосрочный, так и долгосрочный период [10]. Реинфицирование SARS-CoV-2 нашей пациентки во время стационарного лечения в условиях пандемии COVID-19, вероятно, внесло вклад в быстрое прогрессирование и неблагоприятный исход заболевания.
При декомпенсации ХСН на фоне COVID-19 важно ежедневно контролировать диурез, соблюдать рациональный питьевой режим, продолжать прием плановой базовой терапии, включая ингибиторы ангиотензинпревращающего фермента/блокаторы рецептора ангиотензина/антагонисты рецепторов ангиотензина и ингибиторы неприлизина; бета-блокаторы, антагонисты минералокортикоидных рецепторов и др., при необходимости добавлять/увеличивать дозы диуретических препаратов [8]. В рассматриваемом клиническом наблюдении пациентка получала базовую терапию ХСН, но по мере прогрессирования патологического процесса назначение рекомендованных препаратов стало лимитироваться тяжелой артериальной гипотонией. Ингибиторы SGLT2 не назначались в связи с отсутствием доказательной базы для пациентов с ХСНсФВ, актуальных периоду наблюдения пациентки, и отсутствием доказательной базы для данной группы препаратов у пациентов с AL-амилоидозом.
Исследования показывают значительные нарушения в системе свертывания крови у пациентов с COVID-19 и указывают на возможность ранней профилактики осложнений коронавирусной инфекции с помощью пероральных антикоагулянтов. Назначение антикоагулянтной терапии связано с меньшей смертностью и вероятностью интубации среди госпитализированных пациентов с COVID-19 [11]. Антикоагулянтная терапия в связи с высоким тромботическим риском показана большинству пациентов с амилоидной кардиомиопатией, и пациентка также ее получала, хотя назначена данная терапия была в одну из последних госпитализаций [2].
Для AL-амилоидоза характерно мультисистемное поражение с различной степенью органной дисфункции [2]. COVID-19 у пациентов с AL-амилоидозом имеет тяжелое течение и характеризуется высоким риском смерти [4]. В одном из исследований Программы по амилоидозу Калгари (Канада) было продемонстрировано 15 подтвержденных ПЦР случаев COVID-19 в протестированной популяции пациентов с амилоидозом, с более высокой частотой инфицирования именно среди пациентов с AL-амилоидозом по сравнению с когортой ATTR-амилоидоза (26,2% vs 5,1%). Четырем пациентам (26,6%) в связи с инфекцией потребовалась госпитализация (2 с ATTR и 2 с AL-амилоидозом). Из подтвержденных случаев 1 (0,07%) невакцинированный пациент с ATTR умер от COVID-19. Рост смертности был выявлен в обеих когортах при сравнении предпандемийных данных 2018 и 2019гг с данными 2020 и 2021гг [12]. При исследовании 187 пациентов (174 с множественной миеломой, 13 — с AL-амилоидозом), у которых была подтверждена COVID-19 в клинике Мейо между 01.12.2019 и 31.08.2021, у четверти течение COVID-19 было тяжелым. При этом 19 (10%) пациентам потребовалась госпитализация в отделение интенсивной терапии, а 5 (3%) — искусственная вентиляция легких. Смертность среди госпитализированных пациентов с COVID-19 составила 22% (16/72 пациента). Среди пациентов, которые были полностью вакцинированы на момент заражения (n= 12), у 2 (17%) развилась тяжелая COVID-19. При многофакторном анализе лечение антителами к CD38 в течение 6 мес. после заражения COVID-19 (отношение рисков (ОР) 3,6 (95% доверительный интервал (ДИ): 1,2-10,5), p=0,02), сердечное (ОР 4,1 (95% ДИ: 1,3-12,4), p=0,014) или сопутствующие легочные заболевания (ОР 3,6 (95% ДИ: 1,1-11,6); p=0,029) были независимыми предикторами госпитализации в отделение интенсивной терапии. Сопутствующая сердечная патология (ОР 2,6 (95% ДИ: 1,1-6,5), p=0,038) была независимым предиктором смертности, тогда как ремиссия как множественной миеломы, так и AL-амилоидоза были ассоциированы с более низкой смертностью (ОР 0,4 (95% ДИ: 0,2-0,8); р=0,008) [13]. Таким образом, было показано, что активное заболевание увеличивает риск тяжелой COVID-19 и смертность пациентов.
Представленное нами наблюдение показывает трудность диагностики амилоидоза в условиях пандемии COVID-19, когда наличие положительного ПЦР-теста на SARS-CoV-2 затрудняет обращение пациента к врачу, требует изоляции, перевода в обсервационное отделение или госпитализации в инфекционный стационар. Вместе с тем наличие у пациентки положительных результатов ПЦР-тестов не повлияло на диагностический поиск основного заболевания, но, несомненно, отсрочило возможное обращение к гематологу (хотя в момент верификации диагноза тяжесть состояния свидетельствовала о крайне неблагоприятном прогнозе, который вряд ли мог быть улучшен специфическим лечением AL- амилоидоза).
Интересным представляется в данном случае неоднократное выявление вирусного материала SARS-CoV-2 по данным ПЦР: в апреле, августе и декабре 2020г (рис. 6).
Известно, что антителa класса IgМ появляются примерно на 7-е сут. от момента инфицирования и могут сохраняться до ≥2 мес., а антитела класса IgG начинают определяться примерно через 3 нед. и сохраняются длительное время. В апреле 2020г, когда у пациентки впервые выявлена положительная ПЦР, при обследовании данных за пневмонию не было, хотя в отсутствие данных визуализирующих исследований с высокой разрешающей способностью окончательный вывод сделать не представляется возможным. Если предположить факт инфицирования в апреле, то рост уровня иммуноглобулинов к SARS-CoV-2 начался только через 6-7 мес. после первого положительного ПЦР-теста (рис. 6). Отсроченная выработка антител могла быть связана с дефектом гуморального ответа на вирус у пациентки с плазмоклеточной дискразией [12], а также полиорганным отложением амилоида, в т.ч. в кроветворных органах. Нарушения иммунного ответа могли привести к длительной персистенции и, соответственно, детекции вируса в отсутствие адекватной продукции антител. Все же наиболее вероятным вариантом нам представляется повторное заражение в августе 2020г (с учетом данных КТ ОГК). Антитела класса IgM и IgG были выявлены в ноябре 2020г (отсроченно, хотя в октябре их уровень не определяли) при отрицательных результатах ПЦР, что соответствует данной гипотезе. Антитела класса IgM были повышенными вплоть до начала декабря 2020г и при этом повторно выявлена РНК вируса. По данным КТ ОГК в этот момент (участки уплотнения паренхимы по типу "матового стекла" с перибронхиальным и периферическим распределением в 4 сегментах правого легкого), положительного результата ПЦР, наиболее вероятно, имела место реинфекция (возможно, другим вариантом SARS-CoV-2). Кроме того, нельзя исключать еще одну вероятную причину — длительное вирусовыделение у пациентки при отсутствии полной элиминации вируса.
К сожалению, необходимо констатировать, что в данном случае диагноз амилоидоза мог быть поставлен уже в первую госпитализацию, поскольку у пожилых пациентов вероятность дебюта гипертрофической кардиомиопатии крайне низка. Кроме того, диагноз амилоидоза был более вероятен, чем наличие гипертонического сердца, поскольку пациентка отрицала значимое повышение артериального давления в анамнезе. Диагностическая мысль еще при первом обследовании должна была развиваться именно в направлении инфильтративного заболевания сердца, при котором нередко развивается выраженная обструкция выносящего тракта ЛЖ [3]. Отсутствие своевременной диагностики инфильтративного заболевания сердца может свидетельствовать о низкой информированности и амилоидонастороженности врачебного сообщества.
После верифицикации диагноза состояние пациентки было крайне тяжелым, имел место тяжелый кардиоренальный синдром: терминальная СН и массивная потеря белка. Представляется весьма вероятным, что коронавирусная инфекция у нашей пациентки способствовала прогрессированию системного амилоидоза и ускорила наступление летального исхода.
Известно, что пожилой и старческий возраст остается независимым неблагоприятным прогностическим фактором при проведении химиотерапии у пациентов с AL-амилоидозом [14]. Вместе с тем, несмотря на относительно небольшое число исследований, посвященных лечению AL-амилоидоза у пожилых, в ряде из них получены положительные результаты. Так, в исследовании, включавшем 295 пожилых пациентов с AL-амилоидозом старше 75 лет (Национальный центр амилоидоза, Лондон, 2002-2015гг), несмотря на то, что только 1/4 пациентов удалось завершить все 6 циклов химиотерапии, из них 63% достигли гематологического ответа (из них у 1/3 он был хорошим частичным и полным), что привело к удовлетворительным показателям в отношении выживаемости [15]. В связи с этим, к сожалению, можно констатировать, что при более ранней диагностике заболевания у описываемой пациентки, возможно, были бы шансы на более благоприятное течение заболевания и отдаление времени наступления летального исхода.
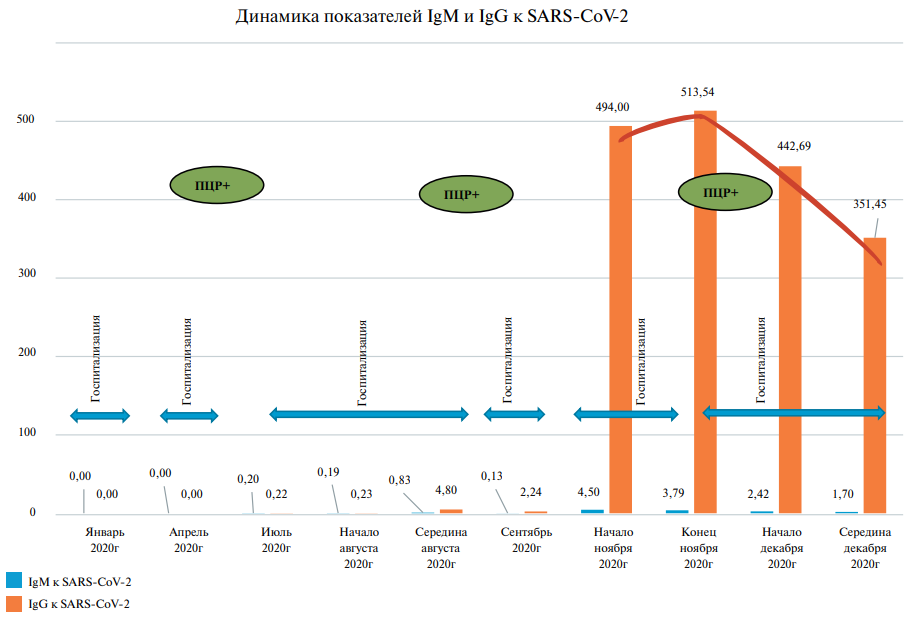
Рис. 6. Хронология заболевания и динамика показателей IgM и IgG к SARS-CoV-2.
Сокращение: ПЦР — полимеразная цветная реакция.
Заключение
Системный амилоидоз — заболевание, при котором несвоевременная диагностика и позднее начало терапии могут быть губительны для пациента. COVID-19 значимо повышает риск летальности при сопутствующих мультисистемных заболеваниях, в т.ч. AL-амилоидозе. Так как заболеваемость амилоидозом по всему миру в настоящее время растет, врач любой специальности должен быть насторожен в отношении амилоидоза, как в период пандемии COVID-19, так и в любое другое время.
Информированное согласие. От пациента было получено письменное добровольное информированное согласие на публикацию результатов обследования и лечения (дата подписания 28.09.2020г)
Отношения и деятельность: все авторы заявляют об отсутствии потенциального конфликта интересов, требующего раскрытия в данной статье.
Список литературы
1. Zhang Y, Coats AJS, Zheng Z, et al. Management of heart failure patients with COVID-19: a joint position paper of the Chinese Heart Failure Association & National Heart Failure Committee and the Heart Failure Association of the European Society of Cardiology. Eur J Heart Fail. 2020;22:941-56. doi:10.1002/ejhf.1915.
2. Резник Е. В., Нгуен Т. Л., Степанова Е. А. и др. Амилоидоз сердца: взгляд терапевта и кардиолога. Архивъ внутренней медицины. 2020;10:430-57. doi:10.20514/2226-67042020-10-6-430-457.
3. Резник Е. В., Нгуен Т. Л., Устюжанин Д. В. и др. "Красные флаги" диагностики инфильтративных заболеваний сердца. Российский кардиологический журнал. 2023;28(1S):5259. doi:10.15829/1560-4071-2023-5259.
4. Crees ZD, Stockerl-Goldstein K. COVID-19 and Light Chain Amyloidosis, Adding Insult to Injury. Am J Med. 2022;135:S49-52. doi:10.1016/j.amjmed.2022.01.005.
5. Kastritis E, Wechalekar A, Schönland S, et al. Challenges in the management of patients with systemic light chain (AL) amyloidosis during the COVID-19 pandemic. Br J Haematol. 2020;190:346-57. doi:10.1111/bjh.16898.
6. Seferovic PM, Ponikowski P, Anker SD, et al. Clinical practice update on heart failure 2019: pharmacotherapy, procedures, devices and patient management. An expert consensus meeting report of the Heart Failure Association of the European Society of Cardiology. Eur J Heart Fail. 2019;21:1169-86. doi:10.1002/ejhf.1531.
7. Chakraborty C, Sharma AR, Sharma G, et al. SARS-CoV-2 causing pneumonia-associated respiratory disorder (COVID-19): diagnostic and proposed therapeutic options. Eur Rev Med Pharmacol Sci. 2020;24:4016-26. doi:10.26355/eurrev_202004_20871.
8. Блохин А. А., Шишкин А. Н., Князева А. И. Cердечно-сосудистые осложнения, обусловленные коронавирусной инфекцией (COVID-19). Juvenis Scientia. 2022;8:6-14. doi:10.32415/jscientia_2022_8_6_6-14.
9. Raisi-Estabragh Z, Cooper J, Salih A, et al. Cardiovascular disease and mortality sequelae of COVID-19 in the UK Biobank. Heart. 2023;109:119-26. doi:10.1136/heartjnl-2022-321492.
10. Bowe B, Xie Y, Al-Aly Z. Acute and postacute sequelae associated with SARS-CoV-2 reinfection. Nat Med. 2022;28:2398-405. doi:10.1038/s41591-022-02051-3.
11. оробьева П. А. Рекомендации по ведению больных с коронавирусной инфекцией COVID-19 в острой фазе и при постковидном синдроме в амбулаторных условиях. Проблемы стандартизации в здравоохранении. 2021;7-8:396. doi:10.26347/1607-2502202107-08003-096.
12. Lewis E, Fine N, Miller RJH, et al. Amyloidosis and COVID-19: experience from an amyloid program in Canada. Ann Hematol. 2022;101:2307-15. doi:10.1007/s00277-022-04964-y.
13. Ho M, Zanwar S, Buadi FK, et al. Risk factors for severe infection and mortality In patients with COVID-19 in patients with multiple myeloma and AL amyloidosis. Am J Hematol. 2023;98:49-55. doi:10.1002/ajh.26762.
14. Skinner M, Sanchorawala V, Seldin DC, et al. High-dose melphalan and autologous stemcell transplantation in patients with AL amyloidosis: an 8-year study. Ann Intern Med. 2004;140:85-93. doi:10.7326/0003-4819-140-2-200401200-00008.
15. Sachchithanantham S, Offer M, Venner C, et al. Clinical profile and treatment outcome of older (>75 years) patients with systemic AL amyloidosis. Haematologica. 2015;100:146976. doi:10.3324/haematol.2015.128025.
Об авторах
Е. В. РезникРоссия
Елена Владимировна Резник — доктор медицинских наук, доцент, заведующий кафедрой пропедевтики внутренних болезней лечебного факультета, врач-кардиолог, терапевт, врач функциональной диагностики.
Москва
Конфликт интересов:
все авторы заявляют об отсутствии потенциального конфликта интересов, требующего раскрытия в данной статье
Т. Л. Нгуен
Вьетнам
Тхань Луан Нгуен — аспирант кафедры пропедевтики внутренних болезней лечебного факультета.
Москва
Конфликт интересов:
все авторы заявляют об отсутствии потенциального конфликта интересов, требующего раскрытия в данной статье
О. А. Эттингер
Россия
Ольга Александровна Эттингер — кандидат медицинских наук, доцент, кафедра госпитальной терапии им. акад. Г. И. Сторожакова лечебного факультета.
Москва
Конфликт интересов:
все авторы заявляют об отсутствии потенциального конфликта интересов, требующего раскрытия в данной статье
В. А. Лазарев
Россия
Владимир Андреевич Лазарев — ассистент кафедры госпитальной терапии им. акад. Г. И. Сторожакова лечебного факультета.
Москва
Конфликт интересов:
все авторы заявляют об отсутствии потенциального конфликта интересов, требующего раскрытия в данной статье
С. В. Борисовская
Россия
Светлана Васильевна Борисовская — кандидат медицинских наук, доцент, кафедра госпитальной терапии им. акад. Г. И. Сторожакова лечебного факультета, заведующий терапевтическим отделением.
Москва
Конфликт интересов:
все авторы заявляют об отсутствии потенциального конфликта интересов, требующего раскрытия в данной статье
А. И. Гусева
Россия
Анна Игоревна Гусева — сотрудник.
Москва
Конфликт интересов:
все авторы заявляют об отсутствии потенциального конфликта интересов, требующего раскрытия в данной статье
А. В. Саликов
Россия
Александр Викторович Саликов — кандидат медицинских наук, главный врач.
Москва
Конфликт интересов:
все авторы заявляют об отсутствии потенциального конфликта интересов, требующего раскрытия в данной статье
Г. Н. Голухов
Россия
Георгий Натанович Голухов — президент, заместитель председателя Общественного совета при Департаменте здравоохранения города Москвы.
Москва
Конфликт интересов:
все авторы заявляют об отсутствии потенциального конфликта интересов, требующего раскрытия в данной статье
Дополнительные файлы
Рецензия
Для цитирования:
Резник Е.В., Нгуен Т., Эттингер О.А., Лазарев В.А., Борисовская С.В., Гусева А.И., Саликов А.В., Голухов Г.Н. Тяжелое течение AL-амилоидоза сердца у пациентки пожилого возраста с многократной реинфекцией SARS-CoV-2. Клинический случай. Российский кардиологический журнал. 2023;28(8):5443. https://doi.org/10.15829/1560-4071-2023-5443. EDN: JMSMHZ
For citation:
Reznik E.V., Nguyen T., Ettinger O.A., Lazarev V.A., Borisovskaya S.V., Guseva A.I., Salikov A.V., Golukhov G.N. Severe cardiac AL amyloidosis in an elderly patient with multiple SARS-CoV-2 reinfection: a case report. Russian Journal of Cardiology. 2023;28(8):5443. (In Russ.) https://doi.org/10.15829/1560-4071-2023-5443. EDN: JMSMHZ
JATS XML

















































