Перейти к:
Риск развития хронической сердечной недостаточности у больных сахарным диабетом 2 типа, получающих терапию инсулином: метаанализ наблюдательных исследований
https://doi.org/10.15829/1560-4071-2023-5375
Аннотация
Цель. Сравнить влияние инсулинотерапии и пероральных сахароснижающих препаратов (ПССП) на риск развития хронической сердечной недостаточности (ХСН) у больных сахарным диабетом (СД) 2 типа с использованием различных баз данных.
Материал и методы. Систематический обзор и метаанализ выполнены в соответствии с международными рекомендациями "Предпочитаемые элементы отчетности для систематических обзоров и метаанализов" (PRISMA). В анализ включались исследования, в которых проводилось сравнение риска развития ХСН у пациентов с СД 2 типа в зависимости от выбора ПССП при наличии группы пациентов, получающих терапию инсулином. Критериями включения исследований в метаанализ были длительность лечения не менее двух лет с общим количеством включенных больных не <1 тыс. В анализ не были включены исследования, в которых сравнивались виды и режимы инсулинотерапии без группы контроля (применение сахароснижающих препаратов), в которые включались больные с острыми осложнениями СД 2 типа и нестабильными состояниями, связанными с коморбидной патологией, в которых не сообщалось о клинических исходах, которые были опубликованы только в виде аннотации. Поиск по ключевым словам проводился в августе 2022г с использованием нескольких баз данных: PubMed, Кохрановский центральный регистр контролируемых исследований (CENTRAL) в Кохрановский библиотеке, Научная электронная библиотека Elibrary с использованием ключевых слов: heart failure development (развитие сердечной недостаточности), 2 type diabetes mellitus (сахарный диабет 2 типа), insulin (инсулин).
Результаты. Из 1085 публикаций, найденных в ходе поиска, 5 ретроспективных наблюдательных когортных клинических исследований, включающих в общей сложности 179777 пациентов со средней длительностью лечения 67,2 мес., соответствовали всем критериям и были включены в анализ. Статистический анализ величины относительного риска (RR) развития ХСН у больных СД 2 типа, получающих инсулинотерапию, среди пяти исследований, включенных в метаанализ, выявил увеличение RR во всех исследованиях с общим RR при использовании модели фиксированных эффектов — 2,598 (95% доверительный интервал (ДИ) 2,346-2,878; p<0,001), при использовании модели случайных эффектов — 2,382 (95% ДИ 1,565-3,626; p<0,001). При проверке статистической неоднородности исследований выявлена неоднородность высокой степени: I2=93,8%, что учитывалось при интерпретации данных.
Заключение. Результаты проведенного метаанализа 5 ретроспективных наблюдательных исследований с включением 179777 больных СД 2 типа со средней продолжительностью лечения 67,2 мес. показали, что инсулинотерапия (без включения инсулинов гларгин и деглюдек) в сравнении с ПССП (без включения ингибиторов натрийглюкозного ко-транспортера 2 типа и агонистов глюкагоноподобного пептида 1 типа) статистически значимо увеличивала RR развития ХСН с использованием модели фиксированных эффектов в 2,6 раза, при использовании модели случайных эффектов — в 2,4 раза (p<0,001 для обоих).
Для цитирования:
Миронова С.В., Козиолова Н.А., Улыбина Е.В. Риск развития хронической сердечной недостаточности у больных сахарным диабетом 2 типа, получающих терапию инсулином: метаанализ наблюдательных исследований. Российский кардиологический журнал. 2023;28(3):5375. https://doi.org/10.15829/1560-4071-2023-5375
For citation:
Mironova S.V., Koziolova N.A., Ulybina E.V. Risk of heart failure in patients with type 2 diabetes receiving insulin therapy: a meta-analysis of observational studies. Russian Journal of Cardiology. 2023;28(3):5375. (In Russ.) https://doi.org/10.15829/1560-4071-2023-5375
Несмотря на результаты рандомизированных клинических исследований (РКИ) и ряда метаанализов РКИ и наблюдательных исследований, до сих пор влияние инсулинотерапии на риск развития хронической сердечной недостаточности (ХСН) у больных сахарным диабетом (СД) 2 типа не определено.
Так, в субанализе РКИ TOPCAT (Treatment of Preserved Cardiac Function Heart Failure With an Aldosterone Antagonist) оценили влияние СД 2 типа и инсулинотерапии на клинические исходы у больных ХСН с сохраненной фракцией выброса левого желудочка. Авторы сравнили 3 группы: пациенты без СД 2 типа; пациенты с СД 2 типа, получающие инсулинотерапию, пациенты с СД 2 типа, использующие пероральные сахароснижающие препараты (ПССП). Риск госпитализации по поводу ХСН у больных СД 2 типа и инсулинотерапией был почти в 2 раза выше (относительный риск (RR) 1,97) по сравнению с пациентами без СД 2 типа, и в 1,6 раза выше (RR 1,65) по сравнению с больными СД 2 типа, получающими ПССП [1].
С другой стороны, в субанализе 2 РКИ было найдено, что инсулинотерапия, в отличие от индекса массы тела, возраста, артериальной гипертензии, сывороточного креатинина, холестерина липопротеидов высокой плотности, длительности комплекса QRS на электрокардиограмме, инфаркта миокарда (ИМ) или коронарного шунтирования, не определяет риск ХСН у больных СД 2 типа [2]. Уровень контроля глюкозы плазмы крови натощак явился предиктором риска развития ХСН у больных СД 2 типа независимо от выбора сахароснижающей терапии.
В подтверждение этому выводу, в одном из наблюдательных исследований было найдено, что именно тяжелые гипогликемии были взаимосвязаны с увеличением риска госпитализаций, связанных с ХСН, среди больных с СД 2 типа, получающих ПССП в комбинации с инсулином или без него [3].
В Кохрейновском метаанализе РКИ у больных СД 2 типа при наличии такой коморбидной патологии, как хроническая болезнь почек (ХБП), в которых оценивалось влияние любой сахароснижающей терапии на риск развития сердечно-сосудистых событий и ХСН, для всех типов, дозировок и способов введения инсулина при прямых сравнениях были доступны только отдельные исследования, поэтому выводы не могли быть сделаны [4].
Более того, продолжение инсулинотерапии у больных с СД 2 типа при наличии ХСН усугубляет прогноз больных, увеличивая RR общей смерти на 46% (95% доверительный интервал (ДИ): 1,14-1,88), сердечно-сосудистой смерти — на 62% (95% ДИ: 1,33-1,96), как представлено в метаанализе 15 наблюдательных исследований [5].
Следовательно, изучение влияния инсулинотерапии на риск развития недостаточности кровообращения у больных СД 2 типа является актуальной задачей, определяющей прогноз больных и продолжительность их жизни.
Цель метаанализа: сравнить влияние инсулинотерапии и ПССП на риск развития ХСН у больных СД 2 типа с использованием различных баз данных.
Материал и методы
Систематический обзор и метаанализ выполнены в соответствии с международными рекомендациями "Предпочитаемые элементы отчетности для систематических обзоров и метаанализов" (PRISMA) [6].
В анализ включались исследования, в которых проводилось сравнение риска развития ХСН у пациентов с СД 2 типа в зависимости от выбора сахароснижающей терапии при наличии группы пациентов, получающих терапию инсулином. Наличие сердечно-сосудистых заболеваний (ССЗ) и применение других не сахароснижающих препаратов в качестве сопутствующей терапии разрешалось.
Критериями включения исследований в метаанализ были длительность лечения не менее двух лет с общим количеством включенных больных не <1 тыс.
Для поиска статей использовалась стратегия PICO [7]:
- пациент (Patient) — пациенты старше 18 лет;
- вмешательство (Intervention) — инсулинотерапия СД 2 типа;
- сравнение (Comparison) — лечение СД 2 типа другими ПССП;
- исходы (Outcomes) — заболеваемость ХСН.
В анализ не были включены исследования, в которых сравнивались виды и режимы инсулинотерапии без группы контроля (применение сахароснижающих препаратов), в которые включались больные с острыми осложнениями СД 2 типа и нестабильными состояниями, связанными с коморбидной патологией, в которых не сообщалось о клинических исходах, которые были опубликованы только в виде аннотации.
Включение исследований в метаанализ выполнялся двумя независимыми исследователями (С. В. Миронова, Н. А. Козиолова). При наличии разногласий учитывалось мнение третьего исследователя путем голосования. В метаанализ включались исследования независимо от даты его проведения и используемого языка. Для отбора исследований сначала анализировались их заголовки и тезисы, при соответствии критериям отбора проводился анализ полнотекстовых статей. При исключении статей, не соответствующих критериям отбора, велась регистрация причин несоответствия.
Этот метаанализ был выполнен на ранее проведенных исследованиях и не содержит каких-либо новых исследований с участием людей или животных, проведенных кем-либо из авторов.
Поиск по ключевым словам проводился в августе 2022г с использованием нескольких баз данных: PubMed (https://www.nlm.nih.gov); Кохрановский центральный регистр контролируемых исследований (CENTRAL) в Кохрановский библиотеке (https://www.cochranelibrary.com/central); Научная электронная библиотека Elibrary (https://www.elibrary.ru/defaultx.asp) с использованием ключевых слов: heart failure development (развитие сердечной недостаточности), 2 type diabetes mellitus (сахарный диабет 2 типа), insulin (инсулин).
Статистическая обработка данных проведена с помощью программного обеспечения MedCalc® statistical software версии 20.113. Непрерывные данные были показаны в виде средневзвешенных различий между группами с 95% ДИ; категориальные данные (частота развития ХСН) — в виде среднего значения ± стандартное отклонение (SD) для наблюдательных исследований. Качественные показатели представлены с использованием долей и процентных значений. Значение P<0,05 считалось статистически значимым. Характеристики и риск систематической ошибки для каждого исследования (результаты не показаны) учитывались при рассмотрении эффектов лечения для развития ХСН. Проверка статистической неоднородности исследований осуществлялась с помощью Q-теста на основе χ2. Модель случайных эффектов была принята при Р<0,1 в тесте χ2 и I2>40%, модель фиксированных эффектов при Р≥0,1 в тесте χ2 и I2≤40%.
Результаты
Из 1085 публикаций, найденных в ходе поиска, 5 ретроспективных наблюдательных когортных клинических исследований, включающих в общей сложности 179777 пациентов со средней длительностью лечения 67,2 мес., соответствовали всем критериям и были включены в анализ (рис. 1) [8-12].
Причины исключения из исследования приведены на рисунке 1.
Обзор исследований, включенных в анализ, представлен ниже (рис. 2).
Nichols GA, et al. (2005) оценили риск развития ХСН у пациентов с СД 2 типа в зависимости от варианта сахароснижающей терапии. В исследование были включены больные из регистра по СД Kaiser Permanente Northwest (KPNW) без предшествующей ХСН (n=8063). Исследователями проанализирован период с 01 января 1998г до 31 декабря 2002г [8]. Рассчитана частота ХСН у пациентов, получающих различные схемы лечения, с поправкой на возраст, пол, длительность СД 2 типа, наличие ишемической болезни сердца, артериальной гипертензии, ХБП и уровень гликемического контроля по показателю гликированного гемоглобина. По результатам исследования показатели заболеваемости ХСН были самыми высокими в группах больных, включающих инсулин. При дополнительном назначении инсулина к исходной терапии частота ХСН увеличивалась в 2,33 раза (p<0,0001) по сравнению с добавлением препаратов сульфонилмочевины и в 2,66 раза (p<0,0001) — по сравнению с добавлением метформина.
Rajagopalan R, et al. (2004) провели ретроспективное наблюдательное исследование с целью оценки риска развития ХСН у пациентов с СД 2 типа, получающих лечение пиоглитазоном и инсулином [9]. В исследование были включены пациенты из базы данных PharMetrics Patient-Centric (n=3336) без ХСН в анамнезе, которые начали лечение в период с января 1999г по декабрь 2001г. В выборку были включены пациенты, для которых имелись данные ≥12 мес. до начала лечения и ≥3 мес. последующего наблюдения. Группы пациентов в исследовании были сопоставимы по количеству включенных больных в соотношении 1:1. Средний возраст пациентов составил 51,2±0,2 года; 50,9% мужчин, 49,1% женщин. Общий показатель заболеваемости ХСН был значительно ниже в группе больных, получающих пиоглитазон, по сравнению с группой пациентов, получающих инсулинотерапию (2,0% vs 4,0%, соответственно; р<0,001).
Karter AJ, et al. (2005) провели ретроспективное наблюдательное когортное исследование в которое были включены пациенты с СД 2 типа из регистра Kaiser Permanente Northern California Diabetes Registry, получающие сахароснижающую терапию (n=23440). Был проанализирован период с октября 1999г по ноябрь 2001г. Исследователи оценили риск развития ХСН в зависимости от сахароснижающей терапии. Пациенты, получающие лечение препаратами сульфонилмочевины, были представлены в качестве контрольной группы. Пиоглитазон был исходной терапией у 15,2% пациентов, у 25,3% — препараты сульфонилмочевины, у 50,9% — метформин, у 8,6% — инсулин. Лечение СД 2 типа в исследовании применялось как в монотерапии, так и в комбинации. После поправки на демографические, поведенческие и клинические факторы, исследователями получены следующие данные: заболеваемость ХСН была значительно выше среди тех, у кого исходная терапия включала инсулин (RR 1,56; 95% ДИ: 1,00-2,45), и ниже среди тех, у кого исходная терапия была начата с применения метформина (RR 0,70; 95% ДИ: 0,49-0,99). Среди пациентов, начавших прием пиоглитазона, статистически значимого RR развития ХСН не зарегистрировано (RR 1,28; 95% ДИ: 0,85-1,92) [10].
Исследование Koro CE, et al. (2005) проводилось на основе данных U.K.-based General Practice Research Database (GPRD) [11]. В период с 1987 по 2001гг было выявлено 21888 пациентов с СД 2 типа. В этой когорте был зарегистрирован 1301 случай ХСН. Расчеты RR развития ХСН в зависимости от сахароснижающей терапии были выполнены с учетом длительности СД 2 типа и сопутствующих заболеваний. По результатам работы RR ХСН на фоне терапии инсулином был выше в 1,5 раза по сравнению с отсутствием сахароснижающей терапии (RR 1,52; 95% ДИ: 1,06-2,17); и в 1,4 раза — по сравнению с терапией препаратами сульфонилмочевины и их комбинацией с метформином (RR 1,38; 95% ДИ: 1,13-1,69).
Ou HT, et al. (2016) оценили риски развития ССЗ, в т.ч. ХСН, связанные с применением ингибиторов дипептидилпептидазы-4 (иДПП-4) и других противодиабетических препаратов у пациентов с СД 2 типа [12]. Пациенты были включены в исследование из Тайваньской национальной исследовательской базы данных медицинского страхования. Всего в 2009-2010гг было зарегистрировано 123050 пациентов с СД 2 типа, которым впервые назначили противодиабетические препараты. Наблюдение проводилось до 2013г. Исходы включали следующие сердечно-сосудистые события: госпитализации по поводу ишемического инсульта, ИМ; развитие ХСН и гипогликемий. При расчетах была произведена поправка на демографические данные пациентов, сопутствующие заболевания, диабетические осложнения и сопутствующую лекарственную терапию. По результатам исследования у пациентов с СД 2 типа, получавших терапию инсулином, RR развития ХСН был выше в 3,73 раза (RR 3,73, 95% ДИ: 3,35-4,14) по сравнению с пациентами, принимающими иДПП-4.
Исходные характеристики ретроспективных наблюдательных исследований, включенных в метаанализ, отличались по сахароснижающей терапии в группах сравнения (табл. 1). Препаратами сравнения в трех исследованиях были препараты сульфонилмочевины, в одном исследовании — пиоглитазон, в одном исследовании — иДПП-4. Самый длинный период лечения составил 168 мес., самый короткий — 24 мес. У большинства больных (67-100%) во включенных исследованиях были сопутствующие ССЗ.
Статистический анализ величины RR развития ХСН у больных СД 2 типа, получающих инсулинотерапию, среди пяти исследований, включенных в метаанализ, выявил увеличение RR во всех исследованиях с общим RR при использовании модели фиксированных эффектов — 2,598 (95% ДИ: 2,346-2,878; p<0,001), при использовании модели случайных эффектов — 2,382 (95% ДИ: 1,565-3,626; p<0,001) (табл. 2).
При проверке статистической неоднородности исследований выявлена неоднородность высокой степени: I2=93,8%, что следует учитывать при интерпретации данных (табл. 3).
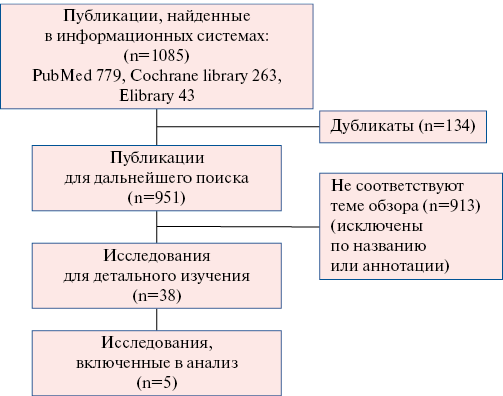
Рис. 1. Дизайн исследования PRISMA для данного исследования.

Рис. 2. Диаграмма изменения RR развития ХСН у пациентов с СД 2 типа, получающих терапию инсулином (n=5).
Таблица 1
Характеристики исследований, включенных в метаанализ (n=5)
|
№ |
Исследование |
Год исследования |
Количество пациентов |
Период наблюдения (мес.) |
Конечные точки |
Препарат сравнения |
RR развития ХСН |
|
1 |
Nichols GA, et al., 2005 [8] |
01.1998 — 12.2002 |
8063 |
60 |
заболеваемость ХСН |
ПСМ |
2,33 |
|
2 |
Rajagopalan R, et al., 2004 [9] |
01.1999 — 12.2001 |
3336 |
36 |
заболеваемость ХСН |
пиоглитазон |
4,00 |
|
3 |
Karter AJ, et al., 2005 [10] |
10.1999 — 11.2001 |
23440 |
24 |
заболеваемость ХСН |
ПСМ |
1,56 |
|
4 |
Koro CE, et al., 2005 [11] |
1987 — 2001 |
21888 |
168 |
заболеваемость ХСН |
ПСМ |
1,38 |
|
5 |
Ou HT, et al., 2016 [12] |
2009 — 2013 |
123050 |
48 |
заболеваемость ХСН |
иДПП-4 |
3,73 |
Сокращения: иДПП-4 — ингибиторы дипептидилпептидазы-4, ПСМ — производные сульфонилмочевины, ХСН — хроническая сердечная недостаточность, RR — относительный риск.
Таблица 2
Результаты метаанализа с расчетом RR развития ХСН с использованием модели фиксированных и случайных эффектов (n=5)
|
Исследование |
RR |
95% ДИ |
Z |
P |
Вес (٪) |
|
Nichols GA, et al., 2005 |
2,330 |
1,847-2,939 |
20,03 |
||
|
Rajagopalan R, et al., 2004 |
4,000 |
3,230-4,954 |
20,22 |
||
|
Karter AJ, et al., 2005 |
1,560 |
1,214-2,004 |
19,83 |
||
|
Koro CE, et al., 2005 |
1,400 |
1,084-1,808 |
19,77 |
||
|
Ou HT, et al., 2016 |
3,700 |
2,967-4,614 |
20,15 |
||
|
Всего (фиксированные эффекты) |
2,598 |
2,346-2,878 |
18,310 |
<0,001 |
100,00 |
|
Всего (случайные эффекты) |
2,382 |
1,565-3,626 |
4,049 |
<0,001 |
100 |
Сокращения: ДИ — доверительный интервал, RR — относительный риск.
Таблица 3
Оценка статистической неоднородности исследований, включенных в метаанализ (n=5)
|
Q |
64,7028 |
|
Уровень значимости |
P<0,0001 |
|
I2 (несогласованность) |
93,82% |
|
95% ДИ для I2 |
88,45-96,69 |
Сокращение: ДИ — доверительный интервал.
Обсуждение
Известно, что пациенты с СД 2 типа имеют двукратный риск развития ХСН, как с сохраненной, так и низкой фракцией выброса левого желудочка [13]. Помимо структурных и функциональных изменений, которые характеризуют диабетическую кардиомиопатию, существуют сложные и взаимосвязанные патофизиологические механизмы, которые запускают процесс формирования ХСН.
Несмотря на успех многих широко используемых сахароснижающих препаратов для контроля гипергликемии при СД 2 типа, высокая распространенность ХСН сохраняется [14]. Таким образом, это повышает вероятность того, что дополнительные факторы, помимо гликемии, такие как применение сахароснижающих препаратов, могут способствовать повышению риска ХСН при СД 2 типа. Так, среди сахароснижающих препаратов метформин, ингибиторы натрийглюкозного ко-транспортера 2 типа (иНГЛТ-2) и некоторые агонисты глюкагонподобного пептида 1 типа (аГПП-1) могут снижать риск госпитализаций, связанных с ХСН, некоторые иДПП-4 проявляют в этом отношении нейтральность, другие, такие как препараты сульфонилмочевины, тиазолидиндионы, инсулин, некоторые аГПП-1 и иДПП-4 могут усугубить или увеличить риск развития ХСН.
Результаты нашего метаанализа, а также все исследования, включенные в него, подтвердили высокий риск развития ХСН у пациентов с СД 2 типа, получающих терапию инсулином в сравнении с препаратами сульфонилмочевины, пиоглитазоном, иДПП-4 [15].
Тем не менее в последние годы высказываются предположения о том, что риск развития ХСН у больных с СД 2 типа может отличаться от вида используемого инсулина.
Так, в шестилетнем РКИ ORIGIN (Outcome Reduction with an Initial Glargine Intervention) терапия инсулином гларгином по сравнению со стандартной терапией, рекомендуемой региональными алгоритмами, не оказала статистически значимого положительного или отрицательного влияния на риск госпитализаций, связанных с ХСН (RR 0,90; 95% ДИ: 0,77-1,05; P=0,16) [16]. Значительными ограничениями этого РКИ для подтверждения безопасности инсулина гларгина в плане риска развития ХСН стали следующие: среди 12537 больных, включенных в РКИ, 11,7% пациентов было рандомизировано без СД 2 типа с нарушением толерантности к глюкозе, у которых применение инсулина не рекомендуется; у 58,9% больных инсулин использовался как дополнительная терапия, а 47% из них уже принимали метформин, как известно, обладающий кардиопротективными эффектами; длительность СД 2 типа у больных в РКИ была кратковременной — 5,5±6,1 лет, что предопределяет менее тяжелое течение СД 2 типа; применение инсулина гларгина по сравнению со стандартной терапией увеличивало RR увеличения веса и развития тяжелых гипогликемий на 69% (p<0,001), что может быть причиной развития неблагоприятных эффектов.
В другом международном РКИ DEVOTE (Trial Comparing Cardiovascular Safety of Insulin Degludec versus Insulin Glargine in Patients with Type 2 Diabetes at High Risk of Cardiovascular Events) сравнивалась кардиоваскулярная эффективность и безопасность двух видов базального инсулина: инсулин гларгин U100 и инсулин деглюдек у 7637 больных СД 2 типа, среди которых у 85,2% больных были ССЗ или ХБП. Длительность СД 2 типа составила 16,4 года [17]. Инсулин деглюдек проявил сопоставимую с инсулином гларгином нейтральную кардиоваскулярную безопасность в плане влияния на первичную конечную точку (сердечно-сосудистая смерть, нефатальный ИМ, нефатальный инсульт), меньшую частоту тяжелых гипогликемий. В субанализе РКИ DEVOTE не было выявлено существенной разницы в RR связанных с ХСН госпитализаций между использованием инсулина гларгин и инсулина деглюдек (RR 0,88; 95% ДИ: 0,72-1,08, p=0,227). Риск госпитализаций, связанных с ХСН, значительно увеличивался после эпизода тяжелой гипогликемии (RR 2,2) и в течение недели после него (RR 11,1) [18].
Еще в одном метаанализе 3 РКИ была сделана попытка определить риск развития ХСН у больных СД 2 типа и предиабетом при использовании инсулинотерапии [19]. В метаанализ было включено 7649 больных, получающих инсулин, и 8322 пациента, получающих ПССП. Средняя продолжительность СД 2 типа была кратковременной, не более 6,2 лет. Авторы показали, что инсулинотерапия в сравнении с ПССП снижает RR развития ХСН на 13% (95% ДИ: 0,75-0,99), а в подгруппе больных с ССЗ не влияет на него (RR 0,69; 95% ДИ: 0,34-1,40). Значительным ограничением этого метаанализа явилась высокая неоднородность когорт больных во включенных РКИ. В РКИ DIGAMI-2 (Diabetes mellitus Insulin-Glucose Infusion in Acute Myocardial Infarction) были включены больные СД 2 типа в острый период ИМ, некоторые из которых были переведены на инсулинотерапию в период госпитализации. В РКИ UKPDS (UK Prospective Diabetes Study 33) были включены больные с вновь выявленным СД 2 типа без ССЗ. В РКИ ORIGIN, как было описано выше, каждый десятый больной был включен не с СД 2 типа, а с нарушением толерантности к глюкозе или гипергликемией натощак. Поэтому полученные в метаанализе РКИ данные имеют низкий доказательный уровень.
Разнородность больных с СД 2 типа, связанная с длительностью заболевания, наличием или отсутствием микрососудистых осложнений, атеросклеротических ССЗ, коморбидной патологии, такой как ХБП, исходной терапией до назначения инсулинотерапии, видом инсулина, контролем углеводного обмена, предопределяет трудности выполнения высокого качества метаанализов выполненных РКИ и наблюдательных исследований. Соответственно, имеющиеся данные проведенных исследований следует интерпретировать с осторожностью, поскольку даже в относительно согласованных когортах, вероятно, существует высокая степень систематической ошибки отбора при распределении пациентов. Представляется целесообразным проведение большого РКИ для определения влияния терапии современными инсулинами у пациентов с СД 2 типа высокого и очень высокого риска на частоту развития ХСН с использованием строгих критериев включения и исключения.
Ограничения исследования. Ограничениями нашего метаанализа явились следующие: для отбора максимально однородной группы больных с СД 2 типа согласно критериям включения мы не смогли включить в метаанализ РКИ и, соответственно, не оценивалось лечение современными инсулинами; в метаанализ включались больные СД 2 типа, как с ССЗ, так и без них, при этом известно, что RR ХСН в этих когортах значительно отличается; в метаанализ из-за отсутствия данных не вошли сравнительные исследования современных инсулинов с иНГЛТ-2 и аГПП-1 в плане риска развития ХСН.
Заключение
Результаты проведенного метаанализа 5 ретроспективных наблюдательных исследований с включением 179777 больных СД 2 типа со средней продолжительностью лечения 67,2 мес. показали, что инсулинотерапия (без включения инсулинов гларгин и деглюдек) в сравнении с ПССП (без включения иНГЛТ-2 и аГПП-1) статистически значимо увеличивала RR развития ХСН с использованием модели фиксированных эффектов в 2,6 раза, при использовании модели случайных эффектов — в 2,4 раза (p<0,001 для обоих).
Отношения и деятельность: все авторы заявляют об отсутствии потенциального конфликта интересов, требующего раскрытия в данной статье.
Список литературы
1. Huynh T, Harty BJ, Claggett B, et al. Comparison of Outcomes in Patients With Diabetes Mellitus Treated With Versus Without Insulin + Heart Failure With Preserved Left Ventricular Ejection Fraction (from the TOPCAT Study). Am J Cardiol. 2019;123(4):611-7. doi:10.1016/j.amjcard.2018.11.022.
2. Segar MW, Vaduganathan M, Patel KV, et al. Machine Learning to Predict the Risk of Incident Heart Failure Hospitalization Among Patients With Diabetes: The WATCH-DM Risk Score. Diabetes Care. 2019;42(12):2298-306. doi:10.2337/dc19-0587.
3. Lee YB, Bae YJ, Kim H, et al. Severe hypoglycemia and risk of hospitalization for heart failure in adults with diabetes treated with oral medications with or without insulin: A population-based study. Diabetes Res Clin Pract. 2022;192:110083. doi:10.1016/j.diabres.2022.110083.
4. Lo C, Toyama T, Wang Y, et al. Insulin and glucose-lowering agents for treating people with diabetes and chronic kidney disease. Cochrane Database Syst Rev. 2018;9(9): CD011798. doi:10.1002/14651858.CD011798.pub2.
5. Liu J, Hu X. Impact of insulin therapy on outcomes of diabetic patients with heart failure: A systematic review and meta-analysis. Diab Vasc Dis Res. 2022;19(3): 14791641221093175. doi:10.1177/14791641221093175.
6. Moher D, Liberati A, Tetzlaff J, et al. Preferred reporting items for systematic reviews and meta-analyses: The PRISMA statement. PLoS Med. 2009;6(7):e1000097. doi:10. 1371/journal.pmed.1000097.
7. Akobeng AK. Principles of evidence based medicine. Arch Dis Child. 2005;90(8):837-40. doi:10.1136/adc.2005.071761.
8. Nichols GA, Koro CE, Gullion CM, et al. The incidence of congestive heart failure associated with antidiabetic therapies. Diabetes Metab Res Rev. 2005;21(1):51-7. doi:10.1002/dmrr.480.
9. Rajagopalan R, Rosenson RS, Fernandes AW, et al. Association between congestive heart failure and hospitalization in patients with type 2 diabetes mellitus receiving treatment with insulin or pioglitazone: a retrospective data analysis. Clin Ther. 2004;26(9):1400-10. doi:10.1016/j.clinthera.2004.09.016.
10. Karter AJ, Ahmed AT, Liu J, et al. Pioglitazone initiation and subsequent hospitalization for congestive heart failure. Diabet Med. 2005;22(8):986-93. doi:10.1111/j.1464-5491.2005.01704.x.
11. Koro CE, Bowlin SJ, Weiss SR. Antidiabetic therapy and the risk of heart failure in type 2 diabetic patients: an independent effect or confounding by indication. Pharmacoepidemiol Drug Saf. 2005;14(10):697-703. doi:10.1002/pds.1069.
12. Ou HT, Chang KC, Li CY, Wu JS. Risks of cardiovascular diseases associated with dipeptidyl peptidase-4 inhibitors and other antidiabetic drugs in patients with type 2 diabetes: a nation-wide longitudinal study. Cardiovasc Diabetol. 2016;15:41. doi:10.1186/s12933-016-0350-4.
13. McDonagh TA, Metra M, Adamo M, et al. ESC Scientific Document Group. 2021 ESC Guidelines for the diagnosis and treatment of acute and chronic heart failure. Eur Heart J. 2021;42(36):3599-3726. doi:10.1093/eurheartj/ehab368.
14. Kenny HC, Abel ED. Heart Failure in Type 2 Diabetes Mellitus. Circ Res. 2019;124(1):121-41. doi:10.1161/CIRCRESAHA.118.311371.
15. Hippisley-Cox J, Coupland C. Diabetes treatments and risk of heart failure, cardiovascular disease, and all cause mortality: cohort study in primary care. BMJ. 2016;354:i3477. doi:10.1136/bmj.i3477.
16. ORIGIN Trial Investigators, Gerstein HC, Bosch J, Dagenais GR, et al. Basal insulin and cardiovascular and other outcomes in dysglycemia. N Engl J Med. 2012;367(4):319-28. doi:10.1056/NEJMoa1203858.
17. Marso SP, McGuire DK, Zinman B, et al. DEVOTE Study Group. Efficacy and Safety of Degludec versus Glargine in Type 2 Diabetes. N Engl J Med. 2017;377(8):723-32. doi:10.1056/NEJMoa1615692.
18. Pratley RE, Husain M, Lingvay I, et al. DEVOTE Study Group. Heart failure with insulin degludec versus glargine U100 in patients with type 2 diabetes at high risk of cardiovascular disease: DEVOTE 14. Cardiovasc Diabetol. 2019;18(1):156. doi:10.1186/s12933-019-0960-8.
19. Li J, Tong Y, Zhang Y, et al. Effects on All-cause Mortality and Cardiovascular Outcomes in Patients With Type 2 Diabetes by Comparing Insulin With Oral Hypoglycemic Agent Therapy: A Meta-analysis of Randomized Controlled Trials. Clin Ther. 2016;38(2):372-86. e6. doi:10.1016/j.clinthera.2015.12.006.
Об авторах
С. В. МироноваРоссия
Миронова Снежана Владимировна — кандидат медицинских наук, ассистент кафедры пропедевтики внутренних болезней № 2.
Пермь
Конфликт интересов:
Нет
Н. А. Козиолова
Россия
Козиолова Наталья Андреевна — доктор медицинских наук, профессор, заведующий кафедры пропедевтики внутренних болезней № 2.
Пермь
Конфликт интересов:
Нет
Е. В. Улыбина
Россия
Улыбина Елизавета Владимировна — ординатор кафедры пропедевтики внутренних болезней № 2.
Пермь
Конфликт интересов:
Нет
Дополнительные файлы
Рецензия
Для цитирования:
Миронова С.В., Козиолова Н.А., Улыбина Е.В. Риск развития хронической сердечной недостаточности у больных сахарным диабетом 2 типа, получающих терапию инсулином: метаанализ наблюдательных исследований. Российский кардиологический журнал. 2023;28(3):5375. https://doi.org/10.15829/1560-4071-2023-5375
For citation:
Mironova S.V., Koziolova N.A., Ulybina E.V. Risk of heart failure in patients with type 2 diabetes receiving insulin therapy: a meta-analysis of observational studies. Russian Journal of Cardiology. 2023;28(3):5375. (In Russ.) https://doi.org/10.15829/1560-4071-2023-5375
JATS XML

















































