Перейти к:
Выбор специфической и антикоагулянтной терапии у пациентов с впервые выявленной хронической тромбоэмболической легочной гипертензией в зависимости от статуса операбельности
https://doi.org/10.15829/1560-4071-2023-5231
Аннотация
Цель. Изучить особенности антикоагулянтной и специфической терапии у впервые выявленных пациентов с хронической тромбоэмболической легочной гипертензией (ХТЭЛГ) в зависимости от статуса операбельности.
Материал и методы. В исследование включено 319 пациентов с ХТЭЛГ, впервые госпитализированных в ФГБУ "НМИЦ Кардиологии им. акад. Е. И. Чазова" Минздрава России за период с 2012 по 2021гг. Диагноз установлен согласно действующим рекомендациям. В зависимости от статуса операбельности, который оценивался мультидисциплинарной командой, сформированы две группы — пациенты с неоперабельной ХТЭЛГ (n=222) и пациенты с операбельной ХТЭЛГ, которым была проведена операция легочной тромбэндартерэктомии (n=97), время с момента установления диагноза до проведения операции у них составило 13,3 [6,3; 27,1] мес. Анализировался демографический, функциональный статус, антикоагулянтная терапия и режимы специфической терапии.
Результаты. На момент первичного поступления в экспертный центр 80,56% больных получали антикоагулянтную терапию, чаще всего варфарином как у неоперабельных (38,74%), так и у операбельных пациентов с ХТЭЛГ (55,67%), соответственно, и ривароксабаном (25,68% и 20,62%, соответственно); 6,27% — принимали только дезагреганты, а 13,17% вовсе были без антикоагулянтной терапии. В стационаре неоперабельным пациентам чаще всего назначались низкомолекулярные гепарины в лечебных дозах (47,3%), варфарин — 38,7% пациентам и в меньшей степени (12,16%) прямые пероральные антикоагулянты (ПОАК). Операбельным пациентам чаще назначался варфарин (54,64%), 37,1% — низкомолекулярные гепарины и единичным пациентам назначались (8,25%) ПОАК.
Специфическую терапию на момент поступления получали 19,59% операбельных и 23,42% неоперабельных пациентов с ХТЭЛГ, преимущественно в режиме монотерапии силденафилом. После верификации диагноза большинство пациентов (64,4% неоперабельных и 46,4% операбельных пациентов с ХТЭЛГ) получали монотерапию силденафилом (72,82%) и риоцигуатом (46,75%). Добавление второго препарата, в основном в режиме стартовой комбинированной терапии, потребовалось у 5,15% операбельных пациентов и 10,81% — неоперабельных, а тройную специфическую терапию принимали 1,06% операбельных пациентов и 0,9% неоперабельных пациентов с ХТЭЛГ.
Заключение. Впервые в российской практике изучены особенности антикоагулянтной и специфической терапии у впервые выявленных пациентов с ХТЭЛГ в зависимости от статуса операбельности.
Ключевые слова
Для цитирования:
Валиева З.С., Мартынюк Т.В. Выбор специфической и антикоагулянтной терапии у пациентов с впервые выявленной хронической тромбоэмболической легочной гипертензией в зависимости от статуса операбельности. Российский кардиологический журнал. 2023;28(3):5231. https://doi.org/10.15829/1560-4071-2023-5231
For citation:
Valieva Z.S., Martynyuk T.V. Choice of specific and anticoagulant therapy in patients with newly diagnosed chronic thromboembolic pulmonary hypertension, depending on operability status. Russian Journal of Cardiology. 2023;28(3):5231. (In Russ.) https://doi.org/10.15829/1560-4071-2023-5231
Хроническая тромбоэмболическая легочная гипертензия (ХТЭЛГ) представляет собой заболевание легочных сосудов, обусловленное тромботическим поражением легочных артерий различной локализации. Легочная эндартерэктомия (ЛЭЭ) является предпочтительным методом лечения, т.к. значительно улучшает исход и прогноз у этих пациентов и способствует разрешению легочной гипертензии (ЛГ) у большинства из них [1-4]. Пациенты с ХТЭЛГ должны быть своевременно направлены в экспертный центр ХТЭЛГ для оценки операбельности. Однако не всем пациентам возможно проведение ЛЭЭ, они признаются неоперабельными из-за дистального поражения легочного сосудистого русла, сопутствующих заболеваний, отказа пациента от ЛЭЭ [5]. У 10-40% больных может быть резидуальная ЛГ после операции из-за развившейся васкулопатии [6][7]. У этих пациентов специфическая терапия, применяемая для лечения легочной артериальной гипертензии (ЛАГ), может улучшить клинические исходы [8][9]. Обоснованием для применения ЛАГ-специфической терапии при неоперабельной ХТЭЛГ является наличие при ХТЭЛГ дистальной артериопатии [10][11]. Эта дистальная артериопатия, которая выявляется в необтурированных сосудистых руслах, возможно, частично является результатом напряжения сдвига, вызванного усилением кровотока через эти сосуды. Возникающие в результате изменения мелких сосудов сходны с изменениями, наблюдаемыми при ЛАГ, и не подлежат хирургическому лечению. Кроме того, как у пациентов с ЛАГ, так и у пациентов с ХТЭЛГ снижен уровень оксида азота, что приводит к снижению регуляции, индуцированной потоком вазодилатации в легких [12]. Пациенты с ХТЭЛГ также имеют повышенный уровень эндотелина-1 по сравнению с контрольной группой, который коррелирует с тяжестью заболевания и худшими хирургическими результатами при ЛЭЭ [13][14].
Риоцигуат в настоящее время является единственным зарегистрированным лекарственным средством для лечения ХТЭЛГ в нашей стране и является препаратом первого выбора, препаратами второй и третьей линии являются ингаляционный илопрост, бозентан, мацитентан, силденафил [2][3]. Было высказано предположение, что медикаментозная терапия у пациентов с операбельной ХТЭЛГ может способствовать улучшению показателей гемодинамики перед операцией, что приводит к снижению риска осложнений и смертности. Использование медикаментозной терапии таким образом в качестве "моста к ЛЭЭ" не имеет доказательств, и есть опасения, что эта практика может отсрочить направление для радикального хирургического лечения без клинической пользы [15][16]. Проспективное рандомизированное плацебо-контролируемое исследование 2 фазы "PEA Bridging" (ClinicalTrials.gov: NCT03273257) было предназначено для оценки эффективности риоцигуата у операбельных пациентов с ХТЭЛГ, с легочным сосудистым сопротивлением (ЛСС) >800 дин×с×см-5 в предоперационном периоде по сравнению с плацебо. Это исследование должно было предоставить доказательства рисков и преимуществ промежуточной терапии, но оно было прекращено досрочно из-за медленного набора и ограничений, наложенных на проведение исследования пандемией новой коронавирусной инфекции. Однако легочные вазодилататоры во время операции широко распространены в клинической практике, и их эффективность в настоящее время изучается в продолжающихся рандомизированных клинических исследованиях с риоцигуатом. Так, в американском регистре почти 40% операбельных пациентов получали специфическую терапию до операции [17].
Базовая терапия ХТЭЛГ включает пожизненную антикоагулянтную терапию, при этом антагонисты витамина К являются основой. Прямые пероральные антикоагулянты (ПОАК) используются все чаще, но необходимы дополнительные доказательства их эффективности и безопасности.
Цель работы — изучение особенностей антикоагулянтной и специфической терапии для лечения ЛАГ у пациентов с ХТЭЛГ в зависимости от статуса операбельности после верификации диагноза в условиях экспертного центра.
Материал и методы
В исследование включено 319 пациентов с ХТЭЛГ, госпитализированных в ФГБУ "НМИЦ Кардиологии им. акад. Е. И. Чазова" Минздрава России за период с 2012 по 2021гг, где им подтверждался диагноз на основании комплексного обследования, включая трансторакальную эхокардиографию, сцинтиграфию легких, мультиспиральную компьютерную томографию-ангиопульмонографию, катетеризацию правых отделов сердца с селективной ангиопульмонографией. В зависимости от статуса операбельности, который оценивался мультидисциплинарной командой, сформированы две группы — пациенты с не- операбельной ХТЭЛГ (n=222) и пациенты с операбельной ХТЭЛГ, которым была проведена операция ЛЭЭ (n=97). Анализировался демографический, функциональный статус, антикоагулянтная терапия и режимы специфической терапии. Исследование проводили в соответствии с этическими положениями Хельсинкской декларации. Работа выполнена без задействования грантов и финансовой поддержки от общественных, некоммерческих и коммерческих организаций.
Статистический анализ проводили с помощью программы Statistica 8.0. Тип распределения оценивался с помощью критерия Колмогорова-Смирнова, при нормальном характере распределения данные представлены как M±m. Категориальные данные представлялись в виде n (%). При распределении непрерывных параметров, отличном от нормального, приводили медиану и интерквартильный размах (Me [Q25; Q75]). Для определения статистической значимости различий в двух независимых группах между непрерывными величинами использовали непараметрический критерий Манна-Уитни, между дискретными параметрами — точный критерий Фишера. Для всех проведенных тестов различия считали достоверными при двустороннем уровне значимости р<0,05.
Результаты
Большинство пациентов (77%) были признаны неоперабельными и только 23% операбельными, т.е. им проведена операция ЛЭЭ (рис. 1). Неоперабельные пациенты были старше, в то время как среди операбельных пациентов преобладали женщины (табл. 1). Пациенты не различались между собой по функциональному статусу, а также по времени с момента установления тромбоэмболии легочной артерии (ТЭЛА) до формирования ЛГ и времени с момента появления жалоб до установления диагноза ХТЭЛГ (табл. 1).
На момент поступления 42 пациента (13,17%) не получали антикоагулянтную терапию, а 20 пациентов (6,27%) принимали только дезагреганты (рис. 2). Среди оральных антикоагулянтов наиболее часто назначался варфарин как у неоперабельных, так и операбельных пациентов с ХТЭЛГ (38,74% и 55,67%, соответственно) и ривароксабан (25,68% и 20,62%, соответственно). После верификации диагноза всем была назначена антикоагулянтная терапия за исключением 4 пациентов, у которых была макрогематурия (0,31%), острый аппендицит (0,31%), острое нарушение мозгового кровообращения (0,31%), эрозивный гастрит в стадии обострения (0,31%). Неоперабельным пациентам чаще всего назначались низкомолекулярные гепарины (НМГ) в лечебных дозах (47,3%), у 38,7% варфарин и у 12,16% ПОАК (рис. 3). Что касается операбельных пациентов, то им чаще (54,6%) рекомендовали терапию варфарином, 37,1% НМГ и единичным пациентам назначались ПОАК (рис. 3).
До верификации диагноза специфическая терапия назначалась редко — 19,59% операбельным и 23,42% неоперабельным пациентам с ХТЭЛГ, преимущественно в режиме монотерапии силденафилом. После установления диагноза более половины (59%) больных находились на монотерапии, 9% на двойной специфической терапии и только 1% принимали тройную специфическую терапию. Без специфической терапии в основном были пациенты с операбельной ХТЭЛГ (46,4%) в связи с сохранным статусом, время ожидания операции составило 13,3 [6,3; 27,1] мес., неоперабельные пациенты не принимали специфическую терапию в 23,9% случаев (табл. 2). Режим монотерапии превалировал как у операбельных, так и у неоперабельных пациентов, причем чаще у последних (46,39% и 64,41%, соответственно). Добавление второго препарата было наиболее распространенной стратегией эскалации терапии, двойную специфическую терапию принимали 5,15% операбельных пациентов и 10,81% неоперабельных (рис. 4), а тройную специфическую терапию принимали 1,06% операбельных пациентов с ХТЭЛГ, тогда как среди неоперабельных пациентов с ХТЭЛГ тройную специфическую терапию получали 0,9% (рис. 5).
Как уже было сказано выше, режим монотерапии был преобладающим в обеих группах. Наиболее часто назначаемым препаратом для неоперабельных и операбельных пациентов с ХТЭЛГ был силденафил, 41,89% и 30,93%, соответственно. У большинства пациентов доза составила 20 мг 3 раза/сут. (табл. 3). Вторым по частоте назначения у неоперабельных и операбельных пациентов был риоцигуат, 26,13% и 20,62%, соответственно. Причем рекомендованную дозу 2,5 мг 3 раза/сут. принимали только 10,0% и 17,2%, соответственно. Илопрост принимали 14,86% неоперабельных пациентов с ХТЭЛГ, в основном в дозе 10 мкг 3 раза/сут., тогда как операбельным пациентам с ХТЭЛГ (9,28%) илопрост назначался в дозе 10 мкг 6 раз/сут.
Доля пациентов, принимающих бозентан, была невелика как в группе неоперабельных пациентов с ХТЭЛГ, так и операбельных, 2,25% и 2,06%, соответственно. Другие антагонисты рецепторов эндотелина (АРЭ), такие как мацитентан и амбризентан, вовсе не были представлены у операбельных пациентов с ХТЭЛГ, а у неоперабельных пациентов составили 2,7% и 0,9%, соответственно.
Двойную специфическую терапию принимали всего 29 (9,09%) пациентов. Большинство из них были пациенты с неоперабельной ХТЭЛГ (89,66%), которые находились преимущественно на комбинированной терапии илопроста с силденафилом (рис. 4). Тройную специфическую терапию принимали всего 4 пациента, 2 из которых операбельные пациенты с ХТЭЛГ на комбинации илопроста с бозентаном и силденафилом (рис. 5).
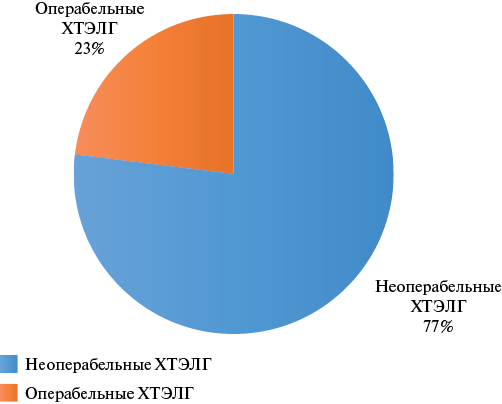
Рис. 1. Распределение пациентов с ХТЭЛГ.
Сокращение: ХТЭЛГ — хроническая тромбоэмболическая легочная гипертензия.
Таблица 1
Характеристика групп неоперабельных и операбельных пациентов с ХТЭЛГ
|
Показатели |
Неоперабельные ХТЭЛГ (n=222) |
Операбельные ХТЭЛГ (n=97) |
р |
|
Возраст, годы |
55,8±14,8 |
51,7±13,4 |
0,020440 |
|
Пол, м/ж, n (%) |
86 (38,74%)/136 (61,26%) |
60 (61,86%)/37 (38,14%) |
0,00014 |
|
ФК (NYHA), n (%) I II III IV |
6 (2,80%) 32 (14,95%) 125 (58,41%) 51 (23,83%) |
3 (3,09%) 18 (18,56%) 55 (56,70%) 21 (21,65%) |
0,86627 |
|
ДТ6МХ, м |
340,5±117,9 |
341,2±130,5 |
0,294690 |
|
Одышка по Боргу, баллы |
4,2±1,8 |
4,5±1,7 |
0,227811 |
|
SрO2 до/после теста, ٪ |
93,8±4,3/90,5±5,7 |
92,7±4,7/89,2±6,9 |
0,256814 |
|
Время с момента установления ТЭЛА до формирования ЛГ, мес., Med [ИКР 25%; 75%] |
2,1 [ 0; 16,2] |
2,9 [ 0; 21,5] |
0,371972 |
|
Время с момента появления жалоб до установления диагноза ХТЭЛГ, мес., Med [ИКР 25%; 75%] |
24,5 [ 7,8; 54,8] |
18,2 [ 5,9; 44,9] |
0,145697 |
Сокращения: ДТ6МХ — дистанция в тесте 6-минутной ходьбы, ИКР — интерквартильный размах, ЛГ — легочная гипертензия, ТЭЛА — тромбоэмболия легочной артерии, ФК — функциональный класс, ХТЭЛГ — хроническая тромбоэмболическая легочная гипертензия, Med — медиана, SрO2 — сатурация кислорода.

Рис. 2. Антикоагулянтная терапия при поступлении.
Сокращение: ХТЭЛГ — хроническая тромбоэмболическая легочная гипертензия.
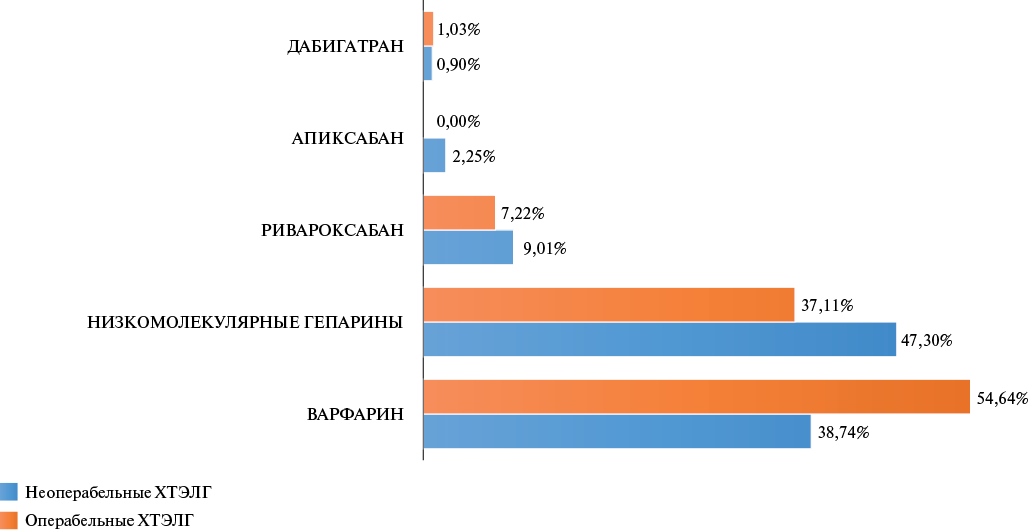
Рис. 3. Антикоагулянтная терапия после верификации диагноза ХТЭЛГ.
Сокращение: ХТЭЛГ — хроническая тромбоэмболическая легочная гипертензия.
Таблица 2
Режимы специфической терапии у операбельных и неоперабельных ХТЭЛГ до поступления
|
Неоперабельные ХТЭЛГ (n=222) |
Операбельные ХТЭЛГ (n=97) |
р |
|
|
Без специфической терапии |
53 (23,87%) |
45 (46,39%) |
0,001 |
|
Монотерапия |
143 (64,41%) |
45 (46,39%) |
0,002 |
|
Двойная специфическая терапия |
24 (10,81%) |
5 (5,15%) |
0,104 |
|
Тройная специфическая терапия |
2 (0,90%) |
2 (2,06%) |
0,484 |
Сокращение: ХТЭЛГ — хроническая тромбоэмболическая легочная гипертензия.
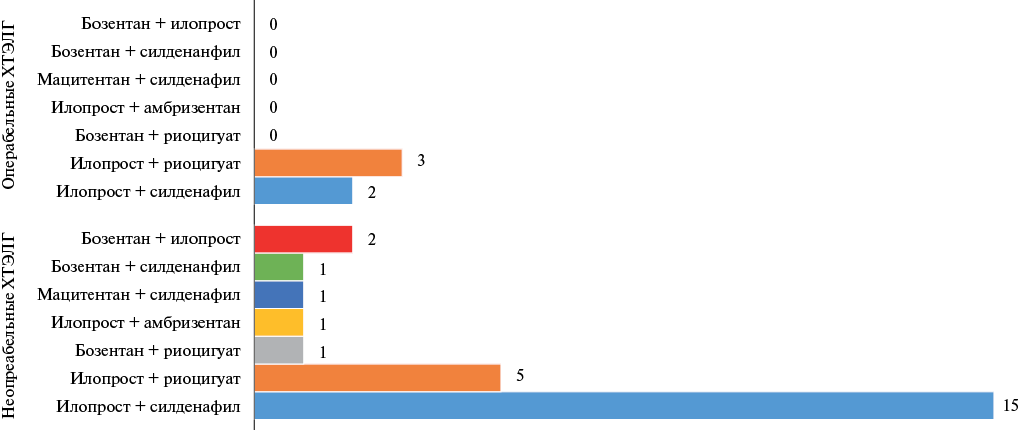
Рис. 4. Количество пациентов с ХТЭЛГ на двойной специфической терапии после верификации диагноза.
Сокращение: ХТЭЛГ — хроническая тромбоэмболическая легочная гипертензия.
Таблица 3
Монотерапия у операбельных и неоперабельных пациентов с дозировкой
|
Операбельные ХТЭЛГ (n=97) |
Неоперабельные ХТЭЛГ (n=222) |
р |
|
|
Мацитентан |
0 |
2,70% |
0,12365 |
|
Суточная доза |
|||
|
– |
10 мг × 1 раз/сут. (100%) |
||
|
Бозентан |
2,06% |
2,25% |
0,53484 |
|
Суточная доза |
|||
|
62,5 мг × 2 раза/сут. (50%) 125 мг × 2 раза/сут. (50%) |
62,5 мг × 2 раза/сут. (20%) 125 мг × 2 раза/сут. (80%) |
||
|
Амбризентан |
0 |
0,90% |
0,37719 |
|
Суточная доза |
|||
|
– |
5 мг × 1 раз/сут. (50%) 10 мг × 1 раз/сут. (50%) |
||
|
Риоцигуат |
20,62% |
26,13% |
0,46337 |
|
Суточная доза |
|||
|
2,5 мг × 3 раза/сут. (10%) 2 мг × 3 раза/сут. (5%) 1 мг × 3 раза/сут. (75%) 0,5 мг × 3 раза/сут. (10%) |
2,5 мг × 3 раза/сут. (17,2%) 2 мг × 3 раза/сут. (6,9%) 1,5 мг × 3 раза/сут. (1,7%) 1 мг × 3 раза/сут. (67,3%) 0,5 мг × 3 раза/сут. (6,9%) |
||
|
Силденафил |
30,93% |
41,89% |
0,06421 |
|
Суточная доза |
|||
|
20 мг × 3 раза/сут. (83,3%) 10 мг × 3 раза/сут. (10,1%) 25 мг × 3 раза/сут. (3,3%) 50 мг × 3 раза/сут. (3,3%) |
20 мг × 3 раза/сут. (78,5%) 20 мг × 6 раз/сут. (2,2%) 20 мг × 4 раза/сут. (1,1%) 10 мг × 3 раза/сут. (6,4%) 25 мг × 3 раза/сут. (4,3%) 50 мг × 3 раза/сут. (1,1%) 12,5 мг × 3 раза/сут. (3,2%) 16,5 мг × 3 раза/сут. (1,1%) 5 мг × 3 раза/сут. (2,1%) |
||
|
Илопрост |
9,28% |
14,86% |
0,19732 |
|
Суточная доза |
|||
|
10 мкг × 6 раз/сут. (77,7%) 10 мкг × 3 раза/сут. (11,1%) 10 мкг × 4 раза/сут. (11,1%) |
5 мкг × 6 раз/сут. (3,03%) 10 мкг × 3 раза/сут. (78,77%) 10 мкг × 4 раза/сут. (18,2%) |
||
Сокращение: ХТЭЛГ — хроническая тромбоэмболическая легочная гипертензия.
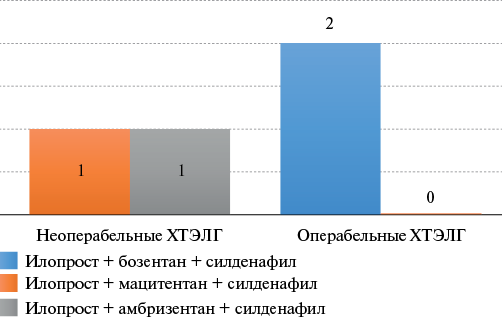
Рис. 5. Количество пациентов с ХТЭЛГ на тройной специфической терапии после верификации диагноза.
Примечание: цветное изображение доступно в электронной версии журнала.
Сокращение: ХТЭЛГ — хроническая тромбоэмболическая легочная гипертензия.
Обсуждение
Наличие дистальной васкулопатиии при ХТЭЛГ послужило основанием для использования препаратов, одобренных для лечения ЛАГ. Исторически сложилось так, что большинство пациентов с ХТЭЛГ получают монотерапию специфическими препаратами [18]. В Международном регистре CTEPH [5] 37,9% больных получали специфические препараты и среди них только 4% комбинированную терапию. В греческом регистре HOPE 60,2% больных принимали специфическую терапию [19].
В нашем исследовании также большинство пациентов (64,41% неоперабельных и 46,39% операбельных пациентов с ХТЭЛГ) получали монотерапию, в основном силденафилом и риоцигуатом, в отличие от работы van Thor MCJ, et al. (2020) [20], где 45% пациентов получали монотерапию, преимущественно АРЭ (58%) или ингибиторами фосфодиэстеразы 5 типа (иФДЭ-5) (34%). Возможно, это связано с тем, что большинство пациентов (75%) в этой работе были диагностированы до широкого внедрения риоцигуата в клиническую практику.
В нашей работе 26,13% неоперабельных и 20,62% операбельных пациентов принимали риоцигуат, однако целевые дозы риоцигуата 2,5 мг 3 раза/сут. принимали только 10,0% неоперабельных и 17,2% операбельных пациентов, соответственно. Преимущественно это было связано со сложностями лекарственного обеспечения у этой категории пациентов. И этим же объясняется большое распространение применения силденафила у пациентов с ХТЭЛГ (41,89% неоперабельные и 30,93% операбельные), т.к. у него меньшая стоимость в сравнении с другими ЛАГ-специфическими препаратами. Ранее было показано, что 54% пациентов с ХТЭЛГ принимали специфические препараты, при этом у 46% оказались перерывы в приеме препаратов 58,4±66,3 дня в основном из-за сложностей лекарственного обеспечения [21].
В работе Schweikert B, et al. (2014) проанализировано 119 пациентов с ХТЭЛГ, из которых 83,9% были признаны неоперабельными, а у 16,0% сохранялась резидуальная ЛГ после ЛЭЭ. У пациентов преобладала монотерапия, в основном бозентаном (57,6%), силденафилом (33,1%) или эпопростенолом (3,4%). Все другие препараты были зарегистрированы менее чем у 2% пациентов. О комбинированной терапии сообщалось только у 1 пациента (АРЭ в сочетании с иФДЭ-5). Ограничение данной работы состоит в том, что на момент его проведения официально зарегистрированного препарата для лечения ХТЭЛГ не было [22].
В американском регистре US-CTEPH-R [17] 44% пациентов на момент включения получали специфическую терапию. Неоперабельные пациенты (n=96) получали специфическую терапию чаще, чем операбельные (64,6% vs 39,4%; р<0,001). Наиболее часто назначали риоцигуат (65%), за ним следовали иФДЭ-5 (27%). Комбинированная терапия использовалась для лечения только 15,5% пациентов.
Концепция комбинированной терапии более устоялась при ЛАГ по сравнению с ХТЭЛГ. Для достижения статуса низкого риска и улучшения исходов рекомендуется использование комбинированной терапии при ЛАГ [1-4]. Исследования, непосредственно оценивающие эту концепцию при ХТЭЛГ, ограничены. Так, использование в исследовании MERIT-1 предшествующей специфической терапии наблюдалось у 61% пациентов, преимущественно иФДЭ-5 и АРЭ [23]. Когортные исследования с использованием комбинированной терапии показали снижение ЛСС при применении силденафила и ингаляционного простациклина [24][25]. В исследовании с подкожным трепростинилом 30% получали другие легочные вазодилататоры [26].
В нашей работе небольшой доле пациентов назначена комбинированная терапия — преимущественно это двойная терапия, у 10,81% неоперабельных пациентов и 5,15% операбельных, а тройную терапию получали единицы, 0,90% и 2,06%, соответственно. Получается, что как неоперабельные, так и операбельные пациенты с ХТЭЛГ нуждаются в приеме специфической терапии.
Хорошо известно, что пожизненная антикоагулянтная терапия является обязательной у пациентов с ХТЭЛГ. Однако остается дискутабельным вопрос о месте ПОАК в стратегии лечения пациентов с ХТЭЛГ. В регистре HOPЕ ПОАК были назначены 36,7% пациентов [19]. В немецком исследовании [27] сообщалось, что ПОАК все чаще используются у пациентов с ХТЭЛГ, несмотря на отсутствие доказательств их использования в этой конкретной популяции. В нашей работе преимущественно пациентам назначался варфарин и НМГ и в меньшей степени ПОАК. Настораживает тот факт, что при поступлении 19,44% были без антикоагулянтной терапии — 20 пациентов принимали только дезагреганты, а 42 пациента и вовсе были без антикоагулянтной терапии, что свидетельствует о достаточно плохой диагностике заболевания на догоспитальном этапе и большой погрешности в приеме антикоагулянтов.
В регистре ХТЭЛГ в США (US-CTEPH-R) (n=566) антикоагулянты не получали 2% пациентов, 1% были на аспирине. Варфарин (47%) был наиболее распространенным антикоагулянтом, за ним следовали ПОАК (40%), НМГ (9%), фондапаринукс (1%) и даже аспирин (1%); отсутствие о приеме антикоагулянтов сообщалось в 2% [17].
В новых европейских рекомендациях варфарин звучит только при антифосфолипидном синдроме и ХТЭЛГ, в то время как у ХТЭЛГ без антифосфолипидного синдрома допускается возможность назначения ПОАК, однако это требует дальнейших рандомизированных клинических исследований [4].
Ограничения исследования: исследование неконтролируемое, одноцентровое.
Заключение
Впервые в российской практике изучены особенности антикоагулянтной и специфической терапии у впервые выявленных пациентов с ХТЭЛГ в зависимости от статуса операбельности.
Отношения и деятельность: все авторы заявляют об отсутствии потенциального конфликта интересов, требующего раскрытия в данной статье.
Список литературы
1. Galie N, Humbert M, Vachiery JL, et al. 2015 ESC/ERS Guidelines for the diagnosis and treatment of pulmonary hypertension. The Joint Task Force for the Diagnosis and Treatment of Pulmonary Hypertension of the European Society of Cardiology (ESC) and the European Respiratory Society (ERS). Eur Respir J. 2015;46(4):903-75. doi:10.1183/13993003.01032-2015.
2. Чазова И. Е., Мартынюк Т. В., Валиева З. С. и др. Евразийские рекомендации по диагностике и лечению хронической тромбоэмболической легочной гипертензии (2020). Евразийский Кардиологический Журнал. 2021;(1):6-43. doi:10.38109/2225-1685-2021-1-6-43.
3. Авдеев С. Н., Барбараш О. Л., Баутин А. Е. и др. Легочная гипертензия, в том числе хроническая тромбоэмболическая легочная гипертензия. Клинические рекомендации 2020. Российский кардиологический журнал. 2021;26(12):4683. doi:10.15829/1560-4071-2021-4683.
4. Humbert M, Kovacs G, Hoeper MM, et al. ESC/ERS Scientific Document Group, 2022 ESC/ERS Guidelines for the diagnosis and treatment of pulmonary hypertension: Developed by the task force for the diagnosis and treatment of pulmonary hypertension of the European Society of Cardiology (ESC) and the European Respiratory Society (ERS). Endorsed by the International Society for Heart and Lung Transplantation (ISHLT) and the European Reference Network on rare respiratory diseases (ERN-LUNG). European Heart Journal. 2022;ehac237. doi:10.1183/13993003.00879-2022.
5. Pepke-Zaba J, Delcroix M, Lang I, et al. Chronic thromboembolic pulmonary hypertension (CTEPH): results from an international prospective registry. Circulation. 2011;124:1973-81. doi:10.1161/CIRCULATIONAHA.110.015008.
6. Mayer E, Jenkins D, Lindner J, et al. Surgical management and outcome of patients with chronic thromboembolic pulmonary hypertension: results from an international prospective registry. J Thorac Cardiovasc Surg. 2011;141:702-10. doi:10.1016/j.jtcvs.2010.11.024.
7. Freed DH, Thomson BM, Berman M, et al. Survival after pulmonary thromboendarterectomy: effect of residual pulmonary hypertension. J Thorac Cardiovasc Surg. 2011;141:383-7. doi:10.1016/j.jtcvs.2009.12.056.
8. Lang I, Meyer BC, Ogo T, et al. Balloon pulmonary angioplasty in chronic thromboembolic pulmonary hypertension. Eur Respir Rev. 2017;26(143):160119. doi:10.1183/16000617.0119-2016.
9. van Thor MCJ, Ten Klooster L, Snijder RJ, et al. Long-term clinical value and outcome of riociguat in chronic thromboembolic pulmonary hypertension. Int J Cardiol Heart Vasc. 2019:28;22:163-8. doi:10.1016/j.ijcha.2019.02.004.
10. Dorfmuller P, Günther S, Ghigna MR, et al. Microvascular disease in chronic thromboembolic pulmonary hypertension: a role for pulmonary veins and systemic vasculature. Eur Respir J. 2014:44(5):1275-88. doi:10.1183/09031936.00169113.
11. Humbert M, Guignabert C, Bonnet S, et al. Pathology and pathobiology of pulmonary hypertension: state of the art and research perspectives. Eur Respir J. 2019;53(1):1801887. doi:10.1183/13993003.01887-2018.
12. Stasch JP, Evgenov OV. Soluble guanylate cyclase stimulators in pulmonary hypertension. Handb Exp Pharmacol. 2013;218:279-313. doi:10.1007/978-3-642-38664-0_12.
13. Langer F, Bauer M, Tscholl D, et al. Circulating big endothelin-1: an active role in pulmonary thromboendarterectomy? J Thorac Cardiovasc Surg. 2005;130(5):1342-7. doi:10.1016/j.jtcvs.2005.06.044.
14. Reesink HJ, Meijer RC, Lutter R, et al. Hemodynamic and clinical correlates of endothelin-1 in chronic thromboembolic pulmonary hypertension. Circ J. 2006;70(8):1058-63. doi:10.1253/circj.70.1058.
15. Delcroix M, Lang I, Pepke-Zaba J, et al. Long-Term Outcome of Patients With Chronic Thromboembolic Pulmonary Hypertension: Results From an International Prospective Registry. Circulation. 2016;133(9):859-71. doi:10.1161/CIRCULATIONAHA.115.016522.
16. Jensen KW, Kerr KM, Fedullo PF, et al. Pulmonary hypertensive medical therapy in chronic thromboembolic pulmonary hypertension before pulmonary thromboendarterectomy. Circulation. 2009;120(13):1248-54. doi:10.1161/CIRCULATIONAHA.109.865881.
17. Kerr KM, Elliott CG, Chin K, et al. Results From the United States Chronic Thromboembolic Pulmonary Hypertension Registry: Enrollment Characteristics and 1-Year Follow-up. Chest. 2021;160(5):1822-31. doi:10.1016/j.chest.2021.05.052.
18. Gall H, Preston IR, Hinzmann B, et al. An international physician survey of chronic thromboembolic pulmonary hypertension management. Pulm Circ. 2016;6(4):472-82. doi:10.1086/688084.
19. Demerouti E, Karyofyllis P, Voudris V, et al. Epidemiology and Management of Chronic Thromboembolic Pulmonary Hypertension in Greece. Real-World Data from the Hellenic Pulmonary Hypertension Registry (HOPE). Journal of Clinical Medicine. 2021;10(19):4547. doi:10.3390/jcm10194547.
20. van Thor MCJ, Snijder RJ, Kelder JC, et al. Does combination therapy work in chronic thromboembolic pulmonary hypertension? Int J Cardiol Heart Vasc. 2020;29:100544. doi:10.1016/j.ijcha.2020.100544.
21. Чазова И. Е., Мартынюк Т. В., Валиева З. С. и др. Оценка бремени хронической тромбоэмболической легочной гипертензии в Российской Федерации. Терапевтический архив. 2018;90(9):101-9. doi:10.26442/terarkh2018909101-109.
22. Schweikert B, Pittrow D, Vizza CD, et al. Demographics, clinical characteristics, health resource utilization and cost of chronic thromboembolic pulmonary hypertension patients: retrospective results from six European countries. BMC Health Serv Res. 2014;14:246. doi:10.1186/1472-6963-14-246.
23. Ghofrani HA, Simonneau G, D’Armini AM, et al. Macitentan for the treatment of inoperable chronic thromboembolic pulmonary hypertension (MERIT-1): results from the multicentre, phase 2, randomised, double-blind, placebo-controlled study. Lancet Respir Med. 2017;5(10):785-94. doi:10.1016/S2213-2600(17)30305-3.
24. Ghofrani HA, Wiedemann R, Rose F, et al. Combination therapy with oral sildenafil and inhaled iloprost for severe pulmonary hypertension. Ann Intern Med. 2002;136(7):515-22. doi:10.7326/0003-4819-136-7-200204020-00008.
25. Voswinckel R, Reichenberger F, Enke B, et al. Acute effects of the combination of sildenafil and inhaled treprostinil on haemodynamics and gas exchange in pulmonary hypertension. Pulm Pharmacol Ther. 2008;21(5):824-32. doi:10.1016/j.pupt.2008.07003.
26. Sadushi-Kolici R, Jansa P, Kopec G, et al. Subcutaneous treprostinil for the treatment of severe non-operable chronic thromboembolic pulmonary hypertension (CTREPH): a double-blind, phase 3, randomised controlled trial. Lancet Respir Med. 2019;7(3):239-48. doi:10.1016/S2213-2600(18)30367-9.
27. Kramm T, Wilkens H, Fuge J, et al. Incidence and characteristics of chronic thromboembolic pulmonary hypertension in Germany. Clin. Res. Cardiol. 2018;107:548-53. doi:10.1007/s00392-018-1215-5.
Об авторах
З. С. ВалиеваРоссия
Валиева Зарина Солтановна — кандидат медицинских наук, старший научный сотрудник отдела легочной гипертензии и заболеваний сердца.
121552, Москва, ул. 3-я Черепковская, 15А
Конфликт интересов:
Нет
Т. В. Мартынюк
Россия
Мартынюк Тамила Витальевна — доктор медицинских наук, руководитель отдела легочной гипертензии и заболеваний сердца Института клинической кардиологии им. А.Л. Мясникова НМИЦ кардиологии им. ак. Е.И. Чазова МЗ РФ; профессор кафедры кардиологии факультета дополнительного профессионального образования РНИМУ им. Н.И. Пирогова МЗ РФ.
121552, Москва, ул. 3-я Черепковская, 15А; 117997, Москва, ул. Островитянова, 1
Конфликт интересов:
Нет
Дополнительные файлы
Рецензия
Для цитирования:
Валиева З.С., Мартынюк Т.В. Выбор специфической и антикоагулянтной терапии у пациентов с впервые выявленной хронической тромбоэмболической легочной гипертензией в зависимости от статуса операбельности. Российский кардиологический журнал. 2023;28(3):5231. https://doi.org/10.15829/1560-4071-2023-5231
For citation:
Valieva Z.S., Martynyuk T.V. Choice of specific and anticoagulant therapy in patients with newly diagnosed chronic thromboembolic pulmonary hypertension, depending on operability status. Russian Journal of Cardiology. 2023;28(3):5231. (In Russ.) https://doi.org/10.15829/1560-4071-2023-5231
JATS XML

















































