ОРИГИНАЛЬНЫЕ СТАТЬИ
Цель. Оценка частоты, выраженности острого повреждения почек (ОПП), его возможностей в реклассификации риска ранней смерти и связи с госпитальной летальностью у пациентов с тромбоэмболией легочной артерии (ТЭЛА) в российской популяции.
Материал и методы. С апреля 2018г по апрель 2019г в Российский многоцентровой регистр СИРЕНА последовательно включались пациенты при наличии признаков, позволяющих диагностировать ТЭЛА, а также умершие, у которых заболевание было выявлено на патологоанатомическом исследовании. ОПП диагностировалось согласно действующим клиническим рекомендациям KDIGO (2012г). За исходный принимали креатинин, рассчитанный по формуле MDRD и соответствующий скорости клубочковой фильтрации 75 мл/мин/1,73 м2 (базальный), с последующей оценкой относительно значения параметра при поступлении. Стратификация риска ранней смерти осуществлялась в соответствии с действующими клиническими Рекомендациями ESC (2019г).
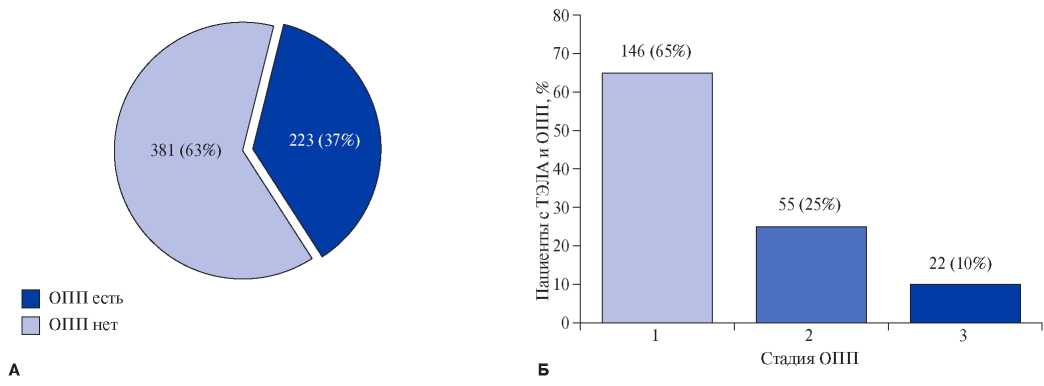
Результаты. Обследовано 604 пациента с ТЭЛА (мужчин — 293 (49%), женщин — 311 (51%); средний возраст — 64±15 лет). ОПП диагностировано у 223 (37%) из них. Первая стадия ОПП выявлена у 146 (65%), 2 — у 55 (25%), 3 — у 22 (10%) пациентов. Хроническая болезнь почек в анамнезе зафиксирована у 61 (10%) обследуемого. У 71 (12%) пациента выявлен высокий риск смерти, у 364 (61%) — промежуточный, у 164 (27%) — низкий. Частота ОПП росла по мере увеличения тяжести ТЭЛА: при низком риске смерти — 26%, промежуточном — 38%, высоком — 59% (p<0,0001). В стационаре умерло 107 (18%) больных. ОПП вело к увеличению летальности внутри групп риска: при низком риске это влияние носило характер тенденции (6 (5%) vs 6 (14%); p=0,052), а при промежуточном и высоком — было достоверным (30 (13%) vs 41 (30%); p<0,001 и 4 (14%) vs 19 (45%); p=0,006, соответственно). Многофакторный регрессионный анализ Кокса продемонстрировал, что ОПП является предиктором смерти в стационаре (отношение шансов (ОШ) 3,66 (95% доверительный интервал (ДИ): 2,37-5,66; р<0,0001), независимо от наличия повышенного уровня тропонина (ОШ 1,31; 95% ДИ: 0,80-2,14; р=0,28) и дисфункции правого желудочка (ОШ 1,23; 95% ДИ: 0,74-2,04; р=0,42).
Заключение. 37% пациентов с ТЭЛА российской популяции имеют ОПП, диагностированное по базальному креатинину. У 2/3 обследованных наблюдается 1 стадия ОПП. Частота ОПП растет по мере увеличения тяжести ТЭЛА. Наличие ОПП реклассифицирует пациентов в более высокую категорию риска смерти и связано со значительным увеличением госпитальной летальности.
ОБЗОРЫ ЛИТЕРАТУРЫ
Одним из методов хирургического лечения патологии аортального клапана является процедура Росса, которая была предложена британским кардиохирургом Д. Россом в 1967г. Многочисленные исследования показали отличные отдаленные результаты данной операции. Однако у некоторых пациентов в отдаленном периоде может произойти дилатация легочного аутографта. Чтобы избежать этого осложнения, были предложены технические модификации данной процедуры. Представлен обзор литературы модифицированных методик операции Росса в качестве профилактики дилатации легочного аутографта.
Болезни сердечно-сосудистой системы являются основными причинами смертности в современном мире. Хроническая сердечная недостаточность (ХСН) — терминальная стадия развития большинства сердечно-сосудистых заболеваний. Распространенность ХСН увеличивается у пациентов старших возрастных групп. В то же время с возрастом растет количество гериатрических синдромов, одним из которых является мальнутриця. Исследования последних лет демонстрируют взаимоотягащающее влияние сердечной недостаточности и мальнутриции, а также то, что коррекция мальнутриции может улучшать течение сердечной недостаточности. Внедрение скрининга и своевременная коррекция мальнутриции позволит снизить частоту госпитализаций и смертность у гериатрических пациентов с ХСН.
Эпикардиальная жировая ткань (ЭЖТ) обладает уникальными свойствами благодаря особой анатомической структуре, функции терморегуляции, метаболической активности. Дисрегуляция ЭЖТ провоцирует синтез провоспалительных цитокинов, нарушения в обмене жиров, глюкозы, способствует жировой дистрофии миокарда и развитию хронической сердечной недостаточности. ЭЖТ может служить фактором риска и биомаркером сердечнососудистых заболеваний, а также является потенциальной терапевтической мишенью. Целью данного обзора было освещение данных актуальных исследований по ЭЖТ, секретируемых адипокинов, их влияние на метаболизм тканей-мишеней и систематизация взаимосвязей между ЭЖТ и сердечнососудистыми заболеваниями. В частности, освещены вопросы её функции, роль при хронической сердечной недостаточности, фибрилляции предсердий, а также прогностическое значение различных микроРНК, определяемых в ЭЖТ.
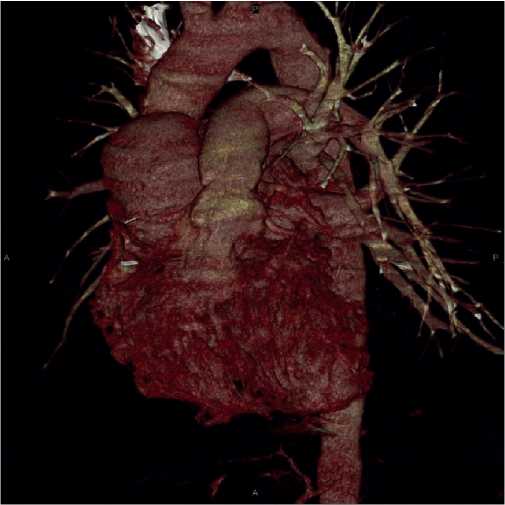
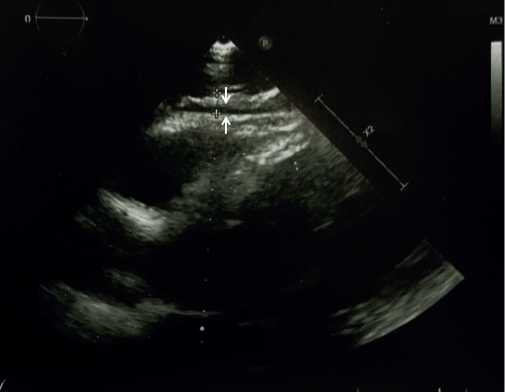
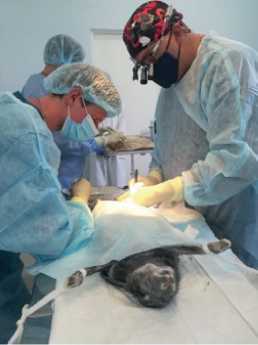
Тромбоэмболия легочной артерии (ТЭЛА) в структуре острых сердечно-сосудистых заболеваний занимает третье место. С каждым годом наблюдается стремительный рост заболеваемости и смертности от ТЭЛА. Лабораторные биомаркеры для диагностики ТЭЛА не обладают необходимой специфичностью, вследствие чего малоэффективны. ТЭЛА требует своевременного активного лечения, в частности — для профилактики серьезных осложнений. В связи с этим необходимы дальнейшие исследования по изучению и поиску новых перспективных биомаркеров для раннего выявления ТЭЛА, патофизиологических механизмов и мишеней для терапевтического воздействия. В значительной степени новую информацию о патофизиологии сердечно-сосудистых заболеваний, в т.ч. и ТЭЛА, ученые получают из экспериментальных исследований с использованием моделей на животных. В настоящем обзоре нами суммированы основные существующие экспериментальные модели ТЭЛА, описаны принципы и методы моделирования данного заболевания. Основными моделями ТЭЛА являются: внутривенная инфузия тромбина, аденозиндифосфат-индуцированная ТЭЛА, индукция ТЭЛА при помощи тромбопластина, человеческого рекомбинантного тканевого фактора или высокомолекулярных полифосфатов, моделирование ТЭЛА посредством коллаген-адреналиновой смеси, внутривенное введение готовых тромбов, приготовленных ex vivo, хирургическая модель. В данной публикации также представлен собственный опыт создания искусственной модели ТЭЛА на животных с использованием внутривенного введения тромба. В нашей модели получено подтверждение ТЭЛА при патологоанатомическом обследовании и повышение уровня биомаркеров: тропонина, N-концевого фрагмента промозгового натрийуретического пептида, D-димера. В данном пилотном исследовании была создана модель ТЭЛА для изучения патогенеза и новых возможностей лечения данного заболевания. Для подтверждения эффективности модели потребуется увеличение объёма эксперимента в будущих исследованиях.
ПРЕСС-РЕЛИЗ
PP-ELI-RUS-166222.01.2022
Служба Медицинской Информации: Medinfo.Russia@Pfizer.com
Доступ к информации о рецептурных препаратах Pfizer в России: www.pfizermedinfo.ru.
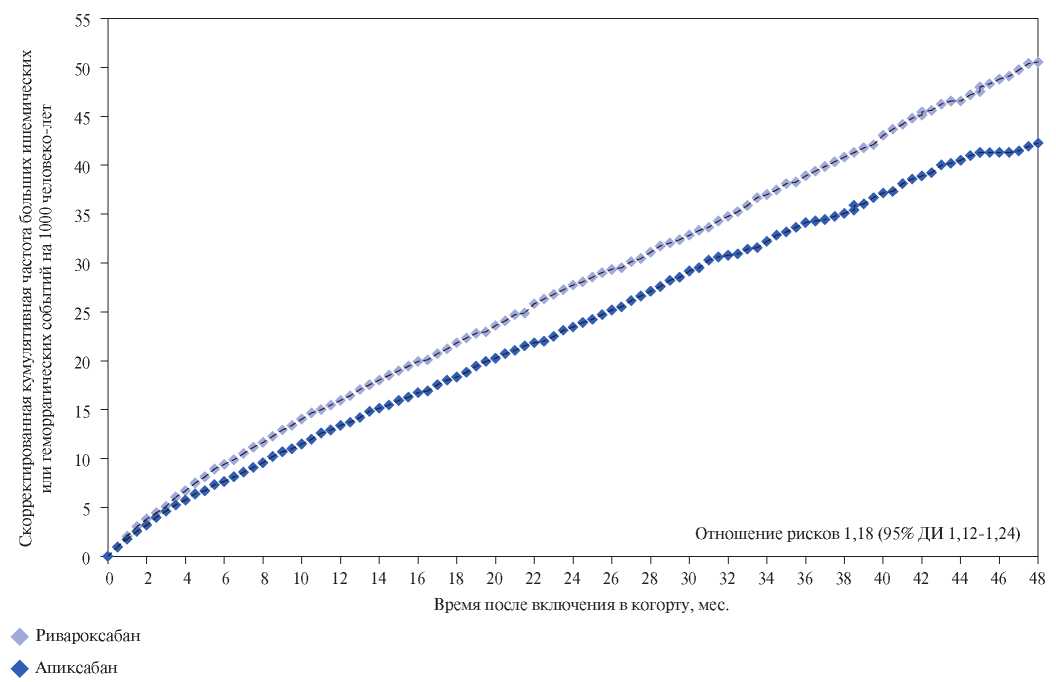
Copyright 2021 Пфайзер Россия. Все права защищены. Информация предназначена только для специалистов здравоохранения Российской Федерации. Исследование имеет ограничения, свойственные изучениям реальной практики. Результаты сравнения ПОАК приведены в качестве гипотезы, их необходимо интерпретировать с осторожностью. Прямых сравнительных РКИ между ПОАК не проводилось.
ISSN 2618-7620 (Online)