Перейти к:
Монотерапия тикагрелором как стратегия для снижения риска кровотечений у пациентов с острым коронарным синдромом, перенесших чрескожное коронарное вмешательство
https://doi.org/10.15829/1560-4071-2025-6482
EDN: YNPEON
Аннотация
Известно, что риск тромботических осложнений у пациентов с острым коронарным синдромом (ОКС) наиболее высок в первый год после события. Независимо от тактики лечения, в течение года после назначают двойную антиагрегантную терапию (ДААТ). ДААТ в значительной степени предотвращает тромботические осложнения, прежде всего повторный инфаркт миокарда. При этом закономерно повышается риск кровотечений. За последние годы получены убедительные данные, что переход от ДААТ на монотерапию тикагрелором через 1-3 мес. после события приводит к значительному снижению риска кровотечений без увеличения частоты тромботических осложнений по сравнению с ДААТ в течение 12 мес. В обзоре проанализированы данные рандомизированных клинических исследований по сравнению ДААТ и монотерапии тикагрелором у больных ОКС и представлены положения российских и международных клинических рекомендаций по лечению ОКА, касающиеся монотерапии тикагрелором.
Целью обзора является обоснование преимущества монотерапии тикагрелором по сравнению со стандартной ДААТ у пациентов с ОКС и чрескожным коронарным вмешательством с помощью детального анализа рандомизированных контролируемых исследований и метаанализов. В практической части приведены соответствующие разделы клинических рекомендаций.
Для цитирования:
Шалагинова Ю.О., Шахнович Р.М. Монотерапия тикагрелором как стратегия для снижения риска кровотечений у пациентов с острым коронарным синдромом, перенесших чрескожное коронарное вмешательство. Российский кардиологический журнал. 2025;30(9):6482. https://doi.org/10.15829/1560-4071-2025-6482. EDN: YNPEON
For citation:
Shalaginova Yu.O., Shakhnovich R.M. Ticagrelor monotherapy as a strategy to reduce the bleeding risk in patients with acute coronary syndrome who underwent percutaneous coronary intervention. Russian Journal of Cardiology. 2025;30(9):6482. (In Russ.) https://doi.org/10.15829/1560-4071-2025-6482. EDN: YNPEON
На сегодняшний день двойная антиагрегантная терапия (ДААТ) является обязательной после чрескожного коронарного вмешательства (ЧКВ) и после острого коронарного синдрома (ОКС) (независимо от стратегии лечения) для снижения рисков тромботических осложнений. Сроки проведения ДААТ зависят от соотношения тромботических и геморрагических рисков и опираются на данные проведенных рандомизированных клинических исследований (РКИ). Согласно текущим клиническим рекомендациям, стандартная продолжительность ДААТ у больных с ОКС составляет 1 год, при проведении планового ЧКВ у больных со стабильной ишемической болезнью сердца (ИБС) — 6 мес. [1-5]. При этом в зависимости от клинической ситуации продолжительность ДААТ может меняться как в сторону увеличения, так в сторону сокращения. Основная категория пациентов, которым назначается тикагрелор в составе ДААТ — это пациенты с ОКС. Однако и при ЧКВ в случае стабильной ИБС у пациентов с сахарным диабетом (СД) и высоким тромботическим риском или при "сложном" ЧКВ (стентирование 3 коронарных артерий, ≥3 установленных стента, бифуркационное стентирование, общая протяженность стентов >60 мм) тикагрелор в дозе 60 мг 2 раза/сут. в составе ДААТ показал преимущество в снижения частоты крупных неблагоприятных сердечно-сосудистых событий [6][7].
При наличии показаний к длительному приему антикоагулянтов ранняя отмена ацетилсалициловой кислоты (АСК) и переход на ДААТ у пациентов с ОКС после ЧКВ в течение недели рекомендованы в случае сопоставимого ишемического и геморрагического рисков (IА), и только у пациентов с высоким ишемическим риском тройная антитромботическая терапия может быть продолжена сроком до 1 мес. (IIa) [1-3][5]. Стратегия ранней отмены АСК становится все более привлекательной для снижения геморрагического риска.
Использование стентов нового поколения позволило снизить риск тромботических осложнений, вместе с тем он остается существенным. Развитие крупных кровотечений на длительной ДААТ независимо увеличивает риск смерти после ЧКВ. Таким образом, необходим поиск оптимальной длительности ДААТ. Основной клинической проблемой при проведении ДААТ является повышение риска кровотечений. При этом вероятность тромботических осложнений у пациентов с ОКС значительно превышает риск кровотечений, и в целом соотношение польза-риск для ДААТ говорит об эффективности и безопасности. В частности, по данным исследования PLATO, за год наблюдения у больных с ОКС общая смертность (в основном от ишемических причин) на терапии тикагрелором составила 4%, клопидогрелом — 5,1% (разница статистически достоверна), при этом частота фатальных кровотечений была на уровне 0,3%, независимо от варианта ДААТ [8]. Тем не менее продолжаются поиски оптимизации ДААТ. Вопрос о составе и продолжительности ДААТ остается открытым и является предметом дискуссии и поводом для проведения научных исследований. Можно выделить три основные возможности оптимизации ДААТ, направленные на уменьшение риска кровотечений:
- Сокращение продолжительности ДААТ. Проведен ряд исследований, в которых сравнивали стандартную ДААТ в течение 12 мес. и различные укороченные схемы — от 1 мес. до 6 мес. Результатом этих исследований явилось сокращение ДААТ до 6 мес. при проведении планового ЧКВ [9-15]. У больных с ОКС не удалось показать, что сокращение продолжительности ДААТ безопасно с точки зрении предотвращения ишемических событий. Так, по данным исследования SMART-DATE, показано, что сокращение ДААТ до 6 мес. приводило к достоверному повышению частоты повторных инфарктов миокарда (ИМ) [16]. Поэтому во всех текущих рекомендациях стандартная продолжительность ДААТ у больных с ОКС 12 мес. Если риск кровотечений существенно повышен, ДААТ может быть сокращена до 3-6 мес. И, напротив, при выраженном ишемическом риске, обусловленном повторным событиями, многососудистым поражением коронарных артерий, СД и т.д., показана пролонгированная ДААТ. Наиболее значимые доказательства преимущества длительной ДААТ получены для тикагрелора на основании исследования PEGASUS-TIMI 54 [17], что отражено в официальных рекомендациях.
- Ранний переход с более патентных ингибиторов рецепторов P2Y12 (иP2Y12) тикагрелора или прасугрела на клопидогрел в составе ДААТ. В медицинской литературе подобный переход часто называют словом "деэскалация". Исследования, которые проводились в этом направлении, были относительно небольшими, с открытым дизайном [18-21] и значительно уступали по количеству включенных больных исследованиям PLATO и TRITON-TIMI 38 [8][22], в которых показано значительное преимущество ДААТ в течение года с тикагрелором и прасугрелом по сравнению с клопидогрелом. В Российских и международных рекомендациях допускается деэскалация у больных с высоким риском кровотечения, но со "слабым" классом и уровнем доказательности — 2В согласно европейской кодировке [1][3]. Особо подчеркивается, что деэскалация ранее 1 мес. от начала ОКС нежелательна, т.к. в этот период риск повторных ишемических событий очень высокий.
- Наконец, третья возможность сделать антитромбоцитарную терапию более безопасной — ранняя отмена АСК и переход на монотерапию иP2Y12, прежде всего тикагрелором. Подобный подход представляется наиболее перспективным. В этом обзоре обсуждается ранний переход на монотерапию тикагрелором у пациентов с ОКС и после ЧКВ, у которых отсутствуют показания к приему антикоагулянтов.
Ниже представлены основные РКИ, в которых показано преимущество монотерапии тикагрелором (Приложение).
Исследования GLOBAL LEADERS
Первое крупное исследование в этом направлении, результаты которого опубликованы в 2018г, GLOBAL LEADERS — открытое рандомизированное исследование, проведенное в 130 центрах в 18 странах [23]. Исследуемая популяция состояла из пациентов, которым было запланировано ЧКВ при стабильной ИБС или ОКС. Этим пациентам была показана ДААТ и не было показаний для приема пероральных антикоагулянтов. Экспериментальная группа — ДААТ в течение 1 мес. с дальнейшим переходом на монотерапию тикагрелором в течение 23 мес. Группа сравнения — ДААТ (АСК + тикагрелор или клопидогрел) в течение 12 мес. В исследование включили 15968 пациентов, которым имплантировали стенты, выделяющие лекарство (биолимус). Дизайн исследования сразу вызывал вопросы, т.к. стандартная продолжительность ДААТ составляет 12 мес. и было бы логично сравнивать ДААТ с монотерапией тикагрелором в течение года, а не двух лет. Эта особенность GLOBAL LEADERS очевидно отразилась на результате. Первичная конечная точка (смерть от всех причин или нефатальный ИМ) наблюдалась у 3,8% группы монотерапии по сравнению с 4,4% контрольной группы (p=0,073). Исследование было направлено на то, чтобы показать преимущество монотерапии, а не доказать, что эта схема не уступает обычной ДААТ. Несмотря на то, что частота ишемических осложнений была ниже на монотерапии, различия не достигали статистической значимости. Вместе с тем дополнительный анализ показал, что в течение первого года наблюдения частота первичной конечной точки на монотерапии тикагрелором была на 21% меньше по сравнению с ДААТ — 1,95% и 2,47%, отличия достоверны (р=0,028). Различий в частоте кровотечений 3 или 5 типа по шкале BARC (Bleeding Academic Research Consortium) в целом выявлено не было. В то же время у больных ОКС на тикагрелоре была достоверно меньше частота кровотечений. А именно эти больные характеризуется особенно высоким риском кровотечений и вопросы безопасности антиагрегантной терапии у них очень актуальны. Таким образом, исходя из целей, поставленных в этом исследовании, не удалось показать преимущество двухлетней монотерапии тикагрелором по сравнению с ДААТ в течение года. Поэтому на тот период не было изменения клинической практики в отношении ДААТ. При этом дополнительные данные, описанные выше, явно говорили в пользу монотерапии, особенно у больных с ОКС. Исследование GLOBAL LEADERS вызвало большой интерес к этой проблеме и послужило триггером для других исследований, в которых учли его ограничения и ошибки.
Исследование TWILIGHT
Исследование TWILIGHT (Ticagrelor With Aspirin or Alone In High-Risk Patients After Coronary Intervention) — ключевое исследование в области назначение монотерапии тикагрелором [24]. Именно его результаты стали основанием для изменения клинических рекомендаций по лечению больных с ОКС. TWILIGHT — рандомизированное двойное слепое плацебо-контролируемое исследование, целью которого было оценить, можно ли после 3 мес. ДААТ безопасно прекратить АСК и продолжить монотерапию тикагрелором, снизив риск кровотечений без увеличения ишемических событий. Критерии включения: 1. возраст ≥18 лет; 2. больные с ИБС после проведения успешного ЧКВ с имплантацией одного или нескольких стентов с лекарственным покрытием (DES) по поводу острого или хронического коронарного синдрома; 3. наличие хотя бы одного клинического или ангиографического признака высокого риска. Клинические факторы высокого риска: СД, требующий медикаментозного лечения, женский пол, возраст ≥65 лет, почечная дисфункция (скорость клубочковой фильтрации <60 мл/мин/1,73 м²), ОКС — ИМ без подъема сегмента ST или нестабильная стенокардия, прием пероральных антикоагулянтов (до момента включения), анемия (Hb <11 г/дл) или тромбоцитопения (PLT <100×10⁹/л). Ангиографические факторы высокого риска: многососудистое поражение, стентирование длинного поражения (≥30 мм), бифуркационные поражения с имплантацией двух стентов, сложные поражения (например, хронические окклюзии, кальцифицированные стенозы), лечение ствола левой коронарной артерии. 4. успешная 3-мес. ДААТ с тикагрелором и АСК, без серьезных кровотечений, ишемических осложнений (инфаркта, инсульта, тромбоза стента). Таким образом, в исследование включались больные с высоким как ишемическим, так и геморрагическим риском. Сравнивали монотерапию тикагрелором после 3 мес. ДААТ (АСК + тикагрелор) и стандартную ДААТ (тикагрелор + АСК) в течение года. В исследование включили 7119 больных из 11 стран и 180 центров. Первичная конечная точка: клинически значимые кровотечения (BARC 2, 3 или 5); вторичная комбинированная конечная точка (ишемическая): смерть от всех причин + ИМ + инсульт. Было показано, что монотерапия тикагрелором через 3 мес. ДААТ по сравнению со стандартным режимом ДААТ приводила к снижению риска кровотечений на 44%, оцениваемых по шкале BARC 2, 3 или 5, (отношение рисков (ОР) 0,56; 95% доверительный интервал (ДИ): 0,45-0,68, р<0,001) без увеличения риска ишемических событий (ОР 0,99; 95% ДИ: 0,78-1,25), (рис. 1, 2).
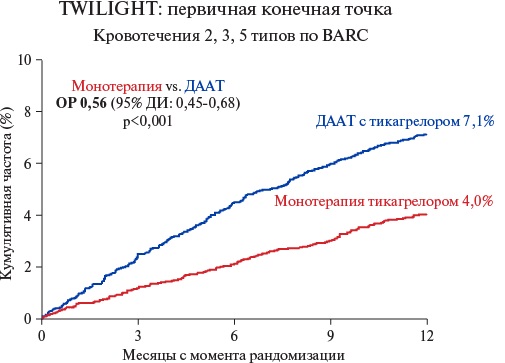
Рис. 1. Кривые Каплана-Мейера, показывающие частоту кровотечений BARC 2, 3 или 5 после рандомизации по данным исследования TWILIGHT ([11], Baber U, et al. Am Heart J. 2016;182:125-34).
Сокращения: ДААТ — двойная антиагрегантная терапия, ДИ — доверительный интервал, ОР — отношение рисков, BARC — Bleeding Academic Research Consortium.
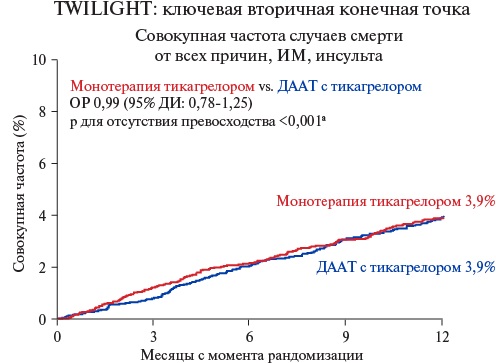
Рис. 2. Кривые Каплана-Мейера, показывающие частоту смерти от всех причин, ИМ или инсульта после рандомизации по данным исследования TWILIGHT ([11], Baber U, et al. Am Heart J. 2016;182:125-34).
Примечание: a — отсутствие превосходства тестировалось при одностороннем уровне альфа, равном 0,025, с использованием абсолютной верхней границы 95% ДИ, равной 1,6%.
Сокращения: ДААТ — двойная антиагрегантная терапия, ДИ — доверительный интервал, ИМ — инфаркт миокарда, ОР — отношение рисков.
В рамках исследования проведен ряд подисследований, которым посвящены отдельные публикации.
- Нас особенно интересует TWILIGHT ACS, где проанализированы больные с ОКС — нестабильной стенокардией и ИМ без подъема сегмента ST [25]. ЧКВ в этой группе было выполнено в течение 24 ч от поступления. Показано, что среди пациентов с ОКС (n=4614 — более половины среди всех включенных в TWILIGHT) монотерапия тикагрелором уменьшала риск кровотечений (BRC 2, 3 или 5) на 53% (3,6% и 7,6%; ОР 0,47, р<0,001). Показатели смерти от всех причин, ИМ или инсульта среди пациентов с ОКС составили 4,3% на тикагрелоре и 4,4% на ДААТ. Следовательно, у пациентов с ОКС монотерапия тикагрелором уменьшила клинически значимые кровотечения без увеличения риска ишемических осложнений по сравнению с ДААТ в течение 12 мес. Преимущества монотерапии тикагрелором в виде снижения частоты кровотечений были более выражены у пациентов с ИМбST по сравнению со стабильной ИБС.
- TWILIGHT-DM — больные с СД [26]. Пациенты с диабетом традиционно относятся к очень высокому ишемическому риску, но также подвержены высокому риску кровотечений, что делает выбор длительности ДААТ особенно актуальным. Всего пациентов с диабетом: 2620, из них 61% — с ОКС. Кровотечения (основная конечная точка): тикагрелор + плацебо: 4,5%; тикагрелор + АСК: 6,7%, — относительное снижение на 35% (p=0,01). Ишемические события (вторичная конечная точка): тикагрелор + плацебо: 4,6%; тикагрелор + АСК: 5,9% (p=0,10). Вывод: у пациентов с диабетом, перенесших ЧКВ и не имевших осложнений в первые 3 мес., отмена АСК и переход на монотерапию тикагрелором снижает риск кровотечений, не увеличивает частоту ишемических событий. Монотерапия тикагрелором может быть предпочтительным вариантом у этой сложной категории больных после 3 мес. ДААТ.
- TWILIGHT-COMPLEX — проспективно спланированный субанализ рандомизированного исследования TWILIGHT [27]. Цель: оценить, безопасна ли отмена АСК после 3 мес. ДААТ у пациентов с ангиографически сложным ЧКВ, получающих тикагрелор. Пациенты со сложной анатомией коронарных артерий после стентирования традиционно считаются в группе высокого ишемического риска, и им часто назначают продленную ДААТ. В TWILIGHT-COMPLEX проверили, можно ли у них отменить АСК без увеличения риска ишемических событий. Включили 2315 пациентов (59% с ОКС), у которых ЧКВ соответствовало критериям ангиографической сложности — ≥1 из следующих признаков: ≥3 имплантированных стентов, общая длина стентирования ≥60 мм, бифуркационное стентирование 2 стентами, ствол левой коронарной артерии, хроническая окклюзия, множественные поражённые сосуды (многососудистое ЧКВ), ≥3 поражённых артерий, выраженный кальциноз, извитость, резкие ангуляции. Результаты: кровотечения: тикагрелор + плацебо — 4,2%, тикагрелор + АСК — 7,7%, относительное снижение на 45% (p=0,001); ишемические события: тикагрелор + плацебо — 3,8%; тикагрелор + АСК — 4,9% (p=0,27). Основной вывод: у пациентов со сложным ангиографическим ЧКВ отмена АСК после 3 мес. ДААТ и переход на монотерапию тикагрелором существенно снижает риск кровотечений и не увеличивает риск ишемических событий. Эти данные ставят под сомнение необходимость продленной ДААТ у пациентов с "анатомически сложными" процедурами.
- TWILIGHT-HBR — субанализ исследования TWILIGHT [28], в котором отдельно выделили пациентов с высоким риском кровотечений, чтобы оценить эффект ранней отмены АСК и продолжения только тикагрелора. Из 7119 рандомизированных пациентов 1064 (17,2%) соответствовали критериям высокого риска кровотечений согласно ARC-HBR (Academic Research Consortium for High Bleeding Risk) — международного консенсуса, разработанного в 2019г для определения пациентов с высоким риском кровотечений после ЧКВ. Результаты: кровотечения — тикагрелор + плацебо — 6,3%, тикагрелор + АСК — 11,4%, относительное снижение на 47% (p=0,004). Ишемические исходы — без статистических различий между группами. Вывод: у пациентов с высоким риском кровотечений отказ от АСК после 3 мес. ДААТ и продолжение лечения тикагрелором значительно снижает частоту кровотечений, не увеличивая риск ишемических осложнений. При этом абсолютный прирост пользы у в этой группе ожидаемо выше, чем у остальных. Таким образом, TWILIGHT-HBR демонстрирует, что стратегия раннего прекращения АСК эффективна и безопасна у наиболее уязвимых пациентов.
Исследование TICO
TICO — рандомизированное многоцентровое открытое исследование, проведенное в Южной Корее [29]. В этом исследовании закрыли "брешь" в доказательной базе после TWILIGHT в отношении эффективности монотерапии тикагрелором, т.к. в TWILIGHT не было больных с ИМ с подъемом сегмента ST (ИМпST). В TICO включили 3056 пациентов с ОКС (36% из них с ИМпST) после ЧКВ с применением биорезорбируемых стентов нового поколения с сиролимусом. Сравнивали два режима антиагрегантной терапии: монотерапия тикагрелором после 3 мес. ДААТ и ДААТ (АСК 100 мг + тикагрелор) в течение года. Первичная комбинированная конечная точка была определена как совокупность крупных кровотечений (шкала TIMI) и неблагоприятных сердечных и цереброваскулярных событий через 1 год, и наблюдалась в 3,9% случаев в группе монотерапии тикагрелором и в 5,9% случаев в группе ДААТ, т.е. на 34% ниже (ОР 0,66; р=0,01). Относительный риск крупного кровотечения был на 44% ниже на тикагрелоре 0,56; р=0,02 (вторичная конечная точка). Достоверных различий в неблагоприятных кардиальных и цереброваскулярных событиях между группами выявлено не было (ОР 0,69; р=0,09), хотя наблюдалась явная тенденция в сторону преимущества монотерапии. Основное ограничение исследования — не включались больные с высоким риском кровотечения. Таким образом, в TICO полностью подтверждены результаты TWILIGHT.
В метаанализ Baber U, et al., 2024 включили только больных с ОКС из двух исследований TWILIGHT и TICO [30]. Вывод: ранняя отмена АСК с переходом на монотерапию тикагрелором приводит к 63% снижению риска опасных (BARC 3/5) кровотечений без повышения ишемических рисков. Эффект на кровотечения и ишемию сохранялся в когортах ИМпST, ИМпST и нестабильной стенокардии. Клиническое значение: метаанализ укрепляет доказательную базу для стратегии "3 мес. ДААТ → монотерапия тикагрелором", позволяя рекомендовать ее более уверенно у пациентов с ОКС после ЧКВ.
Исследование T-PASS
В южнокорейском открытом рандомизированном исследовании сравнивали более ранний переход у больных с ОКС на монотерапию тикагрелором — через 1 мес. после ДААТ (АСК + тикагрелор) и стандартную ДААТ (АКС + тикагрелор) в течение 12 мес. [31]. Всем больным имплантировали биоразлагаемый полимерный сиролимус-содержащий стент (BP-SES; Orsiro). Всего рандомизировано 2850 пациентов с ОКС (40% с ИМпST). Результаты опубликованы в 2024г. Первичная конечная точка состояла из смерти от всех причин, ИМ, тромбоза стента, инсульта и крупного кровотечения через год для анализа "намерение лечить". Первичная конечная точка произошла у 2,8% пациентов в группе, получавших монотерапию тикагрелором после <1 мес. ДААТ, и 5,2% пациентов в группе стандартной ДААТ — снижение на 46% (ОР 0,54; р<0,001 для гипотезы "не хуже"; р=0,002 для гипотезы "лучше"). Серьезные кровотечения происходили значительно реже в группе монотерапии тикагрелором по сравнению с контрольной группой (1,2% и 3,4% снижение на 65%; ОР 0,35, р<0,001). Основной вывод: прекращение приема АСК через месяц после ОКС с переходом на монотерапию тикагрелором не только не уступает, но даже превосходит стандартную ДААТ для однолетнего комбинированного риска значимых осложнений у пациентов с ОКС после ЧКВ. Результаты T-PASS согласуются с данными TWILIGHT/TICO о пользе сокращённой ДААТ и тикагрелор-монотерапии, но расширяют стратегию до <1 мес.
Исследование ULTIMATE-DAPT
Международное рандомизированное плацебо-контролируемое двойное слепое исследование [32]. Центры: 58 центров в Китае (подавляющее большинство), Италии, Пакистане и Великобритании. Включали пациентов с ОКС (n=3400), которым имплантировали современный стент, выделяющий лекарство, при условии отсутствия крупных ишемических и геморрагических событий в течение 1 мес. ДААТ (тикагрелор 90 мг 2 раза/сут. + АСК 100 мг). Далее пациенты были рандомизированы в группу монотерапии тикагрелором 90 мг 2 раза/сут. и группу ДААТ (тикагрелор + АСК 100 мг) длительностью 11 мес. Первичная конечная точка для гипотезы "лучше" (кровотечения 2, 3 или 5 типов по шкале BARC) наблюдалась у 2,1% пациентов, получавших тикагрелор и плацебо, и в 4,6% в группе пациентов, получавших тикагрелор и АСК (снижение на 55%, ОР 0,45; p<0,001). Частота кровотечений снижалась во всех 12 предопределенных подгруппах (возраст, пол, диабет и т.д.) без значимых взаимодействий. Частота достижения другой первичной конечной точки (смерть от сердечно-сосудистых причин, ИМ, ишемический инсульт, тромбоз стента и повторная реваскуляризация) для гипотезы "не хуже" не различалась между группами (3,6% и 3,7%; ОР, 0,98; p "не хуже" <0,0001; p "лучше" =0,89). Кроме того, не было никакой разницы в смертности от всех причин (0,7% и 0,8%; p=0,84), ИМ (0,9% и 0,7%; p=0,29), повторной реваскуляризации (2,4% и 2,4%; p=0,95) или тромбозе стента (0,3% и 0,3%; p=0,96). Данные исследования ULTIMATE-DAPT также как T-PASS показали, что после 1 мес. ДААТ (АСК + тикагрелор) монотерапия тикагрелором снижала риск кровотечения, не увеличивая при этом риск ишемических событий. Серьезный преимуществом ULTIMATE-DAPT двойной слепой дизайн.
Проведен ряд метаанализов, в которых объединили данные пяти вышеперечисленных исследований. Результаты одного из них опубликованы в журнале Lancet в 2024г [33]. Протокол зарегистрирован как PROSPERO, охватывает РКИ с переходом на монотерапию тикагрелором после краткого курса ДААТ (2 нед. — 3 мес.) по сравнению с обычной продолжительностью ДААТ 12 мес. В анализ включены >24 тыс. пациентов. Средний срок перехода: 78 дней с момента ЧКВ; медианная продолжительность терапии — 334 дня. Смерть/ИМ/инсульт — 2,8% на тикагрелоре и 3,2% при ДААТ (доказана концепция "не хуже"). Крупные кровотечения по BARC 3-5: 0,9% и 2,1% (доказана концепция "лучше"). Показано достоверное снижение общей смертности на 24%: 0,9% и 1,2% (p=0,034), особенно у женщин. Преимущество в снижении риска кровотечений особенно выражено у пациентов с ОКС (p interaction =0,022). Следовательно, монотерапия тикагрелором по сравнению с ДААТ является более безопасной и не приводит к увеличению тромботических осложнений. Аналогичные результаты получены в других метаанализах [34-40].
Все понимают, что отмена ДААТ через месяц — не предел. Уже началось изучение возможности вообще не проводить ДААТ, и сразу после ЧКВ назначать монотерапию иP2Y12. В Нидерландах в 2023г проведено пилотное одноцентровое исследование OPTICA [41], в котором впервые изучалась монотерапия тикагрелором или прасугрелом сразу после ЧКВ, без предварительного периода ДААТ, у больных с ОКС и ЧКВ под контролем оптической когерентной томографии для верификации качества стентирования. Пациенты получили нагрузочную дозу тикагрелора (180 мг) или прасугрела (60 мг) за ≥2 ч до ЧКВ. АСК после ЧКВ не назначалась. Далее монотерапия тикагрелором 90 мг × 2 или прасугрелом 10 мг/сут. в течение 12 мес. За период наблюдения не было случаев тромбоза стента или спонтанного ИМ; низкий уровень серьёзных кровотечений. Группы сравнения не было. В другом пилотном исследовании MACT [42], проведенном в Южной Корее, также изучали возможность назначения у больных ОКС монотерапии тикагрелором или прасугрелом сразу после ЧКВ. Дополнительно назначали колхицин в дозе 0,5 мг. Включили 200 пациентов. Всем проводили лабораторное изучение функции тромбоцитов. В течение 3 мес. наблюдения зафиксирован очень низкий риск тромбоза стента (1%) и крупных кровотечений (0,5%), практически полное подавление P2Y12-индуцированной агрегации тромбоцитов. В этом исследовании тоже не было контрольной группы.
Важно понимать, что положительные результаты исследований по монотерапии тикагрелором сложно распространять на другие иP2Y12 — клопидогрел и прасугрел, потому что эти препараты не продемонстрировали безопасность такого подхода с точки зрения ишемических событий. Так, в японском исследовании STOPDAPT2 ACS (n=4169) сравнивали монотерапию клопидогрелом после короткой ДААТ 1-2 мес. и стандартную ДААТ (АСК + клопидогрел) в течение 12 мес. [43]. В исследование включались пациенты с ОКС после ЧКВ с имплантацией стентов, выделяющих эверолимус. Первичная конечная точка (совокупность крупных сердечно-сосудистых осложнений и кровотечений) наблюдалось у 3,2% в группе 1-2 мес. терапии ДААТ и 2,8% в группе 12 мес. терапии ДААТ (р=0,06), т.е. не меньшая эффективность не доказана. В группе сокращенной ДААТ частота кровотечений была меньше. Монотерапия клопидогрелом после короткого курса ДААТ (1-2 мес.) была связана с уменьшением числа кровотечений, однако ассоциировалась с увеличением числа сердечно-сосудистых событий в течение года. В другом недавно опубликованном мультицентровом открытом рандомизированном исследовании STOPDAPT-3 (Short and Optimal Duration of Dual Antiplatelet Therapy After Everolimus-Eluting Cobalt-Chromium Stent-3) включали больных с ОКС и стабильной ИБС (n=5 966), которым провели ЧКВ с использованием выделяющих лекарство стентов Xience [44]. Рандомизация проводилась через месяц после ЧКВ на прием прасугрела в дозе 3,75 мг и ДААТ — прасугрел + АСК; наблюдение в течение года. Исследование проводилось в Японии, чем объясняется назначение редуцированной дозы прасугрела, которая там используется. Не было показано преимущества монотерапии по снижению риска значимых кровотечений. При этом на монотерапии была выше частота незапланированной реваскуляризации: 1,05% и 0,57%; подострого тромбоза стента: 0,58% и 0,17%; определенного/вероятного тромбоза стента: 0,71% и 0,44%. Риск ишемических исходов при отмене АСК был выше у пациентов с ОКС по сравнению со стабильной ИБС. Мы видим, что у больных ОКС монотерапия клопидогрелом и прасугрелом сопряжена с повышением риска ишемических осложнений. Клопидогрел является пролекарством, активируется в печени с участием фермента Р450 (CYP). Генетический полиморфизм этой системы, который обнаруживается примерно у 30% населения, обусловливает пониженную трансформацию клопидогрела в активный метаболит, и как следствие недостаточное подавление агрегации тромбоцитов. Этот факт делает назначение клопидогрела в качестве единственного антитромботического средства у больных с ОКС менее надежным по сравнению с тикагрелором, являющимся активным препаратом и не требующим трансформации в печени. Резистентность к тикагрелору обнаруживается очень редко. С точки зрения частоты резистентности тикагрелор является оптимальным препаратом в качестве монотерапии. Этого недостатка клопидогрела лишен прасугрел, который хоть и является пролекарством, резистентность к нему наблюдается не часто. Но результаты исследования STOPDAPT-3 не позволяют на сегодняшний день рекомендовать прасугрел в качестве монотерапии. Возникает законный вопрос, с чем связан тот факт, что отмена АСК и продолжение монотерапии тикагрелором не приводит к повышению риска тромбозов. Это в какой-то степени объясняется экспериментальными данными о том, что АСК незначительно усиливает ингибирование агрегации тромбоцитов (за счет ингибирования тромбоксан А2-зависимых путей агрегации тромбоцитов) при блокаде рецепторов P2Y12 [45]. То есть более мощное подавление агрегации иP2Y12 практически перекрывает эффект АСК.
В настоящее время продолжаются исследования, направленные на изучение монотерапии тикагрелором после ЧКВ у пациентов с ОКС. В корейском исследовании BULK-STEMI (n=1002) сравнивается монотерапия тикагрелором после 3 мес. стандартной ДААТ со стандартным режимом ДААТ у пациентов с ОКСпST после ЧКВ с использованием стентов, выделяющих сиролимус [46]. В этом исследовании первичные конечные точки заявлены как совокупность ишемических и геморрагических событий (BARC). В другом РКИ TARGET-FIRST (n=2246) у пациентов с ОКС после полной реваскуляризации с использованием биорезорбируемых стентов ДААТ сокращают до 1 мес. [47]. В качестве иP2Y12 назначают клопидогрел, тикагрелор или прасугрел (NCT04753749). В отличающемся по дизайну исследовании MATE после 1 мес. ДААТ пациентов с ОКС (n=2856), которым было выполнено ЧКВ, планируется рандомизировать в группу стандартной ДААТ до 12 мес. и в группу монотерапии тикагрелором еще на 5 мес. с дальнейшей деэскалацией до монотерапии клопидогрелом в течение последних 6 мес. (NCT0493769) [46]. А в исследовании NEOMINDSET у пациентов с ОКС после ЧКВ (n=3400) рандомизация проводится уже на четвертые сутки в группу стандартной ДААТ и группу монотерапии тикагрелором или прасугрелом (NCT04360720) [48]. Выбор между тикагрелором и прасугрелом производится на усмотрения исследователя. В открытом рандомизированном исследовании LEGACY 3090 пациентов с ОКС без подъема сегмента ST планируется рандомизировать сразу после успешного ЧКВ в группу монотерапии иP2Y12 и группу стандартной ДААТ длительностью 12 мес. (NCT05125276) [49].
Монотерапия тикагрелором в клинических рекомендациях по лечению ОКС
- Европейские рекомендации по лечению ОКС 2023г [3].
Монотерапия иP2Y12 описана в разделе "Укорочение ДААТ". Предлагается рассмотреть монотерапию (предпочтительно иP2Y12) у пациентов без ишемических событий в течение 3-6 мес. ДААТ с классом IIaA и через 1 мес. ДААТ у пациентов высокого геморрагического риска с классом IIbB. Более низкий класс рекомендаций для перехода через месяц связан с тем, что ко времени написания рекомендаций еще не были опубликованы результаты исследований T-PASS и ULTIMATE-DAPT. Представляется необоснованной позиция, что, согласно формулировке тезиса рекомендаций, в качестве монотерапии можно назначать любой иP2Y12, и даже АСК. При этом в тексте в качестве доказательной базы для сокращения ДААТ приводят исследования TWILIGHT и TICO. Другое спорное положение — рекомендовать монотерапию главным образом больным с высоким риском кровотечений. При этом в TWILIGHT включали больных как с высоким риском кровотечений, так и с высоким риском тромботических осложнений, а в TICO вообще не включали больных с высоким риском кровотечений.
- Российские обновленные рекомендации по лечению больных с ИМпST и ОКС без подъема сегмента ST от 2024г [1].
В целом позиции российских рекомендаций соответствуют европейским рекомендациям, но есть очень важные отличия и уточнения. Во-первых, подчеркивается предпочтительность монотерапии тикагрелором, и не любым иP2Y12. Во-вторых, монотерапия позиционируется прежде всего для пациентов, у которых отсутствует очень высокий риск ишемических осложнений, а не высокий геморрагический риск. То есть признается факт, что монотерапия тикагрелором снижает риск кровотечений независимо от исходного геморрагического риска.
- Американские рекомендации по лечению пациентов с ОКС от 2025г [5].
В этих рекомендациях, с точки зрения авторов обзора, наиболее точно и адекватно представлена возможность перехода на монотерапию тикагрелором. Прежде всего предлагается перейти не на любой иP2Y12, а именно на тикагрелор. И главное, такой переход можно считать универсальным, т.е. полезным всем больным с ОКС, независимо от исходного ишемического и геморрагического риска. Переходу на монотерапию тикагрелором через 1 мес. после ЧКВ у пациентов с ОКС для снижения риска кровотечения присвоен высший класс рекомендаций — 1А. Авторы приняли во внимание результаты всех исследований, включая T-PASS и ULTIMATE-DAPT, а также метаанализов (табл. 1).
Таблица 1
Рекомендации по режимам сокращения антиагрегантной терапии у пациентов с ОКС после ЧКВ без показаний для длительного приема антикоагулянтной терапии
|
Рекомендации |
Год |
Показания |
Класс и УД |
|
Европейские рекомендации по лечению пациентов о ОКС |
2023 |
Рассмотреть монотерапию (предпочтительно иP2Y12) у пациентов без ишемических событий в течение 3-6 мес. ДААТ и невысокого ишемического риска Монотерапия АСК или иP2Y12 может быть рассмотрена после 1 мес. ДААТ у пациентов высокого геморрагического риска |
IIaA IIbB |
|
Российские рекомендации по лечению пациентов с острым инфарктом миокарда с подъемом сегмента ST/Российские рекомендации по лечению пациентов с ОКС без подъема ST |
2024 |
У пациентов с ИМпST после ЧКВ без высокого ишемического риска в случае отсутствия ишемических событий на ДААТ рекомендовано ограничить ДААТ до 3-6 мес. с дальнейшим переходом на монотерапию иP2Y12 для снижения риска кровотечений (предпочтительна монотерапия тикагрелором) У пациентов с ИМпST и высоким риском кровотечений рекомендован переход на монотерапию иP2Y12 или АСК через 1 ДААТ (предпочтительна терапия тикагрелором) |
IIaA IIbB |
|
Американские рекомендации по лечению пациентов с ОКС |
2025 |
У пациентов с ОКС при отсутствии ишемических событий в течение 1 мес. ДААТ (АКС + тикагрелор) переход на монотерапию тикагрелором после ЧКВ полезен для снижения риска кровотечения У пациентов с ОКС после ЧКВ с высоким риском кровотечений переход на монотерапию (АСК или иP2Y12) после 1 мес. ДААТ может быть разумным для снижения риска кровотечений |
IA 2b B-R |
Сокращения: АСК — ацетилсалициловая кислота, ДААТ — двойная антиагрегантная терапия, иP2Y12 — ингибиторы (блокаторы) рецепторов P2Y12, ИМпST — инфаркт миокарда с подъемом сегмента ST, ОКС — острый коронарный синдром, УД — уровень доказательности, ЧКВ — чрескожное коронарное вмешательство.
Заключение
Переход на монотерапию тикагрелором (без АСК) в дозе 90 мг 2 в раза/сут. через 1-3 мес. ДААТ у всех пациентов с ОКС, которым проводилось ЧКВ, и продолжение этой терапии в течение 9-11 мес. (так, чтобы общая продолжительной ДААТ + тикагрелор составила один год) представляется целесообразным для снижения рисков кровотечений. Такой подход не приводит к увеличению риска ишемических событий. Единственное условие для реализации этой схемы — отсутствие ишемических осложнений и значимых кровотечений в период проведения ДААТ. Этот подход поддерживается как в российских, так и в международных рекомендациях. На сегодняшний день среди всех зарегистрированных лекарственных средств в Российской Федерации, возможность назначения тикагрелора в качестве монотерапии в утвержденной инструкции к препарату предусмотрена только для оригинального тикагрелора — Брилинты. Все исследования по монотерапии тикагрелором, которые обсуждались в настоящем обзоре, проводились с оригинальным препаратом.
Отношения и деятельность: все авторы заявляют об отсутствии потенциального конфликта интересов, требующего раскрытия в данной статье.
Приложение
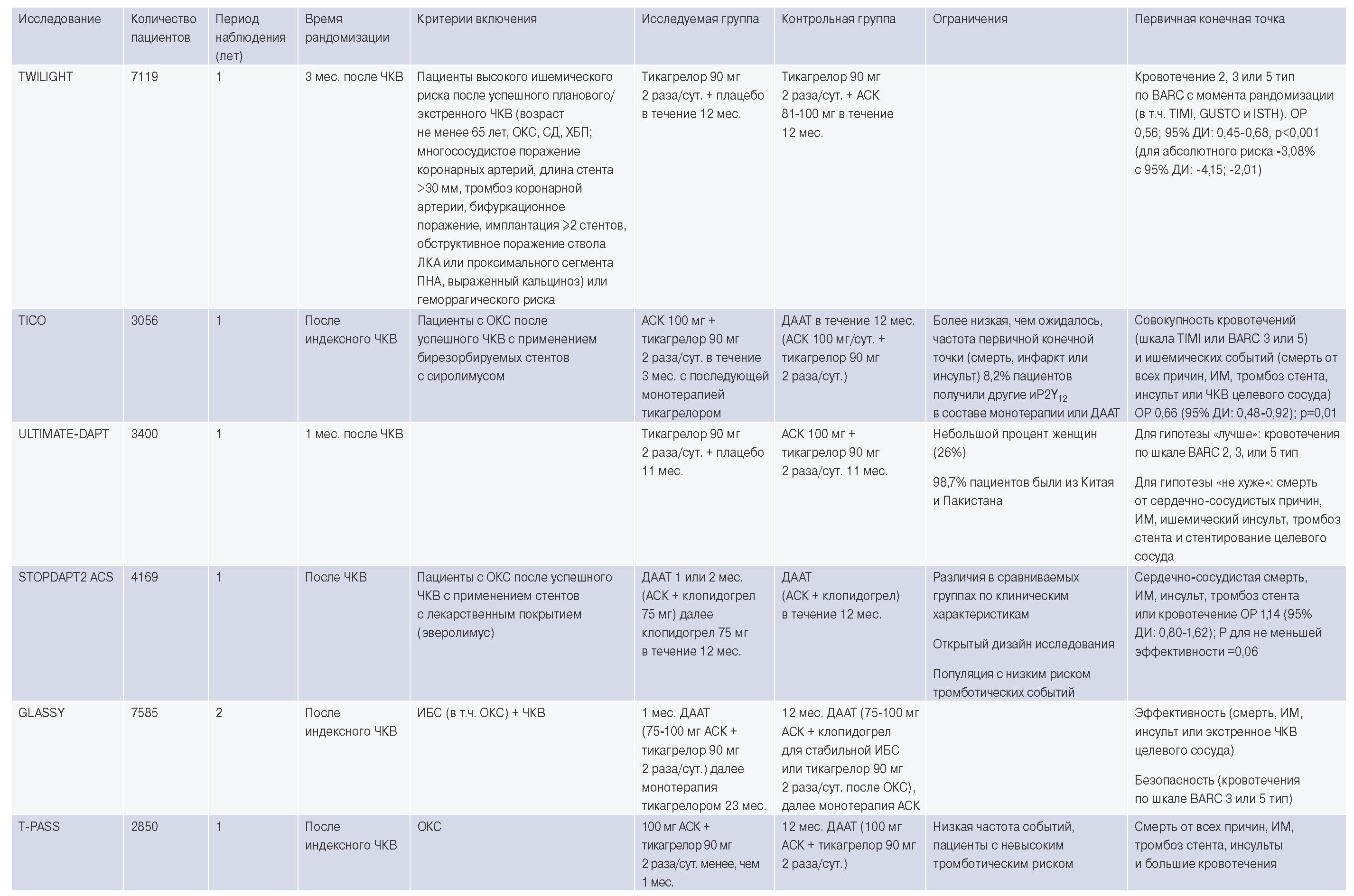
Сокращения: АСК — ацетилсалициловая кислота, ДААТ — двойная антиагрегантная терапия, ДИ — доверительный интервал, ИБС — ишемическая болезнь сердца, иP2Y12 — ингибиторы (блокаторы) рецепторов P2Y12, ИМ — инфаркт миокарда, ИМпST — инфаркт миокарда с подъемом сегмента ST, ЛКА — левая коронарная артерия, ОКС — острый коронарный синдром, ОР — отношение рисков, ПНА — правая нисходящая артерия, СД — сахарный диабет, ХБП — хроническая болезнь почек, ЧКВ — чрескожное коронарное вмешательство, BARC — Bleeding Academic Research Consortium.
Список литературы
1. Аверков О.В., Арутюнян Г.К., Дупляков Д.В. и др. Острый инфаркт миокарда с подъемом сегмента ST электрокардиограммы. Клинические рекомендации 2024. Российский кардиологический журнал. 2025; 30(3):6306. doi:10.15829/1560-4071-2025-6306. EDN: IVJCUK.
2. Аверков О.В., Арутюнян Г.К., Дупляков Д.В. и др. Острый коронарный синдром без подъема сегмента ST электрокардиограммы. Клинические рекомендации 2024. Российский кардиологический журнал. 2025; 30(5):6319. doi:10.15829/1560-4071-2025-6319. EDN: CXJUIB.
3. Byrne RA, Rossello JJ. Coughlan, et al. 2023 ESC Guidelines for the management of acute coronary syndromes: Developed by the task force on the management of acute coronary syndromes of the European Society of Cardiology (ESC). Eur. Heart J. 2023;44(38):3720826. doi:10.1093/eurheartj/ehad870.
4. Барбараш О.Л., Карпов Ю.А., Панов А.В. и др. Стабильная ишемическая болезнь сердца. Клинические рекомендации 2024. Российский кардиологический журнал. 2024;29(9):6110. doi:10.15829/1560-4071-2024-6110.
5. Rao SV, O’Donoghue ML, Ruel M, et al. 2025 ACC/AHA/ACEP/NAEMSP/SCAI Guideline for the Management of Patients With Acute Coronary Syndromes: A Report of the American College of Cardiology/American Heart Association Joint Committee on Clinical Practice Guidelines. Circulation. 2025;151(13):771-862. doi:10.1161/CIR.0000000000001346.
6. Steg PG, Bhatt DL, Simon T, et al. Ticagrelor in Patients with Stable Coronary Disease and Diabetes. N. Engl. J. Med. 2019;381(14):1309-20. doi:10.1056/NEJMoa1908077.
7. Xi Z, Li J, Qiu H, et al. Ticagrelor vs. Clopidogrel After Complex Percutaneous Coronary Intervention in Patients With Stable Coronary Artery Disease. Front. Cardiovasc. Med. Switzerland. 2021;8:768190. doi:10.3389/fcvm.2021.768190.
8. Wallentin L, Becker RC, Budaj A. et al. Ticagrelor versus Clopidogrel in Patients with Acute Coronary Syndromes. N. Engl. J. Med. 2009;361(11):1045-57. doi:10.1056/NEJMoa0904327.
9. Valgimigli M, Bueno H, Byrne RA, et al. 2017 ESC focused update on dual antiplatelet therapy in coronary artery disease developed in collaboration with EACTS: The Task Force for dual antiplatelet therapy in coronary artery disease of the European Society of Cardiology (ESC) and of the European Association for Cardio-¬Thoracic Surgery (EACTS). Eur. Heart J. 2017;39(3):213-60. doi:10.1093/eurheartj/ehx419.
10. Vranckx P, Valgimigli M, Jüni P, et al. Ticagrelor plus aspirin for 1 month, followed by ticagrelor monotherapy for 23 months vs aspirin plus clopidogrel or ticagrelor for 12 months, followed by aspirin monotherapy for 12 months after implantation of a drug-eluting stent: a multicentre, open-label, randomised superiority trial. Lancet. 2018;392(10151):940-9. doi:10.1016/S0140-6736(18)31858-0.
11. Mehran R, Baber U, Sharma SK, et al. Ticagrelor with or without Aspirin in High-¬Risk Patients after PCI. N. Engl. J. Med. 2019;381(21):2032-42. doi:10.1056/NEJMoa1908419.
12. Hahn J-Y, Bin Song Y, Oh J-H, et al. Effect of P2Y12 Inhibitor Monotherapy vs Dual Antiplatelet Therapy on Cardiovascular Events in Patients Undergoing Percutaneous Coronary Intervention: The SMART-CHOICE Randomized Clinical Trial. JAMA. 2019;321(24):242837. doi:10.1001/jama.2019.14331.
13. Watanabe H, Domei T, Morimoto T, et al. Effect of 1-Month Dual Antiplatelet Therapy Followed by Clopidogrel vs 12-Month Dual Antiplatelet Therapy on Cardiovascular and Bleeding Events in Patients Receiving PCI: The STOPDAPT 2 Randomized Clinical Trial. JAMA. 2019;321(24):2414-27. doi:10.1001/jama.2019.8145.
14. Valgimigli M, Frigoli E, Heg D, et al. Dual Antiplatelet Therapy after PCI in Patients at High Bleeding Risk. N. Engl. J. Med. 2021;385(18):1643-55. doi:10.1056/NEJMoa2108749.
15. Hong S-J, Kim J-S, Hong SJ, et al. 1-Month Dual-¬Antiplatelet Therapy Followed by Aspirin Monotherapy After Polymer-¬Free Drug-¬Coated Stent Implantation: One-¬Month DAPT Trial. JACC. Cardiovasc. Interv. United States. 2021;14(16):1801-11. doi:10.1016/j.jcin.2021.06.003.
16. Hahn J-Y, Bin Song Y, Oh J-H, et al. 6 month versus 12 month or longer dual antiplatelet therapy after percutaneous coronary intervention in patients with acute coronary syndrome (SMART-DATE): a randomised, open-label, non-inferiority trial. Lancet. 2018;391(10127):1274-84. doi:10.1016/S0140-6736(18)30493-8.
17. Bonaca MP, Bhatt DL, Cohen M, et al. Long-¬Term Use of Ticagrelor in Patients with Prior Myocardial Infarction. N. Engl. J. Med. 2015;372(19):1791-800. doi:10.1056/NEJMoa1500857.
18. Cuisset T, Deharo P, Quilici J, et al. Benefit of switching dual antiplatelet therapy after acute coronary syndrome: the TOPIC (timing of platelet inhibition after acute coronary syndrome) randomized study. Eur. Heart J. England. 2017;38(41):3070-8. doi:10.1093/eurheartj/ehx175.
19. Kim CJ, Park M-W, Kim MC, et al. Unguided de-escalation from ticagrelor to clopidogrel in stabilised patients with acute myocardial infarction undergoing percutaneous coronary intervention (TALOS-AMI): an investigator-¬initiated, open-label, multicentre, non-inferiority, randomised trial. Lancet. 2021;398(10308):1305-16. doi:10.1016/S0140-6736(21)01445-8.
20. Kim H-S, Kang J, Hwang D, et al. Durable Polymer Versus Biodegradable Polymer Drug-Eluting Stents After Percutaneous Coronary Intervention in Patients with Acute Coronary Syndrome: The HOST-REDUCE-POLYTECH-ACS Trial. Circulation. 2021;143(11):1081-91. doi:10.1161/CIRCULATIONAHA.120.051700.
21. Sibbing D, Aradi D, Jacobshagen C, et al. Guided de-escalation of antiplatelet treatment in patients with acute coronary syndrome undergoing percutaneous coronary intervention (TROPICAL-ACS): a randomised, open-label, multicentre trial. Lancet. 2017;390(10104):1747-57. doi:10.1016/S0140-6736(17)32155-4.
22. Wiviott SD, Braunwald E, McCabe CH, et al. Prasugrel versus Clopidogrel in Patients with Acute Coronary Syndromes. N. Engl. J. Med. 2007;357(20):2001-15. doi:10.1056/NEJMoa0706482.
23. Vranckx P, Valgimigli M, Odutayo A, et al. Efficacy and Safety of Ticagrelor Monotherapy by Clinical Presentation: Pre-¬Specified Analysis of the GLOBAL LEADERS Trial. J. Am. Heart Assoc. England. 2021;10(18):e015560. doi:10.1161/JAHA.119.015560.
24. Nicolas J, Baber U, Mehran R, TWILIGHT: A Randomized Trial of Ticagrelor Monotherapy Versus Ticagrelor Plus Aspirin Beginning at 3 Months in High-risk Patients Undergoing Percutaneous Coronary Intervention. US Cardiol. England. 2020;14:e04. doi:10.15420/usc.2019.02.
25. Baber U, Dangas G, Angiolillo DJ, et al. Ticagrelor alone vs. ticagrelor plus aspirin following percutaneous coronary intervention in patients with non-¬ST-segment elevation acute coronary syndromes: TWILIGHT-ACS. Eur. Heart J. 2020;41(37):3533-45. doi:10.1093/eurheartj/ehaa670.
26. Angiolillo DJ, Baber U, Mehran R. Ticagrelor monotherapy in patients with diabetes mellitus undergoing percutaneous coronary interventions: insights from the TWILIGHT trial. Cardiovasc. Res. 2020;116(7):e70 e72. doi:10.1093/cvr/cvaa120.
27. Dangas G, Baber U, Sharma S, et al. Ticagrelor With or Without Aspirin After Complex PCI. J. Am. Coll. Cardiol. 2020;75(19):2414-24. doi:10.1016/j.jacc.2020.03.011.
28. Escaned J, Cao D, Baber U, et al. Ticagrelor monotherapy in patients at high bleeding risk undergoing percutaneous coronary intervention: TWILIGHT-HBR. Eur. Heart J. England. 2021;42(45):4624-34. doi:10.1093/eurheartj/ehab702.
29. Kim B-K, Hong S-J, Cho Y-H, et al. Effect of Ticagrelor Monotherapy vs Ticagrelor With Aspirin on Major Bleeding and Cardiovascular Events in Patients With Acute Coronary Syndrome: The TICO Randomized Clinical Trial. JAMA. United States. 2020;323(23):240716. doi:10.1001/jama.2020.7580.
30. Baber U, Jang Y, Oliva A, et al. Safety and Efficacy of Ticagrelor Monotherapy in Patients With Acute Coronary Syndromes Undergoing Percutaneous Coronary Intervention: An Individual Patient Data Meta-¬Analysis of TWILIGHT and TICO Randomized Trials. Circulation. 2024;149(8):574-84. doi:10.1161/CIRCULATIONAHA.123.067283.
31. Hong S-J, Lee S-J, Suh Y, et al. Stopping Aspirin Within 1 Month After Stenting for Ticagrelor Monotherapy in Acute Coronary Syndrome: The T-PASS Randomized Noninferiority Trial. Circulation. 2024;149(8):562-73. doi:10.1161/CIRCULATIONAHA.123.066943.
32. Ge Z, Kan J, Gao X, et al. Ticagrelor alone versus ticagrelor plus aspirin from month 1 to month 12 after percutaneous coronary intervention in patients with acute coronary syndromes (ULTIMATE-DAPT): a randomised, placebo-¬controlled, double-¬blind clinical trial. Lancet. 2024;403(10439):1866-78. doi:10.1016/S0140-6736(24)00929-2.
33. Valgimigli M, Hong S-J, Gragnano F, et al. De-escalation to ticagrelor monotherapy versus 12 months of dual antiplatelet therapy in patients with and without acute coronary syndromes: a systematic review and individual patient-¬level meta-analysis of randomised trials. Lancet. 2024;404(10456):937-48. doi:10.1016/S0140-6736(24)01616-7.
34. Hong S-J, Ahn C-M, Kim J-S, et al. Effect of ticagrelor monotherapy on mortality after percutaneous coronary intervention: a systematic review and meta-analysis of randomized trials including 26143 patients. Eur. Hear. journal. Cardiovasc. Pharmacother. 2022;8(1):4855. doi:10.1093/ehjcvp/pvaa119.
35. Mansuri Z, Ashraf H, Taikadan T, et al. Ticagrelor monotherapy after short duration of dual antiplatelet therapy compared to continued dual antiplatelet therapy in patients with acute coronary syndromes undergoing percutaneous coronary interventions: an updated metaanalysis. Coron. Artery Dis. 2024;35(7):590-7. doi:10.1097/MCA.0000000000001417.
36. Guzman RB, Roberson MV, Teixeira L, et al. Ticagrelor Monotherapy Following Short-¬Term DAPT in ACS Undergoing PCI: A Systematic Review and Meta-¬Analysis. Catheter. Cardiovasc. Interv. Off. J. Soc. Card. Angiogr. Interv. 2025;105(6):1381-90. doi:10.1002/ccd.31459.
37. Carvalho PEP, Gewehr DM, Nascimento BR, et al. Short-¬Term Dual Antiplatelet Therapy After Drug-¬Eluting Stenting in Patients With Acute Coronary Syndromes: A Systematic Review and Network Meta-¬Analysis. JAMA Cardiol. 2024;9(12):1094-105. doi:10.1001/jamacardio.2024.3216.
38. Alagna G, Trimarchi G, Cascone A, et al. Effectiveness and Safety of Ticagrelor Monotherapy After Short-¬Duration Dual Antiplatelet Therapy in PCI Patients: A Systematic Review and Meta-¬Analysis. Am.J. Cardiol. 2025;241:69-74. doi:10.1016/j.amjcard.2025.01.014.
39. Valgimigli M, Mehran R, Franzone A, et al. Ticagrelor Monotherapy Versus Dual-¬Antiplatelet Therapy After PCI: An Individual Patient-¬Level Meta-¬Analysis. JACC. Cardiovasc. Interv. 2021;14(4):444-56. doi:10.1016/j.jcin.2020.11.046.
40. Galli M, Laudani C, Occhipinti G, et al. P2Y12 inhibitor monotherapy after short DAPT in acute coronary syndrome: a systematic review and meta-analysis. Eur. Hear. journal. Cardiovasc. Pharmacother. 2024;10(7):588-98. doi:10.1093/ehjcvp/pvae057.
41. van der Sangen NMR, Claessen BEPM, Küçük IT, et al. Single antiplatelet therapy directly after percutaneous coronary intervention in non-¬ST-segment elevation acute coronary syndrome patients: the OPTICA study. EuroIntervention J. Eur. Collab. with Work. Gr. Interv. Cardiol. Eur. Soc. Cardiol. 2023;19(1):63-72. doi:10.4244/EIJ-D-22-00886.
42. Lee SY, Jeong YH, Yun KH, et al. P2Y(12) Inhibitor Monotherapy Combined With Colchicine Following PCI in ACS Patients: The MACT Pilot Study. JACC. Cardiovasc. Interv. 2023;16(15):1845-55. doi:10.1016/j.jcin.2023.05.035.
43. Watanabe H, Morimoto T, Natsuaki M, et al. Comparison of Clopidogrel Monotherapy After 1 to 2 Months of Dual Antiplatelet Therapy With 12 Months of Dual Antiplatelet Therapy in Patients With Acute Coronary Syndrome: The STOPDAPT 2 ACS Randomized Clinical Trial. JAMA Cardiol. 2022;7(4):407-17. doi:10.1001/jamacardio.2021.5244.
44. Natsuaki M, Watanabe H, Morimoto T, et al. An Aspirin-¬Free Versus Dual Antiplatelet Strategy for Coronary Stenting: STOPDAPT 3 Randomized Trial. Circulation. United States. 2024;149(8):585-600. doi:10.1161/CIR.0000000000001255.
45. Armstrong PCJ, Leadbeater PD, Chan MV, et al. In the presence of strong P2Y12 receptor blockade, aspirin provides little additional inhibition of platelet aggregation. J. Thromb. Haemost. 2011;9(3):552-61. doi:10.1111/j.1538-7836.2010.04160.x.
46. Capranzano P, Moliterno D, Capodanno D Aspirin-free antiplatelet strategies after percutaneous coronary interventions. Eur. Heart J. 2024;45(8):572-85. doi:10.1093/eurheartj/ehad876.
47. Tarantini G, Smits PC, Lhermusier T, et al. A prospective study comparing short versus standard dual antiplatelet therapy in patients with acute myocardial infarction: design and rationale of the TARGET-FIRST trial. EuroIntervention J. Eur. Collab. with Work. Gr. Interv. Cardiol. Eur. Soc. Cardiol. 2023;19(3):240-7. doi:10.4244/EIJ-D-22-01006.
48. Guimarães PO, Franken M, Tavares CAM, et al. P2Y12 inhibitor monotherapy versus dual antiplatelet therapy in patients with acute coronary syndromes undergoing coronary stenting: rationale and design of the NEOMINDSET Trial. EuroIntervention J. Eur. Collab. with Work. Gr. Interv. Cardiol. Eur. Soc. Cardiol. 2023;19(4):e323 e329. doi:10.4244/EIJ-D-23-00125.
49. van der Sangen NMR, Küçük IT, Sivanesan S, et al. Less bleeding by omitting aspirin in non-¬ST-segment elevation acute coronary syndrome patients: Rationale and design of the LEGACY study. Am. Heart J. 2023;265:114-20. doi:10.1016/j.ahj.2023.07.011.
Об авторах
Ю. О. ШалагиноваРоссия
Шалагинова Юлия Олеговна — к.м.н., врач-кардиолог отдела неотложной кардиологии
Москва
Р. М. Шахнович
Россия
Шахнович Роман Михайлович — д.м.н., профессор института подготовки кадров высшей квалификации
Москва
- Двойная антиагрегантная терапия (ДААТ), назначенная пациентам, перенесшим инфаркт миокарда, в значительной степени предотвращает тромботические осложнения, прежде всего повторный инфаркт миокарда.
- Получены убедительные данные, что переход от ДААТ на монотерапию тикагрелором через 1-3 мес. после события приводит к значительному снижению риска кровотечений без увеличения частоты тромботических осложнений по сравнению с ДААТ в течение 12 мес.
Рецензия
Для цитирования:
Шалагинова Ю.О., Шахнович Р.М. Монотерапия тикагрелором как стратегия для снижения риска кровотечений у пациентов с острым коронарным синдромом, перенесших чрескожное коронарное вмешательство. Российский кардиологический журнал. 2025;30(9):6482. https://doi.org/10.15829/1560-4071-2025-6482. EDN: YNPEON
For citation:
Shalaginova Yu.O., Shakhnovich R.M. Ticagrelor monotherapy as a strategy to reduce the bleeding risk in patients with acute coronary syndrome who underwent percutaneous coronary intervention. Russian Journal of Cardiology. 2025;30(9):6482. (In Russ.) https://doi.org/10.15829/1560-4071-2025-6482. EDN: YNPEON
JATS XML

















































