Перейти к:
Сравнительное клинико-лабораторное исследование ривароксабана и его воспроизведённых форм у больных стабильной ишемической болезнью сердца
https://doi.org/10.15829/1560-4071-2025-6286
EDN: TEWITO
Аннотация
Течение ишемической болезни сердца и развитие её осложнений связано с прогрессированием атеросклероза и высокой вероятностью атеротромбоза. Антитромботическая терапия является наиболее эффективной стратегией предупреждения сердечно-сосудистых осложнений при заболеваниях, ассоциированных с атеросклерозом. В соответствии с действующими клиническими рекомендациями для профилактики инфаркта миокарда и инсульта всем больным со стабильным течением ишемической болезни сердца рекомендуется прием ацетилсалициловой кислоты (АСК), а для пациентов, имеющих высокий риск ишемических событий без высокого риска кровотечений, открывается возможность присоединения к АСК антикоагулянтного препарата ривароксабана в малых дозах. В статье рассматривается дизайн клинико-лабораторного проcпективного одноцентрового сравнительного исследования, целью которого является сравнение эффективности и безопасности двух биоэквивалентных препаратов: оригинального препарата — ривароксабан (Ксарелто, АО "Байер", Германия) и его генерического варианта (Круоксабан, ООО "Озон", Россия).
Ключевые слова
Для цитирования:
Ломакин Н.В., Ткач И.Ю., Широков Е.А. Сравнительное клинико-лабораторное исследование ривароксабана и его воспроизведённых форм у больных стабильной ишемической болезнью сердца. Российский кардиологический журнал. 2025;30(2):6286. https://doi.org/10.15829/1560-4071-2025-6286. EDN: TEWITO
For citation:
Lomakin N.V., Tkach I.Yu., Shirokov E.A. Comparative clinical and laboratory study of rivaroxaban and its generic forms in patients with stable coronary artery disease. Russian Journal of Cardiology. 2025;30(2):6286. (In Russ.) https://doi.org/10.15829/1560-4071-2025-6286. EDN: TEWITO
Сердечно-сосудистые заболевания остаются одной из главных причин смертности во всем мире. В России в 2022г зарегистрировано ~7,5 млн пациентов с ишемической болезнью сердца (ИБС). В 2022г от ИБС умерло 451 тыс. человек (23,8% от общей доли смертности) или 307,4 на 100 тыс. человек населения, в т. ч. в трудоспособном возрасте — 71,5 на 100 тыс. человек населения [1]. Течение ИБС и развитие её осложнений связано с прогрессированием атеросклероза и высокой вероятностью атеротромбоза. По данным экспертов, каждый четвертый случай смерти от разных причин связан с тромбозом или тромбоэмболией [2, 3]. Антитромботическая терапия (АТТ) является наиболее эффективной стратегией предупреждения сердечно-сосудистых осложнений (ССО) у больных ИБС. В соответствии с современными клиническими рекомендациями для профилактики ССО всем больным со стабильной ИБС рекомендуется прием ацетилсалициловой кислоты (АСК), а для пациентов, имеющих высокий риск ишемических событий без высокого риска кровотечений, рекомендуется рассмотреть возможность присоединения к АСК второго антитромбоцитарного препарата или антикоагулянтного препарата ривароксабана в дозе 2,5 мг 2 раза/сут. [4]. Двойное слепое многоцентровое рандомизированное клиническое исследование COMPASS (Cardiovascular Outcomes for People Using Anticoagulation Strategies), которое включало 27395 пациентов со стабильной ИБС или атеросклерозом периферических артерий, показало высокую эффективность применения малых доз ривароксабана для предупреждения атеротромбоза [5]. Сравнивались эффективность и безопасность комбинации АСК 100 мг 1 раз/сут. и ривароксабана в дозе 2,5 мг 2 раза/сут. с монотерапией ривароксабаном в дозе 5 мг 2 раза/сут. и монотерапией АСК в дозе 100 мг 1 раз/сут. Комбинация АСК с ривароксабаном продемонстрировала статистически значимое снижение относительного риска сердечно-сосудистой смерти, инсульта и инфаркта миокарда на 24% и хороший уровень безопасности (в отношении жизнеугрожающий кровотечений) в сравнении с монотерапией АСК.
Фармакоэкономический анализ показал, что комбинированная терапия ривароксабаном и АСК характеризуется меньшими затратами в сравнении с применением монотерапии АСК. Таким образом, добавление ривароксабана в дозе 2,5 мг 2 раза/сут. к АСК показало не только высокую эффективность и безопасность, но и оказалось экономически выгодным [6]. Между тем, в реальной клинической практике терапевтический потенциал современных прямых оральных антикоагулянтов (ПОАК) реализован не в полной мере. По данным регистра РЕКВАЗА в амбулаторной практике только 4,2% больных получают антикоагулянтные препараты [7]. Отчасти, это связано с высокой стоимостью оригинальных ПОАК. Снижению стоимости лечения ПОАК способствует применение "дженериков" — воспроизведённых форм оригинальных лекарственных препаратов. Однако широкое применение дженериков требует специальных исследований, направленных на оценку биоэквивалентности препаратов оригинальным.
Цель исследования: исследование лабораторных эффектов, отражающих состояние системы гемостаза и фармакодинамику оригинального препарата — ривароксабан (Ксарелто, АО "Байер", Германия) в дозе 2,5 мг 2 раза/сут. и его генерического варианта (Круоксабан, ООО "Озон", Россия) у больных со стабильной ИБС, имеющих высокий риск ишемических событий и не высокий риск кровотечений.
Результаты сравнительного исследования биоэквивалентности препаратов Ксарелто (Германия) и Круоксабан (Российская Федерация)
Клиническое исследование биоэквивалентности лекарственных препаратов проведено в Российской Федерации (РФ) в соответствии с протоколом № RVX001 версии 1.1 от 24.12.2020, требованиями российского законодательства, Правилами надлежащей клинической практики Евразийского экономического сообщества, Правилами проведения исследований биоэквивалентности лекарственных препаратов в рамках Евразийского экономического сообщества и международными правилами проведения клинических исследований (ICH GCP). В ходе исследования изучена сравнительная фармакокинетика и биоэквивалентность двух препаратов ривароксабана: исследуемый препарат — Круоксабан: таблетки, покрытые пленочной оболочкой, 2,5 мг, производства ООО "Озон" (Россия) и препарат сравнения, разрешенный к медицинскому применению в России — Ксарелто: таблетки, покрытые пленочной оболочкой, 2,5 мг (АО "Байер", Германия). Результаты исследования представлены на рисунке 1.
По основным параметрам установлена биоэквивалентность исследуемых препаратов. Сравниваемые препараты имеют сопоставимый профиль безопасности 1.
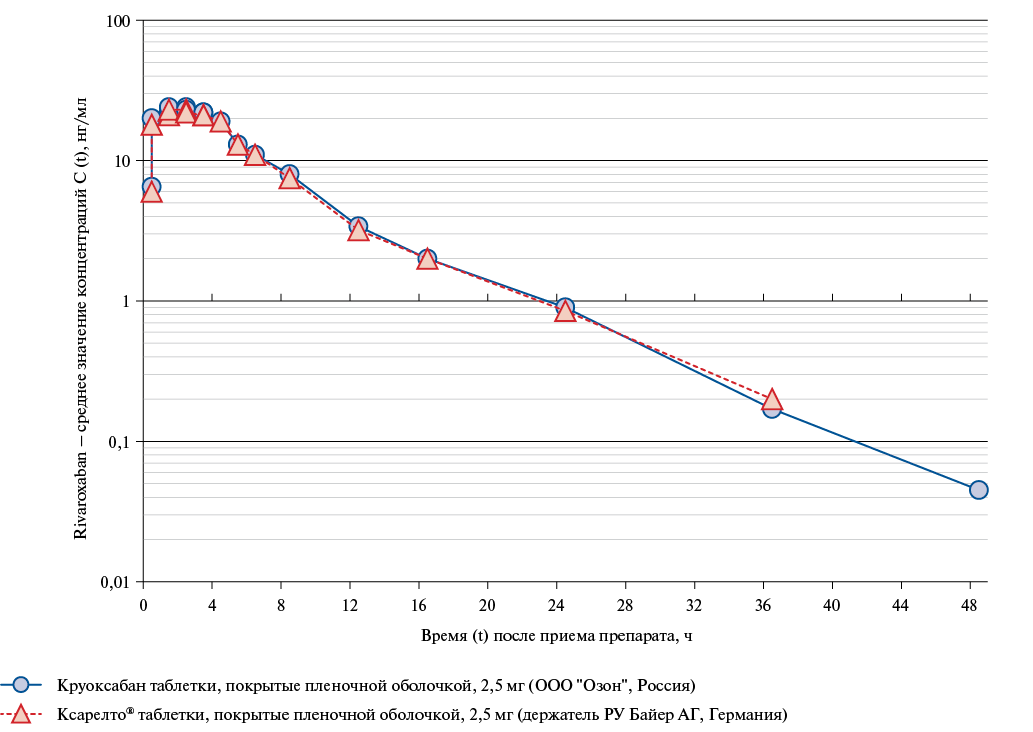
Рис. 1. Фармакокинетика препаратов Круоксабан (РФ) и Ксарелто (Германия).
Организация исследования
Планируемое клинико-лабораторное исследование является: проcпективным одноцентровым неинтервенционным сравнительным исследованием изучения лабораторных эффектов ривароксабана и его воспроизведенных форм у пациентов со стабильной ИБС. В исследование будет включено 50 пациентов со стабильной ИБС, имеющих высокий риск ишемических событий и не имеющих высокого риска кровотечения, старше 18 лет с показанием к назначению двойной антитромбоцитарной терапии. Одной группе пациентов будет назначен препарат "Круоксабан" от компании "Озон Фармацевтика", а второй оригинальный ривароксабан. Решение об инициации АТТ, выборе препаратов будет приниматься лечащим врачом. Наблюдение за пациентами (оценка исследуемых параметров) будет осуществляться до начала лечения (визит 1), в первый день лечения (визит 2) и на 5 день лечения (визит 3) после старта терапии АСК в дозе 75 мг 1 раз/сут. + ривароксабан в дозе 2,5 мг раза/сут. Организация исследования с распределением по этапам представлена на рисунке 2.
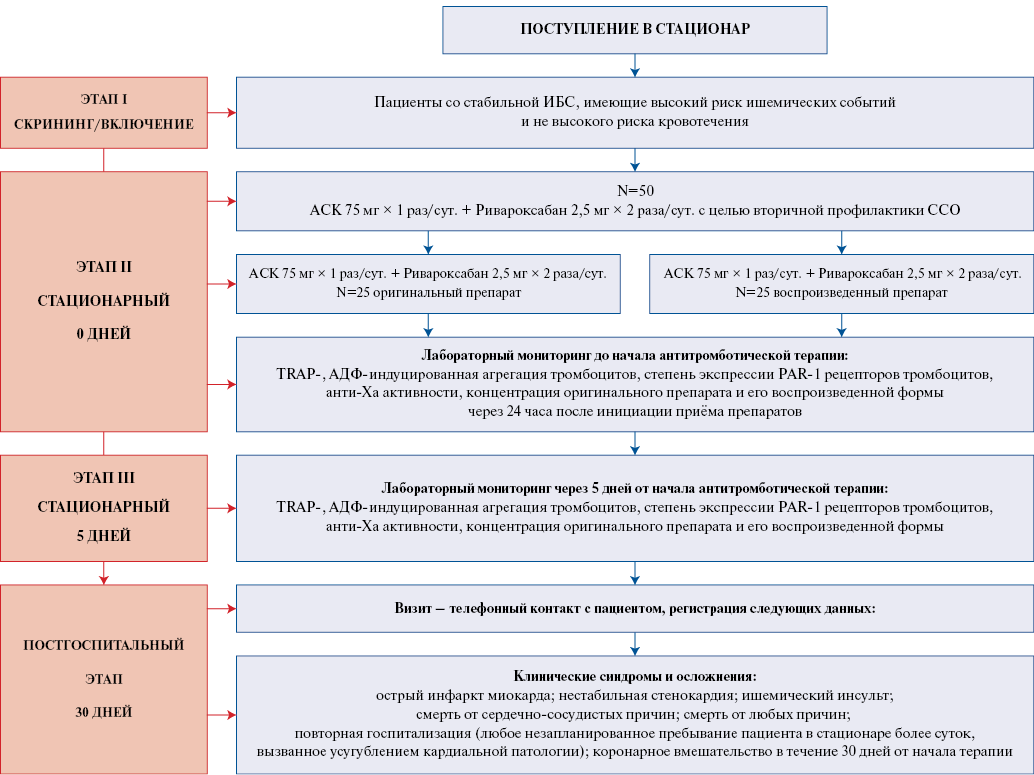
Рис. 2. Дизайн исследования.
Сокращения: АДФ — аденозиндифосфат, АСК — ацетилсалициловая кислота, ИБС — ишемическая болезнь сердца, ССО — сердечно-сосудистые осложнения, TRAP — Thrombin Receptor Activating Peptide.
Критерии включения:
- Возраст старше 18 лет.
- Пациенты, госпитализированные с клиническими проявлениями стабильной ИБС, подтвержденной с помощью одного из следующих методов:
а) стресс-методов (пробы с физической нагрузкой или стресс-эхокардиография);
б) сцинтиграфия миокарда с функциональными пробами, или однофотонная эмиссионная компьютерная томография миокарда перфузионная с функциональными пробами;
в) мультиспиральная компьютерная томография коронарных артерий (компьютерно-томографическая коронарография);
г) инвазивная селективная коронароангиография;
и имеющих высокий риск ишемических событий, что подразумевает:
— многососудистое поражение коронарных артерий (стеноз >50% по данным мультиспиральной компьютерной томографии коронарных артерий/коронароангиография) в сочетании как минимум с одним из следующих признаков:
а) сахарный диабет, требующий приема медикаментов;
б) перенесенный инфаркт миокарда (давность не менее 28 дней);
в) атеросклеротическое поражение периферических артерий;
г) хроническая болезнь почек с расчетной скоростью клубочковой фильтрации 15-59 мл/мин/1,73 м2.
- Отсутствие противопоказаний к назначению АТТ.
- Пациенты, не имеющие опыта приема АСК в дозе 75 мг 1 раз/сут. + ривароксабан в дозе 2,5 мг 2 раза/сут.
- Наличие письменного информированного согласия пациента.
Критерии невключения:
- Противопоказания к приему антитромботических препаратов.
- Высокий риск кровотечения:
а) наличие у пациента внутричерепного кровоизлияния или другой внутричерепной патологии в анамнезе (кроме ишемического инсульта давностью >1 мес.);
б) недавнее кровотечение из желудочно-кишечного тракта (ЖКТ) или анемия вследствие потери крови из ЖКТ;
в) другая патология ЖКТ, ассоциирующаяся с повышенным риском кровотечения;
г) печеночная недостаточность (цирроз, или повышение в 2 раза выше нормы билирубина в сочетании с повышением в 3 раза верхних границ нормы аспартатаминотрансферазы/аланинаминотрансферазы/щелочной фосфатазы);
д) геморрагический диатез;
е) старческий возраст и синдром "хрупкости";
ж) хроническая болезнь почек, требующая диализа, или расчетная скорость клубочковой фильтрации <15 мл/мин/1,73 м2.
- Наличие у пациента других (кроме ИБС) показаний к приему ПОАК.
- Сопутствующий прием других препаратов, влияющих на тромбоцитарное или плазменное звено гемостаза.
- Письменный отказ пациента от приема антитромботических препаратов.
- Участие пациента в других клинических исследованиях во время проведения данного исследования.
- Беременность и период лактации, либо женщины, планирующие наступление беременности в период участия в этом исследовании.
- Отсутствие контакта с пациентом после выписки из стационара.
Конечные точки
Первичные конечные точки эффективности:
а) разница в Thrombin Receptor Activating Peptide (TRAP)-индуцированной агрегации тромбоцитов до и через 5 дней от начала АТТ в двух группах больных;
б) разница в аденозиндифосфат-индуцированной агрегации тромбоцитов до и через 5 дней от начала АТТ в двух группах больных;
в) разница в степени экспрессии PAR-1 рецепторов тромбоцитов (Protease-Activated Receptors) до и через 5 дней от начала АТТ в двух группах больных;
г) корреляция между изменением концентрации оригинального препарата и уровнем TRAP-индуцированной агрегации тромбоцитов до и через 5 дней от начала АТТ в группе больных, получавших оригинальный препарат;
д) разница анти-Ха активности до и через 5 дней от начала АТТ в двух группах больных;
е) разница в морфологических особенностях тромбоцитов до и через 5 дней от начала АТТ в двух группах больных.
Вторичные конечные точки эффективности:
Клинические синдромы и осложнения:
а) острый инфаркт миокарда;
б) нестабильная стенокардия;
в) ишемический инсульт;
г) смерть от сердечно-сосудистых причин;
д) смерть от любых причин;
е) повторная госпитализация (любое незапланированное пребывание пациента в стационаре более суток, вызванное усугублением кардиальной патологии);
ж) коронарное вмешательство в течение 30 дней от начала терапии.
Вторичные конечные точки безопасности:
— кровотечения с оценкой по шкале BARC 1-5 типа в течение 30 дней от начала терапии.
Заключение
В результате анализа клинических данных и лабораторных тестов, полученных при сравнении биоэквивалентных препаратов, будут получены объективные данные об эффективности и безопасности воспроизведенного препарата "Круоксабан" по сравнению с оригинальным препаратом, а также эффективность и безопасность применения комбинированной терапии АСК и малых доз ривароксабана у больных с клиническими признаками стабильной ИБС. Существенное научное и практическое значение будут иметь результаты лабораторных исследований, отражающих влияние комбинированной АТТ на тромбоцитарный и плазменный гемостаз и концентрационные данные исследуемых препаратов. Результаты исследования могут быть полезными для более широкого применения комбинированной АТТ в целях предупреждения ССО у больных ИБС в рамках действующих клинических рекомендаций.
Отношения и деятельность: все авторы заявляют об отсутствии потенциального конфликта интересов, требующего раскрытия в данной статье.
1 Исследование сравнительной фармакокинетики и биоэквивалентности препаратов "Ривароксабан" 2,5 мг и "Ксарелто" 2,5 мг у здоровых добровольцев https://grls.rosminzdrav.ru/CIPermissionMini.aspx?CIStatementGUID=d37394b7-ce65-4106-9eed-a57d38abd25c&CIPermGUID=b5f71dc8-c572-49d9-a739-d75e2371167e.
Список литературы
1. Healthcare in Russia. 2023: Stat. sb./Rosstat. М., З-46 2023. 179 с. (In Russ.). п. 2023: Стат. сб./Росстат. М., З-46 2023. 179 с.
2. GBD 2021 Stroke Risk Factor Collaborators. Global, regional, and national burden of stroke and its risk factors, 1990-2021: a systematic analysis for the Global Burden of Disease Study 2021. Lancet Neurol. 2024;23(10):973-1003. doi:10.1016/S1474-4422(24)00369-7.
3. Wang Y, Haddad Y, Patel R, et al. Factors influencing the outcome of cardiogenic cerebral embolism: a literature review. Neurol Res. 2022;44(3):187-95. doi:10.1080/01616412.2021.1968704.
4. Барбараш О. Л., Карпов Ю. А., Панов А. В. и др. Стабильная ишемическая болезнь сердца. Клинические рекомендации 2024. Российский кардиологический журнал. 2024;29(9):6110. doi:10.15829/1560-4071-2024-6110. EDN HHJJUT.
5. Steffel J, Eikelboom JW, Anand S, et al. The COMPASS Trial: Net Clinical Benefit of Low-Dose Rivaroxaban Plus Aspirin as Compared With Aspirin in Patients With Chronic Vascular Disease. Circulation. 2020;142(1):40-8. doi:10.1161/CIRCULATIONAHA.120.046048.
6. Stewart S, Murphy N, Walker A, et al. Cost of an emerging epidemic. an economic analysis of atrial fibrillation in the UK. Heart. 2004;90:286-92.
7. Бойцов С. А., Лукьянов М. М., Якушин С. С., Марцевич С. Ю. Регистр кардиоваскулярных заболеваний (РЕКВАЗА): Диагностика, лечение, сочетанная сердечно-сосудистая патология и сопутствующие заболевания у больных с диагнозом "фибрилляция предсердий" в условиях реальной амбулаторно-поликлинической практики. Кардиоваскулярная терапия и профилактика. 2014;13(6):44-50.
Об авторах
Н. В. ЛомакинРоссия
д.м.н., зав. кардиологического отделения № 2 (для проведения рентгенохирургических методов лечения) (с палатами реанимации и интенсивной терапии), Главный кардиолог; зав. кафедрой кардиологии.
Москва
Конфликт интересов:
нет
И. Ю. Ткач
Россия
Врач-кардиолог кардиологического отделения № 2 (для проведения рентгенохирургических методов лечения) (с палатами реанимации и интенсивной терапии); ассистент кафедры кардиологии.
Москва
Конфликт интересов:
нет
Е. А. Широков
Россия
д.м.н., профессор кафедры кардиологии.
Москва
Конфликт интересов:
нет
- Всем больным со стабильной ишемической болезнью сердца, имеющим высокий риск ишемических событий без высокого риска кровотечений, рекомендуется рассмотреть возможность присоединения к ацетилсалициловой кислоте второго антитромбоцитарного препарата или антикоагулянтного препарата ривароксабана в дозе 2,5 мг 2 раза/сут.
- Будет проведено исследование лабораторных эффектов, отражающих состояние системы гемостаза и фармакодинамику оригинального препарата — ривароксабан (Ксарелто, АО "Байер", Германия) в дозе 2,5 мг 2 раза/сут. и его генерического варианта (Круоксабан, ООО "Озон", Россия).
Рецензия
Для цитирования:
Ломакин Н.В., Ткач И.Ю., Широков Е.А. Сравнительное клинико-лабораторное исследование ривароксабана и его воспроизведённых форм у больных стабильной ишемической болезнью сердца. Российский кардиологический журнал. 2025;30(2):6286. https://doi.org/10.15829/1560-4071-2025-6286. EDN: TEWITO
For citation:
Lomakin N.V., Tkach I.Yu., Shirokov E.A. Comparative clinical and laboratory study of rivaroxaban and its generic forms in patients with stable coronary artery disease. Russian Journal of Cardiology. 2025;30(2):6286. (In Russ.) https://doi.org/10.15829/1560-4071-2025-6286. EDN: TEWITO

















































