Перейти к:
Взаимосвязь хронического окклюзионного поражения коронарных артерий с проживанием в экстремальных природно-климатических условиях
https://doi.org/10.15829/1560-4071-2025-6156
EDN: YGKAID
Аннотация
Цель. Изучить взаимосвязь хронического окклюзионного поражения коронарных артерий с проживанием в экстремальных природно-климатических условиях Крайнего Севера у пациентов с ишемической болезнью сердца (ИБС).
Материал и методы. Из "Регистра проведенных операций коронарной ангиографии" были отобраны 5679 больных c ИБС. Основную группу составили 2588 некоренных жителей Крайнего Севера, группу сравнения — 3091 пациент, проживающий на Юге Тюменской области. Хроническая окклюзия коронарной артерии определялась при отсутствии антеградного кровотока по коронарной артерии продолжительностью >3 мес. по данным анамнеза, либо предшествующей коронароангиографии. С целью устранения исходного дисбаланса между исследуемыми группами применялся метод сопоставления индексов склонностей (propensity score matching).
Результаты. Пациенты, проживающие на Крайнем Севере, были моложе (53,2±7,49 лет vs 56,8±8,34 лет, p<0,001), среди них чаще встречались мужчины. После проведения propensity score matching, в сбалансированных по основным факторам риска ИБС группах, у пациентов Крайнего Севера чаще определялся значимый коронарный атеросклероз. При этом у пациентов, постоянно проживающих на Крайнем Севере, статистически значимо чаще определялись хронические окклюзии (50,3% vs 41,7%, p<0,001). У пациентов основной группы хронические окклюзии чаще локализовались в проксимальных (35,0% vs 29,0%, p<0,001) и средних сегментах (39,0% vs 33,0%, p<0,001) коронарных артерий в сравнении с группой Юга Тюменской области. Наиболее частая локализация окклюзионного поражения определялась в передней нисходящей артерии (22,0% vs 17,0%, p<0,001) и правой коронарной артерии (28,0% vs 24,0%, p=0,001). По результатам мультивариантного анализа, проживание на Крайнем Севере ассоциировалось с увеличением частоты выявления хронических окклюзий коронарных артерий при проведении коронароангиографии на 39% (отношение шансов 1,39; 95% доверительный интервал: 1,25-1,54; p<0,001).
Заключение. У пациентов с ИБС, проживающих на Крайнем Севере, хронические окклюзии коронарных артерий определяются чаще в сравнении с больными Юга Тюменской области. По результатам мультивариантного анализа проживание в экстремальных природно-климатических условиях являлось независимым предиктором выявления хронических окклюзий коронарных артерий при проведении коронароангиографии.
Ключевые слова
Для цитирования:
Утегенов Р.Б., Сапожников С.С., Бессонов И.С. Взаимосвязь хронического окклюзионного поражения коронарных артерий с проживанием в экстремальных природно-климатических условиях. Российский кардиологический журнал. 2025;30(6):6156. https://doi.org/10.15829/1560-4071-2025-6156. EDN: YGKAID
For citation:
Utegenov R.B., Sapozhnikov S.S., Bessonov I.S. Association between coronary chronic total occlusion and living in extreme natural and climatic conditions. Russian Journal of Cardiology. 2025;30(6):6156. (In Russ.) https://doi.org/10.15829/1560-4071-2025-6156. EDN: YGKAID
Ишемическая болезнь сердца (ИБС) остаётся одной из ведущих причин заболеваемости и смертности как в России, так и в мире [1]. Согласно исследованию, проведенному в рамках проекта Global Burden of Disease, ИБС продолжает занимать лидирующие позиции в статистике смертности, что подчеркивает необходимость глубокого понимания факторов, лежащих в основе её развития и прогрессирования [2].
В этом контексте особый интерес представляют регионы Крайнего Севера (КС), где наряду с традиционными факторами риска, население подвергается воздействию экстремальных природно-климатических условий. Исследования показали, что арктический климат может оказывать негативное влияние на сердечно-сосудистую систему, в частности, способствовать раннему развитию и неблагоприятному течению ИБС [3][4].
Наследственные механизмы адаптации у пришлого населения Севера сталкиваются с серьезными вызовами в экстремальных природно-климатических условиях. Эти механизмы, хотя и обеспечивают краткосрочную адаптацию, но не всегда способны поддерживать нормальные физиологические процессы на длительном промежутке времени. Это обусловливает формирование так называемого "синдрома полярного напряжения". К основным компонентам этого синдрома относятся окислительный стресс, иммунная недостаточность, гипоксия тканей и психоэмоциональное напряжение [5]. Истощение адаптационных возможностей организма, в свою очередь, вызывает каскад дизадаптивных расстройств, приводящих к развитию хронических заболеваний.
Ранее было установлено, что у населения КС коронарный атеросклероз развивается в более молодом возрасте и характеризуется более тяжелым поражением коронарных артерий. В то же время роль хронических окклюзий коронарных артерий (ХОКА) в структуре этих комплексных поражений остаётся малоизученной [6]. Окклюзия коронарных артерий считается хронической, если в течение ≥3 мес. в артерии отсутствует физиологический антеградный кровоток [7]. У данного состояния можно выделить две основные причины. Первая — острый тромбоз, который приводит к внезапной закупорке сосуда вследствие повреждения сосудистой стенки. Вторая — прогрессирование существующего стеноза коронарной артерии, который со временем приводит к полной окклюзии [8]. Согласно одной из гипотез, у пациентов, проживающих на КС, структура атеросклеротических бляшек (АСБ) может способствовать более частому развитию ХОКА. Так, исследование с использованием оптической когерентной томографии показало, что у жителей КС наблюдается более высокая частота формирования фиброатеромы с тонкой капсулой (ФАТК), что делает их более уязвимыми к разрыву, являющемуся ведущим предиктором коронарного тромбоза, а также может способствовать более частому развитию ХОКА [9].
В связи с вышеизложенным, целью настоящего исследования явилось изучение взаимосвязи хронического окклюзионного поражения коронарных артерий с проживанием в экстремальных природно-климатических условиях КС у пациентов с ИБС.
Материал и методы
Из "Регистра проведенных операций коронарной ангиографии"1, содержащего данные 25627 пациентов, были отобраны 5679 больных ИБС, кому в Тюменском кардиологическом научном центре была выполнена коронароангиография (КАГ). В исследование включались пациенты с верифицированной ИБС, подтвержденной инструментальными методами (стресс-эхокардиография, велоэргометрическая проба, тредмил-тест). Из исследования были исключены лица с пропусками в данных, и представители коренного населения КС, а также с окклюзионными поражениями коронарных артерий с подтвержденной давностью <3 мес. (рис. 1).
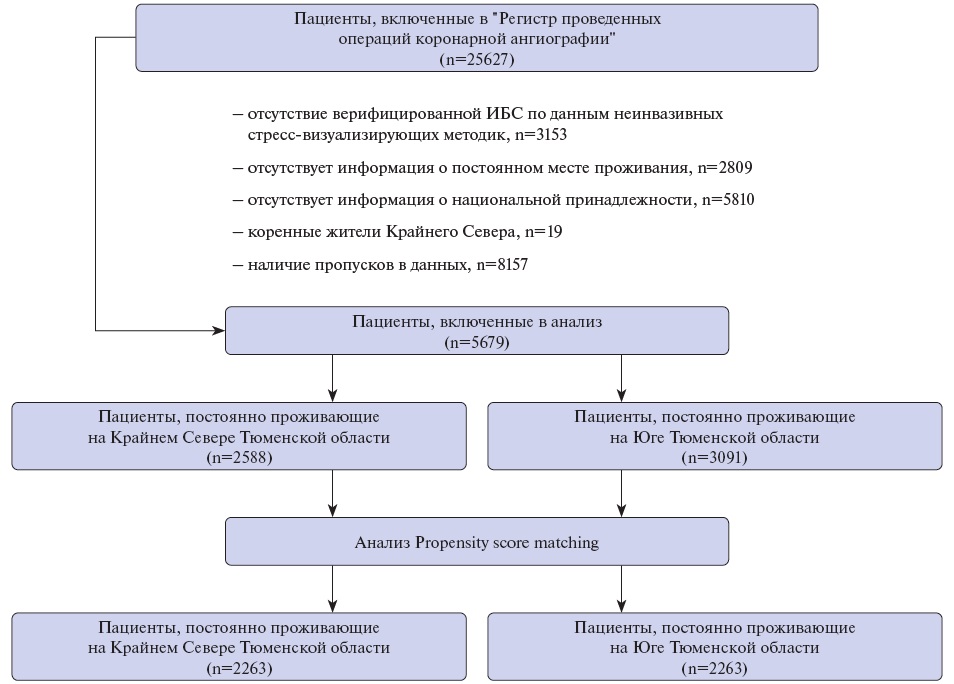
Рис. 1. Дизайн исследования.
Сокращение: ИБС — ишемическая болезнь сердца.
Диагностика ИБС основывалась на клинико-анамнестических данных (перенесенный инфаркт миокарда (ИМ), стенокардия высокого функционального класса, безболевая ишемия миокарда) и результатах инструментальных исследований. Критерием ишемии миокарда по результатам стресс-эхокардиографии считалось появление транзиторных нарушений регионарной и глобальной сократимости левого желудочка на пике нагрузки. Положительным результатом нагрузочных тестов на велоэргометре и тредмил-тесте считалась горизонтальная или косонисходящая депрессия или элевация сегмента ST ≥1 мм в двух смежных отведениях через ≥60-80 мс от точки J во время или сразу после прекращения нагрузки, в т.ч. без ангинозного приступа.
Пациенты с положительным нагрузочными тестами и высокими риском выявления обструктивных поражений коронарных артерий подверглись инвазивному исследованию — КАГ. Для стеноза ствола левой коронарной артерии и проксимального сегмента передней нисходящей артерии (ПНА) значимым считалось сужение ≥50% диаметра, в остальных случаях ≥75% диаметра. ХОКА определялась при отсутствии антеградного кровотока по коронарной артерии продолжительностью не менее 3 мес., диагностируемое по данным анамнеза (перенесенный ИМ) или предшествующей КАГ.
Статистический анализ. Для анализа данных применялись статистические пакеты SPSS 26.0 (IBM, USA) и R4.2 (Vienna). Методом анализа полных случаев (complete case analysis) были исключены пропущенные значения. Непрерывные переменные с нормальным распределением представлены в виде среднего значения ± стандартное отклонение, а при распределении, отличном от нормального, в виде медианы (25‑й — 75‑й перцентиль). Нормальность распределения количественных показателей оценивалась с помощью критерия Колмогорова-Смирнова. Категориальные переменные описаны абсолютными и относительными частотами. Для сравнения количественных переменных использовались критерий t Стьюдента (при нормальном распределении) и непараметрический критерий Манна-Уитни (при распределении, отличном от нормального). Качественные переменные сопоставлялись с помощью критерия χ². С целью устранения исходного дисбаланса между исследуемыми группами применялось сопоставление оценок склонностей (propensity score matching — PSM) по принципу ближайшего соседа в соотношении 1:1 с калипером 0,05. Достижение баланса между группами подтверждалось визуальной оценкой с использованием графиков Love plot, Density plot и функции bal.tab пакета "cobalt" (рис. 2). После PSM сравнение групп проводилось с помощью теста МакНемара для категориальных данных, парного t-теста или знакового рангового теста Уилкоксона для непрерывных данных. Моделирование бинарного отклика осуществлялось с применением генерализованной линейной модели (логистической регрессии) с робастными оценками. Для выявления потенциальной систематической ошибки (unmeasured bias) и оценки устойчивости полученных результатов использовался тест Розенбаума. Для определения факторов, ассоциирующихся с наличием хронической окклюзии проводили мультивариантный анализ — бинарную логистическую регрессию.
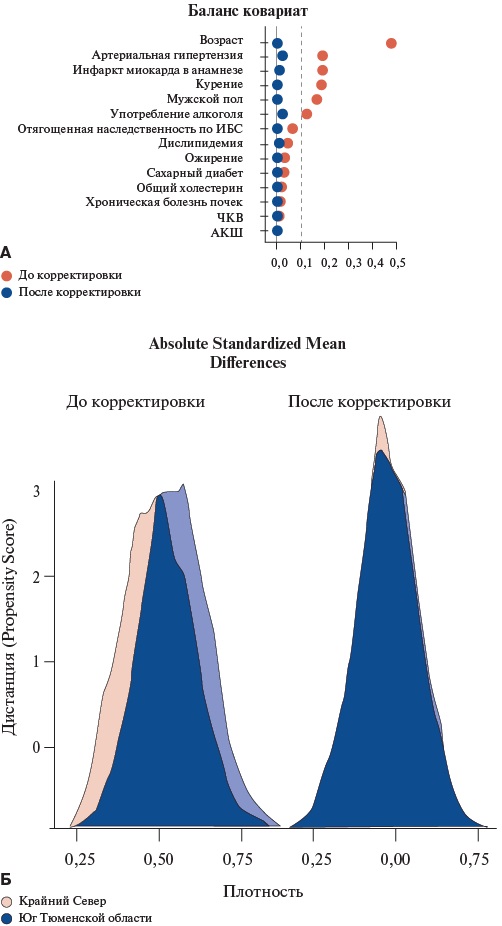
Рис. 2. Сравнение распределения ковариат до и после применения метода Propensity Score Matching с помощью визуализации Love plot (A) и Density plot (Б).
Примечание: цветное изображение доступно в электронной версии журнала.
Сокращения: АКШ — аортокоронарное шунтирование, ИБС — ишемическая болезнь сердца, ЧКВ — чрескожное коронарное вмешательство.
Данное исследование было выполнено в строгом соответствии с этическими принципами, изложенными в Хельсинкской декларации. Протокол исследования прошел экспертизу и получил одобрение локального этического комитета (выписка из протокола заседания № 175 от 16.11.2021).
Результаты
В исследование вошли 5679 пациентов, основную группу которых составили 2588 некоренных жителей Ямало-Ненецкого автономного округа (ЯНАО), относящегося к территориям КС Тюменской области. В группу сравнения были включены 3091 больных, проживающих в умеренной климатической зоне Юга Тюменской области (ЮТО).
Клинико-демографические данные пациентов представлены в таблице 1. Сравнительный анализ клинических характеристик пациентов выявил определенные различия в зависимости от региона постоянного проживания. Так, проживающее на КС пациенты были моложе, с преобладанием лиц мужского пола. Распространенность таких факторов риска, как курение и злоупотребление алкоголем, была также выше среди пациентов, постоянно проживающих на КС. Кроме того, в основной группе чаще регистрировался ИМ в анамнезе. В то же время для проживающих на ЮТО была характерна более высокая частота отягощенной наследственности по ИБС. Также у них чаще встречались артериальная гипертензия и нарушения липидного обмена.
Таблица 1
Клиническая характеристика пациентов до и после сопоставления индексов склонностей
|
Показатели |
До проведения PSM |
После проведения PSM |
||||||
|
Пациенты, проживающие на Севере Тюменской области (n=2588) |
Пациенты, проживающие на Юге Тюменской области (n=3091) |
р |
SMD |
Пациенты, проживающие на Севере Тюменской области (n=2263) |
Пациенты, проживающие на Юге Тюменской области (n=2263) |
р |
SMD |
|
|
Возраст, лет, M±SD |
53,2±7,49 |
56,8±8,34 |
<0,001 |
0,452 |
54,2±7,12 |
54,2±7,34 |
0,400 |
0,020 |
|
Мужской пол, n (%) |
2234 (86,3) |
2499 (80,8) |
<0,001 |
0,152 |
1931 (85,3) |
1934 (85,5) |
1,000 |
<0,001 |
|
Курение, n (%) |
1048 (40,5) |
996 (32,0) |
<0,001 |
0,170 |
862 (37,9) |
865 (38,2) |
0,855 |
0,006 |
|
Употребление алкоголя, n (%) |
507 (20,0) |
462 (15,0) |
<0,001 |
0,120 |
407 (18,0) |
400 (17,7) |
0,800 |
0,010 |
|
Ожирение, n (%) |
1288 (49,8) |
1454 (47,0) |
0,043 |
0,050 |
1113 (49,2) |
1124 (49,7) |
0,800 |
0,01 |
|
Сахарный диабет, n (%) |
418 (16,2) |
444 (14,4) |
0,067 |
0,050 |
343 (15,2) |
343 (15,2) |
0,935 |
0,004 |
|
ХБП, n (%) |
33 (1,3) |
35 (1,1) |
0,716 |
0,010 |
27 (0,01) |
28 (0,01) |
1,000 |
<0,001 |
|
Отягощенная наследственность по ИБС, n (%) |
583 (23,0) |
780 (25,0) |
0,019 |
0,060 |
531 (23,4) |
537 (23,6) |
0,861 |
0,006 |
|
Инфаркт миокарда в анамнезе, n (%) |
1476 (57,1) |
1481 (48,1) |
<0,001 |
0,180 |
1227 (54,2) |
1220 (53,5) |
0,721 |
0,011 |
|
Артериальная гипертония, n (%) |
2112 (81,6) |
2744 (88,8) |
<0,001 |
0,201 |
1916 (84,7) |
1943 (85,9) |
0,300 |
0,03 |
|
ЧКВ в анамнезе, n (%) |
465 (18,0) |
569 (18,4) |
0,675 |
0,012 |
406 (17,9) |
410 (18,0) |
0,908 |
0,005 |
|
АКШ в анамнезе, n (%) |
105 (4,1) |
125 (4,0) |
0,828 |
0,008 |
94 (4,2) |
98 (4,3) |
0,773 |
0,010 |
|
Содержание общего холестерина, ммоль/л, M±SD |
5,15±1,29 |
5,18±1,27 |
0,458 |
0,020 |
5,16±1,27 |
5,15±1,26 |
0,945 |
0,001 |
|
Дислипидемия, n (%) |
2174 (84,0) |
2668 (86,3) |
0,016 |
0,070 |
1922 (84,9) |
1919 (84,8) |
>0,9 |
0,011 |
Сокращения: АКШ — аортокоронарное шунтирование, ИБС — ишемическая болезнь сердца, ЧКВ — чрескожное коронарное вмешательство, ХБП — хроническая болезнь почек, PSM — Propensity Score Matching, SMD — Standardized Mean Difference.
После проведения анализа PSM, статистически значимых различий по базовым клинико-демографическим параметрам, включая факторы риска ИБС, между исследуемыми группами выявлено не было. На рисунке 2 представлен баланс переменных до и после PSM анализа.
В ходе анализа количественных и качественных данных ангиографии (представлены в таблицах 2 и 3) было установлено, что у пациентов, постоянно проживающих в условиях КС, чаще наблюдались более выраженные атеросклеротические поражения коронарного русла. При этом после применения метода PSM большая часть изначально обнаруженных ангиографических различий сохранялась.
Таблица 2
Ангиографическая характеристика качественных показателей
|
Показатели |
До проведения PSM |
После проведения PSM |
||||
|
Пациенты, проживающие на Севере Тюменской области (n=2588) |
Пациенты, проживающие на Юге Тюменской области (n=3091) |
р |
Пациенты, проживающие на Севере Тюменской области (n=2263) |
Пациенты, проживающие на Юге Тюменской области (n=2263) |
р |
|
|
Наличие коронарного атеросклероза, n (%) |
2,174 (84,0) |
2,424 (78,0) |
<0,001 |
1,896 (84,0) |
1,785 (79,0) |
<0,001 |
|
Наличие гемодинамически значимого поражения, n (%) |
1,891 (73,0) |
1,941 (63,0) |
<0,001 |
1,648 (73,0) |
1,427 (63,0) |
<0,001 |
|
Наличие окклюзионного поражения, n (%) |
1,315 (50,8) |
1,281 (41,4) |
<0,001 |
1,139 (50,3) |
944 (41,7) |
<0,001 |
|
Окклюзии в проксимальном сегменте, n (%) |
899 (35,0) |
893 (29,0) |
<0,001 |
783 (35,0) |
655 (29,0) |
<0,001 |
|
Окклюзии в среднем сегменте, n (%) |
1,018 (39,0) |
1,027 (33,0) |
<0,001 |
883 (39,0) |
738 (33) |
<0,001 |
|
Окклюзии в дистальном сегменте, n (%) |
166 (6,4) |
180 (5,8) |
0,4 |
147 (6,5) |
122 (5,4) |
0,13 |
|
Окклюзионное поражение ПНА, n (%) |
594 (23,0) |
508 (16,0) |
<0,001 |
505 (22,0) |
377 (17,0) |
<0,001 |
|
Окклюзионное поражение ОА, n (%) |
328 (13,0) |
354 (11,0) |
0,2 |
295 (13,0) |
252 (11,0) |
0,055 |
|
Окклюзионное поражение ПКА, n (%) |
727 (28,0) |
734 (24,0) |
<0,001 |
637 (28,0) |
540 (24,0) |
0,001 |
|
Окклюзионное поражение ДА, n (%) |
54 (2,1) |
39 (1,3) |
0,02 |
51 (2,3) |
27 (1,2) |
0,009 |
|
Окклюзионное поражение ВТК, n (%) |
120 (4,6) |
138 (4,5) |
0,8 |
106 (4,7) |
102 (4,5) |
0,8 |
|
Окклюзионное поражение ИА, n (%) |
25 (1,0) |
27 (0,9) |
0,8 |
22 (1,0) |
23 (1,0) |
>0,9 |
Сокращения: ВТК — ветвь тупого края, ДА — диагональная артерия, ИА — интермедиарная артерия, ОА — огибающая артерия, ПКА — правая коронарная артерия, ПНА — передняя нисходящая артерия, PSM — Propensity Score Matching.
Таблица 3
Ангиографическая характеристика количественных показателей
|
Показатели |
До проведения PSM |
После проведения PSM |
|||||
|
Пациенты, проживающие на Севере Тюменской области (n=2588) |
Пациенты, проживающие на Юге Тюменской области (n=3091) |
р |
Пациенты, проживающие на Севере Тюменской области (n=2263) |
Пациенты, проживающие на Юге Тюменской области (n=2263) |
р |
||
|
Количество артерий с гемодинамически значимыми стенозами без окклюзионных поражений, n (%) |
0 |
1,433 (55,2) |
1,811 (59,0) |
0,001 |
1,243 (55,1) |
1,361 (60,2) |
0,006 |
|
1 |
784 (30,3) |
809 (26,1) |
684 (30,2) |
594 (26,1) |
|||
|
2 |
266 (10,2) |
321 (10,0) |
237 (10,2) |
211 (9,4) |
|||
|
≥3 |
105 (4,3) |
150 (4,9) |
99 (4,5) |
97 (4,3) |
|||
|
Количество артерий с гемодинамически значимыми стенозами, n (%) |
0 |
697 (27,1) |
1,150 (37,0) |
<0,001 |
615 (27,0) |
836 (37,0) |
<0,001 |
|
1 |
919 (36,0) |
916 (30,0) |
784 (35,0) |
708 (31,0) |
|||
|
2 |
523 (20,0) |
498 (16,0) |
460 (20,0) |
369 (16,5) |
|||
|
≥3 |
449 (16,9) |
527 (17,0) |
404 (18,0) |
350 (15,5) |
|||
|
Количество артерий с гемодинамически незначимыми стенозами, n (%) |
0 |
2,017 (65,1) |
1,740 (67,2) |
0,056 |
1,514 (67,0) |
1,494 (65,0) |
0,8 |
|
1 |
785 (25,3) |
633 (24,1) |
551 (24,0) |
565 (24,6) |
|||
|
2 |
239 (7,8) |
194 (7,7) |
177 (7,8) |
175 (7,1) |
|||
|
≥3 |
50 (1,8) |
21 (1,0) |
21 (1,0) |
29 (1,3) |
|||
|
Общее количество окклюзированных артерий, n (%) |
0 |
1,273 (49,2) |
1,810 (59,0) |
<0,001 |
1,124 (50,0) |
1,319 (58,0) |
<0,001 |
|
1 |
970 (37,0) |
955 (30,8) |
828 (37,0) |
709 (31,0) |
|||
|
2 |
274 (11,0) |
266 (8,3) |
248 (11,0) |
191 (9,0) |
|||
|
≥3 |
71 (2,8) |
60 (1,9) |
63 (2,0) |
44 (1,9) |
|||
|
Стенотическое поражение СтЛКА, n (%) |
<50% |
158 (6,1) |
182 (5,9) |
0,8 |
143 (6,3) |
131 (5,8) |
0,5 |
|
50-75% |
67 (2,6) |
93 (3,0) |
0,4 |
54 (2,4) |
55 (2,4) |
>0,9 |
|
|
75-90% |
38 (1,5) |
47 (1,5) |
>0,9 |
36 (1,6) |
27 (1,2) |
0,3 |
|
|
>90% |
10 (0,4) |
27 (0,9) |
0,035 |
10 (0,4) |
19 (0,8) |
0,14 |
|
|
Наличие стенотического поражения любой коронарной артерии, n (%) |
<50% |
811 (31,1) |
1052 (34,4) |
0,024 |
715 (32,0) |
748 (33,0) |
0,3 |
|
50-75% |
623 (24,0) |
732 (24,0) |
0,8 |
545 (24,0) |
542 (24,0) |
>0,9 |
|
|
75-90% |
740 (29,0) |
849 (27,0) |
0,4 |
658 (29,0) |
603 (27,0) |
0,073 |
|
|
>90% |
461 (18,0) |
523 (17,0) |
0,4 |
410 (18,0) |
358 (16,0) |
0,043 |
|
|
Стенотическое поражение ПНА, n (%) |
<50% |
302 (12,0) |
450 (15,0) |
0,002 |
264 (12,0) |
318 (14,0) |
0,019 |
|
50-75% |
205 (7,9) |
278 (9,0) |
0,2 |
171 (7,6) |
205 (9,1) |
0,076 |
|
|
75-90% |
312 (12,0) |
346 (11,0) |
0,3 |
282 (12,0) |
249 (11,0) |
0,14 |
|
|
>90% |
188 (7,3) |
214 (6,9) |
0,7 |
171 (7,6) |
153 (6,8) |
0,3 |
|
|
Стенотическое поражение ОА, n (%) |
<50% |
209 (8,1) |
268 (8,7) |
0,4 |
194 (8,6) |
183 (8,1) |
0,6 |
|
50-75% |
188 (7,3) |
184 (6,0) |
0,053 |
170 (7,5) |
144 (6,4) |
0,14 |
|
|
75-90% |
213 (8,2) |
256 (8,3) |
>0,9 |
188 (8,3) |
163 (7,2) |
0,2 |
|
|
>90% |
99 (3,8) |
113 (3,7) |
0,8 |
87 (3,8) |
70 (3,1) |
0,2 |
|
|
Стенотическое поражение ПКА, n (%) |
<50% |
280 (11,0) |
381 (12,0) |
0,085 |
244 (11,0) |
277 (12,0) |
0,14 |
|
50-75% |
186 (7,2) |
196 (6,3) |
0,2 |
163 (7,2) |
150 (6,6) |
0,5 |
|
|
75-90% |
210 (8,1) |
278 (9,0) |
0,3 |
183 (8,1) |
198 (8,7) |
0,5 |
|
|
>90% |
142 (5,5) |
149 (4,8) |
0,3 |
122 (5,4) |
100 (4,4) |
0,15 |
|
|
Стенотическое поражение ДА, n (%) |
<50% |
42 (1,6) |
44 (1,4) |
0,6 |
38 (1,7) |
31 (1,4) |
0,5 |
|
50-75% |
63 (2,4) |
96 (3,1) |
0,15 |
60 (2,7) |
69 (3,0) |
0,5 |
|
|
75-90% |
101 (3,9) |
103 (3,3) |
0,3 |
91 (4,0) |
73 (3,2) |
0,2 |
|
|
>90% |
67 (2,6) |
90 (2,9) |
0,5 |
62 (2,7) |
58 (26,0) |
0,8 |
|
|
Стенотическое поражение ВТК, n (%) |
<50% |
78 (3,0) |
73 (2,4) |
0,2 |
72 (3,2) |
50 (2,2) |
0,054 |
|
50-75% |
71 (2,7) |
88 (2,8) |
0,9 |
61 (2,7) |
64 (2,8) |
0,9 |
|
|
75-90% |
114 (4,4) |
119 (3,8) |
0,3 |
105 (4,6) |
86 (3,8) |
0,2 |
|
|
>90% |
32 (1,2) |
56 (1,8) |
0,1 |
30 (1,3) |
37 (1,6) |
0,5 |
|
|
Стенотическое поражение ИА, n (%) |
<50% |
16 (0,6) |
20 (0,6) |
>0,9 |
14 (0,6) |
13 (0,6) |
>0,9 |
|
50-75% |
22 (0,9) |
27 (0,9) |
>0,9 |
21 (0,9) |
21 (0,9) |
>0,9 |
|
|
75-90% |
45 (1,7) |
41 (1,3) |
0,2 |
40 (1,8) |
34 (1,5) |
0,6 |
|
|
>90% |
21 (0,8) |
32 (1,0) |
0,5 |
19 (0,8) |
24 (1,1) |
0,5 |
|
Сокращения: ВТК — ветвь тупого края, ДА — диагональная артерия, ИА — интермедиарная артерия, ОА — огибающая артерия, ПКА — правая коронарная артерия, ПНА — передняя нисходящая артерия, СтЛКА — ствол левой коронарной артерии, PSM — Propensity Score Matching.
Пациенты основной группы чаще имели коронарный атеросклероз с гемодинамически значимыми поражениями одной, двух, трех и более коронарных артериях. В том числе статистически значимые различия определялись по количеству артерий с гемодинамически значимыми стенозами, без учета окклюзионных поражений.
У пациентов основной группы статистически значимо чаще определялось хроническое окклюзионное поражение коронарного русла. Качественный анализ результатов показал, что у пациентов основной группы статистически значимо чаще наблюдались окклюзии проксимальных и средних сегментов коронарных артерий по сравнению с группой сравнения. При этом обращает на себя внимание, что наиболее частая локализация окклюзий наблюдалась в крупных эпикардиальных коронарных артериях, таких как ПНА и правая коронарная артерия (ПКА).
В таблице 4 представлена модель бинарной логистической регрессии. По результатам мультивариантного анализа было установлено, что возраст, мужской пол, курение, ожирение, сахарный диабет, ИМ и аортокоронарное шунтирование в анамнезе являлись независимыми предикторами выявления ХОКА при проведении КАГ. При этом проживание на КС ассоциировалось с увеличением частоты определения ХОКА на 39% (отношение шансов 1,39; 95% доверительный интервал: 1,25-1,54; p<0,001).
Таблица 4
Факторы, ассоциирующиеся с наличием ХОКА
|
Показатель |
Унивариантный анализ |
Мультивариантный анализ |
||
|
ОШ (95% ДИ) |
p, value |
ОШ (95% ДИ) |
p, value |
|
|
Возраст, лет |
1,01 (1,01-1,02) |
<0,001 |
1,02 (1,01-1,03) |
<0,001 |
|
Мужской пол |
2,14 (1,87-2,44) |
<0,001 |
1,85 (1,59-2,15) |
<0,001 |
|
Уровень холестерина |
1,07 (1,03-1,11) |
<0,001 |
1,12 (1,08-1,17) |
<0,001 |
|
Курение |
1,32 (1,20-1,46) |
<0,001 |
1,23 (1,10-1,37) |
<0,001 |
|
Ожирение |
1,20 (1,09-1,32) |
<0,001 |
1,19 (1,07-1,32) |
0,001 |
|
Сахарный диабет |
1,47 (1,29-1,69) |
<0,001 |
1,33 (1,14-1,54) |
<0,001 |
|
ИМ в анамнезе |
3,29 (2,98-3,62) |
<0,001 |
2,98 (2,70-3,30) |
<0,001 |
|
Артериальная гипертензия |
1,19 (1,05-1,35) |
0,005 |
1,19 (1,03-1,36) |
0,015 |
|
АКШ в анамнезе |
15,4 (9,70-26,3) |
<0,001 |
12,1 (7,54-20,8) |
<0,001 |
|
Проживание на Крайнем Севере |
1,39 (1,25-1,54) |
<0,001 |
1,39 (1,25-1,54) |
<0,001 |
Сокращения: АКШ — аортокоронарное шунтирование, ДИ — доверительный интервал, ИМ — инфаркт миокарда, ОШ — отношение шансов.
Обсуждение
Результаты нашего исследования свидетельствуют о том, что у пациентов с верифицированной ИБС, постоянно проживающих в экстремальных природно-климатических условиях, наблюдается более сложное и комплексное течение коронарного атеросклероза с высокой частотой окклюзионного поражения коронарного русла. При этом проживание на КС являлось независимым предиктором наличия окклюзионного поражения коронарных артерий. Эти данные подтверждают, что экстремальные природно-климатические факторы КС могут оказывать негативное влияние на раннее развитие и быстрое прогрессирование атеросклеротического процесса в коронарном русле.
Следует отметить, что в условиях высоких широт, наряду с неблагоприятным воздействием экстремальных климатических условий, значительно меняется образ жизни, характер питания и психоэмоциональный статус пациентов, что также может способствовать развитию и прогрессированию коронарного атеросклероза [10]. Так, в ряде исследований была показана взаимосвязь депрессии, тревожности, уровня доходов и других неконвенционных факторов риска c развитием острого коронарного синдрома в условиях КС [11][12].
Согласно результатам различных исследований, частота выявления ХОКА при проведении диагностической КАГ варьируется от 14,7% до 52% [13-15]. В нашем исследовании частота ХОКА в основной группе составила 50,3%, что соответствует верхней границе диапазона, описанного в литературе. При этом средний возраст пациентов по нашим данным был существенно ниже в сравнении с аналогичными исследованиями.
Несмотря на одинаковую частоту ИМ в анамнезе и частоту предшествующей эндоваскулярной реваскуляризации, в т.ч. по поводу острого ИМ, у пациентов КС значительно чаще выявлялись ХОКА. Эти различия могут быть связаны с особенностями патогенеза сосудистых катастроф в условиях КС. Тромбоз, возникающий при разрыве или эрозии АСБ, может быть тотальным или частично ограничивающим просвет артерии, а его динамика зависит от баланса фибринолитических процессов [16]. Предполагается, что природно-климатические факторы КС могут способствовать развитию стойкого тотального тромбоза без тенденции к реканализации. Данная гипотеза представляется актуальной и нуждается в проведении дополнительных исследований для более глубокого понимания механизмов влияния различных факторов на развитие и прогрессирование коронарного атеросклероза у пациентов, проживающих в условиях Арктического климата.
Локализация ХОКА в различных сосудистых бассейнах коронарного русла имеет важное значение. Полученные в настоящем исследовании данные о локализации хронических окклюзий согласуются с общемировой статистикой, демонстрируя преобладание поражений в ПКА [17]. При этом наибольшую клиническую значимость имеет локализация хронических окклюзий в ПНА. Учитывая, что ПНА обеспечивает кровоснабжение большей части миокарда левого желудочка, ее окклюзия потенциально приводит к более серьезным последствиям, таким как прогрессирование сердечной недостаточности, формирование аневризмы левого желудочка и летальному исходу [18][19]. Вероятно, меньший процент пациентов с ХОКА ПНА, чем ПКА обусловлен тем, что значительная часть этих больных погибает в остром периоде ИМ до проведения КАГ [20]. Этот факт может искажать реальную картину при анализе доминирующей локализации инфаркт-связанной коронарной артерии.
Согласно полученным нами данным, у пациентов, проживающих на КС, статистически значимо чаще окклюзионное поражение локализовалось в проксимальных и средних сегментах крупных эпикардиальных артерий. Следует отметить, что такая локализация поражений является наиболее неблагоприятной. По данным крупного регистра PROGRESS-CTO, у пациентов с ХОКА проксимальных сегментов сердечная недостаточность встречалась значительно чаще по сравнению с пациентами, у которых окклюзии локализовались в средних и дистальных сегментах артерии [21]. Закономерно, что чем проксимальнее расположена окклюзия, тем больше миокарда подвергается ишемии за счет большего вовлечения боковых ветвей, отходящих от основной эпикардиальной коронарной артерии. Именно поэтому практически не встречаются пациенты с хроническими окклюзиями ствола левой коронарной артерии, которые имеют крайне малые шансы на выживание [22].
Высокая частота хронических окклюзионных поражений на КС может быть обусловлена особенностями строения АСБ. Ранее нами было выявлено, что у пациентов на КС по данным оптической когерентной томографии ФАТК определялась чаще, чем у пациентов умеренной климатической зоны. ФАТК считается основным паттерном разрыва АСБ, приводящим к острым тромботическим катастрофам [9].
Ограничения исследования. Основным ограничением данного исследования является его ретроспективный дизайн.
Заключение
Проведенное исследование показало, что у пациентов с ИБС, проживающих на КС, ХОКА определяются чаще в сравнении с больными ЮТО. По результатам мультивариантного анализа проживание в экстремальных природно-климатических условиях являлось независимым предиктором наличия ХОКА при проведении КАГ.
Благодарности. Благодарим научного сотрудника лаборатории РЭМДиЛ Тюменского кардиологического научного цента к.м.н. Каштанова М. Г. за проведенный статистический анализ данных.
Отношения и деятельность: все авторы заявляют об отсутствии потенциального конфликта интересов, требующего раскрытия в данной статье.
1. Кузнецов В. А., Зырянов И. П., Колунин Г. В. и др. Регистр проведенных операций коронарной ангиографии (база данных). Свидетельство: 010620075. Заявка: 2009620515. 2010.
Список литературы
1. Бойцов С. А., Зайратьянц О. В., Андреев Е. М. и др. Сравнение показателей смертности от ишемической болезни сердца среди мужчин и женщин старше 50 лет в России и США. Российский кардиологический журнал. 2017;(6):100-7. doi:10.15829/1560-4071-2017-6-100-107.
2. Moran AE, Forouzanfar MH, Roth GA, et al. Temporal trends in ischemic heart disease mortality in 21 world regions, 1980 to 2010: the Global Burden of Disease 2010 study. Circulation. 2014;129(14):1483-92. doi:10.1161/CIRCULATIONAHA.113.004042.
3. Корчин В. И., Корчина Т. Я., Терникова Е. М. и др. Влияние климатогеографических факторов Ямало-Ненецкого автономного округа на здоровье населения (обзор). Журнал медико-биологических исследований. 2021;9(1):77-88. doi:10.37482/2687-1491-Z046.
4. Марасанов А. В., Стехин А. А., Яковлева Г. В. Подход к обеспечению здоровьесбережения населения Арктической зоны Российской Федерации (обзор). Журнал медико-биологических исследований. 2021;9(2):201-12. doi:10.37482/2687-1491-Z058.
5. Хаснулин В. И., Хаснулин П. В. Современные представления о механизмах формирования северного стресса у человека в высоких широтах. Экология человека. 2012;19(1):3-11. doi:10.17816/humeco17512.
6. Утегенов Р. Б., Сапожников С. С., Каштанов М. Г. и др. Особенности коронарного атеросклероза у пациентов с ишемической болезнью сердца, проживающих на Крайнем Севере. Сибирский журнал клинической и экспериментальной медицины. 2024;39(4):66-74. doi:10.29001/1850-9466-2023-606.
7. Brilakis ES, Mashayekhi K, Tsuchikane E, et al. Guiding Principles for Chronic Total Occlusion Percutaneous Coronary Intervention. Circulation. 2019;140(5):420-33. doi:10.1161/CIRCULATIONAHA.119.039797.
8. Allahwala UK, Brilakis ES, Byrne J, et al. Applicability and Interpretation of Coronary Physiology in the Setting of a Chronic Total Occlusion. Circ Cardiovasc Interv. 2019;12(7): e007813. doi:10.1161/CIRCINTERVENTIONS.119.007813.
9. Утегенов Р. Б., Сапожников С. С., Бессонов И. С. Особенности строения атеросклеротических бляшек по данным оптической когерентной томографии у пациентов с ишемической болезнью сердца, проживающих в экстремальных климатических условиях. Российский кардиологический журнал. 2024;29(8):5865. doi:10.15829/1560-4071-2024-5865.
10. Корнеева Е.В., Трекина Н.Е., Мамина А.А. Влияние пищевого поведения и физической активности на развитие метаболического синдрома у молодого трудоспособного населения, длительно проживающего в условиях Крайнего Севера. Кардиоваскулярная терапия и профилактика. 2015;14(1):41-6. doi:10.15829/1728-8800-2015-1-41-46.
11. Кожокарь К. Г., Урванцева И. А., Николаев К. Ю. Анализ психосоциальных характеристик пациентов с острым коронарным синдромом, проживающих в условиях Севера. Сибирское медицинское обозрение. 2017;(6):110-5. doi:10.20333/2500136-2017-6-110-115.
12. Котелкина О. С., Николаев К. Ю., Лифшиц Г. И. Ассоциации некоторых психосоциальных факторов с сердечно-сосудистыми заболеваниями и приверженностью к медикаментозному лечению у пациентов, перенесших инфаркт миокарда. Атеросклероз. 2022;18(4):395-404. doi:10.52727/2078-256X-2022-18-4-395-404.
13. Christofferson RD, Lehmann KG, Martin GV, et al. Effect of chronic total coronary occlusion on treatment strategy. Am J Cardiol. 2005;95(9):1088-91. doi:10.1016/j.amjcard.2004.12.065.
14. Azzalini L, Jolicoeur EM, Pighi M, et al. Epidemiology, Management Strategies, and Outcomes of Patients With Chronic Total Coronary Occlusion. Am J Cardiol. 2016;118(8):1128-35. doi:10.1016/j.amjcard.2016.07.023.
15. Vemuri KS, Sihag BK, Sharma Y, et al. Real world perspective of coronary chronic total occlusion in third world countries: A tertiary care centre study from northern India. Indian Heart J. 2021;73(2):156-60. doi:10.1016/j.ihj.2021.03.001.
16. Власов Т. Д., Яшин С. М. Артериальные и венозные тромбозы. Всегда ли применима триада Вирхова? Регионарное кровообращение и микроциркуляция. 2022;21(1):78-86. doi:10.24884/1682-6655-2022-21-1-78-86.
17. Rempakos A, Alexandrou M, Mutlu D, et al. Predictors of successful primary antegrade wiring in chronic total occlusion percutaneous coronary intervention. J Invasive Cardiol. 2024;36(6). doi:10.25270/jic/23.00305.
18. Бессонов И. С., Кузнецов В. А., Сапожников С. С. и др. Шкала оценки риска госпитальной летальности у пациентов с острым инфарктом миокарда с подъемом сегмента ST электрокардиограммы. Кардиология. 2021;61(9):11-9. doi:10.18087/cardio.2021.9.n1720.
19. Ferrante G, Barbieri L, Sponzilli C, et al. Predictors of Mortality and Long-Term Outcome in Patients with Anterior STEMI: Results from a Single Center Study. J Clin Med. 2021; 10(23):5634. doi:10.3390/jcm10235634.
20. Бадоян А. Г., Крестьянинов О. В., Хелимский Д. А. и др. Предикторы улучшения качества жизни пациентов с хроническими окклюзиями коронарных артерий в зависимости от тактики ведения. Комплексные проблемы сердечно-сосудистых заболеваний. 2021;10(2):72-83. doi:10.17802/2306-1278-2021-10-2-72-83.
21. Garcia S, Alraies MC, Karatasakis A, et al. Coronary artery spatial distribution of chronic total occlusions: Insights from a large US registry. Catheter Cardiovasc Interv. 2017;90(1):23-30. doi:10.1002/ccd.26844.
22. Kanabar K, Mehrotra S, P R. Ostial left main coronary artery chronic total occlusion presenting as chronic stable angina. Indian Heart J. 2018;70(5):745-9. doi:10.1016/j.ihj.2018.04.012.
Об авторах
Р. Б. УтегеновРоссия
Утегенов Руслан Булатович — м.н.с., врач по рентгенэндоваскулярным диагностике и лечению.
Томск
Конфликт интересов:
Нет
С. С. Сапожников
Россия
Сапожников Станислав Сталикович — м.н.с., лаборатория рентгенэндоваскулярных методов диагностики и лечения, Научный отдел инструментальных методов исследования.
Томск
Конфликт интересов:
Нет
И. С. Бессонов
Россия
Бессонов Иван Сергеевич — д.м.н., зав. лабораторией рентгенэндоваскулярных методов диагностики и лечения, Научный отдел инструментальных методов исследования.
Томск
Конфликт интересов:
Нет
Дополнительные файлы
- Для пациентов с ишемической болезнью сердца, проживающих на Крайнем Севере, характерно более частое и комплексное поражение коронарного русла.
- Выявляемость хронического окклюзионного поражения коронарных артерий на Крайнем Севере достигла 50,3%, что соответствует верхней границе диапазона, описанного в литературе, несмотря на более молодой возраст пациентов.
- Проживание в экстремальных природно-климатических условиях являлось независимым предиктором наличия хронического окклюзионного поражения коронарных артерий при проведении коронароангиографии.
Рецензия
Для цитирования:
Утегенов Р.Б., Сапожников С.С., Бессонов И.С. Взаимосвязь хронического окклюзионного поражения коронарных артерий с проживанием в экстремальных природно-климатических условиях. Российский кардиологический журнал. 2025;30(6):6156. https://doi.org/10.15829/1560-4071-2025-6156. EDN: YGKAID
For citation:
Utegenov R.B., Sapozhnikov S.S., Bessonov I.S. Association between coronary chronic total occlusion and living in extreme natural and climatic conditions. Russian Journal of Cardiology. 2025;30(6):6156. (In Russ.) https://doi.org/10.15829/1560-4071-2025-6156. EDN: YGKAID
JATS XML

















































