Перейти к:
Роль магнитно-резонансной томографии в прогнозе эффективности ресинхронизирующей терапии для лечения пациентов с некомпактным миокардом левого желудочка и хронической сердечной недостаточностью
https://doi.org/10.15829/1560-4071-2024-6150
EDN: IYEWIO
Аннотация
Цель. Оценить роль магнитно-резонансной томографии (МРТ) в прогнозе эффективности ресинхронизирующей терапии (СРТ) для лечения пациентов с некомпактным миокардом левого желудочка (ЛЖ) и хронической сердечной недостаточностью.
Материал и методы. Проведено обсервационное ретроспективное исследование, включившее 26 пациентов с морфологической картиной некомпактной кардиомиопатии ЛЖ по данным эхокардиографии (ЭхоКГ) (выполнение критериев Chin, Jenni, Stollberger) и МРТ (выполнение критерия Petersen). Всем пациентам была выполнена имплантация CРТ. Динамика показателей размеров и функции ЛЖ оценивалась с помощью ЭхоКГ. Перед процедурой СРТ всем пациентам выполнялась МРТ сердца с контрастированием.
Результаты. По принципу наличия или отсутствия ответа на СРТ пациенты были разделены на 3 группы: ответчики (уменьшение конечно-диастолического объема (КДО) ЛЖ по данным ЭхоКГ от 15 до 30%, снижение функционального класса хронической сердечной недостаточности), супер-ответчики (уменьшение КДО ЛЖ более чем на 30%) и неответчики (невыполнение критериев ответа). В ходе исследования были выявлены факторы, влияющие на результаты СРТ, наиболее существенными из которых являлись семейная форма заболевания, пол и возраст пациентов, а также ряд параметров морфологии сердца: миокардиальный фиброз по данным МРТ, выраженность некомпактности миокарда, индексированный объем ЛЖ.
Заключение. МРТ является методикой, способной внести значимый вклад в прогнозирование эффективности СРТ у пациентов с некомпактный миокард ЛЖ и сердечной недостаточностью, поэтому данное исследование следует проводить всем пациентам перед проведением СРТ для оптимизации процедуры отбора и исключения пациентов, которым СРТ с большой вероятностью не принесет пользы.
Ключевые слова
Для цитирования:
Мершина Е.А., Филатова Д.А., Мясников Р.П., Куликова О.В., Мешков А.Н., Харлап М.С., Синицын В.Е. Роль магнитно-резонансной томографии в прогнозе эффективности ресинхронизирующей терапии для лечения пациентов с некомпактным миокардом левого желудочка и хронической сердечной недостаточностью. Российский кардиологический журнал. 2024;29(11):6150. https://doi.org/10.15829/1560-4071-2024-6150. EDN: IYEWIO
For citation:
Mershina E.A., Filatova D.A., Myasnikov R.P., Kulikova O.V., Meshkov A.N., Kharlap M.S., Sinitsyn V.E. Role of magnetic resonance imaging in predicting the efficiency of cardiac resynchronization therapy in patients with left ventricular non-compaction and heart failure. Russian Journal of Cardiology. 2024;29(11):6150. (In Russ.) https://doi.org/10.15829/1560-4071-2024-6150. EDN: IYEWIO
Некомпактный миокард левого желудочка (НМЛЖ) — это заболевание, вокруг которого продолжаются многочисленные дискуссии. В рекомендациях Европейского общества кардиологов по кардиомиопатиям (КМП) от 2023г НМЛЖ не был отнесен к отдельному типу КМП [1], однако это не умаляет вклад истинной некомпактности миокарда в течение и прогноз заболевания. Для НМЛЖ характерно наличие двух слоев миокарда левого желудочка (ЛЖ): нормального компактного и патологического некомпактного [2][3]. Одним из наиболее частых осложнений НМЛЖ является развитие хронической сердечной недостаточности (ХСН). Для коррекции электромеханической диссинхронии миокарда, возникающей у ряда пациентов с ХСН, с целью улучшения сократительной функции ЛЖ возможно применение сердечной ресинхронизирующей терапии (СРТ), однако ответ на нее наблюдается не всегда. Согласно действующим рекомендациям Европейского общества кардиологов 2021г [4], СРТ рекомендуется симптомным пациентам с ХСН (Нью-Йоркская ассоциация сердца (NYHA)) на синусовом ритме с фракцией выброса (ФВ) ЛЖ ≤35%, длительностью QRS ≥130 мс и морфологией QRS с блокадой левой ножки пучка Гиса, несмотря на оптимальную медикаментозную терапию. Эти критерии для имплантации СРТ рассматриваются также для пациентов с НМЛЖ. Показано, что СРТ улучшает сердечную функцию, симптомы и качество жизни пациентов, а также снижает смертность у пациентов с умеренной и тяжелой ХСН, однако следует отметить, что данные положительные эффекты достижимы только при правильном отборе пациентов.
Целью исследования была оценка роли магнитно-резонансной томографии (МРТ) в прогнозе эффективности ресинхронизирующей терапии для лечения пациентов с НМЛЖ и ХСН.
Материал и методы
Дизайн исследования. Обсервационное ретроспективное исследование проведено на базе регистра пациентов с НМЛЖ и их родственников первой и второй линий родства, который ведется на базе ФГБУ "Национальный медицинский исследовательский центр терапии и профилактической медицины" с 2013г по настоящее время и включает в себя 320 человек.
Все включенные в исследование пациенты подписали добровольное информированное согласие на участие в исследовании и обработку персональных данных.
Критерии включения в исследование: совершеннолетние пациенты, морфологическая картина изменений сердца которых соответствовала критериям НМЛЖ по данным выполненного эхокардиографического исследования (ЭхоКГ) (выполнение критериев Chin, Jenni, Stollberger [5]) и МРТ (выполнение критерия Petersen [6]); проведение СРТ.
Критерии невключения: возраст пациентов младше 18 лет, несоответствие критериям НМЛЖ по данным ЭхоКГ и МРТ.
Критерии исключения: выполнение МРТ по нестандартизированному протоколу сканирования или без контрастирования; отказ пациента от участия в исследовании.
Продолжительность исследования составила 8 лет 10 мес. (с декабря 2013г по октябрь 2022г).
Проведение ЭхоКГ. ЭхоКГ проводилась на системе Philips Epiq CVx (Нидерланды). Для диагностики НМЛЖ по данным ЭхоКГ использовались морфологические критерии Chin, Stöllberger, Jenni [5].
Проведение МРТ. Каждому пациенту из выборки была проведена МРТ сердца с внутривенным контрастированием гадолиний-содержащим контрастным препаратом (доза 0,15 мг/кг массы тела) на базе Университетской клиники МНОИ МГУ им. М. В. Ломоносова (томографы Avanto 1,5 Tесла и Vida 3 Tесла, Siemens Healthlineers, ФРГ) или Национального медицинского исследовательского центра терапии и профилактической медицины (томограф Signa 1,5 Тесла, GE Healthcare, США) с электрокардиографической синхронизацией. Использовалась поверхностная катушка для сердца.
Протокол МРТ со срезами толщиной 6 мм включал в себя следующие последовательности: срезы в аксиальной плоскости с "черной" и "белой" кровью для оценки анатомии сердца и крупных сосудов; кино-последовательности по длинной оси сердца в четырех- и двухкамерной проекциях на различных уровнях и по короткой оси сердца (толщина среза 6 мм); последовательности для определения отека миокарда (режимы STIR/TIRM) по длинной оси сердца в четырех- и двухкамерной проекциях (по 1 срезу) и по короткой оси сердца (3 среза на базальном, среднем и апикальном уровнях); последовательности для оценки отсроченного контрастирования миокарда, которые выполнялись через 15 мин после введения контрастного препарата (срезы по длинной оси сердца в четырех- и двухкамерной проекциях и по короткой оси (толщина среза 4-8 мм).
Расчет показателей объемов камер сердца, глобальной сократимости (ФВ), массы миокарда (ММ) и папиллярных мышц производился на базе программного обеспечения cvi42 (Circle Cardiovascular, США).
Для диагностики НМЛЖ по данным МРТ использовался морфологический критерий Petersen (соотношение толщины некомпактного слоя к толщине компактного ≥2,3). При подсчете результатов также учитывалось выполнение других МР-критериев некомпактности: Jacquier (соотношение массы некомпактного и компактного миокарда превышает 20%), Grothoff (соотношение толщины некомпактного и компактного миокарда превышает 3:1 в одном из сегментов 1-3, 7-16; соотношение толщины некомпактного и компактного слоев миокарда превышает 2:1 в сегментах 4-6; отношение массы папиллярных мышц к ММ превышает 25%, индексированная масса папиллярных мышц превышает 15 г/м²) [6].
Проведение СРТ. Всем включенным в исследование пациентам была проведена имплантация СРТ с функцией кардиовертера-дефибриллятора (Boston Scientific Endotak Reliance G, Boston Scientific Dynagen X4, Medtronic VIVA XT, St. Jude Medical Durata).
Показаниями к СРТ, согласно клиническим рекомендациям [4], являлись: ХСН II-IV функционального класса (ФК) по классификации NYHA; ФВ ЛЖ ≤35%; длительность QRS ≥130 мс.
Критерии ответа на СРТ. Критериями ответа на СРТ признавалось уменьшение конечно-диастолического объема (КДО) ЛЖ от 15 до 30% (что свидетельствует о ремоделировании миокарда ЛЖ), а также снижение ФК ХСН по NYHA >1. В случае уменьшения КДО ЛЖ более, чем на 30%, пациент считался супер-ответчиком. Таким образом, в зависимости от ответа на СРТ пациенты были поделены на 3 группы: ответчики, супер-ответчики и неответчики.
Семейная форма НМЛЖ. У некоторых пациентов из выборки имелась генетическая форма НМЛЖ, которая определялась наличием родственника первой линии с верифицированной мутацией в гене, предрасполагающей к развитию НМЛЖ.
Статистический анализ данных. Анализ полученных данных производился на базе статистического пакета JASP (версия 0.18.2, University of Amsterdam, Нидерланды). Непрерывные переменные представлены в виде средних ± стандартное отклонение и медиан с указанием межквартильного размаха. Для анализа данных применялись критерии хи-квадрат, Крускалла-Уоллиса, дисперсионный анализ ANOVA. Порог статистической значимости установлен на уровне р<0,05.
Результаты
Сопоставление групп ответчиков, супер-ответчиков и неответчиков по показателям морфологии и функции ЛЖ
В группу исследования были включены 26 пациентов; средний возраст составил 53,4±14,9 лет, медиана и межквартильный размах возраста составили 57 [ 41; 64] лет. Мужчин в выборке 11 человек (42,3%), женщин — 15 человек (57,7%).
Характеристика групп пациентов в зависимости от ответа на СРТ по полу и возрасту представлена в таблице 1.
Таблица 1
Пол и возраст пациентов в группах ответчиков, супер-ответчиков и неответчиков
|
Число |
Пол |
Возраст, лет, M±SD, |
||
|
Муж. |
Жен. |
|||
|
Ответчики |
4 |
1 (25,0%) |
3 (75,0%) |
65,6±1,1 65,4 [ 65,1; 65,8] |
|
Супер-ответчики |
14 |
6 (42,8%) |
8 (57,2%) |
57,9±12,2 60,1 [ 51,7; 63,5] |
|
Неответчики |
8 |
4 (50,0%) |
4 (50,0%) |
39,4±13,1 39,4 [ 29,1; 49,0] |
Между группами выявлены значимые различия по возрасту: более высокий возраст пациентов отмечался в группе ответчиков, меньший — в группе неответчиков (p=0,003), что показано на рисунке 1.
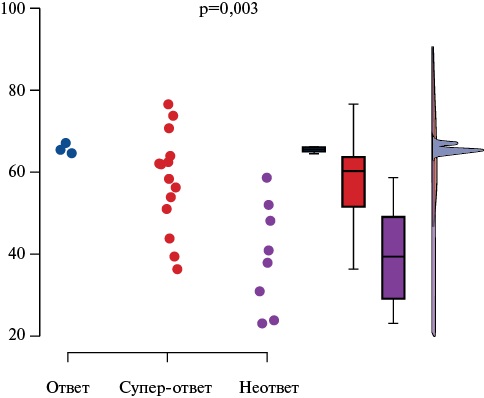
Рис. 1. Разница в возрасте у пациентов из групп ответа, супер-ответа и неответа на СРТ.
Всем пациентам из выборки проводилась МРТ сердца с контрастированием в период от 1 мес. до 1 года до имплантации водителя ритма. Значения основных параметров морфологии и функции ЛЖ по данным МРТ у пациентов из числа ответчиков, супер-ответчиков и неответчиков представлены в таблице 2.
Таблица 2
Параметры морфологии и функции ЛЖ по данным МРТ
|
Все пациенты |
Ответчики |
Супер-ответчики |
Неответчики |
|
|
ИКДО ЛЖ, мл/м² |
158,4±44,0 163,0 [ 122,5; 188,0] |
129,0±30,5 135,0 [ 113,8; 150,3] |
175,1±41,3 177,5 [ 159,5; 197,5] |
143,9±45,2 141,5 [ 104,8; 174,8] |
|
ИКСО ЛЖ, мл/м² |
120,2±41,9 116,5 [ 87,0; 149,3] |
98,8±22,1 98,5 [ 90,0; 107,3] |
135,4±40,8 122,5 [ 104,0; 166,0] |
104,3±44,3 96,5 [ 69,8; 138,0] |
|
ФВ ЛЖ, % |
25,6±9,6 23,0 [ 19,3; 31,7] |
22,5±5,7 20,0 [ 19,8; 22,8] |
23,8±8,8 23,0 [ 17,3; 27,0] |
30,4±11,4 31,5 [ 20,8; 38,3] |
|
ММ ЛЖ, г |
234,9±60,8 228,5 [ 180,8; 274,0] |
215,8±45,1 223,5 [ 204,3; 235,0] |
235,7±58,1 237,5 [ 198,8; 274,0] |
243,0±75,9 232,0 [ 176,5; 312,5] |
|
ИММ ЛЖ, г/м² |
122,2±30,3 117,5 [ 97,5; 145,3] |
106,3±22,6 102,0 [ 93,8; 114,5] |
126,8±33,6 119,5 [ 102,8; 151,3] |
122,3±27,8 117,0 [ 104,8; 143,8] |
|
ИМНМ, г/м² |
27,5±10,1 25,5 [ 19,0; 34,8] |
21,3±11,0 20,5 [ 15,0; 26,8] |
26,9±9,3 25,5 [ 19,0; 33,8] |
31,7±10,5 30,8 [ 24,0; 35,8] |
|
МНМ/ММ ЛЖ, % |
22,2±5,9 22,0 [ 18,3; 26,0] |
18,8±6,9 19,5 [ 15,3; 23,0] |
20,9±3,7 22,0 [ 18,3; 23,0] |
26,5±7,1 26,5 [ 23,0; 30,0] |
Сокращения: ИКДО — индексированный конечно-диастолический объем, ИКСО — индексированный конечно-систолический объем, ИММ — индексированная масса миокарда, ИМНМ — индексированная масса некомпактного миокарда, ЛЖ — левый желудочек, ММ — масса миокарда, МНМ — масса некомпактного миокарда, ФВ — фракция выброса.
Динамика состояния пациентов оценивалась с помощью ЭхоКГ: первое исследование проводилось до СРТ (в интервале от 1 мес. до 2 дней перед имплантацией устройства), второе — не менее, чем через 6 мес. после имплантации. Динамика показателей КДО ЛЖ и ФВ ЛЖ, а также ФК ХСН по NYHA показаны в таблице 3.
Таблица 3
Динамика состояния пациентов до и после СРТ по данным ЭхоКГ (показатели КДО ЛЖ и ФВ ЛЖ) и ФК ХСН по NYHА
|
Ответчики |
Супер-ответчики |
Неответчики |
||
|
КДО ЛЖ |
До СРТ |
206,3±163,2 209,0 [ 68,0; 347,3] |
310,6±87,2 312,5 [ 235,8; 366,0] |
229,5±91,5 220,0 [ 147,3; 297,3] |
|
После СРТ |
170,5±139,0 163,5 [ 54,0; 280,0] |
144,7±47,6 149,0 [ 103,8; 173,5] |
240,1±91,3 250,5 [ 151,0; 303,3] |
|
|
∆ |
19,1±5,9 21,1 [ 17,5; 22,7] |
52,3±13,6 53,9 [ 39,1; 64,3] |
-5,5±10,7 -3,0 [ -7,1; -0,5] |
|
|
ФВ ЛЖ |
До СРТ |
25,0±3,5 26,0 [ 24,5; 26,5] |
26,9±5,3 29,0 [ 23,5; 30,0] |
29,8±7,5 28,0 [ 27,5; 31,0] |
|
После СРТ |
38,3±18,5 43,0 [ 30,3; 51,0] |
46,1±8,2 48,0 [ 41,0; 51,8] |
27,5±7,7 27,5 [ 25,0; 29,8] |
|
|
∆ |
13,3±16,0 16,0 [ 4,3; 25,0] |
19,3±9,2 21,0 [ 15,0; 26,0] |
-2,3±10,1 -1,5 [ -10,0; 6,3] |
|
|
ФК по NYHA |
До СРТ |
II (50%), III (50%) |
II (42,8%), III (57,2%) |
II (62,5%), III (37,5%) |
|
После СРТ |
II (75%), III (25%) |
0 (14,3%), I (50,0%), II (35,7%) |
II (62,5%), III (25,0%), IV (12,5) |
Сокращения: КДО — конечно-диастолический объем, ЛЖ — левый желудочек, СРТ — сердечная ресинхронизирующая терапия, ФВ — фракция выброса, ФК — функциональный класс, NYHA — New York Heart Association.
При проведении анализа с использованием критерия Крускала-Уоллиса были выявлены значимые различия между группами ответчиков, супер-ответчиков и неответчиков по параметру соотношения массы папиллярных мышц к общей ММ ЛЖ: максимальное значение данного параметра выявлено в группе неответчиков (среднее значение 27%), минимальное значение — в группе ответчиков (среднее значение 17,5%) (p<0,05). При сопоставлении показателей индексированного КДО (ИКДО) ЛЖ, индексированного конечно-систолического объема ЛЖ, ФВ ЛЖ, ММ ЛЖ, индексированная ММ ЛЖ, индексированная масса папиллярных мышц ЛЖ между группами значимых различий выявлено не было. Результаты сопоставления представлены на рисунке 2.
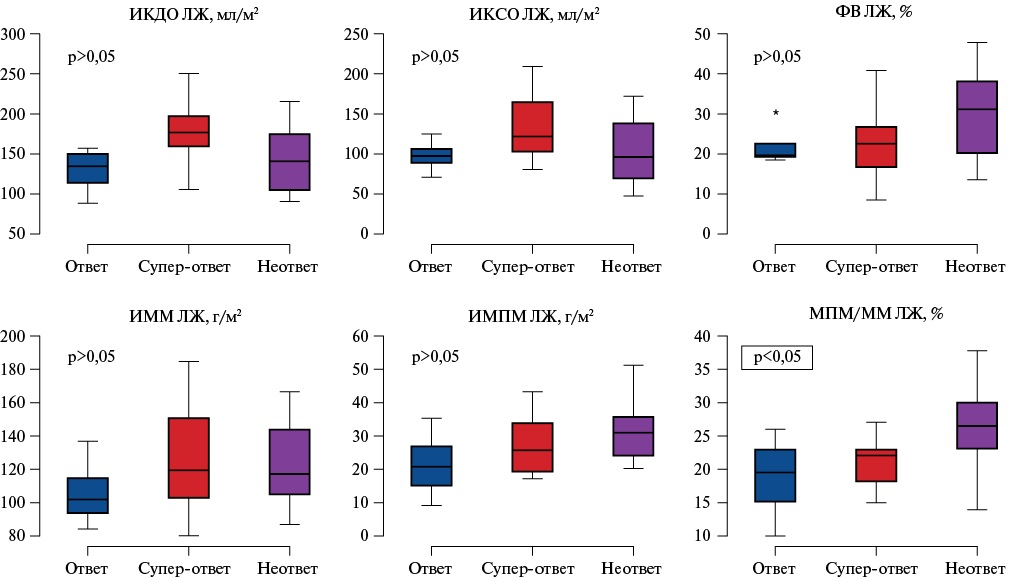
Рис. 2. Результаты сопоставления различных параметров по данным МРТ сердца между группами ответчиков, супер-ответчиков и неответчиков.
Сокращения: ИКДО — индексированный конечно-диастолический объем, ИКСО — индексированный конечно-систолический объем, ИММ — индексированная масса миокарда, ИМПМ — индексированная масса папиллярных мышц, ЛЖ — левый желудочек, ММ — масса миокарда, МПМ — масса папиллярных мышц, ФВ — фракция выброса.
Миокардиальный фиброз
У части пациентов по данным МРТ отмечался миокардиальный фиброз некоронарогенного характера (участки отсроченного контрастирования в миокарде ЛЖ имели субэпикардиальную и интрамуральную локализации). Выраженность миокардиального фиброза по числу вовлеченных сегментов у пациентов из групп ответа, супер-ответа и неответа показана в таблице 4.
Таблица 4
Характеристика миокардиального фиброза у пациентов из разных групп ответа на СРТ
|
Ответчики |
Супер-ответчики |
Неответчики |
||
|
Фиброза нет |
2 |
10 |
3 |
|
|
Фиброз есть |
Вовлечены ≤5 сегментов |
1 |
1 |
1 |
|
6-10 сегментов |
1 |
2 |
3 |
|
|
>10 сегментов |
0 |
1 |
1 |
|
При проведении анализа была выявлена значимая обратная взаимосвязь между повышением ФВ ЛЖ и наличием миокардиального фиброза (р=0,01) (рис. 3). Примечательно, что взаимосвязь между снижением ИКДО ЛЖ и наличием миокардиального фиброза не достигла статистической значимости.
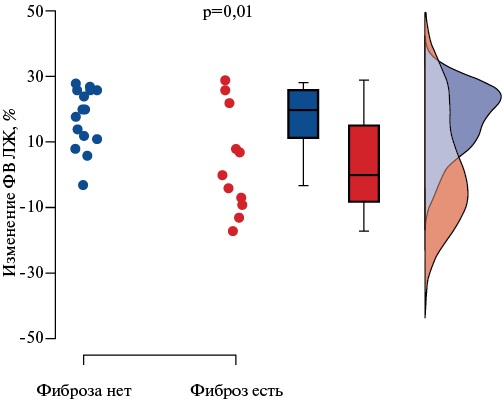
Рис. 3. Динамика ФВ ЛЖ у пациентов с миокардиальным фиброзом и без фиброза по данным МРТ.
Сокращение: ФВ ЛЖ — фракция выброса левого желудочка.
При анализе выраженности фиброза у пациентов из разных групп была выявлена значимая взаимосвязь между повышением ФВ ЛЖ и его наличием в более, чем 10 сегментах (р=0,01) (рис. 4). Связь повышения ФВ ЛЖ и умеренного миокардиального фиброза (<10 сегментов) не достигла статистической значимости.
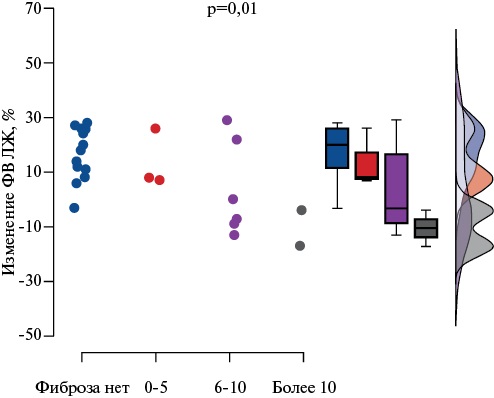
Рис. 4. Связь изменения ФВ ЛЖ (ось ординат) с наличием и выраженностью миокардиального фиброза по данным МРТ сердца (ось абсцисс).
Сокращение: ФВ ЛЖ — фракция выброса левого желудочка.
Примечательно, что наличие миокардиального фиброза и его выраженность не имели связи с выраженностью некомпактности миокарда: индексированной массой папиллярных мышц и соотношения их массы с общей ММ ЛЖ. Ожидаемо, не было выявлено взаимосвязи между наличием миокардиального фиброза и выполнением критериев некомпактности Jacquier и Grothoff. Тем не менее была обнаружена взаимосвязь между наличием миокардиального фиброза и ИКДО ЛЖ перед проведением СРТ (р=0,01): пациенты без миокардиального фиброза имели более высокие показали объема ЛЖ (рис. 5).
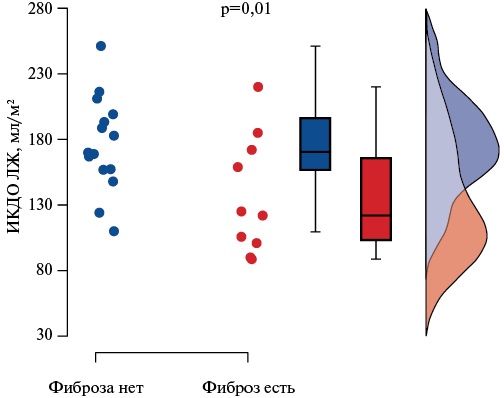
Рис. 5. Сопоставление значений ИКДО ЛЖ в группах пациентов с миокардиальным фиброзом по данным МРТ и без него.
Сокращение: ИКДО — индексированный конечно-диастолический объем.
Примеры пациентов с различной степенью выраженности миокардиального фиброза показаны на рисунке 6.
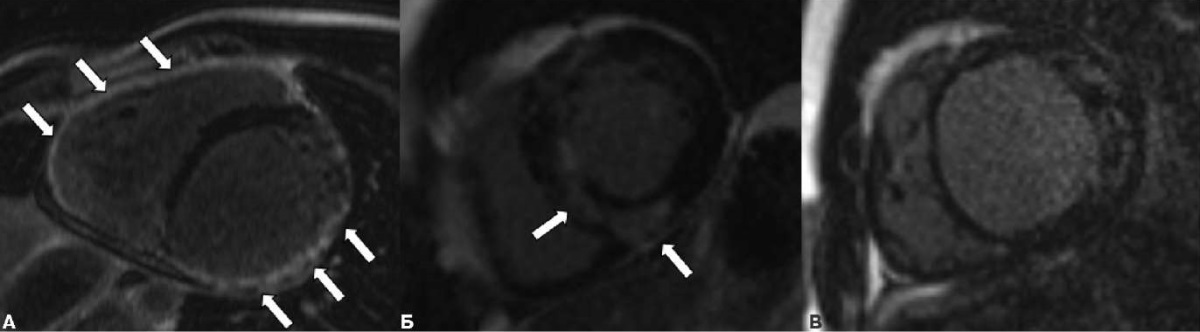
Рис. 6. Миокардиальный фиброз различной степени выраженности у пациентов с некомпактным миокардом и сердечной недостаточностью. А — мужчина, 23 года, группа неответа; Б — женщина, 31 год, группа неответа; В — мужчина, 22 года, группа ответа. Стрелками указаны участки миокардиального фиброза. МРТ, режим отсроченного контрастирования; проекция по короткой оси желудочков на уровне базальных сегментов.
Таким образом, наличие миокардиального фиброза явилось фактором, предрасполагающим к недостаточному ответу на СРТ, и эта закономерность имела связь с выраженностью фиброза. Пациенты без миокардиального фиброза имели большую выраженность дилатации ЛЖ, однако отвечали на СРТ лучше, чем пациенты с миокардиальным фиброзом.
Семейная форма НМЛЖ
В выборке присутствовало 8 пациентов с генетической формой НМЛЖ, распределение их по подгруппам показано в таблице 5.
Таблица 5
Количество пациентов с семейной формой НМЛЖ в каждой из подгрупп
|
Семейная форма |
Несемейная форма |
|
|
Ответчики |
0 |
4 |
|
Супер-ответчики |
2 |
12 |
|
Неответчики |
6 |
2 |
Анализ полученных данных, проведенный методом ANOVA, показал, что семейная форма заболевания являлась независимым фактором, ухудшавшим вероятность ответа на СРТ (р<0,01).
Сравнение групп с семейной и спорадической формами заболевания по основным МР-параметрам морфологии методом ANOVA показало, что у пациентов с семейной формой НМЛЖ отмечалась значимо большая индексированная масса папиллярных мышц ЛЖ и их процентное отношение к ММ ЛЖ (p=0,003) (рис. 7). У пациентов с семейной формой заболевания отмечалось значимо более частое выполнение критериев некомпактности Grothoff (р=0,01).
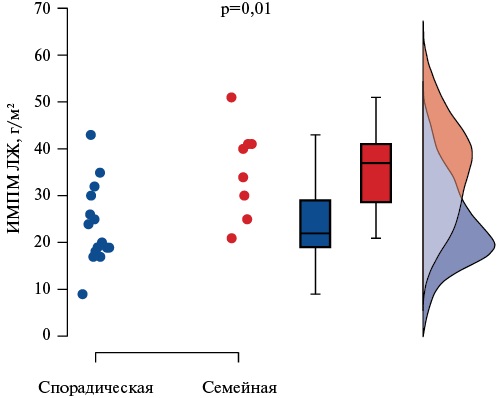
Рис. 7. Сопоставление параметров массы папиллярных мышц ЛЖ и процентного соотношения массы папиллярных мышц к ММ ЛЖ между группами с семейной и спорадической формами заболевания.
Сокращения: ИМПМ — индексированная масса папиллярных мышц, ЛЖ — левый желудочек.
Таким образом, у пациентов с семейной формой заболевания отмечались более выраженные признаки некомпактности миокарда и меньшая вероятность ответа на СРТ.
Долгосрочное наблюдение за пациентами после проведения СРТ
Динамика состояния пациентов, включенных в исследование, отслеживается до настоящего времени; у ряда пациентов из выборки произошли неблагоприятные сердечно-сосудистые события (прогрессирование ХСН, возникновение новых нарушений ритма сердца, тромбоэмболические события, трансплантация сердца, летальный исход). По состоянию на февраль 2024г четверо пациентов умерли от сердечно-сосудистых причин: один в группе ответчиков, один — в группе супер-ответчиков, двое — в группе неответчиков. Различия по количеству прочих неблагоприятных событий между группами пациентов не достигли статистической значимости.
Обсуждение
Проведенное исследование показало, что более часто отвечают на проведение СРТ пациенты с НМЛЖ старшего возраста, имеющие меньшую выраженность некомпактности (соотношение массы папиллярных мышц к общей ММ ЛЖ) и большие значения ИКДО ЛЖ.
Наличие миокардиального фиброза и его выраженность не имеют связи с выраженностью некомпактности миокарда. Тем не менее наличие миокардиального фиброза является важным предиктором отсутствия ответа на СРТ. Выявлено, что у пациентов с фиброзом исходный ИКДО ЛЖ был выше, чем у пациентов без фиброза, однако ответ на СРТ был хуже у пациентов с фиброзом. Выявлена значимая обратная взаимосвязь между повышением ФВ ЛЖ, наличием и выраженностью миокардиального фиброза; при этом обращает на себя внимание отсутствие значимой взаимосвязи между снижением ИКДО ЛЖ и наличием миокардиального фиброза.
Помимо миокардиального фиброза, предиктором плохого ответа на СРТ явилась семейная форма НМЛЖ: показано, что у таких пациентов отмечается значимо большая выраженность некомпактности и меньшая вероятность ответа на СРТ.
Стоит отметить, что в группах ответчиков и супер-ответчиков было больше женщин, чем мужчин (суммарно в двух названных группах 11 женщин и 8 мужчин), в то время как в группе неответчиков количество мужчин и женщин было равным. Это соотносится с литературными данными, свидетельствующими о более значимом улучшении систолической функции у женщин по сравнению с мужчинами [7].
Известно, что эффективность СРТ у пациентов с ХСН и нарушением внутрижелудочковой проводимости в отношении снижения количества госпитализаций и смертности по поводу ХСН доказана в случаях как ишемических, так и неишемических КМП [4], однако по показателям улучшения систолической функции ЛЖ и его обратного ремоделирования пациенты с неишемической КМП достигают лучших результатов по сравнению с пациентами с ишемической КМП [8-10]. В число неишемических КМП в упоминаемых исследованиях включались гипертрофическая, дилатационная, рестриктивная, аритмогенная КМП и НМЛЖ. В настоящем исследовании, включавшем только пациентов с НМЛЖ, подтверждено, что большинство пациентов с ХСН отвечают на СРТ: ответчики составили 69,2% от группы, при этом 77,8% ответчиков были супер-ответчиками. Схожие результаты можно встретить в литературе [11][12].
Одной из основных проблем, связанных с СРТ, является неполный ответ на нее у части пациентов с НМЛЖ. Как отмечалось ранее, ответ на ресинхронизирующую терапию во многом связан с критериями отбора пациентов.
В отношении определения групп пациентов, для которых СРТ наиболее эффективна, интерес представляет работа Bertini М, et al. [11], в которой сравнивалась эффективность СРТ между группами пациентов с дилатационной КМП (ДКМП) и изолированной НМЛЖ и с ДКМП без признаков НМЛЖ; было выявлено, что на ресинхронизирующую терапию лучше отвечают пациенты из первой группы. Предположительно, это связано с тем, что повышенная трабекулярность миокарда ЛЖ может являться отчасти компенсаторным механизмом, позволяющим увеличить кровоснабжение миокарда в условиях сниженной сократительной функции. Такие механизмы адаптации развиваются в течение длительного периода, т. е. должны чаще встречаться среди пациентов старшего возраста, что согласуется с данными, полученными в ходе настоящего исследования о том, что пациенты старшего возраста лучше отвечают на СРТ. Есть предположение, что перспектива ответа на СРТ лучше в случаях, когда повышенная трабекулярность хотя бы частично носит вторичный характер, т. е. является ответом миокарда на систолическую недостаточность, а не представляет собой первичный генетический фенотип. Ранее в литературе сообщалось, что сегменты, удовлетворяющие критериям некомпактности, у пациентов с ДКМП имеют лучшие показатели локальной сократимости по сравнению с сегментами без признаков некомпактности [13]. Таким образом, СРТ достигает лучших результатов у пациентов с вторичной природой повышенной трабекулярности. По-видимому, именно среди таких пациентов отмечается снижение выраженности некомпактности при динамическом наблюдении после проведения СРТ; об этом сообщали Bertini М, et al., Qui Q, et al., Stöllberger C, et al., при этом последние описали случай полного регресса некомпактности миокарда после СРТ у пациента с нейромышечным заболеванием [14].
Парадоксально на этом фоне выглядит полученный в данной работе результат о том, что среди ответчиков выраженность некомпактности миокарда (соотношение массы некомпактного миокарда к общей ММ) была меньше, чем среди неответчиков. Этот результат можно объяснить тем, что среди пациентов с наибольшей выраженностью некомпактности (11 пациентов с индексированной массой некомпактного миокарда >30 г/м²) в основном встречались молодые пациенты (средний возраст 46,0 лет), некомпактность у которых, более вероятно, носила первичный генетический характер и не являлась результатом длительной адаптации сердца к нарушениям гемодинамики. О последнем свидетельствует тот факт, что у 8 из 11 пациентов отмечалась семейная форма заболевания.
В литературе имеются сведения о предиктивной роли миокардиального фиброза у пациентов с наличием показаний к проведению СРТ [15-17], однако имеющиеся на сегодняшний день исследования недостаточно охватывают популяцию пациентов с НМЛЖ. Так, исследование Chen Zh, et al., включавшее пациентов с ишемической КМП, показало, что при наличии рубцовых изменений миокарда снижается вероятность обратного ремоделирования ЛЖ под влиянием СРТ [18]. Эти сведения были подтверждены в работе Duchenne J, et al., где большее число неответчиков на СРТ отмечалось среди пациентов с наличием рубцового поражения миокарда, а также была показана корреляция между выраженностью рубцового поражения ЛЖ в процентах и обратным ремоделированием миокарда ЛЖ [19]. Что касается неишемической КМП, наибольшее количество исследований посвящено изучению взаимосвязи миокардиального фиброза и исхода СРТ у пациентов с ДКМП. Так, исследование Song Y, et al. показало, что у пациентов с миокардиальным фиброзом вероятность развития неблагоприятных событий выше, чем у пациентов без фиброза [15]. Также у пациентов с фиброзом реже отмечалось обратное ремоделирование миокарда ЛЖ, а именно данный параметр является предиктором сердечно-сосудистых осложнений и смертности [20]. Примечательно, что у пациентов с ДКМП и фиброзом, а также у пациентов с ишемической КМП отмечалась схожая вероятность неблагоприятных исходов при длительном наблюдении. При отсутствии интрамиокардиального фиброза у пациентов с ДКМП вероятность неблагоприятных исходов была значимо ниже. В другом исследовании Ahmed W, et al., включавшем пациентов с ишемической и неишемической КМП, соотношение массы миокардиального фиброза к ММ ЛЖ >36,5% было ассоциировано с отсутствием ответа на СРТ с чувствительностью 81,8% и специфичностью 68,4%. Было выявлено, что локализация фиброза в заднелатеральной части ЛЖ, т. е. в зоне типичного расположения электродов при СРТ, вызывает дополнительное уменьшение вероятности ответа на терапию, а отсутствие фиброза в указанной локализации коррелировало с ответом на СРТ [21].
Также в литературе имеются сведения о том, что диффузный мелкоочаговый миокардиальный фиброз так же как и крупноочаговый может являться предиктором неблагоприятного исхода СРТ. В частности, исследование Höke U, et al. показало, что мелкоочаговый миокардиальный фиброз у пациентов с неишемической КМП, определенный с применением методики Т1-картирования, ассоциирован с меньшим обратным ремоделированием ЛЖ после СРТ [22]. Это может указывать на вероятные необратимые изменения миокарда ЛЖ на молекулярном уровне, которые не могут быть скорректированы проведением СРТ и требуют иных терапевтических подходов.
Полученные в ходе настоящего исследования результаты касательно роли миокардиального фиброза в определении вероятности ответа на СРТ во многом согласуются с более ранними литературными данными, что может расширить возможности использования метода МРТ при определении показаний к проведению СРТ. Важно, что выраженность диссинхронии желудочков (длительности QRS) была одинаковой у пациентов с фиброзом и без него, однако ответ на СРТ был хуже в группе пациентов с фиброзом. Это позволяет предположить, что влияние фиброза на обратное ремоделирование ЛЖ после проведения СРТ не зависит от диссинхронии и опосредовано иными механизмами. Миокардиальный фиброз замещает жизнеспособные миофибриллы, в результате чего снижается количество функциональных единиц миокарда, повышается жесткость сохранных участков миокарда и снижается сократительная способность желудочка.
В современных клинических рекомендациях по проведению СРТ среди значимых предикторов ответа на терапию обозначены длительность QRS, наличие блокады левой ножки пучка Гиса и ФВ ЛЖ ≤35%. Однако данные показатели не позволяют производить прецизионный отбор пациентов на СРТ [4]. Как показывают результаты настоящего исследования, использование методики МРТ может позволить увеличить эффективность отбора пациентов за счет выявления ряда факторов, ассоциированных с плохим или недостаточным ответом на терапию.
Ограничения исследования. Настоящее исследование имеет ограничения, которые необходимо учитывать при интерпретации результатов. Во-первых, оно было обсервационным и не включало группу контроля, составленную из пациентов, получавших только медикаментозное лечение. По этой причине невозможно достоверно установить, что пациенты с миокардиальным фиброзом не получают положительного эффекта от СРТ. Во-вторых, количество пациентов с миокардиальным фиброзом было относительно небольшим. В-третьих, не проводился анализ влияния выраженности и локализации миокардиального фиброза на эффективность СРТ. Также не учитывалось возможное наличие диффузного интрамиокардиального фиброза ввиду отсутствия в протоколе МР-сканирования последовательностей в режиме Т1-картирования.
Заключение
Таким образом, в ходе проведенного исследования была выявлена дополнительная роль МРТ в предсказании ответа на СРТ у пациентов НМЛЖ и ХСН. Было установлено, что такие параметры, полученные при анализе данных МРТ сердца, как миокардиальный фиброз, выраженность некомпактности миокарда и индексированный объем ЛЖ, могут предсказывать эффективность СРТ. На основании данной работы и предыдущих исследований можно предложить использовать данные МРТ в комплексном наборе параметров, применяемых для определения показаний к СРТ. Возможно, такая модификация критериев отбора приведет к снижению количества пациентов, которым СРТ не принесет пользы.
Отношения и деятельность: все авторы заявляют об отсутствии потенциального конфликта интересов, требующего раскрытия в данной статье.
Список литературы
1. Arbelo E, Protonotarios A, Gimeno JR, et al. 2023 ESC Guidelines for the management of cardiomyopathies. Eur Heart J. 2023;44(37):3503-626. doi:10.1093/eurheartj/ehad194.
2. Мершина Е. А., Мясников Р. П., Куликова О. В. и др. Некомпактная кардиомиопатия левого желудочка: особенности клинического течения и возможности диагностики. Рациональная Фармакотерапия В Кардиологии. 2015;11(6):638-42. doi:10.20996/1819-6446-2015-11-6-638-642.
3. Поляк М. Е., Мершина Е. А., Заклязьминская Е. В. Некомпактный миокард левого желудочка: симптом, синдром или вариант развития? Российский кардиологический журнал. 2017;(2):106-13. doi:10.15829/1560-4071-2017-2-106-113.
4. 2021 Рекомендации ESC по электрокардиостимуляции и сердечной ресинхронизирующей терапии. Российский кардиологический журнал. 2022;27(7):5159. doi:10.15829/1560-4071-2022-5159.
5. Towbin JA, Lorts A, Jefferies JL. Left ventricular non-compaction cardiomyopathy. Lancet. 2015;386(9995):813-25. doi:10.1016/S0140-6736(14)61282-4.
6. Куликова О. В., Мясников Р. П., Мершина Е. А. и др. Семейная форма некомпактной кардиомиопатии: типы ремоделирования миокарда, варианты клинического течения. Результаты многоцентрового регистра. Терапевтический архив. 2021;93(4):381-8. doi:10.26442/00403660.2021.04.200677.
7. Enina TN, Kuznetsov VA, Soldatova AM, et al. Gender in cardiac resynchronisation therapy. J Cardiovasc Thorac Res. 2018;10(4):197-202. doi:10.15171/jcvtr.2018.34.
8. Shanks M, Delgado V, Bax JJ. Cardiac Resynchronization Therapy in Non-Ischemic Cardiomyopathy. J Atr Fibrillation. 2016;8(5):1362. doi:10.4022/jafib.1362.
9. Sidhu K, Castrini AI, Parikh V, et al. The response to cardiac resynchronization therapy in LMNA cardiomyopathy. Eur J Heart Fail. 2022;24(4):685-93. doi:10.1002/ejhf.2463.
10. Yokoshiki H, Mitsuyama H, Watanabe M, et al. Cardiac resynchronization therapy in ischemic and non-ischemic cardiomyopathy. J Arrhythm. 2017;33(5):410-6. doi:10.1016/j.joa.2017.03.002.
11. Bertini M, Ziacchi M, Biffi M, et al. Effects of cardiac resynchronisation therapy on dilated cardiomyopathy with isolated ventricular non-compaction. Heart Br Card Soc. 2011;97(4):295-300. doi:10.1136/hrt.2010.211607.
12. Qiu Q, Chen YX, Mai JT, et al. Effects of cardiac resynchronization therapy on left ventricular remodeling and dyssynchrony in patients with left ventricular noncompaction and heart failure. Int J Cardiovasc Imaging. 2015;31(2):329-37. doi:10.1007/s10554-014-0568-8.
13. Lofiego C, Biagini E, Ferlito M, et al. Paradoxical contributions of non-compacted and compacted segments to global left ventricular dysfunction in isolated left ventricular noncompaction. Am J Cardiol. 2006;97(5):738-41. doi:10.1016/j.amjcard.2005.09.109.
14. Stöllberger C, Keller H, Finsterer J. Disappearance of left ventricular hypertrabeculation/noncompaction after biventricular pacing in a patient with polyneuropathy. J Card Fail. 2007;13(3):211-4. doi:10.1016/j.cardfail.2006.11.007.
15. Song Y, Chen X, Yang K, et al. Cardiac MRI-derived Myocardial Fibrosis and Ventricular Dyssynchrony Predict Response to Cardiac Resynchronization Therapy in Patients with Nonischemic Dilated Cardiomyopathy. Radiol Cardiothorac Imaging. 2023; 5(5):e220127. doi:10.1148/ryct.220127.
16. Nguyên UC, Claridge S, Vernooy K, et al. Relationship between vectorcardiographic QRS area, myocardial scar quantification, and response to cardiac resynchronization therapy. J Electrocardiol. 2018;51(3):457-63. doi:10.1016/j.jelectrocard.2018.01.009.
17. Beltrami M, Galluzzo A, Brocci RT, et al. The role of fibrosis, inflammation, and congestion biomarkers for outcome prediction in candidates to cardiac resynchronization therapy: is 'response' the right answer? Front Cardiovasc Med. 2023;10:1180960. doi:10.3389/fcvm.2023.1180960.
18. Chen Z, Ma X, Gao Y, et al. Cardiac magnetic resonance-derived myocardial scar is associated with echocardiographic response and clinical prognosis of left bundle branch area pacing for cardiac resynchronization therapy. Europace. 2023;25(11):euad326. doi:10.1093/europace/euad326.
19. Duchenne J, Larsen CK, Cvijic M, et al. Mechanical Dyssynchrony Combined with Septal Scarring Reliably Identifies Responders to Cardiac Resynchronization Therapy. J Clin Med. 2023;12(18):6108. doi:10.3390/jcm12186108.
20. Yu CM, Bleeker GB, Fung JWH, et al. Left ventricular reverse remodeling but not clinical improvement predicts long-term survival after cardiac resynchronization therapy. Circulation. 2005;112(11):1580-6. doi:10.1161/CIRCULATIONAHA.105.538272.
21. Ahmed W, Samy W, Tayeh O, et al. Left ventricular scar impact on left ventricular synchronization parameters and outcomes of cardiac resynchronization therapy. Int J Cardiol. 2016;222:665-70. doi:10.1016/j.ijcard.2016.07.158.
22. Höke U, Khidir MJH, van der Geest RJ, et al. Relation of Myocardial Contrast-Enhanced T1 Mapping by Cardiac Magnetic Resonance to Left Ventricular Reverse Remodeling After Cardiac Resynchronization Therapy in Patients With Nonischemic Cardiomyopathy. Am J Cardiol. 2017;119(9):1456-62. doi:10.1016/j.amjcard.2017.01.023.
Об авторах
Е. А. МершинаРоссия
Мершина Елена Александровна — к.м.н., доцент, в.н.с. отдела лучевой диагностики Университетской клиники медицинского научно-образовательного института (МНОИ); доцент кафедры лучевой диагностики и терапии.
Москва
Конфликт интересов:
Нет
Д. А Филатова
Россия
Филатова Дарья Андреевна — аспирант кафедры лучевой диагностики и терапии факультета фундаментальной медицины, врач-рентгенолог отделения рентгенодиагностики с кабинетами МРТ и КТ Университетской клиники МНОИ.
Москва
Конфликт интересов:
Нет
Р. П. Мясников
Россия
Мясников Роман Петрович — к.м.н., в.н.с. отдела клинической кардиологии, руководитель лаборатории персонализированной диагностики, профилактики и терапии некоронарогенных заболеваний сердца и сердечной недостаточности.
Москва
Конфликт интересов:
Нет
О. В. Куликова
Россия
Куликова Ольга Викторовна — к. м. н., с. н. с. отдела клинической кардиологии, лаборатории персонализированной диагностики, профилактики и терапии некоронарогенных заболеваний сердца и сердечной недостаточности.
Москва
Конфликт интересов:
Нет
А. Н. Мешков
Россия
Мешков Алексей Николаевич — д.м.н., руководитель института персонализированной терапии и профилактики.
Москва
Конфликт интересов:
Нет
М. С. Харлап
Россия
Харлап Мария Сергеевна — к.м.н., в.н.с. отдела нарушений ритма сердца и проводимости.
Москва
Конфликт интересов:
Нет
В. Е. Синицын
Россия
Синицын Валентин Евгеньевич — д.м.н., профессор, зав. отделом лучевой диагностики Университетской клиники МНОИ; зав. кафедрой лучевой диагностики и терапии факультета фундаментальной медицины.
Москва
Конфликт интересов:
Нет
Дополнительные файлы
Что известно о предмете исследования?
- Сердечная ресинхронизирующая терапия (СРТ) используется для лечения пациентов с сердечной недостаточностью и наличием нарушений проводимости сердца.
- Некомпактная кардиомиопатия левого желудочка (ЛЖ) проявляется сердечной недостаточностью, нарушениями ритма и проводимости сердца.
Что добавляют результаты исследования?
- Проведена оценка роли магнитно-резонансной томографии в прогнозе эффективности СРТ у пациентов с некомпактным миокардом ЛЖ.
- Выявлены факторы, влияющие на результаты СРТ: семейная форма заболевания, пол и возраст пациентов, миокардиальный фиброз, выраженность некомпактности миокарда, индексированный объем ЛЖ.
Рецензия
Для цитирования:
Мершина Е.А., Филатова Д.А., Мясников Р.П., Куликова О.В., Мешков А.Н., Харлап М.С., Синицын В.Е. Роль магнитно-резонансной томографии в прогнозе эффективности ресинхронизирующей терапии для лечения пациентов с некомпактным миокардом левого желудочка и хронической сердечной недостаточностью. Российский кардиологический журнал. 2024;29(11):6150. https://doi.org/10.15829/1560-4071-2024-6150. EDN: IYEWIO
For citation:
Mershina E.A., Filatova D.A., Myasnikov R.P., Kulikova O.V., Meshkov A.N., Kharlap M.S., Sinitsyn V.E. Role of magnetic resonance imaging in predicting the efficiency of cardiac resynchronization therapy in patients with left ventricular non-compaction and heart failure. Russian Journal of Cardiology. 2024;29(11):6150. (In Russ.) https://doi.org/10.15829/1560-4071-2024-6150. EDN: IYEWIO
JATS XML

















































