Перейти к:
Определение нуждаемости в паллиативной медицинской помощи пациентов с хронической сердечной недостаточностью в зависимости от состава тела
https://doi.org/10.15829/1560-4071-2025-6126
EDN: SZAESC
Аннотация
Цель. Определение потребности в паллиативной медицинской помощи (ПМП) пациентов с хронической сердечной недостаточностью (ХСН) в зависимости от состава тела.
Материал и методы. В исследовании приняли участие 298 человек (115 мужчин и 183 женщины, средний возраст — 61 [53;69] год), которые были разделены на 5 групп в зависимости от состава тела — наличия ожирения и саркопении. Определялись фракция выброса левого желудочка, значения маркеров N-концевого промозгового натрийуретического пептида (NT-proBNP) и галектина-3. Для оценки выживаемости проводился анализ методом КапланаМайера, для оценки влияния факторов — регрессия Кокса.
Результаты. При анализе потребности в ПМП у пациентов с ХСН в зависимости от состава тела установлено, что максимальные значения срока возникновения потребности в паллиативной помощи характерны для пациентов без нарушения состава тела, а минимальные — для пациентов с саркопеническим ожирением. По результатам регрессии Кокса выявлено статистически значимое увеличение отношения рисков возникновения показаний к ПМП при увеличении отношения индекса мышечной массы к индексу массы тела (ИММ/ИМТ) на 1 — в 22,9 раз (р<0,001), при увеличении ФК на 1 — в 1,99 раз (р<0,001), при увеличении уровня галектина на 1 нг/мл — в 1,02 раза (р=0,002), при снижении индекса Бартела на 1 — в 0,96 раз (р<0,001) и при наличии саркопении — в 3,71 раз (р<0,001).
Заключение. Состав тела пациентов с ХСН влияет на функциональную активность пациента, а значит и на потребность пациентов в оказании ПМП.
Ключевые слова
Для цитирования:
Шевцова В.И., Пашкова А.А., Красноруцкая О.Н. Определение нуждаемости в паллиативной медицинской помощи пациентов с хронической сердечной недостаточностью в зависимости от состава тела. Российский кардиологический журнал. 2025;30(3):6126. https://doi.org/10.15829/1560-4071-2025-6126. EDN: SZAESC
For citation:
Shevtsova V.I., Pashkova A.A., Krasnorutskaya O.N. Assessment of the need for palliative care in patients with heart failure depending on body composition. Russian Journal of Cardiology. 2025;30(3):6126. (In Russ.) https://doi.org/10.15829/1560-4071-2025-6126. EDN: SZAESC
Паллиативная медицинская помощь (ПМП) оказывается пациентам на терминальном этапе заболевания. В актуальной версии федерального закона об основах охраны здоровья граждан является отдельным видом медицинской помощи и представляет собой триаду — медицинские вмешательства, уход и психологическая поддержка1.
В мире в ПМП нуждается >40 млн человек, при этом структура нозологий представлена как онкологическими, так и соматическими заболеваниями [1].
В Российской Федерации (РФ) паллиативная медицина является молодым, развивающимся направлением медицины. При этом большая часть исследований потребности в ПМП проводилась на онкологических пациентах [2].
Однако пациенты с соматической патологией также нуждаются в этом виде медицинской помощи. С учетом распространённости сердечно-сосудистых заболеваний в РФ, пациенты с хронической сердечной недостаточностью (ХСН) представляют собой достаточно большой пул претендентов на оказание ПМП [3].
Согласно Приказу Минздрава России и Министерства труда и социальной защиты РФ 345н/372н от 31.05.2019 для определения нуждаемости в ПМП необходимо, чтобы заболевание пациента входило в группы нозологий. Далее для присвоения паллиативного статуса пациенту необходимо иметь не менее 2 из 3 общих показаний (ухудшение состояния, похудение на 10% за полгода, снижение функциональной активности). При наличии 2 общих показаний требуется оценка показаний по группам заболеваний. Для пациентов с ХСН такими показаниями будут являться 3-4 функциональный класс (ФК) заболевания, фракция выброса (ФВ) <25%, >3 госпитализаций за последний год.
Известно, что на функциональное состояние пациента влияет саркопения. Саркопения — заболевание поперечно-полосатой мускулатуры, при котором снижается мышечная сила, функция и масса [4]. Исследования показывают, что распространенность саркопении у пациентов с ХСН достаточно высока [5-7]. В связи с этим целью настоящего исследования было определение потребности в ПМП пациентов с ХСН в зависимости от состава тела.
Материал и методы
В поперечном описательном обсервационном исследовании приняли участие 298 человек (115 мужчин и 183 женщины, средний возраст — 61 [ 53;69] год), давшие согласие на участие в исследовании. Протокол и дизайн исследования одобрен локальным этическим комитетом ФГБОУ ВО ВГМУ им. Н. Н. Бурденко Минздрава России, все пациенты подписывали информированное согласие на участие в исследовании.
Критериями включения в исследования являлись: подтвержденная, согласно клиническим рекомендациям Минздрава России, ХСН, вследствие сердечно-сосудистых заболеваний и гипертонической болезни, отсутствие выраженных отеков. Критериями исключения были наличие у пациента ХСН другой этиологии, декомпенсированная ХСН, выраженный отечный синдром, невозможность пройти биоимпедансометрию.
С целью оценки состава тела всем пациентам было проведено анкетирование по опроснику SARC-F, выполнена кистевая динамометрия (с помощью электронного ручного медицинского динамометра ДМЭР-120-0,5), биоимпедансометрия (использовался анализатор Tanita BC-731), тест "скорость ходьбы на 4 м". Критерием диагностики саркопении являлись: >4 баллов по опроснику SARC-F, снижение скорости ходьбы <0,8 м/с, а также снижение мышечной массы по результатам проведения биоимпедансометрии. Критерием диагностики ожирения являлся индекс массы тела (ИМТ) ≥30 кг/м². Для определения клинического состояния пациента с ХСН и ФК была использована шкала, утвержденная клиническими рекомендациями и одобренная Минздравом России — шкала оценки клинического состояния (ШОКС), и тест с 6-минутной ходьбой, а также — измерение ФВ левого желудочка (ЛЖ) при помощи УЗИ-аппарата "Vivid E95" ("General Electric", США). Помимо этого, в группах проводилась оценка маркера N-концевого промозгового натрийуретического пептида (NT-proBNP). Показатели NT-proBNP определялись методом иммуноферментного анализа с помощью наборов ELISA Kit for NT-ProBNP (Cloud-Clone Corp., КНР).
Пациенты были разделены на 5 групп в зависимости от состава тела — наличия ожирения и саркопении. 1 группа: сниженная масса + саркопения (n=45); 2 группа: нормальная масса + саркопения (n=79); 3 группа: нормальная масса без саркопении (n=49); 4 группа: ожирение + саркопения (n=72); 5 группа: ожирение без саркопении (n=53).
В течение 4 лет проводилось динамическое ежеквартальное наблюдение за пациентами с оценкой точки нуждаемости в ПМП. Точка нуждаемости в ПМП — это время, когда у пациента регистрировались не менее 2 общих и не менее 1 частного показания к оказанию ПМП. В этом случае пациенту оформлялось медицинское заключение и присваивался статус паллиативного.
Накопление, корректировка, систематизация исходной информации и визуализация полученных результатов проводилась в электронных таблицах Microsoft Office Excell 2010. Статистический анализ проводился с помощью программы IBM SPSS Statistics 25.0. С целью определения целесообразности применения методов параметрического анализа, каждая из сравниваемых совокупностей оценивалась на предмет ее соответствия закону нормального распределения, для этого использовался критерий Колмогорова-Смирнова. Данные во всех группах, включенных в работу, имели распределение, отличное от нормального, поэтому материалы исследования были статистически обработаны с использованием методов непараметрического анализа. В качестве меры центральной тенденции указывалась медиана (Ме), а меры изменчивости — межквартильный интервал (Q1-Q3).
Для анализа половой структуры в различных группах использован точный критерий Фишера. Для оценки наличия статистически значимых различий между изучаемыми параметрами в 5 группах на каждом этапе использовался H-критерий Краскера-Уоллиса. При наличии значимых межгрупповых различий выполнялись апостериорные парные сравнения групп между собой попарно с помощью критерия Данна. Для снижения вероятности возникновения ошибок первого рода уровень значимости межгрупповых различий корректировался с учетом поправки Бонферрони для множественных сравнений.
Различия между группами считались статистически значимыми при p<0,05.
Для оценки выживаемости проводился анализ методом Каплана-Майера, для оценки влияния факторов — регрессия Кокса.
Результаты
Пациенты, принявшие участие в исследовании, в 100% случаях страдали гипертонической болезнью, у 75% была ишемическая болезнь сердца, 45% перенесли инфаркт миокарда. Все пациенты получали лечение согласно актуальным клиническим рекомендациям Министерства здравоохранения РФ, статистически значимых различий по принимаемой терапии выявлено не было. Клинико-демографическая характеристика пациентов представлена в таблице 1.
Таблица 1
Клинико-демографическая характеристика пациентов
|
Показатель |
Статистические показатели |
Группы наблюдений |
Уровень значимости различий (p) |
||||
|
1 (сниженная масса + саркопения) |
2 (нормальная масса + саркопения) |
3 (нормальная масса без саркопении) |
4 (ожирение + саркопения) |
5 (ожирение без саркопении) |
|||
|
Возраст, лет |
Ме |
60 |
61 |
65 |
59 |
59 |
0,369 |
|
Q1-Q3 |
53-69 |
54-68 |
53-71 |
52-66 |
51-67 |
||
|
ИМТ, кг/м² |
Ме |
16,7 |
26,6 |
24,9 |
33,2 |
33,5 |
<0,001* Р1-2<0,001* Р1-3<0,001* Р1-4<0,001* Р1-5<0,001* Р2-4<0,001* Р2-5<0,001* Р3-4<0,001* Р3-5<0,001* |
|
Q1-Q3 |
15,7-17,9 |
24,3-28,0 |
21,6-26,8 |
31,7-35,0 |
32,1-35,4 |
||
|
SARC-F, баллы |
Ме |
8 |
7 |
2 |
7 |
1 |
<0,001* Р1-3<0,001* Р1-5<0,001* Р2-3<0,001* Р2-5<0,001* Р3-4<0,001* Р4-5<0,001* |
|
Q1-Q3 |
6-9 |
5-9 |
1-2 |
5-8 |
1-2 |
||
|
Скорость ходьбы, м/с |
Ме |
0,4 |
0,3 |
1,6 |
0,4 |
1,5 |
<0,001* Р1-3<0,001* Р1-5<0,001* Р2-3<0,001* Р2-5<0,001* Р3-4<0,001* Р4-5<0,001* |
|
Q1-Q3 |
0,2-0,6 |
0,2-0,6 |
1,2-1,9 |
0,2-0,6 |
1,1-1,8 |
||
|
Динамометрия (среднее), кг |
Ме |
11 |
11 |
29 |
10 |
30 |
<0,001* Р1-3<0,001* Р1-5<0,001* Р2-3<0,001* Р2-5<0,001* Р3-4<0,001* Р4-5<0,001* |
|
Q1-Q3 |
8-15 |
8-14 |
23-33 |
7-14 |
24-37 |
||
|
ИММ/ИМТ |
Ме |
0,51 |
0,45 |
0,81 |
0,44 |
0,80 |
<0,001* Р1-3<0,001* Р1-5<0,001* Р2-3<0,001* Р2-5<0,001* Р3-4<0,001* Р4-5<0,001* |
|
Q1-Q3 |
0,41-0,59 |
0,34-0,50 |
0,69-0,87 |
0,37-0,52 |
0,67-0,84 |
||
|
Мышечная масса, % |
Ме |
20 |
15 |
25 |
17 |
26 |
<0,001* Р1-2=0,001* Р1-3=0,001* Р1-5<0,001* Р2-3<0,001* Р2-5<0,001* Р3-4<0,001* Р4-5<0,001* |
|
Q1-Q3 |
16-24 |
12-18 |
23-28 |
14-21 |
23-28 |
||
|
Фракция выброса левого желудочка, % |
Ме |
30 |
38 |
39 |
59,5 |
57 |
<0,001* Р1-2<0,001* Р1-3<0,001* Р1-4<0,001* Р1-5<0,001* Р2-4<0,001* Р2-5<0,001* Р3-4<0,001* Р3-5<0,001* |
|
Q1-Q3 |
27-36 |
37-45 |
37-49 |
53-64 |
52-61 |
||
|
ФК |
Ме |
3 |
3 |
2 |
3 |
3 |
<0,001* Р1-2<0,001* Р1-3<0,001* Р1-4<0,001* Р1-5<0,001* |
|
Q1-Q3 |
3-4 |
2-3 |
2-3 |
2-3 |
2-3 |
||
|
ТШХ, м |
Ме |
153 |
279 |
400 |
192 |
288 |
<0,001* Р1-2<0,001* Р1-3<0,001* Р1-4<0,001* Р1-5<0,001* Р2-3=0,006* Р2-4=0,032* Р3-4<0,001* Р3-5=0,046* Р4-5=0,027* |
|
Q1-Q3 |
68-170 |
226,5-380,5 |
285-413 |
159,5-319,5 |
267-369 |
||
|
NT-proBNP, пг/мл |
Ме |
2171 |
1282,5 |
1299,5 |
641,6 |
482,8 |
<0,001* Р1-2=0,009* Р1-3=0,048* Р1-4<0,001* Р1-5<0,001* Р2-4<0,001* Р2-5<0,001* Р3-4<0,001* Р3-5<0,001* |
|
Q1-Q3 |
1206,2-2605 |
707,05-2015,1 |
657,3-2038,6 |
394,75-890,95 |
386,6-642,8 |
||
|
Индекс Бартела, баллы |
Ме |
32 |
60 |
52 |
34,5 |
36 |
<0,001* Р1-2<0,001* Р1-3<0,001* Р2-4<0,001* Р2-5<0,001* Р3-4<0,001* Р3-5<0,001* |
|
Q1-Q3 |
21-41 |
51-68,5 |
44-62 |
28-40 |
28-44 |
||
Примечание: * — различия между группами статистически значимы при p<0,05.
Сокращения: ИММ/ИМТ — отношение индекса мышечной массы к индексу массы тела, ИМТ — индекс массы тела, ТШХ — тест 6-минутной ходьбы, ФК — функциональный класс, NT-proBNP — N-концевой промозговой натрийуретический пептид.
На первом этапе оценивался срок возникновения так называемой точки нуждаемости в ПМП.
Определялась вероятность того, что показания к ПМП не возникнут в течение срока наблюдения (табл. 2). Для пациентов первой группы анализ не проводился, поскольку они нуждались в ПМП на момент начала наблюдения.
Таблица 2
Вероятность возникновения необходимости в ПМП в течение 4 лет с момента начала наблюдения
|
Временной интервал, мес. |
Число пациентов, оставшихся под наблюдением к началу интервала (которым пока не понадобилась ПМП) |
Число пациентов, выбывших в течение интервала |
Риск наступления конечной точки (необходимости в ПМП) |
Безрецидивная выживаемость (вероятность, что к концу периода ПМП не понадобится) |
|
|
Абс. |
% |
||||
|
У всех пациентов |
|||||
|
В момент начала наблюдения |
298 |
119 |
119 |
39,9 |
60,1 |
|
42-45 |
23 |
1 |
276 |
92,6 |
7,4 |
|
≥45 |
22 |
наблюдение прекращено |
|||
|
У пациентов без саркопении |
|||||
|
В момент начала наблюдения |
102 |
33 |
33 |
32,4 |
67,6 |
|
42-45 |
15 |
1 |
88 |
86,3 |
13,7 |
|
≥45 |
14 |
наблюдение прекращено |
|||
|
У пациентов с саркопенией |
|||||
|
В момент начала наблюдения |
196 |
86 |
86 |
43,9 |
56,1 |
|
42-45 |
8 |
0 |
188 |
95,9 |
4,1 |
|
≥45 |
8 |
наблюдение прекращено |
|||
|
2 группа (пациенты с саркопенией и нормальной массой тела) |
|||||
|
В момент начала наблюдения |
79 |
0 |
0 |
0,0 |
100,0 |
|
42-45 |
5 |
0 |
74 |
93,7 |
6,3 |
|
≥45 |
5 |
наблюдение прекращено |
|||
|
3 группа (пациенты без саркопении и нормальной массой тела) |
|||||
|
В момент начала наблюдения |
49 |
0 |
86 |
0,0 |
100,0 |
|
42-45 |
14 |
1 |
188 |
73,5 |
26,5 |
|
≥45 |
13 |
наблюдение прекращено |
|||
|
4 группа (пациенты с саркопеническим ожирением) |
|||||
|
В момент начала наблюдения |
72 |
41 |
41 |
56,9 |
43,1 |
|
42-45 |
3 |
0 |
69 |
95,8 |
4,2 |
|
≥45 |
3 |
наблюдение прекращено |
|||
|
5 группа (пациенты без саркопении и ожирением) |
|||||
|
В момент начала наблюдения |
53 |
33 |
33 |
62,3 |
37,7 |
|
42-45 |
1 |
0 |
52 |
98,1 |
1,9 |
|
≥45 |
1 |
наблюдение прекращено |
|||
Сокращение: ПМП — паллиативная медицинская помощь.
На втором этапе оценивали зависимость доли пациентов, у которых ожидается появление показаний к ПМП, в зависимости от длительности наблюдения. При выполнении анализа с помощью метода Каплана-Майера из расчета были исключены пациенты, которые сразу же имели показания к ПМП. Аналогично первому этапу анализ не проводился для пациентов первой группы. Срок наступления показаний представлен в таблице 3.
Таблица 3
Срок наступления показания к ПМП в зависимости от состава тела
|
Группа |
Количество пациентов |
Медиана срока наступления показаний к ПМП |
Среднее время наступления показаний к ПМП |
|
Все пациенты |
179 |
19,0±0,9 мес. (95% ДИ: 17,3-20,7) |
22,1±0,9 мес. (95% ДИ: 20,3-23,9) |
|
Пациенты без саркопении |
69 |
25,0±1,6 мес. (95% ДИ: 22,0-28,1) |
27,9±1,4 мес. (95% ДИ: 25,2-30,6) |
|
Пациенты с саркопенией |
110 |
17,0±0,9 мес. (95% ДИ: 15,3-18,7) |
18,5±1,1 мес. (95% ДИ: 16,4-20,6) |
|
2 группа (пациенты с саркопенией с нормальной массой тела) |
79 |
18,0±1,0 мес. от начала наблюдения (95% ДИ: 16-20) |
20,2±1,2 мес. (95% ДИ: 17,9-22,5) |
|
3 группа (пациенты без саркопении и нормальной массой тела) |
49 |
28,0±2,8 мес. (95% ДИ: 22,5-33,5) |
30,1±1,7 мес. (95% ДИ: 26,9-33,4) |
|
4 группа (пациенты с саркопеническим ожирением) |
31 |
11,0±3,2 мес. (95% ДИ: 4,8-17,2) |
14,2±2,2 мес. (95% ДИ: 9,8-18,5) |
|
5 группа (пациенты с ожирением и без саркопении) |
20 |
20,0±0,7 мес. (95% ДИ: 18,6-21,4) |
22,1±0,9 мес. (95% ДИ: 20,3-23,9) |
Сокращения: ДИ — доверительный интервал, ПМП — паллиативная медицинская помощь.
На рисунках 1 и 2 представлены кривые Каплан-Майера для пациентов в зависимости от наличия саркопении и по группам.
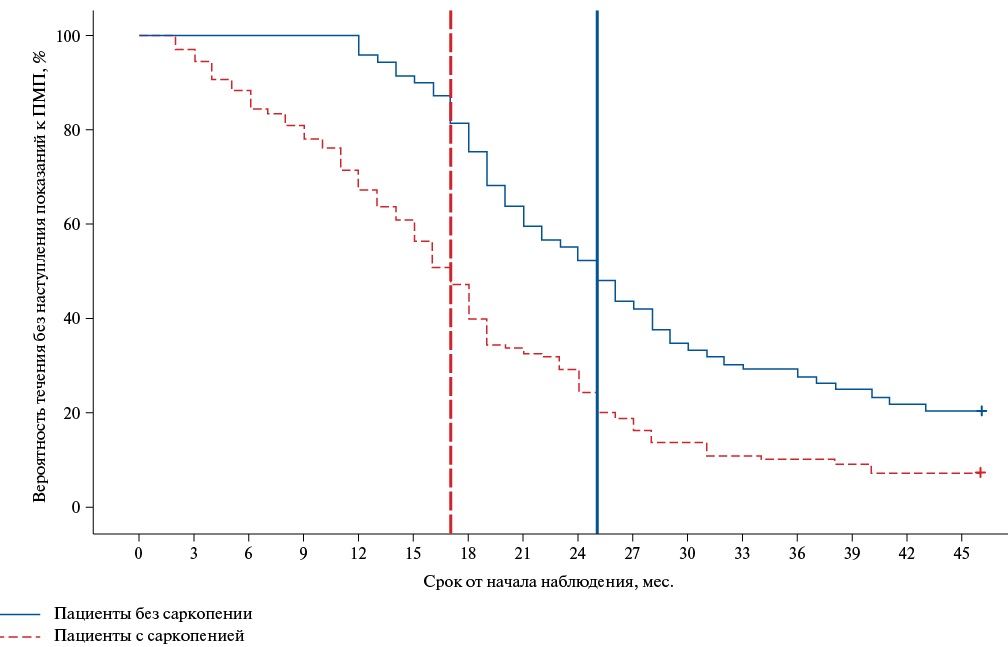
Рис. 1. Кривая Каплана-Мейера в зависимости от наличия саркопении.
Сокращение: ПМП — паллиативная медицинская помощь.
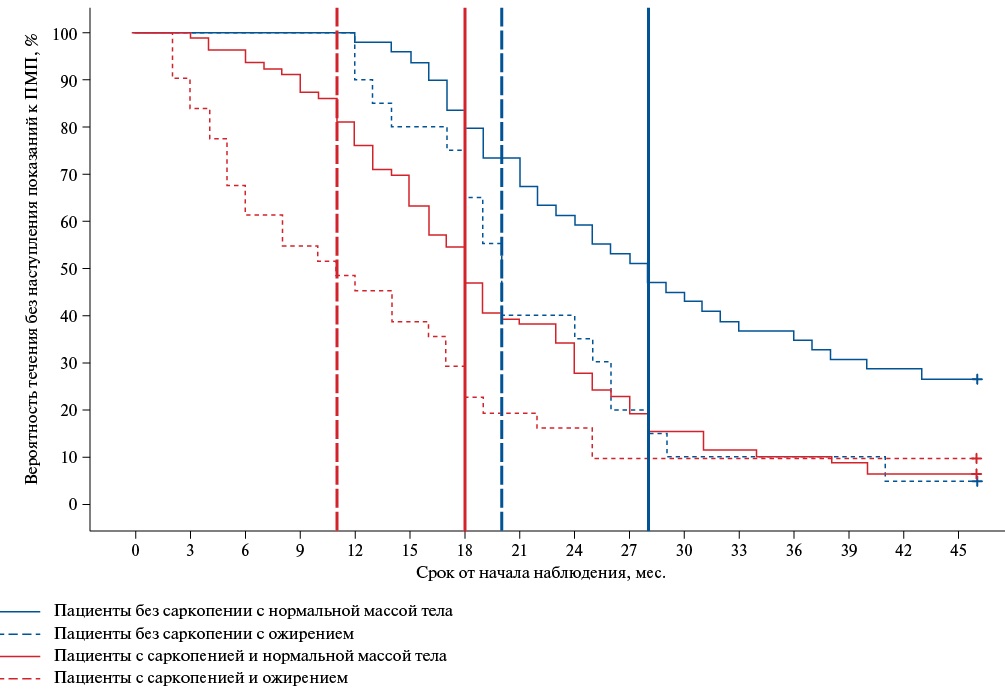
Рис. 2. Кривая Каплана-Мейера для пациентов с разным составом тела.
Сокращение: ПМП — паллиативная медицинская помощь.
На третьем этапе была проведена оценка зависимости изменений вероятности наступления показаний к ПМП от изучаемых в работе параметров.
При оценке комплексного влияния факторов на риск возникновения показаний к ПМП с помощью метода регрессии Кокса была получена следующая модель пропорциональных рисков:
hi(t)=h0(t)*exp(3,133*Х1+0,686*Х2+0,024*Х3-0,044*Х4+1,311*Х5),
где hi(t) — прогнозируемый риск наступления точки нуждаемости в ПМП для i-го пациента за определенный период времени (в %), h0(t) — базовый риск наступления точки нуждаемости в ПМП за определённый временной период t (в %), Х1 — индекс мышечной массы (ИММ)/ИМТ, %, Х2 — ФК, Х3 — уровень галектина, нг/мл, Х4 — индекс Бартела, баллы, Х5 — наличие саркопении (0 — нет, 1 — есть).
Модель была статистически значимой (p<0,001).
Значения базового риска наступления точки нуждаемости в ПМП для разных временных периодов наблюдения представлены в таблице 4.
Таблица 4
Значение базового риска наступления точки нуждаемости в ПМП для разных временных периодов (максимальный срок — 45 мес.)
|
Временные периоды, мес. |
Значение базового риска h0(t) |
|
3 |
2,3 |
|
6 |
2,8 |
|
9 |
3,1 |
|
12 |
3,8 |
|
15 |
4,6 |
|
18 |
6,4 |
|
21 |
8,1 |
|
24 |
9,6 |
|
27 |
12,1 |
|
30 |
13,9 |
|
33 |
15,5 |
|
36 |
16,1 |
|
38 |
17,1 |
|
42 |
18,6 |
|
45 |
19,0 |
Изменение рисков наступления точки нуждаемости в ПМП в зависимости от увеличения значения фактора указано в таблице 5.
Таблица 5
Изменение вероятности возникновения показаний к ПМП в зависимости от влияния показателей, изучаемых в работе
|
Фактор риска |
Изменение рисков при наличии фактора или при увеличении его на 1 ед. |
р |
|
|
Отношение рисков |
95% доверительный интервал |
||
|
ИММ/ИМТ |
22,946 |
7,145-73,691 |
<0,001* |
|
ФК |
1,986 |
1,642-2,4 |
<0,001* |
|
Уровень галектина |
1,024 |
1,008-1,04 |
0,002 |
|
Индекс Бартела |
0,957 |
0,947-0,967 |
<0,001* |
|
Наличие саркопении |
3,710 |
2,337-5,89 |
<0,001* |
Примечание: * — влияние фактора статистически значимо.
Сокращения: ИММ/ИМТ — отношение индекса мышечной массы к индексу массы тела, ФК — функциональный класс.
В соответствии с результатами проведённого анализа, отмечалось статистически значимое увеличение отношения рисков возникновения показаний к ПМП при увеличении ИММ/ИМТ на 1 — в 22,9 раз (р<0,001), при увеличении ФК на 1 — в 1,99 раз (р<0,001), при увеличении уровня галектина на 1 нг/мл — в 1,02 раза (р=0,002), при снижении индекса Бартела на 1 — в 0,96 раз (р<0,001) и при наличии саркопении — в 3,71 раз (р<0,001).
Обсуждение
ХСН является исходом сердечно-сосудистой патологии, которой в настоящий момент отводится первое место среди причин смертности населения. РФ относится к странам с высокой распространенностью сердечно-сосудистых заболеваний [3]. В настоящий момент ХСН встречается у 7% популяции [8]. В связи с этим вопрос потребности пациентов с ХСН в оказании ПМП является актуальным. Однако, несмотря на это, исследования, посвященные аспектам оказания ПМП пациентам с ХСН, единичны [9].
Согласно Положению об организации оказания ПМП, снижение функциональной активности пациента является показанием к оказанию ПМП. Саркопения определяет функциональную активность пациента, в связи с чем в настоящей работе рассмотрен вопрос прогнозирования возникновения точки нуждаемости в ПМП в зависимости от состава тела пациентов. Определено, что без саркопении без рецидивная выживаемость (т. е. потребность в ПМП) пациентов в 4 раза меньше по сравнению с пациентами с саркопенией. При анализе потребности в ПМП у пациентов с ХСН в зависимости от состава тела установлено, что максимальные значения без рецидивной выживаемости характерны для пациентов без нарушения состава тела — с нормальной массой тела и без саркопении. В то же время минимальный показатель характерен для пациентов с саркопеническим ожирением (СОж). При оценке срока наступления показаний к оказанию ПМП вызывают интерес также минимальные значения в группе пациентов с СОж. Следует отметить, что для пациентов с СОж характерны более высокие показатели ФВ ЛЖ, соответствующие ХСН с сохраненной ФВ (ХСНсФВ). ХСНсФВ — фенотип ХСН, характерный для пациентов пожилого возраста и встречающийся чаще у женщин [10]. Таким образом, можно прогнозировать более высокую потребность в ПМП у пациентов с ХСНсФВ.
При этом обращает на себя внимание факт, что в нашем исследовании пациенты с ХСНнФВ имели лучший прогноз, а параметр ФВ ЛЖ не был включен в прогностическую модель. Мы предлагаем связать это с ограничениями исследования — в исследуемой выборке не было пациентов с ФВ ЛЖ <25%, а именно это значение является показанием к ПМП согласно актуальной нормативной базе. Рубаненко О. А. и др. изучались пациенты ХСН III-IV ФК, удовлетворяющие критериям включения в программу оказания паллиативной помощи [11]. Авторы получили схожие с нашими результаты: ХСНнФВ встречалась менее, чем у 40% исследуемых. Shiga T, et al. изучили 1245 пациентов с ХСН, из которых ФВ ЛЖ была <40% только у 36% исследуемых [12]. Авторы указывают на отсутствие значимых различий в показателях смертности в группах пациентов с разной ФВ ЛЖ. Подобные результаты требуют дальнейшего изучения пациентов с фенотипом ХСНсФВ.
При оценке комплексного влияния факторов на риск возникновения показаний к ПМП в модель пропорциональных рисков вошли следующие параметры: ИММ/ИМТ, %, ФК, уровень галектина, индекс Бартела, а также наличие саркопении. Следует отметить, что ФК и индекс Бартела являются факторами, определяющими потребность в ПМП. Уровень галектина изучен в предыдущих работах [13]. Определены статистически значимые различия в уровне маркера галектина у пациентов с разным составом тела, определяющие различное течение ХСН.
При этом в модель вошли 2 параметра, определяющих состав тела — индекс ИММ/ИМТ и наличие саркопении. Показано, что наличие саркопении почти в 4 раза увеличивает вероятность наступления показаний к ПМП у пациентов с ХСН.
В работах Драпкиной О. М., Гуляева Н. И., Микаелян А. А. показано, что саркопения отягощает течение ХСН и ассоциирована с ухудшением прогноза таких пациентов [5][14][15].
Ограничениями исследования является малый размер выборки пациентов, что требует увеличения количества респондентов в дальнейших исследованиях. Включение только пациентов вне декомпенсации сердечной недостаточности не позволяет экстраполировать полученные данные на всю популяцию лиц с ХСН. Ограничение периода наблюдения не позволяет сделать окончательные выводы по вопросу перехода к ПМП у пациентов с ХСН.
Заключение
Потребность в ПМП пациентов без саркопении в 4 раза меньше по сравнению с пациентами с саркопенией. При этом максимальные значения без рецидивной выживаемости характерны для пациентов без нарушения состава тела, а минимальный показатель характерен для пациентов с СОж.
При оценке комплексного влияния факторов на риск возникновения показаний к ПМП в модель пропорциональных рисков вошли следующие параметры: ИММ/ИМТ, ФК, уровень галектина, индекс Бартела, а также наличие саркопении.
Таким образом, состав тела пациентов с ХСН следует учитывать при прогнозировании течения заболевания и потребности пациентов в оказании ПМП. Полученная в ходе исследования модель может послужить основой для инструмента принятия врачебных решений и определения тактики ведения пациентов с ХСН.
Отношения и деятельность: все авторы заявляют об отсутствии потенциального конфликта интересов, требующего раскрытия в данной статье.
1. Федеральный закон Российской Федерации от 21 ноября 2011г № 323-ФЗ "Об основах охраны здоровья граждан в Российской Федерации".
Список литературы
1. Рашид М. А., Новиков Г. А., Вайсман М. А. и др. Паллиативная медицинская помощь при хронической сердечной недостаточности: актуальность, задачи и проблемы. Паллиативная медицина и реабилитация. 2022;3:14-24.
2. Новиков Г. А., Введенская Е. С., Зеленова О. В. и др. Результаты первого в России эпидемиологического исследования потребности онкологических пациентов в паллиативной медицинской помощи и оценка эффективности и безопасности методов диагностики патологических симптомов. Паллиативная медицина и реабилитация. 2018;4:5-10.
3. Бойцов С. А., Драпкина О. М., Шляхто Е. В. и др. Исследование ЭССЕ-РФ (Эпидемиология сердечно-сосудистых заболеваний и их факторов риска в регионах Российской Федерации). Десять лет спустя. Кардиоваскулярная терапия и профилактика. 2021;20(5):3007. doi: 10.15829/1728-8800-2021-3007.
4. Григорьева И. И., Раскина Т. А., Летаева М. В. и др. Саркопения: особенности патогенеза и диагностики. Фундаментальная и клиническая медицина. 2019;4(4):105-16. doi: 10.23946/2500-0764-2019-4-4-105-116.
5. Микаелян А. А., Вараева Ю. Р., Лискова Ю. В. и др. Саркопения и хроническая сердечная недостаточность. Часть 1. Лечебное дело. 2023;2:51-6. doi: 10.24412/2071-5315-2023-12879. EDN LRAULA.
6. Formiga F, Moreno-Gónzalez R, Corsonello A, et al.; SCOPE Investigators. Prevalence of Sarcopenia in Chronic Heart Failure and Modulating Role of Chronic Kidney Disease. Gerontology. 2024;70(5):507-16. doi: 10.1159/000536465.
7. Kılıç R, Güzel T, Aktan A, et al. Prevalence of sarcopenia in heart failure with mildly reduced ejection fraction and its impact on clinical outcomes. Acta Cardiol. 2024:1-9. doi: 10.1080/00015385.2024.2410604.
8. Поляков Д.С., Фомин И.В., Беленков Ю.Н. и др. Хроническая сердечная недостаточность в Российской Федерации: что изменилось за 20 лет наблюдения? Результаты исследования ЭПОХА-ХСН. Кардиология. 2021;61(4):4-14. doi: 10.18087/cardio.2021.4.n1628.
9. Ларина В. Н., Чукаева И. И., Ларин В. Г. Современные тенденции и возможности оказания паллиативной медицинской помощи при хронической сердечной недостаточности. Кардиология. 2019;59(1):84-92. doi: 10.18087/cardio.2019.1.10219.
10. Сережина Е. К., Обрезан А. Г. Особенности фенотипирования пациентов с сердечной недостаточностью с сохраненной фракцией выброса. Российский кардиологический журнал. 2023;28(3S):5348. doi: 10.15829/1560-4071-2023-5348. EDN ONOGLD.
11. Рубаненко О. А., Скрипник И. В., Матюхина К. В. и др. Короткий регистр тяжелых форм хронической сердечной недостаточности в Самарской области. Кардиология. 2024;64(3):46-54.
12. Shiga T, Suzuki A, Haruta S. Clinical characteristics of hospitalized heart failure patients with preserved, mid-range, and reduced ejection fractions in Japan. ESC Heart Fail. 2019;6(3):475-86. doi: 10.1002/ehf2.12418.
13. Шевцова В. И., Пашкова А. А., Колпачева М. Г. и др. Уровень биомаркера галектин-3 у пациентов с хронической сердечной недостаточностью. Научно-медицинский вестник Центрального Черноземья. 2024; 96:75-81.
14. Драпкина О. М., Скрипникова И. А., Яралиева Э. К. и др. Состав тела у пациентов с хронической сердечной недостаточностью. Кардиоваскулярная терапия и профилактика. 2022;21(12):3451. doi: 10.15829/1728-8800-2022-3451.
15. Гуляев Н. И., Адамов А. А., Ахметшин И. М. Влияние саркопении на течение и прогноз у пациентов с хронической сердечной недостаточностью. Медико-фармацевтический журнал "Пульс". 2023;25(2):124-33.
Об авторах
В. И. ШевцоваРоссия
к.м.н., доцент, доцент кафедры инфекционных болезней
и клинической иммунологии
Воронеж
Конфликт интересов:
нет
А. А. Пашкова
д.м.н., профессор, проректор по учебной работе, зав. кафедрой поликлинической терапии
Воронеж
Конфликт интересов:
нет
О. Н. Красноруцкая
д.м.н., доцент, зав. кафедрой инфекционных болезней и клинической иммунологии
Воронеж
Конфликт интересов:
нет
Дополнительные файлы
- Нарушения состава тела влияют на потребность пациентов с хронической сердечной недостаточностью в паллиативной медицинской помощи; у пациентов без саркопении она в 4 раза меньше по сравнению с пациентами с саркопенией.
- Отношение индекса мышечной массы к индексу массы тела, функциональный класс, уровень галектина, индекс Бартела, а также наличие саркопении вошли в модель пропорциональных рисков возникновения показаний к паллиативной медицинской помощи.
Рецензия
Для цитирования:
Шевцова В.И., Пашкова А.А., Красноруцкая О.Н. Определение нуждаемости в паллиативной медицинской помощи пациентов с хронической сердечной недостаточностью в зависимости от состава тела. Российский кардиологический журнал. 2025;30(3):6126. https://doi.org/10.15829/1560-4071-2025-6126. EDN: SZAESC
For citation:
Shevtsova V.I., Pashkova A.A., Krasnorutskaya O.N. Assessment of the need for palliative care in patients with heart failure depending on body composition. Russian Journal of Cardiology. 2025;30(3):6126. (In Russ.) https://doi.org/10.15829/1560-4071-2025-6126. EDN: SZAESC
JATS XML

















































