Перейти к:
Прогностическое значение нового индекса жесткости артерий START у пациентов с ишемической болезнью сердца после коронарного шунтирования
https://doi.org/10.15829/1560-4071-2024-5952
EDN: XPBYYL
Аннотация
Цель. Изучить долговременное прогностическое значение нового индекса сосудистой жесткости START у больных ишемической болезнью сердца (ИБС) после аортокоронарного шунтирования (АКШ).
Материал и методы. В исследование вошли 256 пациентов ИБС, подвергшихся АКШ на базе НИИ КПССЗ г. Кемерово. Перед операцией оценивали сосудистую жесткость с помощью сердечно-лодыжечного индекса haSTART. Средний период наблюдения составил 9,7±0,9 лет. Были сформированы две группы исследования: I группа haSTART ниже медианы (Ме) индекса 8,4 (haSTART <Ме, n=118), II группа haSTART равный или выше Ме (haSTART ≥Ме, n=138). Прогностическое значение haSTART изучалось в отношении комбинированной конечной точки (ККТ): летальный исход, нефатальный инфаркт миокарда или инсульт.
Результаты. Пациенты в группе haSTART ≥Ме были статистически значимо старше, чем в группе haSTART <Ме (р<0,001). В обеих группах превалировали мужчины (76,2%). За период наблюдения летальный исход от всех причин достоверно чаще встречался в группе с haSTART ≥Ме (34,1%), чем в группе с haSTART <Ме (19,5%), р=0,009. Смерть от сердечных причин также чаще наблюдалась в группе haSTART ≥Ме, чем haSTART <Ме (23,2%, vs 8,5%, р=0,001). У больных с haSTART ≥Ме ККТ отмечалась в 45,7% случаев, по сравнению с больными с haSTART <Ме — в 30,5% случаях, р=0,013. Среди больных с наступлением летального исхода была выше частота больных со значениями haSTART ≥Ме, чем в группе выживших (67,1% и 48,9%, р=0,009). Среди больных с развитием ККТ — частота выявления у них значений индекса haSTART ≥Ме составила 63,6%, что было достоверно выше, чем в группе выживших без сердечно-сосудистых событий (47,8%, р=0,013). Кривые Каплана-Мейера выявили лучший долгосрочный прогноз в группе со значениями индекса haSTART <Ме по сравнению с группой, в которой индекс haSTART ≥Ме (р>0,05).
Заключение. Оценка индекса жесткости haSTART перед операцией АКШ, возможно, имеет прогностическое значение в отдаленном периоде наблюдения у больных ИБС.
Для цитирования:
Сумин А.Н., Щеглова А.В., Барбараш О.Л. Прогностическое значение нового индекса жесткости артерий START у пациентов с ишемической болезнью сердца после коронарного шунтирования. Российский кардиологический журнал. 2024;29(12):5952. https://doi.org/10.15829/1560-4071-2024-5952. EDN: XPBYYL
For citation:
Sumin A.N., Shcheglova A.V., Barbarash O.L. Prognostic significance of the novel START arterial stiffness index in patients with coronary artery disease after coronary artery bypass grafting. Russian Journal of Cardiology. 2024;29(12):5952. (In Russ.) https://doi.org/10.15829/1560-4071-2024-5952. EDN: XPBYYL
В современной кардиологии отмечается парадокс: известен интегральный показатель сердечно-сосудистого риска — жесткость артериальной стенки, оценка которого может быть полезна в профилактических программах [1] и имеет прогностическое значение при сердечно-сосудистых заболеваниях [2], но в клинической практике не находит широкого распространения. Причины это парадокса известны, они заключаются в отсутствии удобной технологии определения данного показателя. Традиционный неинвазивный метод оценки сосудистой жесткости — каротидно-феморальная скорость пульсовой волны (СПВ) [3] вследствие трудоемкости обследования, зависимости от квалификации персонала и уровня артериального давления (АД), не может заполнить данную нишу. Решение проблемы было найдено японскими исследователями, был предложен новый метод определения сердечно-лодыжечной СПВ (haСПВ), основанный на параметре жесткости β с расчетом сердечно-лодыжечного сосудистого индекса (CAVI) посредством объемной сфигмографии [4][5]. Изучение данного показателя позволило установить его прогностическую значимость в популяционных исследованиях [6][7] и у пациентов с сердечно-сосудистыми заболеваниями [8]. Несомненным преимуществом данного индекса является его независимость от уровня АД и простота его определения [9], что позволяет использовать его при динамической оценке состояния жесткости сосудистой стенки. Однако в настоящее время определение данного индекса возможно только с использованием зарубежных приборов, что делает его малодоступным для отечественных учреждений первичного звена из-за его высокой цены.
С учетом недостатков существующих методов расчета артериальной жесткости российские исследователи недавно разработали новый индекс START (STiffness of ARTeries). Расчет данного индекса основан на другой математической формуле, в основе которой лежат законы сохранения массы и импульса, а также стандартный метод вывода условий на разрыве, при котором фронт пульсовой волны моделируется как разрыв. При этом также учитываются нелинейные эффекты, в результате чего коррекция фактора АД при измерении сосудистой жесткости осуществляется более точно. Индекс жесткости START может быть измерен любым устройством с оценкой СПВ на любом участке артериального русла, при этом в название индекса вносится буквенное обозначение исследуемого участка [10].
Опубликованные ранее исследования показали, что новый индекс START значимо коррелирует с хорошо зарекомендовавшим себя в клинической практике индексом сосудистой жесткости CAVI как у здоровых лиц [11][12], так и у больных артериальной гипертензией [12][13] и ишемической болезнью сердца (ИБС) [14]. Тем не менее для использования в клинической практике необходимо убедиться в том, что индекс START имеет схожее прогностическое значение. Соответственно, цель исследования — изучить долговременное прогностическое значение нового индекса сосудистой жесткости START у больных ИБС после аортокоронарного шунтирования (АКШ).
Материал и методы
В одноцентровом когортном исследовании приняли участие 267 пациентов (из них 66 женщин и 201 мужчина), в возрасте от 33 до 77 лет, поступившие на плановое АКШ в период с 2012 по 2013гг в клинику НИИ "Комплексных проблем сердечно-сосудистых заболеваний" (г. Кемерово). Критерии исключения из исследования были следующие: значение лодыжечно-плечевого индекса (ЛПИ) ≤0,9, поскольку наличие гемодинамически значимого стеноза артерий нижних конечностей искажает истинные показатели жесткости сосудистой стенки, и отказ от участия в исследовании. После подписания добровольного информированного согласия пациенты были включены в исследование. Дизайн исследования был одобрен комитетом по этике института и соответствовал принципам Хельсинкской декларации.
Всем поступившим в стационар пациентам проведено стандартное предоперационное клинико-инструментальное обследование. Жесткость сосудистой стенки определяли на профессиональном аппарате для объемной сфигмографии VaSera VS-1000 (Fukuda Denshi, Япония). Для расчета нового национального индекса START использовали онлайн-калькулятор, расположенный в свободном доступе (https://stelari-start.com). Индекс рассчитывался на участке от клапана сердца до лодыжки (haSTART) [10]. В ходе анализа значимых различий между haSTART справа и слева выявлено не было (p>0,05), что позволило при анализе использовать среднее значение. Таким образом, медиана (Ме) haSTART составила 8,4 [ 7,2;9,8]. Если значение показателя haSTART было ниже выборочной Me <8,4, то пациента относили к первой группе, если haSTART ≥8,4, то ко второй группе. Дизайн исследования представлен на рисунке 1.
Кардиохирургические вмешательства всем включенным в исследование пациентам были проведены в стандартных условиях. Всем пациентам было выполнено изолированное АКШ. После операции была назначена оптимальная медикаментозная терапия и даны рекомендации по изменению образа жизни.
Средний период наблюдения за исходно сформированной когортой составил 9,7±0,9 лет. В результате непрямых контактов с пациентами была получена информация в отношении 256 пациентов. Из выборки пациентов в отдаленном периоде были сформированы две группы исследования: с haSTART <Ме (n=118) и haSTART ≥Ме (n=138). Прогностическое значение haSTART изучалось в отношении первичной комбинированной конечной точки (ККТ) — летальный исход, нефатальный инфаркт миокарда или инсульт (n=99).
Статистический анализ всех полученных данных производился с использованием приложения "Statistica 8.0" (Dell Software, Inc., США) и SPSS 17.0 software package. Критерий Шапиро-Уилка применяли для проверки анализируемых показателей на нормальность распределения. В связи с ненормальным распределением для межгрупповых сравнений количественных переменных использовали непараметрический критерий Манна-Уитни. Количественные данные описывались с помощью Me, а также нижнего и верхнего квартилей (Me±Q). Качественные показатели анализировали с помощью критерия χ2 с поправкой Йетса. Для сравнения выживаемости за время наблюдения был использован метод выживаемости Каплана-Мейера с использованием логарифмического критерия. Различия считались статистически значимыми при p<0,05.
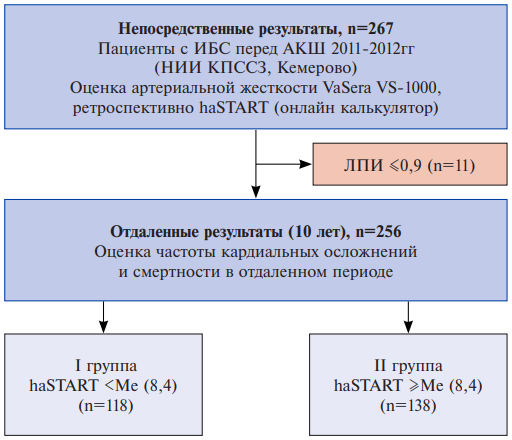
Рис. 1. Дизайн исследования.
Сокращения: АКШ — аортокоронарное шунтирование, ИБС — ишемическая болезнь сердца, ЛПИ — лодыжечно-плечевой индекс, haSTART — сердечно-лодыжечный индекс жесткости (STiffness of ARTeries), Me — медиана.
Результаты
В изучаемой выборке пациенты первой группы haSTART ≥Ме были статистически значимо старше, чем пациенты второй группы haSTART <Ме (р<0,001). В обеих группах превалировали мужчины (76,2%), большинство имели в анамнезе артериальную гипертензию (86,3%), инфаркт миокарда (61,0%) и хроническую сердечную недостаточность I-II функционального класса (66,8%). Ранее перенесли реваскуляризацию миокарда 9,0% пациентов, острое нарушение мозгового кровообращения встречалось ранее в 6,6% случаев. Сахарный диабет 2 типа был диагностирован у 15,2% пациентов. Несмотря на то, что пациенты с ЛПИ <0,9 исключались из исследования, мультифокальный атеросклероз >50% в изучаемой выборке встречался в 19,0% случаях. Не было выявлено статистически значимых различий в исходных лабораторных параметрах между группами. По результатам эхокардиографии Ме размера левого предсердия и межжелудочковой перегородки была выше у пациентов с haSTART ≥Ме, чем в группе haSTART <Ме (р=0,016 и р=0,018, соответственно). Остальные эхокардиографические параметры были сопоставимы (табл. 1).
У пациентов haSTART ≥Ме были выше показатели по шкале EuroSCORE II, которая позволяет рассчитать риск смерти после операции на сердце, по сравнению с пациентами haSTART <Ме (p=0,001). При анализе исходных анатомических характеристик коронарных артерий статистически достоверных различий между группами выявлено не было, что объясняет и отсутствие различий по количеству наложенных коронарных шунтов во время операции (табл. 2).
В таблице 3 представлены результаты для всех анализируемых параметров гемодинамики и сосудистой жесткости, измеренных при помощи сфигмографии. Отмечены статистически достоверно большие значения CAVI и haСПВ в группе с haSTART ≥Ме, в сравнении с группой, где индекс haSTART <Ме (p<0,001). Уровень АД в обеих группах был в пределах оптимальных значений, однако во второй группе с haSTART ≥Ме он был статистически достоверно выше, чем в первой группе с haSTART <Ме (p<0,001). При этом Ме пульсового АД статистически не различалась в обеих группах и была <60 мм рт.ст.
За все время наблюдения частота приема медикаментозной терапии была низкой в обеих группах и не имела статистических различий между группами (р>0,05) (рис. 2).
За период наблюдения в обследованной выборке произошло 70 (27,3%) смертей от всех причин, из них 42 (16,4%) — от сердечно-сосудистых событий. Количество случаев ККТ составило 99 (38,7%), включая нефатальный инфаркт миокарда у 14 (5,5%) и инсульт у 19 (7,4%) больных. При этом летальный исход от всех причин достоверно чаще встречался в группе с haSTART ≥Ме у 47 (34,1%) пациентов, в группе с haSTART <Ме у 23 (19,5%), р=0,009. Смерть от сердечных причин также чаще наблюдалась во второй группе, чем в первой (23,2% vs 8,5%, р=0,001). У больных с haSTART ≥Ме ККТ отмечалась в 63 (45,7%) случаях, по сравнению с больными с haSTART <Ме — в 36 (30,5%) случаях, р=0,013 (табл. 4).
Среди больных с наступлением летального исхода была выше частота больных со значениями haSTART ≥Ме (рис. 3), чем в группе выживших (67,1% и 48,9%, р=0,009). Похожая тенденция отмечена и среди больных с развитием ККТ — частота выявления у них значений индекса haSTART ≥Ме составила 63,6%, что было достоверно выше, чем в группе выживших без сердечно-сосудистых событий (47,8%, р=0,013).
Кривые Каплана-Мейера выявили лучший долгосрочный прогноз в группе со значениями индекса haSTART <Ме по сравнению с группой, в которой индекс haSTART был ≥Ме (рис. 4, 5). Различия были статистически значимыми как для показателей выживаемости (p=0,030, p=0,008 и p=0,011, соответственно, для лог-рангового критерия, тестов Бреслоу и Тарона-Уэра), так и для выживания без событий (p=0,042, p=0,026 и p=0,026, соответственно, для лог-рангового критерия, тестов Бреслоу и Тарона-Уэра) (табл. 5).
Таблица 1
Сравнение исходных характеристик пациентов ИБС
Показатели | I группа, haSTART <Ме (n=118) | II группа, haSTART ≥Ме (n=138) | p |
Общие данные и социальный статус | |||
Возраст (лет) | 56,0 [ 51,0;61,0] | 61,0 [ 56,0;67,0] | <0,001 |
Мужчины (n, %) | 94 (79,7) | 101 (73,2) | 0,226 |
Курение (n, %) | 40 (33,9) | 37 (26,8) | 0,218 |
Стаж курения (лет) | 30,0 [ 20,0;40,0] | 35,0 [ 25,0;40,0] | 0,107 |
Работающий (n, %) | 63 (53,3) | 38 (27,5) | <0,001 |
Антропометрические показатели | |||
Рост (см) | 170,0 [ 164,0;176,0] | 169,0 [ 164,0;175,0] | 0,377 |
Вес (кг) | 80,0 [ 69,0;89,0] | 80,0 [ 73,0;89,0] | 0,553 |
ИМТ (кг/см2) | 28,4 [ 24,8;31,6] | 28,3 [ 25,9;31,1] | 0,596 |
Клинико-анамнестические данные | |||
ХСН II-III стадии (n, %) | 33 (28,0) | 52 (37,7) | 0,099 |
ИМ в анамнезе (n, %) | 78 (66,1) | 78 (56,5) | 0,117 |
АГ в анамнезе (n, %) | 97 (82,2) | 124 (89,9) | 0,075 |
ОНМК/ТИА в анамнезе (n, %) | 5 (4,2) | 12 (8,7) | 0,153 |
СД в анамнезе (n, %) | 15 (12,7) | 24 (17,4) | 0,299 |
Реваскуляризация миокарда в анамнезе (n, %) | 11 (9,3) | 12 (8,7) | 0,861 |
Вмешательство на сонных артериях (n, %) | 2 (1,7) | 2 (1,5) | 0,874 |
Мультифокальный атеросклероз >50% (n, %) | 17(14,4) | 32 (23,2) | 0,075 |
Лабораторные данные | |||
Общий ХС (ммоль/л) | 4,9 [ 4,1;5,7] | 5,1 [ 4,1;6,1] | 0,667 |
ХС ЛНП (ммоль/л) | 2,8 [ 2,2;3,5] | 2,9 [ 2,2;3,8] | 0,429 |
Триглицериды (ммоль/л) | 1,8 [ 1,4;2,4] | 1,7 [ 1,2;2,3] | 0,166 |
Глюкоза, венозная плазма (ммоль/л) | 5,5 [ 5,1;6,4] | 5,5 [ 5,0;6,4] | 0,588 |
Креатинин (мкмоль/л) | 83,0 [ 71,0;100,0] | 82,5 [ 72,0;102,0] | 0,812 |
СКФ, CKD-EPI (мл/мин/1,73 м2) | 83,8 [ 67,2;102,7] | 82,3 [ 65,6;98,4] | 0,345 |
ЭхоКГ | |||
Левое предсердие (см) | 4,1 [ 3,8;4,5] | 4,3 [ 3,9;4,5] | 0,016 |
Межжелудочковая перегородка (см) | 1,0 [ 1,0;1,1] | 1,1 [1,0;1,2] | 0,018 |
Задняя стенка ЛЖ (см) | 1,0 [ 1,0;1,2] | 1,1 [ 1,0;1,2] | 0,060 |
Конечный диастолический объем ЛЖ (мл) | 155,0 [ 135,5;184,0] | 151,5 [ 135,0;187,5] | 0,911 |
Конечный систолический объем ЛЖ (мл) | 62,0 [ 47,0;91,0] | 61,0 [ 49,0;88,0] | 0,914 |
Конечный диастолический размер ЛЖ (см) | 5,6 [ 5,3;6,2] | 5,5 [ 5,2;6,1] | 0,698 |
Конечный систолический размер ЛЖ (см) | 3,8 [ 3,4;4,6] | 3,8 [ 3,5;4,6] | 0,576 |
Индекс массы миокарда ЛЖ (г/м2) | 156,0 [ 130,7;182,9] | 162,3 [ 127,9;200,0] | 0,277 |
Фракция выброса ЛЖ (%) | 60,0 [ 51,0;64,0] | 60,0 [ 51,5;64,0] | 0,671 |
Е/А | 0,9 [ 0,7;1,2] | 0,8 [ 0,7;1,1] | 0,090 |
Примечание: данные указаны в виде Me [LQ;UQ], если не указано иное.
Сокращения: АГ — артериальная гипертензия, ИМ — инфаркт миокарда, ИМТ — индекс массы тела, ЛЖ — левый желудочек, ЛНП — липопротеины низкой плотности, ОНМК — острое нарушение мозгового кровообращения, СД — сахарный диабет, СКФ — скорость клубочковой фильтрации, ТИА — транзиторная ишемическая атака, ХС — холестерин, ХСН — хроническая сердечная недостаточность, ЭхоКГ — эхокардиография, Е/А — отношение скоростей раннего (E) и позднего (A) наполнения желудочков, haSTART — сердечно-лодыжечный индекс жесткости (STiffness of ARTeries), Me — медиана.
Таблица 2
Тяжесть поражения коронарных артерий и интраоперационная характеристика пациентов ИБС
Показатели | I группа, haSTART<Ме (n=118) | II группа, haSTART ≥Ме (n=138) | p |
Коронарография | |||
Поражение ствола ЛКА (n, %) | 27 (22,9) | 26 (18,8) | 0,426 |
Поражение одной КА (n, %) | 21 (17,8) | 24 (17,4) | 0,932 |
Поражение двух КА (n, %) | 40 (33,9) | 45 (32,6) | 0,827 |
Поражение трех КА (n, %) | 49 (41,5) | 62 (44,9) | 0,584 |
Интраоперационные данные | |||
Euroscore (баллы) | 2,0 [ 1,0;3,0] | 3,0 [ 2,0;4,0] | 0,052 |
Euroscore (%) | 1,33 [ 0,88;2,2] | 1,7 [ 1,2;2,8] | 0,001 |
Операция с ИК (n, %) | 105 (89,0) | 114 (82,6) | 0,148 |
Количество шунтов | 3,0 [ 2,0;3,0] | 3,0 [ 2,0;3,0] | 0,748 |
Длительность ИК (мин) | 96,0 [ 77,0;110,0] | 98,0 [ 81,0;111,0] | 0,413 |
Длительность операции (мин) | 240,0 [ 201,0;300,0] | 246,0 [ 198,0;300,0] | 0,772 |
Вентрикулопластика (n, %) | 5 (4,2) | 8 (5,8) | 0,571 |
Тромбэктомия (n, %) | 4 (3,4) | 3 (2,2) | 0,552 |
КЭЭ (n, %) | 2 (1,7) | 3 (2,2) | 0,784 |
Радиочастотная аблация (n, %) | 2 (1,7) | 2 (1,5) | 0,874 |
Примечание: данные указаны в виде Me [LQ;UQ], если не указано иное.
Сокращения: ИК — искусственное кровообращение, КА — коронарная артерия, КЭЭ — каротидная эндартерэктомия, ЛКА — левая коронарная артерия, haSTART — сердечно-лодыжечный индекс жесткости (STiffness of ARTeries), Me — медиана.
Таблица 3
Показатели гемодинамики и сосудистой жесткости по данным сфигмографии у больных ИБС
Показатели | I группа, haSTART <Ме (n=118) | II группа, haSTART ≥Ме (n=138) | p |
R-САД (мм рт.ст.) | 125,5 [ 114,0;136,0] | 132,0 [ 121,0;147,0] | <0,001 |
L-САД (мм рт.ст.) | 128,5 [ 118,0;143,0] | 133,5 [ 122,0;146,0] | 0,116 |
R-ДАД (мм рт.ст.) | 77,0 [ 70,0;83,0] | 81,0 [ 74,0;88,0] | <0,001 |
L-ДАД (мм рт.ст.) | 80,0 [ 73,0;85,0] | 82,0 [ 77,0;89,0] | <0,001 |
R-ПАД (мм рт.ст.) | 50,0 [ 44,0;60,0] | 56,0 [ 46,0;65,0] | 0,054 |
L-ПАД (мм рт.ст.) | 51,5 [ 44,5;59,0] | 54,0 [ 47,0;63,0] | 0,165 |
R-haСПВ | 7,3 [ 6,8;7,7] | 8,5 [ 8,0;9,2] | <0,001 |
L-haСПВ | 7,2 [ 6,8;7,7] | 8,4 [ 8,0;9,4] | <0,001 |
R-haSTART | 7,5 [ 6,6;7,9] | 9,9 [ 8,9;11,4] | <0,001 |
L-haSTART | 7,1 [ 6,4;7,5] | 10,0 [ 8,7;10,9] | <0,001 |
R-CAVI | 7,9 [ 7,2;8,1] | 9,2 [ 8,7;9,8] | <0,001 |
L-CAVI | 7,8 [ 7,2;8,1] | 9,2 [ 8,7;9,8] | <0,001 |
R-ЛПИ | 1,1 [ 1,02;1,2] | 1,2 [ 1,1;1,2] | 0,19 |
L-ЛПИ | 1,1 [ 1,02;1,1] | 1,1 [ 1,03;1,2] | 0,104 |
Примечание: данные указаны в виде Me [LQ;UQ], если не указано иное.
Сокращения: ДАД — диастолическое артериальное давление, ЛПИ — лодыжечно-плечевой индекс, ПАД — пульсовое артериальное давление, САД — систолическое артериальное давление, ЧСС — частота сердечных сокращений, CAVI — сердечно-лодыжечный сосудистый индекс (Cardio-Ankle Vascular Index), haSTART — сердечно-лодыжечный индекс жесткости (STiffness of ARTeries), haСПВ — метод определения сердечно-лодыжечной СПВ, Me — медиана, R — справа, L — слева.
Таблица 4
Осложнения десятилетнего периода в зависимости haSTART
Показатели | I группа, haSTART | II группа, haSTART ≥Ме (n=138) | p |
Смерть | 23 (19,5) | 47 (34,1) | 0,009 |
Сердечная смерть | 10 (8,5) | 32 (23,2) | 0,001 |
ИМ нефатальный | 8 (6,8) | 6 (4,4) | 0,394 |
ОНМК нефатальный | 7 (5,9) | 12 (8,7) | 0,401 |
ККТ (смерть+ИМ+ОНМК) | 36 (30,5) | 63 (45,7) | 0,013 |
Сокращения: ИМ — инфаркт миокарда, ККТ — комбинированная конечная точка, ОНМК — острое нарушение мозгового кровообращения, haSTART — сердечно-лодыжечный индекс жесткости (STiffness of ARTeries), Me — медиана.

Рис. 2. Прием оптимальной медикаментозной терапии в группах в зависимости от индекса haSTART исходно и через 10 лет наблюдения.
Сокращения: АКК — антагонисты кальциевых каналов, АРА — антагонисты рецепторов ангиотензина II типа, иАПФ — ингибиторы ангиотензин-превращающего фермента, haSTART — сердечно-лодыжечный индекс жесткости (STiffness of ARTeries), Me — медиана.
Таблица 5
Сравнение выживаемости между группами haSTART ≥Ме и haSTART <Ме (Лог-ранговый критерий, тесты Бреслоу, Тарона-Уэра)
Chi-Square | df | Sig. | |
Сравнение выживаемости MACE | |||
Лог-ранговый критерий | 4,684 | 1 | 0,030 |
Тест Бреслоу | 6,990 | 1 | 0,008 |
Тест Тарона-Уэра | 6,545 | 1 | 0,011 |
Сравнение выживаемости без MACE | |||
Лог-ранговый критерий | 4,154 | 1 | 0,042 |
Тест Бреслоу | 4,968 | 1 | 0,026 |
Тест Тарона-Уэра | 4,968 | 1 | 0,026 |
Сокращение: MACE – неблагоприятные сердечно-сосудистые события.
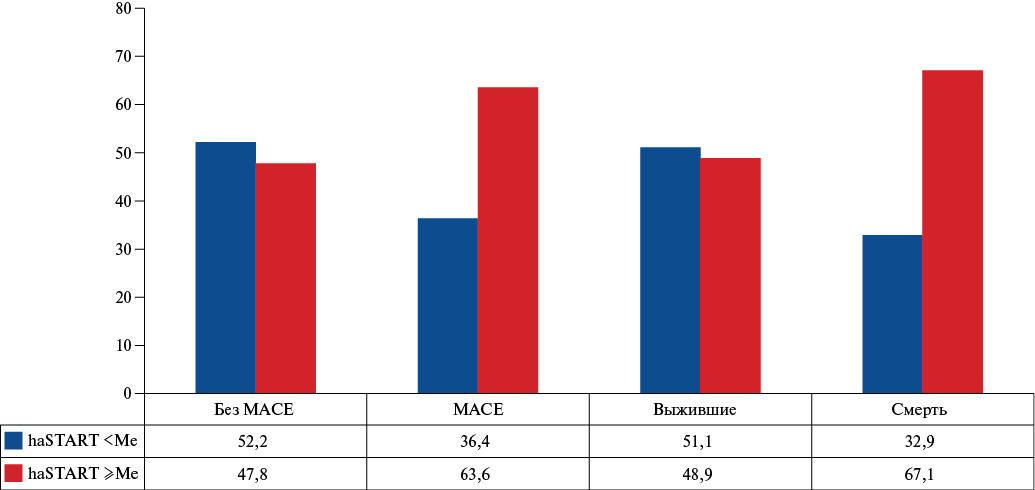
Рис. 3. Состояние сосудистой жесткости haSTART в группах с наличием/отсутствием неблагоприятных сердечно-сосудистых событий и летального исхода при длительном наблюдении после АКШ.
Сокращения: MACE — неблагоприятные сердечно-сосудистые события, haSTART — сердечно-лодыжечный индекс жесткости (STiffness of ARTeries), Me — медиана.
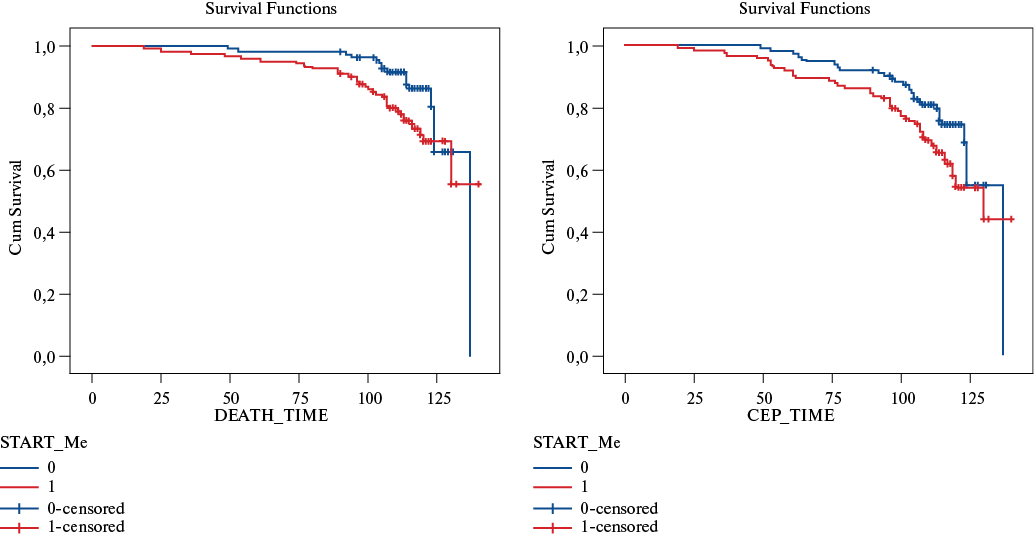
Рис. 4. Влияние индекса haSTART на долгосрочную выживаемость после АКШ.
Примечание: Группа 1 — haSTART ≥Ме, Группа 2 — haSTART <Ме.
Рис. 5. Влияние индекса haSTART на долгосрочную выживаемость без событий после АКШ.
Примечание: Группа 1 — haSTART ≥Ме, Группа 2 — haSTART <Ме.
Обсуждение
В настоящем исследовании впервые было показано, что новый индекс сосудистой жесткости haSTART имеет прогностическую ценность в долгосрочном наблюдении за пациентами ИБС после операции АКШ. Во-первых, в группе с индексом haSTART ≥Ме в период наблюдения чаще наблюдались смерть от всех причин, сердечно-сосудистая смерть и развитие ККТ. Во-вторых, группа с индексом haSTART <Ме имела лучшую выживаемость и лучшую выживаемость без событий по сравнению с пациентами, у которых индекс haSTART ≥Ме по данным лонг-рангового критерия при анализе кривых Каплана-Майера.
До настоящего времени не проводилось исследований прогностического значения индекса артериальной жесткости START. Этот индекс разработан в качестве альтернативы индексу CAVI, поскольку он также не зависит от уровня АД, поэтому предыдущие исследования были направлены на сопоставление этих индексов [10-14]. Так, в многоцентровом исследовании на базе пяти клинических центров с включением 928 человек, как здоровых лиц, так и больных артериальной гипертонией, показано, что индекс артериальной жесткости haSTART достоверно коррелирует с индексом CAVI. При этом не выявлено существенных различий между этими индексами в количественной взаимосвязи с АД, индексом массы тела, частотой сердечных сокращений и полом у различных подгрупп обследованных. Другими словами, несмотря на различия в методах расчета индексов, сравнительный анализ показал, что индексы сходным образом ведут себя в отношении корреляций с различными демографическими и физиологическими показателями [12]. В дальнейшем аналогичные корреляции между показателями haSTART и CAVI были выявлены у больных ИБС [14]. Важно подчеркнуть, что индекс haSTART следует тем же закономерностям, что и CAVI, что позволяет предположить, что индексы схожи в оценке сосудистой жесткости и, следовательно, предполагают одинаковую эффективность haSTART в качестве прогностического маркера для оценки сердечно-сосудистого риска. Однако это предположение не означает, что индекс haSTART обладает схожим с индексом CAVI прогностическим значением, это требовало подтверждения в соответствующих исследованиях. Необходимость такого анализа можно проиллюстрировать примером другой модификации индекса CAVI — индексом CAVI0, который был разработан с целью его дальнейшего улучшения и был призван в еще большей степени нивелировать зависимость от АД [15]. Тем не менее CAVI продемонстрировал большую точность в клинических ситуациях и имел лучшую прогностическую ценность по сравнению как с CAVI0, так и с другим показателем артериальной жесткости, плече-лодыжечной СПВ [8]. В настоящем исследовании нам удалось продемонстрировать прогностическую ценность индекса haSTART, подтвердив предположение авторов вышеупомянутой статьи [12]. Ранее было показано, что индекс CAVI имеет влияние на долгосрочный прогноз у больных ИБС [7], а также на прогноз в других когортах больных [5]. Настоящее исследование показало, что, по крайней мере, у больных ИБС индекс haSTART имеет сходное прогностическое значение. Насколько оно подтвердится в других обследованных когортах — требуются дополнительные исследования.
Клиническое значение исследования — наличие отечественного индекса позволит использовать его в отечественных недорогих приборах, необходимость разработки которых отмечалась ранее [12]. Это, в свою очередь, открывает широкие перспективы использования оценки артериальной жесткости в программах первичной и вторичной профилактики [3], донозологической диагностики, выявления субклинических проявлений атеросклероза артерий нижних конечностей. В этом плане будут необходимы исследования как по возможности оценки изменений индекса haSTART под влиянием лечебных и профилактических мероприятий, так и прогностические возможности серийной оценки индекса haSTART. Первые шаги в данном направлении уже сделаны, в исследовании нашей группы было показано, что у больных ИБС через год после операции КШ уменьшение индекса сосудистой жесткости haSTART наблюдалось в половине случаев. В этой группе было больше женщин, они чаще принимали антагонисты кальциевых каналов, чаще наблюдались в течение года у кардиолога. Были выявлены также неблагоприятные факторы, ассоциированные с возрастанием индекса haSTART — помимо возраста больных это было наличие коморбидных заболеваний (сахарный диабет, мультифокальный атеросклероз, сердечная недостаточность), а также дистрессорного типа личности Д.
Ограничения исследования. Исследование является пилотным, в связи с чем для подтверждения настоящих выводов требуется продолжение наблюдения. Во-первых, в настоящее время не существует нормативных значений индекса haSTART, поэтому мы не могли распределить пациентов на группы с нормальными или патологическими значениями haSTART, как это было в работах по оценке индекса CAVI [7]. Однако простая оценка индекса haSTART (выше/ниже Ме) позволила нам сформировать группы больных ИБС с различным отдаленным прогнозом. Во-вторых, мы не сравнивали прогностическую ценность индексов haSTART и CAVI, возможно, это могло бы более точно позиционировать использование этих индексов на практике. Это задача будущих исследований, хотя индекс haSTART разрабатывается для тех ситуаций, когда использование индекса CAVI невозможно (например, при использовании другого устройства). В-третьих, оценка индекса haSTART проводилась ретроспективно, что не позволяет оценить эффекты отдельных вмешательств, направленных на коррекцию факторов риска или медикаментозную терапию. В-четвертых, когорта пациентов ограничена пациентами с ИБС, перенесшими операцию АКШ. Остается неясным, можно ли распространить результаты этого исследования на другие заболевания. В-пятых, исследование проводилось в одном из российских центров; неясно, можно ли распространить его результаты на другие центры и регионы. Тем не менее сам факт выявления прогностического влияния индекса haSTART заслуживает внимания и подтверждения в дальнейших исследованиях.
Заключение
Настоящее исследование показало, что оценка индекса жесткости артерий haSTART перед операцией АКШ, возможно, имеет прогностическое значение в отдаленном периоде наблюдения за больными ИБС, в данном аспекте, планируются дальнейшие исследования. Также необходимо изучить, может ли динамика индекса haSTART при его серийной оценке влиять на прогноз у этих больных, а также какие вмешательства могут влиять на динамику этого индекса.
Отношения и деятельность. Результаты получены при поддержке Российской Федерации в лице Министерства науки и высшего образования РФ в рамках Соглашения о предоставлении из федерального бюджета грантов в форме субсидий от "30" сентября 2022г № 075-15-2022-1202, комплексной научно-технической программы полного инновационного цикла "Разработка и внедрение комплекса технологий в областях разведки и добычи твердых полезных ископаемых, обеспечения промышленной безопасности, биоремедиации, создания новых продуктов глубокой переработки из угольного сырья при последовательном снижении экологической нагрузки на окружающую среду и рисков для жизни населения", утвержденной распоряжением Правительства Российской Федерации от 11 мая 2022г № 1144-р.
Список литературы
1. Arnett DK, Blumenthal RS, Albert MA, et al. 2019 ACC/AHA Guideline on the Primary Prevention of Cardiovascular Disease: A Report of the American College of Cardiology/ American Heart Association Task Force on Clinical Practice Guidelines. Circulation. 2019;140(11):e596-646. doi:10.1161/CIR.0000000000000678.
2. Sang T, Lv N, Dang A, et al. Brachial-ankle pulse wave velocity and prognosis in patients with atherosclerotic cardiovascular disease: a systematic review and meta-analysis. Hypertens Res. 2021;44(9):1175-85. doi:10.1038/s41440-021-00678-2.
3. Васюк Ю. А., Иванова С. В., Школьник Е. Л. и др. Согласованное мнение российских экспертов по оценке артериальной жесткости в клинической практике. Кардиоваскулярная терапия и профилактика. 2016;15(2):4-19. doi:10.15829/1728-8800-2016-2-4-19.
4. Shirai K, Utino J, Otsuka K, et al. Novel Blood Pressure-independent Arterial Wall Stiffness Parameter; Cardio-Ankle Vascular Index (CAVI). Journal of Atherosclerosis and Thrombosis. 2006;13(2):101-7. doi:10.5551/jat.13.101.
5. Namba T, Masaki N, Takase B, Adachi T. Arterial Stiffness Assessed by Cardio-Ankle Vascular Index. International Journal of Molecular Sciences. 2019;20(15):3664. doi:10.3390/ijms20153664.
6. Matsushita K, Ding N, Kim ED, et al. Cardio-ankle vascular index and cardiovascular disease: Systematic review and meta-analysis of prospective and cross-sectional studies. J. Clin. Hypertens. 2019;21:16-24. doi:10.1111/jch.13425.
7. Заирова А. Р., Рогоза А. Н., Ощепкова Е. В. и др. Значение показателя артериальной жесткости "сердечно-лодыжечный сосудистый индекс — CAVI" для прогноза сердечно-сосудистых событий в популяционной выборке взрослого городского населения (по материалам исследования ЭССЕ-РФ, Томск). Кардиоваскулярная терапия и профилактика. 2021;20(5):2967. doi:10.15829/1728-8800-2021-2967.
8. Sumin AN, Shcheglova AV, ZHidkova II, et al. Assessment of Arterial Stiffness by Cardio-Ankle Vascular Index for Prediction of Five-Year Cardiovascular Events After Coronary Artery Bypass Surgery. Global Heart. 2021;16(1):90. doi:10.5334/gh.1053.
9. Shirai K, Suzuki K, Tsuda S, et al. Comparison of Cardio-Ankle Vascular Index (CAVI) and CAVI0 in Large Healthy and Hypertensive Populations. J Atheroscler Thromb. 2019; 26(7):603-15. doi:10.5551/jat.48314.
10. Бахолдин И. Б., Милягин В. А., Талов А. В. и др. Индекс STELARI START — новый перспективный показатель сосудистой жесткости. Вестник Смоленской государственной медицинской академии. 2022;21(3):95-192. doi:10.37903/vsgma.2022.3.11.
11. Сумин А. Н., Щеглова А. В., Бахолдин И. Б. Возможности нового показателя START в оценке сосудистой жесткости у здоровых лиц. Артериальная гипертензия. 2023;29(1):38-50. doi:10.18705/1607-419X-2023-29-1-38-50.
12. Васютин И. А., Леон К., Сафронова Т. А. и др. Сравнение нового индекса жесткости сосудистой стенки START с индексом CAVI, оценка их значений и корреляций с клиническими показателями. Российский кардиологический журнал. 2023;28(1):5272. doi:10.15829/1560-4071-2023-5272.
13. Сумин А. Н., Щеглова А. В., Бахолдин И. Б. Сравнительный анализ значений индексов артериальной жесткости START и CAVI у больных артериальной гипертензией. Кардиоваскулярная терапия и профилактика. 2023;22(3): 3473. doi:10.15829/1728-8800-2023-3473.
14. Sumin AN, Shcheglova AV, Gorelova IV, et al. Potential of the novel START index in assessing arterial stiffness in patients with coronary artery disease. Russian Open Medical Journal. 2023;12:e0410. doi:10.15275/rusomj.2023.0410.
15. Spronck B, Avolio AP, Tan I, et al. Arterial stiffness index beta and cardio-ankle vascular index inherently depend on blood pressure but can be readily corrected. J Hypertens. 2017;35(1):98-104. doi:10.1097/HJH.0000000000001132.
Об авторах
А. Н. СуминРоссия
Д. м. н., зав. лабораторией коморбидности при сердечно-сосудистых заболеваниях отдела клинической кардиологии.
Кемерово
Конфликт интересов:
Нет
А. В. Щеглова
Россия
К.м.н., н.с. лаборатории коморбидности при сердечно-сосудистых заболеваниях отдела клинической кардиологии.
Кемерово
Конфликт интересов:
Нет
О. Л. Барбараш
Россия
Д.м.н., профессор, академик РАН, директор.
Кемерово
Конфликт интересов:
Нет
Дополнительные файлы
- Новый индекс сосудистой жесткости haSTART имеет прогностическую ценность при долгосрочном наблюдении за пациентами с ишемической болезнью сердца (ИБС) после операции аортокоронарного шунтирования.
- При индексе haSTART больше медианы у больных ИБС в период наблюдения чаще наблюдались смерть от всех причин, сердечно-сосудистая смерть и развитие комбинированной конечной точки.
- У больных ИБС с индексом haSTART ниже медианы отмечена лучшая выживаемость и лучшая выживаемость без событий по данным анализа Каплана-Майера.
Рецензия
Для цитирования:
Сумин А.Н., Щеглова А.В., Барбараш О.Л. Прогностическое значение нового индекса жесткости артерий START у пациентов с ишемической болезнью сердца после коронарного шунтирования. Российский кардиологический журнал. 2024;29(12):5952. https://doi.org/10.15829/1560-4071-2024-5952. EDN: XPBYYL
For citation:
Sumin A.N., Shcheglova A.V., Barbarash O.L. Prognostic significance of the novel START arterial stiffness index in patients with coronary artery disease after coronary artery bypass grafting. Russian Journal of Cardiology. 2024;29(12):5952. (In Russ.) https://doi.org/10.15829/1560-4071-2024-5952. EDN: XPBYYL
JATS XML

















































