Перейти к:
Прогнозирование фибрилляции предсердий у больных ишемической болезнью сердца с использованием методов математического моделирования
https://doi.org/10.15829/1560-4071-2025-5868
EDN: KTACGP
Аннотация
Цель. Создать способ оценки вероятности выявления фибрилляции предсердий (ФП) у пациентов с ишемической болезнью сердца (ИБС).
Материал и методы. В проведенное нами открытое сплошное ретроспективное нерандомизированное исследование были включены данные больных женского и мужского пола с диагнозом ИБС в количестве n=181 человек, проходивших лечение в Государственном бюджетном учреждении Новосибирской области "Городская клиническая больница № 1" г. Новосибирска по поводу ИБС, которые были приняты в отделение кардиологии с сентября 2022г по сентябрь 2023г. На основе полученных данных разработаны модели предсказания вероятности выявления ФП.
Результаты. Построены прогностические модели риска ФП у больных ИБС. Модель с объясняющими переменными: фракция выброса левого желудочка, наличие артериальной гипертензии, уровень липопротеидов высокой плотности крови, GGвариант гена интерлейкина6 показала чувствительность 84% и специфичность 92% при скользящем экзамене.
Заключение. Построенный прогностический метод оценки риска развития ФП у больных ИБС имеет хорошую прогностическую ценность и достаточно прост в использовании, в т.ч. для врачей практического здравоохранения.
Ключевые слова
Для цитирования:
Кузин С.В., Ложкина Н.Г., Шефер Е.И., Рузанкин П.С. Прогнозирование фибрилляции предсердий у больных ишемической болезнью сердца с использованием методов математического моделирования. Российский кардиологический журнал. 2025;30(5):5868. https://doi.org/10.15829/1560-4071-2025-5868. EDN: KTACGP
For citation:
Kuzin S.V., Lozhkina N.G., Shefer E.I., Ruzankin P.S. Prediction of atrial fibrillation in patients with coronary artery disease using mathematical modeling methods. Russian Journal of Cardiology. 2025;30(5):5868. (In Russ.) https://doi.org/10.15829/1560-4071-2025-5868. EDN: KTACGP
Распространенность как ишемической болезни сердца (ИБС), так и фибрилляции предсердий (ФП) увеличивается с возрастом, и данные патологии часто сосуществуют [1]. Однако эта связь не является простым совпадением, в частности, Weng LC, et al. указывают на сложные взаимоотношения между ними [2].
Численность населения, страдающего фенотипом ИБС, при котором она сочетается с ФП, быстро растет. Сообщалось о сильной корреляции между этими двумя заболеваниями, и многие общие факторы риска могут играть важную роль в их развитии [3].
ИБС является основной причиной смертности как в развитых, так и в развивающихся странах, и за последние десятилетия её доля продолжает увеличиваться1. Многие исследования показали, что у пациентов с ИБС чрезвычайно часто развивается ФП, а согласно данным Ярославской Е. И. и др., показана зависимость между частотой и формой течения ФП, протяженностью и специфической локализацией поражения коронарного русла [4].
ФП является наиболее распространенной аритмией среди населения в целом. С начала века заболеваемость ФП значительно возросла. Об этой тенденции свидетельствуют как общемировые [5], так и российские данные [6].
Параллельно сообщалось, что у пациентов с ФП более вероятно поражение коронарных артерий [7][8], что указывает на высокий риск ишемического поражения миокарда.
Эти две патологии обладают общими, частично пересекающимися факторами риска, которые вызывают различные патофизиологические реакции, приводящие к одному или обоим заболеваниям. Согласно многочисленным данным в научной литературе, сахарный диабет (СД), артериальная гипертензия (АГ), пожилой возраст, дислипидемия, ожирение, курение и снижение физической активности являются основными факторами риска развития ИБС. Действительно, те же самые факторы риска чаще всего оказываются причастными к инициации и прогрессированию ФП [9-11].
В дополнение к "классическим" факторам риска развития ФП, обоснованным на многочисленных предшествующих популяционных исследованиях, представляются чрезвычайно интересными разработки в направлении поисков новых маркеров риска, в частности генетического характера. Правильное определение генетической предрасположенности позволяет своевременно предпринимать превентивные меры и разрабатывать индивидуализированные стратегии лечения.
Поэтому, в качестве дополнения к созданию комплексного подхода предсказания сочетания ФП и ИБС, нами было выделено 3 аллельных варианта гена интерлейкина-6 (ИЛ-6) как потенциальный новый прогностический маркер.
Ген ИЛ-6 расположен в локусе хромосомы 7p21-24 с промотором длиной 303 н. п. Было доказано, что распространенный однонуклеотидный полиморфизм, который приводит к изменению G>C-174 (rs1800795) в промоторной области гена ИЛ-6, изменяет скорость его транскрипции.
Согласно данным Oikonomou E, et al. [12], системное воспаление является фактором риска развития ФП, а повышенные уровни С-реактивного белка и ИЛ-6, как отражение высокой активности данного воспаления, показывают воспалительный профиль пациентов с ФП.
А метаанализ данных, проведенный Tai M, et al., показал корреляцию повышенного уровня ИЛ-6 в крови с повышенным риском тромбоэмболических осложнений и геморрагических событий у пациентов с ФП [13].
Также была показана связь высокого уровня ИЛ-6 сыворотки с повышенным риском рецидива ФП после электрической кардиоверсии и катетерной аблации [14].
В связи с этим персонифицированный подход не только к определению риска сочетания ФП с ИБС у одних больных, но и поиск возможности управления этими рисками делает актуальным изучение данной проблемы. Дополнительное применение современных методов математической статистики и математического моделирования позволит обеспечить дополнительную прогностическую силу и усилит возможности современного профилактического здравоохранения.
Учитывая всё вышеизложенное, целью нашего исследования явилась разработка метода оценки вероятности обнаружения ФП у больных с ИБС.
Материал и методы
В проведенное открытое сплошное ретроспективное нерандомизированное исследование были включены данные больных женского и мужского пола с диагнозом ИБС в количестве n=181 человек, проходивших лечение в Государственном бюджетном учреждении Новосибирской области "Городская клиническая больница № 1" г. Новосибирска по поводу ИБС, которые были приняты в отделение кардиологии с сентября 2022г по сентябрь 2023г. Пациенты были поделены на 2 группы: группа исследования состояла из пациентов, больных ФП на фоне ИБС; группу сравнения составляли больные ИБС, не имеющие ФП. 1 группа — ИБС в сочетании с ФП — составляла 82 человека, 2 группа — ИБС без ФП — 99 человек. Некоторые клинические характеристики пациентов из обеих подгрупп, отражающие набор выбранных для анализа предикторов риска, представлены в таблице 1.
Таблица 1
Некоторые клинические характеристики пациентов из подгрупп исследования
|
Группа контроля (99 человек) |
Группа исследования (82 человек) |
р — уровень значимости |
|
|
Женщины, % |
45,2 |
43,9 |
1,30** |
|
Возраст, лет (M±SD) |
65,1±7,4 |
70±10 |
0,15* |
|
ИМТ, кг/м² (M±SD) |
26,9±4,8 |
27,4±4,3 |
0,61* |
|
ФВ ЛЖ, % (M±SD) |
62,2±2,4 |
50,3±9,1 |
0,043* |
|
ОХС, ммоль/л (M±SD) |
5,8±1,4 |
5,0±1,4 |
0,99* |
|
ЛВП, ммоль/л (M±SD) |
2±1,1 |
1,1±0,3 |
6,99* |
|
ЛНП, ммоль/л (M±SD) |
3±1,3 |
3±1 |
0,22* |
|
АГ, % |
89,9 |
100 |
3,00** |
|
СД, % |
36,4 |
40,2 |
0,65** |
Примечание: * — t-критерий Стьюдента, ** — точный двухсторонний тест Фишера.
Сокращения: АГ — артериальная гипертензия, ИМТ — индекс массы тела, ЛВП — липопротеиды высокой плотности, ЛНП — липопротеиды низкой плотности, ОХС — общий холестерин, СД — сахарный диабет, ФВ ЛЖ — фракция выброса левого желудочка.
Критерии включения:
- Мужчины и женщины старше 18 лет;
- Поступившие в клинику с диагнозом "ишемическая болезнь сердца", подтвержденным всесторонним предшествующим обследованием: основой диагностики служили рекомендации Американского колледжа кардиологии и Европейского общества кардиологов [15][16]. При этом учитывалось одно из следующих: а) гемодинамически значимый стеноз просвета как минимум одной коронарной артерии по данным селективной коронароангиографии; б) изменения электрокардиограммы в ≥2 последовательных отведениях (патологический Q, или наличие QR); в) наличие зон локального гипокинеза по данным эхокардиографии;
- Подписавшие добровольное информированное согласие на участие в исследовании.
Клинические характеристики подгрупп пациентов в соответствии с формами ИБС и ФП представлены в таблице 2.
Таблица 2
Клиническая характеристика подгрупп исследования по фенотипам ИБС, ФП и ХСН
|
Группа исследования (ИБС+ФП) |
Группа контроля (ИБС без ФП) |
р — уровень значимости |
|
|
Формы ФП |
|||
|
Пароксизмальная, % |
58,5 |
— |
|
|
Персистирующая (в т. ч. длительно-персистирующая), % |
8,5 |
— |
|
|
Постоянная, % |
33,0 |
— |
|
|
Формы ИБС |
|||
|
Хронические коронарные синдромы |
|||
|
Стабильная стенокардия ФК 1-2, % |
60,9 |
65,7 |
0,63** |
|
Стабильная стенокардия ФК 3-4, % |
26,8 |
30,3 |
0,18** |
|
Безболевая ишемия миокарда, % |
0 |
2,02 |
0,36** |
|
Перенесенный в прошлом острый ИМ, % |
18,3 |
22,2 |
0,64** |
|
Фенотипы ХСН |
|||
|
ХСН отсутствует, % |
6,1 |
12,1 |
0,033** |
|
ХСН с сохраненной ФВ ЛЖ, % |
28,0 |
42,5 |
0,05** |
|
ХСН с умеренно-сниженной ФВ ЛЖ, % |
37,8 |
32,3 |
0,08** |
|
ХСН со сниженной ФВ ЛЖ, % |
28,1 |
13,1 |
0,032** |
Примечание: ** — точный двухсторонний тест Фишера.
Сокращения: ИБС — ишемическая болезнь сердца, ИМ — инфаркт миокарда, ФВ ЛЖ — фракция выброса левого желудочка, ФК — функциональный класс, ФП — фибрилляция предсердий, ХСН — хроническая сердечная недостаточность.
Критерии невключения:
- Отсутствие подписанного добровольного информированного согласия;
- Наличие тяжелой сопутствующей соматической патологии в стадии декомпенсации (тяжелая активно-протекающая аутоиммунная патология, цирроз печени классов В и С по Чайльд-Пью, тяжелое нарушение функции почек с расчетной скоростью клубочковой фильтрации <15 мл/мин, нахождение на программном гемодиализе);
- Исходно-диагностированное психическое расстройство;
- Наличие активно-протекающих злокачественных новообразований любой локализации.
Статистический анализ данных проводился пакетом R version 4.3.3 (The R Foundation for Statistical Computing, Австрия).
Для построения моделей предсказания вероятности обнаружения ФП рассматривались модели логистической регрессии. При этом перебирались все возможные наборы переменных из следующих: пол, возраст, фракция выброса (ФВ) левого желудочка (ЛЖ), АГ, общий холестерин, липопротеиды высокой плотности (ЛВП), липопротеиды низкой плотности (ЛНП), СД, варианты гена ИЛ-6: CC, CG, GG. Выбор переменных был произведён на основании анализа предшествующих публикаций [9-12]. В моделях использовались веса, уравновешивающие группы с положительным и отрицательным исходом. Точность моделей оценивалась с помощью скользящего экзамена (leave-one-out cross validation), при котором оценивались чувствительность — доля пациентов с положительным исходом, правильно определяемых как таковые, и специфичность — доля пациентов с отрицательным исходом, правильно определяемых как таковые, при этом считался предсказанным положительный исход если предсказанная вероятность была >1/2.
Исследование было выполнено в соответствии со стандартами надлежащей клинической практики (Good Clinical Practice) и принципами Хельсинкской декларации. Протокол исследования был одобрен Этическими комитетами всех участвующих клинических центров. До включения в исследование у всех участников было получено письменное информированное согласие.
Результаты и обсуждение
В работе проанализировано влияние клиническо-анамнестических, лабораторных и инструментальных факторов на вероятность обнаружения ФП у 181 больного ИБС.
Модель предсказания данной вероятности ФП с наибольшей чувствительностью включала следующие объясняющие переменные: ФВ ЛЖ, наличие АГ, уровень ЛВП крови, GG-вариант гена ИЛ-6. Эта модель продемонстрировала чувствительность 84,1% и специфичность 91,9% при скользящем экзамене (leave-one-out cross validation). Вероятность развития ФП в этой модели оценивается как:
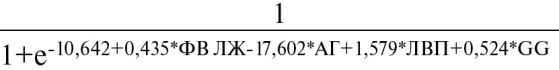 .
.
Модель с наибольшей суммой чувствительности и специфичности включала следующие объясняющие переменные: пол, ФВ ЛЖ, наличие АГ, СД, и продемонстрировала чувствительность 79,2% и специфичность 97,0% при скользящем экзамене.
Модели с наибольшей чувствительностью представлены в таблице 3.
Таблица 3
Модели с наибольшей чувствительностью
|
Чувствительность |
Специфичность |
Объясняющие переменные |
|
0,841 |
0,919 |
ФВ ЛЖ, АГ, ЛВП, GG |
|
0,841 |
0,919 |
ФВ ЛЖ, АГ, ОХС, ЛВП, GG |
|
0,829 |
0,919 |
ФВ ЛЖ, АГ, ЛВП, ЛНП, GG |
|
0,829 |
0,919 |
Пол, ФВ ЛЖ, АГ, ОХС, ЛВП, ЛНП |
|
0,829 |
0,919 |
Возраст, ФВ ЛЖ, АГ, ОХС, ЛВП, GG |
|
0,829 |
0,909 |
Пол, ФВ ЛЖ, АГ, ЛВП, ЛНП |
|
0,829 |
0,909 |
Пол, Возраст, ФВ ЛЖ, АГ, ЛВП, ЛНП |
|
0,829 |
0,909 |
Пол, Возраст, ФВ ЛЖ, АГ, ОХС, ЛВП, ЛНП |
|
0,829 |
0,909 |
Пол, ФВ ЛЖ, АГ, ОХС, ЛВП, ЛНП, СД |
|
0,829 |
0,909 |
Пол, ФВ ЛЖ, АГ, ОХС, ЛВП, ЛНП, CC |
|
0,817 |
0,939 |
Пол, ФВ ЛЖ, ОХС, ЛВП, ЛНП, GG |
|
0,817 |
0,939 |
Пол, Возраст, ФВ ЛЖ, ОХС, ЛВП, ЛНП, GG |
|
0,817 |
0,939 |
Пол, Возраст, ФВ ЛЖ, ОХС, ЛВП, ЛНП, СД, GG |
Примечание: чувствительность и специфичность указаны при скользящем экзамене.
Сокращения: АГ — артериальная гипертензия, ЛВП — липопротеиды высокой плотности, ЛНП — липопротеиды низкой плотности, ОХС — общий холестерин, СД — сахарный диабет, ФВ ЛЖ — фракция выброса левого желудочка, GG — GG-вариант гена интерлейкина-6, CC — CC-вариант гена интерлейкина-6.
При анализе субгрупп внутри всего массива пациентов были выявлены следующие закономерности.
Среди пациентов без ФП у 86 больных наблюдалась АГ (89,9%), в то время как у больных с ФП АГ наблюдалась в 100% случаев: у всех 82 пациентов.
В группе пациентов ИБС с ФП у 33 (40,2%) коморбидным заболеванием был СД. Несмотря на противоречащие данные литературы по теме [17] по указанному параметру в данном исследовании группы достоверно не различались: среди пациентов ИБС без ФП СД диагностирован у 36 пациентов (в 36,4% случаев). Причиной подобного распределения предполагается вероятный адекватный контроль гликемии пациентами из обеих групп, а также отсутствия впервые выявленной повышенной гликемии на момент пребывания в профильном кардиологическом стационаре.
Согласно мировым литературным данным, значимый вклад в риск возникновения ФП вносят некоторые показатели эхокардиограммы, в частности такой показатель сердечной функции как ФВ ЛЖ, указывающий на тяжесть хронической сердечной недостаточности [18]. В проведенном нами исследовании ФВ ЛЖ была достоверно ниже в группе больных ИБС с ФП: в данной подгруппе исследования её показатель составлял 50,33±9,14%, тогда как в подгруппе больных ИБС без ФП аналогичный показатель составил — 62,22±2,40%. Данное наблюдение кажется нам достаточно важным, в связи с чем более полная характеристика подгрупп пациентов в зависимости от фенотипа хронической сердечной недостаточности представлена в таблице 2.
Как известно, недостаточно контролируемые показатели липидного профиля плазмы крови пациентов характеризуют худший прогноз в течении ИБС. На основании недавно полученных данных отсутствие должного контроля, недостаточно интенсивная терапия и как следствие более высокие показатели уровня общего холестерина крови не только предсказывают впервые выявленные и повторные негативные коронарные события, но и способствуют возникновению других побочных явлений [19]. Что касается, в частности, нарушений ритма сердца, одним из которых является ФП, то одним из интересных, на наш взгляд, наблюдений в области коррекции липидного профиля пациентов является повышение риска развития впервые возникшей ФП при более низких показателях уровня ЛВП [20].
Стоит отметить, что разработка диагностических и прогностических моделей — лишь первые шаги к их имплементации в области здравоохранения. Конечная цель моделей клинического прогнозирования выходит за рамки прогнозирования производительности — она заключается в улучшении принятия медицинских решений, для чего хорошо прогнозируемая производительность является лишь предпосылкой, но далеко не только самым главным условием реализации оценки способности модели улучшить медицинское обслуживание и исключить непропорционально-значимые показатели вреда [21].
Объективной целью практического применения нашего исследования в области здравоохранения мы видим способность к более тщательной диагностике ФП, с повышением точности всех предшествующих методов. В случае нашей работы, с возможностью конкретного количественного определения параметров вероятности обнаружения ФП у пациентов с ИБС, ставится вопрос о дальнейшем развитии стратегий прогнозирования.
В случае обнаружения повышенной вероятности обнаружения ФП у конкретного больного, по нашему мнению, для улучшения клинической практики, могут быть предприняты меры дальнейшего диагностического поиска. Таким образом, разработанные нами модели по своей сути способны служить методом скрининга для выявления ФП при её отсутствии у больного на данном этапе.
Заключение
Предложена модель прогнозирования вероятности обнаружения ФП у пациентов с ИБС. Эта модель содержит следующие объясняющие переменные: ФВ ЛЖ, наличие АГ, уровень ЛВП крови, GG-вариант гена ИЛ-6 и демонстрирует чувствительность 84% и специфичность 92% при скользящем экзамене (leave-one-out cross validation). Применение настоящего подхода позволит специалистам практического здравоохранения рассчитывать индивидуализированный риск наличия ФП у отдельных пациентов с ИБС, чтобы в дальнейшем оптимизировать их ведение.
Отношения и деятельность: все авторы заявляют об отсутствии потенциального конфликта интересов, требующего раскрытия в данной статье.
1. World Health Organization. Global Health Estimates. Deaths by Cause, Age, Sex, by Country and by Region, 2000-2016. Geneva, Switzerland: World Health Organization, 2018. https://www.who.int/data/gho/data/themes/mortality-and-global-health-estimates.
Список литературы
1. Roth GA, Mensah GA, Johnson CO, et al. GBD-NHLBI-JACC Global Burden of Cardiovascular Diseases Writing Group. Global Burden of Cardiovascular Diseases and Risk Factors, 1990-2019: Update From the GBD 2019 Study. J Am Coll Cardiol. 2020;76: 2982-3021. doi:10.1016/j.jacc.2020.11.010.
2. Weng LC, Preis SR, Hulme OL, et al. Genetic Predisposition, Clinical Risk Factor Burden, and Lifetime Risk of Atrial Fibrillation. Circulation. 2018;137:1027-38. doi:10.1161/ CIRCULATIONAHA.117.031431.
3. Feng L, Yi W. Coronary heart disease and atrial fibrillation: a vicious cycle. American Journal of Physiology-Heart and Circulatory Physiology. 2021;320(1):H1-H12. doi:10.1152/ajpheart.00702.2020.
4. Ярославская Е. И., Кузнецов В. А., Горбатенко Е. А. и др. Связь фибрилляции предсердий с поражением коронарного русла у больных ишемической болезнью сердца. Кардиология. 2019;59(9):5-12. doi:10.18087/cardio.2019.9.2641.
5. Linz D, Gawalko M, Betz K, et al. Atrial fibrillation: epidemiology, screening and digital health. Lancet Reg Health Eur. 2024;37:100786. doi:10.1016/j.lanepe.2023.100786.
6. Мареев Ю. В., Поляков Д. С., Виноградова Н. Г. и др. ЭПОХА: Эпидемиология фибрилляции предсердий в репрезентативной выборке Европейской части Российской Федерации. Кардиология. 2022;62(4):12-9. doi:10.18087/cardio.2022.4.n1997.
7. Кобалава Ж. Д., Лазарев П. В. Риск развития коронарных осложнений при фибрилляции предсердий. Кардиология. 2020;60(1):43-52. doi:10.18087/cardio.2020.1.n828.
8. Киртбая Л. Н. Эпидемиология и механизм развития фибрилляции предсердий после коронарных вмешательств. Анналы аритмологии. 2021;18(4):247-53. doi:10.15275/ annaritmol.2021.4.7.
9. Савельева Е. А., Соколова Н. Ю., Анохин А. В. и др. Интраоперационные факторы риска впервые возникшей фибрилляции предсердий у пациентов с хронической ИБС. Бюллетень НЦССХ им. А. Н. Бакулева РАМН. Сердечно-сосудистые заболевания. 2023;24(S6):52. doi:10.24022/1810-0694. EDN UOBVDY.
10. Петракова Е. С., Савина Н. М., Молочков А. В. Фибрилляция предсердий после операций аортокоронарного шунтирования: факторы риска, профилактика и лечение. Кардиология. 2020;60(9):134-48. doi:10.18087/cardio.2020.9.n1074. EDN VQVACV.
11. Тлегенова Ж. Ш., Жолдин Б. К., Кудайбердиева Г. З., Абдрахманов А. С. Факторы риска развития фибрилляции предсердий у больных артериальной гипертензией с сохраненной систолической функцией левого желудочка. Кардиология. 2019;59(S5):37-46. doi:10.18087/cardio.2617. EDN RLTEMJ.
12. Oikonomou E, Zografos T, Papamikroulis GA, et al. Biomarkers in Atrial Fibrillation and Heart Failure. Curr Med Chem. 2019;26(5):873-87. doi:10.2174/0929867324666170830100424.
13. Tai M, Shi H, Wang H, et al. Pilot study of peripheral blood chemokines as biomarkers for atrial fibrillation-related thromboembolism and bleeding in elderly patients. Front Public Health. 2022;10:844087. doi:10.3389/fpubh.2022.844087.
14. Scott LJr, Li N. Role of Inflammatory Signaling in Atrial Fibrillation. Int J Cardiol. 2019;287:195-200. doi:10.1016/j.ijcard.2018.10.020.
15. Virani SS, Newby KL, Arnold SV, et al. 2023 AHA/ACC/ACCP/ASPC/NLA/PCNA Guideline for the Management of Patients With Chronic Coronary Disease: A Report of the American Heart Association/American College of Cardiology Joint Committee on Clinical Practice Guidelines, Journal of the American College of Cardiology. 2023;82(9). doi:10.1016/j.jacc.2023.04.003.
16. Vrints C, Andreotti F, Koskinas KC, et al. 2024 ESC Guidelines for the management of chronic coronary syndromes: Developed by the task force for the management of chronic coronary syndromes of the European Society of Cardiology (ESC). European Journal of Cardiology. 2024;45(36):3415-537. doi:10.1093/eurheartj/ehae177.
17. Yildiz M, Lavie CJ, Morin DP, Oktay AA. The complex interplay between diabetes mellitus and atrial fibrillation. Expert Rev Cardiovasc Ther. 2022;20(9):707-17. doi:10.1080/14779072.2022.2115357.
18. Anter E, Jessup M, Callans DJ. Atrial Fibrillation and Heart Failure: Treatment Considerations for a Dual Epidemic. Circulation. 2009;119(18). doi:10.1161/CIRCULATIONAHA.108.821306.
19. Pirillo A, Norata GD. The burden of hypercholesterolemia and ischemic heart disease in an ageing world. Pharmacol Res. 2023;193:106814. doi:10.1016/j.phrs.2023.106814.
20. Watanabe H, Tanabe N, Yagihara N, et al. Association between lipid profile and risk of atrial fibrillation. Circ J. 2011;75(12):2767-74. doi:10.1253/circj.cj-11-0780.
21. Hendriksen JM, Geersing GJ, Moons KG, de Groot JA. Diagnostic and prognostic prediction models. J Thromb Haemost. 2013;11 Suppl 1:129-41. doi:10.1111/jth.12262.
Об авторах
С. В. КузинРоссия
Станислав Викторович Кузин — аспирант
Новосибирск
Н. Г. Ложкина
Россия
Наталья Геннадьевна Ложкина — д.м.н., профессор, г.н.с., руководитель группы клиническая и экспериментальная кардиология
Новосибирск
Е. И. Шефер
Россия
Евгений Игоревич Шефер — к.ф.м.н., н.с., лаборатория прикладных обратных задач
Новосибирск
П. С. Рузанкин
Россия
Павел Сергеевич Рузанкин — к.ф.м.н., с.н.с., лаборатория прикладных обратных задач
Новосибирск
- Сочетание фибрилляции предсердий с ишемической болезнью сердца значительно ухудшает течение обоих заболеваний.
- Методы математического моделирования позволяют с высокой достоверностью и эффективностью прогнозировать заболевания с выявлением частных индивидуальных рисков.
- В данном исследовании представлен один из вариантов разработки метода оценки вероятности обнаружения фибрилляции предсердий у больных ишемической болезнью сердца, который возможно использовать в практическом здравоохранении.
Рецензия
Для цитирования:
Кузин С.В., Ложкина Н.Г., Шефер Е.И., Рузанкин П.С. Прогнозирование фибрилляции предсердий у больных ишемической болезнью сердца с использованием методов математического моделирования. Российский кардиологический журнал. 2025;30(5):5868. https://doi.org/10.15829/1560-4071-2025-5868. EDN: KTACGP
For citation:
Kuzin S.V., Lozhkina N.G., Shefer E.I., Ruzankin P.S. Prediction of atrial fibrillation in patients with coronary artery disease using mathematical modeling methods. Russian Journal of Cardiology. 2025;30(5):5868. (In Russ.) https://doi.org/10.15829/1560-4071-2025-5868. EDN: KTACGP
JATS XML


















































