Перейти к:
Инфекционный эндокардит у пациента с обструктивной гипертрофической кардиомиопатией. Клинический случай
https://doi.org/10.15829/1560-4071-2025-5859
EDN: KJHLLW
Аннотация
Инфекционный эндокардит, возникший у пациентов, имеющих гипертрофическую кардиомиопатию, является редким клиническим сочетанием. Однако данная комбинация заболеваний увеличивает и без того высокий риск летального исхода у пациентов с гипертрофической кардиомиопатией. В связи с этим необходима ранняя диагностика данной патологии, своевременное проведение антибактериальной терапии, а также при необходимости проведение оперативного лечения. В статье приводится описание клинического случая.
Ключевые слова
Для цитирования:
Саркисян Л.Л., Кручинова С.В., Скалецкий К.В., Намитоков А.М., Барбухатти К.О., Космачева Е.Д. Инфекционный эндокардит у пациента с обструктивной гипертрофической кардиомиопатией. Клинический случай. Российский кардиологический журнал. 2025;30(5S):5859. https://doi.org/10.15829/1560-4071-2025-5859. EDN: KJHLLW
For citation:
Sarkisyan L.L., Kruchinova S.V., Skaletsky K.V., Namitokov A.M., Barbukhatti K.O., Kosmacheva E.D. Infective endocarditis in a patient with hypertrophic obstructive cardiomyopathy: а case report. Russian Journal of Cardiology. 2025;30(5S):5859. (In Russ.) https://doi.org/10.15829/1560-4071-2025-5859. EDN: KJHLLW
Введение
Пациенты с гипертрофической кардиомиопатией (ГКМП) относятся к категории промежуточного риска инфекционного эндокардита (ИЭ), наряду с больными ревматическими, неревматическими и врожденными заболеваниями клапанов (в т. ч. двустворчатый аортальный клапан (АК)), а также имеющими имплантированные устройства [1]. Некоторые современные эпидемиологические данные, в частности, датские национальные регистры, показывают, что заболевания из этой категории связаны с более высоким риском ИЭ по сравнению с общей популяцией [2][3]. Так, у пациентов с ГКМП кумулятивный риск развития ИЭ при 10-летнем наблюдении составил 0,5%. Это, тем не менее, в 6,5 раз выше по сравнению с общей популяцией. Наличие обструкции выводного тракта левого желудочка (ВТЛЖ), которая ранее считалась одним из основных факторов риска ИЭ [3], не изменяло этот риск, что также было продемонстрировано в других исследованиях [4-6]. Наличие у пациента ГКМП имплантированного кардиовертера-дефибриллятора дополнительно повышало риск ИЭ почти в 3,5 раза.
В данном клиническом примере мы описываем случай сочетания ГКМП и ИЭ, в котором от начала симптомов до постановки диагноза и операции прошло не менее 1 года. Тяжесть состояния и возникающие осложнения не позволяли быстро компенсировать состояние больного и выполнить хирургическое лечение. Принятие решения усложняло и то, что в литературе данная проблема описана довольно скудно, в основном в виде различных клинических наблюдений и единичных, преимущественно эпидемиологических, исследований.
Клинический случай
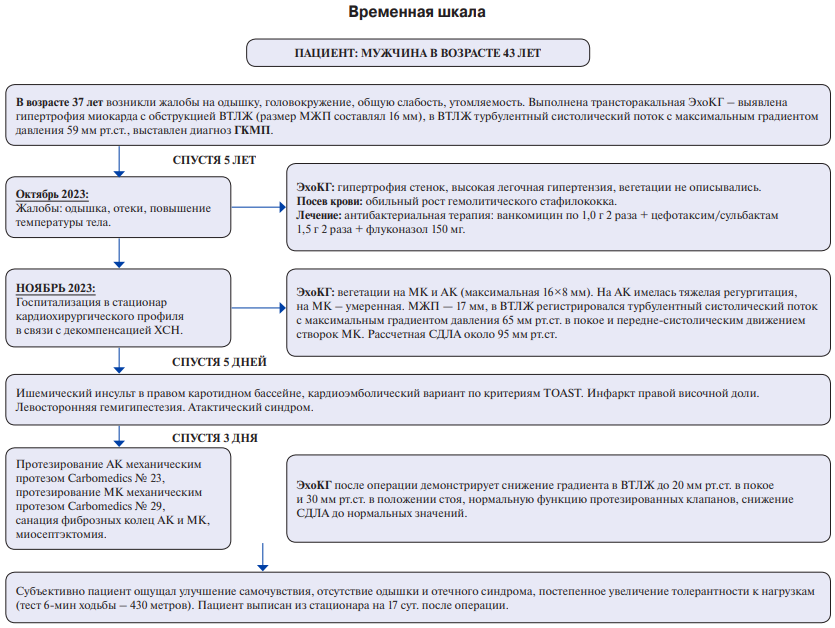
В ноябре 2023г в клинику поступил мужчина 43 лет с жалобами на одышку при минимальных физических нагрузках и в покое в горизонтальном положении, из-за чего в течение месяца перед поступлением спал преимущественно полусидя. Также пациента беспокоил приступообразный кашель, потливость, учащенное сердцебиение, периодически головокружение и потемнение в глазах. Он отметил, что за месяц постепенно увеличился в объеме живот, повысилась масса тела на 11 кг, пожелтела кожа и сильно отекли ноги.
Из анамнеза известно, что в возрасте 37 лет в связи с появлением одышки, периодического головокружения, общей слабости и быстрой утомляемости пациенту проведена трансторакальная эхокардиография (ЭхоКГ), по результатам которой была выявлена гипертрофия миокарда с обструкцией ВТЛЖ (размер межжелудочковой перегородки (МЖП) составлял 16 мм, толщина верхушечно-боковой и передне-верхушечной области — 19 мм, задней стенки — 15 мм), в ВТЛЖ регистрировался турбулентный систолический поток с максимальным градиентом давления 59 мм рт.ст., выставлен диагноз ГКМП. На фоне назначенного лечения (не уточняется какого) больной почувствовал себя лучше и в течение последующих 5 лет за медицинской помощью не обращался. Наследственный анамнез сомнительный — родной дядя умер от неуточненного заболевания сердца в возрасте 40 лет.
С осени 2022г пациент стал регулярно отмечать частые "простудные заболевания", с периодическим повышением температуры тела (максимально до 37,6 С). Пациент лечился самостоятельно парацетамолом и амоксициллином с клавулановой кислотой (курсами по 5 дней) с временным положительным эффектом и последующим рецидивированием симптомов. Ухудшение состояния с октября 2023г, когда стали беспокоить одышка при привычной нагрузке, кашель и отеки нижних конечностей. В ноябре 2023г пациент обратился за медицинской помощью по месту жительства, проведено лабораторное обследование — в общем анализе крови выявлены анемия и лейкоцитоз, в биохимическом анализе крови повышение С-реактивного белка (СРБ) до 42 мг/л. Выполнен посев крови, по результатам которого выявлен обильный рост гемолитического стафилококка, начата антибактериальная терапия (АБТ): ванкомицин по 1,0 г 2 раза + цефотаксим/сульбактам 1,5 г 2 раза + флуконазол 150 мг. Выбор данной комбинации препаратов обусловлен чувствительностью к ним выделенных микроорганизмов, определенной по результатам посевов крови. Выполнена ЭхоКГ, где помимо имеющейся ранее гипертрофии миокарда левого желудочка (ЛЖ) выявлена высокая легочная гипертензия, вегетации на клапанах не описывались.
На фоне АБТ у пациента отмечалась положительная лабораторная динамика маркеров воспаления, уровень СРБ снизился до 13,9 мг/л, а при повторном посеве крови роста микрофлоры выявлено не было. Однако, вероятно, из-за обильной инфузионной терапии стали прогрессировать признаки застоя, появился асцит и наросли отеки нижних конечностей. В связи с клинической картиной прогрессирующей хронической сердечной недостаточности, расцененной как проявление обструктивной ГКМП, больной направлен специализированный кардиохирургический центр.
При поступлении состояние пациента расценено как тяжелое, при объективном осмотре обращали на себя внимание выраженная одышка, положение ортопноэ, частота дыханий 30 в мин, сатурация кислорода на воздухе составляла 92-93%. Кожа с желтушным оттенком, на нижних конечностях массивные отеки до средней трети бедра. Гемодинамика была с тенденцией к гипотонии, артериальное давление (АД) 100/40 мм рт.ст., пульс 96 в минуту, без дефицита, хорошего наполнения. При аускультации определялся грубый систолический шум в точке Боткина, а также систолический шум на верхушке с проведением до средней подмышечной линии. Во второй точке аускультации выслушивался диастолический шум. Температура тела была нормальной.
Пациенту выполнена электрокардиография, на которой определялись характерные для ГКМП изменения реполяризации, признаки гипертрофии ЛЖ (рис. 1). ЭхоКГ выявила признаки ИЭ АК и митрального клапана (МК) с наличием вегетаций различного размера (максимальная 16×8 мм). На АК имелась тяжелая регургитация, на МК — умеренная. МЖП и задняя стенка ЛЖ были утолщены до 17 мм, толщина верхушечно-боковой и передне-верхушечной области составляла 16 мм. В ВТЛЖ регистрировался турбулентный систолический поток с максимальным градиентом давления 65 мм рт.ст. в покое и передне-систолическим движением створок МК. Расчетное систолическое давление в легочной артерии составило ~95 мм рт.ст., нижняя полая вена расширена до 33 мм и не реагировала на дыхание. Кроме того, присутствовал малый гидроперикард и малый двусторонний гидроторакс. Глобальная сократимость ЛЖ была нормальной, фракция выброса ЛЖ составляла 55% (рис. 2).
По данным компьютерной томографии (КТ) у больного диагностирован инфаркт селезенки, без признаков абсцедирования. Также пациенту проведена магнитно-резонансная томография (МРТ) сердца, где были выявлены изменения миокарда, которые, вероятно, соответствовали миокардиту (при отсроченном контрастировании через 3 и 15 мин отмечался участок накопления контрастного препарата в 7 сегменте на уровне средних отделов ЛЖ, занимающий всю толщину миокарда, в этом же участке на Т2-fat-sat определялся гипоинтенсивный участок (отек)), а также признаки гипертрофии миокарда ЛЖ без нарушения локальной сократимости (рис. 3).
Из результатов лабораторного обследования обращало на себя внимание небольшое увеличение СРБ до 12 мг/л, прокальцитонина до 0,07 нг/мл, повышение уровня общего билирубина до 48 мкмоль/л за счет прямого билирубина, аспартатаминотрансферазы до 97 ед./л, аланинаминотрансферазы до 251 ед./л.
У нашего пациента определялись два больших критерия Дюка (при двукратном посеве крови выявлен рост гемолитического стафилококка, по данным ЭхоКГ выявлены вегетации) и 2 малых критерия (предшествующее заболевание сердца, септический отсев в селезенку), что позволило нам выставить диагноз ИЭ АК и МК.
Продолжена АБТ ванкомицином 1 г 2 раза/сут. до получения результатов бактериологического исследования крови. Спустя несколько дней в посеве крови роста микрофлоры выявлено не было. Кроме того, проводилась диуретическая терапия фуросемидом 10,0 в/в на инфузомате и спиронолактоном 100 мг по 1 таблетке 1 раз/сут., проведение которой затрудняла часто возникающая гипотония.
Спустя 5 дней пребывания в нашем стационаре у пациента развился неврологический дефицит в виде онемения левой верхней конечности, дизартрии. По результату КТ головного мозга неврологом выставлен диагноз: "Ишемический инсульт в правом каротидном бассейне, кардиоэмболический вариант по критериям TOAST. Инфаркт правой височной доли. Левосторонняя гемигипестезия. Атактический синдром".
С целью предотвращения повторной эмболии, учитывая наличие крупных вегетаций на АК (16×8 мм), тяжелую недостаточность АК и МК, наличие однократного эпизода эмболии, пациенту показано оперативное вмешательство в объеме санации полостей сердца с протезированием пораженных клапанов.
Спустя 3 дня пациенту проведена операция: протезирование АК механическим протезом Carbomedics № 23, протезирование МК механическим протезом Carbomedics № 29, санация фиброзных колец АК и МК, миосептэктомия. Время искусственного кровообращения составило 141 мин, а время ишемии миокарда 102 мин. В ходе интраоперационной чреспищеводной ЭхоКГ толщина МЖП после ее редукции в базальном сегменте составила 11 мм. По результатам гистологического исследования АК и МК были выявлены признаки полипозно-язвенного эндокардита с дегенеративными изменениями. При микроскопическом исследовании удаленной части МЖП (удалённо 8 г) обнаружена дискомплексация (нарушение параллельного по отношению друг к другу расположения) мышечных волокон, а также гипертрофия кардиомиоцитов с полиморфизмом и зазубренностью контуров их ядер с перинуклеарными вакуолями внутри кардиомиоцитов. При бактериологическом исследовании АК и МК роста микрофлоры выявлено не было.
Послеоперационный период протекал относительно благоприятно с однократным эпизодом генерализованных тонико-клонических судорог, купированных спонтанно. По данным КТ головного мозга — стабильная картина ишемических изменений в правой теменно-височной области. ЭхоКГ после операции демонстрирует снижение градиента в ВТЛЖ до 20 мм рт.ст. в покое и 30 мм рт.ст. в положении стоя (рис. 4, 5), нормальную функцию протезированных клапанов, снижение СДЛА до нормальных значений.
Субъективно пациент ощущал улучшение самочувствия, отсутствие одышки и отечного синдрома, постепенное увеличение толерантности к нагрузкам. АД стабилизировалось на уровне 120/70 мм рт.ст. Пациент выписан из стационара на 17 сут. после операции с рекомендациями о продолжении проводимой АБТ (ампициллин + сульбактам 1,5 г × 4 раза/сут., даптомицин 800 мг × 1 раз/сут.) в стационаре по месту жительства и амбулаторной терапии бисопрололом 5 мг, торасемидом 5 мг и варфарином под контролем международного нормализованного отношения.
Сокращения: АК — аортальный клапан, ВТЛЖ — выводной тракт левого желудочка, ГКМП — гипертрофическая кардиомиопатия, МЖП — межжелудочковая перегородка, МК — митральный клапан, СДЛА — систолическое давление в легочной артерии, ХСН — хроническая сердечная недостаточность, ЭхоКГ — эхокардиография.
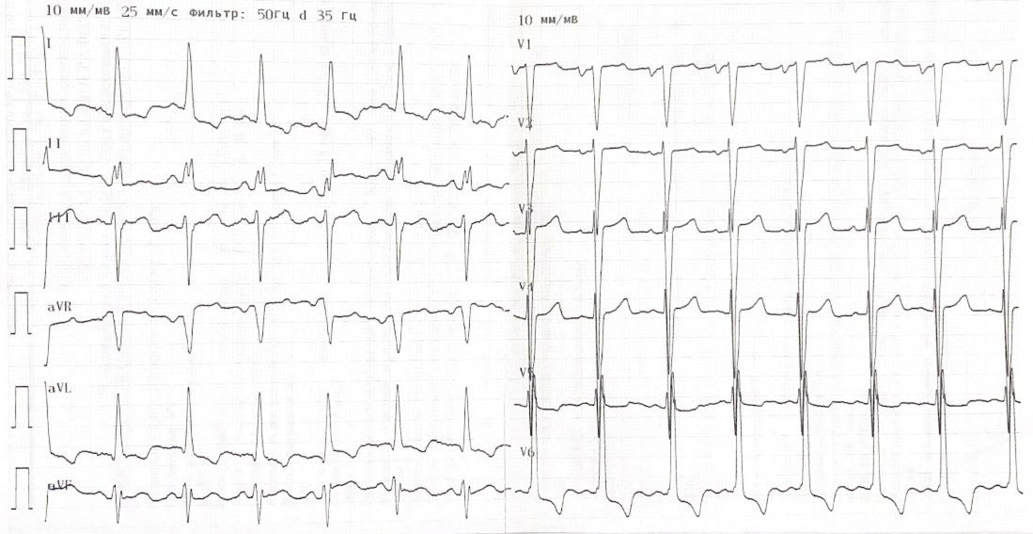
Рис. 1. Электрокардиограмма пациента с ГКМП.
Примечание: на данной электрокардиограмме определяются признаки гипертрофии миокарда ЛЖ (критерий Соколова-Лайона — 45 мм).
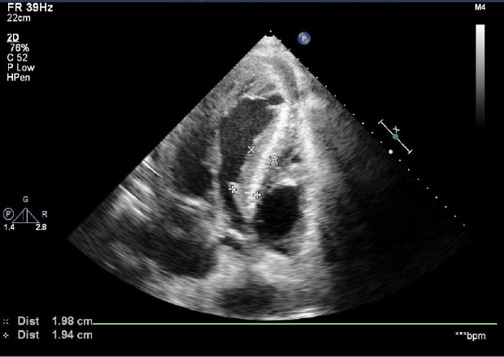
Рис. 2. Апикальная пятикамерная позиция, измерение толщины МЖП на уровне базальных и средних отделов.
Примечание: стрелками обозначены размеры базального (17 мм) и среднего (17 мм) сегментов МЖП.
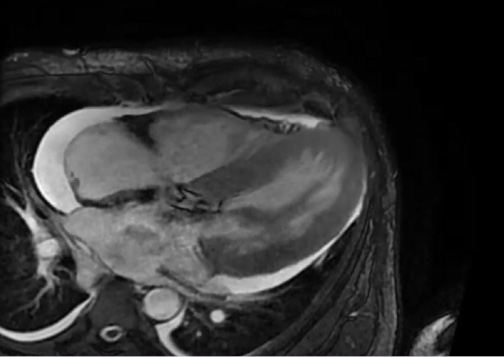
Рис. 3. МРТ сердца пациента с ГКМП.
Примечание: на данном изображении определяется гипертрофия миокарда ЛЖ. Размер МЖП по данным МРТ составлял 15 мм, задней стенки — 14 мм, размер стенки ЛЖ в области верхушки был равен 16 мм.
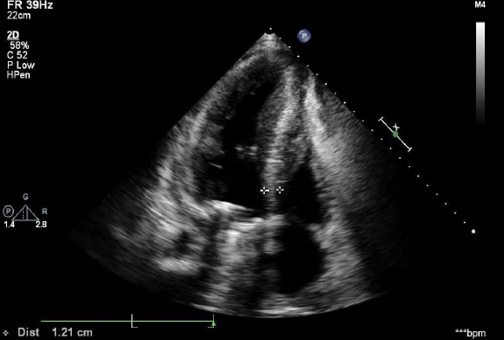
Рис. 4. Апикальная четырёхкамерная позиция после оперативного лечения.
Примечание: стрелками обозначен размер МЖП (11 мм) на уровне базального сегмента.
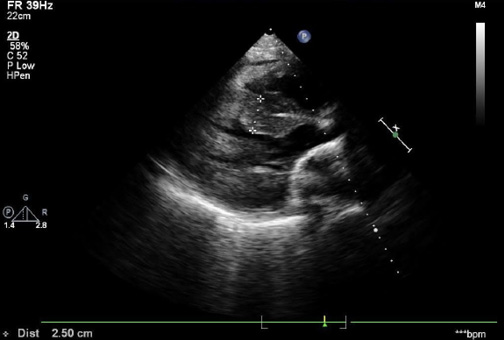
Рис. 5. Парастернальная позиция по длинной оси ЛЖ.
Примечание: стрелками обозначен размер МЖП (16 мм) на уровне средних отделов.
Обсуждение
Клинический случай демонстрирует сложности диагностики и лечения ИЭ у больного ГКМП начиная с амбулаторного этапа, где время от начала симптомов до постановки диагноза затянулось до 1 года, заканчивая трудностями в лечении и принятии решения об операции в крупном кардиохирургическом центре. Задержка в постановке диагноза ИЭ даже без сопутствующей ГКМП может сильно различаться и зависит от многих факторов, в т. ч. вида микроорганизма, доступности медицинской помощи, раннего приема антибиотиков и др., но по некоторым данным до трети случаев время до точного диагноза может составлять более трех месяцев [7]. В случае комбинации ИЭ и ГКМП такие данные отсутствуют, но мы предполагаем, что основной причиной задержки в диагностике в нашем случае явилась ГКМП, которая могла ввести в заблуждение относительно симптомов сердечной недостаточности, а также первичная и последующая ЭхоКГ, не выявившие вегетаций и поражения клапанов. Кроме того, отсутствовала четкая связь с каким-то триггером инфекции.
Согласно данным регистра GAMES IE [4], полость рта была основным предполагаемым источником инфекции (в 23% случаев ИЭ у больных ГКМП), а Streptococcus spp. был наиболее часто выявляемым инфекционным агентом (39%). У нашего пациента стоматологическая процедура (удаление зуба) также проводилась, но за 1 год до начала симптомов, поэтому ее связь с заболеванием является спорной. Антибиотикопрофилактика при этом не проводилась, что соответствует современным рекомендациям [1] с 2007г, в которых она была пересмотрена и отменена. Считается, что принимать профилактические меры для снижения риска ИЭ, такие как гигиена полости рта и кожи, санация очагов инфекции и т. д., является достаточным для категории пациентов промежуточного риска ИЭ. Такая позиция основана на соотношении потенциального вреда и пользы в связи с риском анафилаксии от антибиотика и отсутствии доказательств в рандомизированных исследованиях, которые бы подтверждали тезис об эффективности профилактики АБТ в предотвращении ИЭ у этих групп пациентов. Ряд авторов подчеркивают, что ИЭ слишком грозное осложнение ГКМП, чтобы не сопровождать антибиотикопрофилактикой процедуры высокого риска [8][9]. Так, под данным того же испанского регистра GAMES IE, госпитальная летальность у больных ИЭ и ГКМП составила 31% [4].
Заключение
Тщательная оценка клинической картины у нашего пациента, а именно: низкое диастолическое АД, шум регургитации, рецидивирующий субфебрилитет, рост гемокультуры и фон в виде ГКМП, позволила бы раньше заподозрить ИЭ и, возможно, нацелить врача, выполняющего ЭхоКГ, на детальный поиск признаков внутрисердечной инфекции. Не следует забывать и о проведении чреспищеводной ЭхоКГ в сомнительных случаях, когда клиническая вероятность ИЭ высока. Несмотря на положительный результат хирургического лечения, исход мог быть иным при менее удачном стечении обстоятельств. Мы надеемся, что данный материал поможет коллегам раньше верифицировать столь грозное осложнение ГКМП, как ИЭ, и принимать решение в схожей клинической ситуации, опираясь на наш опыт.
Информация о полученном согласии у пациентов на проведение исследования. Пациент госпитализирован в НИИ. Согласие на использование информации в научных целях получено одновременно с согласием на обследование и лечение.
Отношения и деятельность: все авторы заявляют об отсутствии потенциального конфликта интересов, требующего раскрытия в данной статье.
Список литературы
1. Delgado V, Ajmone Marsan N, de Waha S, et al. 2023 ESC Guidelines for the management of endocarditis [published correction appears in Eur Heart J. 2023] [published correction appears in Eur Heart J. 2024;45(1):56]. Eur Heart J. 2023;44(39):3948-4042. doi:10.1093/eurheartj/ehad193.
2. Spirito P, Rapezzi C, Bellone P, et al. Infective endocarditis in hypertrophic cardiomyopathy: prevalence, incidence, and indications for antibiotic prophylaxis. Circulation. 1999; 99(16):2132-7. doi:10.1161/01.cir.99.16.2132.
3. Ostergaard L, Valeur N, Wang A, et al. Incidence of infective endocarditis in patients considered at moderate risk. Eur Heart J. 2019;40:1355-61. doi:10.1093/eurheartj/ehy629.
4. Dominguez F, Ramos A, Bouza E, et al. Infective endocarditis in hypertrophic cardiomyopathy: A multicenter, prospective, cohort study. Medicine (Baltimore). 2016;95(26): e4008. doi:10.1097/MD.0000000000004008.
5. Sims JR, Anavekar NS, Bhatia S, et al. Clinical, Radiographic, and Microbiologic Features of Infective Endocarditis in Patients With Hypertrophic Cardiomyopathy. Am J Cardiol. 2018;121(4):480-4. doi:10.1016/j.amjcard.2017.11.010.
6. Oberoi M, Schaff HV, Nishimura RA, et al. Surgical Management of Hypertrophic Cardiomyopathy Complicated by Infective Endocarditis. Ann Thorac Surg. 2022;114(3): 744-9. doi:10.1016/j.athoracsur.2022.01.016.
7. N'Guyen Y, Duval X, Revest M, et al. Time interval between infective endocarditis first symptoms and diagnosis: relationship to infective endocarditis characteristics, microorganisms and prognosis. Ann Med. 2017;49(2):117-25. doi:10.1080/07853890.2016. 1235282.
8. Maron BJ, Lever H. In defense of antimicrobial prophylaxis for prevention of infective endocarditis in patients with hypertrophic cardiomyopathy. J Am Coll Cardiol. 2009; 54(24):2339-40; author reply 2340. doi:10.1016/j.jacc.2009.07.050.
9. CarrelT. Commentary: Endocarditis in hypertrophic cardiomyopathy: A reason to strengthen the guidelines? JTCVS Tech. 2020;4:286-7. doi:10.1016/j.xjtc.2020.10.046.
Об авторах
Л. Л. СаркисянРоссия
ординатор 2-го года обучения по специальности "Кардиология" кафедры терапии № 1
Краснодар
Конфликт интересов:
Нет
С. В. Кручинова
Россия
к.м.н., врач-кардиолог кардиологического отделения № 2 для больных с инфарктом миокарда, ассистент кафедры терапии № 1
Краснодар
Конфликт интересов:
Нет
К. В. Скалецкий
Россия
к.м.н., врач-кардиолог кардиологического отделения № 3, ассистент кафедры терапии № 1
Краснодар
Конфликт интересов:
Нет
А. М. Намитоков
Россия
к.м.н., зав. кардиологическим отделением № 2 для больных с инфарктом миокарда, ассистент кафедры терапии № 1
Краснодар
Конфликт интересов:
Нет
К. О. Барбухатти
Россия
д.м.н., зав. кафедрой кардиологии и кардиохирургии, главный кардиохирург Краснодарского края
Краснодар
Конфликт интересов:
Нет
Е. Д. Космачева
Россия
д.м.н., зав. кафедрой терапии № 1, зам. главного врача по лечебной работе
Краснодар
Конфликт интересов:
None
Дополнительные файлы

|
1. Презентация случая | |
| Тема | ||
| Тип | Исследовательские инструменты | |
Скачать
(143KB)
|
Метаданные ▾ | |
- Сочетание гипертрофической кардиомиопатии и инфекционного эндокардита встречается довольно редко.
- Основным методом диагностики данного состояния является эхокардиографическое исследование.
- Лечение данной группы пациентов требует индивидуального подхода, в зависимости от локализации и площади поражения объем лечения может включать антибиотикотерапию, санацию полостей сердца, протезирование пораженных клапанов, а также коррекцию гипертрофии методом миосептэктомии.
- Данный клинический случай демонстрирует сложности в своевременной постановке диагноза эндокардита у пациента с гипертрофической кардиомиопатией и направлен на формирование большей клинической настороженности у коллег.
Рецензия
Для цитирования:
Саркисян Л.Л., Кручинова С.В., Скалецкий К.В., Намитоков А.М., Барбухатти К.О., Космачева Е.Д. Инфекционный эндокардит у пациента с обструктивной гипертрофической кардиомиопатией. Клинический случай. Российский кардиологический журнал. 2025;30(5S):5859. https://doi.org/10.15829/1560-4071-2025-5859. EDN: KJHLLW
For citation:
Sarkisyan L.L., Kruchinova S.V., Skaletsky K.V., Namitokov A.M., Barbukhatti K.O., Kosmacheva E.D. Infective endocarditis in a patient with hypertrophic obstructive cardiomyopathy: а case report. Russian Journal of Cardiology. 2025;30(5S):5859. (In Russ.) https://doi.org/10.15829/1560-4071-2025-5859. EDN: KJHLLW
JATS XML

















































