Перейти к:
Персонифицированный выбор сосудистого доступа для реализации изолированной химиоперфузии печени: анализ программ стратификации риска осложнений
https://doi.org/10.15829/1560-4071-2023-5486
Аннотация
В статье представлены три клинических разбора изолированной химиоперфузии печени с применением аппарата искусственного кровообращения. Ретроспективно оценена вероятность развития осложнений, послеоперационных осложнений с применением программного обеспечения стратификации риска неблагоприятного исхода. Сделан вывод об эффективности представленного программного обеспечения.
Ключевые слова
Для цитирования:
Унгурян В.М., Казанцев А.Н., Коротких А.В., Иванов С.А., Белов Ю.В., Каприн А.Д. Персонифицированный выбор сосудистого доступа для реализации изолированной химиоперфузии печени: анализ программ стратификации риска осложнений. Российский кардиологический журнал. 2023;28(7):5486. https://doi.org/10.15829/1560-4071-2023-5486
For citation:
Unguryan V.M., Kazantsev A.N., Korotkikh A.V., Ivanov S.A., Belov Yu.V., Kaprin A.D. Personalized choice of vascular access for isolated hepatic perfusion: analysis of complication risk stratification programs. Russian Journal of Cardiology. 2023;28(7):5486. (In Russ.) https://doi.org/10.15829/1560-4071-2023-5486
Коллаборация сосудистой хирургии и онкологии позволяет выполнять лечение пациентов с нерезектабельными онкологическими заболеваниями. Одним из таких являются метастазы увеальной меланомы (УМ) в печени [1-3]. Применение аппарата искусственного кровообращения при полной изоляции печени от системного кровотока позволяет выполнить регионарную химиотерапию, что продлевает жизнь пациента на несколько лет [1-5].
Во всем мире на сегодня выполнено ~300 подобных вмешательств [1-5]. Изолированная химиоперфузия печени (ИХП) — достаточно травматичная операция [6-8]. Однако до сих пор не было внедрено шкал и программ, позволяющих рассчитать риск послеоперационных осложнений. Пациенты, направляющиеся на ИХП, разнородны по своему коморбидному фону и возрасту [6-10]. Среди них встречаются и молодые без какой-либо серьезной сопутствующей патологии, и пожилые больные, в ряде случаев с генерализованным атеросклерозом, сахарным диабетом и т.д. [1-5]. Персонифицированный подход в определении оптимальной стратегии лечения этой когорты пациентов способствовал бы снижению частоты послеоперационных осложнений.
Целью настоящей статьи стала демонстрация работы программного обеспечения, позволяющего персонифицировано определить оптимальную тактику лечения пациентов с метастазами УМ печени.
Блок-схема и программное обеспечение, которое позволяет выбирать оптимальный способ сосудистого доступа для реализации ИХП на основе показаний/противопоказаний к каждому из них
Существует 3 вида сосудистого доступа для реализации ИХП. Выбор между кава-порто-артериальным или кава-артериальным осуществляется на усмотрение оперирующего хирурга. Третий вид сосудистого доступа — вынужденный. Он включает в себя ситуацию, когда интраоперационно происходит перфорация яремной вены с развитием кровотечения, что вызывает необходимость в остановке химиоперфузии и дальнейшего продолжения операции. Другой вариант вынужденного доступа: кава-портальный сосудистый доступ, который применяется после многочисленных эмболизаций артерий печени.
Таким образом, на дооперационном этапе единственным противопоказанием для кава-порто-артериального или кава-артериального сосудистых доступов являются многочисленные эмболизации артерий печени в анамнезе.
Исходно блок-схема включает в себя показания или противопоказания для реализации ИХП и всех видов сосудистого доступа. Блок-схема с помощью языка программирования Python интегрирована в программное обеспечение1. На первом этапе предлагается выбор срока с момента верификации лечения первичного очага: более года или менее года. Данный шаг в программном обеспечении представлен на рисунке 1.
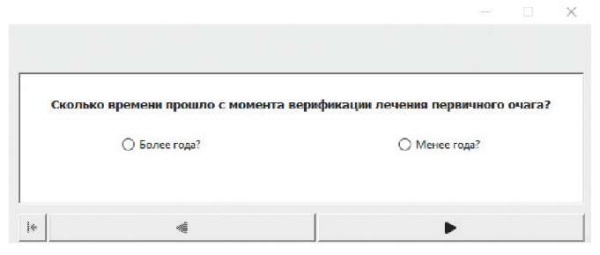
Рис. 1. Блок-схема, интегрированная в программное обеспечение:
выбор срока с момента верификации лечения первичного очага.
На втором этапе предлагается выбрать особенность метастатического поражения печени и организма в целом: наличие резектабельных очагов в печени, наличие нерезектабельных очагов в печени, наличие преимущественного поражения печени, наличие мультиорганного поражения. Данный шаг в программном обеспечении представлен на рисунке 2.
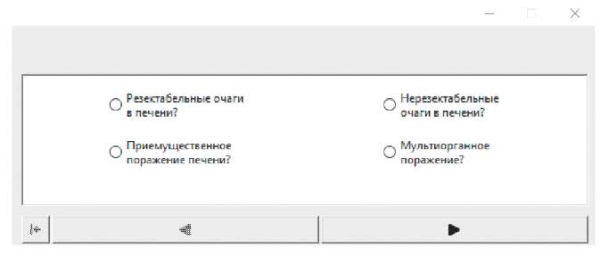
Рис. 2. Блок-схема, интегрированная в программное обеспечение:
выбор особенностей метастатического поражения печени и организма в целом.
Если с момента верификации лечения первичного очага прошло более года, и имеются резектабельные очаги в печени, то блок-схема предлагает выбрать количество очагов: <4 или >4. Данный этап представлен на рисунке 3.

Рис. 3. Блок-схема, интегрированная в программное обеспечение:
выбор количества очагов в печени.
Если очагов <4, то блок-схема предложит их резекцию с дальнейшим наблюдением пациента. Данный этап представлен на рисунке 4.
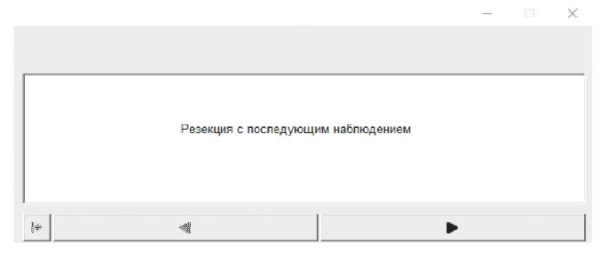
Рис. 4. Блок-схема, интегрированная в программное обеспечение:
выбор в пользу резекции с последующим наблюдением.
Если очагов >4, то блок-схема предложит реализацию ИХП и позволит выбрать вид сосудистого доступа. Для этого предлагается уточнить, выполнялись ли множественные эмболизации артерий печени в анамнезе. Данный этап представлен на рисунке 5.
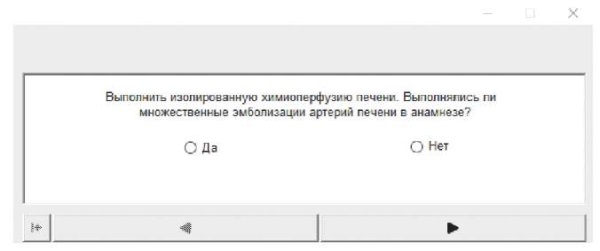
Рис. 5. Блок-схема, интегрированная в программное обеспечение:
выбор вида сосудистого доступа для реализации ИХП.
Подобный интерфейс программного обеспечения имеют и другие этапы выбора. Так, если с момента верификации лечения первичного очага прошло более года и имеются нерезектабельные очаги в печени, то блок-схема предлагает выбрать процент поражения печени согласно данным компьютерной томографии (КТ): <50% или >50%. При поражении <50% предлагается ИХП и далее выбор сосудистого доступа. При поражении >50% предлагается один из видов эмболизации.
Если с момента верификации лечения первичного очага прошло более года и имеется преимущественное поражение печени, то блок-схема предлагает выбрать процент поражения печени согласно данным КТ: <50% или >50%. При поражении <50% предлагается ИХП и далее выбор сосудистого доступа. При поражении >50% предлагается один из видов эмболизации.
Если с момента верификации лечения первичного очага прошло более года и имеется мультиорганное поражение, то блок-схема предлагает только лекарственную терапию заболевания.
Если с момента верификации лечения первичного очага прошло менее года, то блок-схема предлагает выбрать особенность метастатического поражения печени и организма в целом: наличие резектабельных очагов в печени, наличие нерезектабельных очагов в печени, наличие преимущественного поражения печени, наличие мультиорганного поражения.
Если с момента верификации лечения первичного очага прошло менее года и имеются резектабельные очаги в печени, то блок-схема предлагает выбрать количество очагов: <4 или >4. Если очагов <4, то блок-схема предложит их резекцию с сочетанным выполнением ИХП. Если очагов >4, то блок-схема предлагает выполнить только ИХП. Если значение равно 4, то может быть выбран любой из двух пунктов.
Если с момента верификации лечения первичного очага прошло менее года и имеются нерезектабельные очаги в печени, то блок-схема предлагает выбрать процент поражения печени согласно данным КТ: <50% или >50%. При поражении <50% предлагается ИХП и далее выбор сосудистого доступа. При поражении >50% предлагается один из видов эмболизации. Если значение равно 50, то может быть выбран любой из двух пунктов.
Если с момента верификации лечения первичного очага прошло менее года и имеется преимущественное поражение печени, то блок-схема предлагает выбрать процент поражения печени согласно данным КТ: <50% или >50%. При поражении <50% предлагается ИХП и далее выбор сосудистого доступа. При поражении >50% предлагается один из видов эмболизации.
Если с момента верификации лечения первичного очага прошло менее года и имеется мультиорганное поражение, то блок-схема предлагает только лекарственную терапию заболевания.
Программное обеспечение для стратификации риска послеоперационных осложнений ИХП
На основе анализа базы данных 38 клинических случаев ИХП, реализованных в Костромском онкологическом диспансере, мы выделили клинические характеристики пациентов, влияющие на развитие послеоперационных осложнений2.
Среди них предоперационные и интраоперационные параметры. Для каждого из них был рассчитан прогностический коэффициент, отражающий в цифровом эквиваленте влияние фактора на вероятность формирования неблагоприятного исхода. В таблицах 1 и 2 представлены величины прогностических коэффициентов.
Таблица 1
Прогностические коэффициенты для предоперационных факторов
|
Показатель |
Прогностический коэффициент, % |
|
Мужской пол |
1 |
|
Молодой возраст (до 44 лет) |
1 |
|
Утолщение межжелудочковой перегородки >1 см |
5 |
|
Утолщение комплекса интима-медиа общей сонной артерии >1 мм |
3 |
|
Незначимый стеноз внутренней сонной артерии |
1 |
|
Кальциноз внутренней сонной артерии |
1 |
|
Варикозное расширение вен нижних конечностей |
1 |
|
Гипертоническая болезнь |
2 |
|
Сахарный диабет |
10 |
|
Хроническая сердечная недостаточность |
3 |
|
Ишемическая болезнь сердца |
8 |
|
Атеросклеротическое изменение аорты |
3 |
|
Анемия |
6 |
|
COVID-19 в течение 6 мес. до операции |
7 |
|
III класс по классификации ASA |
5 |
|
IV класс по классификации ASA |
7 |
|
Индекс Карновского <90 |
10 |
|
Индекс Чарлсона >9 |
10 |
|
Площадь поверхности тела >1,73 м2 |
6 |
|
Индекс массы тела >24,9 кг/м2 |
9 |
|
Трансартериальная химиоэмболизация печени в анамнезе |
2 |
Таблица 2
Прогностические коэффициенты для интраоперационных факторов
|
Показатель |
Прогностический коэффициент, % |
|
Длительность операции >500 мин |
5 |
|
Длительность перфузии без химиопрепарата >20 мин |
3 |
|
Длительность экстракорпорального кровообращения >90 мин |
3 |
|
Химиоперфузия без bypass, на пережатии нижней полой вены |
8 |
|
Длительность пережатия нижней полой вены >70 мин |
3 |
|
Длительность химиоперфузии с химиопрепаратом >60 мин |
4 |
|
Перфорация внутренней яремной вены |
10 |
|
Разрыв устья правой диафрагмальной вены |
2 |
|
Количество аутотрансфузии через cellserver >700 мл |
5 |
|
Кровопотеря >1500 мл |
10 |
|
pCO2 в конце операции ниже нормы |
3 |
|
pCO2 в конце операции выше нормы |
3 |
|
pO2 в конце операции ниже нормы |
3 |
|
pO2 в конце операции выше нормы |
3 |
|
ctHb в конце операции ниже нормы |
3 |
|
sO2 в конце операции выше нормы |
4 |
|
sO2 в конце операции ниже нормы |
4 |
|
Уровень глюкозы в конце операции >15,0 ммоль/л |
5 |
|
Лактат в конце операции выше нормы 7 ммоль/л |
15 |
|
Общий билирубин в конце операции выше нормы |
4 |
Сумма прогностических коэффициентов отражала риск развития послеоперационных осложнений для пациента, направляющегося на ИХП. Мы определили следующие диапазоны вероятности: 0-30% — низкий риск; 31-60% — средний риск; 61-100% — высокий риск. Полученные расчеты с применением языка программирования Python были интегрированы в программное обеспечение:
- Программное обеспечение, позволяющее определять риск развития осложнений (летальный исход, кровотечение, комбинированная конечная точка) разных способов сосудистого доступа для ИХП3.
- Программное обеспечение, позволяющее рассчитать риск развития послеоперационных осложнений (летальный исход, кровотечение, комбинированная конечная точка) на основе анализа интраоперационных характеристик пациента4.
Ретроспективный анализ программ стратификации риска послеоперационных осложнений ИХП на примере клинических случаев
Клинический пример 1. Женщина, 43 года. Индекс массы тела 25,0 кг/м2. Индекс Карновского =100. Индекс Чарлсона =9. В 2016г заметила острое снижение зрения. Был установлен диагноз: злокачественное новообразование сосудистой оболочки. Выполнена брахитерапия. 15.04.2022 при контрольном обследовании по данным магнитно-резонансной томографии (МРТ) обнаружены метастазы в S5, S6 сегментах печени. По данным трепанобиопсии установлено наличие метастазов УМ в печени. Также по данным ультразвукового исследования органов малого таза визуализирована миома матки (увеличена до 15 нед. беременности).
Консилиумом в составе онколога, хирурга, гинеколога, анестезиолога, реаниматолога принято решение о реализации симультанного оперативного лечения: экстирпация матки с левыми придатками + изолированная артерио-портальная химиогипертермическая перфузия печени мелфаланом.
17.05.2022 реализована запланированная стратегия операции.
Послеоперационный период протекал без особенностей. На 2 сут. после вмешательства пациентка была переведена из отделения реанимации в общую палату. На 16 сут. после операции пациентка выписана из учреждения в удовлетворительном состоянии. При ретроспективной оценке риска осложнений ИХП согласно программе "Программное обеспечение, позволяющее определять риск развития осложнений (летальный исход, кровотечение, комбинированная конечная точка) разных способов сосудистого доступа для изолированной химиоперфузии печени" риск осложнений оценивался как низкий и равнялся 4% (рис. 6).
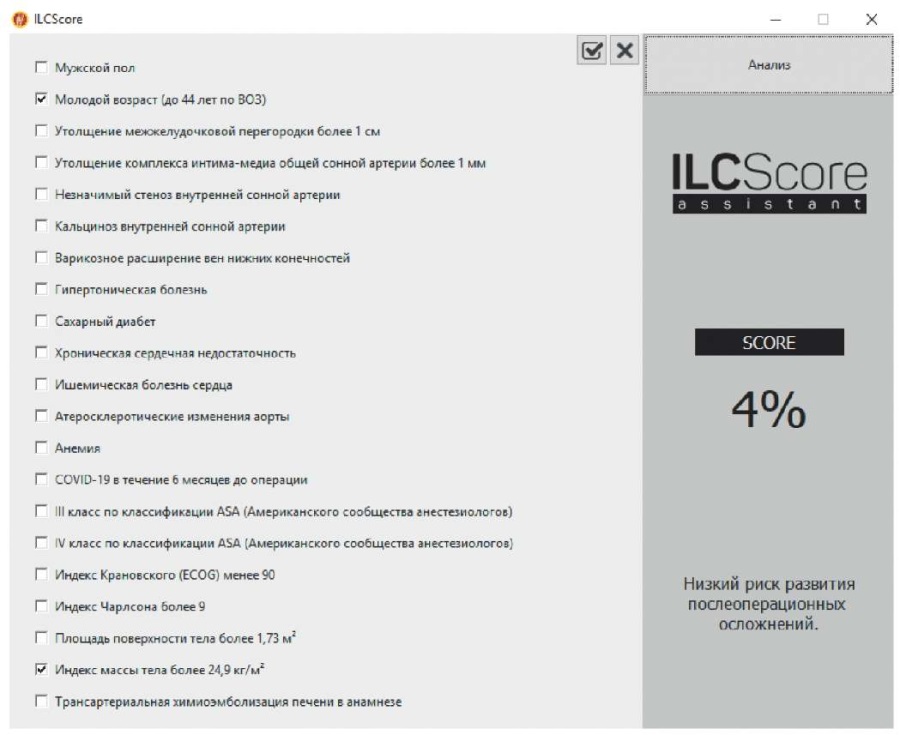
Рис. 6. Ретроспективная оценка риска осложнений ИХП
согласно программе "Программное обеспечение,
позволяющее определять риск развития осложнений
(летальный исход, кровотечение, комбинированная конечная точка)
разных способов сосудистого доступа
для изолированной химиоперфузии печени"
в клиническом примере 1.
При ретроспективной оценке риска осложнений ИХП согласно программе "Программное обеспечение, позволяющее рассчитать риск развития послеоперационных осложнений (летальный исход, кровотечение, комбинированная конечная точка) на основе анализа интраоперационных характеристик пациента" риск осложнений оценивался как низкий и равнялся 10% (рис. 7).

Рис. 7. Ретроспективная оценка риска осложнений ИХП
согласно программе "Программное обеспечение,
позволяющее рассчитать риск развития послеоперационных осложнений
(летальный исход, кровотечение, комбинированная конечная точка)
на основе анализа интраоперационных характеристик пациента"
в клиническом примере 1.
Таким образом, оба программных обеспечения ретроспективно определили низкий риск развития послеоперационных осложнений у пациентки, что подтвердилось положительным исходом лечения.
Клинический пример 2. Мужчина, 55 лет. Индекс массы тела 22,0 кг/м2. Индекс Карновского =90. Индекс Чарлсона =8. В 2018г заметил снижение зрения. Был установлен диагноз: злокачественное новообразование сосудистой оболочки. Выполнена энуклеация правого глаза. Через 3 года при контрольном обследовании по данным МРТ обнаружены метастазы в S8 сегменте печени. По данным трепанобиопсии установлено наличие метастазов УМ в печени.
По данным дуплексного сканирования брахиоцефальных артерий выявлено утолщение комплекса интима-медиа общей сонной артерии до 1,2 мм, кальциноз внутренних сонных артерий. Также у пациента выявлена следующая коморбидная патология: Гипертоническая болезнь II, риск 2; хроническая сердечная недостаточность 2 функционального класса по NYHA; ишемическая болезнь сердца; атеросклероз аорты; хронический панкреатит; хронический колит; дивертикулез сигмовидной кишки.
Консилиумом в составе онколога, хирурга, анестезиолога, реаниматолога принято решение о реализации оперативного лечения: изолированная артерио-портальная химиогипертермическая перфузия печени мелфаланом. 01.11.2022 реализована запланированная стратегия операции. Ранний послеоперационный период протекал без особенностей. Однако 02.11.2022 отмечено нарастание уровня печеночных ферментов, продолжающееся геморрагическое отделяемое по дренажам (1020 мл крови). Принято решение о релапаротомии. По данным повторной операции источником кровотечения явилась задняя верхняя панкреатическая артерия, место кровотечения прошито полипропиленовой нитью 5/0. При ревизии зоны операции общая печеночная артерия не пульсирует. Выполнена артериотомия. В просвете артерии — тромботические массы. Причина тромбоза — отслоившаяся интима. Выполнена тромбэктомия с резекцией интимы. Произведена пластика артерии аутовенозной (из большой подкожной вены) заплатой. В послеоперационном периоде отмечается дальнейшее нарастание печеночной недостаточности с последующим летальным исходом.
При ретроспективной оценке риска осложнений ИХП согласно программе "Программное обеспечение, позволяющее определять риск развития осложнений (летальный исход, кровотечение, комбинированная конечная точка) разных способов сосудистого доступа для изолированной химиоперфузии печени" риск осложнений оценивался как средний и равнялся 31% (рис. 8).

Рис. 8. Ретроспективная оценка риска осложнений ИХП
согласно программе "Программное обеспечение,
позволяющее определять риск развития осложнений
(летальный исход, кровотечение, комбинированная конечная точка)
разных способов сосудистого доступа
для изолированной химиоперфузии печени"
в клиническом примере 2.
При ретроспективной оценке риска осложнений ИХП согласно программе "Программное обеспечение, позволяющее рассчитать риск развития послеоперационных осложнений (летальный исход, кровотечение, комбинированная конечная точка) на основе анализа интраоперационных характеристик пациента" риск осложнений оценивался как низкий и равнялся 11% (рис. 9).
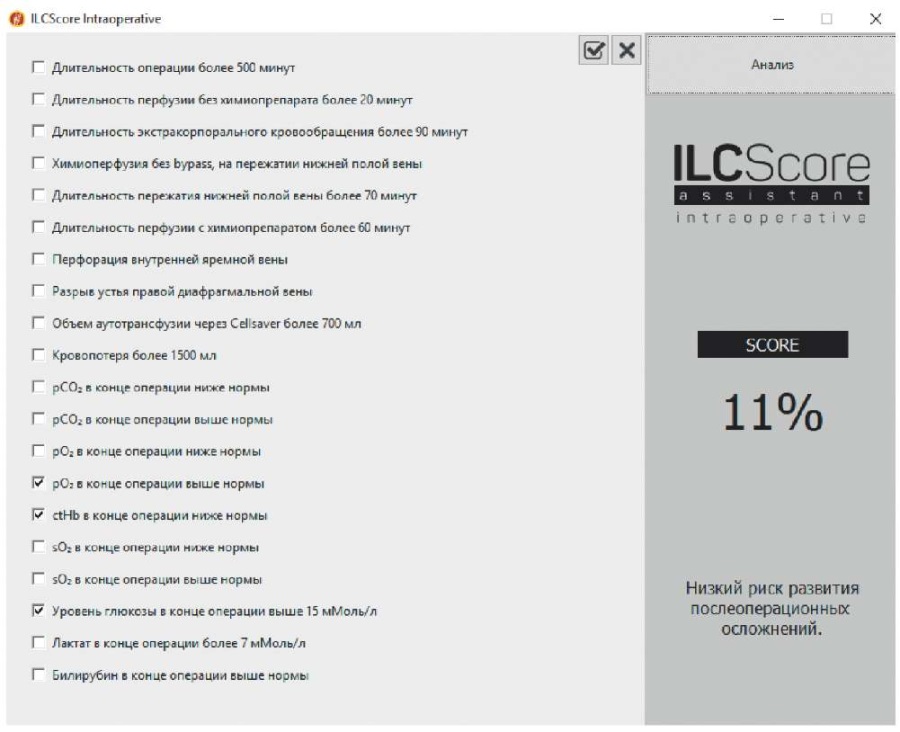
Рис. 9. Ретроспективная оценка риска осложнений ИХП
согласно программе "Программное обеспечение,
позволяющее рассчитать риск развития послеоперационных осложнений
(летальный исход, кровотечение, комбинированная конечная точка)
на основе анализа интраоперационных характеристик пациента"
в клиническом примере 2.
Таким образом, первое программное обеспечение ретроспективно определило средний риск формирования послеоперационных осложнений у пациента, что подтвердилось развитием кровотечения, тромбоза и летального исхода.
Клинический пример 3. Женщина, 68 лет. Индекс массы тела 33,0 кг/м2. Индекс Карновского =100. Индекс Чарлсона =10. В январе 2022г заметила снижение зрения в правом глазу. Был установлен диагноз: злокачественное новообразование сосудистой оболочки. Выполнена поднадкостничная экстерация орбиты справа с сохранением век. Через 3 мес. при контрольном обследовании по данным МРТ обнаружены метастазы в печени (метахромное поражение). По данным трепанобиопсии установлено наличие метастазов УМ в печени.
По данным дуплексного сканирования брахиоцефальных артерий выявлено утолщение комплекса интима-медиа общей сонной артерии до 1,7 мм, гемодинамически незначимые стенозы внутренних сонных артерий. По данным эхокардиографии определено утолщение межжелудочковой перегородки (12 мм), фракция выброса левого желудочка 75%. Также у пациентки выявлена следующая коморбидная патология: Гипертоническая болезнь II, риск 2; хроническая сердечная недостаточность 1 функционального класса по NYHA; ишемическая болезнь сердца; атеросклероз аорты.
Консилиумом в составе онколога, хирурга, анестезиолога, реаниматолога принято решение о реализации оперативного лечения: изолированная артерио-портальная химиогипертермическая перфузия печени мелфаланом. 16.09.2022 реализована запланированная стратегия операции. Нужно добавить, что во время операции появилась необходимость в адреналэктомии справа. При изоляции ретропеченочного сегмента нижней полой вены обычно пересекаются все венозные притоки, в т.ч. правая надпочечниковая вена. Через последнюю, как правило, дренируется до 80% крови. В случае неразвитых коллатералей, которые отводят кровь от надпочечника в правую почечную вену, происходит его критическое полнокровие. Данное состояние может привести к кровотечению в послеоперационном периоде. Поэтому адреналэктомия выполнялась с целью профилактики геморрагических осложнений.
В раннем послеоперационном периоде отмечено поступление кровяного отделяемого по дренажам (1100 мл). Принято решение о проведении релапаротомии. Выявленный источник кровотечения — мышцы передней брюшной стенки. В дальнейшем послеоперационный период протекал без особенностей. Пациентка выписана из учреждения в удовлетворительном состоянии.
При ретроспективной оценке риска осложнений ИХП согласно программе "Программное обеспечение, позволяющее определять риск развития осложнений (летальный исход, кровотечение, комбинированная конечная точка) разных способов сосудистого доступа для изолированной химиоперфузии печени" риск осложнений оценивался как высокий и равнялся 64% (рис. 10).
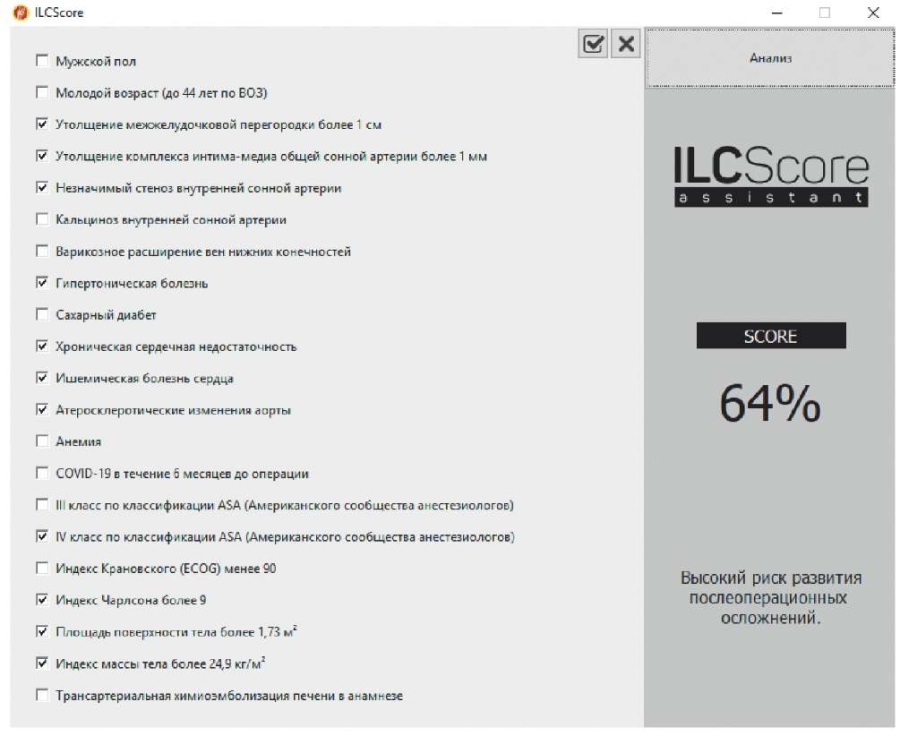
Рис. 10. Ретроспективная оценка риска осложнений ИХП
согласно программе "Программное обеспечение,
позволяющее определять риск развития осложнений
(летальный исход, кровотечение, комбинированная конечная точка)
разных способов сосудистого доступа
для изолированной химиоперфузии печени"
в клиническом примере 3.
При ретроспективной оценке риска осложнений ИХП согласно программе "Программное обеспечение, позволяющее рассчитать риск развития послеоперационных осложнений (летальный исход, кровотечение, комбинированная конечная точка) на основе анализа интраоперационных характеристик пациента" риск осложнений оценивался как низкий и равнялся 14% (рис. 11).

Рис. 11. Ретроспективная оценка риска осложнений ИХП
согласно программе "Программное обеспечение,
позволяющее рассчитать риск развития послеоперационных осложнений
(летальный исход, кровотечение, комбинированная конечная точка)
на основе анализа интраоперационных характеристик пациента"
в клиническом примере 3.
Таким образом, первое программное обеспечение ретроспективно определило высокий риск формирования послеоперационных осложнений у пациента, что подтвердилось развитием кровотечения.
Исследование одобрено Локальным этическим комитетом Российского научного центра хирургии имени академика Б. В. Петровского, г. Москва. Дата 16.02.2023. Выписка из заседания Локального этического комитета № 2 от 16.02.2023г.
Обсуждение
По данным литературы летальность в госпитальном периоде после ИХП может достигать 27%. Среди причин выделяются как сосудистые осложнения (кровотечения, тромбозы), так и общесистемные (печеночная недостаточность, системная полиорганная недостаточность).
В настоящее время существует два зарекомендовавших себя способа создания программного обеспечения стратификации риска послеоперационных осложнений. Первый основан на сложных статистических анализах и возможен при наличии крупных выборок пациентов. При помощи применения бинарного логистического регрессионного анализа определяются предикторы развития осложнений и протективные факторы. На основе их наличия или отсутствия создается программное обеспечение с внедрением в него интегративных показателей (сумма факторов). Такой метод зарекомендовал себя в одном из исследований отечественных авторов, посвященном стратификации риска симультанных вмешательств на коронарном и брахиоцефальном бассейнах [11-15].
Второй способ основан на вычислении прогностических коэффициентов каждого фактора, имеющегося у пациента. Прогностический показатель — математическая величина, выражающаяся в "%", отражающая вероятность развития осложнения. Сумма прогностических коэффициентов демонстрирует общий риск развития неблагоприятных послеоперационных событий у больного. Такая методика хороша тем, что она может применяться для создания программного обеспечения и в больших, и в малых выборках. Так, в исследовании Стрелкова Д. А. и др. компьютерная программа "TAVISCORE" была создана на основе анализа когорты из двух групп: 1 группа (n=61) — открытое протезирование аортального клапана; 2 группа (n=67) — транскатетерная имплантация аортального клапана5. Для каждого из этих вмешательств "TAVISCORE" эффективно рассчитывала риск развития послеоперационных осложнений [16].
В исследовании Закеряева А. Б. и др. было создано программное обеспечение, позволяющее определить риск развития тромбоза шунта и ампутации конечности в отдаленном послеоперационном периоде после бедренно-подколенного шунтирования6. Были проанализированы результаты 473 операций [17]. Авторы выделили шесть видов операций, и для каждого из них на основе прогностических коэффициентов программа рассчитывала вероятность развития указанных осложнений. Наименьшие группы включали 9 пациентов с применением синтетического протеза, 59 — аутовены "in situ" и 73 — вены верхней конечности [17]. Анализ показал эффективность представленного программного обеспечения.
В исследовании Казанцева А. Н. и др. способ расчета прогностических коэффициентов для последующего создания программного обеспечения стратификации риска был реализован на основе самой большой на сегодня выборки из 25812 пациентов [18-21]. Продуктом этой работы стала компьютерная программа carotidscore.ru, позволяющая рассчитывать вероятность развития неблагоприятных кардиоваскулярных событий после каротидной эндартерэктомии [18-21].
Еще один интерактивный калькулятор на основе расчета прогностических коэффициентов был создан Тарасовым Р. С. и Ганюковым В. И.7. Данная разработка позволяет определить оптимальный способ реваскуляризации миокарда при наличии инфаркта миокарда с элевацией сегмента ST [22]. В свою очередь, Черных К. П. и др. предложили программное обеспечение, действующее по такому же принципу и предлагающее персонифицированную оптимальную тактику лечения варикозной болезни нижних конечностей8 [23][24].
Нужно отметить, что существуют иные популярные калькуляторы стратификации риска осложнений: Syntax Score, Euro Score II, STS score [25-27]. Идея их создания основана на определении предикторов развития неблагоприятных кардиоваскулярных событий в результате сложных статистических анализов. Они нашли свое применения в сердечно-сосудистой хирургии и доказали высокую эффективность [25-27]. Однако их минусом является то, что они не способны определять оптимальный способ лечения, как это делают российские разработки.
Наравне с созданием многочисленных программных обеспечений стратификации риска послеоперационных осложнений в сосудистой хирургии набирает популярность направление по внедрению методов компьютерного моделирования [28-30]. В частности, в одном из исследований авторы предложили анализировать потоки крови и физические основы бифуркации сонных артерий после каротидной эндартерэктомии. При выявлении участков с турбулентным кровотоком и зонами застоя крови пациенты относились к больным с высоким риском рестеноза внутренней сонной артерии [28-30]. Это позволяло вести более частый визуализационный скрининг в средне-отдаленном и отдаленном периодах наблюдения для реализации превентивных действий развития ишемического инсульта, связанного с потерей просвета сосуда [28-30].
Предложенные компьютерные программы стратификации риска послеоперационных осложнений ИХП являются первыми во всем мире. Требуется дальнейшее увеличение выборки пациентов с интеграцией результатов лечения в предложенные программные обеспечения для повышения точности и эффективности стратификации риска осложнений ИХП.
Ограничение исследования. Небольшое число клинических наблюдений.
Заключение
Программные обеспечения стратификации риска послеоперационных осложнений ИХП могут применяться мультидисциплинарной командой при выборе способа лечения пациентов с метастазами УМ в печени.
Отношения и деятельность: все авторы заявляют об отсутствии потенциального конфликта интересов, требующего раскрытия в данной статье.
1. Унгурян В. М., Казанцев А. Н., Сироткин А. А., Кравчук В. Н., Ермаков В. С., Петров Л. О., Белов Ю. В. Блок-схема, интегрированная в программное обеспечение, которое позволяет выбирать оптимальный способ сосудистого доступа для реализации изолированной химиоперфузии печени на основе показаний/противопоказаний к каждому из них. Свидетельство о регистрации программы для ЭВМ 2023617557, 11.04.2023. Заявка № 2023616674 от 07.04.2023.
2. Унгурян В. М., Петров Л. О., Казанцев А. Н., Белов Ю. В., Каприн А. Д. Регистр случаев изолированной химиоперфузии печени, выполненной в костромском онкологическом диспансере за период с 2022 по 2023 гг. Свидетельство о регистрации базы данных 2023621367, 02.05.2023. Заявка № 2023621017 от 19.04.2023.
3. Унгурян В. М., Казанцев А. Н., Сироткин А. А., Кравчук В. Н., Ермаков В. С., Петров Л. О., Белов Ю. В. Программное обеспечение, позволяющее определять риск развития осложнений (летальный исход, кровотечение, комбинированная конечная точка) разных способов сосудистого доступа для изолированной химиоперфузии печени. Свидетельство о регистрации программы для ЭВМ 2023615348, 14.03.2023. Заявка № 2023614215 от 09.03.2023.
4. Унгурян В. М., Казанцев А. Н., Сироткин А. А., Кравчук В. Н., Ермаков В. С., Петров Л. О., Белов Ю. В. Программное обеспечение, позволяющее рассчитать риск развития послеоперационных осложнений (летальный исход, кровотечение, комбинированная конечная точка) на основе анализа интраоперационных характеристик пациента. Свидетельство о регистрации программы для ЭВМ 2023616941, 04.04.2023. Заявка № 2023615095 от 21.03.2023.
5. Стрелков Д. А., Зубарев Д. Д., Пищугин А. С., Гурьев В. В., Куликов Д. И., Постникова З. Н., Кравчук В. Н., Жарова А. С., Казанцев А. Н. TAVISCORE. Свидетельство о регистрации программы для ЭВМ 2022666343, 30.08.2022. Заявка № 2022665834 от 29.08.2022.
6. Закеряев А. Б., Виноградов Р. А., Бутаев С. Р., Тумасов Д. М., Бахишев Т. Э., Дербилов А. И., Кравчук В. Н., Казанцев А. Н. Программа для прогнозирования вероятности развития тромбоза бедренно-подколенного шунта и ампутации нижней конечности в отдаленном периоде наблюдения. Свидетельство о регистрации программы для ЭВМ 2022612588, 28.02.2022. Заявка № 2022612036 от 17.02.2022.
7. Тарасов Р. С., Ганюков В. И., Барбараш О. Л., Барбараш Л. С. Способ реваскуляризации множественного поражения коронарного русла при инфаркте миокарда с элевацией сегмента ST. Патент на изобретение RU 2544096 C1, 10.03.2015. Заявка № 2013147211/14 от 22.10.2013.
8. Черных К. П., Казанцев А. Н., Багдавадзе Г. Ш., Лидер Р. Ю., Жарова А. С., Кравчук В. Н. PHLEBOSCORE. Свидетельство о регистрации программы для ЭВМ 2022665852, 22.08.2022. Заявка № 2022664838 от 10.08.2022.
Список литературы
1. Amaro A, Gangemi R, Piaggio F, et al. The biology of uveal melanoma. Cancer Metastasis Rev. 2017;36(1):109-40. doi:10.1007/s10555-017-9663-3.
2. Aronow ME, Topham AK, Singh AD. Uveal Melanoma: 5-Year Update on Incidence, Treatment, and Survival (SEER 1973-2013). Ocul Oncol Pathol. 2018;4(3):145-51. doi:10.1159/000480640.
3. Kaliki S, Shields CL. Uveal melanoma: relatively rare but deadly cancer. Eye (Lond). 2017;31(2):241-57. doi:10.1038/eye.2016.275.
4. Alexander HR Jr, Libutti SK, Pingpank JF, et al. Hyperthermic isolated hepatic perfusion using melphalan for patients with ocular melanoma metastatic to liver. Clin Cancer Res. 2003;9(17):6343-9.
5. Shields CL, Shields JA. Ocular melanoma: relatively rare but requiring respect. Clin Dermatol. 2009;27(1):122-33. doi:10.1016/j.clindermatol.2008.09.010.
6. Ulmer A, Beutel J, Süsskind D, et al. Visualization of circulating melanoma cells in peripheral blood of patients with primary uveal melanoma. Clin Cancer Res. 2008;14(14):4469-74. doi:10.1158/1078-0432.CCR-08-0012.
7. Rowcroft A, Loveday BPT, Thomson BNJ, et al. Systematic review of liver directed therapy for uveal melanoma hepatic metastases. HPB (Oxford). 2020;22(4):497-505. doi:10.1016/j.hpb.2019.11.002.
8. Ben-Shabat I, Belgrano V, Ny L, et al. Long-Term Follow-Up Evaluation of 68 Patients with Uveal Melanoma Liver Metastases Treated with Isolated Hepatic Perfusion. Ann Surg Oncol. 2016;23(4):1327-34. doi:10.1245/s10434-015-4982-5.
9. Yang XY, Xie F, Tao R, et al. Treatment of liver metastases from uveal melanoma: a retrospective single-center analysis. Hepatobiliary Pancreat Dis Int. 2013;12(6):602-6. doi:10.1016/s1499-3872(13)60095-8.
10. Ben-Shabat I, Belgrano V, Hansson C, Olofsson Bagge R. The effect of perfusate buffering on toxicity and response in isolated hepatic perfusion for uveal melanoma liver metastases. Int J Hyperth. 2017;1-17.
11. Тарасов Р.С., Казанцев А.Н., Иванов С.В. и др. Факторы риска неблагоприятного исхода различных хирургических стратегий лечения пациентов с сочетанным поражением коронарного русла и сонных артерий в 30-дневном послеоперационном периоде. Патология кровообращения и кардиохирургия. 2018;22(1):36-48. doi:10.21688/1681-3472-2018-1-36-48.
12. Kazantsev AN, Korotkikh AV, Lider RY, et al. Mathematical Model for the Choice of Tactics of Revascularization in Case of Combined Lesions of the Carotid and Coronary Arteries. Curr Probl Cardiol. 2023;48(1):101436. doi:10.1016/j.cpcardiol.2022.101436.
13. Тарасов Р.С., Казанцев А.Н., Иванов С.В. и др. Хирургическое лечение мультифокального атеросклероза: патология коронарного и брахиоцефального бассейнов и предикторы развития ранних неблагоприятных событий. Кардиоваскулярная терапия и профилактика. 2017;16(4):37-44. doi:10.15829/1728-8800-2017-4-37-44.
14. Казанцев А.Н., Тарасов Р.С., Бурков Н.Н. и др. Госпитальные результаты чрескожного коронарного вмешательства и каротидной эндартерэктомии в гибридном и поэтапном режимах. Ангиология и сосудистая хирургия. 2019;25(1):101-7. doi:10.33529/angio2019114.
15. Тарасов Р.С., Казанцев А.Н., Бурков Н.Н. и др. Структура госпитальных и отдаленных осложнений хирургического лечения стенотических поражений коронарных и сонных артерий. Ангиология и сосудистая хирургия. 2020;26(1):89-95. doi:10.33529/ANGIO2020113.
16. Стрелков Д.А., Зубарев Д.Д., Пищугин А.С. и др. Taviscore — компьютерная программа стратификации риска осложнений после вмешательств на аортальном клапане у пациентов со сниженной фракцией выброса. Российский кардиологический журнал. 2023;28(1):5283. doi:10.15829/1560-4071-2023-5283.
17. Закеряев А.Б., Виноградов Р.А., Сухоручкин П.В. и др. Отдаленные результаты нового способа бедренно-подколенного шунтирования. Российский кардиологический журнал. 2022;27(8):4843. doi:10.15829/1560-4071-2022-4843.
18. Казанцев А. Н., Хасанова Д.Д., Алпацкая А.Д. и др. Carotidscore.ru - стратификация риска осложнений после каротидной эндартерэктомии. Российский кардиологический журнал. 2022;27(5):5031. doi:10.15829/1560-4071-2022-5031. EDN KXSMIZ.
19. Kazantsev A, Korotkikh A, Lider R, et al. Results of carotid endarterectomy with the use of temporary shunts with reduced retrograde pressure in the internal carotid artery - analysis of the multicenter Russian register. Indian J Thorac Cardiovasc Surg. 2023;39(3):244-50. doi:10.1007/s12055-023-01487-7.
20. Kazantsev AN, Korotkikh AV, Unguryan VM, Belov YV. Update in Carotid Disease. Curr Probl Cardiol. 2023;48(6):101676. doi:10.1016/j.cpcardiol.2023.101676.
21. Kazantsev AN, Abdullaev IA, Danilchuk LB, et al. CAROTIDSCORE.RU-The first Russian computer program for risk stratification of postoperative complications of carotid endarterectomy. Vascular. 2022:17085381221124709. doi:10.1177/17085381221124709.
22. Тарасов Р.С., Ганюков В.И. Определение оптимальной стратегии реваскуляризации у больных инфарктом миокарда с элевацией сегмента st при многососудистом поражении коронарного русла при помощи интерактивного калькулятора. Комплексные проблемы сердечно-сосудистых заболеваний. 2015;4:42-52.
23. Черных К. П., Кубачев К.Г., Казанцев А.Н. и др. Предикторы развития реканализации у пациентов с варикозной болезнью нижних конечностей после комбинированной флебэктомии. Медицина в Кузбассе. 2020;19(4):25-32. doi:10.24411/2687-0053-2020-10036.
24. Черных К.П., Кубачев К.Г., Казанцев А.Н. и др. Выраженность клинического эффекта и уровень болевого синдрома у пациентов после эндовазальной лазерной облитерации и комбинированной флебэктомии. Медицина в Кузбассе. 2020;19(2):5-12. doi:10.24411/2687-0053-2020-10011.
25. Вачев А.Н., Терешина О.В., Дмитриев О.В. и др. Факторы риска развития инфаркта миокарда при выполнении операции каротидной эндартерэктомии у пациентов с ишемической болезнью сердца высокого риска. Российский кардиологический журнал. 2022;27(12):5267. doi:10.15829/1560-4071-2022-5267.
26. Прохорихин А.А., Таркова А.Р., Зубарев Д.Д. и др. Хирургические аспекты и непосредственные результаты одноцентрового проспективного регистра транскатетерной имплантации протеза аортального клапана. Российский кардиологический журнал. 2018;(11):77-82. doi:10.15829/1560-4071-2018-11-77-82.
27. Тарасов Р.С., Казанцев А.Н., Барбараш Л. С. и др. Результаты целесообразной неполной реваскуляризации миокарда с использованием миниинвазивной и стандартной техники коронарного шунтирования. Российский кардиологический журнал. 2018;(7):47-52. doi:10.15829/1560-4071-2018-7-47-52.
28. Kazantsev AN, Korotkikh AV, Lider RY, et al. Computer Modeling of Carotid Endarterectomy With the Different Shape Patches and Prediction of the Atherosclerotic Plaque Formation Zones. Curr Probl Cardiol. 2023;48(2):101505. doi:10.1016/j.cpcardiol.2022.101505.
29. Казанцев А.Н., Виноградов Р.А., Захаров Ю.Н. и др. Прогнозирование рестеноза после каротидной эндартерэктомии методом компьютерного моделирования. Неотложная медицинская помощь. Журнал им. Н.В. Склифосовского. 2021;10(2):401-7. doi:10.23934/2223-9022-2021-10-2-401-407.
30. Казанцев А. Н., Бурков Н. Н., Борисов В. Г. и др. Компьютерное моделирование гемодинамических показателей в бифуркации сонных артерий после каротидной эндартерэктомии. Ангиология и сосудистая хирургия. 2019;25(3):107-12. doi:10.33529/ANGIO2019311.
Об авторах
В. М. УнгурянУнгурян Владимир М. — кандидат медицинских наук, главный врач
Кострома
А. Н. Казанцев
Россия
Казанцев Антон Николаевич — заведующий отделением сосудистой хирургии, заведующий отделением кардиохирургии, главный внештатный сердечно-сосудистый хирург Костромской области
Кострома, Москва
А. В. Коротких
Коротких Александр В. — главный врач
Благовещенск
С. А. Иванов
Иванов Сергей А. — доктор медицинских наук, профессор, директор
Обнинск
Ю. В. Белов
Белов Юрий В. — академик РАН, профессор, доктор медицинских наук, директор; заведующий кафедрой госпитальной хирургии
Москва
А. Д. Каприн
Каприн Андрей Д. — доктор медицинских наук, профессор, академик РАН, директор
Москва
Дополнительные файлы
Рецензия
Для цитирования:
Унгурян В.М., Казанцев А.Н., Коротких А.В., Иванов С.А., Белов Ю.В., Каприн А.Д. Персонифицированный выбор сосудистого доступа для реализации изолированной химиоперфузии печени: анализ программ стратификации риска осложнений. Российский кардиологический журнал. 2023;28(7):5486. https://doi.org/10.15829/1560-4071-2023-5486
For citation:
Unguryan V.M., Kazantsev A.N., Korotkikh A.V., Ivanov S.A., Belov Yu.V., Kaprin A.D. Personalized choice of vascular access for isolated hepatic perfusion: analysis of complication risk stratification programs. Russian Journal of Cardiology. 2023;28(7):5486. (In Russ.) https://doi.org/10.15829/1560-4071-2023-5486
JATS XML

















































