Перейти к:
Комплексная оценка исходов острого инфаркта миокарда нижней стенки по данным эхокардиографии у пациентов после чрескожного коронарного вмешательства
https://doi.org/10.15829/1560-4071-2023-5438
Аннотация
Цель. Выделить значимые эхокардиографические (ЭхоКГ) показатели при скрининговой оценке отдаленных исходов острого инфаркта миокарда (ОИМ) нижней стенки с первичным чрескожным коронарным вмешательством (ЧКВ) с использованием логистической регрессионной модели.
Материал и методы. В исследование вошли результаты обследования 144 человек с нижним ОИМ с первичным ЧКВ при поступлении, выписке и через 6, 12, 24 мес. после выписки. В логистический регрессионный анализ по выявлению значимых для скрининговой оценки исходов нижнего ОИМ включили 184 переменных, в т.ч. 131 ЭхоКГ. Дисперсионный анализ проводили с использованием метода ANOVA Type II, качество моделей оценивалось с использованием теста отношения правдоподобия и критерия Акаике.
Результаты. У пациентов с нижним ОИМ и проведенным первичным ЧКВ в 59,7% случаев наблюдали неблагоприятные исходы в виде повторных инфаркта миокарда и ЧКВ, аортокоронарного шунтирования, развития хронической сердечной недостаточности 2 стадии и/или повторных госпитализаций. Для отдаленного прогноза нижнего ОИМ значимыми ЭхоКГ предикторами помимо общепризнанных (фракции выброса левого желудочка, митрального Е/А, индекса объема левого предсердия и суммарного индекса движения стенки — WMSI) выступили измеренные в импульсноволновом режиме тканевого допплера показатели, характеризующие состояние правого желудочка (трикуспидальные S’ и e’) и рассчитанные по спекл-трекинг технологии — циркулярная деформация медиального уровня, продольные деформации апикального и базального уровней левого желудочка, продольная деформация сегментов, входящих в территорию кровоснабжения огибающей артерии.
Заключение. ЭхоКГ-показатели с использованием тканевого допплера и спекл-трекинг технологии доказали значимость при скрининговой оценке исходов ОИМ нижней стенки с ЧКВ.
Ключевые слова
Для цитирования:
Акрамова Э.Г., Савельев А.А., Хамитова Р.Я., Власова Е.В. Комплексная оценка исходов острого инфаркта миокарда нижней стенки по данным эхокардиографии у пациентов после чрескожного коронарного вмешательства. Российский кардиологический журнал. 2023;28(7):5438. https://doi.org/10.15829/1560-4071-2023-5438
For citation:
Akramova E.G., Savelyev A.A., Khamitova R.Ya., Vlasova E.V. Comprehensive assessment of the outcomes of inferior wall myocardial infarction according to echocardiography in patients after percutaneous coronary intervention. Russian Journal of Cardiology. 2023;28(7):5438. (In Russ.) https://doi.org/10.15829/1560-4071-2023-5438
По данным Всемирной организации здравоохранения (2017), ежегодно в мире регистрируют >15 млн новых случаев инфаркта миокарда (ИМ). На протяжении многих лет острый ИМ (ОИМ) остается ведущей причиной смертности взрослого населения.
До 30-50% всех инфарктов поражают нижнюю стенку левого желудочка (ЛЖ) [1]. В госпитальный и краткосрочный период нижний ИМ имеет лучший прогноз, чем передний. Однако осложнение в острый период высокой атриовентрикулярной блокадой и/или инфарктом правого желудочка (ПЖ) повышает внутригоспитальную летальность с 2-9% до 12-17% [2]. Совершенствование тактики лечения под контролем новых технологий улучшает течение ОИМ. Так, использование в клинической практике реперфузии снижает смертность при ОИМ и в сочетании с инфарктом ПЖ; установка временного электрокардиостимулятора улучшает прогноз при возникновении атриовентрикулярной блокады 2-3 степени [3][4]. Тромболизис и чрескожное коронарное вмешательство (ЧКВ) увеличивают выживаемость пациентов с ОИМ в острый период, но не уменьшают частоту повторных госпитализаций [5].
Подавляющее большинство исследований по прогнозным оценкам ОИМ основано на клинических, лабораторных и коронароангиографических (КАГ) показателях. Калькуляторы, программы и модели расчета риска возникновения осложнений при ОИМ, как правило, не включают широкий спектр параметров эхокардиографии (за исключением фракции выброса (ФВ) ЛЖ), хотя данный визуализирующий метод рекомендован как российским стандартом оказания медицинской помощи при ОИМ с подъемом сегмента ST, так и комплексным алгоритмом ранней стратификации сердечно-сосудистого риска [6].
Одной из причин, возможно, является многообразие используемых приборов, технологий, показателей эхокардиографического (ЭхоКГ) обследования и уровня квалификации специалистов, что существенно расширяет качественный и количественный диапазон получаемых результатов и затрудняет их интерпретацию в конкретной ситуации. Большое количество данных и недостаточно изученные их взаимосвязи, определяющие метод лечения пациента, свидетельствуют о важности применения многомерных статистических методов их анализа как для разработки прогностических программ, так и систем поддержки принятия врачебных решений.
Цель: выделить наиболее значимые ЭхоКГ-показатели при комплексной оценке отдаленных исходов ОИМ нижней стенки с первичным ЧКВ с использованием логистической регрессионной модели.
Материал и методы
В когортное проспективное исследование вошли результаты обследования 144 человек (116 мужчин в возрасте до 65 лет и 28 женщин до 60 лет) с нижним ОИМ, госпитализированных в Медсанчасть Казанского федерального университета в 2019-2021гг, при поступлении, выписке и через 6, 12, 24 мес. после выписки.
В математический анализ включили 184 параметра: 131 ЭхоКГ, 15 клинико-анамнестических, 9 биохимических, 1 электрокардиографический, 2 КАГ, 7 ЧКВ, 17 холтеровского мониторирования и 2 дуплексного сканирования сонных артерий.
Эхокардиографию проводили на ультразвуковом сканере Epiq-7 (Philips, США) в двухмерном, М-, импульсноволновом и постоянноволновом режимах, цветовом и тканевом допплере. Глобальную, сегментарную продольную (LS) и циркулярную деформацию (CS) ЛЖ и ПЖ сердца рассчитывали по спекл-трекинг технологии.
Нормальность распределения вариационных рядов проверяли с помощью критерия Колмогорова-Смирнова: при нормальном распределении указывали среднее значение со стандартным отклонением, в случае отклонения от нормального — медиану и интерквартильный размах 25-75% Me [Q1; Q3]. На всех этапах статистического анализа приводили значение статистической вероятности (p), за критический уровень которого принимали величину 0,05. По коэффициенту детерминации линии тренда (R2) оценивали динамику показателей: чем больше его значение, тем выше соответствие фактического ряда и тренда; при значении R2<0,6 точность прогноза снижается. Статистическую значимость различий временных рядов определяли по критерию Манна-Уитни (U-критерия).
Прогнозная модель, вычисляющая вероятность (p) возникновения сердечно-сосудистых событий в определенный период времени с указанием границ 95% доверительного интервала у пациентов с нижним ОИМ, которым было выполнено первичное ЧКВ, строилась в системе статистического анализа с использованием языка программирования R (R Core Team (2018))1. Модель строилась последовательным добавлением значимых переменных, для оценки значимости использовались статистические критерии отношения правдоподобия и тест Акаике.
Использовали программу Statistica 6 и надстройку для Microsoft Excel AtteStat: версия 12.0.5 (И. П. Гайдышев, Россия).
Работа одобрена локальным этическим комитетом при ФГБОУ ВО "Казанский (Приволжский) Федеральный Университет" 04.10.2022 (протокол № 38). Все участники исследования подписывали информированное добровольное согласие.
Результаты
При проведении ЧКВ у 46/31,9% пациентов с нижним ОИМ из 144 человек, включенных в анализ, возникали осложнения: реперфузионный синдром, массивный протяженный тромбоз коронарной артерии, появление пароксизмальных нарушений ритма и эпизодов нарушения проводимости, в т.ч. желудочковой тахикардии, фибрилляции желудочков, потребовавшие электроимпульсной терапии. Реперфузионный синдром наблюдали у 8/5,6%; установка временного электрокардиостимулятора потребовалась у 10/6,9%. Один пациент был исключен из анализа из-за смерти после оперативного вмешательства — пластики осложнённой аневризмы с вторичным дефектом межжелудочковой перегородки.
По результатам, полученным через 2 года после выписки из стационара, пациентов разделили на две группы: с благоприятным (отсутствовали жалобы, повторные госпитализации и оперативные кардиоваскулярные вмешательства) у 58/40,3% и неблагоприятным исходом у 86/59,7% пациентов, проявляющимся различными событиями (рис. 1).
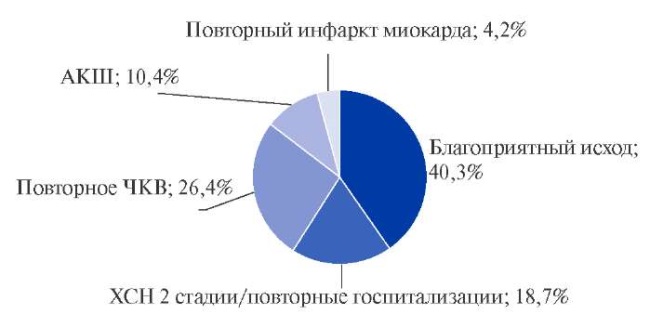
Рис. 1. Структура исходов нижнего ОИМ за 2 года после первичного ЧКВ.
Сокращения: АКШ — аортокоронарное шунтирование,
ХСН — хроническая сердечная недостаточность,
ЧКВ — чрескожное коронарное вмешательство.
В 41% случаев неблагоприятные события возникали в течение 6 мес. после выписки. Раньше других развивался повторный инфаркт — медиана постгоспитального периода после выписки из стационара до его развития равнялась 1,1 нед. Аналогичный показатель в отношении аортокоронарного шунтирования соответствовал 3 нед., повторного ЧКВ — 4 нед., развития хронической сердечной недостаточности (ХСН) 2 стадии и/или повторных госпитализаций 4,5 нед. (рис. 2).
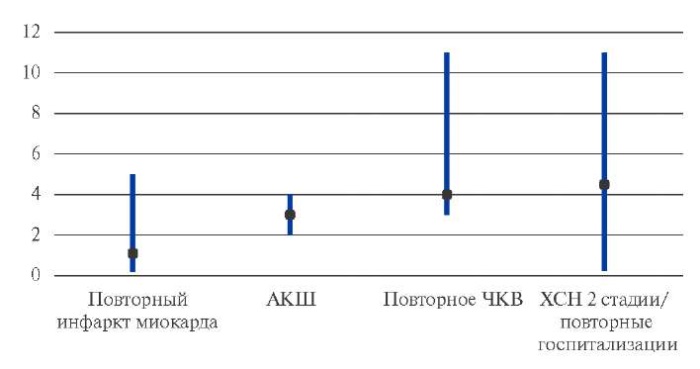
Рис. 2. Медианы [Q1; Q3] периода появления осложнений
при нижнем ОИМ и проведения первичного ЧКВ.
По вертикали — время в неделях.
Сокращения: АКШ — аортокоронарное шунтирование,
ХСН — хроническая сердечная недостаточность,
ЧКВ — чрескожное коронарное вмешательство.
Среди 131 ЭхоКГ-показателя в группе с благоприятным исходом только два статистически значимо были лучше, чем при неблагоприятных исходах — ФВ ЛЖ и WMSI (Wall Motion Score Index — суммарный индекс движения стенки). Если в группе с благоприятным течением нижнего ОИМ после ЧКВ медиана ФВ ЛЖ равнялась 55% [ 52; 58], то в группе с осложнениями — 52% [ 48; 56] при p=0,003; медианы WMSI — 1,12 [ 1,06; 1,19] и 1,19 [ 1,13; 1,31], соответственно, при р=0,005.
Из 15 клинико-анамнестических показателей статистически значимые различия между группами по течению постгоспитального периода определились только по структуре ХСН: при благоприятном исходе у всех 58 человек развивалась ХСН 1 стадии, тогда как среди лиц с неблагоприятным исходом ХСН 1 стадии лишь у 64% (p=0,0002). У остальных 36% (31 пациент) диагностировали ХСН 2 стадии.
Скрининговый прогноз отдаленных клинических исходов предполагает использование ограниченного числа предикторов, поэтому на начальном этапе их ранжировали по значимости методом ANOVA, Type II с использованием отношения правдоподобия. Этот тест, как и информационный критерий Акаике, позволяет оценить значимость улучшения модели при добавлении переменной. Оптимальная модель строилась последовательно, в первую очередь добавлялись наиболее значимые переменные.
Нелинейный характер зависимостей осложняет прогнозирование исходов. Так, следует учитывать влияние выхода предиктора за границы нормы на вероятность неблагоприятного исхода, и практически отсутствие такого влияния, если предиктор находится в допустимых границах. ЭхоКГ-показатели имели потенциально нелинейные зависимости от исхода ОИМ, поэтому предварительно ультразвуковые показатели преобразовали в нормированные безразмерные переменные, которые отмечены как "norm" (табл. 1). Для нормированных переменных коэффициент со знаком "+" означает, что вероятность благоприятного исхода повышается по мере увеличения выхода их значений за границы нормальности; знак "-" свидетельствует о росте вероятности неблагоприятных исходов. Нормированные переменные имеют ненулевые значения только при выходе предиктора за допустимые границы.
Таблица 1
Коэффициенты логистической регрессионной модели
развития неблагоприятных постгоспитальных событий
у пациентов с нижним ОИМ и их значимости
|
Показатель |
Коэффициент |
SE |
р |
|
Трикуспидальный S’.norm |
58,43 |
21,58 |
0,007 |
|
Индекс левого предсердия.norm |
18,29 |
6,53 |
0,005 |
|
ФВ ЛЖ.norm |
6,62 |
1,88 |
0,0004 |
|
LS территории ОА.norm |
1,92 |
0,57 |
0,0007 |
|
CS на медиальном уровне.norm |
0,22 |
0,07 |
0,001 |
|
Постгоспитальный период |
0,12 |
0,02 |
<0,0001 |
|
ЧСС |
0,05 |
0,02 |
0,006 |
|
Объем использованного контраста |
-0,006 |
0,002 |
0,003 |
|
WMSI.norm |
-0,12 |
0,04 |
0,002 |
|
LS на базальном уровне.norm |
-0,97 |
0,34 |
0,005 |
|
ХСН |
-1,82 |
0,34 |
<0,0001 |
|
LS на апикальном уровне.norm |
-2,24 |
0,56 |
<0,0001 |
|
Митральный Е/А |
-3,17 |
1,11 |
0,004 |
|
Трикуспидальный e’.norm |
-35,80 |
10,57 |
0,0007 |
Сокращения: митральный Е/А — соотношение раннего и позднего диастолических пиков трансмитрального потока, ОА — огибающая артерия, трикуспидальный e’ — ранняя диастолическая скорость движения латеральной части трикуспидального кольца в импульсноволновом режиме тканевого допплера, трикуспидальный S’ — систолическая скорость движения латеральной части трикуспидального кольца в импульсноволновом режиме тканевого допплера, ФВ ЛЖ — фракция выброса левого желудочка, ХСН — хроническая сердечная недостаточность, ЧСС — частота сердечных сокращений, CS — циркулярная деформация, LS — продольная деформация, SE — стандартная ошибка, WMSI — Wall Motion Score Index, суммарный индекс движения стенки.
Достаточным уровнем значимости для скрининговой оценки исходов нижнего ОИМ среди 184 ковариантов обладали 14 переменных (табл. 1): 1. постгоспитальный период; 2. частота сердечных сокращений; 3. ХСН; 4. объем контраста, использованного при проведении КАГ и ЧКВ; 5. ФВ ЛЖ; 6. WMSI; 7. соотношение объема левого предсердия (ЛП) и площади поверхности тела (индекс ЛП); 8. соотношение раннего и позднего диастолических пиков трансмитрального потока (митральный Е/А); 9. систолическая скорость движения латеральной части трикуспидального кольца в импульсноволновом режиме тканевого допплера (трикуспидальный S’); 10. ранняя диастолическая скорость движения латеральной части трикуспидального кольца в импульсноволновом режиме тканевого допплера (трикуспидальный e’); 11. CS на медиальном уровне ЛЖ; 12. LS на территории огибающей артерии; 13. LS на базальном уровне ЛЖ; 14. LS на апикальном уровне ЛЖ.
Переменной, максимально улучшающей модель, которая статистически значимо отличалась от предыдущего варианта, оказалась "постгоспитальный период" (рис. 3). Зависимость исхода нижнего ОИМ после проведения ЧКВ от данного показателя имела выраженно нелинейный вид, что отчасти обозначилось и в отношении другой переменной — "объем контраста, используемого при проведении КАГ и ЧКВ".
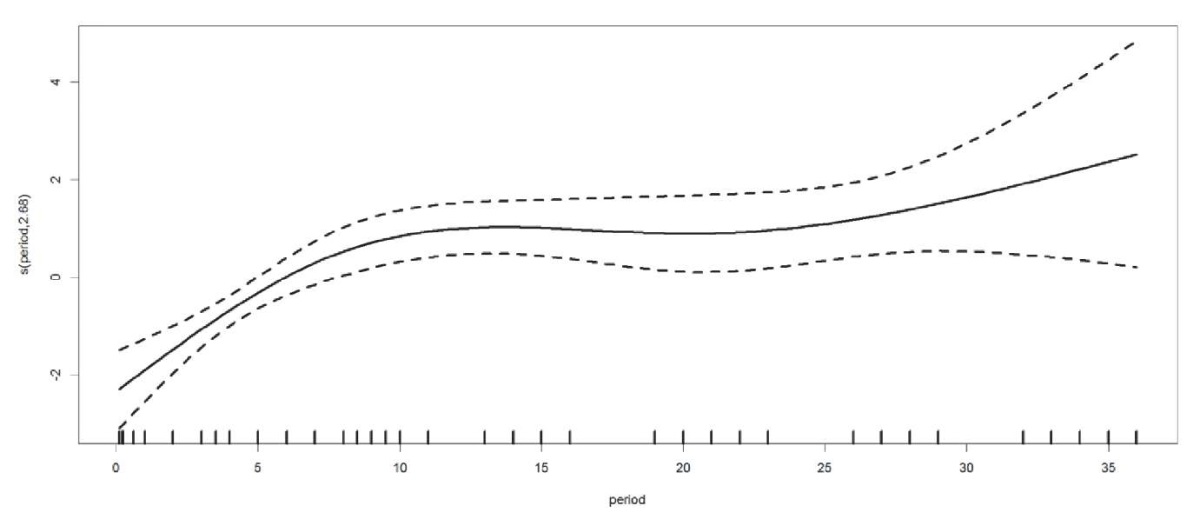
Рис. 3. Нелинейная зависимость исхода нижнего ОИМ
от "постгоспитального периода".
Вероятность благоприятного исхода нижнего ОИМ после ЧКВ возрастала по мере повышения величины трикуспидального S’, индекса ЛП, ФВ ЛЖ, LS сегментов на территории огибающей артерии, CS на медиальном уровне ЛЖ. Прогноз улучшался по мере удлинения постгоспитального периода и увеличения частоты сердечных сокращений.
Вместе с тем выход величины WMSI, LS на базальном и апикальном уровнях ЛЖ, митрального Е/А, трикуспидального e’ за границу нормированных значений свидетельствует о высокой вероятности неблагоприятного прогноза. Ухудшало прогноз увеличение использованного объема контраста и стадии ХСН.
Отобранные 14 переменных высоко значимо коррелировали с исходом нижнего ОИМ после проведения ЧКВ и слабо между собой. Логистическая регрессионная модель, прогнозирующая развитие неблагоприятных постгоспитальных событий у пациентов с нижним ОИМ, созданная на основе этих переменных, обладает чувствительностью 83%, специфичностью 80% и коэффициентом AUC (площадь под кривой ROC) равной 0,876 при прогнозировании благоприятного постгоспитального исхода нижнего ОИМ. Псевдо-R2 для построенной модели составляет 47,2% (p<0,0001).
Обсуждение
ИМ является одним из наиболее серьезных осложнений ишемической болезни сердца и глобальной проблемой общественного здоровья с высокими российскими показателями заболеваемости и смертности, соответствуя в 2019г 141,4 и 37,3 случаям на 100 тыс. населения [7]. Согласно официальной статистике за 15-летний период наблюдается тенденция снижения первичного ИМ как в регионах, так и по России при статистически значимом снижении смертности по стране и лишь тенденции на региональном уровне (рис. 4). Приведенные данные мотивируют к поиску путей снижения смертности и увеличения продолжительности жизни населения.
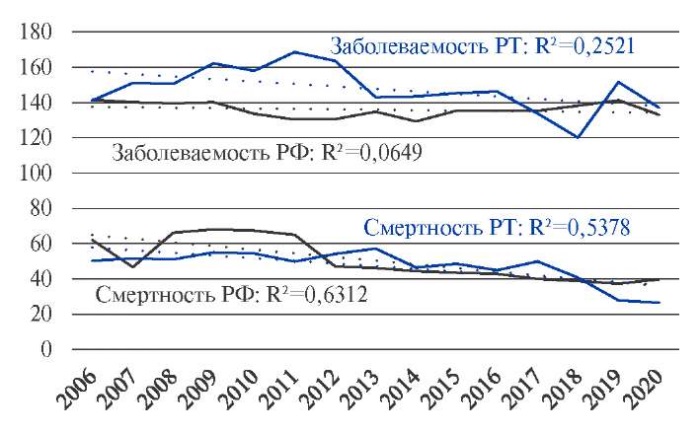
Рис. 4. Показатели заболеваемости и смертности от ОИМ на 100 тыс. населения
Российской Федерации (РФ) и Республики Татарстан (РТ).
Из 14 переменных значимо взаимосвязанных с исходами нижнего ОИМ после первичного ЧКВ 10 оказались ЭхоКГ, из которых 4 показателя получены с помощью спекл-трекинг технологии.
Значения ФВ ЛЖ и WMSI основаны на визуальной оценке систолических движения и утолщения стенки ЛЖ, что определяет их низкую воспроизводимость, т.к. зависят от квалификации врача. Спекл-трекинг технология корректирует субъективную оценку глобальной и локальной систолической функции сердца полуавтоматической цифровой. Другим достоинством данной технологии является возможность измерения деформации в трех направлениях: продольном, циркулярном и радиальном. Обычно в клинический анализ включают только глобальную LS ЛЖ, являющуюся среднеарифметическим значением LS 17 сегментов, как наиболее воспроизводимую и проще интерпретируемую. Карта-схема ЛЖ детализирует степень деформации отдельных сегментов ЛЖ, проявляясь локальным изменением цветовой маркировки "бычьего глаза" (рис. 5).
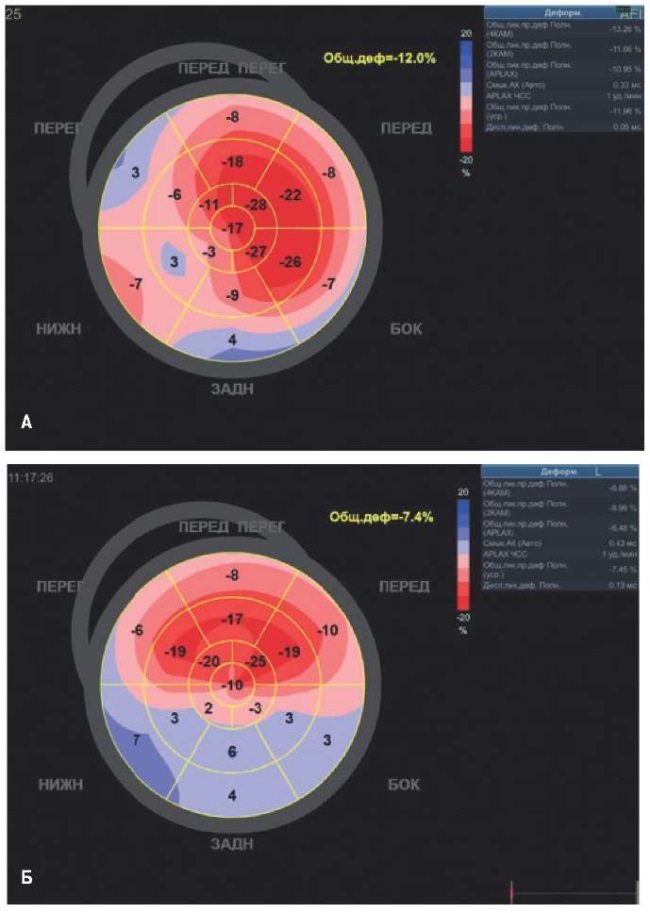
Рис. 5. Глобальная и LS ЛЖ по спекл-трекинг технологии.
Пример "бычьего глаза" пациента с ОИМ:
А — нижней стенки ЛЖ, Б — нижней и нижнебоковой стенок ЛЖ.
Примечание: цветное изображение доступно в электронной версии журнала.
Среди прогностически значимых ультразвуковых показателей 4 были получены спекл-трекинг эхокардиографией: CS на медиальном уровне, LS на территории кровоснабжения огибающей артерии, базальном и апикальном уровнях. Следовательно, для прогноза исхода нижнего ОИМ важно не только состояние сократимости сегментов ЛЖ, входящих в зону кровоснабжения правой коронарной артерии, но и снижение деформации сегментов территории кровоснабжения левой коронарной артерии и ее ветвей — огибающей и передней нисходящей. Статистически значимыми при прогностической оценке исхода нижнего ОИМ определились изменения трикуспидальных S’ и e’, характеризующих соответственно систолическую и диастолическую функции ПЖ.
Известно, что циркулярные миофибриллы в большей степени расположены в субэпикардиальном слое миокарда желудочков, а продольные — в субэндокардиальном. По-видимому, снижение сегментарной CS позволяет косвенно судить о глубине некроза и объясняет ее сохранность на ранней стадии инфаркта в отличие от продольной [8]. При ОИМ сохранность CS отражает вероятность восстановления систолической функции ЛЖ в долгосрочной перспективе, тогда как прогностическая значимость LS не так однозначна [5]. Использование показателей спекл-трекинг технологии повышает объективность индивидуального прогноза в острый период. Тем не менее, по данным Европейской ассоциации сердечно-сосудистой визуализации, из 96 лабораторий по эхокардиографии программу спекл-трекинг визуализации используют повседневно 37% и иногда — 59% [9].
Согласно российским "Стандартам медицинской помощи взрослым при остром инфаркте миокарда с подъемом сегмента ST электрокардиограммы (диагностика, лечение и диспансерное наблюдение)" от 10 июня 2021г № 612н периодичность на протяжении 1 года после выписки консультации кардиолога должна быть ежемесячной, диспансерный прием — 1 раз в 4 мес. и ЭхоКГ обследование 1 раз в 6 мес. Для повышения эффективности ЭхоКГ обследования на постгоспитальном этапе в вышеуказанный стандарт следует внести пункт о важности использования спекл-трекинг технологии для оценки состояния ЛЖ и импульсноволнового режима тканевого допплера — ПЖ. Согласно рисунку 3 вероятность неблагоприятного события после нижнего ОИМ достигает плато через 12 мес. и держится на одном уровне до 25 мес., подтверждая обоснованность действующего графика наблюдения за данным контингентом. Развитие у пациента неблагоприятных событий через год после выписки с большой вероятностью обусловлено различными внутренними и внешними факторами и в минимальной степени осложнением после ОИМ.
Внедрение в практику многомерного статистического анализа данных обследования пациента с нижним ОИМ и первичным ЧКВ с расширенным перечнем ЭхоКГ-показателей, полученных различными технологиями, для скрининговой оценки постгоспитального исхода требует проведения перекрестной проверки модели в других медицинских учреждениях. Данный этап позволит придать ей устойчивости к возможному влиянию артефактов и оптимизировать перечень значимых переменных.
Заключение
У пациентов с нижним ОИМ и проведенным первичным ЧКВ в 59,7% случаев наблюдали неблагоприятные исходы в виде повторных ИМ и ЧКВ, аортокоронарного шунтирования, развития ХСН 2 стадии и/или повторных госпитализаций. Прогностически значимыми для отдаленных исходов нижнего ОИМ выступили 14 переменных, из которых 10 оказались ЭхоКГ, в т.ч. 4 классических (ФВ ЛЖ, WMSI, митральный Е/А и индекс объема ЛП), 2 полученных в импульсноволновом режиме тканевого допплера о функции ПЖ (трикуспидальные S’ и e’) и 4 спекл-трекинг технологией, характеризующих сократимость ЛЖ (CS на медиальном уровне, LS на территории кровоснабжения огибающей артерии, базальном и апикальном уровнях).
Отношения и деятельность: все авторы заявляют об отсутствии потенциального конфликта интересов, требующего раскрытия в данной статье.
1. R: A language and environment for statistical computing. R Foundation for Statistical Computing, Vienna, Austria. URL: https://www.R-project.org/.
Список литературы
1. Hattab FE, Radi FZ, Hara L, et al. Infarctus du myocarde inférieur: première série marocaine, à propos de 103 cas [Inferior myocardial infarction: first Moroccan study of 103 cases]. Pan. Afr. Med. J. 2019;33:74. French. doi:10.11604/pamj.2019.33.74.16047.
2. Kumar V, Sinha S, Kumar P, et al. Short-term outcome of acute inferior wall myocardial infarction with emphasis on conduction blocks: a prospective observational study in Indian population. Anatol J Cardiol. 2017;17(3):229-34. doi:10.14744/AnatolJCardiol.2016.6782.
3. Hu M, Lu Y, Wan S, et al. China Acute Myocardial Infarction Registry Investigators. Long-term outcomes in inferior ST-segment elevation myocardial infarction patients with right ventricular myocardial infarction. Int J Cardiol. 2022;351:1-7. doi:10.1016/j.ijcard.2022.01.003.
4. Yanase T, Sakakura K, Jinnouchi H, et al. Factors associated with temporary pacing insertion in patients with inferior ST-segment elevation myocardial infarction. PLoS One. 2021;16(5):e0251124. doi:10.1371/journal.pone.0251124.
5. Mangion K, McComb C, Auger DA, et al. Magnetic Resonance Imaging of Myocardial Strain After Acute ST-Segment-Elevation Myocardial Infarction: A Systematic Review. Circ Cardiovasc Imaging. 2017;10(8):e006498. doi:10.1161/CIRCIMAGING.117.006498.
6. Prastaro M, Pirozzi E, Gaibazzi N, et al. Expert Review on the Prognostic Role of Echocardiography after Acute Myocardial Infarction. J. Am. Soc. Echocardiogr. 2017;30(5):431-43.e2. doi:10.1016/j.echo.2017.01.020.
7. Шальнова С.А., Драпкина О.М., Куценко В.А. от имени участников исследования ЭССЕ-РФ. Инфаркт миокарда в популяции некоторых регионов России и его прогностическое значение. Российский кардиологический журнал. 2022;27(6):4952. doi:10.15829/1560-4071-2022-4952.
8. Tomoaia R, Beyer RS, Simu G, et al. Understanding the role of echocardiography in remodeling after acute myocardial infarction and development of heart failure with preserved ejection fraction. Med Ultrason. 2019;21(1):69-76. doi:10.11152/mu-1768.
9. Ajmone Marsan N, Michalski B, Cameli M, et al. EACVI survey on standardization of cardiac chambers quantification by transthoracic echocardiography. Eur Heart J Cardiovasc Imaging. 2020;21(2):119-23. doi:10.1093/ehjci/jez297.
Об авторах
Э. Г. АкрамоваРоссия
Доктор медицинских наук, доцент, врач отделений ультразвуковой и функциональной диагностики, медико-санитарная часть; профессор кафедры профилактической медицины Института фундаментальной медицины и биологии
Казань
А. А. Савельев
Россия
Доктор биологических наук, профессор, ведущий научный сотрудник учебно-научной лаборатории "Центр агро- и экобиотехнологий" Института экологии и природопользования
Казань
Р. Я. Хамитова
Россия
Доктор медицинских наук, профессор, профессор кафедры профилактической медицины Института фундаментальной медицины и биологии
Казань
Е. В. Власова
Россия
Врач ультразвуковой диагностики отделения ультразвуковой диагностики, медико-санитарная часть; ассистент кафедры профилактической медицины Института фундаментальной медицины и биологии
Казань
Дополнительные файлы
Рецензия
Для цитирования:
Акрамова Э.Г., Савельев А.А., Хамитова Р.Я., Власова Е.В. Комплексная оценка исходов острого инфаркта миокарда нижней стенки по данным эхокардиографии у пациентов после чрескожного коронарного вмешательства. Российский кардиологический журнал. 2023;28(7):5438. https://doi.org/10.15829/1560-4071-2023-5438
For citation:
Akramova E.G., Savelyev A.A., Khamitova R.Ya., Vlasova E.V. Comprehensive assessment of the outcomes of inferior wall myocardial infarction according to echocardiography in patients after percutaneous coronary intervention. Russian Journal of Cardiology. 2023;28(7):5438. (In Russ.) https://doi.org/10.15829/1560-4071-2023-5438
JATS XML

















































