Перейти к:
Прогнозирование внутригоспитальной летальности у больных острым инфарктом миокарда с подъемом сегмента ST после чрескожного коронарного вмешательства
https://doi.org/10.15829/1560-4071-2023-5414
EDN: UOAERW
Аннотация
Цель. Разработка моделей прогнозирования внутригоспитальной летальности (ВГЛ) у больных инфарктом миокарда с подъемом сегмента ST (ИМпST) на электрокардиограмме после чрескожного коронарного вмешательства (ЧКВ) на основе многофакторной логистической регрессии (МЛР).
Материал и методы. Проведено ретроспективное когортное исследование по данным 4735 электронных историй болезни пациентов (3249 мужчин и 1486 женщин) с ИМпST в возрасте от 26 до 93 лет с медианой 63 года, которым выполнялось ЧКВ. Было выделено 2 группы лиц, первую из которых составили 321 (6,8%) больных, умерших в стационаре, вторую — 4413 (93,2%) — с благоприятным исходом ЧКВ. Для разработки прогностических моделей использовали однофакторную логистическую регрессию (ОЛР) и МЛР. Точность моделей оценивали по 3 метрикам: площадь под ROC-кривой (AUC), чувствительность и специфичность. Конечная точка исследования была представлена показателем ВГЛ больных ИМпST после ЧКВ от всех причин.
Результаты. Статистический анализ показателей клинико-функционального статуса больных позволил выделить факторы, линейно связанные с ВГЛ. Методом ОЛР были определены их весовые коэффициенты, характеризующие предиктивный потенциал. Прогностические алгоритмы ВГЛ на основе предикторов шкалы GRACE, представленных как суммой баллов в модели ОЛР, так и 5 факторами в непрерывной форме в модели МЛР, обладали приемлемой предсказательной точностью (AUC — 0,83 и 0,86, соответственно). Наилучшие метрики качества имела модель МЛР, структура которой помимо 5 факторов GRACE включала показатели фракции выброса (ФВ) левого желудочка (ЛЖ) и уровня лейкоцитов крови (WBC) (AUC — 0,93, чувствительность — 0,87, специфичность — 0,86). Наибольший вклад в реализацию конечной точки был связан с классом ОСН по T. Killip и ФВ ЛЖ, а наименьший — с WBC и возрастом больных.
Заключение. Предсказательная точность разработанных моделей МЛР была выше, чем шкалы GRACE. Наиболее высокие метрики качества имела модель, структура которой была представлена 5 факторами GRACE, ФВ ЛЖ и WBC.
Ключевые слова
Для цитирования:
Гельцер Б.И., Шахгельдян К.И., Домжалов И.Г., Куксин Н.С., Кокарев Е.А., Котельников В.Н., Рублев В.Ю. Прогнозирование внутригоспитальной летальности у больных острым инфарктом миокарда с подъемом сегмента ST после чрескожного коронарного вмешательства. Российский кардиологический журнал. 2023;28(6):5414. https://doi.org/10.15829/1560-4071-2023-5414. EDN: UOAERW
For citation:
Geltser B.I., Shahgeldyan K.I., Domzhalov I.G., Kuksin N.S., Kokarev E.A., Kotelnikov V.N., Rublev V.Yu. Prediction of in-hospital mortality in patients with ST-segment elevation acute myocardial infarction after percutaneous coronary intervention. Russian Journal of Cardiology. 2023;28(6):5414. (In Russ.) https://doi.org/10.15829/1560-4071-2023-5414. EDN: UOAERW
Ишемическая болезнь сердца (ИБС) занимает одну из лидирующих позиций в структуре смертности населения в большинстве стран мира и является глобальной проблемой здравоохранения1. К наиболее опасным осложнениям ИБС относится острый инфаркт миокарда (ИМ) с подъемом сегмента ST (ИМпST) на электрокардиограмме, который чаще всего развивается вследствие атеротромботической окклюзии коронарных артерий [1]. По данным национальных регистров внутригоспитальная летальность (ВГЛ) пациентов с ИМпST в странах Европы варьирует от 6 до 14%, а годовая летальность составляет ~10% [2]. Показатель смертельных исходов у больных с ИМпST в стационарах Российской Федерации фиксируется на уровне 5-8%, что свидетельствует о сопоставимых значениях этих индикаторов и необходимости прогнозирования неблагоприятных событий на различных горизонтах наблюдения [3]. К одним из наиболее эффективных методов лечения ИМпST относят реваскуляризацию миокарда посредством чрескожного коронарного вмешательства (ЧКВ), проведение которого необходимо в кратчайшие сроки от начала заболевания. ВГЛ при плановых ЧКВ составляет 0,5-1%, а при экстренных — от 4 до 7%. При этом фиксируется зависимость данного показателя от степени поражения коронарного русла, сроков проведения ЧКВ, наличия постинфарктного кардиосклероза, профиля и активности коморбидной патологии и других факторов. К основным причинам летального исхода после ЧКВ относятся невосстановление коронарного кровотока (феномен "no-reflow"), повторный ИМ, желудочковые тахиаритмии, геморрагические и тромбоэмболические осложнения. Для оценки рисков неблагоприятных исходов у больных с острыми формами ИБС профессиональными сообществами разработаны шкалы, позволяющие персонифицировать прогноз фатальных событий на основе анализа данных, характеризующих клинико-функциональный статус больных. К ним относят шкалы TIMI, GRACE, APACHE II, PAMI, PURSUIT, CADILLAC, РЕКОРД, Syntax Score II и другие. Стратификация больных с выделением групп высокого риска позволяет определить оптимальную стратегию реваскуляризации миокарда, повысить эффективность лечения, продолжительность и качество жизни пациентов. В реальной клинической практике для оценки ближайшего прогноза у больных с ИМпST чаще всего используется шкала GRACE (Global Registry of Acute Coronary Events) [4][5]. Вместе с тем в ряде исследований было показано, что ее предсказательная ценность ограничивается в когортах пациентов молодого и пожилого возраста, а также среди больных после ЧКВ, что послужило поводом для многочисленных исследований по ее совершенствованию [6]. В последние годы постоянно возрастает интерес к разработке и практическому применению прогностических алгоритмов для оценки госпитальных и отдаленных результатов ЧКВ на основе методов машинного обучения (МО) [7]. Их использование позволяет автоматизировать обработку и анализ больших объемов данных, выявлять скрытые или неочевидные закономерности и извлекать новые знания. К наиболее известным инструментам МО, применяемым для построения прогностических моделей в клинической медицине, относят многофакторную логистическую регрессию (МЛР).
Цель исследования состояла в разработке моделей прогнозирования ВГЛ у больных с ИМпST после ЧКВ на основе МЛР.
Материал и методы
Выполнено ретроспективное когортное исследование, для реализации которого анализировали данные из 4735 электронных историй болезни пациентов (3249 мужчин и 1486 женщин) с ИМпST в возрасте от 26 до 93 лет с медианой 63 года и 95% доверительным интервалом (ДИ) (62; 63), поступивших в 2015-2021гг в кардиологическое отделение Регионального сосудистого центра ГБУЗ "Приморская краевая клиническая больница № 1" г. Владивостока. Всем пациентам в первые сутки стационарного лечения была выполнена инвазивная коронарография с последующей транслюминальной баллонной ангиопластикой со стентированием инфаркт-связанных артерий на ангиографической системе General Electric Innova 3100. Оценку риска летального исхода в стационаре выполняли с помощью шкалы GRACE. Низкий риск имел место у 410 (8,7%) больных, средний — у 2388 (50,4%), высокий — у 1937 (40,9%). У 201 (4,2%) больного в анамнезе имел место ИМ, по поводу которого 109 (2,3%) из них было проведено ЧКВ. Среди больных было выделено 2 группы лиц, первую из которых составили 321 (6,8%) человек, умерших в период госпитализации в стационаре, вторую — 4414 (93,2%) — с благоприятным исходом ЧКВ. Сроки наступления летального исхода у большинства (90%) больных фиксировались в течение 7 дней после ЧКВ, у 6% — от 10 до 20 дней и у 4% — от 20 до 30 дней. Причиной смерти у 201 больного было повторное ишемическое событие, у 35 — рецидивирующие желудочковые тахиаритмии, у 28 — геморрагические осложнения, у 43 — полиорганная недостаточность на фоне тяжелой коморбидности и инфекционных осложнений, у 14 — интраоперационные осложнения ЧКВ.
Клинико-функциональный статус больных оценивали в первые сутки стационарного лечения с помощью 136 факторов, основные из которых представлены в таблице 1. Помимо демографических и анамнестических данных анализировали показатели клинического анализа крови, креатинин (Cr) сыворотки крови, скорость клубочковой фильтрации, международное нормализованное отношение (МНО), тромбиновое время (ТВ), протромбиновый индекс (ПТИ), активированное частичное тромбопластиновое время (АЧТВ), уровень фибриногена. Эхокардиографическое исследование проводилось на аппарате GE Vivid S60 согласно стандартному протоколу с определением поперечного (LA1) и продольного (LA2) размеров левого и правого предсердий, конечного систолического и диастолического размеров левого желудочка (ЛЖ), фракции выброса (ФВ) ЛЖ методом Тейхольца. Рассчитывали индикаторы гипертрофии ЛЖ: индекс относительной толщины его задней стенки и индекс массы миокарда ЛЖ, который для исключения влияния гендерного фактора нормировали на верхнюю границу его референсных значений, ассоциированных с полом, с вычислением относительного индекса массы миокарда ЛЖ (ОИММЛЖ). Конечная точка исследования была представлена показателем ВГЛ больных после ЧКВ от всех причин в форме категориального бинарного признака ("отсутствие" или "развитие"). Входные признаки — подгруппа потенциальных предикторов выражалась в форме непрерывных и категориальных переменных.
Для обработки и анализа данных использовали методы статистического анализа и МО. Первые из них были представлены тестами хи-квадрат, Фишера, Манна-Уитни и однофакторной логической регрессии (ОЛР) с расчетом весовых коэффициентов по нормализованной выборке, вторые — методом МЛР. Показатели были представлены медианными значениями (Me) и их 95% ДИ. Статистическая значимость подтверждалась значением p-value <0,05. Качество моделей оценивали по 3 метрикам: площадь под ROC-кривой (AUC), чувствительность (Sen) и специфичность (Sp). Порог отсечения определяли методом поиска точки баланса между чувствительностью и специфичностью (Sen ≈ Sp). Дизайн исследования включал 3 этапа. На первом из них для выделения потенциальных предикторов, линейно связанных с летальностью в стационаре, в группах сравнения был проведен статистический анализ 136 факторов. На втором этапе по нормализованным данным с помощью моделей ОЛР определяли весовые коэффициенты отдельных показателей. На третьем этапе на основе ОЛР и МЛР были разработаны прогностические модели ВГЛ с использованием предикторов шкалы GRACE и показателей, выделенных на предыдущих этапах исследования. Базовой моделью считали ОЛР с единственным предиктором — суммой баллов по шкале GRACE. Авторские модели разрабатывали на основе предикторов модели GRACE с последовательным включением в их структуру новых факторов, выделенных на предыдущих этапах исследования. Если включение фактора не повышало точность модели, то его не рассматривали в качестве предиктора. Анализ данных и разработку моделей выполняли на языке Python.
Результаты
Анализ показателей клинико-функционального статуса больных в группах сравнения показал, что большинство из них имеют статистически значимые различия (табл. 1). Так, больные первой группы отличались более старшим возрастом, преобладанием лиц женского пола, наличием переднего ИМ, фибрилляции предсердий (ФП), более низкими значениями систолического артериального давления (САД), диастолического артериального давления, ФВ ЛЖ. По отношению к лицам с благоприятным исходом реваскуляризации миокарда у умерших больных размеры левого и правого предсердий, конечный систолический размер ЛЖ, а также частота сердечных сокращений (ЧСС), сумма баллов по шкале GRACE, класс острой сердечной недостаточности (ОСН) по T. Killip, систолическое давление в легочной артерии и ОИММЛЖ были значимо выше. Анализ клинико-биохимических показателей крови демонстрировал, что у лиц первой группы имел место лейкоцитоз, более высокий уровень Cr и снижение скорости клубочковой фильтрации. Несмотря на достоверность межгрупповых различий показателей эритроцитов, гемоглобина, тромбоцитов, ПТИ, МНО и АЧТВ, последние находились в пределах физиологической нормы. Необходимо отметить, что в анамнезе умерших больных чаще фиксировался сахарный диабет, хроническая болезнь почек и острое нарушение мозгового кровообращения, а распространенность хронической обструктивной болезни легких и артериальной гипертензии существенно не отличалась от группы сравнения (p-value — 0,27 и 0,49, соответственно). В отличие от лиц с благоприятным исходом ЧКВ больным первой группы значительно реже (в 2,3 раза) проводилась тромболитическая терапия (ТЛТ) на догоспитальном этапе. По данным статистического анализа уровень индекса массы тела, концентрация фибриногена, ТВ, а также ИМ в анамнезе не имели межгрупповых различий и не ассоциировались с ВГЛ. Вместе с тем вероятность летального исхода существенно возрастала (отношение шансов =2,1, p=0,02) среди лиц с ранее перенесенным ИМ и повторным ЧКВ. На втором этапе исследования для уточнения степени влияния отдельных показателей на конечную точку исследования были построены модели ОЛР с расчетом весовых коэффициентов, характеризующих их предиктивный потенциал (табл. 2). Результаты анализа демонстрировали, что наиболее высокий уровень весовых коэффициентов имел место у 12 показателей: Cr, суммы баллов по шкале GRACE, ФВ ЛЖ, САД, ПТИ, возраста, МНО, ЧСС, класса ОСН по T. Killip, диастолического артериального давления, LA1. При этом максимальное значение весового коэффициента (6,35 усл. ед.) ассоциировалось с показателем Cr. Необходимо также отметить, что значения индикаторов предиктивного потенциала таких факторов госпитальной летальности, как передний ИМ, перенесенный ИМ и повторное ЧКВ, отсутствие догоспитального ТЛТ, ФП, находились в диапазоне 0,31-1,17 усл. ед., что может свидетельствовать об их ограниченном влиянии на конечную точку исследования. На третьем этапе исследования были разработаны 3 варианта моделей ВГЛ (табл. 3). Первый из них был представлен моделью (1) на основе ОЛР, которая включала единственный предиктор — сумму баллов по шкале GRACE. Для построения второго варианта моделей была использована МЛР. В структуру этой модели (2) входили 5 предикторов классической шкалы GRACE в непрерывной форме (возраст, ЧСС, САД, класс ОСН по T. Killip, концентрация Cr в сыворотке крови). Ввиду того, что категориальные признаки этой шкалы (подъем сегмента ST, положительный тропониновый тест и отсутствие остановки кровообращения на момент поступления в стационар) у всех больных анализируемой когорты были с нулевой дисперсией, они не включались в структуру моделей. Третий вариант моделей на основе МЛР предполагал последовательное расширение состава предикторов шкалы GRACE дополнительными признаками, выделенными на предыдущих этапах исследования (табл. 1, 2). Основным условием для их использования в качестве предикторов было увеличение метрик качества моделей. Сравнительный анализ индикаторов качества прогностических алгоритмов на основе факторов шкалы GRACE демонстрировал более высокую точность модели МЛР (2) с предикторами в непрерывной форме по сравнению с моделью ОЛР (1), где в качестве предиктора использовалась сумма баллов этой шкалы (табл. 3). Расширение состава предикторов, входящих в структуру модели МЛР (2), за счет ФВ ЛЖ приводило к существенному росту метрик качества модели МЛР (3): AUC — 0,88, Sen — 0,88 и Sp — 0,82. Фактор гендерной принадлежности в модели МЛР (4) увеличивал только её чувствительность (Sen — 0,91), но не влиял на другие критерии качества. Точность прогноза повышалась в модели МЛР (7), в которой базовые предикторы шкалы GRACE дополнялись комбинацией факторов: ФВ ЛЖ, ФП и ПТИ (AUC — 0,89). Максимальный подъем показателей точности имел место в модели МЛР (8) с предикторами шкалы GRACE, ФВ ЛЖ и уровнем лейкоцитов в крови (WBC) (AUC — 0,92). Тестирование предиктивной ценности других факторов (размеры камер сердца, локализация ИМ, варианты коморбидной патологии и др.) показало, что они не влияли или даже снижали параметры точности моделей. Результаты поиска оптимального порога отсечения для лучшей модели МЛР (8) позволили определить точку баланса между чувствительностью и специфичностью на уровне 0,05 (5%), что соответствует высокому риску фатального события (рис. 1). Относительный вклад различных предикторов в реализацию конечной точки исследования определяли путем последовательного исключения отдельных факторов из структуры моделей и их повторного построения на оставшихся. При этом выраженность снижения параметра AUC указывала на прогностическую ценность удаленного предиктора. Анализ предиктивного потенциала факторов шкалы GRACE в модели МЛР (2) показал, что наибольшее влияние на конечную точку оказывает класс ОСН по T. Killip, относительный вклад которого составляет 58%. Исключение из структуры модели показателя САД снижало ее точность по метрике AUC на 17%, ЧСС — на 11%, а последовательное удаление признаков возраста и Cr сокращало уровень AUC на 8% и 5%, соответственно (рис. 2). Аналогичная процедура оценки предиктивной ценности факторов лучшей модели МЛР (8) демонстрировала доминирующий вклад в реализацию конечной точки двух признаков: класс ОСН по T. Killip (28%) и ФВ ЛЖ (22%). Влияние на точность прогнозирования показателей САД (18%) и ЧСС (12%) было менее заметным, а признаков WBC и возраста — существенно меньшим (7% и 6%, соответственно) (рис. 3). Таким образом, превалирующее значение в определении точности прогноза ВГЛ больных с ИМпST после ЧКВ имели клинико-функциональные маркеры ОСН.
Таблица 1
Клинико-функциональная характеристика больных (Me, 95% ДИ)
|
Предиктор |
Группа 1 (n=321) |
Группа 2 (n=4414) |
ОШ (9٥٪) ДИ |
p-value |
|
Возраст, лет |
71 [ 69;72] |
62 [ 62;63] |
– |
<0,0001 |
|
Женский пол, абс. (%) |
144 (44,9%) |
1341 (30,39%) |
1,86 [ 1,48;2,34] |
<0,0001 |
|
ИМТ, кг/м2 |
27,68 [ 26,12;27,54] |
26,83 [ 27,45;27,71] |
– |
0,045 |
|
ЧСС, уд./мин |
87 [ 83,5;90] |
72 [ 72;72] |
– |
<0,0001 |
|
САД, мм рт.ст. |
110 [ 110;120] |
130 [ 130;130] |
– |
<0,0001 |
|
ДАД, мм рт.ст. |
72 [ 70;80] |
80 [ 80;80] |
– |
<0,0001 |
|
Передний ИМ, абс. (%) |
183 (57%) |
2048 (46,4%) |
1,53 [ 1,22;1,92] |
0,00026 |
|
Класс ОСН по T. Killip |
3,00 [ 3;3] |
1,00 [ 1;1] |
– |
<0,0001 |
|
GRACE, сумма баллов |
203,5 [ 197;211] |
147 [ 146;149] |
– |
<0,0001 |
|
GRACE >156 баллов, абс. (%) |
227 (70,7%) |
1731 (39,2%) |
9,2 [ 6,5;13,1] |
<0,0001 |
|
ФП, абс. (%) |
74 (23%) |
374 (8,5%) |
3,9 [ 2,9;5,2] |
<0,0001 |
|
ФВ ЛЖ, ٪ |
47 [ 45;49] |
56 [ 56;56] |
– |
<0,0001 |
|
КДР ЛЖ, см |
5 [ 4,9;5,2] |
5 [ 5;5] |
– |
0,364 |
|
КСР ЛЖ, см |
3,7 [ 3,6;3,9] |
3,4 [ 3,4;3,4] |
– |
<0,0001 |
|
LA1, см |
4,2 [ 4,1;4,3] |
3,9 [ 3,9;3,9] |
– |
<0,0001 |
|
LA2, см |
5,2 [ 5,1;5,4] |
4,9 [ 4,9;5] |
– |
<0,0001 |
|
RA1, см |
3,8 [ 3,8;3,9] |
3,6 [ 3,6;3,6] |
– |
<0,0001 |
|
RA2, см |
4,9 [ 4,8;5] |
4,7 [ 4,7;4,7] |
– |
<0,0001 |
|
ОИММЛЖ, усл. ед. |
1,06 [ 0,97;1,13] |
0,96 [ 0,95;0,97] |
– |
0,00022 |
|
ИОТ ЗСЛЖ, усл. ед. |
0,408 [ 0,392;0,431] |
0,417 [ 0,417;0,42] |
– |
0,591 |
|
СДЛА, мм рт.ст. |
35 [ 32;38] |
28 [ 27;28] |
– |
<0,0001 |
|
WBC, 109/л |
14,1 [ 12,9;15] |
10,5 [ 10,4;10,7] |
– |
<0,0001 |
|
RBC, 1012/л |
4,25 [ 4,05;4,45] |
4,45 [ 4,42;4,48] |
– |
0,002 |
|
Hb, г/л |
134 [ 129,59;138,41] |
140 [ 139,11;140,89] |
– |
0,001 |
|
PLT, 109/л |
245 [ 221,60;269,40] |
218 [ 214,47;221,53] |
– |
0,013 |
|
ПТИ, ٪ |
75,5 [ 72,3;78,4] |
89,1 [ 88,6;89,4] |
– |
<0,0001 |
|
МНО, ед. |
1,26 [ 1,08;1,44] |
1,06 [ 1,05;1,07] |
– |
<0,0001 |
|
Фб, г/л |
3,3 [ 3,05;3,55] |
3,3 [ 3,24;3,36] |
– |
0,995 |
|
ТВ, сек |
21,4 [ 1,19;43,99] |
21,2 [ 18,53;23,87] |
– |
0,053 |
|
АЧТВ, сек |
39,7 [ 32,99;46,41] |
36,5 [ 35,08;37,92] |
– |
<0,0001 |
|
Cr, мкмоль/л |
129,8 [ 122,9;141,1] |
96,9 [ 96;97,9] |
– |
<0,0001 |
|
СКФ, мл/мин/м2 |
45,6 [ 41;50,8] |
77,76 [ 76,6;78,9] |
– |
<0,0001 |
|
ПИМ, абс. (%) |
19 (5,86%) |
182 (4,12%) |
1,4 [ 0,89;2,36] |
0,173 |
|
ПИМ+ПЧКВ, абс. (%) |
14 (4,32%) |
95 (2,15%) |
2,1 [ 1,16;3,64] |
0,022 |
|
АГ, абс. (%) |
152 (47,35%) |
1968 (44,59%) |
1,7 [ 0,54;5,55] |
0,494 |
|
ХОБЛ, абс. (%) |
50 (15,58%) |
794 (17,99%) |
0,83 [ 0,6;1,15] |
0,297 |
|
СД 2, абс. (%) |
98 (30,5%) |
845 (19,1%) |
1,86 [ 1,45;2,38] |
<0,0001 |
|
ОНМК в анамнезе, абс. (%) |
6 (1,87%) |
24 (0,54%) |
3,5 [ 1,43;8,75] |
0,013 |
|
ХБП, абс. (%) |
84 (26,1%) |
678 (15,3%) |
1,97 [ 1,5;2,56] |
<0,0001 |
|
Отсутствие догоспитального ТЛТ, абс. (%) |
270 (84,1%) |
2918 (66,1%) |
2,88 [ 2,1;3,9] |
<0,0001 |
Сокращения: АГ — артериальная гипертензия, АЧТВ — активированное частичное тромбопластиновое время, ДАД — диастолическое артериальное давление, ИМТ — индекс массы тела, ИМ — инфаркт миокарда, ИОТ ЗСЛЖ — индекс относительной толщины задней стенки левого желудочка, КДР ЛЖ — конечный диастолический размер левого желудочка, КСР ЛЖ — конечный систолический размер левого желудочка, МНО — международное нормализованное отношение, ОИММЛЖ — относительный индекс массы миокарда левого желудочка, ОНМК — острое нарушение мозгового кровообращения, ОСН — острая сердечная недостаточность, ПИМ+ПЧКВ — повторный инфаркт миокарда и повторное чрескожное коронарное вмешательство, ПТИ — протромбиновый индекс, САД — систолическое артериальное давление, СД 2 — сахарный диабет 2 типа, СДЛА — систолическое давление в легочной артерии, СКФ — скорость клубочковой фильтрации, ТВ — тромбиновое время, ТЛТ — тромболизис, Фб — фибриноген, ФВ ЛЖ — фракция выброса левого желудочка, ФП — фибрилляция предсердий, ХБП — хроническая болезнь почек, ХОБЛ — хроническая обструктивная болезнь легких, ЧСС — частота сердечных сокращений, Cr — креатинин, Hb — гемоглобин, LA1 — поперечный размер левого предсердия, LA2 — продольный размер левого предсердия, RA1 — поперечный размер правого предсердия, RA2 — продольный размер правого предсердия, RBC — эритроциты, PLT — тромбоциты, WBC — лейкоциты.
Таблица 2
Весовые коэффициенты однофакторных моделей логистической регрессии (Me, 95% ДИ)
|
Предиктор |
Коэффициент |
p-value |
|
Cr |
6,35 [ 6,353;6,355] |
<0,0001 |
|
GRACE |
5,92 [ 5,917;5,923] |
<0,0001 |
|
ФВ ЛЖ |
-5,28 [ -5,288;-5,280] |
<0,0001 |
|
САД |
-4,57 [ -4,576;-4,575] |
<0,0001 |
|
ПТИ |
-4,39 [ -4,402;-4,395] |
<0,0001 |
|
Возраст |
4,23 [ 4,232;4,242] |
<0,0001 |
|
МНО |
4,12 [ 4,126;4,129] |
<0,0001 |
|
ЧСС |
3,69 [ 3,695;3,697] |
<0,0001 |
|
Класс ОСН по T. Killip |
3,47 [ 3,466;3,481] |
<0,0001 |
|
ДАД |
-3,44 [ -3,446;-3,444] |
<0,0001 |
|
LA1 |
3,23 [ 3,234;3,239] |
<0,0001 |
|
LА2 |
2,82 [ 2,821;2,827] |
<0,0001 |
|
КДР ЛЖ |
2,76 [ 2,762;2,768] |
<0,0001 |
|
RA1 |
2,68 [ 2,685;2,691] |
<0,0001 |
|
WBC |
2,46 [ 2,466;2,469] |
<0,0001 |
|
КСР ЛЖ |
2,45 [ 2,447;2,454] |
<0,0001 |
|
СКФ |
-2,17 [ -2,173;-2,172] |
<0,0001 |
|
RA2 |
2,02 [ 2,024;2,029] |
<0,0001 |
|
PLT |
1,59 [ 1,586;1,595] |
<0,0001 |
|
RBC |
-1,49 [ -1,502;-1,493] |
<0,0001 |
|
АЧТВ |
1,48 [ 1,484;1,487] |
<0,0001 |
|
ТВ |
1,41 [ 1,413;1,420] |
<0,0001 |
|
ФП |
1,17 [ 1,162;1,179] |
<0,0001 |
|
ОНМК в анамнезе |
1,04 [ 1,040;1,045] |
0,0036 |
|
Отсутствие догоспитального ТЛТ |
0,97 [ 0,958;0,986] |
<0,0001 |
|
ПИМ+ПЧКВ |
0,69 [ 0,686;0,695] |
<0,0001 |
|
Женский пол |
0,61 [ 0,603;0,630] |
<0,0001 |
|
СД 2 |
0,57 [ 0,568;0,591] |
<0,0001 |
|
ИМТ |
-0,56 [ -0,567;-0,561] |
<0,0001 |
|
АГ |
0,35 [ 0,344;0,359] |
<0,0001 |
|
ПИМ |
0,34 [ 0,338;0,350] |
<0,0001 |
|
Передний ИМ |
0,31 [ 0,301;0,330] |
<0,0001 |
Сокращения: АГ — артериальная гипертензия, АЧТВ — активированное частичное тромбопластиновое время, ДАД — диастолическое артериальное давление, ИМ — инфаркт миокарда, ИМТ — индекс массы тела, КДР ЛЖ — конечный диастолический размер левого желудочка, КСР ЛЖ — конечный систолический размер левого желудочка, МНО — международное нормализованное отношение, ОНМК — острое нарушение мозгового кровообращения, ОСН — острая сердечная недостаточность, ПИМ+ПЧКВ — повторный инфаркт миокарда и повторное чрескожное коронарное вмешательство, ПТИ — протромбиновый индекс, САД — систолическое артериальное давление, СД 2 — сахарный диабет 2 типа, СКФ — скорость клубочковой фильтрации, ТВ — тромбиновое время, ТЛТ — тромболизис, ФВ ЛЖ — фракция выброса левого желудочка, ФП — фибрилляция предсердий, ЧСС — частота сердечных сокращений, Cr — креатинин, LA1 — поперечный размер левого предсердия, LA2 — продольный размер левого предсердия, PLT — тромбоциты, RA1 — поперечный размер правого предсердия, RA2 — продольный размер правого предсердия, RBC — эритроциты, WBC — лейкоциты.
Таблица 3
Оценка точности прогностических моделей
|
№ п/п |
Предикторы моделей |
Тестовые выборки |
Выборки для валидации |
||||
|
AUC |
Sen |
Sp |
AUC |
Sen |
Sp |
||
|
1 |
GRACE, сумма баллов |
0,839 |
0,766 |
0,768 |
0,825 |
0,755 |
0,78 |
|
2 |
Возраст, ОСН по T. Killip, ЧСС, Cr, САД |
0,864 |
0,758 |
0,8 |
0,86 |
0,796 |
0,795 |
|
3 |
Возраст, ОСН по T. Killip, ЧСС, Cr, САД, ФВ ЛЖ |
0,879 |
0,751 |
0,867 |
0,886 |
0,882 |
0,828 |
|
4 |
Возраст, ОСН по T. Killip, ЧСС, Cr, САД, ФВ ЛЖ, женский пол |
0,879 |
0,752 |
0,866 |
0,886 |
0,912 |
0,829 |
|
5 |
Возраст, ОСН по T. Killip, ЧСС, Cr, САД, ФВ ЛЖ, ПТИ |
0,878 |
0,717 |
0,862 |
0,891 |
0,879 |
0,837 |
|
6 |
Возраст, ОСН по T. Killip, ЧСС, Cr, ФВ ЛЖ, ФП |
0,878 |
0,757 |
0,869 |
0,889 |
0,882 |
0,834 |
|
7 |
Возраст, ОСН по T. Killip, ЧСС, Cr, САД, ФВ ЛЖ, ФП, ПТИ |
0,878 |
0,761 |
0,869 |
0,896 |
0,879 |
0,843 |
|
8 |
Возраст, ОСН по T. Killip, ЧСС, Cr, САД, ФВ ЛЖ, WBC |
0,881 |
0,752 |
0,875 |
0,927 |
0,87 |
0,861 |
|
9 |
Возраст, ОСН по T. Killip, ЧСС, Cr, САД, ПТИ |
0,852 |
0,715 |
0,822 |
0,864 |
0,767 |
0,815 |
|
10 |
Возраст, ОСН по T. Killip, ЧСС, Cr, САД, LA1 |
0,859 |
0,693 |
0,868 |
0,864 |
0,757 |
0,859 |
|
11 |
Возраст, ОСН по T. Killip, ЧСС, Cr, САД, КДР ЛЖ |
0,859 |
0,671 |
0,863 |
0,856 |
0,754 |
0,853 |
|
12 |
Возраст, ОСН по T. Killip, ЧСС, Cr, САД, RA1 |
0,859 |
0,674 |
0,872 |
0,863 |
0,757 |
0,863 |
|
13 |
Возраст, ОСН по T. Killip, ЧСС, Cr, САД, Передний ИМ |
0,866 |
0,765 |
0,795 |
0,845 |
0,796 |
0,803 |
|
14 |
Возраст, ОСН по T. Killip, ЧСС, Cr, САД, СД 2 |
0,863 |
0,772 |
0,811 |
0,858 |
0,796 |
0,781 |
Сокращения: ИМ — инфаркт миокарда, КДР ЛЖ — конечный диастолический размер левого желудочка, ОСН — острая сердечная недостаточность, ПТИ — протромбиновый индекс, САД — систолическое артериальное давление, СД 2 — сахарный диабет 2 типа, ФВ ЛЖ — фракция выброса левого желудочка, ФП — фибрилляция предсердий, ЧСС — частота сердечных сокращений, AUC — площадь под ROC-кривой, Cr — креатинин, LA1 — поперечный размер левого предсердия, RA1 — поперечный размер правого предсердия, Sen — чувствительность, Sp — специфичность, WBC — лейкоциты.
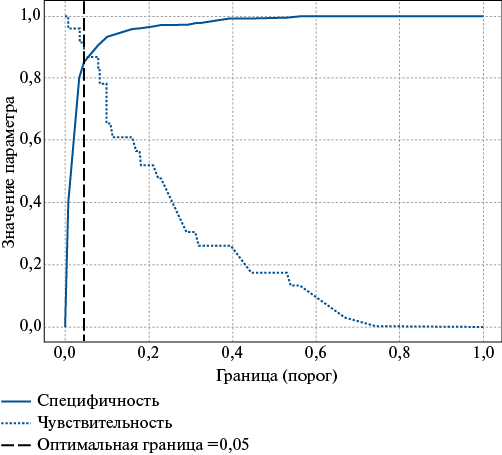
Рис. 1. Roc-анализ — поиск оптимального порога отсечения в лучшей модели МЛР (8).
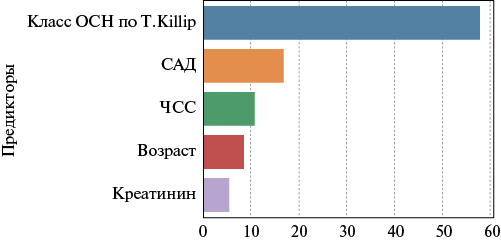
Рис. 2. Относительный вклад отдельных предикторов в реализацию конечной точки в модели МЛР (2), %.
Сокращения: ОСН — острая сердечная недостаточность, САД — систолическое артериальное давление, ЧСС — частота сердечных сокращений.
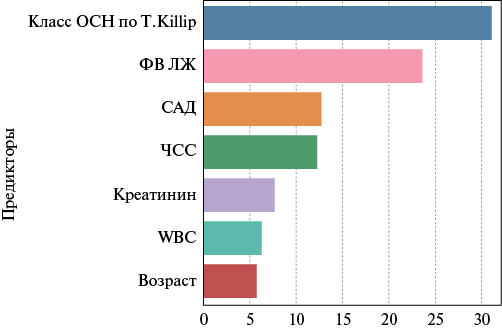
Рис. 3. Относительный вклад отдельных предикторов в реализацию конечной точки в модели МЛР (8), %.
Сокращения: ОСН — острая сердечная недостаточность, САД — систолическое артериальное давление, ФВ ЛЖ — фракция выброса левого желудочка, ЧСС — частота сердечных сокращений, WBC — лейкоциты.
Обсуждение
В настоящее время в кардиологической практике используются различные технологии рискометрии, позволяющие оценить вероятность развития неблагоприятных событий у больных ИМ. Одним из наиболее надежных и доступных прогностических инструментов является шкала GRACE, которая была рекомендована к практическому применению Европейским обществом кардиологов [4]. В нашем исследовании применение шкалы GRACE в когорте больных с ИМпST показало, что сумма баллов у умерших после ЧКВ в стационаре была в 1,4 раза выше, чем у лиц с благоприятным исходом реваскуляризации (203,5 и 147 баллов, соответственно, p<0,0001). При этом среди умерших высокий риск госпитальной летальности (>156 баллов для ИМпST) фиксировался в 70,7% случаев, а средний — в 22,5% (табл. 1). Важно также отметить, что высокий риск ВГЛ имел место у 39,2% больных с благоприятным исходом ЧКВ. Эти данные указывают на значительную долю ложноположительных результатов при использовании балльной оценки шкалы GRACE и необходимость повышения точности прогнозирования. В нашем исследовании эта задача выполнялась путем многоступенчатой процедуры отбора предикторов и разработки прогностических моделей на основе МЛР. Для подтверждения гипотезы о возможном неравенстве клинико-функциональных и лабораторных показателей у больных первой и второй групп были использованы методы математической статистики, применение которых показало достоверность различий по 34 из 40 входных данных. Так, у больных, умерших в стационаре, фиксировались более выраженные признаки ремоделирования миокарда, включая увеличение линейных размеров предсердий, ЛЖ и показателя ОИММЛЖ. Для больных этой группы было характерным также наличие промежуточной ФВ с медианным значением 47% и 95% ДИ (45; 49). Незначительно выраженное снижение ФВ ЛЖ на фоне ОСН 3 класса по T. Killip может объясняться тем, что этот показатель отражает лишь один из механизмов острого ишемического повреждения миокарда, связанного с развитием систолической дисфункции. Вместе с тем нарушение насосной функции сердца может быть связано с преобладанием диастолических расстройств, ассоциированных не только с ИБС, но и с сердечно-сосудистыми проявлениями коморбидной патологии. Одним из важных лабораторных признаков, отличающих больных первой группы от второй, был существенный подъем уровня WBC крови (14,1*109/л vs 10,5*109/л, p<0,0001). Необходимо отметить, что в последние годы показатели клинического анализа крови все чаще используются в качестве предикторов прогностических моделей в кардиологии [8]. Повышение содержания WBC является ключевым индикатором интенсивности воспалительного ответа и эндогенной интоксикации при различных патологических состояниях, в т.ч. ИМ. В ряде исследований доказана взаимосвязь этого показателя с ростом смертности от ИБС и развитием застойной сердечной недостаточности. В нашем исследовании на предварительном этапе отбора предикторов показатель WBC имел высокий уровень весового коэффициента (2,46 усл. ед.) и в дальнейшем использовался при построении прогностических моделей. Проведение ТЛТ на догоспитальном этапе является важным условием для эффективной реваскуляризации миокарда и снижения госпитальной летальности. В нашем исследовании ТЛТ была проведена 16% больных первой группы и 34% — во второй. При этом вероятность летального исхода в стационаре среди пациентов, которым не проводилась ТЛТ, возрастала почти в 3 раза (отношение шансов — 2,88, p<0,0001). Вместе с тем этот показатель не демонстрировал достаточный прогностический потенциал, на что указывали сравнительно низкое значение его весового коэффициента (-1,04) и результаты последующего тестирования при построении прогностических моделей. В ряде работ признак ТЛТ использовался в прогностических моделях фатальных осложнений ИМпST [9].
В настоящем исследовании концепция разработки прогностических моделей ВГЛ больных ИМпST после ЧКВ базировалась на предварительном анализе предиктивной ценности факторов шкалы GRACE с последующим включением в структуру моделей новых показателей, увеличивающих их прогностическую точность. Результаты анализа показали, что приемлемую точность прогноза демонстрировала даже модель ОЛР, где в качестве единственного предиктора использовали сумму баллов по шкале GRACE. Увеличение метрик качества фиксировалось в модели МЛР (2), предикторами которой были 5 факторов GRACE в непрерывной форме, что подтверждает их высокий прогностический потенциал. Вместе с тем в ряде исследований предпринимались попытки повысить эффективность стратификации рисков ВГЛ у больных с ИМпST после ЧКВ на основе модификаций шкалы GRACE. Так, включение в ее структуру 9 факторов коморбидности позволило существенно повысить точность модели среди пациентов с ИМпST, подвергшихся эндоваскулярной реваскуляризации (AUC — 0,9 vs 0,8 по шкале GRACE) [3]. В нашем исследовании повышение точности прогностических моделей с предикторами шкалы GRACE ассоциировалось с влиянием 4 дополнительных факторов: ФВ ЛЖ, ФП, ПТИ и WBC. Вместе с тем наибольшее значение для повышения прогностической точности имело сочетание факторов шкалы GRACE и показателей ФВ ЛЖ и WBC в модели МЛР (8). Наличие этих предикторов демонстрировало патофизиологическое значение систолической дисфункции ЛЖ и системной воспалительной реакции в прогнозировании неблагоприятных исходов ИМпST, что повышает объяснимость результатов моделирования и возможность их клинической интерпретации. Непрозрачность причинно-следственных связей прогностических моделей может быть частично преодолена за счет стратификации факторов риска с различной степенью влияния на результирующую переменную. В нашем исследовании наибольший вклад в реализацию конечной точки был связан с классом ОСН по T. Killip и ФВ ЛЖ, а наименьший — с WBC и возрастом больных.
Ограничения исследования. Ограничения связаны с необходимостью расширения спектра предикторов, методов МО, оценки эффективности ЧКВ и валидации моделей на рандомизированных данных из других лечебных учреждений.
Заключение
Результаты проведенных исследований показали, что разработанные прогностические алгоритмы ВГЛ у больных с ИМпST после ЧКВ на основе предикторов классической шкалы GRACE, представленных как суммой баллов в модели ОЛР, так и 5 факторами в непрерывной форме (возраст, класс ОСН по T. Killip, ЧСС, Cr, САД) в модели МЛР, обладают приемлемой предсказательной точностью. Анализ предиктивного потенциала других показателей демонстрировал его высокий уровень только у 4 факторов: ФВ ЛЖ, ПТИ, ФП и WBC. Наилучшие метрики качества (AUC — 0,927, Sen — 0,87, Sp — 0,861) имела модель МЛР, структура которой помимо 5 факторов GRACE включала показатели ФВ ЛЖ и WBC.
Отношения и деятельность. Исследование выполнено при финансовой поддержке гранта Российского научного фонда № 23-21-00250 https://rscf.ru/project/23-21-00250/.
1 The top 10 causes of death: WHO. https://www.who.int/ru/newsroom/factsheets/detail/thetop10causesofdeath.htm (27 May 2022).
Список литературы
1. Нишонов А. Б., Тарасов Р. С., Иванов С. В., Барбараш Л. С. Результаты коронарного шунтирования и чрескожного вмешательства при остром коронарном синдроме без подъема сегмента ST высокого риска. Комплексные проблемы сердечно-сосудистых заболеваний. 2023;12(1):151-9. doi:10.17802/2306-1278-2023-12-1-151-159.
2. Hadanny A, Shouval R, Wu J, et al. Predicting 30-day mortality after ST elevation myocardial infarction: Machine learning- based random forest and its external validation using two independent nationwide datasets. J Cardiol. 2021;78(5):439-46. doi:10.1016/j.jjcc.2021.06.002.
3. Зыков М. В., Дьяченко Н. В., Велиева Р. М. и др. Возможности совместного использования шкалы GRACE и различных индексов коморбидности для повышения эффективности оценки риска госпитальной летальности у больных с острым коронарным синдромом. Терапевтический архив. 2022;94(7):816-21. doi:10.26442/00403660.2022.07.201742.
4. Szabo D, Szabo A, Magyar L, et al. Admission lactate level and the GRACE 2.0 score are independent and additive predictors of 30-day mortality of STEMI patients treated with primary PCI-Results of a real-world registry. PLoS One. 2022;17(11):e0277785. doi:10.1371/journal.pone.0277785.
5. Wilson RS, Malamas P, Dembo B, et al. The CADILLAC risk score accurately identifies patients at low risk for in-hospital mortality and adverse cardiovascular events following ST elevation myocardial infarction. BMC Cardiovasc Disord. 2021;21(1):533. doi:10.1186/s12872-021-02348-0.
6. Figtree GA, Vernon ST, Hadziosmanovic N, et al. Mortality in STEMI patients without standard modifiable risk factors: a sex-disaggregated analysis of SWEDEHEART registry data. Lancet. 2021;397(10279):1085-94. doi:10.1016/S0140-6736(21)00272-5.
7. Гельцер Б. И., Рублев В. Ю., Циванюк М. М., Шахгельдян К. И. Машинное обучение в прогнозировании ближайших и отдаленных результатов реваскуляризации миокарда: систематический обзор. Российский кардиологический журнал. 2021;26(8):4505. doi:10.15829/1560-4071-2021-4505.
8. Lim J, Davies A, Brienesse S, et al. Inflammatory cell response following ST-elevation myocardial infarction treated with primary percutaneous coronary intervention and its impact on cardiovascular outcomes: A systematic review and meta-analysis. Int J Cardiol. 2023;376:1-10. doi:10.1016/j.ijcard.2023.01.082.
9. Dogra N, Puri GD, Thingnam SKS, et al. Early thrombolysis is associated with decreased operative mortality in postinfarction ventricular septal rupture. Indian Heart J. 2019; 71(3):224-8. doi:10.1016/j.ihj.2019.04.011.
Об авторах
Б. И. ГельцерРоссия
Доктор медицинских наук, профессор, член-корр. РАН, Школа медицины, зам. директора по научной работе.
Владивосток
Конфликт интересов:
Нет конфликта
К. И. Шахгельдян
Россия
Доктор технических наук, доцент, Школа медицины, зав. лабораторией анализа больших данных в медицине и здравоохранении, директор института информационных технологий.
Владивосток
Конфликт интересов:
нет конфликтов
И. Г. Домжалов
Россия
Аспирант департамента клинической медицины, Школа медицины, Приморская краевая клиническая больница № 1, врач отделения реанимации и интенсивной терапии регионального сосудистого центра.
Владивосток
Конфликт интересов:
нет конфликтов
Н. С. Куксин
Россия
Магистрант.
Владивосток
Конфликт интересов:
нет конфликта
Е. А. Кокарев
Россия
Кандидат медицинских наук, Приморская краевая клиническая больница № 1, зав. отделением реанимации и интенсивной терапии отделения реанимации и интенсивной терапии регионального сосудистого центра.
Владивосток
Конфликт интересов:
нет конфликтов
В. Н. Котельников
Россия
Доктор медицинских наук, профессор, Школа медицины, профессор департамента клинической медицины.
Владивосток
Конфликт интересов:
нет конфликтов
В. Ю. Рублев
Россия
Школа медицины, аспирант департамента клинической медицины, врач сердечно-сосудистый хирург медицинского центра.
Владивосток
Конфликт интересов:
нет конфликтов
Дополнительные файлы
Рецензия
Для цитирования:
Гельцер Б.И., Шахгельдян К.И., Домжалов И.Г., Куксин Н.С., Кокарев Е.А., Котельников В.Н., Рублев В.Ю. Прогнозирование внутригоспитальной летальности у больных острым инфарктом миокарда с подъемом сегмента ST после чрескожного коронарного вмешательства. Российский кардиологический журнал. 2023;28(6):5414. https://doi.org/10.15829/1560-4071-2023-5414. EDN: UOAERW
For citation:
Geltser B.I., Shahgeldyan K.I., Domzhalov I.G., Kuksin N.S., Kokarev E.A., Kotelnikov V.N., Rublev V.Yu. Prediction of in-hospital mortality in patients with ST-segment elevation acute myocardial infarction after percutaneous coronary intervention. Russian Journal of Cardiology. 2023;28(6):5414. (In Russ.) https://doi.org/10.15829/1560-4071-2023-5414. EDN: UOAERW
JATS XML

















































