Перейти к:
Российский консенсус по диагностике и лечению пациентов со стенозом сонных артерий
https://doi.org/10.15829/1560-4071-2022-5284
Аннотация
Стеноз сонных артерий — мультидисциплинарная проблема, требующая вовлечения команды специалистов, включающей сердечно-сосудистых хирургов, нейрохирургов, рентгенэндоваскулярных хирургов, кардиологов, неврологов, терапевтов. В настоящем консенсусе группой экспертов рассмотрены основные этапы диагностики стеноза сонных артерий, обсуждены необходимые методы профилактики, особенности выбора оптимального метода лечения с учетом современных подходов. Цель настоящего документа (консенсуса) — представить краткую и структурированную информацию по ведению пациентов со стенозом сонных артерий. Данный документ разработан на основании обновленных клинических рекомендаций Европейского общества сосудистых хирургов и Американского общества сосудистых хирургов, с учетом согласованного мнения российских экспертов.
Ключевые слова
Для цитирования:
Чернявский М.А., Иртюга О.Б., Янишевский С.Н., Алиева А.С., Самочерных К.А., Абрамов К.Б., Вавилова Т.В., Лукьянчиков В.А., Курапеев Д.И., Ванюркин А.Г., Чернова Д.В., Шелуханов Н.К., Козленок А.В., Кавтеладзе З.А., Малеванный М.В., Виноградов Р.А., Хафизов Т.Н., Иванова Г.Е., Жуковская Н.В., Фокин А.А., Игнатьев И.М., Карпенко А.А., Игнатенко П.В., Астапов Д.А., Семенов В.Ю., Порханов В.А., Крылов В.В., Усачев Д.Ю., Светликов А.В., Алекян Б.Г., Акчурин Р.С., Чернявский А.М., Конради А.О., Шляхто Е.В. Российский консенсус по диагностике и лечению пациентов со стенозом сонных артерий. Российский кардиологический журнал. 2022;27(11):5284. https://doi.org/10.15829/1560-4071-2022-5284
For citation:
Chernyavsky M.A., Irtyuga O.B., Yanishevsky S.N., Alieva A.S., Samochernykh K.A., Abramov K.B., Vavilova T.V., Lukyanchikov V.A., Kurapeev D.I., Vanyurkin A.G., Chernova D.V., Shelukhanov N.K., Kozlyonok А.V., Kavteladze Z.A., Malevanny M.V., Vinogradov R.A., Khafizov T.N., Ivanova G.E., Zhukovskaya N.V., Fokin A.A., Ignatiev I.M., Karpenko A.A., Ignatenko P.V., Astapov D.A., Semenov V.Yu., Porkhanov V.A., Krylov V.V., Usachev D.Yu., Svetlikov A.V., Alekyan B.G., Akchurin R.S., Chernyavsky A.M., Konradi A.O., Shlyakhto E.V. Russian consensus statement on the diagnosis and treatment of patients with carotid stenosis. Russian Journal of Cardiology. 2022;27(11):5284. (In Russ.) https://doi.org/10.15829/1560-4071-2022-5284
Стеноз сонных артерий — нозология, вызывающая интерес многих специалистов: сердечно-сосудистых хирургов, нейрохирургов, рентгенэндоваскулярных хирургов, кардиологов, неврологов и даже терапевтов. На сегодняшний день опубликованы многочисленные руководства и рекомендации по диагностике и лечению данного заболевания. Национальные рекомендации по ведению пациентов с заболеваниями брахиоцефальных артерий 2013г; Рекомендации "Закупорка и стеноз сонной артерии" Министерства здравоохранения Российской Федерации 2016г — официальные руководства, на которые может ссылаться практикующий специалист при лечении пациентов. Помимо этого, в 2017г Европейское общество сосудистых хирургов опубликовало документ "Лечение атеросклеротических заболеваний сонных и позвоночных артерий: клинические рекомендации Европейского общества сосудистой хирургии 2017 года". Также, в январе 2022г Американское общество сосудистых хирургов издало руководство "Клинические рекомендации общества сосудистой хирургии по лечению экстракраниальных цереброваскулярных заболеваний". Представленные рекомендации отражают разные аспекты этой междисциплинарной проблемы и не всегда согласуются между собой, учитывая временные промежутки в т.ч. Также стоит отметить, что с 1 января 2022г вступили в силу изменения в Федеральный закон от 21 ноября 2011г № 323-ФЗ "Об основах охраны здоровья граждан в Российской Федерации", касающиеся обязательного применения медицинскими организациями клинических рекомендаций, утвержденных Министерством здравоохранения, при оказании медицинской помощи. Обновленные отечественные клинические рекомендации по лечению пациентов с заболеваниями периферических артерий готовятся профессиональным сообществом, но еще не опубликованы, что лишь подтверждает сложность формирования единых подходов к определению данной патологии, унифицированному описанию факторов ее развития, диагностики и лечения. Поскольку в лечении стеноза сонных артерий и его проявлений доступно несколько методов лечения, при современном мультидисциплинарном подходе выбор оптимальной тактики ведения пациента может вызвать трудности ввиду возможных разногласий у врачей смежных специальностей.
С учетом вышеизложенного, группа экспертов выступила с инициативой создания согласительного документа (консенсуса), целью которого является обобщение и консолидация мнений отечественных специалистов (хирургов, кардиологов, неврологов) по актуальным вопросам оценки группы сердечнососудистого риска (ССР), диагностики и лечения пациентов с атеросклерозом сонной артерии. Эксперты и члены рабочей группы подготовили литературные справки, изучили соответствующие вопросы в зарубежных согласительных документах, оценили доказательную базу, на основании которой сформулированы актуальные клинические рекомендации и положения.
Определение и этиология
Стеноз сонной артерии — это состояние, связанное с сужением просвета артерии, вызванное в первую очередь атеросклеротической бляшкой. Стеноз сонной артерии является следствием системного атеросклеротического заболевания. Таким образом, любой фактор риска (ФР), предрасполагающий к прогрессированию атеросклероза, потенциально может проявляться в виде стеноза сонной артерии с последующим развитием ишемического инсульта (ИИ) или транзиторной ишемической атаки (ТИА).
ИИ — клинический синдром, вызванный фокальным инфарктом головного мозга, возникающим в результате внезапного нарушения кровоснабжения [1].
ТИА — транзиторный эпизод неврологической дисфункции вследствие фокальной ишемии головного мозга без формирования очага инфаркта. Критерии ТИА: кратковременный эпизод неврологического дефицита, вызванный очаговой ишемией головного мозга с клиническими симптомами, длящимися ≤24 ч без формирования морфологических признаков острого инфаркта головного мозга по данным нейровизуализации (в т.ч. магнитно-резонансной томографической последовательности диффузионно-взвешенного изображения) [1].
Атеросклеротическое поражение экстракраниального отдела сонных артерий является одной из основных причин ИИ и ТИА, на долю которых приходится до 20% случаев [2][3]. По данным ряда авторов, стеноз сонной артерии >50% был связан с вероятностью развития ИИ до 36%. Пациенты со стенозом сонной артерии <50% также требуют дополнительной диагностики с целью определения морфологических характеристик атеросклеротической бляшки по данным визуализации, т.к. эмбологенная атеросклеротическая бляшка в сонной артерии является потенциальной причиной эмболического инсульта из неустановленного источника [2].
Факторы риска
При обследовании и лечении пациентов с атеросклерозом сонных артерий рекомендовано выявлять наличие наследственных заболеваний и обращать внимание на следующие ФР, способные повлиять на тактику лечения:
- Сведения о ранее перенесенном остром нарушении мозгового кровообращения (ОНМК) или ТИА;
- Поражение других сосудистых бассейнов (ишемическая болезнь сердца (ИБС), атеросклероз артерий нижних конечностей, аневризма аорты и др.);
- Наследственная гиперхолестеринемия (≥6 баллов по шкале Голландских липидных клиник) [3];
- Сопутствующий сахарный диабет (СД);
- Вредные привычки: курение (>5 сигарет в день), злоупотребление спиртными напитками (>10 у.е. в нед. для мужчин и >5 у.е. для женщин);
- Артериальная гипертензия (АГ);
- Хроническая почечная недостаточность.
Оценка ССР не только у относительно здоровых, но и у пожилых пациентов с подтвержденными атеросклеротическими сердечно-сосудистыми заболеваниями (ССЗ) или СД является основой для персонифицированного вмешательства на индивидуальном уровне. Для оценки ССР рекомендовано использовать шкалы SCORE2 и SCORE2-OP. Алгоритм SCORE2-OP оценивает 5-летние и 10-летние фатальные и нефатальные сердечно-сосудистые события (инфаркт миокарда, инсульт) с поправкой на конкурирующие риски у практически здоровых людей в возрасте >70 лет. Данные шкалы откалиброваны для четырех кластеров стран (низкий, средний, высокий и очень высокий ССР), в котором Россия относится к кластеру с очень высоким ССР. Алгоритм SCORE2 может быть рассчитан в приложении ESC CVD Risk (в бесплатном доступе в AppStore) и в таблице по оценке риска (табл. 1).
Таблица 1
SCORE2 (систематическая оценка коронарного риска 2 (Systematic Coronary Risk Estimation 2)) и SCORE2-OP (систематическая оценка коронарного риска 2 для пожилых лиц (Systematic Coronary Risk Estimation 2-Older Persons)). У относительно здоровых лиц 40-69 лет для оценки 10-летнего риска фатальных и нефатальных (инфаркт миокарда, инсульт) ССЗ используется алгоритм SCORE2; у относительно здоровых лиц ≥70 лет применим SCORE2-OP
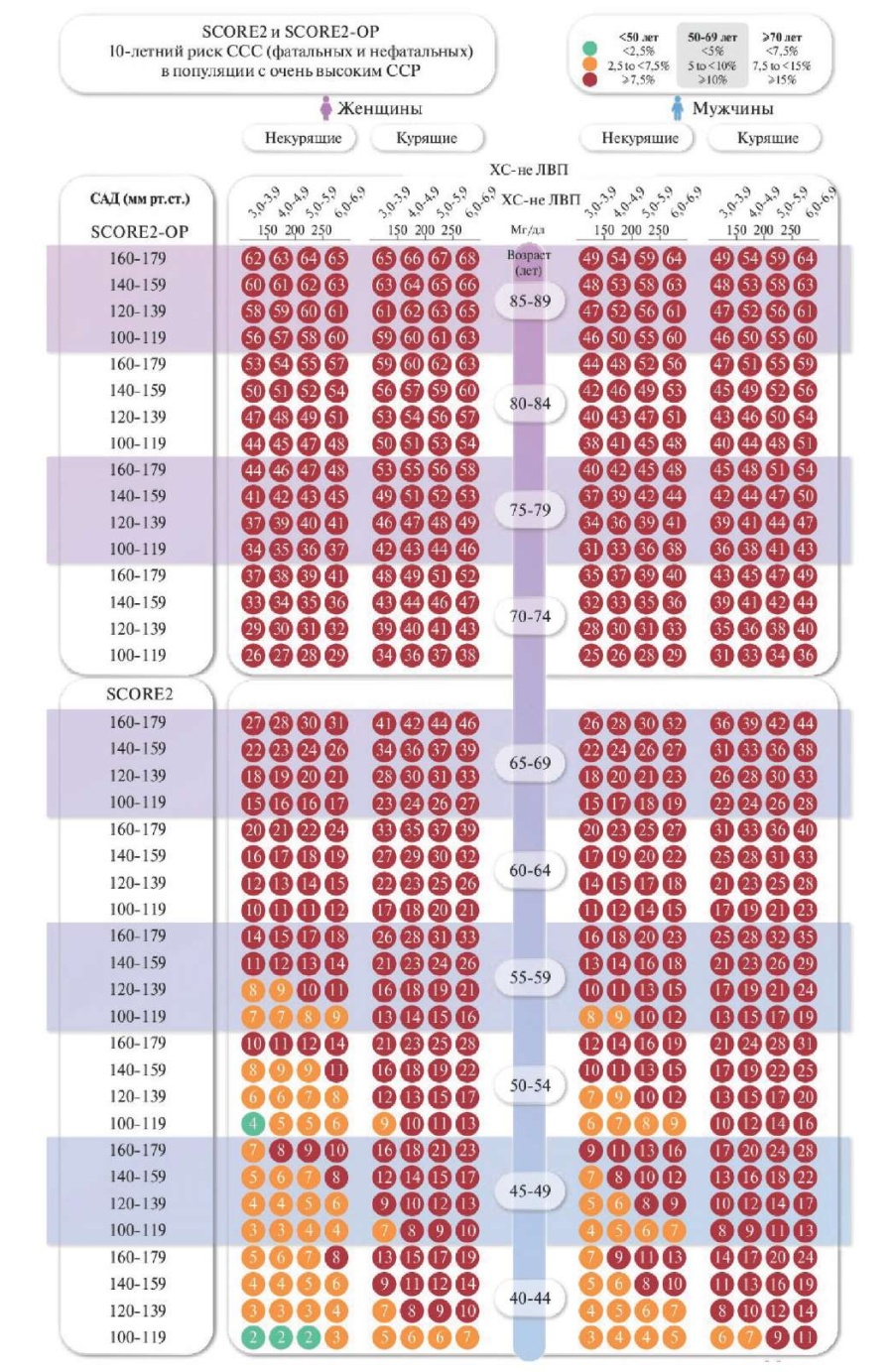
Сокращения: САД — систолическое артериальное давление, ССЗ — сердечно-сосудистое заболевание, ССР — сердечно-сосудистый риск, ССС — сердечнососудистое событие, ХС-неЛВП — холестерин не-липопротеинов высокой плотности.
Диагностика и методы визуализации
При осмотре пациентов со стенозом сонной артерии рекомендуется обращать внимание на дефицит неврологического статуса, который может характеризоваться следующими признаками: присутствие гемипареза, гемигипестезии, эпизодов транзиторных нарушений памяти, нарушение ориентировки во времени и пространстве, нарушение речи, походки и другие неврологические симптомы, свидетельствующие о ранее перенесенном нарушении мозгового кровообращения.
Аускультация артерий шеи с целью выявления систолического шума является стандартной частью врачебного осмотра взрослых, но обнаружение шума более тесно коррелирует с системным атеросклерозом, чем со значимым стенозом сонных артерий. В самом крупном исследовании, сообщающем о скрининге среди бессимптомных больных, распространенность стеноза сонных артерий >35% у пациентов без систолического шума над бифуркацией общей сонной артерии составила 6,6%, а распространенность 75% стеноза сонных артерий у этой же категории пациентов составила 1,2% [4][5]. Несмотря на то, что чувствительность обнаружения шума на сонных артериях и положительная прогностическая ценность для гемодинамически значимого стеноза сонных артерий являются относительно низкими, выполнение в последующем ультразвукового дуплексного сканирования (УЗДС) сонных артерий может быть оправданным в некоторых группах бессимптомных пациентов с высоким ССР, независимо от результатов, полученных при аускультации [6].
У бессимптомных пациентов высокого ССР с подозрением на наличие стеноза сонных артерий требуется выполнение УЗДС (в качестве визуализации первого ряда) [7-9]. Магнитно-резонансная ангиография (МРА) и/или мультиспиральная компьютерная ангиография (МСКТА) рекомендуются для оценки протяженности поражения и степени тяжести экстракраниального каротидного стеноза по любой из шкал (NASCET и/или ECST) (рис. 1).

Рис. 1. Методы оценки стеноза сонной артерии по NASCET и ECST. Примечание: адаптировано из Common Carotid Method. Lancet 1998; 351;1372. NASCET: North American Symptomatic Carotid Endarterectomy Trial; ECST: European Carotid Surgery Trial.
Сокращения: ВСА — внутренняя сонная артерия, НСА — наружная сонная артерия, ОСА — общая сонная артерия.
Выполнение УЗДС брахиоцефальных артерий рекомендуется асимптомным пациентам старше 50 лет, у которых имеются ≥2 ФР:
- АГ;
- Дислипидемия;
- Курение;
- Семейный анамнез среди ближайших родственников со случаями проявления атеросклероза в возрасте до 60 лет или случаев ИИ в семейном анамнезе.
УЗДС брахиоцефальных артерий не рекомендуется для рутинного скрининга стенозирующих и окклюзирующих заболеваний сонных артерий при первичной профилактике инсульта у бессимптомных пациентов.
В случае получения противоречивых заключений по данным неинвазивных исследований (УЗДС, МРА или МСКТА) или неудовлетворительной визуализации артерий рекомендуется выполнение рентгенконтрастной ангиографии. Основным недостатком прямой рентгенконтрастной ангиографии являются риски, связанные с выполнением инвазивной процедуры. Инсульт — самое опасное осложнение этого метода, частота которого <1%, когда исследование выполняется опытным специалистом. По данным ACAS71, в нескольких центрах с необычно частыми осложнениями отмечались существенно более высокие показатели инсульта (1,2%) при диагностической ангиографии. Частота осложнений в других исследованиях была существенно ниже, и большинство авторов считают уровень инсульта >1% неприемлемым при диагностической ангиографии [9].
В случае планирования стентирования сонной артерии, после каждого УЗДС рекомендуется проведение либо МРА, либо МСКТА для визуализации как дуги аорты, так и экстраи интракраниального кровообращения для оценки риска интраоперационной эмболии при попытках катетеризации сонной артерии.
Коррекция дислипидемии
Нарушения липидного обмена являются ключевым драйвером прогрессии атеросклероза, одним из клинических проявлений которого является инсульт.
Существуют убедительные доказательства того, что назначение оптимальной гиполипидемической терапии является высокоэффективным способом снижения риска инсульта у пациентов с атеросклерозом сонных артерий. Длительная терапия статинами в адекватных дозах ассоциирована с улучшением прогноза, выживаемости, стабилизацией атеросклеротической бляшки и снижением риска рестеноза после стентирования сонной артерии. Лечение статинами рекомендовано для всех пациентов с атеросклеротическим поражением экстракраниальных артерий, которые перенесли ИИ [10-12]. Для диагностики дислипидемии рекомендуется провести анализ на содержание общего холестерина, липопротеидов высокой плотности, липопротеидов низкой плотности (ЛНП), липопротеида (а), повышение триглицеридов. Также рекомендовано провести анализ на наличие нарушений свертываемости крови. В качестве скрининга — активированное частичное тромбопластиновое время, международное нормализованное отношение при приеме антагонистов витамина К, протромбиновый индекс по Квику, фибриноген для определения риска кровотечений при выполнении инвазивных процедур и оценки эффективности терапии антикоагулянтами (если они принимаются).
Пациенты со стенозом сонных артерий >50% должны быть стратифицированы как лица очень высокого ССР без оценки 10-летнего риска фатальных сердечно-сосудистых осложнений с целевым уровнем ЛНП <1,4 ммоль/л [13] (табл. 2).
Таблица 2
Шкала глобальной оценки 10-летнего ССР

Сокращения: АД — артериальное давление, ЛНП — липопротеиды низкой плотности, СГХС — семейная гиперхолестеринемия, СД — сахарный диабет, СКФ — скорость клубочковой фильтрации, CCЗ — сердечно-сосудистые заболевания, ТИА — транзиторная ишемическая атака, ФР — фактор риска, ХБП — хроническая болезнь почек, ХС — холестерин.
Для коррекции дислипидемии показана высокоинтенсивная терапия статинами в максимально переносимых дозах. Если на фоне максимально переносимых доз статинов целевой уровень ЛНП не достигнут, показано добавление эзетимиба. В зоне вторичной профилактики, а также у пациентов очень высокого ССР в зоне первичной профилактики, при недостижении целевых значений на фоне максимально переносимой дозы статинов (+/эзетимиб) показано добавление ингибиторов PCSK9 [13].
У пациентов с подтвержденным атеросклеротическим ССЗ, перенесших повторное сосудистое событие в течение 2 лет (не обязательно в том же сосудистом бассейне), несмотря на прием максимально переносимой дозы статинов, рекомендован целевой уровень холестерина ЛНП <1,0 ммоль/л (табл. 3).
Таблица 3
Рекомендуемые целевые уровни холестерина ЛНП в зависимости от категории риска

Сокращение: ХС ЛНП — холестерин липопротеидов низкой плотности.
Артериальная гипертензия
АГ является общепризнанным ФР развития атеросклеротических ССЗ, включая поражение сонных артерий и инсульт. Метаанализ 4 рандомизированных клинических исследований (RESPECT, PASTBP, SPS3, PODCAST) выявил достоверное снижение риска повторного инсульта при использовании более строгих целевых показателей артериального давления (АД) <130 и 80 мм рт.ст. Следует отметить, что у пациентов с атеросклерозом крупных внутричерепных артерий (50-99%) рекомендовано достижение АД <140 и 90 мм рт.ст. Каждое повышение АД на 10 мм рт.ст. связано с повышением риска инсульта на 30-45%, а снижение АД на каждые 10 мм рт.ст. у пациентов с АГ снижает риск инсульта на 33% [14]. Антигипертензивная терапия рекомендуется пациентам с АГ и асимптомным атеросклеротическим поражением экстракраниальных артерий с достижением целевых цифр АД, согласно клиническим рекомендациям, одобренным научно-практическим советом Министерства здравоохранения Российской Федерации "Артериальная гипертензия у взрослых" [15]. Целевые значения АД представлены в таблице 4.
Таблица 4
Целевые значения АД, измеренного в медицинском учреждении, в зависимости от возраста и сопутствующих заболеваний
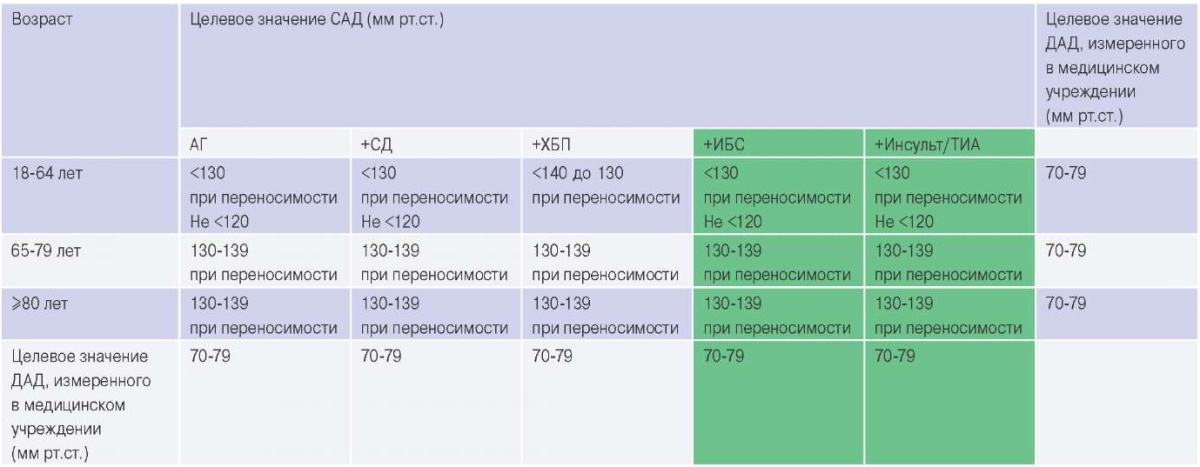
Сокращения: АГ — артериальная гипертензия, ДАД — диастолическое артериальное давление, ИБС — ишемическая болезнь сердца, САД — систолическое артериальное давление, СД — сахарный диабет, ТИА — транзиторная ишемическая атака, ХБП — хроническая болезнь почек.
В последней версии Европейских рекомендаций по кардиоваскулярной профилактике от 2021г пересмотрены позиции достижения целевого систолического АД (САД) 120-130 мм рт.ст. в сторону увеличения верхней границы возраста с 65 до 69 лет, при этом у пациентов старше 70 лет обозначено целевое значение САД <140 мм рт.ст. со снижением до 130 мм рт.ст. при хорошей переносимости. В связи с тем, что переносимость снижения АД у пациентов со стенозами сонных артерий может отличаться от таковой в общей популяции больных АГ, в настоящее время целевые уровни АД у всех пациентов, а особенно в возрастной категории >65 лет должны рассматриваться лечащим врачом индивидуально у каждого пациента с учетом индивидуальной переносимости. Однако с точки зрения прогноза целесообразно достигать снижения АД 130 и 80 мм рт.ст. и ниже у всех категорий пациентов [16].
В острейшем периоде ИИ пациентам с АГ и симптомным атеросклеротическим поражением экстракраниальных артерий рекомендуется гипотензивная терапия, согласно клиническим рекомендациям, одобренным НПС Минздрава России "Артериальная гипертензия у взрослых" и "Ишемический инсульт и транзиторная ишемическая атака у взрослых". С целью сокращения риска повторного ОНМК назначение антигипертензивной терапии рекомендовано сразу после ТИА и через несколько дней после ИИ с учетом рисков усиления церебральной ишемии при чрезмерном снижении АД. Пациентам, которым планируется проведение внутривенной тромболитической терапии, АД рекомендуется осторожно снизить и поддерживать на <180/105 мм рт.ст. в течение как минимум 24 ч после тромболизиса в связи с доказанными преимуществами в отношении прогноза неврологического восстановления. Пациентам с САД ≥220 и/или диастолического АД ≥120 мм рт.ст., которым не проводился тромболизис, рекомендуется назначение лекарственной терапии с целью снижения АД на 15% и в течение первых суток после инсульта решение принимается на основании оценки клинической ситуации. Рекомендовано снижать АД до цифр 180/100-105 мм рт.ст. у пациентов с гипертонической болезнью в анамнезе, а в остальных случаях — до уровня 160-180/90-100 мм рт.ст. Целесообразно продолжение гипотензивной терапии, начатой до дебюта ОНМК [1].
Антитромботическая терапия
Кардиоэмболический генез ИИ, возникающий в основном при фибрилляции предсердий, требует назначения антикоагулянтной терапии. Пациентам с атеросклерозом экстракраниальных артерий, которым показана антикоагулянтная терапия в связи с наличием механического протеза митрального или аортального клапана, рекомендовано назначение антагонистов витамина К (как, например, варфарин, со средним значением международного нормализованного отношения 2,5 (от 2,0 до 3,0)) для профилактики тромбоэмболических ишемических явлений. При наличии у пациента фибрилляции предсердий, без механического протеза, рекомендовано назначение непрямых оральных антикоагулянтов, что более эффективно и безопасно, чем антагонисты витамина К. При выполнении стентирования сонных артерий у пациентов, принимающих по показаниям варфарин, показан подбор антиагрегантной терапии (двойной или монотерапии) по данным лабораторного контроля коагулограммы, т.к. монотерапии антикоагулянтом недостаточно для предотвращения тромбоза стента [17].
Атеротромботический генез ИИ требует назначения антиагрегантной терапии [18]. Наиболее изученной в этой группе является ацетилсалициловая кислота (АСК). Назначение АСК в дозе от 100 мг ежедневно снижает риск повторного ИИ и серьезных сосудистых осложнений и рекомендуется всем пациентам со стенозом сонных артерий >50% [19].
Клопидогрел в дозировке 75 мг или сочетание ривароксабана 2,5 мг 2 раза/сут. с АСК 100 мг рекомендуется следующим группам пациентов при низком риске кровотечений:
- Пациентам с бессимптомным стенозом сонных артерий (≥60%) в сочетании с ИБС или другими формами атеросклероза;
- Пациентам с нелакунарным некардиоэмболическим ИИ или ТИА в сочетании c ИБС или другими формами атеросклероза, через 1 мес. после перенесенного события для снижения риска повторного инсульта/ТИА и сердечно-сосудистой смерти;
- Пациентам с ИБС или другими формами атеросклероза, после открытых и эндоваскулярных реконструктивных операций на сонных артериях [19][20].
Назначение антиагрегантной терапии у пациентов после ТИА или ИИ проводится согласно клиническим рекомендациям, одобренным научно-практическим советом Минздрава России "Ишемический инсульт и транзиторная ишемическая атака": двойная антиагрегантная терапия рекомендуется пациентам с малым (балл по NIHSS ≤3) некардиоэмболическим ИИ или ТИА высокого риска (>3 баллов по шкале ABCD2), ранняя (начало через 12-24 ч с момента появления симптомов (возможно позже, но не позже чем через 7 сут. с момента появления симптомов)) двойная антиагрегантная терапия (АСК и клопидогрел) продолжительностью не <21 сут. (но не >90 сут.) с последующим переходом на монотерапию антиагрегантным препаратом для снижения риска повторного ИИ [1].
Пациентам со стенозами <60% и не имеющим других показаний для антитромботической терапии назначать антиагреганты нецелесообразно, т.к. для больных данной группы не доказано преимущество такой терапии для профилактики инсульта в сравнении с риском геморрагических осложнений.
Хирургическое лечение
Целью лечения пациентов с каротидным стенозом является снижение риска возникновения инсульта. Основными детерминантами клинического течения у пациентов со стенозом каротидной бифуркации является наличие или отсутствие неврологической симптоматики и тяжесть стеноза. Лечение выбирают на основе оценки риска, связанного с вмешательством, и вероятности того, что конкретное вмешательство благоприятно изменит течение заболевания. Угроза инсульта у бессимптомных пациентов со стенозом внутренней сонной артерии (ВСА) <60% и у симптомных пациентов со стенозом <50% считается незначительной и не требует хирургического вмешательства. Результаты исследований ECST и NASCET продемонстрировали, что каротидная эндартерэктомия (КЭЭ) не приводит к значительному снижению частоты последующих неврологических событий у пациентов с неврологическими симптомами и стенозом бифуркации с уменьшением диаметра менее чем на 50%, и это фактически связано с увеличением заболеваемости по сравнению с медикаментозным лечением [21][22].
У пациентов с асимптомным стенозом >60% рекомендовано хирургическое лечение с целью профилактики инсульта. Оперативное лечение должно проводиться в учреждениях с частотой госпитальных осложнений (инсульт, смертельный исход) <2%. У пациентов с симптомным стенозом ВСА 50-99% (ТИА или ИИ) рекомендовано хирургическое лечение с целью профилактики повторного инсульта. Оперативное лечение должно проводиться в учреждениях с частотой госпитальных осложнений (инсульт, смертельный исход) <4% [23].
Предпочтительным методом лечения гемодинамически значимого стеноза сонной артерии является КЭЭ. Помимо симптоматического статуса пациента, существуют определенные анатомические и физиологические состояния, которые могут увеличить риск применения определенной методики реваскуляризации сонной артерии. Например, высокое расположение бифуркации сонной артерии или ранее перенесенное облучение шеи может увеличивать риск КЭЭ [23][24], а извитость брахиоцефальных артерий или морфологическая нестабильность атеросклеротической бляшки могут увеличить риск трансфеморального стентирования каротидных артерий [25][26].
При выборе техники КЭЭ (с пластикой заплатой или эверсионная) следует обращать внимание на характер поражения ВСА (длина атеросклеротической бляшки, степень выраженности кальциноза, диаметр ВСА) и анатомические взаимоотношения в операционной ране (уровень бифуркации общей сонной артерии, взаимоотношение с подъязычным нервом, ветвями лицевого нерва и др.). При выполнении КЭЭ через продольную артериотомию (классическая, открытая методика) рекомендуется пластика артериотомического дефекта заплатой. Использование первичного шва в такой ситуации повышает частоту рестенозов и окклюзий оперированной ВСА и связанную с ними частоту инсультов и летальности от инсультов в отдаленном периоде [27][28]. Рекомендовано применение как аутовенозных заплат, так и заплат из синтетических материалов (PTFE или дакрон), биологических материалов (ксеноперикард, консервированная твердая мозговая оболочка) или аутоартериальной заплаты из верхней щитовидной артерии.
Для пациентов с симптомными стенозами от 50% до 99%, которым требуется как КЭЭ, так и аортокоронарное шунтирование, рекомендовано выполнение КЭЭ до или одновременно с аортокоронарным шунтированием, что позволяет потенциально снизить риск инсульта или смерти. Последовательность вмешательства зависит от клинической картины и институционального опыта [29-35].
КЭЭ должна быть отложена у пациентов со стенозом ВСА 50-99% и острым инсультом, если уровень неврологического дефицита составляет ≥3 баллов по Шкале Рэнкина, имеется угнетение уровня бодрствования (любого), признаки ишемии головного мозга (>1/3 территории кровоснабжения средней мозговой артерии), в связи с высоким риском послеоперационных осложнений. Хирургическое лечение возможно после стабилизации инсульта через 48 ч от ишемического эпизода [1].
Рекомендовано рассмотреть необходимость использования интраоперационного введения протамина сульфата для инактивации гепарина после выполнения КЭЭ с целью уменьшения количества шейных гематом, требующих проведения повторных вмешательств [36].
При симптоматическом стенозе ВСА >50% и наличии у пациента трахеостомы или при перенесенном ранее облучении шеи, предпочтительно выполнять стентирование сонной артерии [37]. Также выполнение стентирования рекомендовано при рестенозе после ранее выполненной КЭЭ, контралатерального пареза черепно-мозговых нервов, предыдущего хирургического вмешательства на органах шеи, при распространении атеросклеротического поражения на внутричерепные отделы ВСА и в случае отсутствия должного опыта хирурга и технической возможности выполнения КЭЭ из-за анатомических особенностей расположения бифуркации сонной артерии.
Диспансерное наблюдение
После выполненной КЭЭ рекомендовано избегать интенсивных физических нагрузок в течение 2-3 нед. после операции. Всем пациентам, перенесшим открытые или эндоваскулярные операции по поводу стенозов ВСА, рекомендовано динамическое наблюдение кардиолога, с выполнением УЗДС брахиоцефальных артерий через 3 мес. после операции, далее — 1 раз в 6 мес., далее — 1 раз в год пожизненно.
Согласно Приказу Минздрава России от 15.03.2022 № 168Н "Об утверждении Порядка проведения диспансерного наблюдения за взрослыми", пациентам со стенозом ВСА от 40% при сочетании с ИБС и симптомным атеросклеротическим поражением периферических артерий или артерий другого сосудистого русла рекомендовано пожизненное диспансерное наблюдение врачом-кардиологом. Минимальная периодичность диспансерных приемов при закупорке и стенозе сонной артерии составляет не реже 2 раз в год.
Контролируемые показатели состояния здоровья в рамках проведения диспансерного наблюдения кардиологом:
- Вес (индекс массы тела);
- Окружность талии;
- АД, частота сердечных сокращений;
- Общетерапевтический биохимический анализ крови (с расчетом скорости клубочковой фильтрации), не реже 1 раза в год;
- Клинический анализ крови (не реже 1 раза в год);
- Холестерин ЛНП (не реже 2 раз в год);
- Электрокардиография (не реже 1 раз в год);
- УЗДС брахиоцефальных артерий (не реже 1 раза в год).
Пациентам со стенозом ВСА от 40% (за исключением сочетания с ИБС и симптомным атеросклеротическим поражением периферических артерий или артерий другого сосудистого русла) рекомендовано пожизненное диспансерное наблюдение врачом-терапевтом. Минимальная периодичность диспансерных приемов при закупорке и стенозе сонной артерии составляет не реже 2 раз в год.
Контролируемые показатели состояния здоровья в рамках проведения диспансерного наблюдения:
- Вес (индекс массы тела);
- Окружность талии;
- Статус курения;
- АД, частота сердечных сокращений;
- Холестерин ЛНП (не реже 2 раз в год);
- Уровень стеноза сонных артерий по данным ультразвукового допплеровского исследования сонных артерий (не реже 1 раза в год).
Пациентам с АГ 2-3 степени с поражением органов-мишеней, но без ССЗ, цереброваскулярной болезни и хронической болезни почек рекомендовано выполнение УЗДС сонных артерий у мужчин >40 лет, женщин >50 лет при индексе массы тела >30 кг/м2 и общем холестерине >5 ммоль/л при взятии под диспансерное наблюдение, далее по показаниям, но не реже 1 раза в 2 года с целью определения толщины интима медии и наличия атеросклеротических бляшек [15].
Пациентам, перенесшим ИИ или ТИА, рекомендовано диспансерное наблюдение невролога в течение 2 лет [1].
Диета и физическая активность
Диета, физические упражнения и сахароснижающие препараты рекомендованы для пациентов с СД и атеросклерозом экстракраниальных артерий.
Диета (содержащая овощи, свежие фрукты, молочные продукты с низким содержанием жиров, цельнозерновые продукты, рыбу и ненасыщенные жирные кислоты, с ограничением употребления мяса и насыщенных жирных кислот) [38].
Физические упражнения (как минимум 30 мин умеренных динамических аэробных физических нагрузок (ходьба, бег, езда на велосипеде или плавание) 5-7 дней/нед. Выполнение физических упражнений 2-3 раза/нед. также может быть рекомендовано. Для дополнительного эффекта здоровым лицам рекомендуется постепенное увеличение аэробных физических нагрузок средней интенсивности до 300 мин/нед. или высокой интенсивности — до 150 мин, или эквивалентная комбинация различных вариантов нагрузок [39].
Отношения и деятельность: все авторы заявляют об отсутствии потенциального конфликта интересов, требующего раскрытия в данной статье.
Список литературы
1. Акжигитов Р. Г., Алекян Б. Г., Алферова В. В. и др. Ишемический инсульт и транзиторная ишемическая атака у взрослых: Клинические рекомендации. 2021. 181 с. EDN DJFPJB.
2. Bulwa Z, Gupta A. Embolic stroke of undetermined source: The role of the nonstenotic carotid plaque. J Neurol Sci. 2017;382:49-52. doi:10.1016/j.jns.2017.09.027.
3. Nordestgaard BG, Chapman MJ, Humphries SE, et al. Familial hypercholesterolaemia is underdiagnosed and undertreated in the general population: guidance for clinicians to prevent coronary heart disease: consensus statement of the European Atherosclerosis Society. European heart journal. 2013;34(45):3478-90.
4. Blackham KA, Ansari SA, Hetts SW, et al. American College of Radiology. Standard for the performance of diagnostic cervicocerebral angiography in adults. Mance of diagnostic cervicocerebral angiography in adults. American College of Radiology Standards 2000-2001. Res-American College of Radiology Standards 2000-2001. Reston, Va: American College of Radiology; 2000: 415ton, Va: American College of Radiology. 2000:415-26.26.
5. Абугов С. А., Алекян Б. Г., Аракелян В. С. и др. Закупорка и стеноз сонной артерии: Клинические рекомендации. Москва: Министерство здравоохранения Российской Федерации, 2016.
6. Wardlaw JM, Chappell FM, Stevenson M, et al. Accurate, practical and cost-effective assessment of carotid stenosis in the UK. Health Technol Assess 2006; p. 1-182.
7. Naylor AR, Adair W. Cerebrovascular Disease: Diagnostic Evaluation. In: Sidawy A. N., Perler B. A., editors. Rutherford’s textbook of vascular surgery and endovascular therapy. 9th ed. Philadelphia: Elsevier; 2018. p. 1149-65.
8. Поморцев А. В., Шевелев В. И., Багдасарян К. А. Ультразвуковая диагностика патологий сонных артерий. Российский электронный журнал лучевой диагностики. 2020;10(2):195-204. doi:10.21569/2222-7415-2020-10-2-195-204. EDN UNBYFX.
9. Walker MD, Marler JR, Goldstein M, et al. Executive Committee for the Asymptomatic Carotid Atherosclerosis Study. Endarterectomy for asymptomatic carotid artery stenosis. JAMA. 1995;273:1421-8.
10. Amarenco P, Kim JS, Labreuche J, et al. A comparison of two LDL cholesterol targets after ischemic stroke. N Engl J Med. 2020;382(1):9. doi:10.1056/NEJMoa1910355.
11. Baigent C, Blackwell L, Emberson J, et al. Cholesterol Treatment Trialists Collaboration. Efficacy and safety of more intensive lowering of LDL cholesterol: a metaanalysis of data from 170,000 participants in 26 randomised trials. Lancet. 2010;376:1670-81.
12. Fulcher J, O’Connell R, Voysey M. Cholesterol Treatment Trialists Collaboration. Efficacy and safety of LDL-lowering therapy among men and women: metaanalysis of individual data from 174,000 participants in 27 randomised trials. Lancet. 2015;385:1397-405.
13. Kukharchuk VV, Yezhov MV, Sergienko IV, et al. Clinical recommendations of the Eurasian Association of Cardiologists (EOC)/National Society for the Study of Atherosclerosis (NOA, Russia) on the diagnosis and correction of lipid metabolism disorders for the prevention and treatment of atherosclerosis (2020). Eurasian Journal of Cardiology. 2020;(2):6-29. (In Russ.) doi:10.38109/2225-1685-2020-2-6-29.
14. Lawes CM, Bennett DA, Feigin VL, et al. Blood pressure and stroke: an overview of published reviews. Stroke. 2004;35:1024.
15. Кобалава Ж. Д., Конради А. О., Недогода С. В. и др. Артериальная гипертензия у взрослых. Клинические рекомендации 2020. Российский кардиологический журнал. 2020;25(3):3786. doi:10.15829/1560-4071-2020-3-3786.
16. ESC Scientific Document Group. 2021 ESC Guidelines on cardiovascular disease prevention in clinical practice: Developed by the Task Force for cardiovascular disease prevention in clinical practice with representatives of the European Society of Cardiology and 12 medical societies With the special contribution of the European Association of Preventive Cardiology (EAPC), European Heart Journal. 2021;42(34):3227-37. doi:10.1093/eurheartj/ehab484.
17. Рекомендации ЕОК/ЕОСХ по диагностике и лечению заболеваний периферических артерий 2017. Российский кардиологический журнал. 2018;(8):164-221. doi:10.15829/1560-4071-2018-8-164-221.
18. Фокин А. А., Трейгер Г. А. Новые возможности антитромботической терапии, улучшающие прогноз у пациентов со стенозирующим атеросклерозом сонных артерий. Ангиология и сосудистая хирургия. 2020;26(2):16-22. doi:10.33529/ANGIO2020215. EDN EFCUFZ.
19. Bonaca MP, Bauersachs RM, Anand SS, et al. Rivaroxaban in peripheral artery disease after revascularization. N Engl J Med. 2020;382:1994-2004.
20. Sharma M, Hart RG, Connolly SJ, et al. Stroke Outcomes in the COMPASS Trial. Circulation. 2019;139(9):1134-45. doi:10.1161/CIRCULATIONAHA.118.035864.
21. Psychogios M, Brehm A, López-Cancio E, et al. European Stroke Organisation guidelines on treatment of patients with intracranial atherosclerotic disease. Eur Stroke J. 2022;7(3):III-IV. doi:10.1177/23969873221099715.
22. Warlow Ch. MRC European Carotid Surgery Trial: interim results for symptomatic patients with severe (70-99%) or with mild (0-29%) carotid stenosis. European Carotid Surgery Trialists’ Collaborative Group. Lancet. 1991;337:1235-43.
23. Bonati LH, Kakkos S, Berkefeld J, et al. European Stroke Organisation guideline on endarterectomy and stenting for carotid artery stenosis. European Stroke Journal. 2021;6(2):I-XLVII. doi:10.1177/23969873211012121.
24. Simonian GT, Pappas PJ, Padberg FT, et al. Mandibular subluxation for distal internal carotid exposure: technical considerations. J Vasc Surg. 1999;30:1116-20.
25. Алекян Б. Г., Бокерия Л. А., Голухова Е. З. и др. Непосредственные и отдаленные результаты стентирования и каротидной эндартерэктомии у пациентов с атеросклеротическим поражением внутренней сонной артерии. Эндоваскулярная хирургия. 2021;8(1):27-36. doi:10.24183/2409-40802021-8-1-27-36. EDN LRFABX.
26. Faggioli G, Ferri M, Gargiulo M, et al. Measurement and impact of proximal and distal tortuosity in carotid stenting procedures. J Vasc Surg. 2007;46:1119-24.
27. Дюжиков А. А., Хрипун А. В., Малеванный М. В. и др. Ближайшие и отдаленные результаты применения каротидной эндартерэктомии и стентирования внутренних сонных артерий. Ангиология и сосудистая хирургия. 2013;19(2):93-110. EDN QAHCJZ.
28. Bond R, Rerkasem K, AbuRahma AF, et al. Patch angioplasty versus primary closure for carotid endarterectomy. Cochrane Database Syst Rev. 2004:Cd000160.
29. Ren S, Li X, Wen J, et al. Systematic review of randomized controlled trials of different types of patch materials during carotid endarterectomy. PLoS One. 2013;8:e55050.
30. Naylor AR, Mehta Z, Rothwell PM. Carotid artery disease and stroke during coronary artery bypass: a critical review of the literature. Eur J Vasc Endovasc Surg. 2002;23:283-94.
31. Schoof J, Lubahn W, Baeumer M, et al. Impaired cerebral autoregulation distal to carotid stenosis/occlusion is associated with increased risk of stroke at cardiac surgery with cardiopulmonary bypass. J Thorac Cardiovasc Surg. 2007;134:690-6.
32. Алекян Б. Г., Покровский А. В., Зотиков А. Е. и др. Результаты различных стратегий лечения пациентов с сочетанным поражением внутренних сонных и коронарных артерий. Эндоваскулярная хирургия. 2021;8(2):144-53. doi:10.24183/2409-4080-2021-8-2-144-153. EDN ZOOOVM.
33. Алекян Б. Г., Карапетян Н. Г., Мелешенко Н. Н., Ревишвили А. Ш. Результаты реваскуляризации миокарда у больных ишемической болезнью сердца с пограничным поражением коронарных артерий под контролем моментального резерва кровотока. Эндоваскулярная хирургия. 2021;8(1):20-6. doi:10.24183/2409-4080-2021-8-1-20-26. EDN KFSSNF.
34. Stamou SC, Hill PC, Dangas G, et al. Stroke after coronary artery bypass: incidence, predictors, and clinical outcome. Stroke. 2001;32:1508-13.
35. Naylor AR. Delay may reduce procedural risk, but at what price to the patient? Eur J Vasc Endovasc Surg. 2008;35:383-91.
36. Newhall KA, Saunders EC, Larson RJ, et al. Use of protamine for anticoagulation during carotid endarterectomy: a meta-analysis. JAMA Surg. 2016;151:247-55.
37. Bonati LH, Fraedrich G. Age modifies the relative risk of stenting versus endarterectomy for symptomatic carotid stenosis — a pooled analysis of EVA-3S, SPACE and ICSS. Eur J Vasc Endovasc Surg. 2011;41:153-8.
38. Драпкина О. М., Карамнова Н. С., Концевая А. В. и др. Российское общество профилактики неинфекционных заболеваний (РОПНИЗ). Алиментарно-зависимые факторы риска хронических неинфекционных заболеваний и привычки питания: диетологическая коррекция в рамках профилактического консультирования. Методические рекомендации. Кардиоваскулярная терапия и профилактика. 2021;20(5):2952. doi:10.15829/1728-8800-2021-2952.
39. Pelliccia A, Sharma S, Gati S, et al.; ESC Scientific Document Group. 2020 ESC Guidelines on sports cardiology and exercise in patients with cardiovascular disease. Eur Heart J. 2021;42(1):17-96. doi:10.1093/eurheartj/ehaa605. Erratum in: Eur Heart J. 2021;42(5):548-9.
Об авторах
М. А. ЧернявскийРоссия
Доктор медицинских наук, заведующий НИО сосудистой и интервенционной хирургии, главный научный сотрудник, сердечно-сосудистый хирург.
Санкт-Петербург
Конфликт интересов:
нет
О. Б. Иртюга
Россия
Кандидат медицинских наук, доцент кафедры кардиологии ИМО, заведующий НИЛ врожденных и приобретенных пороков сердца.
Санкт-Петербург
Конфликт интересов:
нет
С. Н. Янишевский
Россия
Доктор медицинских наук, доцент кафедры нервных болезней, заведующий НИЛ неврологии и нейрореабилитации, главный научный сотрудник НИЛ технологий прогнозирования риска развития сердечно-сосудистых осложнений.
Санкт-Петербург
Конфликт интересов:
нет
А. С. Алиева
Россия
Врач-кардиолог, кандидат медицинских наук, заведующий НИЛ нарушений липидного обмена и атеросклероза, руководитель Центра Атеросклероза и нарушений липидного обмена.
Санкт-Петербург
Конфликт интересов:
нет
К. А. Самочерных
Россия
Доктор медицинских наук, директор РНХИ им. проф. А. Л. Поленова, филиал.
Санкт-Петербург
Конфликт интересов:
нет
К. Б. Абрамов
Россия
Кандидат медицинских наук, заместитель главного врача по лечебной работе РНХИ им. проф. А.Л. Поленова, филиал.
Санкт-Петербург
Конфликт интересов:
нет
Т. В. Вавилова
Россия
Доктор медицинских наук, профессор, заведующий кафедрой лабораторной медицины и генетики.
Санкт-Петербург
Конфликт интересов:
нет
В. А. Лукьянчиков
Россия
Доктор медицинских наук, нейрохирург, профессор кафедры нейрохирургии и нейрореанимации.
Москва
Конфликт интересов:
нет
Д. И. Курапеев
Россия
Кандидат медицинских наук, заместитель генерального директора по информационным технологиям.
Санкт-Петербург
Конфликт интересов:
нет
А. Г. Ванюркин
Россия
Младший научный сотрудник НИО сосудистой и интервенционной хирургии.
Санкт-Петербург
Конфликт интересов:
нет
Д. В. Чернова
Россия
Сердечно-сосудистый хирург, врач ультразвуковой диагностики.
Санкт-Петербург
Конфликт интересов:
нет
Н. К. Шелуханов
Врач по лечебной физкультуре, врач физиотерапевт, заведующий отделом восстановительного лечения и медицинской реабилитации.
Санкт-Петербург
Конфликт интересов:
нет
А. В. Козленок
Россия
Кандидат медицинских наук, заведующий отделом функциональной и ультразвуковой диагностики.
Санкт-Петербург
Конфликт интересов:
нет
З. А. Кавтеладзе
Россия
Доктор медицинских наук, профессор, заместитель главного врача по региональному сосудистому центру ГКБ им. М.Е. Жадкевича.
Москва
Конфликт интересов:
нет
М. В. Малеванный
Россия
Кандидат медицинских наук, врач эндоваскулярный хирург, заведующий отделением, главный рентгенхирург Ростовской области.
Ростов-на-Дону
Конфликт интересов:
нет
Р. А. Виноградов
Россия
Доктор медицинских наук, заведующий отделением сосудистой хирургии.
Краснодар
Конфликт интересов:
нет
Т. Н. Хафизов
Россия
Кандидат медицинских наук, заведующий отделением по рентгенэндоваскулярным методам диагностики и лечения № 2, доцент кафедры госпитальной хирургии.
Уфа
Конфликт интересов:
нет
Г. Е. Иванова
Россия
Доктор медицинских наук, профессор, заведующий кафедрой медицинской реабилитации, руководитель Научно-исследовательского центра медицинской реабилитации.
Москва
Конфликт интересов:
нет
Н. В. Жуковская
Россия
Кандидат медицинских наук, заведующий отделением неврологии с ОНМК.
Санкт-Петербург
Конфликт интересов:
нет
А. А. Фокин
Россия
Доктор медицинских наук, профессор, заведующий кафедрой хирургии факультета послевузовского и дополнительного профессионального образования.
Челябинск
Конфликт интересов:
нет
И. М. Игнатьев
Россия
Доктор медицинских наук, профессор, член-корр. Академии наук Республики Татарстан, сердечно-сосудистый хирург.
Казань
Конфликт интересов:
нет
А. А. Карпенко
Россия
Доктор медицинских наук, профессор, руководитель центра сосудистой и гибридной хирургии.
Новосибирск
Конфликт интересов:
нет
П. В. Игнатенко
Россия
Заведующий отделением, сердечно-сосудистый хирург кардиохирургического отделения сосудистой патологии и гибридных технологий.
Новосибирск
Конфликт интересов:
нет
Д. А. Астапов
Россия
Доктор медицинских наук, врач сердечно-сосудистый хирург, заместитель генерального директора по организационно-методической работе.
Новосибирск
Конфликт интересов:
нет
В. Ю. Семенов
Россия
Доктор медицинских наук, профессор, заместитель Директора.
Москва
Конфликт интересов:
нет
В. А. Порханов
Россия
Доктор медицинских наук, профессор, академик РАН, директор.
Краснодар
Конфликт интересов:
нет
В. В. Крылов
Россия
Академик РАН, заведующий кафедрой нейрохирургии и нейрореанимации, главный научный сотрудник отделения неотложной нейрохирургии.
Москва
Конфликт интересов:
нет
Д. Ю. Усачев
Россия
Академик РАН, доктор медицинских наук, профессор.
Москва
Конфликт интересов:
нет
А. В. Светликов
Россия
Доктор медицинских наук, доцент кафедры факультетской хирургии СПбГУ, заведующий отделением сосудистой хирургии.
Санкт-Петербург
Конфликт интересов:
нет
Б. Г. Алекян
Россия
Академик РАН, доктор медицинских наук, профессор, руководитель Центра рентгенэндоваскулярной хирургии.
Москва
Конфликт интересов:
нет
Р. С. Акчурин
Россия
Академик РАН, профессор, заместитель генерального директора по хирургии, руководитель отдела сердечно-сосудистой хирургии НИИ Клинической кардиологии им. А. Л. Мясникова.
Москва
Конфликт интересов:
рпт
А. М. Чернявский
Россия
Академик РАН, доктор медицинских наук, профессор, директор.
Новосибирск
Конфликт интересов:
нет
А. О. Конради
Россия
Академик РАН, доктор медицинских наук, профессор, заместитель генерального директора по научной работе.
Санкт-Петербург
Конфликт интересов:
нет
Е. В. Шляхто
Россия
Академик РАН, доктор медицинских наук, профессор, генеральный директор, Президент Российского кардиологического общества, Заслуженный деятель науки РФ, главный кардиолог Санкт-Петербурга и Северо-Западного федерального округа.
Санкт-Петербург
Конфликт интересов:
нет
Рецензия
Для цитирования:
Чернявский М.А., Иртюга О.Б., Янишевский С.Н., Алиева А.С., Самочерных К.А., Абрамов К.Б., Вавилова Т.В., Лукьянчиков В.А., Курапеев Д.И., Ванюркин А.Г., Чернова Д.В., Шелуханов Н.К., Козленок А.В., Кавтеладзе З.А., Малеванный М.В., Виноградов Р.А., Хафизов Т.Н., Иванова Г.Е., Жуковская Н.В., Фокин А.А., Игнатьев И.М., Карпенко А.А., Игнатенко П.В., Астапов Д.А., Семенов В.Ю., Порханов В.А., Крылов В.В., Усачев Д.Ю., Светликов А.В., Алекян Б.Г., Акчурин Р.С., Чернявский А.М., Конради А.О., Шляхто Е.В. Российский консенсус по диагностике и лечению пациентов со стенозом сонных артерий. Российский кардиологический журнал. 2022;27(11):5284. https://doi.org/10.15829/1560-4071-2022-5284
For citation:
Chernyavsky M.A., Irtyuga O.B., Yanishevsky S.N., Alieva A.S., Samochernykh K.A., Abramov K.B., Vavilova T.V., Lukyanchikov V.A., Kurapeev D.I., Vanyurkin A.G., Chernova D.V., Shelukhanov N.K., Kozlyonok А.V., Kavteladze Z.A., Malevanny M.V., Vinogradov R.A., Khafizov T.N., Ivanova G.E., Zhukovskaya N.V., Fokin A.A., Ignatiev I.M., Karpenko A.A., Ignatenko P.V., Astapov D.A., Semenov V.Yu., Porkhanov V.A., Krylov V.V., Usachev D.Yu., Svetlikov A.V., Alekyan B.G., Akchurin R.S., Chernyavsky A.M., Konradi A.O., Shlyakhto E.V. Russian consensus statement on the diagnosis and treatment of patients with carotid stenosis. Russian Journal of Cardiology. 2022;27(11):5284. (In Russ.) https://doi.org/10.15829/1560-4071-2022-5284
JATS XML

















































