Перейти к:
Сравнительный анализ показателей деформации миокарда левого желудочка больных хронической сердечной недостаточностью ишемического и неишемического генеза
https://doi.org/10.15829/1560-4071-2022-5085
Аннотация
Цель. Провести сравнительный анализ деформационных показателей миокарда левого желудочка (ЛЖ), определяемых методом двухмерного стрейна, у больных хронической сердечной недостаточности (ХСН) с фракцией выброса (ФВ) ЛЖ ≤35% в зависимости от причины ХСН.
Материал и методы. В исследование было включено 133 больных ХСН NYHA 3-4 функционального класса с ФВ ЛЖ ≤35%, принимающих оптимальную медикаментозную терапию. Исходя из причины ХСН, были сформированы 2 группы больных ишемической кардиомиопатией (ИКМП), n=70, и неишемической кардиомиопатией (НКМП), n=63, которым проводилась speckletracking эхокардиография.
Результаты. У всех пациентов, включенных в исследование, были выявлены значительные сдвиги параметров продольной деформации в большинстве сегментов миокарда, максимально выраженные в базальных и средних отделах ЛЖ. При сравнительном анализе значений максимального систолического продольного стрейна худшие деформационные характеристики у больных ИКМП были выявлены в апикальных (р=0,008), а у пациентов с НКМП — в базальных сегментах ЛЖ (р=0,046). Изучаемые группы имели сопоставимые значения показателей глобального продольного и циркулярного стрейна ЛЖ (р=0,26; р=0,67; соответственно).
Заключение. Группы больных ХСН ишемического и неишемического генеза, несмотря на сопоставимые значения ФВ ЛЖ, различаются по характеру распределения снижения локальной продольной деформации отдельных сегментов ЛЖ. Худшие деформационные характеристики у больных ИКМП выявляются в апикальных сегментах, а у пациентов с НКМП — в базальных сегментах ЛЖ.
Для цитирования:
Илов Н.Н., Стомпель Д.Р., Бойцов С.А., Пальникова О.В., Нечепуренко А.А. Сравнительный анализ показателей деформации миокарда левого желудочка больных хронической сердечной недостаточностью ишемического и неишемического генеза. Российский кардиологический журнал. 2022;27(12):5085. https://doi.org/10.15829/1560-4071-2022-5085
For citation:
Ilov N.N., Stompel D.R., Boytsov S.A., Palnikova O.V., Nechepurenko A.A. Comparative analysis of left ventricular strain parameters in patients with heart failure of ischemic and non-ischemic genesis. Russian Journal of Cardiology. 2022;27(12):5085. (In Russ.) https://doi.org/10.15829/1560-4071-2022-5085
Распространенность синдрома хронической сердечной недостаточности (ХСН) неуклонно растёт. Согласно последним эпидемиологическим данным, ХСН страдает 1-2% всего взрослого населения развитых стран, а в возрасте старше 70 лет частота ХСН достигает >10% [1]. По оценкам экспертов около половины этой когорты составляют больные ХСН со сниженной фракцией выброса (ФВ) (ХСНнФВ) левого желудочка (ЛЖ).
Согласно действующим рекомендациям Европейского общества кардиологов, установление причины ХСН является первым шагом, имеющим решающее значение для планирования обоснованной терапии [1][2]. В ряде исследований было отмечено, что больные ишемической кардиомиопатией (ИКМП) — ХСН ишемического генеза чаще повторно обращаются за стационарной помощью, имеют более высокий риск внезапной сердечной смерти [3] и общую летальность [4], что может объясняться различиями в структурно-функциональном состоянии миокарда сердца и, в частности, ЛЖ. Имеющиеся работы, опирающиеся на результаты трансторакальной эхокардиографии (ЭхоКГ), свидетельствуют о значительном расширении камер сердца и тотальном ухудшении сократимости ЛЖ, характерных для всей когорты больных ХСНнФВ [2]. Имеющаяся ультразвуковая методика speckle-tracking ЭхоКГ позволяет провести комплексную оценку сократимости желудочков, исследуя утолщение стенок в радиальном направлении и укорочение в продольном и циркулярном направлении. Работы, посвященные изучению показателей деформации продольных и циркулярных волокон миокарда ЛЖ у больных ХСНнФВ, немногочисленны, что в сочетании с потенциальной возможностью получить дополнительную диагностическую информацию для разработки индивидуального подхода к ведению больных ХСНнФВ [5] может указывать на актуальность данного оригинального исследования.
Целью настоящего исследования стало проведение сравнительного анализа показателей деформации продольных и циркулярных волокон миокарда ЛЖ у больных ХСНнФВ с ФВ ЛЖ ≤35% в зависимости от происхождения ХСН.
Материал и методы
Отбор больных. Данное исследование было выполнено в соответствии со стандартами надлежащей клинической практики (Good Clinical Practice) и принципами Хельсинкской декларации. Дизайн исследования был одобрен локальным этическим комитетом ФГБОУ ВО Астраханского ГМУ Минздрава России (Протокол № 3 заседания ЛЭК от 30.12.2021г).
Набор больных проводился в период с 2018 по 2021гг. В исследование включались больные ХСН NYHA 3-4 функционального класса с ФВ ЛЖ ≤35% на фоне оптимальной медикаментозной терапии в течение, как минимум, трех последних месяцев, которым планировалось проведение имплантации кардиовертера-дефибриллятора с целью первичной профилактики внезапной сердечной смерти.
Из исследования исключались пациенты с гипертрофической кардиомиопатией, аритмогенной дисплазией правого желудочка, клапанной болезнью сердца и верифицированными наследственными каналопатиями. Критерием исключения также являлось наличие показаний к кардиохирургическому вмешательству (реваскуляризации, коррекции клапанной недостаточности), наличие выраженных нарушений ритма сердца, манифестирующих в период госпитализации.
После проверки на соответствие критериям включения/исключения в исследование было включено 133 больных. Ишемический генез ХСН устанавливался по клинико-анамнестическим данным и результатам ранее проведенной коронароангиографии. В случае наличия стенозирующего атеросклеротического поражения коронарных артерий пациента относили в группу ИКМП. В остальных случаях после исключения других заболеваний, которые могут приводить к ХСН, выставлялся диагноз "дилатационная кардиомиопатия", этих больных относили в группу неишемической кардиомиопатии (НКМП).
Включенные в исследование больные ИКМП были старше и чаще имели артериальную гипертензию (табл. 1).
Анализ ЭхоКГ. Всем пациентам двумя экспертами в условиях нормосистолии проводилась speckletracking ЭхоКГ на ультразвуковом аппарате экспертного класса EPIQ 5 (Philips, Нидерланды). Обязательным условием было наличие синусового ритма во время проведения исследования. С целью определения фаз сердечного цикла использовалась синхронная запись с электрокардиограммой. При обследовании пациентов производилась запись на жесткий диск ультразвукового аппарата для последующего просмотра и покадрового анализа различных параметров работающего сердца больного в реальном масштабе и времени. Для анализа механики ЛЖ регистрировали кинопетли из 3 сердечных циклов при частоте кадров не <60 в сек из парастернальной позиции по короткой оси на уровне митрального клапана и верхушки. Затем проводилась оценка механики ЛЖ с помощью ультразвуковой технологии speckle-tracking imaging с использованием аналитической программы (EchoPAC, GE Healthcare, США). Двухмерные изображения ЛЖ, зарегистрированные из парастернальной позиции по короткой оси ЛЖ на уровне митрального клапана, папиллярных мышц и верхушки, автоматически "замораживались" в конце систолы, и проводилось оконтуривание границ эндокарда.
Статистический анализ. Материалы исследования были подвергнуты статистической обработке с использованием методов параметрического и непараметрического анализа. Накопление, корректировка, систематизация исходной информации и визуализация полученных результатов проводилась в электронных таблицах Microsoft Office Excel 2010. Статистический анализ осуществлялся с использованием программы IBM SPSS Statistics 23. Описание и сравнение количественных показателей выполнялось с учетом распределения, соответствие которого нормальному оценивалось с помощью критерия Колмогорова-Смирнова. При подтверждении нормальности распределения данные описывались с помощью средней арифметической (M) и стандартного отклонения (SD). Сравнение выполнялось с помощью t-критерия Стьюдента. При отсутствии нормальности распределения указывались значения медианы (Me), нижнего и верхнего квартилей (Q1; Q3), показатели сравнивались с помощью критерия Манна-Уитни. Сравнение показателей, измеренных в номинальной шкале, проводилось при помощи критерия χ2 Пирсона. Критический уровень значимости при проверке статистических гипотез принимали равным 0,05.
Таблица 1
Клинико-демографическая характеристика пациентов, включенных в исследование
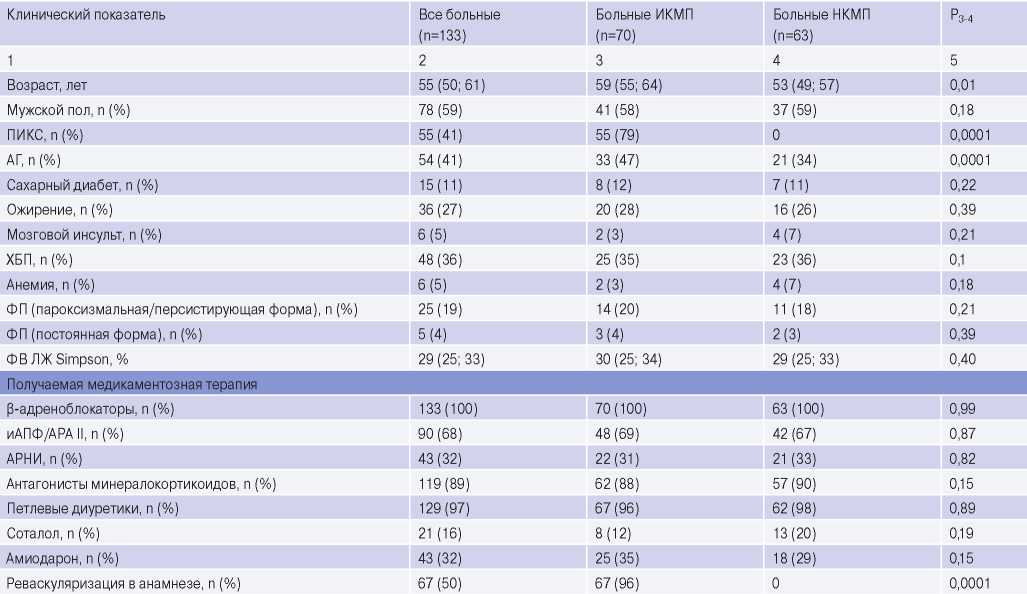
Примечание: данные представлены в виде Me (Q1; Q3), если не указано иное.
Сокращения: АГ — артериальная гипертензия, АРА II — антагонисты к рецепторы ангиотензина II, АРНИ — ангиотензиновых рецепторов и неприлизина ингибиторы, иАПФ — ингибиторы ангиотензинпревращающего фермента, ИКМП — ишемическая кардиомиопатия, НКМП — неишемическая кардиомиопатия, ПИКС — постинфарктный кардиосклероз, ФВ ЛЖ — фракция выброса левого желудочка, ФП — фибрилляция предсердий, ХБП — хроническая болезнь почек.
Результаты
У всех пациентов, включенных в исследование, было выявлено значительное снижение параметров продольной деформации ЛЖ в большинстве сегментов миокарда, максимально выраженное на уровне базальных сегментов и папиллярных мышц (табл. 2).
При сравнительном анализе значений максимального систолического продольного стрейна худшие деформационные характеристики у больных ИКМП были выявлены в апикальных (р=0,008), а у пациентов с НКМП — в базальных сегментах ЛЖ (р=0,046) (рис. 1). Изучаемые группы имели сопоставимые значения показателей глобального продольного и циркулярного стрейна ЛЖ.
Таблица 2
Показатели регионарной продольной и глобальной продольной и циркулярной деформации миокарда (%)
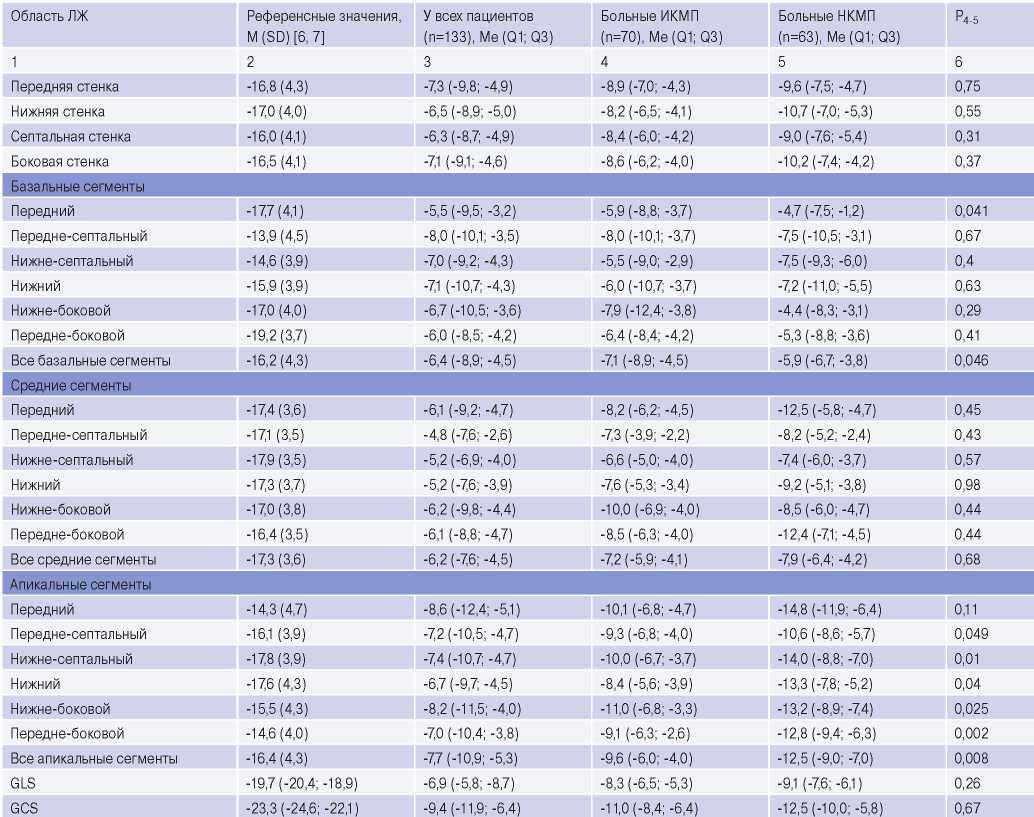
Примечание: данные представлены в виде Me (Q1; Q3), если не указано иное.
Сокращения: ИКМП — ишемическая кардиомиопатия, ЛЖ — левый желудочек, НКМП — неишемическая кардиомиопатия, GLS — глобальный продольный стрейн, GCS — глобальный циркулярный стрейн.

Рис. 1. Характер распределения регионарного продольного стрейна на 18-сегментарной модели ЛЖ ("бычий глаз") двух пациентов из сравниваемых групп. Для пациентов ИКМП было характерно максимальное снижение продольных стрейнов в апикальных сегментах (А), в группе НКМП худшие показатели продольной деформации миокарда ЛЖ выявлены в базальных сегментах (Б).
Обсуждение
В исследовании была проведена сравнительная оценка показателей деформации продольных и циркулярных волокон миокарда ЛЖ у больных с выраженной сердечной недостаточностью в зависимости от причины ХСН. На наш взгляд, заслуживают обсуждения зарегистрированные паттерны снижения показателей деформации миокарда. Так, у больных ИКМП было верифицировано выраженное снижение деформационных характеристик миокарда апикальных сегментов. Данный паттерн может быть связан с более плохим прогнозом, традиционно ассоциированным с течением ХСН ишемического происхождения. Хорошо известно, что миокардиальные волокна накапливают потенциальную энергию во время систолы и что высвобождение этой энергии во время очень ранней диастолы ускоряет релаксацию ЛЖ. Этот феномен, названный эластической отдачей, осуществляется благодаря инерционным усилиям, возникающим при сокращении апикальных сегментов ЛЖ [8]. Нарушения сократимости этой области могут привести к тяжелой диастолической дисфункции и ухудшению коронарной перфузии, что приобретает особое значение при исходно скомпрометированном кровотоке в коронарных артериях.
Согласно полученным результатам, для НКМП было характерно преобладание нарушений деформации в базальных сегментах ЛЖ. Похожие изменения были описаны исследователями при миокардитах [9], инфильтративных кардиомиопатиях, как проявление повреждения миокарда у больных новой коронавирусной инфекции (COVID-19) [10]. При проведении магнитно-резонансного исследования сердца у большинства реконвалесцентов COVID-19 выявлялся фиброз и миокардиальный отек преимущественно базальных и средних сегментов ЛЖ [11]. Zuo H, et al., изучив результаты speckle-tracking ЭхоКГ 84 больных ХСН (конечно-диастолический размер ЛЖ >55 мм, ФВ ЛЖ <45%), также обнаружили, что больные НКМП в сравнении с пациентами ИКМП имели более высокие значения продольного стрейна в апикальных (-11,8±5,4% vs -9,3±4,9%, p=0,027) и низкие показатели в базальных сегментах ЛЖ (-6,8±3,7% vs -9,1±3,8%, p=0,008) [12]. Павлюкова Е. Н. и др. на небольшой когорте больных ХСН продемонстрировали, что у больных с дилатационной кардиомиопатией глобальная деформация ЛЖ по окружности на уровне базальных сегментов в систолу снижена по сравнению со значениями этих показателей у пациентов с ИКМП. Авторам не удалось обнаружить существенных различий в глобальной деформации ЛЖ в продольном направлении [13].
Несмотря на малочисленность описанных случаев, схожесть полученных результатов заставляет задуматься о возможной повышенной восприимчивости базальных регионов ЛЖ к воспалительным или системным стрессорам [14]. Такое локальное ремоделирование может поддерживаться залегающей в атриовентрикулярной борозде эпикардиальной жировой тканью, объем которой коррелирует с уровнем профибротических факторов [8].
Ограничения исследования. К ограничениям исследования можно отнести одноцентровый характер, а также тот факт, что speckle-tracking ЭхоКГ проводилась только при отсутствии нарушений ритма во время проведения исследования.
Заключение
Результаты проведенного исследования указывают на то, что группы больных ХСНнФВ ишемического и неишемического генеза различаются по характеру распределения снижения локальной продольной деформации отдельных сегментов ЛЖ. Худшие деформационные характеристики у больных ИКМП выявляются в апикальных сегментах, а у пациентов с НКМП — в базальных сегментах ЛЖ.
Отношения и деятельность: все авторы заявляют об отсутствии потенциального конфликта интересов, требующего раскрытия в данной статье.
Список литературы
1. McDonagh TA, Metra M, Adamo M, et al. 2021 ESC Guidelines for the diagnosis and treatment of acute and chronic heart failure. Eur Heart J. 2021;42:3599-726. doi:10.1093/eurheartj/ehab368.
2. Tymińska A, Ozierański K, Balsam P, et al. Ischemic Cardiomyopathy versus NonIschemic Dilated Cardiomyopathy in Patients with Reduced Ejection Fraction — Clinical Characteristics and Prognosis Depending on Heart Failure Etiology (Data from European Society of Cardiology Heart Failure Registries). Biology (Basel). 2022;11:341. doi:10.3390/biology11020341.
3. Илов Н. Н., Пальникова О. В., Стомпель Д. Р. и др. Клинические предикторы возникновения желудочковых тахиаритмий у больных со сниженной систолической функцией левого желудочка. Результаты одноцентрового проспективного исследования. Кардиология. 2021;61(5):32-40. doi:10.18087/cardio.2021.5.n1480.
4. Beiert T, Straesser S, Malotki R, et al. Increased mortality and ICD therapies in ischemic versus non-ischemic dilated cardiomyopathy patients with cardiac resynchronization having survived until first device replacement. Arch Med Sci AMS. 2019;15:845. doi:10.5114/aoms.2018.75139.
5. Mandoli GE, Pastore MC, Benfari G, et al. New echocardiographic indices of shift to biventricular failure to optimize risk stratification of chronic heart failure. ESC Heart Failure. 2022;9:476-85. doi:10.1002/ehf2.13722.
6. Dalen H, Thorstensen A, Aase SA, et al. Segmental and global longitudinal strain and strain rate based on echocardiography of 1266 healthy individuals: the HUNT study in Norway. Eur Hear J. Cardiovasc Imaging. 2010;11:176-83. doi:10.1093/ejechocard/jep194.
7. Yingchoncharoen T, Agarwal S, Popović ZB, et al. Normal ranges of left ventricular strain: A meta-analysis. J Am Soc Echocardiogr. 2013;26:185-91. doi:10.1016/j.echo.2012.10.008.
8. Гриценко О. В., Чумакова Г. А., Груздева О. В. и др. Взаимосвязь эпикардиального ожирения и уровней маркеров фиброза миокарда. Российский кардиологический журнал. 2019;(4):13-9. doi:10.15829/1560-4071-2019-4-13-19.
9. Ha SJ, Woo JS, Kwon SH, et al. Acute regional myocarditis with normal ventricular wall motion diagnosed by two-dimensional speckle tracking imaging. Korean J Intern Med. 2013;28:732. doi:10.3904/kjim.2013.28.6.732.
10. Stöbe S, Richter S, Seige M, et al. Echocardiographic characteristics of patients with SARS-CoV-2 infection. Clin Res Cardiol. 2020;109:1549-66. doi:10.1007/s00392-02001727-5.
11. Huang L, Zhao P, Tang D, et al. Cardiac involvement in patients recovered from COVID2019 identified using magnetic resonance imaging. Cardiovasc Imaging 2020;13:2330-9. doi:10.1016/j.jcmg.2020.05.004.
12. Zuo H, Zhang Y, Ma F, et al. Myocardial Deformation Pattern Differs between Ischemic and Non-ischemic Dilated Cardiomyopathy: The Diagnostic Value of Longitudinal Strains. Ultrasound Med Biol. 2020;46:233-43. doi:10.1016/j.ultrasmedbio.2019.10.006.
13. Павлюкова Е. Н., Трубина Е. В., Карпов Р. С. Деформация левого желу дочка у больных с ишемической и дилатационной кардиомиопатией по данным ультразвуковой технологии "след пятна". Сибирский медицинский журнал. 2012;27(3):37-42.
14. Esposito R, Galderisi M, Santoro C, et al. Prominent longitudinal strain reduction of left ventricular basal segments in treatment-naïve Anderson-Fabry disease patients. Eur Hear Journal-Cardiovascular Imaging. 2019;20:438-45. doi:10.1093/ehjci/jey108.
Об авторах
Н. Н. ИловРоссия
Николай Николаевич Илов — кандидат медицинских наук, доцент кафедры сердечно-сосудистой хирургии, врач сердечно-сосудистый хирург отделения хирургического лечения сложных нарушений ритма сердца и электрокардиостимуляции.
Астрахань
Конфликт интересов:
все авторы заявляют об отсутствии потенциального конфликта интересов, требующего раскрытия в данной статье
Д. Р. Стомпель
Россия
Динара Рафаиловна Стомпель — заведующий отделением функциональной диагностики.
Астрахань
Конфликт интересов:
все авторы заявляют об отсутствии потенциального конфликта интересов, требующего раскрытия в данной статье
С. А. Бойцов
Россия
Сергей Анатольевич Бойцов — академик РАН, профессор, доктор медицинских наук, генеральный директор.
Москва
Конфликт интересов:
все авторы заявляют об отсутствии потенциального конфликта интересов, требующего раскрытия в данной статье
О. В. Пальникова
Россия
Олеся Викторовна Пальникова — врач-кардиолог отделения хирургического лечения сложных нарушений ритма сердца и электрокардиостимуляции.
Астрахань
Конфликт интересов:
все авторы заявляют об отсутствии потенциального конфликта интересов, требующего раскрытия в данной статье
А. А. Нечепуренко
Россия
Анатолий Анатольевич Нечепуренко — кандидат медицинских наук, заведующий отделением хирургического лечения сложных нарушений ритма сердца и электрокардиостимуляции.
Астрахань
Конфликт интересов:
все авторы заявляют об отсутствии потенциального конфликта интересов, требующего раскрытия в данной статье
Дополнительные файлы
Рецензия
Для цитирования:
Илов Н.Н., Стомпель Д.Р., Бойцов С.А., Пальникова О.В., Нечепуренко А.А. Сравнительный анализ показателей деформации миокарда левого желудочка больных хронической сердечной недостаточностью ишемического и неишемического генеза. Российский кардиологический журнал. 2022;27(12):5085. https://doi.org/10.15829/1560-4071-2022-5085
For citation:
Ilov N.N., Stompel D.R., Boytsov S.A., Palnikova O.V., Nechepurenko A.A. Comparative analysis of left ventricular strain parameters in patients with heart failure of ischemic and non-ischemic genesis. Russian Journal of Cardiology. 2022;27(12):5085. (In Russ.) https://doi.org/10.15829/1560-4071-2022-5085

















































