Перейти к:
Сравнительное изучение клинической эффективности биоаналогичного препарата Нектелиза (tenecteplase) по результатам рандомизированного клинического исследования
https://doi.org/10.15829/1560-4071-2025-6441
EDN: TTRUUD
Аннотация
Цель. Представить результаты сравнительного исследования эффективности и безопасности отечественного биоаналога Нектелиза (АО "ГЕНЕРИУМ", Россия) и референтного биологического препарата Метализе ("Берингер Ингельхайм Фарма ГмбХ и Ко.КГ", Германия) при применении у пациентов с инфарктом миокарда с подъемом сегмента ST (ИМпST) на электрокардиограмме.
Материал и методы. В исследование включены 244 пациента мужского (204) и женского (41) пола от 36 до 75 лет с ИМпST. Исследование проводилось в 14 клинических центрах Российской Федерации и 2 центрах Беларуси. Пациенты были рандомизированы в две группы 1:1: 122 пациента получали отечественный биоаналог Нектелиза, 122 пациента — референтный препарат Метализе. Основной критерий эффективности — частота реперфузии миокарда (3 степень коронарного кровотока по критериям TIMI). Оценка безопасности включала анализ нежелательных реакций, геморрагических осложнений тромболитической терапии и иммуногенности.
Результаты. Частота реперфузии миокарда (TIMI 3) составила 53,7% в группе Нектелиза и 57,1% в группе Метализе, что подтверждает терапевтическую эквивалентность препаратов (разница -3,4%, 95% доверительный интервал: от -16,0% до 9,1%). Профиль безопасности препарата Нектелиза был сопоставим с профилем безопасности Метализе, при этом в группе Нектелиза зафиксировано меньше нежелательных реакций (доля пациентов в группе Нектелиза 7,4% vs доли пациентов в группе Метализе 15,7%). Большая часть зарегистрированных нежелательных реакций представляла собой геморрагические осложнения тромболитической терапии (кровотечения различной степени и локализации). За время исследования было отмечено 13 эпизодов кровотечений у 8 пациентов группы Нектелиза и 30 эпизодов кровотечений у 16 пациентов группы Метализе. Частота возникновения больших кровотечений в группе Нектелиза и группе Метализе группы TIMI составляла 0,8% и 2,5%, по классификации ISTH — 0,8% и 3,3%, категории 5b по классификации BARC — 0% и 10%, соответственно. Частота геморрагических инсультов составила 1,2%, все случаи зарегистрированы в группе Метализе.
Заключение. На основании результатов проведенного клинического исследования доказано, что препарат Нектелиза (АО "ГЕНЕРИУМ", Россия) является биологическим аналогом препарата Метализе ("Берингер Ингельхайм Фарма ГмбХ и Ко.КГ", Германия).
Ключевые слова
Для цитирования:
Агиров М.М., Адзерихо И.Э., Исаева Е.Н., Калинина С.Г., Кашталап В.В., Константинов С.Л., Лапин О.М., Луганова А.Ю., Пристром А.М., Рошкаева И.П., Рябов В.В., Супрядкина Т.В., Хаишева Л.А., Шпагина Л.А., Юркин Е.П. Сравнительное изучение клинической эффективности биоаналогичного препарата Нектелиза (tenecteplase) по результатам рандомизированного клинического исследования. Российский кардиологический журнал. 2025;30(6):6441. https://doi.org/10.15829/1560-4071-2025-6441. EDN: TTRUUD
For citation:
Agirov M.M., Adzeriho I.E., Isaeva E.N., Kalinina S.G., Kashtalap V.V., Konstantinov S.L., Lapin O.M., Luganova A.Yu., Pristrom A.M., Roshkaeva I.P., Ryabov V.V., Supryadkina T.V., Khaisheva L.A., Shpagina L.A., Yurkin E.P. Comparative study of clinical efficacy of biosimilar Nektelisa (tenecteplase) based on randomized clinical trial. Russian Journal of Cardiology. 2025;30(6):6441. (In Russ.) https://doi.org/10.15829/1560-4071-2025-6441. EDN: TTRUUD
Тромболитическая терапия (ТЛТ) занимает прочное место в ряду способов лечения острого инфаркта миокарда (ОИМ), несмотря на достижения хирургических методов. При остром инфаркте миокарда (ИМ) с подъемом сегмента ST (ИМпST) введение тромболитических средств рекомендуется во всех случаях, когда нет возможности выполнить чрескожное эндоваскулярное вмешательство в течение 2 ч от начала симптомов, как можно раньше после постановки диагноза, т.е. на догоспитальном этапе [1].
Тенектеплаза как современный тромболитик третьего поколения демонстрирует высокую эффективность и безопасность, что подтверждается результатами клинических исследований и находит отражение в клинических рекомендациях1 [2].
Разработка биоаналогов представляет собой важное направление современной фармацевтической индустрии, обусловленное необходимостью повышения доступности высокоэффективных биологических препаратов для пациентов.
В данной статье представлены результаты сравнительного исследования эффективности и безопасности отечественного биоаналога Нектелиза (АО "ГЕНЕРИУМ", Россия) и референтного биологического препарата Метализе ("Берингер Ингельхайм Фарма ГмбХ и Ко.КГ", Германия) (NCT05601999 clinicaltrials.gov). Препарат Нектелиза, разработанный в качестве биоаналога препарата Метализе, показал высокую степень сопоставимости по показателям специфической активности in vitro, фармакодинамики in vivo, токсикокинетики, иммуногенности и общетоксического действия. По итогам пилотного сравнительного исследования I фазы были получены данные об отсутствии различий по изучаемым параметрам безопасности, иммуногенности, фибринолитической активности, эффективности и фармакокинетике, что послужило основанием для продолжения клинической разработки препарата Нектелиза и проведения настоящего исследования.
Целью исследования явилось сравнительное изучение эффективности и безопасности применения препаратов Нектелиза и Метализе у пациентов с ИМпST.
Материал и методы
Данное исследование было многоцентровым рандомизированным простым слепым сравнительным исследованием в параллельных группах эффективности и безопасности препаратов Нектелиза и Метализе у пациентов с острым ИМпST с централизованной заслепленной оценкой результатов коронарографии. Исследование проводилось в период с 2021 по 2024гг на базе 14 клинических центров на территории Российской Федерации и 2 клинических центров на территории Республики Беларусь. Проведение исследования было одобрено регуляторными органами Российской Федерации и Республики Беларусь. Исследование выполнено в соответствии с этическими принципами Хельсинкской декларации, с правилами ICH GCP, правилами надлежащей клинической практики ЕАЭС № 79 от 03 ноября 2016 г. Все документы исследования прошли локальную этическую экспертизу во всех клинических центрах. Каждым пациентом данного исследования было подписано информированное согласие до выполнения каких-либо процедур исследования.
Критерии отбора пациентов. В исследование были включены пациенты мужского или женского пола в возрасте от 18 до 75 лет на момент подписания формы информированного согласия с диагнозом ИМпST, установленном в соответствии с рекомендациями Европейского общества кардиологов [1].
Критерии невключения были определены в соответствии принципом безопасности участников исследования Надлежащей клинической практики, с соблюдением противопоказаний и ограничений, описанных в инструкции референтного препарата Метализе. Основное ограничение состояло в предотвращении участия в исследовании пациентов с заболеваниями и состояниями, существенно повышающими риск возникновения кровотечений различной локализации. Также критерии невключения обеспечивали минимизирование возможного влияния препаратов сопутствующей терапии на фармакокинетику и фармакодинамику исследуемой терапии.
Процедуры исследования. Исследование состояло из периода скрининга (до 6 ч с момента появления симптомов ОИМ), периода сравнительного лечения (введение препарата Нектелиза/Метализе не позднее 6 ч от начала заболевания) и периода наблюдения до 90 дней, из которых до 7 дней в условиях стационара. Исследуемые препараты вводились путем быстрой однократной внутривенной инъекции, доза препаратов рассчитывалась в зависимости от массы тела, максимальная доза не превышала 10000 ЕД (50 мг тенектеплазы). Введение препаратов осуществлялось на догоспитальном этапе в клинических центрах с собственной выездной бригадой скорой помощи или в стационаре в условиях отделения кардиореанимации или ангиографии под наблюдением врача-исследователя. Оценка эффективности и безопасности проводилась в дни 1, 2, 3, 7, 30 (заочно) и 90 (заочно).
Критерии оценки. Основным критерием оценки эффективности в исследовании являлась частота реперфузии миокарда при применении препаратов Нектелиза и Метализе по результатам независимой оценки коронарографии (3 степень коронарного кровотока по критериям TIMI). Коронарография проводилась всем пациентам в течение 24 ч, но не ранее 3 ч от начала введения препаратов в случае успешного тромболизиса или немедленно — при отсутствии эффекта от ТЛТ по данным электрокардиографии (ЭКГ) (снижение сегмента ST менее чем на 50% через 60 мин после начала введения). Централизованная независимая оценка эффективности реперфузии миокарда по результатам коронарографии осуществлялась как минимум двумя сертифицированными специалистами (рентгенэндоваскулярными хирургами), неосведомлёнными о целях и задачах настоящего исследования и назначенной терапии.
Дополнительные критерии эффективности включали оценку частоты реперфузии миокарда по результатам независимой оценки коронарографии (3 или 2 степень коронарного кровотока по критериям TIMI), частоты реперфузии миокарда по данным ЭКГ по снижению сегмента ST на 30%, 50%, 70% и более через 90 мин от начала введения препарата, динамики уровней тропонина Т и креатинкиназы МВ, смертности в течение 90 дней после перенесенного ИМ, сердечно-сосудистой смертности в период 30 и 90 дней после перенесённого ИМ, частоты развития постинфарктных осложнений за исключением нарушений ритма (истинного кардиогенного шока, клинических признаков застойной сердечной недостаточности (СН), острой аневризмы левого желудочка (ЛЖ), разрыва сердца, ранней постинфарктной стенокардии, повторного ИМ, инфаркта мозга) в первые 30 дней, частоты развития комбинированных событий "смерть от сердечно-сосудистых заболеваний (ССЗ) + рецидив ИМ + инсульт" и "смерть от ССЗ + рецидив ИМ + инсульт + СН" в течение 30 дней после перенесенного ИМ.
Показателями фибринолитической активности являлись динамика уровней фибриногена и D-димера.
В рамках сравнительного изучения фармакокинетики были рассчитаны следующие параметры: AUC0-t — площадь под кривой "концентрация-время" от момента введения до времени t, Cmax — максимальная концентрация (нг/мл), AUCinf — площадь под кривой "концентрация — время" от нулевого до бесконечности, Tmax — время достижения максимальной концентрации, T1/2 — период полувыведения, Kel — константа элиминации, Cl — клиренс, Vd — кажущийся объем распределения.
К оцениваемым показателям безопасности ТЛТ относились частота и тяжесть геморрагических осложнений (тяжесть определялась по классификации группы TIMI, по классификации BARC и по классификации ISTH), частота развития геморрагического инсульта, частота и тяжесть других нежелательных явлений (НЯ), связанных с применением препаратов, исследуемые показатели клинического и биохимического анализов крови, общего анализа мочи, а также количество и доля пациентов с наличием антилекарственных антител (АЛА); титр АЛА и их нейтрализующая активность.
Статистический анализ. Пациенты, рандомизированные с помощью Интерактивной автоматизированной системы, были распределены в две группы лечения в соотношении 1:1. Анализ данных выполнен с использованием программного обеспечения Stata версии 182.
При проведении статистического анализа было изучено четыре популяции пациентов: все пациенты, включенные в исследование (FAS, full analysis set), все пациенты, получившие исследуемый или референтный препарат (популяция безопасности), пациенты, завершившие исследование без значительных отклонений от протокола и для которых имелись данные по оценке, по крайней мере, одного параметра эффективности (PP-популяция), популяция для анализа фармакокинетических (ФК) параметров.
Для анализа основного критерия эффективности проводилось построение двустороннего 95% доверительного интервала (ДИ) для разности долей пациентов с реперфузией миокарда в сравниваемых группах с установленной двусторонней границей эквивалентности ±20%. Для оценки значения p использован χ²-критерий. Пациенты, у которых отсутствовали данные коронарографии, не включались в FAS- и PP-популяции при проведении анализа первичной конечной точки эффективности. Для анализа дополнительных критериев эффективности использовался χ²-критерий и, в случае необходимости, точный тест Фишера. Для учета влияния различных ковариат (пол, возраст, данные анамнеза и др.) использовалось построение модели логистической регрессии. При этом для каждого включенного параметра была дана точечная оценка для соотношения шансов, а также 95% ДИ для соотношения шансов.
Для оценки смертности и сердечно-сосудистой смертности после перенесенного ОИМ использовались метод Каплана-Мейера и регрессия Кокса. Сравнение кривых выживаемости проводилось с помощью лог-ранг теста.
Для анализа динамики уровней тропонина Т и креатинкиназы МВ, а также уровня фибриногена и D-димера использовалось построение обобщенной линейной модели (GLM). В зависимости от типа распределения переменных для post-hoc попарного межгруппового сравнения данных на скрининге и на различных визитах использовался t-тест либо критерий Манна-Уитни.
Для оценки индивидуальных значений ФК-параметров использовались актуальные значения времени взятия образца. Анализ данных на нормальность распределения был проведен при помощи критерия Шапиро-Уилка, а также с помощью теста на асимметрию и эксцесс. Для статистического анализа ФК-параметров и обработки ФК-кривых использовали программы Stata 18 и PkSolver.
Кодировка НЯ производилась в соответствии со словарем медицинских терминов для нормативно-правовой деятельности MedDRA. Частота развития НЯ рассчитывалась для каждого класса систем органов и по предпочтительному термину (ПТ) по каждому препарату. Для межгруппового сравнения этих показателей использовался χ²-критерий либо точный тест Фишера (в зависимости от типа распределения переменных). Для оценки динамики лабораторных показателей и показателей жизненно важных функций использовался дисперсионный анализ с повторными измерениями (RM-ANOVA) либо тест Фридмана. Для post-hoc попарного сравнения изменений указанных показателей относительно скрининга использовался парный t-тест (в зависимости от типа распределения переменных). При межгрупповом сравнении изменений относительно скрининга использовался t-тест либо критерий Манна-Уитни (в зависимости от типа распределения переменных). Для сравнительной оценки частоты образования АЛА был использован χ²-критерий или в случае необходимости точный тест Фишера (в зависимости от типа распределения переменных).
Результаты
В исследовании было скринировано 247 пациентов, 244 из которых (98,8%) соответствовали критериям включения/невключения и были рандомизированы в исследовании в соотношении 1:1 (FAS-популяция) (по 122 пациента в каждой группе лечения). В анализ параметров безопасности были включены данные 243 пациентов (99,6%), поскольку один пациент в группе Метализе досрочно выбыл из исследования, не получив введение назначенного препарата, и был исключен из состава популяции безопасности. Двоим пациентам ошибочно был введен препарат, не соответствующий распределению, в связи с чем в анализ параметров безопасности данные пациенты были включены по фактически полученному лечению. Распределение пациентов в популяциях приведено на рисунке 1.
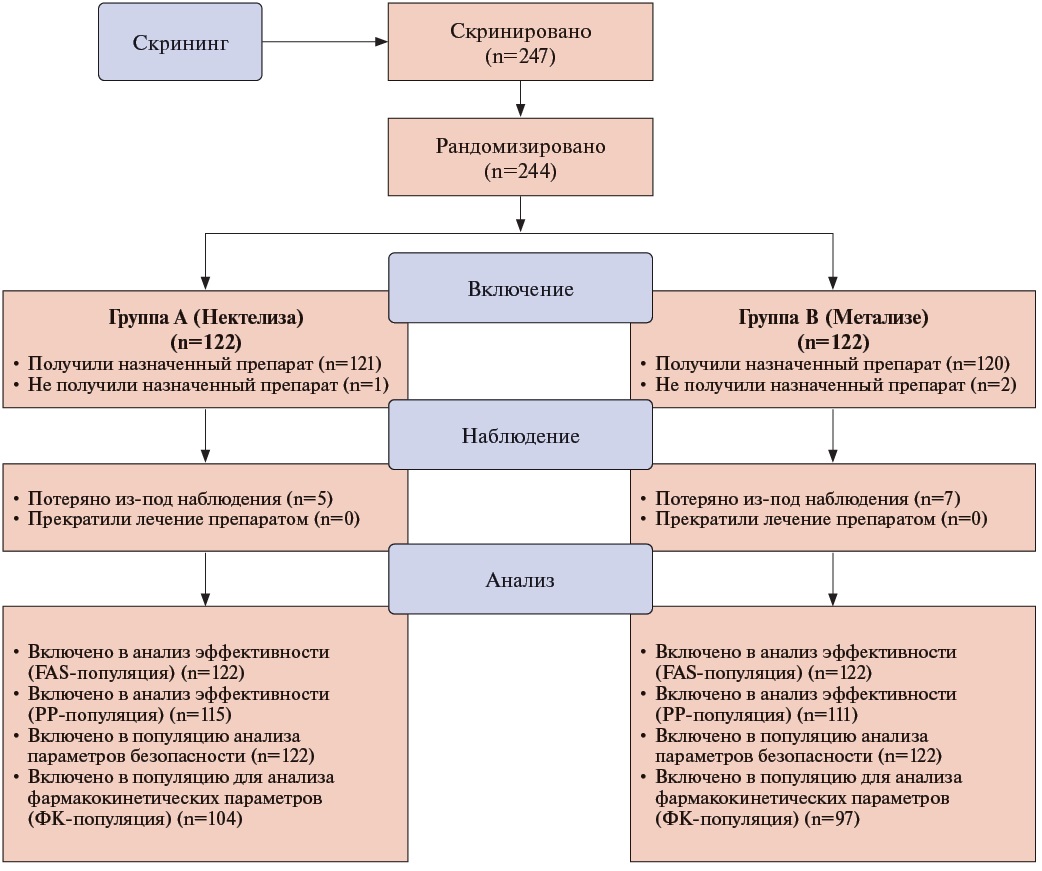
Рис. 1. Распределение пациентов исследования.
В исследование были включены пациенты в возрасте от 36 до 75 лет. Средний возраст составил 59,4±9,4 лет в группе А (Нектелиза) и 57,9±9,8 лет в группе Б (Метализе). Большая часть пациентов были мужского пола (83,2%), европеоидной расовой принадлежности (99,6%). Были выявлены статистически значимые различия в распределении пациентов по полу между группами, однако при проведении анализа первичного критерия эффективности построение модели логистической регрессии показало, что фактор пола не влиял на шансы достижения 3 степени коронарного кровотока по критериям TIMI. Среди перенесенных и сопутствующих заболеваний наиболее часто регистрировались нарушения со стороны сосудов, нарушения со стороны сердца и нарушения метаболизма и питания. Анализ данных по элевации сегмента ST ЭКГ в 12 отведениях на этапе скрининга показал, что группы были сопоставимы по значениям элевации ST во всех отведениях (p>0,05). Таким образом, проведенный анализ показал, что группы лечения были сопоставимы по исходным характеристикам. Основные исходные характеристики пациентов представлены в таблице 1.
Таблица 1
Исходные характеристики пациентов
|
Группа А (Нектелиза), n=122 |
Группа Б (Метализе), n=122 |
р |
|
|
Демографические данные |
|||
|
Возраст, лет (М±SD) |
59,4±9,4 |
57,9±9,8 |
0,223 |
|
Масса тела, кг (М±SD) |
83,6±15,6 |
82,9±13,4 |
0,707 |
|
ИМТ, кг/м² (М±SD) |
28,1±4,6 |
27,7±4,1 |
0,438 |
|
Пол (м/ж) (n (%)) |
95/27 (77,8/22,1) |
108/14 (88,5/11,5) |
0,026 |
|
Данные анамнеза по классам систем органов и предпочтительным терминам |
|||
|
Нарушения со стороны сосудов (N (%)) |
105 (86,1%) |
102 (85,0%) |
0,592 |
|
— артериальная гипертензия |
103 (84,4%) |
100 (82%) |
0,607 |
|
Нарушения со стороны сердца (N (%)) |
97 (79,5%) |
92 (75,4%) |
0,444 |
|
— сердечная недостаточность |
45 (36,9%) |
36 (29,5%) |
0,221 |
|
— хроническая сердечная недостаточность |
31 (25,4%) |
27 (22,1%) |
0,547 |
|
— стенокардия |
17 (13,9%) |
13 (10,7%) |
0,436 |
|
— инфаркт миокарда |
10 (8,2%) |
12 (9,8%) |
0,655 |
|
Нарушения метаболизма и питания (N (%)) |
92 (75,4%) |
88 (72,1%) |
0,560 |
|
— дислипидемия |
60 (49,2%) |
53 (43,4%) |
0,369 |
|
— ожирение |
38 (31,1%) |
34 (27,9%) |
0,574 |
|
— гипергликемия |
13 (10,7%) |
15 (12,3%) |
0,688 |
|
— гиперхолестеринемия |
12 (9,8%) |
15 (12,3%) |
0,540 |
|
— сахарный диабет 2 типа |
12 (9,8%) |
12 (9,8%) |
1,000 |
Сокращение: ИМТ — индекс массы тела.
Наиболее часто (от 50% до 100%) сопутствующее медикаментозное лечение пациентов включало антикоагулянтную и антиагрегантную терапию, применение препаратов группы бета-адреноблокаторов, анальгезирующих средств, рентген-контрастных веществ, препаратов, влияющих на ренин-ангиотензиновую систему и других препаратов для лечения заболеваний сердца, что соответствует стандартам оказания медицинской помощи пациентам с ОИМ. В соответствии с действующими стандартами лечения пациентов с ОИМ в качестве немедикаментозного лечения применялось чрескожное коронарное вмешательство (ЧКВ). В ходе исследования ЧКВ было проведено практически всем выжившим пациентам. Исключение составили 5 выживших пациентов, которым не было выполнено ЧКВ по различным причинам (у троих пациентов отсутствовали показания для проведения ЧКВ, 1 пациенту проведение ЧКВ было противопоказано, т.к. диаметр инфаркт-связанной артерии был <1 мм, одному пациенту ЧКВ не было выполнено по техническим причинам).
Эффективность
По результатам независимой оценки коронарографии достижение реперфузии миокарда (TIMI 3) в популяции FAS было выявлено у 65 пациентов из 121 (53,7%) в группе А (Нектелиза) и у 68 пациентов из 119 (57,1%) в группе Б (Метализе). Средняя разница составила -3,4% с 95% ДИ от -16,0% до 9,1%. Статистически значимых различий между группами не выявлено (р=0,594). Полученный 95% ДИ для FAS-популяции находился в пределах установленных границ эквивалентности ±20%. Аналогичный результат был получен для PP-популяции: средняя разница между группами составила -5,1% с 95% ДИ от -18,1 до 7,8%. Статистически значимых различий между группами не выявлено (р=0,438). Полученный 95% ДИ для РР-популяции также находился в пределах установленных границ эквивалентности ±20%. Результаты анализа эффективности ТЛТ по данным независимой оценки КАГ представлены в таблице 2.
Таблица 2
Данные по частоте достижения реперфузии миокарда по результатам независимой оценки коронарографии
|
Группа |
FAS-популяция |
PP-популяция |
||
|
Реперфузия миокарда TIMI 3 |
P (χ²) |
Реперфузия миокарда TIMI 3 |
P (χ²) |
|
|
Группа А (Нектелиза) |
65/121 (53,7%) |
0,594 |
61/115 (53,0%) |
0,438 |
|
Группа Б (Метализе) |
68/119 (57,1%) |
64/110 (58,2%) |
||
|
95% ДИ для разности |
-3,4% (-16,0%; 9,1%) |
-5,1% (-18,1%; 7,8%) |
||
Сокращения: ДИ — доверительный интервал, FAS — full analysis set, все пациенты, включенные в исследование, PP-популяция — пациенты, завершившие исследование без значительных отклонений от протокола и для которых имелись данные по оценке, по крайней мере, одного параметра эффективности.
Для учета влияния различных ковариат (пол, возраст) было проведено построение модели логистической регрессии для шансов достижения реперфузии (TIMI 3). Анализ не выявил факторов, имеющих статистически значимую ассоциацию с шансами достижения коронарного кровотока TIMI 3 как в FAS-популяции, так и в РР-популяции (p>0,05).
Анализ данных по результатам независимой оценки коронарографии показал, что реперфузия (TIMI 3+2) в популяции FAS была достигнута у 70,3% группы А (Нектелиза) и у 69,8% группы Б (Метализе). Статистически значимых различий между группами не выявлено (p=0,933), среднее значение величины различий составило 0,5% с 95% ДИ от -11,1% до 7,7%. Аналогичные результаты были получены в популяции РР: реперфузия миокарда была достигнута у 69,6% пациентов группы А (Нектелиза) и у 70,9% пациентов группы Б (Метализе) (среднее значение для разности -1,3% (95% ДИ от -13,3% до 10,6%), р=0,826). В целом между группами по достижению любой степени коронарного кровотока в пораженном сосуде по критериям TIMI не было выявлено статистически значимых отличий ни в FAS-популяции, ни в РР-популяции (р>0,05).
Анализ частоты реперфузии миокарда при применении препаратов Нектелиза и Метализе по данным ЭКГ через 60 мин от начала введения препарата показал, что реперфузия миокарда (снижение сегмента ST ≥50%) в FAS-популяции наступила у 57,5% в группе А (Нектелиза) и у 67,8% в группе Б (Метализе) (p=0,233). Аналогичные результаты получены для РР-популяции.
Анализ маркеров ОИМ (тропонина Т и креатинкиназы МВ) показал динамику, характерную для клинического течения ОИМ. Статистически значимых различий между группами ни в одной точке не выявлено (р>0,05) (рис. 2).
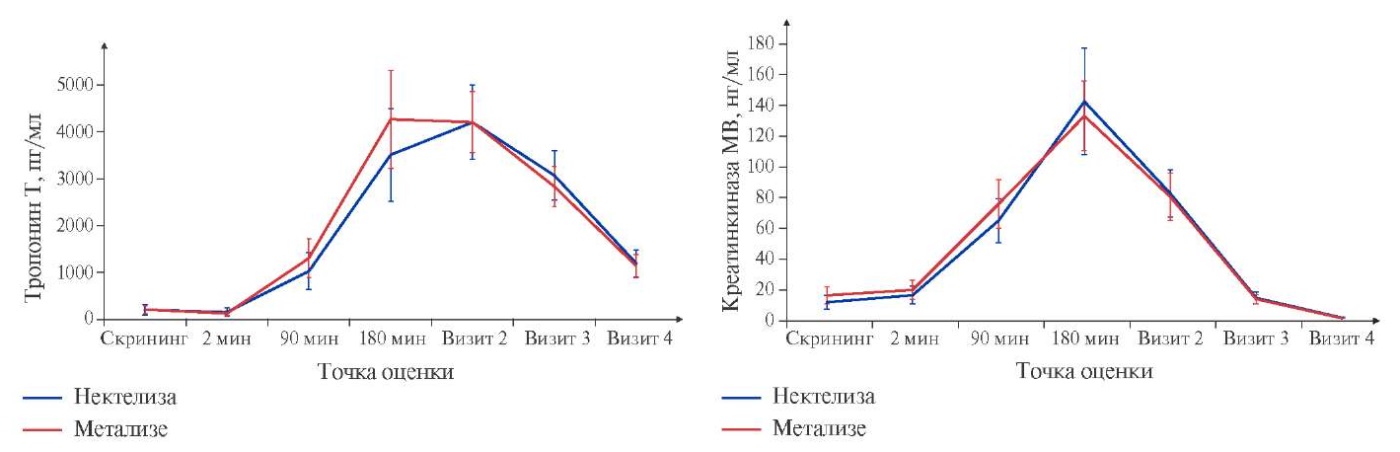
Рис. 2. Сравнительная динамика уровней тропонина Т и креатинкиназы МВ входе исследования (до введения, через 2 мин, 180 мин, 360 мин, на 2, 3 и 7 день после введения исследуемого препарата/референтного препарата).
Для оценки смертности и сердечно-сосудистой смертности за время исследования был использован метод Каплана-Мейера (рис. 3). Статистически значимых отличий между группами лечения не выявлено (FAS-популяция, р=0,524; РР-популяция, р=0,319). За время исследования умерло 10 пациентов (4 пациента группы А, 6 пациентов группы Б), из них 4 пациента от сердечно-сосудистых причин (по 2 пациента в каждой группе) в первые 30 дней после перенесенного ОИМ.
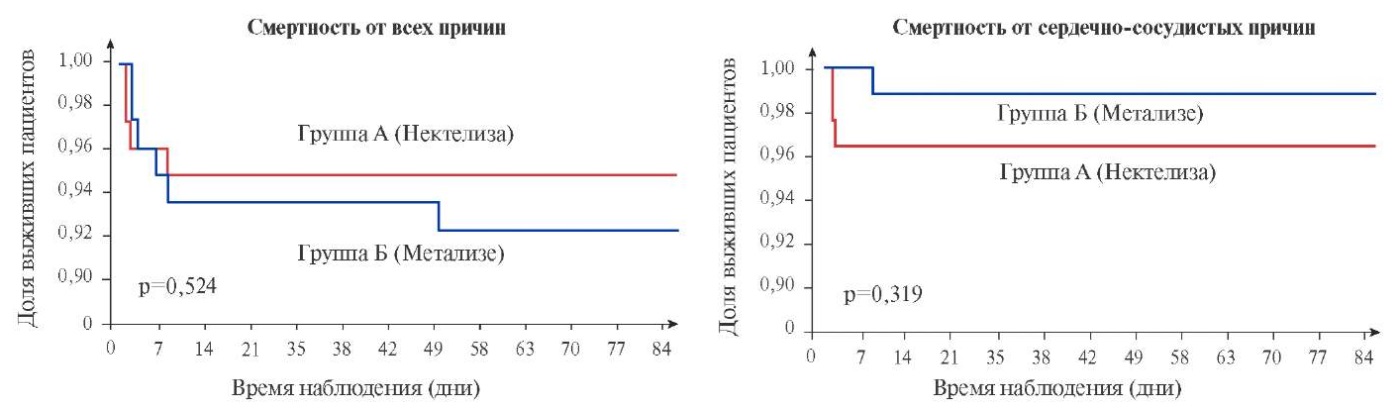
Рис. 3. Кривые Каплана-Мейера для смертности за время исследования (FAS-популяция).
Анализ данных по результатам регистрации постинфарктных осложнений (истинного кардиогенного шока, клинических признаков застойной СН, острой аневризмы ЛЖ, разрыва сердца, ранней постинфарктной стенокардии, повторного ИМ, инфаркта мозга) показал, что среди постинфарктных осложнений наиболее часто регистрировались клинические признаки застойной СН в обеих группах лечения: у 17,2% пациента в группе А (Нектелиза) и у 20,5% пациентов в группе Б (Метализе). Все остальные осложнения встречались с частотой <5%. Аналогичные данные были получены для РР-популяции. Статистически значимых отличий между группами лечения не выявлено (p>0,05).
Комбинированные события "смерть от ССЗ + рецидив ИМ + инсульт" были зарегистрированы у 2,5% пациентов группы A (Нектелиза) и у 6,6% пациентов группы Б (Метализе). Комбинированные события "смерть от ССЗ + рецидив ИМ + инсульт + СН" были зарегистрированы у 19,7% пациентов из группы A (Нектелиза) и у 26,2% пациентов из группы Б (Метализе). Схожая частота развития комбинированных событий наблюдалась в РР-популяции. Между группами не было статистически значимых отличий по частоте развития комбинированных событий в течение 30 сут. после перенесенного ОИМ (р>0,05).
Анализ показал, что исследуемый препарат Нектелиза эквивалентен референтному препарату Метализе по основному критерию эффективности. Было показано отсутствие различий по всем дополнительным критериям оценки эффективности.
Показателями фибринолитической активности являлись динамика уровней фибриногена и D-димера и определялись на скрининге, сразу после введения, через 180 и 360 мин после введения исследуемого и референтного препарата в дни 2, 3 и 7 (рис. 4). При межгрупповом сравнении не было выявлено статистически значимых отличий по уровням фибриногена и D-димера в каждой из точек в обеих популяциях (p>0,05).
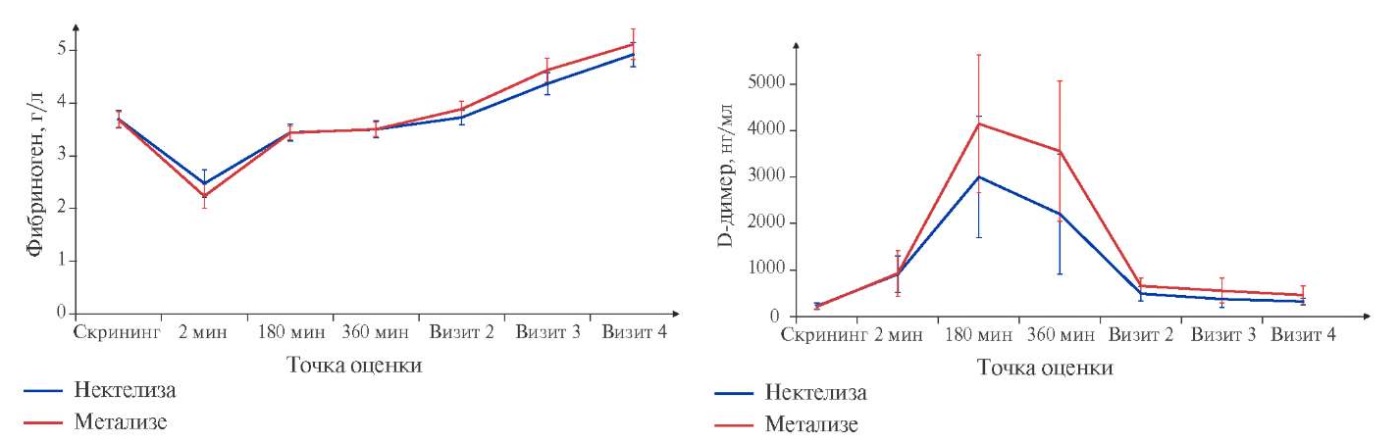
Рис. 4. Сравнительная динамика уровней показателей фибринолитической активности входе исследования (до введения, через 2 мин, 180 мин, 360 мин, на 2, 3 и 7 день после введения исследуемого препарата/референтного препарата).
Фармакокинетика
Для оценки индивидуальных значений ФК-параметров были использованы актуальные значения времени взятия образца. На рисунке 5 приведены усредненные ФК-кривые "концентрация — время". Были получены следующие значения ФК-параметров (указаны медианы и Q1, Q3): в группе исследуемого препарата Нектелиза AUC0-t — 540,52 (409,07, 691,77) мкг×мин/мл, Cmax — 11,08 (8,71, 13,73) мкг/мл, AUC0-inf — 557,07 (418,21, 739,03) мкг×мин/мл, Tmax — 2 (2, 2) мин, T1/2 — 69,3 (62,5, 74,1) мин, Kel — 0,0100 (0,0093, 0,0111) мин -¹, Cl — 80,03 (59,50, 103,81) мл/мин, Vd — 7,98 (5,83, 10,04) л; в группе референтного препарата Метализе AUC0-t — 538,61 (455,36, 657,31) мкг×мин/мл, Cmax — 11,19 (8,91, 13,64) мкг/мл, AUC0-inf — 550,42 (466,45, 671,28) мкг×мин/мл, Tmax — 2 (2, 2) мин, T1/2 — 66,3 (61,7, 72,2) мин, Kel — 0,0105 (0,0096, 0,0112) мин -¹, Cl — 80,80 (61,84, 95,60) мл/мин, Vd — 7,92 (5,64, 10,27) л.
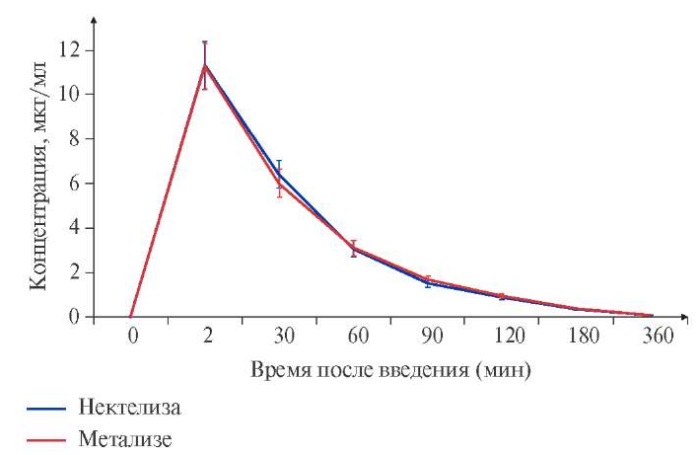
Рис. 5. Усредненные ФК-кривые (ФК-популяция).
Статистически значимых отличий между группами по концентрации тенектеплазы в образцах крови пациентов ни в одной из измеряемых временных точек не выявлено (p>0,05), что говорит о схожести ФК-профилей исследуемого препарата Нектелиза и референтного препарата Метализе. Проведенное межгрупповое сравнение ФК параметров Cmax, AUC0-t, AUC0-inf, Tmax, T1/2, Кel, Cl, Vd не выявило статистически значимых отличий между группами (p>0,05).
Безопасность
Данные 243 пациентов, получивших однократное введение исследуемого препарата Нектелиза или препарата сравнения Метализе, были учтены для анализа безопасности. Всего в исследовании было зарегистрировано 753 эпизода НЯ, развившихся у 213 пациентов. При сравнении по любому ПТ статистически значимых различий по частоте НЯ между группами лечения не было (р=0,981).
Среди всех зарегистрированных НЯ только 15 эпизодов имели связь с исследуемым препаратом Нектелиза, 35 НЯ имели связь с референтным препаратом Метализе. Таким образом, доля пациентов с нежелательными реакциями (НР) в группе А (Нектелиза) составила 7,4%, в группе Б (Метализе) составила 15,7%. Большая часть НР представляла собой геморрагические осложнения ТЛТ. При межгрупповом сравнении по любому ПТ доля пациентов с НР в группе Б (Метализе) была достоверно выше (р=0,042). Также статистически достоверная разница зарегистрирована в доле пациентов с НР "спонтанная гематома" за счет большего количества пациентов группы Б (Метализе) (р=0,029). По остальным НР статистически значимых отличий между группами лечения не выявлено (p>0,05) (табл. 3).
Таблица 3
НЯ, по мнению исследователя, связанные с введением исследуемого препарата (НР)
|
Описание |
Группа А (Нектелиза), N=122 |
Группа Б (Метализе), N=121 |
p-value |
||
|
N |
% |
N |
% |
||
|
Любой предпочтительный термин |
9 |
7,4 |
19 |
15,7 |
0,042 |
|
Общие нарушения и реакции в месте введения |
4 |
3,3 |
6 |
5,0 |
0,539 |
|
Гематома в месте инъекции |
4 |
3,3 |
5 |
4,1 |
0,749 |
|
Гематома в месте прокола сосуда |
0 |
0,0 |
1 |
0,8 |
0,498 |
|
Нарушения со стороны почек и мочевыводящих путей |
2 |
1,6 |
7 |
5,8 |
0,102 |
|
Гематурия |
2 |
1,6 |
7 |
5,8 |
0,102 |
|
Нарушения со стороны крови и лимфатической системы |
2 |
1,6 |
6 |
5,0 |
0,172 |
|
Спонтанная гематома |
0 |
0,0 |
5 |
4,1 |
0,029 |
|
Анемия |
1 |
0,8 |
1 |
0,8 |
1,000 |
|
Постгеморрагическая анемия |
1 |
0,8 |
0 |
0,0 |
1,000 |
|
Желудочно-кишечные нарушения |
2 |
1,6 |
3 |
2,5 |
0,684 |
|
Десневое кровотечение |
1 |
0,8 |
1 |
0,8 |
1,000 |
|
Пищеводное кровотечение |
0 |
0,0 |
2 |
1,7 |
0,247 |
|
Желудочно-кишечное кровотечение |
1 |
0,8 |
0 |
0,0 |
1,000 |
|
Гематемезис |
1 |
0,8 |
0 |
0,0 |
1,000 |
|
Нарушения со стороны нервной системы |
0 |
0,0 |
3 |
2,5 |
0,122 |
|
Геморрагический инсульт |
0 |
0,0 |
3 |
2,5 |
0,122 |
|
Нарушения со стороны сердца |
0 |
0,0 |
2 |
1,7 |
0,247 |
|
Стенокардия |
0 |
0,0 |
1 |
0,8 |
0,498 |
|
Брадикардия |
0 |
0,0 |
1 |
0,8 |
0,498 |
|
Травмы, интоксикации и осложнения процедур |
0 |
0,0 |
2 |
1,7 |
0,247 |
|
Кровоподтек |
0 |
0,0 |
1 |
0,8 |
0,498 |
|
Реокклюзия коронарной артерии |
0 |
0,0 |
1 |
0,8 |
0,498 |
|
Нарушения со стороны сосудов |
0 |
0,0 |
2 |
1,7 |
0,247 |
|
Гематома |
0 |
0,0 |
1 |
0,8 |
0,498 |
|
Гипотензия |
0 |
0,0 |
1 |
0,8 |
0,498 |
|
Лабораторные и инструментальные данные |
1 |
0,8 |
0 |
0,0 |
1,000 |
|
Снижение количества тромбоцитов |
1 |
0,8 |
0 |
0,0 |
1,000 |
|
Нарушения со стороны дыхательной системы, органов грудной клетки и средостения |
1 |
0,8 |
0 |
0,0 |
1,000 |
|
Носовое кровотечение |
1 |
0,8 |
0 |
0,0 |
1,000 |
Все зарегистрированные НР описаны ранее в литературе и инструкции референтного препарата.
Критериям серьезности в исследовании отвечали 55 эпизодов (СНЯ), развившихся у 40 пациентов: 24 у 19 пациентов в группе А (Нектелиза) и 31 у 21 пациента в группе Б (Метализе). Статистически значимых различий по числу СНЯ между группами лечения не выявлено (р>0,05). Три СНЯ, завершившиеся летальным исходом, имели связь с применением референтного препарата Метализе, представляли собой геморрагические осложнения ТЛТ (геморрагический инсульт).
За время исследования было отмечено 43 эпизода НЯ у 24 пациентов, которые были квалифицированы, как геморрагические осложнения ТЛТ, и были связаны с исследуемой терапией. Оценка частоты и тяжести геморрагических осложнений проводилась по трем классификациям: группы TIMI, BARC и ISTH. Межгрупповое сравнение не выявило статистически значимой разницы по частоте и тяжести геморрагических осложнений ни в одной из классификаций (р>0,05).
В соответствии с классификациями группы TIMI к большим кровотечениям относились 6 НЯ: 3 случая геморрагического инсульта, желудочно-кишечное кровотечение, рвота кровью, постгеморрагическая анемия, которые развились у 4 пациентов. Частота развития геморрагических осложнений в каждой группе представлена в таблице 4.
Таблица 4
Частота развития геморрагических осложнений по критериям группы TIMI
|
Показатель |
Группа А (Нектелиза), N=122 |
Группа Б (Метализе), N=121 |
p-value |
||
|
Число пациентов |
% |
Число пациентов |
% |
||
|
Большие кровотечения |
1 |
0,8% |
3 |
2,5% |
0,255 |
|
Умеренные кровотечения |
0 |
0,0% |
2 |
1,7% |
|
|
Минимальные кровотечения |
7 |
5,7% |
11 |
9,1% |
|
|
Геморрагический инсульт |
0 |
0% |
3 |
2,5% |
0,122 |
По классификации ISTH было определено 7 эпизодов больших кровотечений — 3 случая геморрагического инсульта, желудочно-кишечное кровотечение, рвота кровью, постгеморрагическая анемия, пищеводное кровотечение, 3 из которых развились у 1 пациента группы А (Нектелиза) и 4 у 4 пациентов группы Б (Метализе). Все фатальные кровотечения (type 5b) по классификации BARC представляли собой геморрагические инсульты.
Частота развития геморрагических инсультов составила 1,2% в популяции безопасности, при этом все 3 случая зарегистрированы у пациентов группы Б (Метализе) (2,5%), все завершились летальным исходом.
Около половины всех зарегистрированных НЯ (49,5%) разрешились без последствий, 1,3% НЯ завершились летальным исходом. Всего в исследовании было зарегистрировано 10 летальных исходов: 4 в группе А (Нектелиза) и 6 в группе Б (Метализе). Межгрупповое сравнение по исходам НЯ выявило статистически значимые различия (р=0,028), при этом отличия в долях пациентов незначительные, и не имеют клинической значимости, учитывая особенности исследуемой популяции.
Большинство НЯ не требовали медикаментозной коррекции (70,7%). В отношении 29,3% эпизодов НЯ для их купирования потребовалось медикаментозное лечение, проведение повторного ЧКВ или другие методы лечения. Статистически значимых отличий между группами по принятым мерам в отношении НЯ не зарегистрировано (р=0,934).
Оценка лабораторных показателей, параметров физикального обследования, жизненно важных функций организма, ЭКГ также не выявило существенных различий между группами.
Анализ показателей иммуногенности не выявил статистически значимых отличий между группами по частоте обнаружения АЛА (p>0,05). Нейтрализующие антитела к тенектеплазе определялись у двух пациентов (по одному в каждой группе лечения) на 7 день. Ни у одного из пациентов с наличием АЛА не было зарегистрировано реакций гиперчувствительности.
Обсуждение
Разработка и исследования биоаналогов в Российской Федерации проводятся в соответствии с международными требованиями с целью доказательства их сопоставимости по показателям качества, безопасности и эффективности оригинальному препарату.
В статье представлены результаты многоцентрового рандомизированного простого слепого исследования в параллельных группах эффективности и безопасности препарата Нектелиза в сравнении с препаратом Метализе у пациентов с острым ИМпST с централизованной заслепленной оценкой результатов коронарографии.
В качестве первичной конечной точки исследования выбрана доля пациентов с ангиографической реперфузией 3 степени по критериям TIMI. Частота достижения полной реваскуляризации (реперфузия TIMI 3) инфаркт-связанной артерии на 90 мин является релевантной клинической конечной точкой, поскольку она высоко коррелирует с достижением клинических исходов, таких как смертность и функция ЛЖ3 [3]. По сравнению со степенью реперфузии TIMI 2, полная реваскуляризация в течение 90 мин после проведения тромболизиса ассоциируется с 46% снижением уровня смертности4. В опубликованном метаанализе по оценке связи степени восстановления коронарного кровотока, смертностью и клиническими исходами Anderson JL, et al. было показано, что полная реперфузия (TIMI 3) является положительным прогностическим фактором для выживаемости, степени восстановления функции ЛЖ, восстановления скорости нормализации уровня сердечных ферментов и низкого риска развития СН [4]. Общая смертность по 5 исследованиям, включенным в метаанализ, составила 8,8% для TIMI 0-1; 7,0% для TIMI 2 и 3,7% для TIMI 3 (p<0,0001 при сравнении TIMI 3 и TIMI <3, и р<0,001 при сравнении TIMI 3 и 2).
Настоящее исследование проводилось с целью показать, что доля пациентов с ангиографической реперфузией 3 степени в группе исследуемого препарата не будет отличаться от доли пациентов в группе сравнения более чем на 20% (абсолютная разница).
По результатам независимой оценки коронарографии 3 степень коронарного кровотока по критериям TIMI в популяции FAS была выявлена у 53,7% в группе А (Нектелиза) и у 57,1% в группе Б (Метализе). Средняя разница составила -3,4% с 95% ДИ от -16,0% до 9,1%. Статистически значимых различий между группами не выявлено (р=0,594). Таким образом, полученный 95% ДИ для FAS-популяции находился в пределах установленных границ эквивалентности ±20%. Полученные данные согласуются с результатами опорного исследования референтного препарата, на основании которого производился расчет выборки (частота реперфузии TIMI 3-62,7%) [5].
По дополнительным конечным точкам эффективности также не выявлено статистически значимых различий между группами лечения.
Не было выявлено статистически значимых различий между препаратами Нектелиза и Метализе по воздействию на уровни фибриногена и D-димера в динамике у пациентов с ОИМ, что свидетельствует о том, по что исследуемый препарат Нектелиза и референтный препарат Метализе обеспечивают одинаковые фармакодинамические эффекты.
Препарат Нектелиза продемонстрировал профиль безопасности схожий с профилем безопасности препарата Метализе.
Среди всех зарегистрированных в ходе исследования НЯ 15 эпизодов имели связь с исследуемым препаратом Нектелиза, 35 НЯ имели связь с референтным препаратом Метализе. Доля пациентов с НР в группе А (Нектелиза) составила 7,4%, в группе Б (Метализе) составила 15,7%. При межгрупповом сравнении по развитию любого НР доля пациентов в группе Б (Метализе) была достоверно выше (р=0,042). Также статистически достоверная разница в доле пациентов с зафиксированной спонтанной гематомой за счет пациентов группы Метализе (р=0,029). Данное отличие вероятно обусловлено влиянием коморбидного фона пациентов, а также потенцирующим действием препаратов сопутствующей терапии (например, антиагрегантов и антикоагулянтов). По остальным НР статистически значимых отличий между группами лечения не выявлено (p>0,05). Большая часть НР представляла собой геморрагические осложнения ТЛТ. Все зарегистрированные НР описаны ранее в литературе и инструкции референтного препарата5. Частота развития геморрагических инсультов составила 1,2% в популяции безопасности, при этом все 3 случая зарегистрированы у пациентов группы Б (Метализе). Данные по частоте развития внутричерепных кровоизлияний (в т.ч. геморрагического инсульта) согласуются с литературными данными по референтному препарату — частота возникновения внутричерепных кровоизлияний при ТЛТ, предшествующей ЧКВ, составляет ~1,6%5.
Заключение
Результаты проведенного многоцентрового рандомизированного простого слепого исследования подтверждают терапевтическую эквивалентность по основному критерию эффективности биоаналогичного лекарственного препарата Нектелиза (АО "ГЕНЕРИУМ", Россия) и оригинального (референтного) лекарственного препарата Метализе ("Берингер Ингельхайм Фарма ГмбХ и Ко.КГ", Германия) при лечении пациентов с острым ИМпST, а также отсутствие различий по изучаемым параметрам эффективности, безопасности, иммуногенности и фармакокинетики.
Благодарности. Авторы выражают благодарность сотрудникам аналитической лаборатории в лице к.б.н. Лягоскина И. В, научному менеджеру проекта к.м.н. Матюшиной Р. О., операционному менеджеру проекта Онищуку А. А., медицинскому монитору д.м.н. Зозуле О. В., специалисту по управлению данными Гутковской Л. А. за сбор и подготовку данных, обсуждение результатов работы, ценные замечания и предложения.
Отношения и деятельность. Финансирование для этого исследования было предоставлено АО "ГЕНЕРИУМ". АО "ГЕНЕРИУМ" отвечало за дизайн исследования, а также за сбор и анализ данных. Решение представить рукопись было сделано авторами и одобрено АО "ГЕНЕРИУМ". Все перечисленные авторы соответствуют критериям авторства, установленным Международным комитетом редакторов медицинских журналов.
1. World Health Organization (WHO). (2020). Guidelines for the management of acute myocardial infarction. https://www.who.int.
2. Stata Statistical Software: Release 18. College Station T: SL, 2.
3. Guideline on clinical investigation of new medicinal products for the treatment of acute coronary syndrome EMA/CHMP/760125/2016 20 July 2017.
4. Fath-OrdDubadi F, Huehns T, AI-Mohammad A, et al. 1022-105 TIMI Grade 2 Flow is not Equivalent to TIMI 3: Implications for the Use of Thrombolytic Therapy. A Meta--Analysis of the Trials. JACC. 1995 Feb, 25 (2_Supplement_1) 401A. doi:10.1016/0735-1097(95)93121-R.
5. Metalyse: EPAR-Product Information/Annex I — Summary of product characteristics.
Список литературы
1. Аверков О. В., Арутюнян Г. К., Дупляков Д. В. и др. Острый инфаркт миокарда с подъемом сегмента ST электрокардиограммы. Клинические рекомендации 2024. Российский кардиологический журнал. 2025;30(3):6306. doi:10.15829/1560-4071-2025-6306. EDN: IVJCUK.
2. Tanswell P, Modi N, Combs D, Danays T. Pharmacokinetics and pharmacodynamics of tenecteplase in fibrinolytic therapy of acute myocardial infarction. Clin Pharmacokinet. 2002;41(15):1229-45. doi:10.2165/00003088-200241150-00001.
3. Gibson CM, Cannon CP, Murphy SA, et al. Relationship of TIMI myocardial perfusion grade to mortality after administration of thrombolytic drugs. Circulation. 2000;101(2):125-30. doi:10.1161/01.cir.101.2.125.
4. Anderson JL, Karagounis LA, Califf RM. Metaanalysis of five reported studies on the relation of early coronary patency grades with mortality and outcomes after acute myocardial infarction. Am J Cardiol. 1996;78(1):1-8. doi:10.1016/s0002-9149(96)00217-2.
5. Cannon CP, Gibson CM, McCabe CH, et al. TNK-tissue plasminogen activator compared with front-loaded alteplase in acute myocardial infarction: results of the TIMI 10B trial. Thrombolysis in Myocardial Infarction (TIMI) 10B Investigators. Circulation. 1998;98(25):2805-14. doi:10.1161/01.cir.98.25.2805.
Об авторах
М. М. АгировРоссия
Зав. отделением реанимации и интенсивной терапии 2 подразделения РЦВМТ.
Нальчик
Конфликт интересов:
Нет
И. Э. Адзерихо
Беларусь
Д.м.н., профессор кафедры клинической фармакологии и фармакотерапии.
Минск
Конфликт интересов:
Нет
Е. Н. Исаева
Россия
К.м.н., руководитель отдела клинических исследований, врач кардиолог.
Казань; Арск
Конфликт интересов:
Нет
С. Г. Калинина
Россия
Д.м.н., зав. отделением кардиореанимации и интенсивной терапии.
Екатеринбург
Конфликт интересов:
Нет
В. В. Кашталап
Россия
Д.м.н., зав. отделом клинической кардиологии.
Кемерово
Конфликт интересов:
Нет
С. Л. Константинов
Россия
Зав. отделением неотложной кардиологии.
Белгород
Конфликт интересов:
Нет
О. М. Лапин
Россия
К.м.н., зав. кардиологическим отделением для лечения больных инфарктом миокарда.
Пермь
Конфликт интересов:
Нет
А. Ю. Луганова
Россия
Врач-кардиолог.
Барнаул
Конфликт интересов:
Нет
А. М. Пристром
Беларусь
Д.м.н., профессор, зав. кафедрой кардиологии и ревматологии.
Минск
Конфликт интересов:
Нет
И. П. Рошкаева
Россия
Зав. подстанцией — врач скорой медицинской помощи.
Томск
Конфликт интересов:
Нет
В. В. Рябов
Россия
Д.м.н., профессор, член-корр. РАН, зам. директора по научной и лечебной работе.
Томск
Конфликт интересов:
Нет
Т. В. Супрядкина
Россия
К.м.н., доцент кафедры госпитальной терапии и эндокринологии, зав. отделением неотложной кардиологии.
Архангельск
Конфликт интересов:
Нет
Л. А. Хаишева
Россия
Д.м.н., доцент, зав. кафедрой терапии.
Ростов-на-Дону
Конфликт интересов:
Нет
Л. А. Шпагина
Россия
Д.м.н., профессор, зав. кафедрой госпитальной терапии и медицинской реабилитации.
Новосибирск
Конфликт интересов:
Нет
Е. П. Юркин
Россия
К.м.н., зам. директора по медицинской части.
Кемерово
Конфликт интересов:
Нет
Рецензия
Для цитирования:
Агиров М.М., Адзерихо И.Э., Исаева Е.Н., Калинина С.Г., Кашталап В.В., Константинов С.Л., Лапин О.М., Луганова А.Ю., Пристром А.М., Рошкаева И.П., Рябов В.В., Супрядкина Т.В., Хаишева Л.А., Шпагина Л.А., Юркин Е.П. Сравнительное изучение клинической эффективности биоаналогичного препарата Нектелиза (tenecteplase) по результатам рандомизированного клинического исследования. Российский кардиологический журнал. 2025;30(6):6441. https://doi.org/10.15829/1560-4071-2025-6441. EDN: TTRUUD
For citation:
Agirov M.M., Adzeriho I.E., Isaeva E.N., Kalinina S.G., Kashtalap V.V., Konstantinov S.L., Lapin O.M., Luganova A.Yu., Pristrom A.M., Roshkaeva I.P., Ryabov V.V., Supryadkina T.V., Khaisheva L.A., Shpagina L.A., Yurkin E.P. Comparative study of clinical efficacy of biosimilar Nektelisa (tenecteplase) based on randomized clinical trial. Russian Journal of Cardiology. 2025;30(6):6441. (In Russ.) https://doi.org/10.15829/1560-4071-2025-6441. EDN: TTRUUD

















































