Перейти к:
Роль ремоделирования левого предсердия при подтвержденной сердечной недостаточности с сохраненной фракцией выброса: фокус на своевременную диагностику
https://doi.org/10.15829/1560-4071-2025-6308
EDN: SGCIBB
Аннотация
Цель. Исследовать структурно-функциональное состояние сердца при подтвержденной сердечной недостаточности с сохраненной фракцией выброса (СНсФВ) в зависимости от тяжести диастолической дисфункции (ДД) левого желудочка (ЛЖ).
Материал и методы. Осуществлен анализ данных 303 пациентов с ДД ЛЖ (45,2% мужчин, средний возраст 66,3±6,0 года). Диастолический стресс-тест (ДСТ) проведен при недостаточном количестве критериев для заключения о СНсФВ по данным эхокардиографии покоя (n=251). В исследование включены 153 пациента с подтвержденной СНсФВ (35,3% мужчин, средний возраст 67,0±5,6 года). Группу I (n=101) составили пациенты со снижением диастолического резерва ЛЖ при ДСТ (E/e′ >14); группу II (n=52) — больные с выраженной ДД ЛЖ в покое, не требующие ДСТ для заключения о СНсФВ. Метод отслеживания движения пятен (speckle tracking echo) использован для оценки деформации резервуарной фазы левого предсердия (Left Atrial reservoir Strain, LASr).
Результаты. При анализе основных клинико-функциональных параметров между группами были выявлены статистически значимые различия по тесту 6-мин ходьбы (400,0 [360,0;440,0] м в группе I и 365,5 [310,5;401,5] м в группе II, соответственно; р<0,001) и концентрации N-концевого промозгового натрийуретического пептида (NT-proBNP) (257,7 [100,0;443,3] пг/мл и 412,0 [191,4;780,2] пг/мл; р=0,002). При проведении эхокардиографии покоя выявлены достоверные различия по индексу объема левого предсердия (иоЛП) (33,5 [29,2;40,1] мл/м2 и 40,8 [37,3;47,6] мл/м2; р<0,001), отношению E/e′ (11,3 [10,1;12,6] и 16,3 [14,9;19,2]; р<0,001), LASr (21,3 [19,5;24,7]% и 15,0 [12,5;17,3]%; р<0,001). По данным корреляционного анализа у больных СНсФВ выявлены связи умеренной силы: LASr и E/e′ (r=-0,538; р<0,001), LASr и иоЛП (r=-0,443; р<0,001), отмечено отсутствие связи между LASr и NT-proBNP (r=-0,157; р=0,060). При анализе ДСТ были выявлены статистически значимые различия по всем характеристикам увеличения ДН ЛЖ в группе I.
Заключение. Для пациентов с подтвержденной СНсФВ при увеличении давления наполнения ЛЖ характерно угнетение резервуарной функции ЛП и расширение полости ЛП. Фазовый анализ деформации ЛП и проведение ДСТ позволяет своевременно диагностировать СНсФВ.
Ключевые слова
Для цитирования:
Широков Н.Е., Ярославская Е.И., Криночкин Д.В., Мусихина Н.А. Роль ремоделирования левого предсердия при подтвержденной сердечной недостаточности с сохраненной фракцией выброса: фокус на своевременную диагностику. Российский кардиологический журнал. 2025;30(9):6308. https://doi.org/10.15829/1560-4071-2025-6308. EDN: SGCIBB
For citation:
Shirokov N.E., Yaroslavskaya E.I., Krinochkin D.V., Musikhina N.A. Role of left atrial remodeling in confirmed heart failure with preserved ejection fraction: focus on timely diagnosis. Russian Journal of Cardiology. 2025;30(9):6308. (In Russ.) https://doi.org/10.15829/1560-4071-2025-6308. EDN: SGCIBB
Увеличение давления наполнения (ДН) левого желудочка (ЛЖ) — ключевого критерия диагностики сердечной недостаточности с сохраненной фракцией выброса (СНсФВ) при проведении эхокардиографии (ЭхоКГ) — сопровождается последовательным изменением структурно-функционального состояния сердца [1]. В случаях выраженной диастолической дисфункции (ДД) ЛЖ рутинной ЭхоКГ может быть достаточно для оценки более значимого ремоделирования: дилатации полости левого предсердия (ЛП) и легочной гипертензии (ЛГ). Такие больные жалуются на одышку при минимальной/незначительной физической нагрузке (ФН), у большинства определяется высокий уровень натрийуретических пептидов (НУП). Трудности диагностики СНсФВ возникают при менее ремоделированном сердце ввиду незначительной ДД ЛЖ по данным традиционной ЭхоКГ покоя (изолированное нарушение расслабления ЛЖ). Концентрация НУП в этих случаях может находиться ниже пороговых значений, что характерно для страдающих ожирением больных [2]. Одышка возникает при незначительной/умеренной ФН и может считаться не объясненной ввиду отсутствия убедительной связи с поражением сердца.
У пациентов с необъясненной одышкой соответствие результатов применения претестовой части алгоритма HFA-PEFF и шкалы H2FPEF варьируется (валидные методы выявления СНсФВ), в значительной степени отмечена низкая согласованность между ними [3][4]. Тем не менее предлагается сочетанное использование этих метрик, т.к. с увеличением количества баллов и, соответственно, с выделением высокой вероятности СНсФВ ассоциированы значительные риски госпитализации/смерти ввиду декомпенсации СНсФВ [4]. Вторым — наиболее важным — ограничением инструментов претестовой диагностики является встречающаяся у большей части больных промежуточная вероятность СНсФВ (неубедительные результаты использования метрик) [3]. Такое положение требует дальнейшего функционального тестирования. Поэтому в качестве следующего шага для диагностики СНсФВ в рамках алгоритма HFA-PEFF предусмотрен диастолический стресс-тест (ДСТ) при проведении стресс-ЭхоКГ с дозированной ФН [5], шкала H2FPEF такой возможности лишена. Согласно национальным клиническим рекомендациям по хронической сердечной недостаточности (2024г), ДСТ рекомендован для оценки изменения ДН ЛЖ и подтверждения/опровержения диагноза СНсФВ [6].
Цель: исследовать структурно-функциональное состояние сердца при подтвержденной СНсФВ в зависимости от тяжести ДД ЛЖ.
Материал и методы
Проведено одномоментное исследование, соответствующее стандартам надлежащей клинической практики и положениям Хельсинкской декларации; протокол исследования одобрен локальным этическим комитетом. Информированное согласие получено от всех пациентов, включенных в исследование.
Критерии включения: фракция выброса ЛЖ ≥50%; ДД ЛЖ со снижением ранней диастолической скорости движения кольца митрального клапана, оцененной при помощи тканевой допплерографии (tissue Doppler imaging, TDI). Использован диагностический алгоритм EACVI/ASE от 2016г по оценке диастолической функции [7].
Осуществлен анализ данных 303 пациентов (45,2% мужчин, средний возраст 66,3±6,0 года) с артериальной гипертонией, ишемической болезнью сердца, ожирением, имеющих жалобы на одышку, болевой синдром/дискомфорт в грудной клетке при ФН (рис. 1). На ДСТ направлены пациенты (n=251), имеющие <2 критериев, достаточных для заключения о СНсФВ в состоянии покоя: отношение E/e′ >14, индекс объема ЛП (иоЛП) >34 мл/м², скорость трикуспидальной регургитации >2,8 м/с [8]. ДСТ в рамках стресс-ЭхоКГ с горизонтальной велоэргометрической пробой (ВЭМП) выполнен согласно действующим рекомендациям [8]. Критерием положительного ДСТ для подтверждения СНсФВ считали угнетение диастолического резерва (ДР) ЛЖ — Е/e′ >14 [6]. Индекс диастолического функционального резерва (diastolic functional reserve index, DFRI) рассчитывали при использовании тканевой допплерографии (Δe′ × e′ покой).
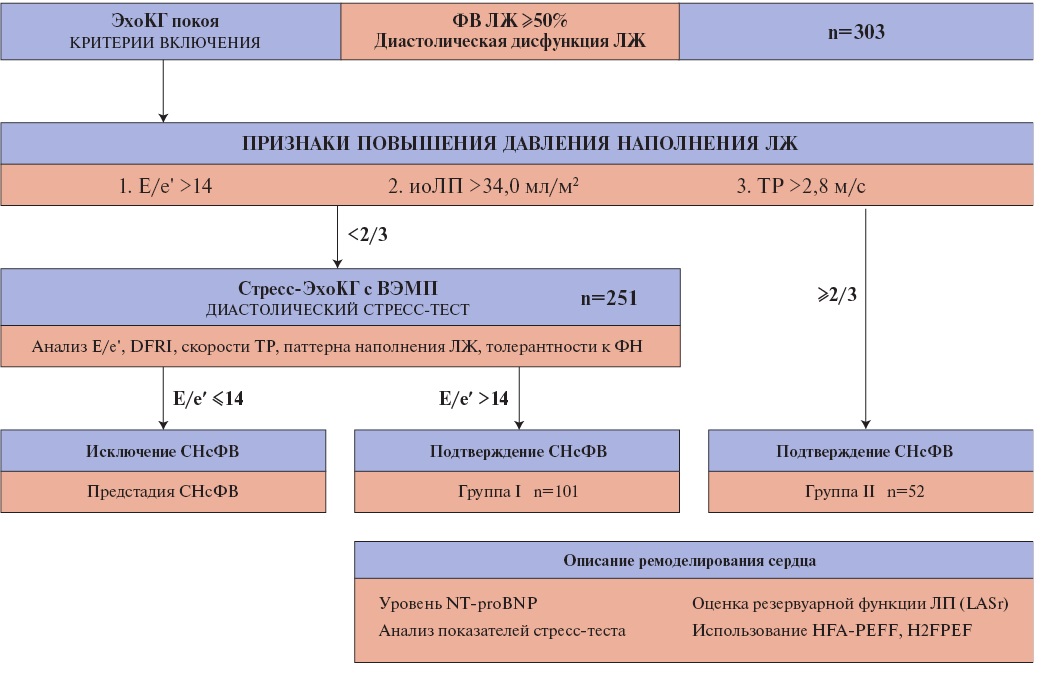
Рис. 1. Дизайн исследования.
Сокращения: ВЭМП — велоэргометрическая проба, иоЛП — индекс объема левого предсердия, ЛЖ — левый желудочек, ЛП — левое предсердие, СНсФВ — сердечная недостаточность с сохраненной фракцией выброса, ТР — трикуспидальная регургитация, ФВ — фракция выброса, ФН — физическая нагрузка, ЭхоКГ — эхокардиография, DFRI — Diastolic Functional Reserve Index (индекс диастолического функционального резерва), E/e’ — отношение ранней диастолической скорости трансмитрального потока (Е) к ранней диастолической скорости движения фиброзного кольца митрального клапана (е’), HFA-PEFF — Heart Failure Association score (диагностический алгоритм Европейского общества кардиологов), H2FPEF — диагностическая шкала Американской ассоциации кардиологов, LASr — Left Atrial reservoir Strain (деформация резервуарной фазы левого предсердия), NT-proBNP — N-концевой промозговой натрийуретический пептид.
В исследование включены 153 пациента с подтвержденной СНсФВ (35,3% мужчин, средний возраст 67,0±5,6 года). Группу I (n=101) составили пациенты со снижением ДР ЛЖ при выполнении ДСТ (положительная проба); группу II (n=52) — больные с высоким ДН ЛЖ в состоянии покоя, не требующие ДСТ для заключения о СНсФВ (рис. 1). Клиническая, функциональная и лабораторная характеристики представлены в таблицах 1-4.
Таблица 1
Клинико-функциональная характеристика больных (n=153)
|
Показатель |
Группа I (n=101) |
Группа II (n=52) |
р |
|
Пол, муж., % |
37,6 |
30,8 |
0,476 |
|
Возраст, лет |
66,7±5,4 |
67,3±5,9 |
0,502 |
|
АГ, % |
100,0 |
100,0 |
0,998 |
|
АГ, стадия, % 1 2 3 |
1,0 8,9 90,1 |
0,0 11,5 88,5 |
0,682 |
|
АГ, риск, % 3 4 |
7,9 92,1 |
3,8 96,2 |
0,496 |
|
ИБС, % |
83,2 |
82,7 |
0,941 |
|
Стенокардия напряжения, ФК по NYHA, % 0 1 2 3 |
6,7 15,8 54,5 3,0 |
32,7 1,9 59,6 5,8 |
0,064 |
|
ИМ в анамнезе, % |
13,9 |
19,2 |
0,482 |
|
Пароксизмальная ФП, % |
15,0 |
23,1 |
0,263 |
|
СД 2 типа, % |
34,7 |
51,9 |
0,055 |
|
ИМТ, кг/м² |
32,0±4,9 |
32,5±5,0 |
0,501 |
|
Ожирение, % |
62,4 |
59,6 |
0,861 |
|
ХБП, % |
10,9 |
26,9 |
0,019 |
|
Креатинин, мкмоль/л |
74,7±15,4 |
84,4±20,8 |
0,001 |
|
СКФ, мл/мин |
82,5 [ 71,0;94,5] |
72,4 [ 61,4;85,8] |
0,001 |
|
ФК ХСН по NYHA, % I II III |
15,8 81,2 3,0 |
17,3 69,2 13,5 |
0,067 |
|
Т6Х, м |
400,0 [ 360,0;440,0] |
365,5 [ 310,5;401,5] |
0,004 |
|
HFA-PEFF, балл |
5,0 [ 4,0;6,0] |
6,0 [ 5,0;6,0] |
0,001 |
|
HFA-PEFF, ≥5 баллов |
59,4 |
78,8 |
0,019 |
|
H2FPEF, балл |
4,5±1,4 |
4,9±1,7 |
0,175 |
|
H2FPEF, ≥5 баллов |
59,4 |
67,3 |
0,382 |
|
NT-proBNP, пг/мл |
257,7 [ 100,0;443,3] |
412,0 [ 191,4;780,2] |
0,002 |
|
NT-proBNP >125 пг/мл, % |
74,0 |
87,8 |
0,085 |
|
NT-proBNP >220 пг/мл, % |
58,3 |
67,3 |
0,368 |
Сокращения: АГ — артериальная гипертония, ИБС — ишемическая болезнь сердца, ИМ — инфаркт миокарда, ИМТ — индекс массы тела, СД — сахарный диабет, СКФ — скорость клубочковой фильтрации, СНсФВ — сердечная недостаточность с сохраненной фракцией выброса, Т6Х — тест 6-минутной ходьбы, ФК — функциональный класс, ФП — фибрилляция предсердий, ХБП — хроническая болезнь почек, ХСН — хроническая сердечная недостаточность, HFA-PEFF — Heart Failure Association score (диагностический алгоритм Европейского общества кардиологов), H2FPEF — диагностическая шкала Американской ассоциации кардиологов, NT-proBNP — N-концевой промозговой натрийуретический пептид, NYHA — New York heart association (Нью-Йоркская ассоциация сердца).
Таблица 2
Проводимая медикаментозная терапия (n=153)
|
Препарат, % |
Группа I (n=101) |
Группа II (n=52) |
р |
|
БАБ |
74,3 |
67,3 |
0,448 |
|
иАПФ |
31,7 |
25,0 |
0,456 |
|
БРА |
57,4 |
59,6 |
0,863 |
|
АМКР |
9,9 |
21,2 |
0,081 |
|
Диуретики |
42,6 |
55,8 |
0,128 |
|
БКК |
34,7 |
44,2 |
0,292 |
|
Моксонидин |
5,9 |
9,6 |
0,511 |
|
Дезагреганты |
56,4 |
57,7 |
0,997 |
|
Антикоагулянты |
17,8 |
19,2 |
0,828 |
|
Статины |
82,2 |
69,2 |
0,100 |
|
ААС |
9,9 |
13,5 |
0,589 |
|
Ингибиторы SGLT2 |
12,9 |
17,3 |
0,473 |
Сокращения: ААС — антиаритмические средства, АМКР — антагонисты минералокортикоидных рецепторов, БАБ — β-адреноблокаторы, БКК — блокаторы кальциевых каналов, БРА — блокаторы рецепторов ангиотензина II, иАПФ — ингибиторы ангиотензинпревращающего фермента, SGLT2 — sodium-glucose cotransporter-2 (натрий-глюкозный котранспортер-2).
Таблица 3
Структурно-функциональное состояние сердца (n=153)
|
Показатель |
Группа I (n=101) |
Группа II (n=52) |
р |
|
Структурное состояние |
|||
|
Аорта, мм |
34,3±3,7 |
34,0±3,4 |
0,627 |
|
МЖП, мм |
12,7±1,7 |
13,8±2,7 |
0,010 |
|
ЗС ЛЖ, мм |
11,1±1,2 |
11,7±1,4 |
0,005 |
|
ММ ЛЖ, г |
214,0 [ 188,5;247,0] |
234,5 [ 194,0;277,5] |
0,006 |
|
Индекс ММ ЛЖ, г/м² |
112,9 [ 103,6;127,5] |
128,3 [ 108,0;144,2] |
0,007 |
|
КДО ЛЖ, мл |
80,0 [ 70,0;90,1] |
76,0 [ 67,5;86,8] |
0,350 |
|
КДО ЛЖ индекс, мл/м² |
43,0±8,2 |
40,6±9,7 |
0,109 |
|
Передне-задний размер ЛП, мм |
41,0±4,0 |
43,3±4,1 |
0,001 |
|
Объем ЛП, мл |
65,0 [ 53,5;73,0] |
74,5 [ 65,3;89,8] |
<0,001 |
|
иоЛП, мл/м² |
33,5 [ 29,2;40,1] |
40,8 [ 37,3;47,6] |
<0,001 |
|
Встречаемость дилатации ЛП (иоЛП >34 мл/м²), % |
46,5 |
84,6 |
<0,001 |
|
Объем ПП, мл |
42,4±9,1 |
48,2±13,5 |
0,002 |
|
иоПП, мл/м² |
22,2 [ 19,3;25,9] |
25,2 [ 21,4;28,7] |
0,004 |
|
Размер ПЖ, мм |
27,5±2,6 |
28,0±2,4 |
0,283 |
|
Функциональное состояние |
|||
|
ФВ ЛЖ, % |
66,0±3,5 |
65,7±3,6 |
0,673 |
|
GLS, % |
18,4±2,8 |
18,0±3,3 |
0,417 |
|
Встречаемость GLS <18%, % |
36,0 |
45,0 |
0,423 |
|
Пик Е, см/с |
71,0 [ 61,5;81,5] |
94,0 [ 81,3;105,8] |
<0,001 |
|
Пик А, см/с |
87,0 [ 77,2;99,0] |
92,5 [ 60,0;113,5] |
0,924 |
|
Е/А |
0,8 [ 0,7;1,0] |
1,1 [ 0,8;1,5] |
<0,001 |
|
TDI e’ sept, см/с |
5,5±1,1 |
5,0±1,3 |
0,008 |
|
TDI e’ lat, см/с |
7,2±1,4 |
6,2±1,5 |
<0,001 |
|
E/e’ average |
11,3 [ 10,1;12,6] |
16,3 [ 14,9;19,2] |
<0,001 |
|
LASr, % |
21,3 [ 19,5;24,7] |
15,0 [ 12,5;17,3] |
<0,001 |
|
Встречаемость LASr <24%, % |
70,3 |
100,0 |
<0,001 |
|
LAScd, % |
9,3 [ 7,6;11,5] |
7,2 [ 5,6;9,3] |
<0,001 |
|
LASct, % |
11,8 [ 9,1;14,7] |
7,3 [ 4,9;10,5] |
<0,001 |
|
Комплаентность ЛП (LASr / E/e’) |
1,9 [ 1,6;2,3] |
0,9 [ 0,7;1,1] |
<0,001 |
|
Встречаемость комплаентности ЛП <2,4, % |
75,2 |
100,0 |
<0,001 |
|
СДЛА, мм рт.ст. |
24,5±6,5 |
26,0±7,2 |
0,201 |
Сокращения: ЗС — задняя стенка, иоЛП — объем левого предсердия, индексированный по площади поверхности тела, ЛЖ — левый желудочек, ЛП — левое предсердие, КДО — конечно-диастолический объем, ММ — масса миокарда, МЖП — межжелудочковая перегородка, ПЖ — правый желудочек, ПП — правое предсердие, СДЛА — систолическое давление в легочной артерии, ФВ — фракция выброса, E/e’ average — усредненное отношение ранней диастолической скорости трансмитрального потока (Е) к ранней диастолической скорости движения фиброзного кольца митрального клапана (е’), GLS — Global Longitudinal Strain (глобальная продольная деформация), LAScd — Left Atrial coduit Strain (деформация кондуитной фазы левого предсердия), LASct — Left Atrial contraction Strain (деформация контрактильной фазы левого предсердия), LASr — Left Atrial reservoir Strain (деформация резервуарной фазы левого предсердия), TDI e’ lat — left ventricular annular velocity assessed by Tissue Doppler Imaging, peak e’ lateral (ранняя диастолическая скорость движения латеральной части кольца митрального клапана), TDI e’ sept — left ventricular annular velocity assessed by Tissue Doppler Imaging, peak e’ septal (ранняя диастолическая скорость движения септальной части кольца митрального клапана).
Таблица 4
Стресс-ЭхоКГ с ВЭМП в группе I (n=101)
|
Показатель, % |
Покой |
ФН |
р |
|
Пик Е, см/с |
71,0 [ 61,5;81,5] |
123,0 [ 112,0;133,0] |
<0,001 |
|
Пик А, см/с |
87,0 [ 77,2;99,0] |
107,0 [ 93,0;127,0] |
<0,001 |
|
Е/А |
0,8 [ 0,7;1,0] |
1,1 [ 0,9;1,3] |
<0,001 |
|
TDI e’ sept, см/с |
5,0 [ 5,0;6,0] |
7,0 [ 7,0;8,0] |
<0,001 |
|
TDI e’ lat, см/с |
7,0 [ 6,0;8,0] |
9,0 [ 8,0;10,0] |
<0,001 |
|
Е/е’ average |
11,3 [ 10,1;12,6] |
14,7 [ 14,0;15,5] |
<0,001 |
|
Е/е’ sept |
13,0 [ 11,4;14,6] |
16,7 [ 15,2;18,0] |
<0,001 |
|
Градиент ТР, мм рт.ст. |
20,0 [ 15,5;25,0] |
35,0 [ 23,0;46,0] |
<0,001 |
|
DFRI (N ≥13,5) |
9,0 [ 6,0;12,8] |
– |
|
|
Е/А паттерн (Е>А), % |
50,5 |
– |
|
|
Толерантность к ФН, Ватт |
75,0 [ 50,0;75,0] |
– |
|
|
Продолжительность стресс-теста, мин |
5,3±1,4 |
– |
|
|
Максимальная ЧСС, уд./мин |
100,0 [ 94,5;107,0] |
– |
|
|
Стресс-индуцированная ишемия, % |
8,0 |
– |
|
Сокращения: стресс-ЭхоКГ с ВЭМП — стресс-эхокардиография с горизонтальной велоэргометрической пробой, ТР — трикуспидальная регургитация, ФН — физическая нагрузка, ЧСС — частота сердечных сокращений, DFRI — Diastolic Functional Reserve Index (индекс диастолического функционального резерва).
Критерии невключения: гемодинамически значимые врожденные/приобретенные пороки сердца; аневризма/дискинезия миокарда ЛЖ; имплантированные внутрисердечные устройства; тромбы в полостях сердца; тромбофлебит, флеботромбоз нижних конечностей; облитерирующий атеросклероз артерий нижних конечностей; заболевания опорно-двигательного аппарата, сопровождающиеся болевым синдромом при движении нижних конечностей. Критерии исключения: недостижение частоты сердечных сокращений, достаточной для завершения ДСТ; возникновение тахиаритмии, затрудняющей диагностику СНсФВ.
Использованы ультразвуковой аппарат экспертного класса General Electric (GE) Vivid E9 с матричным датчиком M5S-D (1,5-4,6 МГц), велоэргометр GE eBike. Данные сохранялись в формате DICOM. Интерпретация изображений, кинопетель осуществлялась на рабочей станции IntelliSpace Cardiovascular, платформе TomTec (Philips, США) в соответствии с действующими методическими рекомендациями [9]. Метод отслеживания движения пятен (speckle tracking echo, STE) применен для фазового анализа деформации ЛП и глобальной продольной деформации ЛЖ (global longitudinal strain, GLS).
Статистический анализ полученных данных проведен при помощи пакета программ IBM SPSS Statistics 23.0. Для определения нормальности распределения использовали критерий Колмогорова-Смирнова. Анализ количественных величин несвязанных групп при их нормальном распределении выполняли с помощью критерия t-Стьюдента; результаты представлены в виде M±SD (М — среднее арифметическое, SD — стандартное отклонение). Для анализа количественных величин при распределении, отличном от нормального, использовали критерий Манна-Уитни; результаты представлены в виде медианы (Me) и интерквартильного размаха [ Q25; Q75]. Для анализа количественных величин связанных групп при распределении, отличном от нормального, использовали критерий Уилкоксона. Качественные величины сравнивали при помощи критерия хи-квадрат Пирсона. Для определения выраженности связей проводили корреляционный анализ Спирмена. Статистически значимыми считали различия переменных при p<0,05.
Результаты
При анализе основных клинико-функциональных параметров между группами были выявлены статистически значимые различия по тесту 6-минутной ходьбы, количеству баллов претестовой части алгоритма HFA-PEFF и концентрации N-концевого фрагмента промозгового НУП (NT-proBNP) (табл. 1). Следует отметить отсутствие достоверных различий по основным сердечно-сосудистым заболеваниям, за исключением хронической болезни почек — в группе II заболевание встречалось чаще (табл. 1). При анализе исходной проводимой медикаментозной терапии статистически значимых различий между группами обнаружено не было (табл. 2).
При анализе показателей ЭхоКГ покоя между группами найдены достоверные различия по параметрам, описывающим ремоделирование левых отделов сердца (табл. 3). Определены различия показателей, характеризующих структуру сердца: в группе II в сравнении с группой I увеличены толщина межжелудочковой перегородки (МЖП) и задней стенки ЛЖ, масса миокарда ЛЖ, увеличены полости обоих предсердий. Нужно отметить статистически значимое увеличение всех показателей, описывающих дилатацию полости ЛП в группе II: передне-задний размер ЛП, объем ЛП и иоЛП. Более того, между группами установлены различия по большинству характеристик степени тяжести ДД ЛЖ: ранняя диастолическая скорость трансмитрального потока (пик Е), ее отношение к поздней диастолической скорости (отношение Е/А), ранние диастолические (в области МЖП и боковой стенки ЛЖ) скорости движения кольца митрального клапана, ДН ЛЖ (отношение E/e′), деформация резервуарной фазы ЛП (Left Atrial reservoir Strain, LASr) и комплаентность ЛП (табл. 3). Следует указать на отсутствие достоверных различий по систолическому давлению в легочной артерии. По данным корреляционного анализа, у больных СНсФВ (общая группа) были выявлены связи умеренной силы: LASr и отношение E/e′ (r=-0,538; р<0,001), LASr и иоЛП (r=-0,443; р<0,001), отмечено отсутствие связи между LASr и NT-proBNP (r=-0,157; р=0,060) (рис. 2).
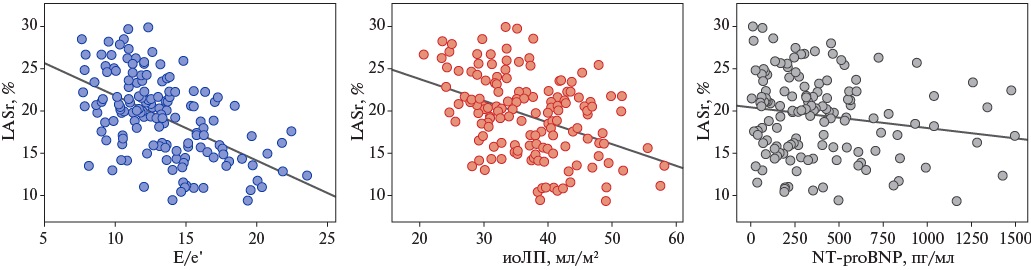
Рис. 2. Корреляции исследуемых показателей, описывающих увеличение давления в полости ЛП.
Сокращения: иоЛП — объем левого предсердия, индексированный по площади поверхности тела, LASr — Left Atrial reservoir Strain (деформация резервуарной фазы левого предсердия), NT-proBNP — N-концевой промозговой натрийуретический пептид.
При анализе показателей, полученных при проведении ДСТ, были выявлены статистически значимые различия по компонентам угнетения ДР ЛЖ в группе I (табл. 4). С увеличением ранней (пик Е) и поздней (пик А) диастолических скоростей трансмитрального потока было зафиксировано угнетение ДР ЛЖ (рост отношения E/e′) даже при повышении ранних диастолических (в области МЖП и боковой стенки ЛЖ) скоростей движения кольца митрального клапана (табл. 4). По данным корреляционного анализа у пациентов группы I обнаружены связи слабой и умеренной силы: DFRI и комплаентность ЛП при ЭхоКГ покоя (r=0,292; р=0,003), DFRI и E/e′ при ДСТ (r=-0,415; р<0,001), DFRI и отношение Е/А при ДСТ (r=0,332; р=0,001), DFRI и толерантность к ФН (r=0,224; р=0,024), DFRI и NT-proBNP (r=-0,204; р=0,047).
Обсуждение
Рекомендации по применению стресс-ЭхоКГ с ВЭМП от EACVI/ASE 2017г содержат исчерпывающее описание особенностей диагностики СНсФВ при проведении ДСТ [8]. Однако отмечено, что реальный клинико-диагностический процесс сопровождается неопределенностью/отсутствием консенсуса относительно универсальных критериев положительной пробы ДСТ [10]. Важно добавить, что именно угнетение ДР ЛЖ — достижение Е/е′ >14 при выполнении ФН — повышает чувствительность определения СНсФВ c 34% до 90%, несколько снижая специфичность — от 83% до 71% в сравнении с традиционной ЭхоКГ покоя (верификация СНсФВ по данным катетеризации правых отделов сердца) [11]. В действующих национальных клинических рекомендациях по хронической сердечной недостаточности (2024) этот критерий предложен впервые, используется как основной и наиболее важный, увеличение Е/е′ >14 считается достаточным для диагностики СНсФВ [6]. Также рекомендовано учитывать увеличение скорости трикуспидальной регургитации как признак проявления ЛГ [6][8]. Согласно нашим данным, в рамках проведения комплексного анализа, вероятно, стоит выделить дополнительные признаки угнетения ДР ЛЖ: DFRI и паттерн наполнения ЛЖ (E>A), которые соответственно позволяют учитывать возможность к растяжению ткани миокарда ЛЖ и распределение наполнения ЛЖ (рис. 3, табл. 4). Указанные особенности при их дальнейшем исследовании, вероятно, можно учитывать для дифференциации вариантов диастолического ответа на дозированную ФН (рис. 3).
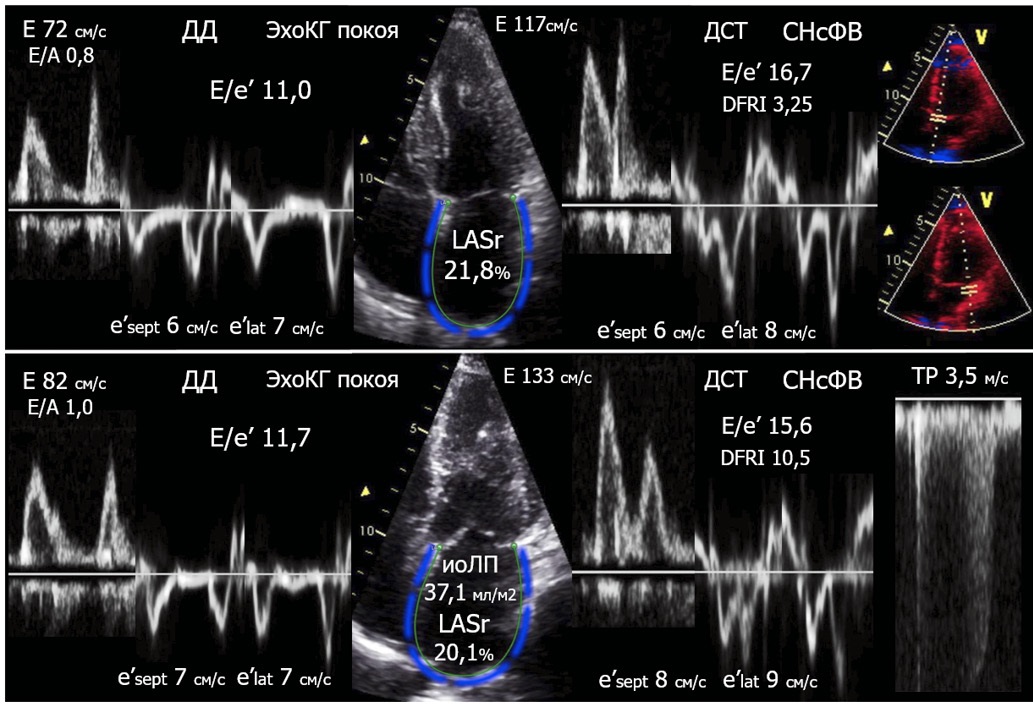
Рис. 3. Варианты положительного ДСТ.
Примечание: верхняя панель: достижение E/e’ >14; DFRI значимо <13,5; Е/А=1,0; признаки ЛГ при ФН отсутствуют. Нижняя панель: достижение E/e’ >14; DFRI <13,5; Е/А=1,4; наличие ЛГ при ФН. Цветное изображение доступно в электронной версии журнала.
Сокращения: ДД — диастолическая дисфункция, ДСТ — диастолический стресс-тест, иоЛП — объем левого предсердия, индексированный по площади поверхности тела, СНсФВ — сердечная недостаточность с сохраненной фракцией выброса, ЭхоКГ — эхокардиография, LASr — Left Atrial reservoir Strain (деформация резервуарной фазы левого предсердия).
Применение современного фазового анализа деформации ЛП с использованием STE позволяет количественно оценить резервуарную, кондуитную и контрактильную функции ЛП. LASr при проведении ЭхоКГ покоя рекомендована BSEcho с 2024г для диагностики СНсФВ, т.к. ее значимое угнетение опережает расширение полости ЛП (рис. 3) [12]. Чувствительность LASr в определении СНсФВ составляет 77%, специфичность — 93% [13]. Важно добавить, что LASr отражает среднее давление в полости ЛП: опосредованно с этим показателем связаны давление заклинивания легочной артерии при катетеризации правых отделов сердца и отношение Е/е′ при ЭхоКГ [13]. Результаты метаанализа Dal Canto E, et al. (2022) демонстрируют значение мультифакторного/комплексного подхода диагностики СНсФВ, поддерживая потенциальную роль LASr при ЭхоКГ покоя в сочетании с проведением ДСТ [13]. Также предлагается использовать комплаентность ЛП (LASr / E/e′) в качестве наиболее точного показателя соответствия компонентов диастолической функции левых отделов сердца [14].
ДСТ позволяет выявить больных СНсФВ с незначительным ремоделированием сердца (ранняя/своевременная диагностика). По нашим данным, такие пациенты менее чем в 50% случаев имеют дилатацию полости ЛП, у них отсутствуют признаки ЛГ в покое. При этом умеренное угнетение резервуарной функции ЛП (LASr <24% [12]) выявлено у 70% пациентов. Напротив, больные СНсФВ с более значимой ДД, выявленной без проведения стресс-теста, в большинстве имеют расширение ЛП и выраженное снижение LASr <18% [12], сочетающиеся с увеличением массы миокарда ЛЖ (рис. 4). В этом контексте важно указать на NT-proBNP, уровень которого значимо растет при продолжающемся структурно-функциональном ремоделировании сердца [2].
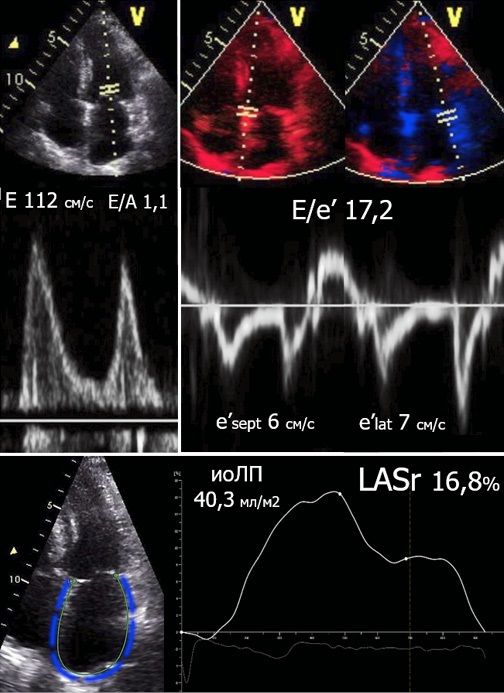
Рис. 4. Анализ диастолической функции ЛЖ с определением выраженного увеличения среднего давления полости ЛП в состоянии покоя: E/e′ >14, LASr <18%, иоЛП >34,0 мл/м².
Примечание: цветное изображение доступно в электронной версии журнала.
Сокращения: иоЛП — объем левого предсердия, индексированный по площади поверхности тела, LASr — Left Atrial reservoir Strain (деформация резервуарной фазы левого предсердия).
Ограничения исследования. Необходимы более масштабные, спланированные исследования для оценки дополнительной диагностической/прогностической ценности представленных современных инструментов ЭхоКГ.
Заключение
Для пациентов с подтвержденной СНсФВ при увеличении ДН ЛЖ характерно угнетение резервуарной функции ЛП и расширение полости ЛП. Фазовый анализ деформации ЛП и проведение ДСТ позволяет своевременно диагностировать СНсФВ.
Отношения и деятельность: все авторы заявляют об отсутствии потенциального конфликта интересов, требующего раскрытия в данной статье.
Список литературы
1. Овчинников А.Г., Потехина А.В., Филатова А.Ю. и др. Роль левого предсердия в патогенезе сердечной недостаточности с сохраненной фракцией выброса. Кардиология. 2024;64(11):132-47. doi:10.18087/cardio.2024.11.n2799.
2. Reddy YNV, Tada A, Obokata M, et al. Evidence-¬Based Application of Natriuretic Peptides in the Evaluation of Chronic Heart Failure With Preserved Ejection Fraction in the Ambulatory Outpatient Setting. Circulation. 2025;151(14):976-989. doi:10.1161/CIRCULATIONAHA.124.072156.
3. Nikorowitsch J, Bei der Kellen R, Kirchhof P, et al. Applying the ESC 2016, H2FPEF, and HFAPEFF diagnostic algorithms for heart failure with preserved ejection fraction to the general population. ESC Heart Fail. 2021;8(5):3603-12. doi:10.1002/ehf2.13532.
4. Selvaraj S, Myhre PL, Vaduganathan M, et al. Application of Diagnostic Algorithms for Heart Failure With Preserved Ejection Fraction to the Community. JACC Heart Fail. 2020;8(8):64053. doi:10.1016/j.jchf.2020.03.013.
5. Li S, Zhu X, Zhang Y, et al. Validation of heart failure algorithm for diagnosing heart failure with preserved ejection fraction: a meta-analysis. ESC Heart Fail. 2023;10(4):2225-35. doi:10.1002/ehf2.14421.
6. Галявич А.С., Терещенко С.Н., Ускач Т.М. и др. Хроническая сердечная недостаточность. Клинические рекомендации 2024. Российский кардиологический журнал. 2024;29(11): 6162. doi:10.15829/1560-4071-2024-6162.
7. Nagueh SF, Smiseth OA, Appleton CP, et al. Recommendations for the Evaluation of Left Ventricular Diastolic Function by Echocardiography: An Update from the American Society of Echocardiography and the European Association of Cardiovascular Imaging. European Heart Journal — Cardiovascular Imaging. 2016;17(12):1321-60. doi:10.1093/ehjci/jew082.
8. Lancellotti P, Pellikka PA, Budts W, et al. The Clinical Use of Stress Echocardiography in Non-Ischaemic Heart Disease: Recommendations from the European Association of Cardiovascular Imaging and the American Society of Echocardiography. Journal of the American Society of Echocardiography. 2017;30(2):101-38. doi:10.1016/j.echo.2016.10.016.
9. Мацкеплишвили С.Т., Саидова М.А., Мироненко М.Ю. и др. Выполнение стандартной трансторакальной эхокардиографии. Методические рекомендации 2024. Российский кардиологический журнал. 2025;30(2):6271. doi:10.15829/1560-4071-2025-6271.
10. Tani Y, Reddy YNV, Verbrugge FH, et al. Variability in approach to exercise stress echocardiography for diagnosis of heart failure with preserved ejection fraction: an international survey on real-world practice. Eur Heart J Imaging Methods Pract. 2024;2(1):qyae059. doi:10.1093/ehjimp/qyae059.
11. Obokata M, Kane GC, Reddy YN, et al. Role of Diastolic Stress Testing in the Evaluation for Heart Failure With Preserved Ejection Fraction: A Simultaneous Invasive-¬Echocardiographic Study. Circulation. 2017;135(9):825-38. doi:10.1161/CIRCULATIONAHA.116.024822.
12. Robinson S, Ring L, Oxborough D, et al. The assessment of left ventricular diastolic function: Guidance and recommendations from the British Society of Echocardiography. Echo Res Pract. 2024;11(1):16. doi:10.1186/s44156-024-00051-2.
13. Dal Canto E, Remmelzwaal S, van Ballegooijen AJ, et al. Diagnostic value of echocardiographic markers for diastolic dysfunction and heart failure with preserved ejection fraction. Heart Fail Rev. 2022;27(1):207-18. doi:10.1007/s10741-020-09985-1.
14. Shirokov NE, Yaroslavskaya EI, Krinochkin DV, et al. Diagnostic value of left atrial compliance in determining heart failure with preserved ejection fraction. Russian Open Medical Journal. 2024;13:e0409. doi:10.15275/rusomj.2024.0409.
Об авторах
Н. Е. ШироковРоссия
Широков Никита Евгеньевич — к.м.н., врач ультразвуковой диагностики, н.с. лаборатории инструментальной диагностики научного отдела инструментальных методов исследования
Томск
Е. И. Ярославская
Россия
Ярославская Елена Ильинична — д.м.н., в.н.с., зав. лабораторией инструментальной диагностики научного отдела инструментальных методов исследования
Томск
Д. В. Криночкин
Россия
Криночкин Дмитрий Владиславович — к.м.н., зав. отделением ультразвуковой диагностики, с.н.с. лаборатории инструментальной диагностики научного отдела инструментальных методов исследования
Томск
Н. А. Мусихина
Россия
Мусихина Наталья Алексеевна — к.м.н., в.н.с., зав. отделением неотложной кардиологии научного отдела клинической кардиологии
Томск
Дополнительные файлы
- Диагностика сердечной недостаточности с сохраненной фракцией выброса представляет собой сложную задачу.
- Анализ резервуарной функции левого предсердия при эхокардиографии покоя в сочетании с дополнительными признаками угнетения диастолического резерва при диастолическом стресс-тесте составляют многофакторный/комплексный подход к диагностике сердечной недостаточности с сохраненной фракцией выброса.
Рецензия
Для цитирования:
Широков Н.Е., Ярославская Е.И., Криночкин Д.В., Мусихина Н.А. Роль ремоделирования левого предсердия при подтвержденной сердечной недостаточности с сохраненной фракцией выброса: фокус на своевременную диагностику. Российский кардиологический журнал. 2025;30(9):6308. https://doi.org/10.15829/1560-4071-2025-6308. EDN: SGCIBB
For citation:
Shirokov N.E., Yaroslavskaya E.I., Krinochkin D.V., Musikhina N.A. Role of left atrial remodeling in confirmed heart failure with preserved ejection fraction: focus on timely diagnosis. Russian Journal of Cardiology. 2025;30(9):6308. (In Russ.) https://doi.org/10.15829/1560-4071-2025-6308. EDN: SGCIBB

















































