Перейти к:
Альбуминурия в оценке риска сердечно-сосудистых осложнений и кровотечений у пациентов с ишемической болезнью сердца и периферическим атеросклерозом
https://doi.org/10.15829/1560-4071-2025-6141
EDN: WFLDIS
Аннотация
Цель. Оценить значимость альбуминурии в отношении предсказания прогноз-определяющих событий (ПОС) — сердечно-сосудистых (ССО) и геморрагических осложнений (ГО) — у пациентов с мультифокальным атеросклерозом, в т.ч. в сопоставлении с общепринятым лабораторным маркером эндотелиальной дисфункции — фактором Виллебранда (ФВ).
Материал и методы. В исследование включались участники одноцентрового проспективного регистра РЕГАТА-1 с ишемической болезнью сердца и периферическим атеросклерозом. Определялось соотношение альбумин-креатинин в разовой утренней порции мочи, активность ФВ в плазме. Первичная конечная точка — сумма ПОС: инфаркт миокарда, нестабильная стенокардия, инсульт, транзиторная ишемическая атака, периферические артериальные тромбозы, ампутация, большое/клинически значимое кровотечение BARC 2-5.
Результаты. Включено 148 пациентов (медиана возраста 66 [65; 67] лет, 79,1% мужчины). Повышение уровня альбумина в моче (как минимум, легкое, >10 мг/г) выявлено у 71,3% пациентов.
Медиана длительности наблюдения 17 [15; 20] мес.; зарегистрировано 7 ССО и 18 кровотечений BARC 2-3. Согласно ROC-анализу, отрезной точкой для альбуминурии, значения выше которой ассоциируются с увеличением частоты ПОС, является уровень 10,6 мг/г. ПОС зарегистрированы у 4,5% пациентов с альбуминурией <10,6 мг/г и у 21,9% пациентов с более высокими значениями, plog-rank=0,007, по данным многофакторного анализа отношение шансов (ОШ) составило 5,5 (95% доверительный интервал (ДИ): 1,23-24,72), р=0,026. При анализе вторичных конечных точек отмечалась тенденция к увеличению риска ССО (p=0,065) и ГО (р=0,05). В данной когорте не продемонстрирована связь скорости клубочковой фильтрации и риска ПОС.
Отрезной точкой для ФВ оказался уровень 157%. Частота ПОС была достоверно выше у лиц с повышенным ФВ (23,0% vs 10,8%, p=0,048); в многофакторном анализе ФВ утратил свою значимость (ОШ 2,18; 95% ДИ: 0,84-5,65; р=0,11). У 31,2% пациентов отмечалось одновременное повышение альбуминурии и ФВ, в этой подгруппе каждый третий перенес ПОС; в многофакторном анализе ОШ составило 3,53 (95% ДИ: 1,31-9,49), р=0,012. Наличие комбинированного маркера ассоциируется с повышением риска ГО (р=0,006) и ССО (р=0,027).
Заключение. У пациентов с мультифокальным атеросклерозом альбуминурия >10,6 мг/г является независимым (в т.ч. от расчетной скорости клубочковой фильтрации) предиктором ССО и ГО. Наиболее неблагоприятный прогноз у пациентов с сочетанием альбуминурии >10,6 мг/г и ФВ >157%.
Ключевые слова
Для цитирования:
Шахматова О.О., Комаров А.Л., Хакимова М.Б., Кривошеева Е.Н., Титаева Е.В., Добровольский А.Б., Амелюшкина В.А., Гомыранова Н.В., Панченко Е.П. Альбуминурия в оценке риска сердечно-сосудистых осложнений и кровотечений у пациентов с ишемической болезнью сердца и периферическим атеросклерозом. Российский кардиологический журнал. 2025;30(6):6141. https://doi.org/10.15829/1560-4071-2025-6141. EDN: WFLDIS
For citation:
Shakhmatova O.O., Komarov A.L., Khakimova M.B., Krivosheeva E.N., Titaeva E.V., Dobrovolsky A.B., Ameljushkina V.A., Gomyranova N.V., Panchenko E.P. Albuminuria in assessing the risk of cardiovascular events and bleeding in patients with coronary and peripheral artery disease. Russian Journal of Cardiology. 2025;30(6):6141. (In Russ.) https://doi.org/10.15829/1560-4071-2025-6141. EDN: WFLDIS
Хроническая болезнь почек (ХБП) — общепризнанный фактор риска сердечно-сосудистых заболеваний и их осложнений. Стойкая умеренная (30-300 мг/сут.) и тяжелая (>300 мг/сут.) альбуминурия отражает повреждение почек и является одним из диагностических критериев ХБП, а также доказанным фактором риска прогрессирования почечной патологии, сердечно-сосудистых заболеваний и смерти [1].
В последнее время накопились данные, что прогностически значимой может оказаться альбуминурия в пределах диапазона <30 мг/сут. В исследовании Inoue K, et al. [2] прирост альбуминурии в этих пределах ассоциировался с увеличением общей и сердечно-сосудистой смертности. Исследование Mahemuti N, et al. [3] продемонстрировало связь между приростом альбуминурии в пределах "нормального" диапазона и общей смертностью, причем в большей степени взаимосвязь была выражена у пациентов с факторами риска сердечно-сосудистых осложнений (ССО). Это позволило нам предположить, что альбуминурия — удачный кандидат в качестве потенциального маркера резидуального риска у наиболее тяжелых кардиологических пациентов, например, страдающих мультифокальным атеросклерозом (МФА). Ценность этого маркера определяется еще и тем, что он может отражать потенциально обратимые процессы повреждения почек. Оптимизация лечения сопутствующей патологии, назначение нефропротективной терапии потенциально способны снизить риск не только почечных, но и ССО. Так, post hoc анализ исследований FIDELIO-DKD и FIGARO-DKD показал, что уменьшение риска ССО на фоне приема финеренона у пациентов с сахарным диабетом (СД) и ХБП на 37% обусловлен снижением альбуминурии [4].
Для пациентов с заболеваниями, обусловленными атеросклерозом, помимо ишемических большое значение имеют геморрагические осложнения (ГО). ХБП является общепринятым фактором риска кровотечений, однако в кардиологической практике с этой точки зрения принято рассматривать только скорость клубочковой фильтрации. Возможное влияние альбуминурии на риск ГО практически не изучено.
Наконец, отсутствует четкое понимание механизмов связи между альбуминурией и ССО. Предполагается, что альбуминурия может быть маркером системной эндотелиальной дисфункции, в т.ч. влияющей на активность прокоагулянтных факторов [5]. Данные о "взаимоотношениях" альбуминурии с другими маркерами эндотелиальной дисфункции ограничены и противоречивы [5-7].
Таким образом, целью исследования стала оценка значимости альбуминурии в отношении предсказания прогноз-определяющих событий (ПОС) (ССО и ГО) у пациентов с ишемической болезнью сердца (ИБС) и сопутствующим периферическим атеросклерозом, в т.ч. в сопоставлении с общепринятым лабораторным маркером эндотелиальной дисфункции — фактором Виллебранда (ФВ).
Материал и методы
В исследование включались участники одноцентрового проспективного РЕГистра длительной Антитромботической ТерАпии РЕГАТА-1 (ClinicalTrials NCT04347200) в 2020-2022 гг. Исследование выполнено в соответствии со стандартами надлежащей клинической практики и принципами Хельсинкской декларации. Протокол исследования одобрен локальным этическим комитетом. Письменное информированное согласие получено у всех участников до включения в исследование.
Критериями включения было наличие ангиографически подтвержденной ИБС в сочетании с клинически значимым периферическим атеросклерозом (стеноз ≥50%), по крайней мере, в одном сосудистом бассейне. Основными критериями невключения были наличие показаний к длительной терапии пероральными антикоагулянтами в "полной дозе" (фибрилляция предсердий, венозная тромбоэмболия, тромбоз левого желудочка и др.), <12 мес. после острого коронарного синдрома и/или чрескожного коронарного вмешательства, высокий риск кровотечений.
Вследствие высокого риска ишемических осложнений пациенты принимали комбинированную антитромботическую терапию — ацетилсалициловую кислоту 75-100 мг/сут. в комбинации с ривароксабаном 2,5 мг 2 раза/сут. или с клопидогрелом 75 мг/сут. Продленная комбинированная терапия с клопидогрелом использовалась только у пациентов после чрескожного коронарного вмешательства >12 мес. назад.
Альбуминурия оценивалась по альбумин-креатининовому соотношению в разовой утренней порции мочи. Концентрация альбумина определялась методом иммуноферментного анализа ("Micro-Albumin ELIZA", ORGENTEC Diagnostika), креатинина — кинетическим методом Яффе ("ARCHITECT", Abbott), активность ФВ — иммунотурбидиметрическим методом (Liatest vWF, Diagnostica Stago). Расчетная скорость клубочковой фильтрации (рСКФ) определялась по формуле Chronic Kidney Disease Epidemiology Collaboration.
Пациенты наблюдались не менее года. Первичной конечной точкой, характеризующей суммарную эффективность лечения, являлась совокупность основных ПОС, включая ССО и большие/клинически значимые кровотечения (типы 2-5 по классификации Bleeding Academic Research Consortium (BARC)). В качестве ССО регистрировались такие события, как инфаркт миокарда (ИМ), инсульт, транзиторная ишемическая атака, госпитализация в связи с нестабильной стенокардией, критическая ишемия или ампутация нижней конечности, острая ишемия почек или внутренних органов, ранее не планируемая реваскуляризация в любом сосудистом бассейне. Вторичными конечными точками являлись 1) ССО; 2) кровотечения BARC 2-5.
Статистическая обработка проведена с помощью пакета программ MedCalc 19.6.4. Значения непрерывных величин представлены в виде медианы и интерквартильного размаха, категориальные величины представлены в виде частоты встречаемости.
Поиск отрезных точек осуществлялся с помощью ROC-анализа; за отрезную точку принималось значение с максимальным значением индекса Юдена. Визуализация частоты ССО и кровотечений в зависимости от изучаемых параметров проводилась путем построения кривых Каплана-Мейера. Сравнение кривых проведено с использованием логарифмического рангового критерия.
Оценка прогностической роли альбуминурии, повышения активности ФВ и их сочетания проводилась методом логистической регрессии, а также многофакторный анализ методом пропорциональной регрессии Кокса. Соответствующие категориальные величины формировались на основе выявленной отрезной точки. В многофакторный анализ включались основные факторы риска ГО и ССО, в отношении которых по результатам однофакторного анализа получены значимые (p<0,05) или близкие к значимым (p<0,1) различия между группами.
Значимость различий для проверяемых гипотез устанавливалась на уровне p<0,05.
Результаты
В исследование было включено 148 пациентов, характеристика которых представлена в таблице 1. В соответствии с критериями включения пациенты характеризовались высоким риском ишемических осложнений: помимо ИБС и периферического атеросклероза, каждый третий страдал СД, каждый четвертый — сердечной недостаточностью (СН), более половины пациентов перенесли ИМ. Все пациенты переносили в прошлом коронарную реваскуляризацию.
Таблица 1
Исходная клинико-демографическая характеристика пациентов
|
Признак |
Значение |
|
Мужской пол, % |
79,1 |
|
Возраст, медиана [ИР], годы |
66 [ 65; 67] |
|
Факторы риска повышенной альбуминурии, % — артериальная гипертония — сахарный диабет — ожирение — хроническая сердечная недостаточность |
87,2 32,4 40,5 23,7 |
|
Курение, % |
41,9 |
|
ЧКВ в анамнезе, % |
71,0 |
|
Коронарное шунтирование в анамнезе, % |
35,1 |
|
Инфаркт миокарда в анамнезе, % |
55,4 |
|
Инсульт/ТИА в анамнезе, % |
8,1 |
|
Клинически значимый атеросклероз, % — в 2 сосудистых бассейнах — в 3 сосудистых бассейнах — в 4-5 бассейнах |
52,0 39,9 8,1 |
|
рСКФ <60 мл/мин/1,73 м², % |
16,9 |
|
Онкологическое заболевание в анамнезе, % |
7,4 |
|
Эрозивно-язвенное поражение верхних отделов ЖКТ в анамнезе, % |
35,1 |
|
АСК+клопидогрел/АСК+ривароксабан 2,5 мг 2 раза/сут., % |
50/50 |
Сокращения: АСК — ацетилсалициловая кислота, ИР — интерквартильный размах, ЖКТ — желудочно-кишечный тракт, рСКФ — расчетная скорость клубочковой фильтрации, ТИА — транзиторная ишемическая атака, ЧКВ — чрескожное коронарное вмешательство.
Было показано, что более чем у 2/3 пациентов отмечается как минимум легкое повышение уровня альбумина в моче (>10 мг/г) (рис. 1).
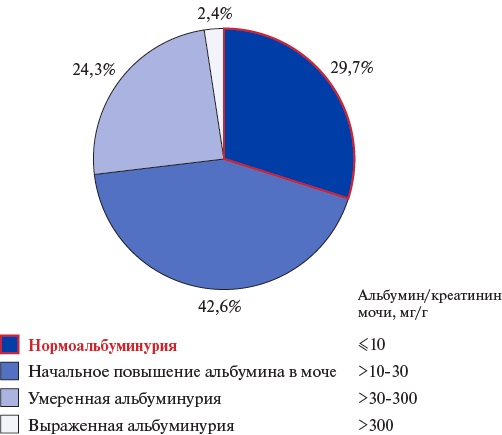
Рис. 1. Частота выявления альбуминурии различной степени выраженности.
Частота выявления вероятной ХБП в соответствии с номенклатурой Kidney Disease: Improving Global Outcomes (KDIGO) [1], которая включает в себя как снижение рСКФ <60 мл/мин/1,73 м², так и присутствие маркеров почечного повреждения, в т.ч. умеренной/тяжелой альбуминурии (>30 мг/г), составила 37,2%. Оценка уровня альбуминурии более чем вдвое увеличила число пациентов с заподозренной ХБП, требующей верификации через 3 мес. (чтобы исключить транзиторную почечную дисфункцию) [1].
Значимость альбуминурии в отношении предсказания ПОС (ССО и ГО)
Медиана длительности наблюдения составила 17 [ 15; 20] мес. За этот период зарегистрировано 25 (17%) ПОС: 7 ССО и 18 кровотечений BARC 2-3 (кровотечений BARC 4-5 не зарегистрировано).
ROC-анализ показал, что отрезной точкой для значений альбуминурии, ассоциирующихся с увеличением частоты ПОС, является уровень 10,6 мг/г. ПОС были зарегистрированы у 2 (4,5%) пациентов с уровнем альбуминурии <10,6 мг/г и у 23 (21,9%) пациентов с более высокими значениями, plog-rank=0,007 (рис. 2 А). Следует отметить, что снижение рСКФ <60 мл/мин/1,73 м² не ассоциировалось с достоверным увеличением частоты ПОС (рис. 2 Б).
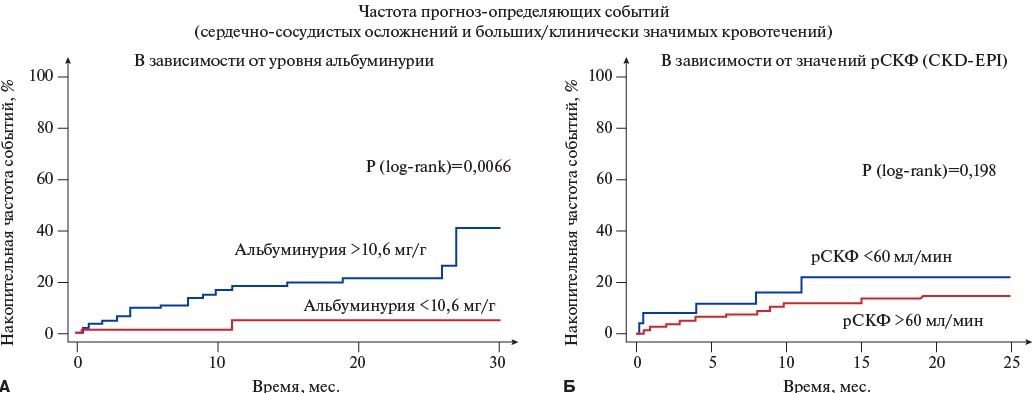
Рис. 2. Частота всех ПОС в зависимости от уровня альбуминурии и рСКФ.
Сокращение: рСКФ — расчетная скорость клубочковой фильтрации.
Для оценки роли альбуминурии >10,6 мг/г как независимого предиктора ПОС выполнен многофакторный анализ. Финальная модель представлена в таблице 2 (хи-квадрат модели 23,7, р=0,005). Помимо альбуминурии >10,6 мг/г, значимым предиктором ПОС оказался анамнез онкологического заболевания. Модель включала, помимо прочего, снижение рСКФ <60 мл/мин/1,73 м² и состояния, которые являются общепризнанными факторами риска альбуминурии (артериальная гипертония, СД, хроническая СН, ожирение), а также тип антитромботической терапии. Для пациентов с альбуминурией >10,6 мг/г отношение шансов (ОШ) развития ПОС составило 5,5 (95% доверительный интервал (ДИ): 1,23-24,72), р=0,026.
Таблица 2
Предикторы ПОС (многофакторный анализ)
|
Признак |
Отношение шансов (95% ДИ) |
Уровень Р |
|
Альбуминурия >10,6 мг/г |
5,50 (1,23-24,72) |
0,026 |
|
Онкологическое заболевание в анамнезе |
3,64 (1,05-12,63) |
0,042 |
|
Инфаркт миокарда в анамнезе |
2,59 (0,97-6,91) |
0,058 |
|
Курение |
2,43 (0,89-6,64) |
0,083 |
Сокращение: ДИ — доверительный интервал.
Выявленное нами отрезное значение для альбуминурии оказалось очень близким к формальной границе легкого повышения альбуминурии — 10 мг/г. С практической точки зрения удобнее использовать именно это значение. При выборе этой отрезной точки значимость альбуминурии как предиктора ПОС снизилась несущественно: в той же многофакторной модели ОШ для альбуминурии >10 мг/г составило 5,17 (95% ДИ: 1,13-23,55), р=0,03; общая значимость модели снизилась незначительно (хи-квадрат 23, р=0,006).
Проводилась раздельная оценка влияния уровня альбуминурии на частоту ССО и ГО (вторичные конечные точки). Все зафиксированные в данном наблюдении ССО произошли у пациентов с уровнем альбуминурии >10,6 мг/г, что осложняет возможности статистической обработки. По данным логистического регрессионного анализа рассчитать относительный риск не представляется возможным, однако связь альбуминурии >10,6 мг/г с частотой ССО оценивается как значимая (р=0,018). По тем же самым причинам оценить значимость альбуминурии >10,6 мг/г в отношении ССО в рамках регрессии Кокса также не представляется возможным. Что касается ГО, выявлена тенденция к большей частоте кровотечений BARC 2-3 у пациентов с альбуминурией >10,6 мг/г: plog-rank=0,05, ОШ по данным однофакторного логистического регрессионного анализа 4,2 (95% ДИ: 0,93-19,2), р=0,06. Недостаточное количество конечных точек не позволило выявить ни одного значимого предиктора кровотечений BARC 2-3 по данным многофакторного анализа; для альбуминурии >10,6 мг/г ОШ составило 3,68 (95% ДИ: 0,81-16,73), р=0,092 c поправкой на пол, возраст, рСКФ, анамнез эрозивно-язвенного поражения желудка, анамнез онкозаболеваний, курение, ИМ, инсульт/транзиторная ишемическая атака, хроническая СН, тип антитромботической терапии. Для ривароксабана 2,5 мг в составе комбинированной антитромботической терапии (в сравнении с клопидогрелом) ОШ составило 2,54 (95% ДИ: 0,96-8,57), р=0,067.
Значимость ФВ в отношении предсказания ПОС
По данным ROC-анализа отрезной уровень для активности ФВ, ассоциирующийся с увеличением риска ПОС, составил 157% (что совпадает с верхней границей нормы). Частота ПОС составила 10,8% у пациентов с уровнем ФВ <157% и 23,0% у пациентов с уровнем ФВ, превышающим это значения, plog-rank=0,048. При включении параметра ФВ >157% вместо альбуминурии в представленную в таблице 2 модель Кокса он не продемонстрировал достоверной ассоциации с ПОС (ОШ 2,18; 95% ДИ: 0,84-5,65; р=0,11). При одновременном включении в модель альбуминурии >10,6 мг/г и ФВ >157% значимость обоих факторов оказалась сопоставимой, повысившись для ФВ (р=0,049) и снизившись для альбуминурии (р=0,048), что говорит, вероятно, о наличии взаимодействия между этими параметрами, в т.ч. с точки зрения влияния на прогноз. Суммарная значимость модели (хи-квадрат 21,3, р=0,013) была ниже, чем в случае изолированного учета альбуминурии.
Прогностическая значимость сочетания повышенных альбуминурии и ФВ
Доля пациентов с одновременным повышением уровня альбуминурии >10,6 мг/г и ФВ >157% составила 31,2%. ПОС перенес каждый третий пациент из этой подгруппы, в подгруппе пациентов с отсутствием повышения обоих маркеров не произошло ни одного события (рис. 3). Многофакторный анализ показал, что сочетание двух маркеров является независимым предиктором ПОС: ОШ составило 3,53 (95% ДИ: 1,31-9,49), р=0,012. Данная модель характеризовалась наибольшей суммарной значимостью (хи-квадрат 27,4, р=0,0012).
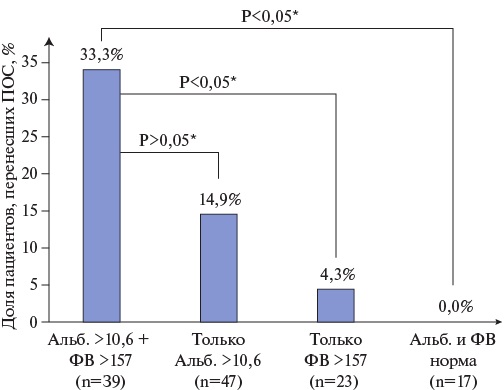
Рис. 3. Частота ПОС в зависимости от уровня альбуминурии и активности ФВ.
Примечание: * — тест Фишера.
Сокращения: Альб. — альбуминурия, ПОС — прогноз-определяющие события, ФВ — фактор Виллебранда.
При раздельной оценке влияния сочетанного повышения альбуминурии и ФВ на ССО и ГО было показано, что наличие комбинированного маркера ассоциируется со статистически достоверным повышением риска обоих типов осложнений (рис. 4).
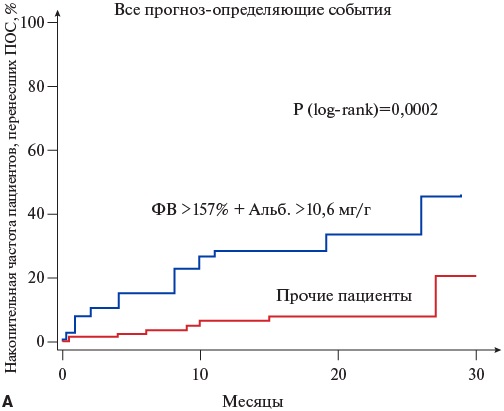
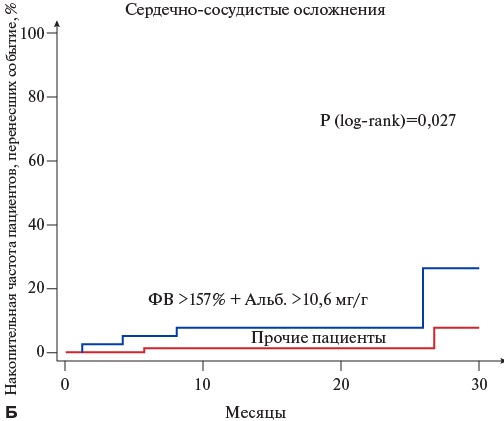
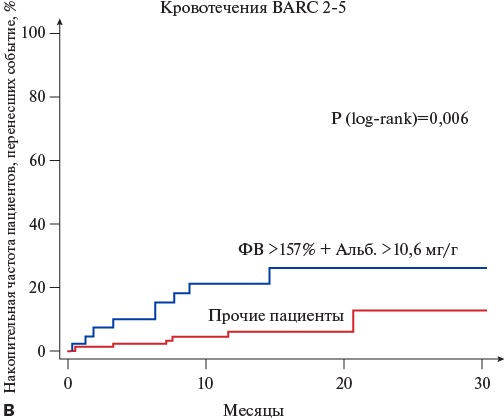
Рис. 4. Накопительная частота неблагоприятных событий в зависимости от наличия или отсутствия сочетанного повышения альбуминурии и ФВ.
Сокращения: Альб. — альбуминурия, ПОС — прогноз-определяющие события, ФВ — фактор Виллебранда.
Обсуждение
Наше исследование показало, что пациенты с МФА характеризуются высокой частотой легкой и умеренной альбуминурии; оценка альбуминурии позволяет более чем в 2 раза увеличить группу пациентов с подозрением на такую важную сопутствующую патологию, как ХБП.
Даже однократная оценка альбуминурии может вносить существенный вклад в стратификацию риска ССО и кровотечений BARC 2-5 у пациентов с ИБС и сопутствующим периферическим атеросклерозом, получающих комбинированную антитромботическую терапию. Альбуминурия >10,6 мг/г является независимым (в т.ч. от рСКФ) предиктором ПОС, объединяющих ССО и ГО. В реальной клинической практике можно использовать формальное пограничное значение этого маркера >10 мг/г. Тип антитромботической терапии (комбинация ацетилсалициловой кислоты с клопидогрелом или ривароксабаном) не влиял на основные результаты.
Недостаточная мощность исследования не позволила достоверно продемонстрировать связь альбуминурии отдельно с ССО и ГО, однако соответствующие тенденции были выявлены. Одновременное повышение альбуминурии >10,6 мг/г и ФВ >157% является независимым предиктором ССО и кровотечений у пациентов с МФА с наибольшей статистической значимостью, причем для этого комбинированного маркера продемонстрирована связь отдельно как с ССО, так и с ГО.
Принципиально новой задачей в данном исследовании стала оценка связи альбуминурии с кровотечениями. Учитывая небольшой объем исследования, кровотечения были включены в комбинированную конечную точку — ПОС, при этом они составляли большую часть зарегистрированных событий. Нами впервые было показано, что альбуминурия ассоциируется не только с риском ССО, но и всех ПОС. При раздельном анализе конечных точек была выявлена практически достигшая достоверности тенденция к увеличению риска кровотечений BARC 2-5 у пациентов с альбуминурией >10,6 мг/г. Ранее связь с кровотечениями была показана только в общей популяции для более высоких значений альбуминурии [8].
Полученные нами результаты свидетельствуют о целесообразности смещения отрезного значения для определения прогностически неблагоприятного "повышения" уровня альбуминурии с 30 до 10 мг/г. Аналогичные результаты недавно были получены в рамках крупного метаанализа, который показал, что риск сердечно-сосудистой смерти, ИМ, инсульта, периферического атеросклероза, фибрилляции предсердий и СН повышается при значениях альбумин-креатининового соотношения >10 мг/г независимо от рСКФ [9]. Такой подход нашел отражение в новых рекомендациях KDIGO по ХБП (2024г) [1], вышедших уже во время подготовки данной публикации.
В исследованной нами когорте рСКФ в отличие от альбуминурии не продемонстрировала связи с ПОС. Наши результаты позволяют сделать вывод, что у пациентов с МФА прогностически ценная информация может быть получена путем выявления ранней, потенциально обратимой стадии поражения почек, проявляющейся начальной альбуминурией, при еще сохранной экскреторной функции. Отсутствие связи уровня рСКФ с прогнозом в нашей когорте, вероятно, обусловлено небольшой представленностью пациентов с нарушенной экскреторной функцией почек — 16,9%. Оценить, насколько наша когорта репрезентативна для пациентов с МФА, оказалось затруднительно: статистика о распространенности ХБП у таких пациентов практически отсутствует. Для косвенного сравнения могут быть использованы данные у пациентов с МФА и СД. В этой когорте рСКФ <60 мл/мин выявлялась у 34,8% [10]. Для сравнения, в нашем исследовании СД диагностирован у каждого третьего пациента, что закономерно уменьшает частоту ХБП. Так или иначе, выявленные нами преимущества альбуминурии по отношению к рСКФ как прогностического маркера у пациентов с МФА требуют дополнительного изучения в масштабных исследованиях.
Неизученными остаются механизмы связи альбуминурии с CCО и кровотечениями. Мы показали, что альбуминурия является предиктором ПОС у пациентов с МФА независимо от сопутствующей патологии, которая традиционно рассматривается как причина альбуминурии. Таким образом, нет оснований считать, что альбуминурия просто является маркером коморбидности.
Существует мнение, что альбуминурия отражает не только локальное почечное повреждение, но и эндотелиальную дисфункцию [11], которая, в свою очередь, может быть причиной прогрессирования и обострения атеротромбоза, а также нарушения процессов гемостаза. Альбуминурия является следствием нарушения функционирования почечного фильтрационного барьера, состоящего из эндотелия, базальной мембраны и подоцитов. Регуляция функционирования барьера осуществляется путем взаимных паракринных влияний эндотелия и подоцитов с участием сосудистого эндотелиального фактора роста А, ангиопоэтинов, эндотелина-1, интерлейкина 6 и др. [12]. Таким образом, системная эндотелиальная дисфункция может проявляться повреждением фильтрационного барьера. С другой стороны, первичное повреждение почек по механизму нарушения паракринной регуляции, вероятно, может влиять на функцию эндотелия за их пределами.
Ранее нами было показано отсутствие корреляции между альбуминурией и "классическим" маркером эндотелиальной дисфункции ФВ у пациентов с МФА [6]. В данном исследовании альбуминурия и ФВ демонстрировали сложные взаимоотношения в рамках прогностических моделей, не заменяя друг друга как аналоги, а скорее проявляя синергию. Максимальную прогностическую значимость имел комбинированный маркер, объединяющий повышение альбуминурии и ФВ. На наш взгляд, отсутствие прямой корреляции между концентрациями и функциональными проявлениями этих маркеров отнюдь не исключают того, что альбуминурия является маркером эндотелиальной дисфункции. Более вероятно, что альбуминурия и изменения активности ФВ отражают нарушения разных функций эндотелия, а сочетанное повышение обоих маркеров характерно для наиболее тяжелого поражения эндотелия, которое реализуется в увеличение риска неблагоприятных событий.
Ограничения исследования. Исследование носит пилотный характер, относительно небольшой объем выборки не позволяет статистически подтвердить ряд выявленных тенденций. Указанные ограничения могут быть преодолены в ходе исследований на большей выборке.
Заключение
Альбуминурия >10 мг/г может быть использована как доступный в рутинной практике маркер повышенного резидуального риска ССО и кровотечений у пациентов с МФА, получающих комбинированную антитромботическую терапию, независимо от рСКФ. Альбуминурия является частично обратимым феноменом, поэтому потенциально может быть мишенью для воздействия, а в перспективе — маркером эффективности проводимого лечения у этой категории пациентов. Наиболее неблагоприятным прогнозом характеризуются пациенты при одновременном повышении двух маркеров эндотелиальной дисфункции — альбуминурии и активности ФВ. Требуется проведение дальнейших исследований, которые позволили бы найти пути снижения риска осложнений у этой категории пациентов.
Отношения и деятельность: все авторы заявляют об отсутствии потенциального конфликта интересов, требующего раскрытия в данной статье.
Список литературы
1. Kidney Disease: Improving Global Outcomes (KDIGO) CKD Work Group. KDIGO 2024 Clinical Practice Guideline for the Evaluation and Management of Chronic Kidney Disease. Kidney Int. 2024;105(4S): S117-S314. doi:10.1016/j.kint.2023.10.018.
2. Inoue K, Streja E, Tsujimoto T, et al. Urinary albumin-to-creatinine ratio within normal range and all-cause or cardiovascular mortality among U.S. adults enrolled in the NHANES during 1999-2015. Ann Epidemiol. 2021;55:15-23. doi:10.1016/j.annepidem.2020.12.004.
3. Mahemuti N, Zou J, Liu C, et al. Urinary Albumin-to-Creatinine Ratio in Normal Range, Cardiovascular Health, and All-Cause Mortality. JAMA Netw Open. 2023;6(12): e2348333. doi:10.1001/jamanetworkopen.2023.48333.
4. Agarwal R, Tu W, Farjat AE, et al. Impact of Finerenone-Induced Albuminuria Reduction on Chronic Kidney Disease Outcomes in Type 2 Diabetes: A Mediation Analysis. Ann Intern Med. 2023;176(12):1606-16. doi:10.7326/M23-1023.
5. Kario K, Matsuo T, Kobayashi H, et al. Activation of tissue factor-induced coagulation and endothelial cell dysfunction in non-insulin-dependent diabetic patients with microalbuminuria. Arterioscler Thromb Vasc Biol. 1995;15(8):1114-20. doi:10.1161/01.atv.15.8.1114.
6. Шахматова О. О., Комаров А. Л., Кривошеева Е. Н. и др. Альбуминурия у пациентов с мультифокальным атеросклерозом как маркер распространенности поражения и возможный предиктор прогноз-определяющих событий. Терапевтический архив. 2023;95(9):763-8. doi:10.26442/00403660.2023.09.202434.
7. Миронова С. А., Юдина Ю. С., Ионов М. В. и др. Взаимосвязь новых маркеров поражения почек и состояния сосудов у больных артериальной гипертензией. Российский кардиологический журнал. 2019;(1):44-51. doi:10.15829/1560-4071-2019-1-44-51.
8. Molnar AO, Bota SE, Garg AX, et al. The Risk of Major Hemorrhage with CKD. J Am Soc Nephrol. 2016;27(9):2825-32. doi:10.1681/ASN.2015050535.
9. Writing Group for the CKD Prognosis Consortium. Estimated Glomerular Filtration Rate, Albuminuria, and Adverse Outcomes: An Individual-Participant Data Meta-Analysis. JAMA. 2023;330(13):1266-77. doi:10.1001/jama.2023.17002.
10. Verma S, Mazer CD, Inzucchi SE, et al. Impact of polyvascular disease with and without co-existent kidney dysfunction on cardiovascular outcomes in diabetes: A post hoc analysis of EMPA-REG OUTCOME. Diabetes Obes Metab. 2021;23(5):1173-81. doi:10.1111/dom.14326.
11. Kakutani Y, Morioka T, Mori K, et al. Albuminuria rather than glomerular filtration rate is associated with vascular endothelial function in patients with type 2 diabetes. J Diabetes Complications. 2020;34(12):107702. doi:10.1016/j.jdiacomp.2020.107702.
12. Li M, Armelloni S, Mattinzoli D, et al. Crosstalk mechanisms between glomerular endothelial cells and podocytes in renal diseases and kidney transplantation. Kidney Res Clin Pract. 2024;43(1):47-62. doi:10.23876/j.krcp.23.071.
Об авторах
О. О. ШахматоваРоссия
Шахматова Ольга Олеговна — к.м.н., н.с. отделения клинических проблем атеротромбоза.
Москва
Конфликт интересов:
Нет
А. Л. Комаров
Россия
Комаров Андрей Леонидович — д.м.н., в.н.с., отделения клинических проблем атеротромбоза.
Москва
Конфликт интересов:
Нет
М. Б. Хакимова
Россия
Хакимова Мария Борисовна — аспирант отделения клинических проблем атеротромбоза.
Москва
Конфликт интересов:
Нет
Е. Н. Кривошеева
Россия
Кривошеева Елена Николаевна — к.м.н., м.н.с. отделения клинических проблем атеротромбоза.
Москва
Конфликт интересов:
Нет
Е. В. Титаева
Россия
Титаева Елена Владимировна — к.б.н., с.н.с. отделения клинических проблем атеротромбоза.
Москва
Конфликт интересов:
Нет
А. Б. Добровольский
Россия
Добровольский Анатолий Борисович — д.б.н., г.н.с. отделения клинических проблем атеротромбоза.
Москва
Конфликт интересов:
Нет
В. А. Амелюшкина
Россия
Амелюшкина Вера Алексеевна — врач лабораторной диагностики.
Москва
Конфликт интересов:
Нет
Н. В. Гомыранова
Россия
Гомыранова Наталья Вячеславовна — зав. клинико-диагностической лабораторией.
Москва
Конфликт интересов:
Нет
Е. П. Панченко
Россия
Панченко Елизавета Павловна — д.м.н., г.н.с. отделения клинических проблем атеротромбоза.
Москва
Конфликт интересов:
Нет
Дополнительные файлы
- У 3/4 пациентов с мультифокальным атеросклерозом выявляется повышение альбуминурии (чаще легкое или умеренное).
- Даже однократная оценка альбуминурии может вносить существенный вклад в стратификацию риска сердечно-сосудистых осложнений и кровотечений у пациентов с ишемической болезнью сердца и периферическим атеросклерозом.
- Предиктором перечисленных осложнений является альбуминурия >10,6 мг/г (независимо от скорости клубочковой фильтрации); в реальной клинической практике можно использовать формальное пограничное значение >10 мг/г.
- Наиболее неблагоприятным прогнозом характеризуются пациенты при одновременном повышении альбуминурии и активности фактора Виллебранда (что, вероятно, отражает выраженную эндотелиальную дисфункцию).
Рецензия
Для цитирования:
Шахматова О.О., Комаров А.Л., Хакимова М.Б., Кривошеева Е.Н., Титаева Е.В., Добровольский А.Б., Амелюшкина В.А., Гомыранова Н.В., Панченко Е.П. Альбуминурия в оценке риска сердечно-сосудистых осложнений и кровотечений у пациентов с ишемической болезнью сердца и периферическим атеросклерозом. Российский кардиологический журнал. 2025;30(6):6141. https://doi.org/10.15829/1560-4071-2025-6141. EDN: WFLDIS
For citation:
Shakhmatova O.O., Komarov A.L., Khakimova M.B., Krivosheeva E.N., Titaeva E.V., Dobrovolsky A.B., Ameljushkina V.A., Gomyranova N.V., Panchenko E.P. Albuminuria in assessing the risk of cardiovascular events and bleeding in patients with coronary and peripheral artery disease. Russian Journal of Cardiology. 2025;30(6):6141. (In Russ.) https://doi.org/10.15829/1560-4071-2025-6141. EDN: WFLDIS
JATS XML

















































