Перейти к:
Случай первичной диагностики дилатационой кардиомиопатии в сочетании с некомпактным миокардом у больной пожилого возраста
https://doi.org/10.15829/1560-4071-2023-5344
Аннотация
Классификации Всемирной организации здравоохранения, Европейского общества кардиологов и Американской ассоциации сердца указывают на существование нескольких фенотипов некомпактного миокарда (НКМ) со специфическими структурно-функциональными изменениями. Фенотип "НКМ+дилатационная кардиомиопатия (ДКМП)" считается одним из самых тяжелых вариантов заболевания. Продолжаются споры о том, расценивать НКМ как самостоятельную нозологическую форму или как следствие ДКМП и сердечной недостаточности, приводятся аргументы в пользу каждого из этих положений. Другими словами, НКМ остается одним из самых загадочных заболеваний сердца. В качестве иллюстрации фенотипа НКМ+ДКМП авторы предлагают историю болезни пациентки, которая с юности имела кардиологический анамнез, но сохранила удовлетворительное самочувствие и работоспособность до преклонного возраста. Симптомы аритмии и сердечной недостаточности с массивным гидроперикардом впервые описаны у нее в 66 лет, что нехарактерно для данного фенотипа НКМ и является особенностью клинического случая. Обращается внимание на трудности дифференциальной диагностики НКМ в связи с неспецифичностью его клинической картины, на роль эхокардиографии в распознавании заболевания и предикторы его неблагоприятного исхода. То обстоятельство, что у пациентки даже при выявлении типичных признаков НКМ при эхокардиографии первоначально в качестве основного диагноза указывалась ишемическая болезнь сердца, свидетельствует об актуальности публикации еще одного клинического случая, посвященного этой достаточно редкой патологии, для улучшения информированности о ней кардиологов и специалистов общей врачебной практики.
Ключевые слова
Для цитирования:
Вахненко Ю.В., Багдасарян Е.А., Савченко Д.А. Случай первичной диагностики дилатационой кардиомиопатии в сочетании с некомпактным миокардом у больной пожилого возраста. Российский кардиологический журнал. 2023;28(5):5344. https://doi.org/10.15829/1560-4071-2023-5344
For citation:
Vakhnenko Yu.V., Bagdasaryan E.A., Savchenko D.A. Primary diagnosis of dilated cardiomyopathy in combination with myocardial non-compaction in an elderly patient: a case report. Russian Journal of Cardiology. 2023;28(5):5344. (In Russ.) https://doi.org/10.15829/1560-4071-2023-5344
Наряду с изолированной формой некомпактного миокарда (НКМ) выделяют его сочетания с другими заболеваниями сердца. Так, классификация MOGE(S) рассматривает и существование НКМ как самостоятельной патологии, и его сочетание с дилатационной кардиомиопатией (ДКМП) [1]. Brescia ST, et al. считают дилатационную форму НКМ и его смешанную форму (НКМ+ДКМП+гипертрофическая кардиомиопатия) наиболее тяжелыми в клиническом и прогностическом плане [2]. К ним присоединяются и другие исследователи, описывающие сочетание НКМ с дилатацией левого желудочка (ЛЖ) при увеличении его конечно-диастолического размера (КДР) >5,6 см и снижением фракции выброса (ФВ) до 42,2% как наиболее неблагоприятный клинический вариант, связанный с максимумом тромбоэмболических событий, случаев сердечной недостаточности, внезапной сердечной смерти и трансплантаций сердца [3]. В детской когорте пятилетние показатели комбинированной конечной точки — смерть/трансплантация (смерть/включение в список на трансплантацию) — составляют 6% (6%) для изолированного НКМ ЛЖ, 43% (45%) для НКМ+ДКМ и 33% (42%) для групп с неопределенным фенотипом НКМ ЛЖ [4]. Смертность не коррелирует с коэффициентом NC/C и количеством некомпактных сегментов. Ее предикторами являются парные/политопные желудочковые экстрасистолы, пароксизмы желудочковой тахикардии, тромботические события, "оправданные срабатывания дефибрилляторов" [5][6]. Сочетание НКМ с другими кардиомиопатиями (КМП) составляет 33% всех случаев НКМ [7].
При НКМ описаны мутации почти 60 генов. Преимущественно это гены саркомерных белков миокарда. Наличие у одного больного разных мутаций характерно для тяжелого течения смешанных вариантов НКМ с резистентностью к терапии, гемодинамически значимыми аритмиями, высоким риском внезапной сердечной смерти [8][9]. Генетические "пересечения" НКМ с вышеуказанными КМП описаны многими авторами [10]. При этом результирующий фенотип, вероятно, определяется не столько определенной мутацией, сколько генами-модификаторами, эпигеномными факторами и влиянием среды обитания [11].
Мнения о "нозологической самостоятельности" НКМ неоднозначны. Одни считают, что НКМ у больных с ДКМП является самостоятельным нозологическим вариантом, а не результатом выраженной декомпенсации, аргументируя это распространенностью НКМ у некоторых категорий здоровых лиц, отсутствием признаков НКМ у большинства больных с тяжелой хронической сердечной недостаточностью (ХСН) [12]. Другие утверждают, что НКМ часто сочетается с другими КМП, врожденными пороками сердца, аортопатиями, а его клиника неспецифична, что ставит под сомнение предыдущее положение [13][14].
Действительно, сложно дифференцировать самостоятельный НКМ и выраженную трабекулярность ЛЖ вследствие ДКМП, которые не имеют ни достоверных клинических различий, ни патогномоничных параметров эхокардиографии (ЭхоКГ). Это нацеливает на продолжение поиска критериев дифференциальной диагностики НКМ и ДКМП с признаками некомпактности. Одним из них может быть изменение пиковой продольной деформации миокарда, рассчитанной при помощи ЭхоКГ и спекл-томографии, т.к. при НКМ более существенна деформация апикальных сегментов ЛЖ и величина апикально-базального отношения. При ДКМП апикально-базальный градиент не выражен [15].
Описание случая
Предлагаем читателям случай первичной диагностики ДКМП в сочетании с НКМ ЛЖ у пациентки 66 лет, предъявляющей жалобы на одышку при малейшей физической нагрузке, давящие боли в области сердца разной продолжительности, не иррадиирущие, не имеющие четкой связи с физическим напряжением, на перебои в работе сердца, головокружение и быструю утомляемость при тенденции к артериальной гипотонии.
Эпизодические боли в области сердца и перебои в его работе впервые появились в 16 лет после тяжелой ангины. Тонзилэктомия была отложена из-за наступившей беременности, протекавшей нормально. Вторая беременность и роды тоже прошли без осложнений, однако впоследствии сохранялись редкие кардиалгии и экстрасистолы. Диагноз, установленный по месту жительства, больная назвать затрудняется. Общее самочувствие оставалось удовлетворительным, работоспособность не страдала.
Ухудшение с 66 лет, когда постепенно участились экстрасистолы, снизилась переносимость нагрузок — появились одышка и отеки на голенях. Госпитали- зирована в Клинику кардиохирургии Амурской государственной медицинской академии. При ЭхоКГ выявлена митральная регургитация 1 степени, трикус- пидальная регургитация 2-3 степени (площадь 6,5 см2 — 27% правого предсердия). Конечно-диастолический объем (КДО) 183 мл, конечно-систолический объем 110 мл, КДР 61 мм, конечно-систолический размер 51 мм, ФВ 35%. Расчетное давление в правом желудочке 35 мм рт.ст. Левое предсердие 39×58 мм. Правое предсердие 44×52 мм. Характер движения межжелудочковой перегородки неопределенный. Снижена экскурсия задней стенки ЛЖ. Жидкость в полости перикарда по правому предсердию 3 см, по свободной стенке правого желудочка 1 см (ориентировочно 300 мл). Не исключен НКМ ЛЖ. Сократительная способность ЛЖ снижена в продольном и поперечном направлении. Диастолическая функция ЛЖ нарушена.
При компьютерной томографии (КТ) выявлены кардиомегалия, гидроторакс справа до 2 см, гидроперикард до 30-50 мм по передней, боковым и нижней поверхностям и 15 мм по задней поверхности сердца (рис. 1 А, Б). Поэтапно удалено 700, 300 и 170 мл светло-желтой прозрачной жидкости, которая содержала 20 г/л белка и единичные клеточные элементы. Проба Ривальта была отрицательной. Таким образом, жидкость представляла собой транссудат.
В клиническом и биохимическом анализе крови отклонений показателей от нормальных величин не обнаружено. Это относится к числу лейкоцитов (6,75-5,52×109/л), удельному весу нейтрофилов (54,7-58,5%) и лимфоцитов (35,8-39,2%), скорости оседания эритроцитов (2-5 мм/ч), значениям аспартаминотрансферазы (23,6 ЕД/л), аланинаминотрансферазы (13,5 ЕД/л), МВ-фракции креатинфосфокиназы (88,3 ЕД/л), фибриногена (1,6-1,9 г/л). При неоднократной 3-часовой термометрии температура тела не превышала норму. В анамнезе отсутствовали указания на связь ухудшения самочувствия с каким-либо инфекционным или воспалительным процессом, не выявлен интоксикационный синдром, перикардиальная жидкость имела "невоспалительный характер". Таким образом, данные за миокардит отсутствовали. Уровни тиреотропного гормона и тироксина соответствовали норме (13,2 пмоль/л и 2,4 мЕД/мл, соответственно). В процессе ультразвукового исследования щитовидной железы ее структурных изменений не выявлено. Это позволило исключить тиреотоксическую миокардиодистрофию. У пациентки не было анамнеза и клинических синдромов хронической болезни почек. Уровень креатинина, определенный неоднократно, соответствовал норме (62-88,4 мкмоль/л), скорость клубочковой фильтрации составила CKD-EPI: 84 мл/мин/1,73 м2, MDRD: >60 мл/мин/1,73 м2, Кокрофт-Голт: 49 мл/мин (60 мл/мин/1,73 м2), что свидетельствовало о ее начальном снижении. При таких значениях объемный выпот в перикарде не мог рассматриваться как следствие почечной недостаточности. У больной не выявлены клинические признаки аутоиммунных заболеваний ни в анамнезе, ни при опросе и осмотре. Кроме того, как правило, перикардит сопровождает активную фазу коллагенозов, а данные за острый воспалительный процесс, как указано выше, отсутствовали. В качестве возможных причин появления жидкости в перикарде рассматривались его злокачественные поражения (в частности, мезотелиома) или метастазирование в перикард первичных опухолей, а также синдром Мейгса. Жалоб со стороны органов и систем, за исключением сердечно-сосудистой, у больной не было. Она осмотрена гинекологом, прошла рентгенологическое и ультразвуковое обследование, фиброэзофагогастродуоденоскопию — патологии не выявлено. При КТ структурных изменений перикарда и плевры также не обнаружено, что позволило усомниться в наличии опухолевого процесса. Отоларинголог признаков острого и хронического воспалительного процесса ЛОР-органов не обнаружил.
Вышеперечисленное позволило сделать вывод о том, что транссудат в перикардиальной полости явился следствием ХСН, тем более, что у пациентки имели место и другие ее проявления — одышка, периферические отеки, гидроторакс, а также кардиалгия, нарушения ритма и проводимости. Кроме того, имели место серьезные структурные изменения сердца, подтвержденные лучевыми методами диагностики.
Проводилась адекватная терапия ХСН с положительным эффектом — позитивными изменениями объективного статуса, показателей контрольной ЭхоКГ (увеличение ФВ ЛЖ до 44%, уменьшение полостей сердца, отсутствие жидкости в полости перикарда). В качестве основного диагноза указана ишемическая болезнь сердца (ИБС), стабильная стенокардия напряжения. НКМ в выписке не фигурирует.
Пациентка утверждает, что впоследствии наблюдалась у кардиолога. Жидкость в полости перикарда не накапливалась, однако документальных подтверждений этому не предоставлено.
Следующая госпитализация в Клинику в возрасте 71 года. Сложилось впечатление об отсутствии приверженности больной рекомендованной терапии. Толерантность к нагрузкам в указанный период продолжала снижаться. В настоящее время пациентка избегает даже незначительного напряжения из-за выраженной одышки, сердцебиения, аритмии и быст- рой утомляемости.
Особенности анамнеза жизни. В юношеском возрасте — экссудативный плеврит туберкулезной этиологии. После специфического лечения жидкость не накапливалась. Пациентка снята с учета в противотуберкулезном диспансере, однако регулярно проходила флюорографию. Патологических изменений не находили. В возрасте 45 лет ей выполнена гистерэктомия по поводу фибромиомы матки. Со слов больной, химио- и лучевую терапию она не получала, что позволяет думать о доброкачественном генезе новообразования. В 70 лет она перенесла острое ишемическое нарушение мозгового кровообращения.
Наследственный анамнез по заболеваниям сердца и сосудов не отягощен.
Общее состояние тяжелое, акроцианоз. Астеническое телосложение. Частота дыхания при незначительной нагрузке 18 в мин. Левая граница сердца расположена на 1,5 сантиметра кнаружи от левой среднеключичной линии. Тоны приглушены, аритмичны. Систолический шум над верхушкой и мечевидным отростком грудины. Частота сердечных сокращений 68 уд./мин. Артериальное давление на обеих руках 120/80 мм рт.ст. Отеки на голенях и стопах.
При чреспищеводной ЭхоКГ обнаружены митральная регургитация 2 степени с площадью 5,67 см2, трикуспидальная регургитация 2-3 степени с площадью 8,8 см2. Параметры ЛЖ: КДО 206 мл, конечно-систолический объем 147 мл, КДР 64 мм, конечно-систолический размер 55 мм, ФВ ЛЖ 28%. Атриомегалия. Межжелудочковая перегородка: толщина в диастолу в базальном сегменте 11,0 мм, гипокинез. Нижняя стенка ЛЖ: толщина в диастолу компактного слоя в базальном сегменте 8,0 мм, некомпактного слоя 16,3 мм, гипокинез (рис. 2 А, Б). Заключение: ДКМП. По нижней и нижнебоковой стенкам ЛЖ — выраженный трабекулярный слой (N/C 2,03). Митральная регургитация 2 степени. Трикуспидальная регургитация 3 степени. Сократимость продольных и циркулярных волокон миокарда ЛЖ снижена. Диастолическая функция ЛЖ нарушена.
На электрокардиограмме — полная блокада левой ножки пучка Гиса, атриовентрикулярная блокада I степени, частая желудочковая экстрасистолия (рис. 3).
При КТ в S5 обоих легких — участки линейного локального пневмоплеврофиброза. Кардиомегалия. В верхнем и заднем отделах полости перикарда — выпот толщиной 10-12 мм и плотностью 0-10 ед. Х.
При селективной коронароангиографии стенозирующих изменений не выявлено. Имеется неровность контуров правой коронарной артерии.
При ультразвуковом исследовании брахиоцефальных артерий — атеросклеротический стеноз сонных артерий до 35-40% с обеих сторон.
Дислипидемии не выявлено.
Выставлен диагноз: ДКМП в сочетании с НКМ ЛЖ. Относительная митральная недостаточность II степени. Относительная трикуспидальная недостаточность III степени. Желудочковая экстрасистолия IV градации по Lown, периодическая квадригеминия. Транзиторная атриовентрикулярная блокада I степени. Полная блокада левой ножки пучка Гиса. ХСН IIБ со сниженной ФВ ЛЖ, функциональный клаcс III по NYHA. Стенозирующий атеросклероз церебральных артерий. Дисциркуляторная энцефалопатия II степени.
Больная получала амиодарон, периндоприл, верошпирон, диувер, кардиомагнил, препараты калия и антигипоксанты с незначительным эффектом в отношении симптомов сердечной недостаточности. Учитывая наличие ХСН с низкой ФВ ЛЖ (28%), полной блокады левой ножки пучка Гиса и характер основного заболевания, запланирована имплантация ресинхронизирующего устройства.

Рис. 1А. Компьютерная томограмма органов грудной клетки до перикардиальной пункции. Кардиомегалия. Большое количество жидкости в полости перикарда (стрелки).
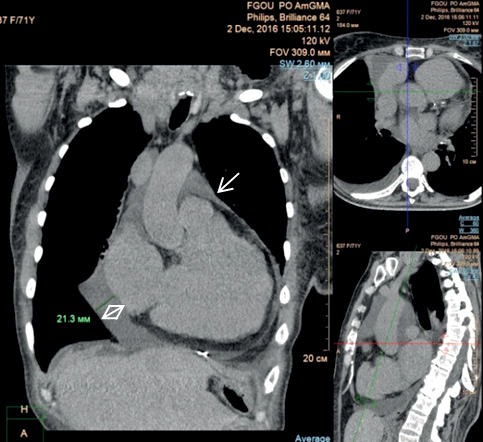
Рис. 1Б. Компьютерная томограмма органов грудной клетки после перикардиальных пункций. Количество жидкости в полости перикарда значительно уменьшилось (стрелки).
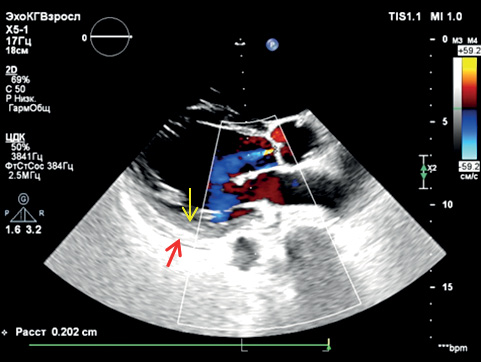
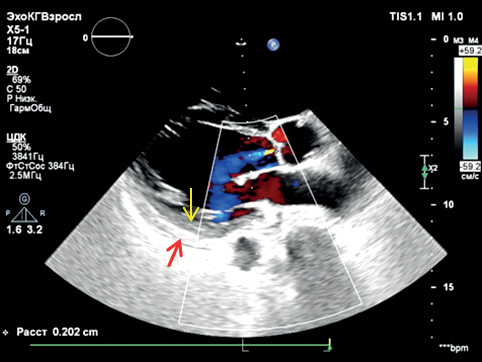
Рис. 2А. ЭхоКГ. Выраженная митральная регургитация и двуслойность миокарда ЛЖ: компактный (красная стрелка) и трабекулярный (желтая стрелка) слои.
Примечание: цветное изображение доступно в электронной версии журнала.
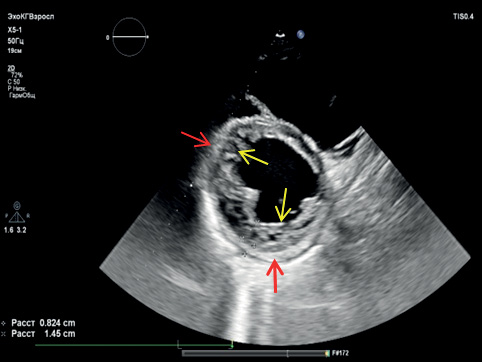
Рис. 2Б. ЭхоКГ. Двуслойность миокарда ЛЖ — более тонкий компактный (красные стрелки) и выраженный трабекулярный (желтые стрелки) слои.
Примечание: цветное изображение доступно в электронной версии журнала.
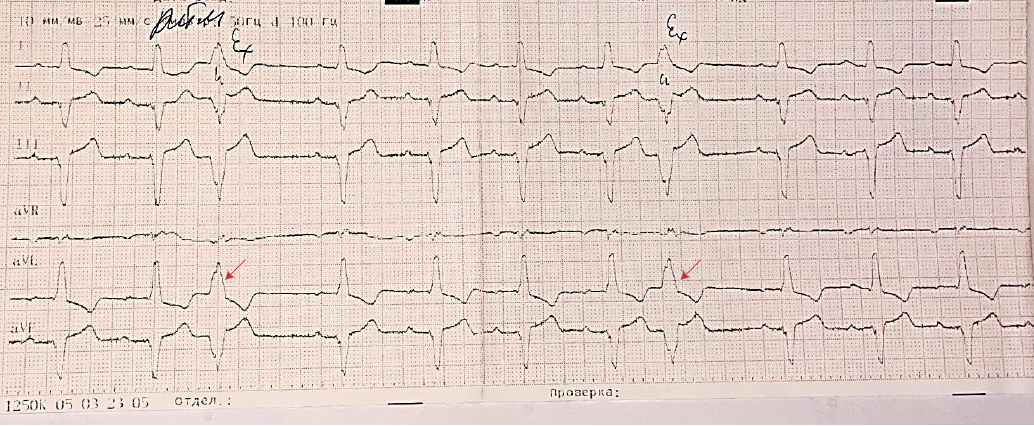
Рис. 3. Электрокардиограмма. Полная блокада левой ножки пучка Гиса. Частые желудочковые экстрасистолы.
Обсуждение
Одной из особенностей данного клинического случая является непрерывный продолжительный кардиальный анамнез (кардиалгии и нарушение ритма с 16 лет), который не сразу был учтен при обследовании в зрелом возрасте, и больной выставлен диагноз ИБС. Именно с ней изначально связывали тяжелую ХСН. В то же время характер болей в сердце не полностью соответствовал критериям стенокардии. В итоге на основании селективной коронароангиографии стенозирующие изменения сосудов исключены, и внимание специалистов привлекли выраженные структурные изменения сердца, описанные врачом ультразвуковой диагностики — повышенная трабекулярность ЛЖ и значительное увеличение камер, соответствующие критериям НКМ и ДКМП.
В данном случае у пациентки имелись ЭхоКГ-признаки ДКМП и выраженной некомпактности миокарда ЛЖ, что можно рассматривать как сочетанный фенотип НКМ — НКМ+ДКМП. Однако, не имея протоколов ЭхоКГ за более ранние периоды жизни больной, это нельзя утверждать определенно. Не исключено, что НКМ явился следствием тяжелой ХСН на фоне самостоятельной ДКМП, которая по каким-то причинам прогрессировала в зрелом возрасте. Кроме того, НКМ может быть одной из возрастных трансформаций сердечной мышцы, которые описаны в доступных литературных источниках. Тем более, теоретически фенотип НКМ+ДКМП должен протекать значительно тяжелее, а в данном случае качество жизни и общее состояние пациентки существенно ухудшились только с 65 лет, что является особенностью описанной истории болезни и подтверждает разнообразие вариантов клинического течения КМП.
НКМ до сих пор остается предметом оживленного обсуждения. Далеко не все исследователи признают его отдельным видом КМП, считая фенотипическим проявлением широкого спектра заболеваний сердечной мышцы. Однозначно лишь то, что врачи общей практики, а тем более кардиологи, должны быть осведомлены о существовании синдрома НКМ, понимать его суть, многообразие вариантов НКМ и возможности медицинской помощи этой категории больных.
Ограничения исследования. Диагноз НКМ был установлен на основании критериев Jenni R, Oechslin E, Schneider J, Jost CA, Kaufmann PA (2001) как наиболее полных по мнению большинства авторов в настоящее время. Существенную информацию о выраженности и распространенности НКМ, безусловно, могла предоставить магнитно-резонансная томография, проведению которой препятствовало диспноэ в горизонтальном положении больной, которая, к тому же, психологически не была готова к данной процедуре. Это явилось одним из ограничений данной работы.
К сожалению, нам не удалось обследовать родственников пациентки и провести генетические исследования, результаты которых были бы крайне интересны для ученых-кардиологов с учетом неординарности клинического случая. Возможно, именно особенности генома больной определяли специфику течения ее заболевания. Это явилось вторым ограничением проведенного исследования.
Временная шкала
|
Возрастные периоды |
Патологические изменения |
|
Возрастные периоды |
Патологические изменения |
|
16 лет |
Дебют заболевания в виде перебоев в работе сердца и болей в области сердца неопределенного характера и продолжительности, без иррадиации. Архивные документы отсутствуют. Точных сведений о диагнозе нет. |
|
18 лет, 22 года |
Беременности и самостоятельные роды, прошедшие без осложнений. Сохраняются эпизодические боли в области сердца и перебои в его работе, не имеющие четкой связи с физической нагрузкой или какими-либо определенными причинами. Информации о диагнозе нет. |
|
23 года — 64 года |
Самочувствие и состояние без отрицательной динамики. Признаков сердечной недостаточности, со слов больной, нет. |
|
65 лет |
Боли в области сердца и перебои в его работе существенно учащаются. Появляется одышка при обычной физической нагрузке и отеки на стопах. |
|
66 лет |
Без каких-либо провоцирующих факторов существенно снижается толерантность к физической нагрузке — прогрессирует одышка, отеки распространяются на голени и бедра. По данным ЭхоКГ — увеличение камер сердца, преимущественно ЛЖ (КДР 61 мм, КДО 183 мл) с нарушением его систолической (ФВ ЛЖ 35٪) и диастолической функций, незначительная митральная и выраженная трикуспидальная недостаточность, большое количество жидкости в полости перикарда, умеренное — в плевральной полости. Впервые не исключается НКМ. При пункциях удалено 1170 мл транссудата, назначена комплексная терапия ХСН с положительным эффектом. Проведена дифференциальная диагностика ИБС с миоперикардитом, тиреотоксической миокардиодистрофией, новообразованиями перикарда. Рабочий диагноз — ИБС. |
|
66 лет — 70 лет |
Самочувствие длительное время остается удовлетворительным, однако в отсутствии приверженности лечению толерантность к физической нагрузке постепенно снижается, нарастает одышка, наблюдается тенденция к артериальной гипотонии, снижается масса тела. В 70 лет больная переносит острое нарушение мозгового кровообращения ишемического характера. |
|
71 год |
Одышка при подъеме на один лестничный пролет. Отеки на нижних конечностях. Выраженная общая слабость. При чреспищеводной ЭхоКГ обнаружены митральная регургитация 2 степени, трикуспидальная регургитация 2-3 степени. КДО ЛЖ 206 мл, КДР ЛЖ 64 мм, ФВ ЛЖ 28٪, атриомегалия, гипокинез межжелудочковой перегородки и нижней стенки ЛЖ. Последняя в нижнем сегменте имеет компактный слой (8,0 мм) и некомпактный слой (16,3 мм). N/C 2,03. Умеренное количество жидкости в перикардиальной и плевральной полостях. При селективной коронароангиографии стенозирующие изменения не обнаружены. На ЭКГ — полная блокада левой ножки пучка Гиса, частые желудочковые экстрасистолы. Причиной тяжелой ХСН названо сочетание ДКМП и НКМ. Консервативное лечение ХСН способствовало уменьшению периферических и центральных отеков, но одышка сохраняется в прежнем объеме. Решено направить больную для имплантации ресинхронизирующего устройства. |
Сокращения: ДКМП — дилатационная кардиомиопатия, ИБС — ишемическая болезнь сердца, КДО — конечно-диастолический объем, КДР — конечно-диастолический размер, ЛЖ — левый желудочек, НКМ — некомпактный миокард, ФВ — фракция выброса, ХСН — хроническая сердечная недостаточность, ЭКГ — электрокардиография, ЭхоКГ — эхокардиография.
Отношения и деятельность: все авторы заявляют об отсутствии потенциального конфликта интересов, требующего раскрытия в данной статье.
Список литературы
1. Arbustini E, Narula N, Dec GW, et al. The MOGE(S) classification for a phenotype-genotype nomenclature of cardiomyopathy: Endorsed by the world heart federation. Journal of the American College of Cardiology. 2013;62(22):2046-72.
2. Brescia ST, Rossano JW, Pignatelli R, et al. Mortality and sudden death in pediatric left ventricular noncompaction in a tertiary referral center. Circulation. 2013;127(22):2202-8. doi:10.1161/CIRCULATIONAHA.113.002511.
3. Куликова О. В., Мясников Р. П., Мершина Е. А. и др. Семейная форма некомпактной кардиомиопатии: типы ремоделирования миокарда, варианты клинического течения. Результаты многоцентрового регист-ра. Терапевтический архив. 2021;93(4):381-8. doi:10.26442/00403660.2021.04.200677.
4. Jefferies JL, Wilkinson JD, Sleeper LA, et al. Pediatric Cardiomyopathy Registry Investi¬gators. Cardiomyopathy Phenotypes and Outcomes for Children With Left Ventricular Myocardial Noncompaction: Results From the Pediatric Cardiomyopathy Registry. J Card Fail. 2015;21(11):877-84. doi:10.1016/j.cardfail.2015.06.381.
5. Умарова М. К., Басаргина Е. Н., Сильнова И. В. Связь характеристик некомпактного слоя миокарда с риском наступления летального исхода и развития тромботических осложнений при дилатационном фенотипе некомпактного миокарда у детей: результаты когортного исследования. Вопросы современной педиатрии. 2016;15(2):161-7. doi:10.15690/vsp.v15i2.1534.
6. Aung N, Doimo S, Ricci F, et al. Prognostic Significance of Left Ventricular Noncompaction: Systematic Review and Meta-Analysis of Observational Studies. Circ Cardiovasc Imaging. 2020;13(1):e009712. doi:10.1161/CIRCIMAGING.119.009712.
7. Miller EM, Hinton RB, Czosek R, et al. Genetic Testing in Pediatric Left Ventricular Noncompaction. Circ Cardiovasc Genet. 2017;10(6):e001735. doi:10.1161/CIRCGENETICS.117.001735.
8. Поляк М. Е., Букаева А. А., Шестак А. Г. и др. Сочетание двух мутаций у больной с аритмической формой синдрома некомпактного миокарда левого желудочка. Российский кардиологический журнал. 2016;(10):98-104. doi:10.15829/1560-4071-2016-10-98-104.
9. Sedaghat-Hamedani F, Haas J, Zhu F, et al. Clinical genetics and outcome of left ventricular non-compaction cardiomyopathy. Eur Heart J. 2017;38(46):3449-60. doi:10.1093/eurheartj/ehx545.
10. Cuevas J, Fernández R, Persia-Paulino YR, et al. Noncompaction cardiomyopathy as a cause of ventricular tachycardia in a young adult. Arch Cardiol Mex. 2022;92(2):283-5. doi:10.24875/ACM.20000462.
11. Стрельцова А. А., Гудкова А. Я., Костарева А. А. Некомпактный миокард: современные представления о генетических основах, клинической картине, диагностике и лечении. Терапевтический архив. 2019;91(12):90-7. doi:10.26442/00403660.2019.12.000142.
12. Благова О. В., Павленко Е. В., Вариончик Н. В. и др. Некомпактный миокард с дилатационным фенотипом: проявления, лечение и исходы в сравнении другими формами синдрома дилатационной кардиомиопатии. Рациональная Фармакотерапия в Кардиологии. 2022;18(1):27-35. doi:10.20996/1819-6446-2022-02-01.
13. Митрофанова Л. Б., Моисеева О. М., Хащевская Д. А. и др. Некомпактный миокард левого желудочка. Клинико-морфологическое исследование. Архив патологии. 2016;78(2):29-35. doi:10.17116/patol201678229-35.
14. Доровских И. Е., Вахненко Ю. В., Шабанов В. В. и др. Случай диагностики и лечения кардиомиопатии "Некомпактный миокард" с применением имплантированного кардиовертера-дефибриллятора. Патология кровообращения и кардиохирургия. 2016;20(3):126-32. doi:10.21688/1681-3472-2016-2-126-132.
15. Huttin O, Venner C, Frikha Z, et al. Myocardial deformation pattern in left ventricular non-compaction: Comparison with dilated cardiomyopathy. Int J Cardiol Heart Vasc. 2014;5:9-14. doi:10.1016/j.ijcha.2014.11.001.
Об авторах
Ю. В. ВахненкоРоссия
Вахненко Юлия Викторовна — кандидат медицинских наук, ассистент кафедры госпитальной терапии с курсом фармакологии
Благовещенск
Е. А. Багдасарян
Россия
Багдасарян Екатерина Альбертовна — заместитель главного врача Клиники кардиохирургии
Благовещенск
Д. А. Савченко
Россия
Савченко Дмитрий Александрович — врач-кардиолог Клиники кардиохирургии
Благовещенск
Дополнительные файлы
Рецензия
Для цитирования:
Вахненко Ю.В., Багдасарян Е.А., Савченко Д.А. Случай первичной диагностики дилатационой кардиомиопатии в сочетании с некомпактным миокардом у больной пожилого возраста. Российский кардиологический журнал. 2023;28(5):5344. https://doi.org/10.15829/1560-4071-2023-5344
For citation:
Vakhnenko Yu.V., Bagdasaryan E.A., Savchenko D.A. Primary diagnosis of dilated cardiomyopathy in combination with myocardial non-compaction in an elderly patient: a case report. Russian Journal of Cardiology. 2023;28(5):5344. (In Russ.) https://doi.org/10.15829/1560-4071-2023-5344

















































